Авторы: A. Tulzer, W. Arzt, G. Tulzer
Цель
Критический стеноз аорты (КСА) с рестриктивной межпредсердной перегородкой может привести к застойной сердечной недостаточности и водянке плода, что обычно приводит к гибели плода, если его не лечить. Целью этого исследования было оценить влияние вальвулопластики аорты плода (ВПАП) на гемодинамику и исходы у этих пациентов.
Методы
Это был ретроспективный обзор плодов с КСА и признаками водянки, перенесших ВПАП в нашем центре в период с 2000 по 2020 годы. Эхокардиограммы и карты пациентов были проанализированы на предмет размеров желудочков и клапанов, а также на исход.
Полученные результаты
Водянка присутствовала во время вмешательства у 15 плодов с КСА, которые прошли ВПАП в нашем центре в течение периода исследования. Все пациенты, кроме одного, прошли по крайней мере одну технически успешную процедуру. Смертей, связанных с процедурой, не было, но произошло три внутриутробных смерти. Двенадцать субъектов были живорожденными, двое из которых умерли в течение 24 часов после рождения из-за стойкой водянки. Функция желудочков улучшилась, и водянка исчезла в течение 3-4 недель после ВПАП у 71,4% (10/14) плодов при технически успешном вмешательстве. Бивентрикулярный результат был достигнут у 50% успешно пролеченных пациентов.
Выводы
Плоды с КСА и водянкой можно успешно лечить с помощью ВПАП. Эта процедура может восстановить достаточный сердечный выброс плода, что может привести к исчезновению водянки. Выжившие пациенты кажутся хорошими кандидатами на бивентрикулярный исход. © 2020 Международное общество ультразвука в акушерстве и гинекологии
ВСТУПЛЕНИЕ
Критический стеноз аорты плода (КСА) может привести к неиммунной водянке из-за застойной сердечной недостаточности. Обычно присутствует митральная регургитация более высокой степени с ограничением или преждевременным закрытием овального отверстия.
Дисфункция правого желудочка вызвана расширением левого желудочка под высоким давлением, что приводит к нарушению наполнения правого желудочка, повышению системного венозного давления и низкому сердечному выбросу. Если водянка развивается в этой обстановке, и если ее не лечить, то может наступить внутриутробная смерть (ВУС) или неонатальная смерть почти во всех зарегистрированных случаях.
Возможными терапевтическими вариантами являются преждевременные роды и послеродовое лечение, трансплацентарное введение дигоксина или вальвулопластика аорты плода (ВПАП) с септостомией предсердий или без нее; тем не менее, зарегистрированный уровень смертности остается высоким даже в случаях вмешательства.
В серии случаев, опубликованных группой в Бостоне в 2011 году, из 10 плодов с КСА и водянкой, которые подверглись пренатальному вмешательству на сердце с помощью ВПАП и / или стентирования или дилатации межпредсердной перегородки, только двое были живы при последнем наблюдении.
Результаты аналогичной когорты были опубликованы группой из Германии в 2020 году. В этой серии из семи плодов с КСА и водянкой, перенесших пренатальное кардиологическое вмешательство, только два пациента были живы при последнем наблюдении.
Целью этого исследования было оценить непосредственные эффекты и исходы ВПАП у плодов с КСА и водянкой, леченных в Детском кардиологическом центре, Линц, Австрия.
МЕТОДЫ
Все пациенты с КСА и водянкой, которые прошли ВПАП в нашем центре в период с октября 2000 г. по февраль 2020 г., были включены в это исследование, которое было одобрено местным комитетом по этике (исследование № 1009/2017); информированное согласие не требовалось.
Все пациенты прошли эхокардиографическое обследование с использованием ультразвукового аппарата Vivid 7, Vivid E9 или Vivid E95 (GE Healthcare, Zipf, Австрия) за несколько дней до и после процедуры (средний интервал после вмешательства, 1 день (диапазон, 1-3 дня)) тем же опытным врачом.
Эхокардиографические данные были проанализированы ретроспективно в отношении размеров и соотношений желудочков и клапанов, а также внутри- и экстракардиальной гемодинамики. Легочный венозный кровоток оценивался по соотношению ретроградного и антеградного интеграла скорости-времени (VTI).
Все вмешательства проводились, как описано ранее, под контролем УЗИ и под общей анестезией матери без отдельной анальгезии плода. Левый желудочек плода был пунктирован иглой 17, 18 или 19 калибра (Cook Medical Systems, Лимерик, Ирландия). Для дилатации клапана использовался коронарный баллонный катетер диаметром 3, 4 или 5 мм (Maverick, Boston Scientific, Вена, Австрия; Tyshak Mini, NuMed for Children, Орландо, Флорида, США). После ВПАП всем пациентам до срока назначали трансплацентарный дигоксин (целевой уровень 0,5–1,5 нг / мл) для поддержки сердечной функции плода.
Карты пациентов были проанализированы ретроспективно на предмет послеродовых процедур и исходов. Диагноз КСА ставился, если у пациента был тяжелый стеноз аортального клапана в сочетании с плохо сокращающимся, расширенным левым желудочком, ретроградным кровотоком дуги аорты и шунтированием слева направо через овальное отверстие.
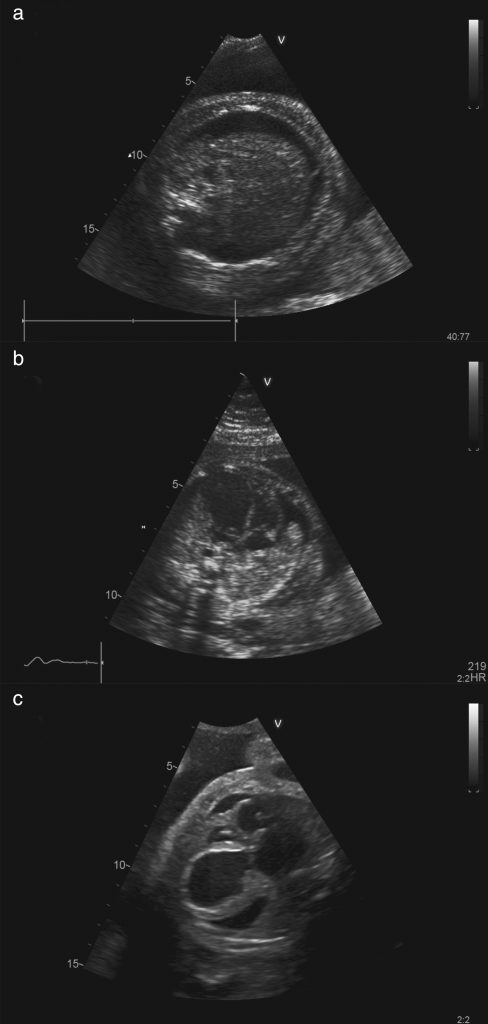
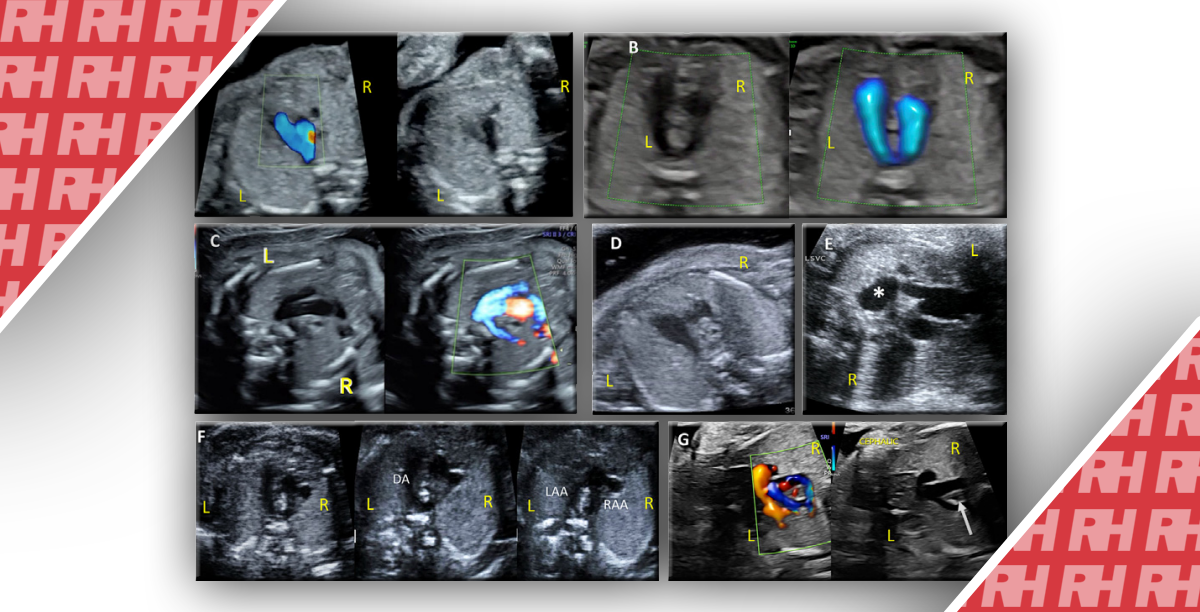
От умеренной до тяжелой водянки считалось скопление жидкости по крайней мере в двух отделах плода (т.е. асцит, плевральный выпот, перикардиальный выпот или отек кожи) (Рисунок 1).
ВПАП считалась успешной, если аортальный клапан был пройден и расширен баллонным катетером с последующим улучшением антеградного кровотока и / или новой регургитацией аортального клапана. Бивентрикулярный исход определялся как кровообращение, при котором левый желудочек был единственным источником системного кровотока при отсутствии каких-либо признаков легочной артериальной гипертензии.
Рисунок 1: Ультразвуковые изображения плодов с застойной сердечной недостаточностью и водянкой, вызванной критическим стенозом аорты, показывающие наличие асцита (а), плеврального выпота (б) и перикардиального выпота (в). Водянка также может сопровождаться отеком кожи от умеренного до тяжелого в конце спектра.
Постнатально в нашем центре пролечены шесть пациентов. Все остальные пациенты были доставлены и лечились в специализированных центрах их родной страны. Изменения функции и размеров левого желудочка до и после ВПАП оценивались с использованием парного t-критерия Стьюдента; P ≤ 0,05 считалось показателем статистической значимости. Для отчета о результатах использовался анализ «намерение лечиться».
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
В период с октября 2000 года по февраль 2020 года в Детском кардиологическом центре в Линце было выполнено 180 внутрисердечных вмешательств у 137 плодов. За этот период было выполнено 115 ВПАП 95 плодам. Водянка присутствовала у 15 из этих плодов, все из которых имели тяжелую дилатацию левого желудочка, эндокардиальный фиброэластоз (EFE), дисфункцию и митральную регургитацию высокой степени.
Ни у одного из плодов не было диагностировано основного генетического синдрома или экстракардиальной аномалии. У одного плода (Случай 12) диагностирована гемофилия типа А. Овальное отверстие считалось ограничивающим у 14 плодов и закрытым у одного. Средний срок беременности на момент вмешательства составлял 28 + 2 (диапазон от 22 + 0 до 30 + 3) недель.
В нашем центре не было плодов с диагнозом КСА и водянки, которые не прошли бы ВПАП. ВПАП потребовалось две попытки в двух случаях. У всех пациентов, кроме одного, была хотя бы одна технически успешная процедура, поэтому общий показатель успеха составил 82,4% (14 из 17 процедур).
Смертность, осложнения и недоношенность
В нашей когорте произошло три ВУС, ни одна из которых не считалась связанной с процедурой. У двух плодов, несмотря на успешное вмешательство, водянка быстро прогрессировала, что привело к появлению ВУС через 2 дня. У обоих этих плодов были выраженные признаки сердечной недостаточности с выраженной пульсацией пупочной вены и признаки низкого давления в левом и правом желудочке, что оценивалось по скорости трикуспидальной и митральной регургитации.
Третий плод родился мертворожденным после индуцированных родов на сроке 31 + 1 неделя из-за материнского HELLP-синдрома, через 3 недели после технически неудачной процедуры. Двенадцать пациенток родились живыми со средним сроком беременности 39 + 3 (диапазон от 33 + 4 до 40 + 0) недель.
Пять (33,3%) пациентов имели стойкую брадикардию во время ВПАП, требующую лечения, у одного (6,7%) развился тяжелый перикардиальный выпот, который требовал лечения, и у двух (13,3%) пациентов был тромб левого желудочка, который спонтанно разрешился в течение 2 дней. Четыре из 12 (33,3%) пациентов родились преждевременно (в возрасте от 33 + 4 до 35 + 6 недель), и все они были живы на момент написания.
Гемодинамические изменения после ВПАП у живых плодов
Двенадцать плодов выжили после ВПАП без дальнейшего прогрессирования водянки. Сердечные измерения выживших плодов до и после успешного вмешательства показаны в таблице 1. Значительные изменения наблюдались в индексе пульсации венозного протока, наполнении правого желудочка (трикуспидальный клапан VTI (TV-VTI) × частота сердечных сокращений ( ЧСС)) и Z-показатель длины левого желудочка.
Данных о кровотоке в легочных венах не хватало из-за сложности допплеровского отслеживания при увеличении левого предсердия у этих пациентов. У пяти пациентов с данными допплерографии легочной вены до и после ВПАП можно было наблюдать тенденцию к лучшему антеградному кровотоку в легочной вене. Скорость струи митральной регургитации оставалась высокой и даже увеличивалась у некоторых плодов после успешного вмешательства.
| Параметр | n | До ВПАП | После ВПАП | Р |
| Длина ЛЖ Z-показатель | 11 | 2.42 (0.13–4.06) | 1.81 (–0.39 to 3.92) | 0.01194 |
| Соотношение ПЖ / ЛЖ | 11 | 0.976 (0.842–1.170) | 1.004 (0.819–1.297) | 0.05817 |
| Время наполнения ЛЖ | 12 | 0.37 (0.18–0.44) | 0.38 (0.26–0.53) | 0.19235 |
| МК ‐ Vмакс | 12 | 3.15 (2.00–3.92) | 3.3 (2.0–4.2) | 0.6557 |
| TV ‐ VTI × ЧСС (см × уд / мин) | 11 | 885 (611–1372) | 994 (728–1367) | 0.0323 |
| Коэффициент допплера легочных вен (ретроградный / антеградный VTI) | 5 | 0.33 (0.17–0.48) | 0.09 (0.05–0.38) | 0.08061 |
| Индекс пульсации венозного протока | 7 | 1.11 (0.83–2.19) | 0.97 (0.67–1.83) | 0.00798 |
Водянка
Перед ВПАП у всех плодов наблюдалась водянка средней и тяжелой степени. Водянка исчезла у 10/14 (71,4%) плодов после технически успешной ВПАП.
У 2/14 плодов (14,3%) водянка быстро прогрессировала, несмотря на успешное расширение аортального клапана, что привело к ВУС. Два других плода родились живыми с тяжелой формой водянки, но умерли в течение первых часов после рождения; один родился преждевременно, а другой родился после искусственных родов из-за прогрессирующей водянки (точный срок беременности отсутствует для обоих случаев).
У одного субъекта с технически неудачной процедурой водянка не исчезла, и плод родился мертвым после индуцированных родов из-за материнского HELLP-синдрома.
Послеродовой исход
Десять пациентов родились живыми без водянки, и всем удалось добиться бивентрикулярного кровообращения. Три субъекта (случаи 2, 3 и 5) умерли через 90, 47 и 60 дней соответственно.
Пациент 2 родился в срок и перенес операцию по восстановлению коарктации без дальнейшего вмешательства на выводном тракте левого желудочка. Этот субъект умер через 90 дней из-за стойкой легочной гипертензии и левожелудочковой недостаточности. Пациент 3 родился доношенным в нашем центре и перенес неонатальную операцию Росс-Конно с резекцией EFE на 10-й день. Смерть наступила через 1,5 месяца из-за некротического энтероколита и почечной недостаточности.
Пациенту 5 была выполнена неонатальная вальвулопластика аорты без хирургических вмешательств на выводном тракте левого желудочка, и в конечном итоге он умер в возрасте 2 месяцев от сердечной недостаточности слева с легочной артериальной гипертензией.
7 из 14 успешно пролеченных пациентов (50,0%; 46,7% от всей когорты) были бивентрикулярными и были живы на момент написания после среднего периода наблюдения 2 года (диапазон 0,02–12,38 года). У всех этих пациентов не было эхокардиографических признаков легочной гипертензии, и ни один пациент не получал лечение легочными вазодилататорами или дополнительным кислородом.
ОБСУЖДЕНИЕ
Водянка у плодов с КСА обычно связана с быстрым прогрессированием и ухудшением состояния, приводящим к ВУС. В этой серии пациентов с КСА и водянкой мы показали, что технически успешная процедура ВПАП может спасти большинство плодов, изменив состояние низкого сердечного выброса.
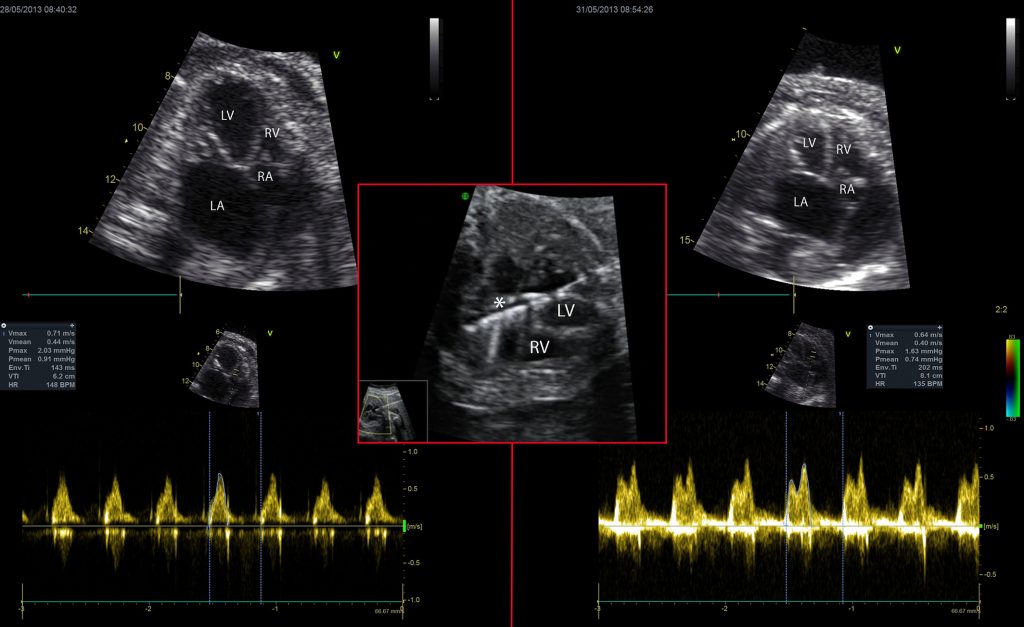
Это было достигнуто за счет декомпрессии левого желудочка и значительного немедленного уменьшения размера левого желудочка (Z-оценка длины левого желудочка) и объема. Кроме того, это привело к значительному улучшению наполнения и функции правых отделов сердца, о чем свидетельствует значительно увеличенное произведение TV-VTI × ЧСС (Рисунок 2), а также снижение центрального венозного давления, о чем свидетельствует значительно сниженный индекс пульсации венозного протока.
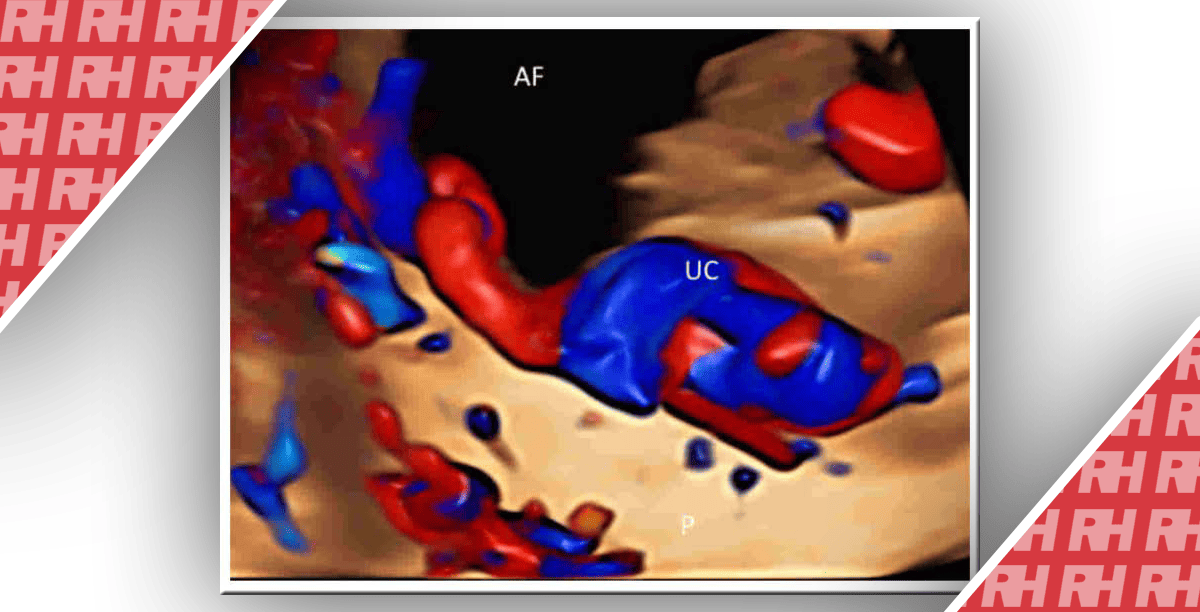
Рисунок 2: Четырехкамерные изображения и соответствующие доплеровские кривые у пациента с критическим стенозом аорты (КСА) до (левая панель) и после (правая панель) вальвулопластики аорты плода (ВПАП) (центральная панель). КСА с рестриктивной межпредсердной перегородкой может привести к серьезному увеличению левого желудочка (ЛЖ) с высоким давлением ЛЖ, ухудшающим комбинированный сердечный выброс плода за счет компрессии правого желудочка (ПЖ) (левая панель). ВПАП (центральная панель) может эффективно уменьшить размер ЛЖ, что приведет к улучшению наполнения ПЖ и снижению центрального венозного давления, спасая плод от внутриутробной гибели. Обратите внимание на уменьшение размера ЛЖ и увеличение размера ПЖ после процедуры (справа). Допплерография притока трехстворчатого клапана показывает изменение от монофазного к двухфазному паттерну и увеличение VTI × HR с 917 см / с до 1093 см / с. Звездочка (изображение) указывает на надутый баллонный катетер через кольцо аортального клапана.
В заключение, ВПАП может спасти плоды с КСА и водянкой. Большие левые желудочки с высоким давлением, с одной стороны, наиболее вероятно ответственны за развитие водянки за счет нарушения наполнения и функции правого желудочка, но с другой стороны, они являются благоприятными предпосылками для хорошего бивентрикулярного исхода. Кажется, есть точка невозврата в отношении восстановления функции левого желудочка, поэтому ВПАП следует проводить как можно скорее после диагностики КСА.