🤖 Короткий переказ від ШІ
Критичний стеноз аорти (КСА) з рестриктивною міжпередсердною перегородкою може призвести до серцевої недостатності та водянки плоду. Це дослідження оцінює вплив вальвулопластики аорти плода (ВПАП) на гемодинаміку та результати у таких пацієнтів.
ВПАП успішно лікує плоди з КСА та водянкою, відновлюючи серцевий викид і призводячи до зникнення водянки у 71,4% випадків. Вижилі пацієнти мають добрі шанси на бішлунковий результат. Дослідження підкреслює важливість раннього проведення ВПАП для запобігання незворотним змінам. Додаткову інформацію про УЗД апарати можна знайти на нашому сайті.
✅ Ключові тези зі статті:
- Діагностика: Діагностика КСА включає оцінку стенозу аортального клапана, дилатації лівого шлуночка та ретроградного кровотоку.
- Лікування: Вальвулопластика аорти плода (ВПАП) є ефективним методом лікування плодів з КСА та водянкою.
- Переваги: ВПАП може відновити достатній серцевий викид, зменшити водянку та покращити функцію серця плода.
- Обмеження: Існують ризики, пов’язані з ВПАП, такі як внутрішньоутробна смерть, брадикардія та розвиток водянки, що прогресує.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: A. Tulzer, W. Arzt, G. Tulzer
Мета
Критичний стеноз аорти (КСА) з рестриктивною міжпередсердною перегородкою може привести до застійної серцевої недостатності і водянки плоду, що зазвичай призводить до загибелі плоду, якщо його не лікувати. Метою цього дослідження було оцінити вплив вальвулопластики аорти плода (ВПАП) на гемодинаміку і результати у цих пацієнтів.
Методи
Це був ретроспективний огляд плодів з КСА і ознаками водянки, які перенесли ВПАП в нашому центрі в період з 2000 по 2020 роки. Ехокардіограми і карти пацієнтів були проаналізовані на предмет розмірів шлуночків і клапанів, а також на результат.
Отримані результати
Водянка була присутня під час втручання у 15 плодів з КСА, які пройшли ВПАП в нашому центрі протягом періоду дослідження. Всі пацієнти, крім одного, пройшли принаймні одну технічно успішну процедуру. Смертей, пов’язаних з процедурою, не було, але сталося три внутрішньоутробних смерті. Дванадцять суб’єктів були живонародженими, двоє з яких померли протягом 24 годин після народження через стійку водянку. Функція шлуночків покращилася, і водянка зникла протягом 3-4 тижнів після ВПАП у 71,4% (10/14) плодів при технічно успішному втручанні. Бівентрикулярний результат був досягнутий у 50% успішно пролікованих пацієнтів.
Висновки
Плоди з КСА і водянкою можна успішно лікувати за допомогою ВПАП. Ця процедура може відновити достатній серцевий викид плоду, що може привести до зникнення водянки. Ті, що вижили пацієнти здаються хорошими кандидатами на бівентрикулярний результат. © 2020 Міжнародне товариство ультразвуку в акушерстві і гінекології
ВСТУП
Критичний стеноз аорти плода (КСА) може привести до неімунної водянки через застійну серцеву недостатність. Зазвичай присутня мітральна регургітація більш високого ступеня з обмеженням або передчасним закриттям овального отвору.
Дисфункція правого шлуночка викликана розширенням лівого шлуночка під високим тиском, що призводить до порушення наповнення правого шлуночка, підвищення системного венозного тиску і низького серцевого викиду. Якщо водянка розвивається в цій обстановці, і якщо її не лікувати, то може наступити внутрішньоутробна смерть (ВУС) або неонатальна смерть майже у всіх зареєстрованих випадках.
Можливими терапевтичними варіантами є передчасні пологи і післяпологове лікування, трансплацентарне введення дигоксину або вальвулопластика аорти плода (ВПАП) з септостомією передсердь або без неї; тим не менш, зареєстрований рівень смертності залишається високим навіть у випадках втручання.
У серії випадків, опублікованих групою в Бостоні в 2011 році, з 10 плодів з КСА і водянкою, які зазнали пренатального втручання на серці за допомогою ВПАП і / або стентування або дилатації міжпередсердної перегородки, тільки двоє були живі при останньому спостереженні.
Результати аналогічної когорти були опубліковані групою з Німеччини в 2020 році. У цій серії з семи плодів з КСА і водянкою, які перенесли пренатальне кардіологічне втручання, тільки два пацієнта були живі при останньому спостереженні.
Метою цього дослідження було оцінити безпосередні ефекти та наслідки ВПАП у плодів з КСА і водянкою, які лікувалися в Дитячому кардіологічному центрі, Лінц, Австрія.
МЕТОДИ
Всі пацієнти з КСА і водянкою, які пройшли ВПАП в нашому центрі в період з жовтня 2000 року по лютий 2020 р були включені в це дослідження, яке було схвалено місцевим комітетом з етики (дослідження № 1009/2017); інформована згода не була потрібна.
Всі пацієнти пройшли ехокардіографічне обстеження з використанням ультразвукового апарату Vivid 7, Vivid E9 або Vivid E95 (GE Healthcare, Zipf, Австрія) за кілька днів до і після процедури (середній інтервал після втручання, 1 день (діапазон, 1-3 дні)) тим же досвідченим лікарем.
Ехокардіографічні дані були проаналізовані ретроспективно щодо розмірів і співвідношень шлуночків і клапанів, а також внутрішньо- і екстракардіальної гемодинаміки. Легеневий венозний кровотік оцінювався по співвідношенню ретроградного і антеградного інтеграла швидкості-часу (VTI).
Всі втручання проводилися, як описано раніше, під контролем УЗД і під загальною анестезією матері без окремої аналгезії плода. Лівий шлуночок плода був пунктований голкою 17, 18 або 19 калібру (Cook Medical Systems, Лімерик, Ірландія). Для дилатації клапана використовувався коронарний балонний катетер діаметром 3, 4 або 5 мм (Maverick, Boston Scientific, Відень, Австрія; Tyshak Mini, NuMed for Children, Орландо, Флорида, США). Після ВПАП всім пацієнтам до терміну призначали трансплацентарний дігоксин (цільовий рівень 0,5-1,5 нг / мл) для підтримки серцевої функції плода.
Карти пацієнтів були проаналізовані ретроспективно на предмет післяпологових процедур і результатів. Діагноз КСА ставився, якщо у пацієнта був важкий стеноз аортального клапана в поєднанні з погано скорочувальним, розширеним лівим шлуночком, ретроградним кровотоком дуги аорти і шунтуванням зліва направо через овальний отвір.
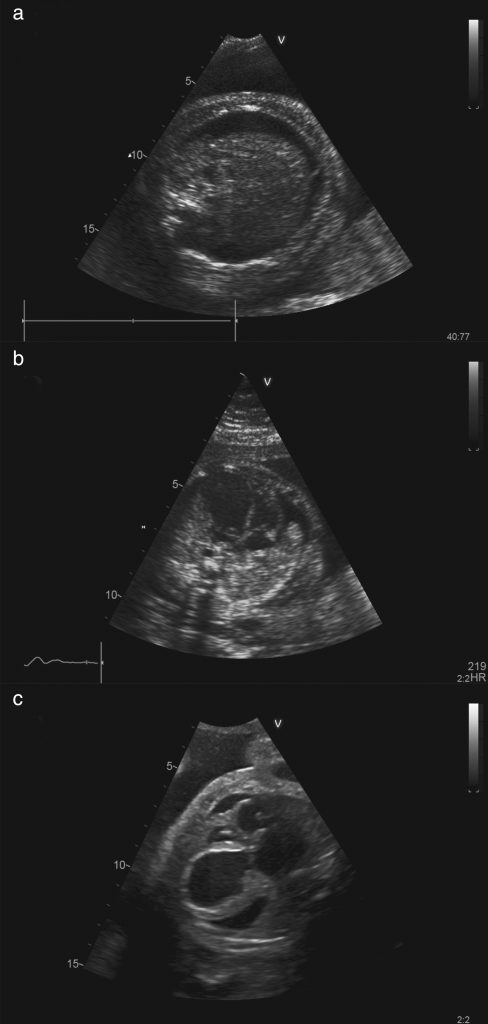
Від помірної до важкої водянки вважалося скупчення рідини по крайній мірі в двох відділах плода (тобто асцит, плевральний випіт, перикардіальний випіт або набряк шкіри) (Зображення 1).
ВПАП вважалася успішною, якщо аортальний клапан був пройдений і розширений балонним катетером з подальшим поліпшенням антеградного кровотоку і / або новою регургитацією аортального клапана. Бівентрікулярний результат визначався як кровообіг, при якому лівий шлуночок був єдиним джерелом системного кровотоку при відсутності будь-яких ознак легеневої артеріальної гіпертензії.
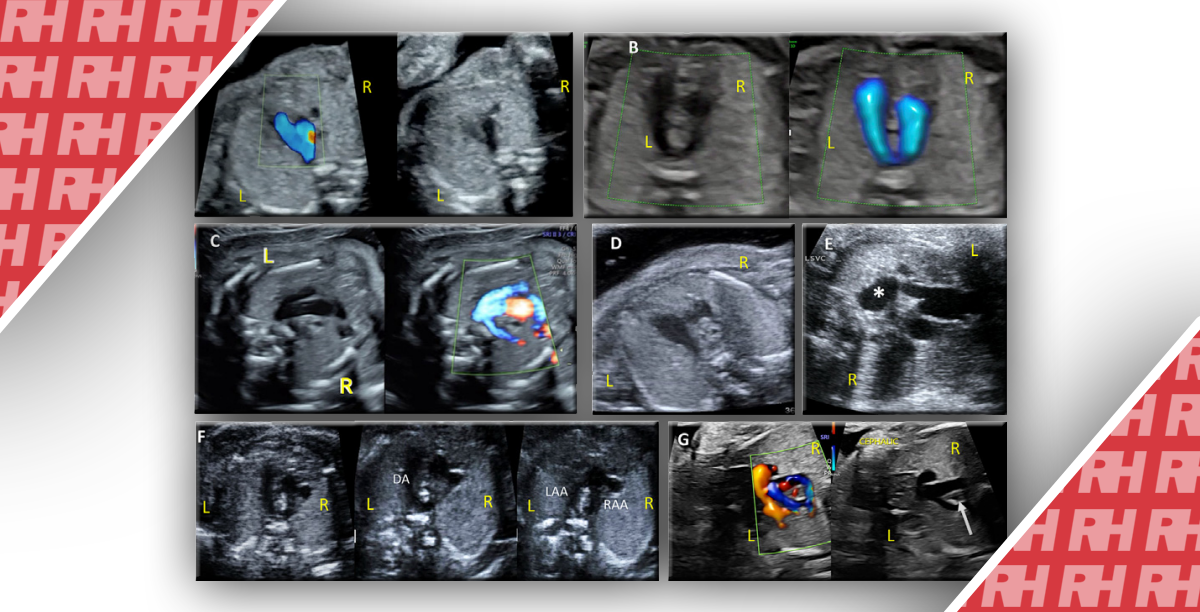
Зображення 1: Ультразвукові зображення плодів із застійною серцевою недостатністю і водянкою, викликаної критичним стенозом аорти, що показують наявність асциту (а), плеврального випоту (б) і перикардіального випоту (в). Водянка також може супроводжуватися набряком шкіри від помірного до важкого в кінці спектра.
Постнатально в нашому центрі проліковано шість пацієнтів. Всі інші пацієнти були доставлені і лікувалися в спеціалізованих центрах їх рідної країни. Зміни функції і розмірів лівого шлуночка до та після ВПАП оцінювалися з використанням парного t-критерію Стьюдента; P ≤ 0,05 вважалося показником статистичної значущості. Для звіту про результати використовувався аналіз «намір лікуватися».
ОТРИМАНІ РЕЗУЛЬТАТИ
У період з жовтня 2000 року по лютий 2020 року в Дитячому кардіологічному центрі в Лінці було виконано 180 внутрішньосерцевих втручань у 137 плодів. За цей період було виконано 115 ВПАП 95 плодам. Водянка була присутня у 15 з цих плодів, всі з яких мали важку дилатацію лівого шлуночка, ендокардіальний фіброеластоз (EFE), дисфункцію і мітральну регургітацію високого ступеня.
У жодного з плодів не було діагностовано основного генетичного синдрому або екстракардіальної аномалії. У одного плоду (Випадок 12) діагностована гемофілія типу А. Овальний отвір вважався обмежуючим у 14 плодів і закритим у одного. Середній термін вагітності на момент втручання становив 28 + 2 (діапазон від 22 + 0 до 30 + 3) тижнів.
У нашому центрі не було плодів з діагнозом КСА і водянки, які не пройшли б ВПАП. ВПАП знадобилося дві спроби в двох випадках. У всіх пацієнтів, крім одного, була хоча б одна технічно успішна процедура, тому загальний показник успіху склав 82,4% (14 з 17 процедур).
Смертність, ускладнення і недоношеність
В нашій когорті сталося три ВУС, жодна з яких не вважалася пов’язаної з процедурою. У двох плодів, незважаючи на успішне втручання, водянка швидко прогресувала, що призвело до появи ВУС через 2 дня. У обох цих плодів були виражені ознаки серцевої недостатності з вираженою пульсацією пупкової вени і ознаки низького тиску в лівому і правому шлуночку, що оцінювалося за швидкістю трикуспідальної і мітральної регургітації.
Третій плід народився мертвонародженим після індукованих пологів на терміні 31 + 1 тиждень через материнський HELLP-синдром, через 3 тижні після технічно невдалої процедури. Дванадцять пацієнток народилися живими з середнім терміном вагітності 39 + 3 (діапазон від 33 + 4 до 40 + 0) тижнів.
П’ять (33,3%) пацієнтів мали стійку брадикардію під час ВПАП, що вимагає лікування, у одного (6,7%) розвинувся важкий перикардіальний випіт, який вимагав лікування, і у двох (13,3%) пацієнтів був тромб лівого шлуночка, який спонтанно розв’язався протягом 2 днів. Чотири з 12 (33,3%) пацієнтів народилися передчасно (у віці від 33 + 4 до 35 + 6 тижнів), і всі вони були живі на момент написання.
Гемодинамічні зміни після ВПАП у живих плодів
Дванадцять плодів вижили після ВПАП без подальшого прогресування водянки. Серцеві вимірювання виживших плодів до і після успішного втручання показані в таблиці 1. Значні зміни спостерігалися в індексі пульсації венозної протоки, наповненні правого шлуночка (трикуспідального клапан VTI (TV-VTI) × частота серцевих скорочень (ЧСС)) і Z-показник довжини лівого шлуночка .
Даних про кровотік в легеневих венах не вистачало через складність доплерівського відстеження при збільшенні лівого передсердя у цих пацієнтів. У п’яти пацієнтів з даними доплерографії легеневої вени до і після ВПАП можна було спостерігати тенденцію на кращий антеградний кровотік в легеневій вені. Швидкість струменя мітральної регургітації залишалася високою і навіть збільшувалася у деяких плодів після успішного втручання.
| Параметр | n | До ВПАП | Після ВПАП | Р |
| Довжина ЛШ Z-показник | 11 | 2.42 (0.13–4.06) | 1.81 (–0.39 to 3.92) | 0.01194 |
| Співвідношення ПШ / ЛШ | 11 | 0.976 (0.842–1.170) | 1.004 (0.819–1.297) | 0.05817 |
| Час наповнення ЛШ | 12 | 0.37 (0.18–0.44) | 0.38 (0.26–0.53) | 0.19235 |
| МК ‐ Vмакс | 12 | 3.15 (2.00–3.92) | 3.3 (2.0–4.2) | 0.6557 |
| TV ‐ VTI × ЧСС (см × уд / хв) | 11 | 885 (611–1372) | 994 (728–1367) | 0.0323 |
| Коефіцієнт доплеру легеневих вен (ретроградний / антеградний VTI) | 5 | 0.33 (0.17–0.48) | 0.09 (0.05–0.38) | 0.08061 |
| Індекс пульсації венозної протоки | 7 | 1.11 (0.83–2.19) | 0.97 (0.67–1.83) | 0.00798 |
Водянка
Перед ВПАП у всіх плодів спостерігалася водянка середнього та тяжкого ступеня. Водянка зникла у 10/14 (71,4%) плодів після технічно успішної ВПАП.
У 2/14 плодів (14,3%) водянка швидко прогресувала, незважаючи на успішне розширення аортального клапана, що призвело до ВУС. Два інших плода народилися живими з важкою формою водянки, але померли протягом перших годин після народження; один народився передчасно, а інший народився після штучних пологів через прогресуючу водянку (точний термін вагітності відсутній для обох випадків).
У одного суб’єкта з технічно невдалої процедурою водянка не зникла, і плід народився мертвим після індукованих пологів через материнський HELLP-синдром.
Післяпологовий результат
Десять пацієнтів народилися живими без водянки, і всім вдалося домогтися бівентрікулярного кровообігу. Три суб’єкта (випадки 2, 3 і 5) померли через 90, 47 і 60 днів відповідно.
Пацієнт 2 народився в термін і переніс операцію по відновленню коарктації без подальшого втручання на вивідному тракті лівого шлуночка. Цей суб’єкт помер через 90 днів через стійку легеневу гіпертензію і лівошлуночкову недостатність. Пацієнт 3 народився доношеним в нашому центрі і переніс неонатальную операцію Росс-Кінно з резекцією EFE на 10-й день. Смерть наступила через 1,5 місяці через некротичний ентероколіт і ниркову недостатність.
Пацієнту 5 була виконана неонатальна вальвулопластика аорти без хірургічних втручань на вивідному тракті лівого шлуночка, і в кінцевому підсумку він помер у віці 2 місяців від серцевої недостатності зліва з легеневою артеріальною гіпертензією.
7 з 14 успішно пролікованих пацієнтів (50,0%; 46,7% від усієї когорти) були бівентрікулярними і були живі на момент написання після середнього періоду спостереження 2 роки (діапазон 0,02-12,38 року). У всіх цих пацієнтів не було ехокардіографічних ознак легеневої гіпертензії, і жоден пацієнт не отримував лікування легеневими вазодилататорами або додатковим киснем.
ОБГОВОРЕННЯ
Водянка у плодів з КСА зазвичай пов’язана з швидким прогресуванням і погіршенням стану, що призводить до ВУС. У цій серії пацієнтів з КСА і водянкою ми показали, що технічно успішна процедура ВПАП може врятувати більшість плодів, змінивши стан низького серцевого викиду.
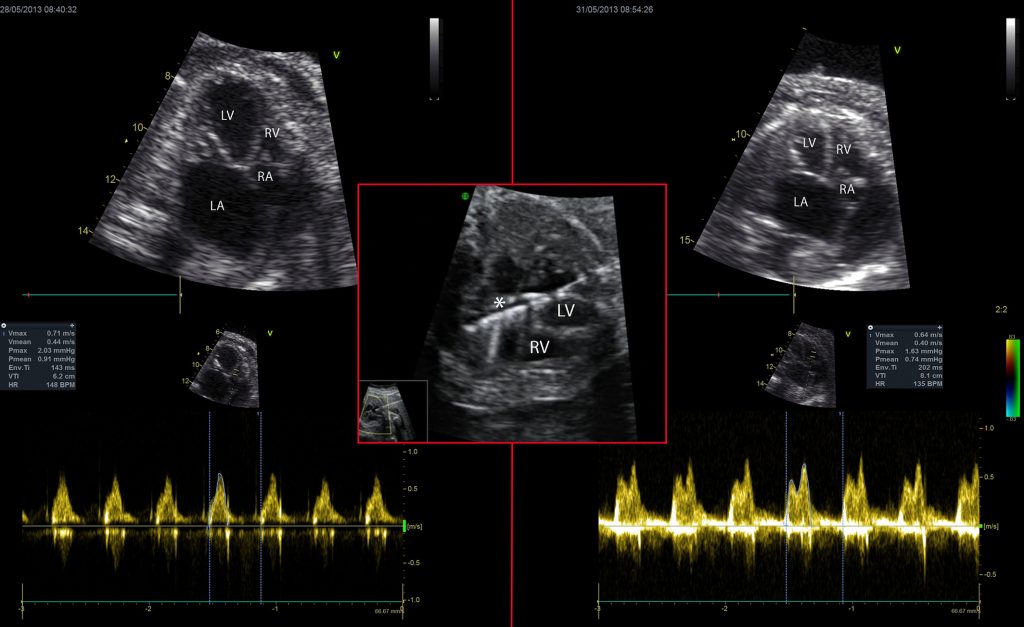
Це було досягнуто за рахунок декомпресії лівого шлуночка і значного негайного зменшення розміру лівого шлуночка (Z-оцінка довжини лівого шлуночка) і об’єму. Крім того, це призвело до значного поліпшення наповнення і функції правих відділів серця, про що свідчить значно збільшене TV-VTI × ЧСС (Зображення 2), а також зниження центрального венозного тиску, про що свідчить значно знижений індекс пульсації венозної протоки.
Зображення 2: Чотирикамерні зображення і відповідні доплерівські криві у пацієнта з критичним стенозом аорти (КСА) до (ліва панель) і після (права панель) вальвулопластики аорти плода (ВПАП) (центральна панель). КСА з рестриктивною міжпередсердною перегородкою може привести до серйозного збільшення лівого шлуночка (ЛШ) з високим тиском ЛШ, що погіршує комбінований серцевий викид плоду за рахунок компресії правого шлуночка (ПШ) (ліва панель). ВПАП (центральна панель) може ефективно зменшити розмір ЛШ, що призведе до поліпшення наповнення ПШ і зниження центрального венозного тиску, рятуючи плід від внутрішньоутробної загибелі. Зверніть увагу на зменшення розміру ЛШ і збільшення розміру ПШ після процедури (праворуч). Доплерографія припливу тристулкового клапана показує зміну від монофазного до двофазного паттерну і збільшення VTI × HR з 917 см / с до 1093 см / с. Зірочка (зображення) вказує на надутий балонний катетер через кільце аортального клапана.
На закінчення, ВПАП може врятувати плоди з КСА і водянкою. Великі ліві шлуночки з високим тиском, з одного боку, найбільш ймовірно відповідальні за розвиток водянки за рахунок порушення наповнення і функції правого шлуночка, але з іншого боку, вони є сприятливими передумовами для хорошого бівентрикулярного результату. Здається, є точка неповернення щодо відновлення функції лівого шлуночка, тому ВПАП слід проводити якомога швидше після діагностики КСА.
Питання та відповіді (FAQ)
Що таке критичний стеноз аорти (КСА)?
- Критичний стеноз аорти (КСА) – це важке звуження аортального клапана, що призводить до обмеження кровотоку з лівого шлуночка в аорту. Це може спричинити застійну серцеву недостатність та водянку плоду.
Що таке вальвулопластика аорти плода (ВПАП)?
- Вальвулопластика аорти плода (ВПАП) – це мінімально інвазивна процедура, яка використовується для розширення звуженого аортального клапана у плода. Вона проводиться під контролем УЗД.
Які показання до проведення ВПАП?
- ВПАП показана при критичному стенозі аорти з ознаками водянки плоду, що загрожує життю плода.
Яка ефективність ВПАП?
- ВПАП показала високу ефективність у поліпшенні гемодинаміки та зменшенні водянки у плодів з КСА. У 71,4% випадків водянка зникла після процедури.
Які ризики пов’язані з ВПАП?
- Ризики ВПАП включають внутрішньоутробну смерть, брадикардію, перикардіальний випіт та тромбоз лівого шлуночка. Однак, смертність, пов’язана безпосередньо з процедурою, низька.
Які результати після ВПАП?
- Більшість плодів, які вижили після ВПАП, досягли бівентрикулярного кровообігу. Однак, деякі пацієнти померли після народження через різні ускладнення.
Коли слід проводити ВПАП?
- ВПАП слід проводити якомога швидше після діагностики КСА та водянки плоду, щоб запобігти незворотним змінам у серці плода.