🤖 Короткий переказ від ШІ
Нейроендокринні пухлини тонкої кишки (НЕП-ТК) стають все більш поширеними, а їх діагностика та лікування вимагають застосування сучасних ендоскопічних методів, таких як ендоскопічне УЗД та ендоскопічна резекція.
Огляд підкреслює важливість ендоскопічного УЗД для оцінки розміру та глибини інвазії при НЕП дванадцятипалої кишки, що впливає на вибір лікування, та детально розглядає різні ендоскопічні техніки, включаючи УЗД апарати, для діагностики та лікування НЕП-ТК, відзначаючи їх переваги та обмеження.
✅ Ключові тези зі статті:
- Діагностика: Ендоскопічні методи, такі як ЕУЗД та відеокапсульна ендоскопія, відіграють ключову роль у виявленні та стадіюванні НЕП-ТК.
- Лікування: Ендоскопічні техніки, включаючи ЕРСО, ЕПСД та ЕПР, застосовуються для лікування НЕП дванадцятипалої кишки, тоді як для пухлин порожньої та клубової кишки хірургічна резекція залишається основою.
- Переваги: Ендоскопічні методи пропонують менш інвазивні варіанти лікування, що дозволяє уникнути хірургічних ускладнень та прискорити відновлення.
- Обмеження: Деякі ендоскопічні процедури можуть бути технічно складними, пов’язані з ризиком ускладнень та обмеженою частотою резекції R0, особливо для пухлин порожньої та клубової кишки.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: Ji Yoon Yoon, Nikhil A. Kumta, Michelle Kang Kim
Зміст:
- Вступ
- Нейроендокринні пухлини дванадцятипалої кишки
- Ендоскопічна УЗД
- Ендоскопічна резекція
- Нейроендокринні пухлини порожньої та клубової кишки
- Відеокапсульна ендоскопія
- Балонна ентероскопія
- Висновки
Вступ
Нейроендокринні пухлини (НЕП) шлунково-кишкової системи є гетерогенною групою новоутворень, поведінка яких відрізняється в залежності від первинної локалізації, гістології та стадії.
Аналіз популяційних регістрів, таких як Програма спостереження, епідеміології та кінцевих результатів (SEER), продемонстрував зростання захворюваності на НЕП, так що станом на 2000 р. НЕП були найбільш поширеним злоякісним новоутворенням тонкої кишки, обігнавши аденокарциному.
НЕП тонкої кишки (НЕП-ТК) становлять приблизно 30% НЕП шлунково-кишкового тракту. На додаток до їх зростаючої частоти, НЕП-ТК, ймовірно, будуть навіть більш поширеними, ніж зафіксовано в реєстрі SEER, що може виключити дрібніші, локалізованіші НЕП, які часто вважаються доброякісними.
НЕП часто безсимптомні та діагностуються випадково при візуалізації у поперечному перерізі або ендоскопії за іншими показаннями. Клінічна картина НЕП-ТК часто підступна і неспецифічна, з такими симптомами, як дискомфорт у животі та діарея, які виявляються за роки до встановлення діагнозу.
Типовий карциноїдний синдром зустрічається рідко навіть при НЕП-ТК: у 26% пацієнтів спостерігається діарея, у 13% гіперемія і у 2% бронхоконстрикція. До чверті пацієнтів може мати кишкову непрохідність.
НЕП-ТК класифікуються за стадіями відповідно до системи стадування TNM Американського об’єднаного комітету з раку (AJCC) (таблиця 1) та класифікуються відповідно до системи оцінок Європейського товариства нейроендокринних пухлин/Всесвітньої організації охорони здоров’я (таблиця 2) для прогнозування.
Таблиця 1:
| Дванадцятипала кишка (за винятком фатерової ампули) | Порожня і клубова кишка | |
| Первинна пухлина (Т) | ||
| Тх | Первинна пухлина може бути оцінена | Первинна пухлина може бути оцінена |
| Т0 | Немає ознак первинної пухлини | Немає ознак первинної пухлини |
| Т1 | Залучена лише слизова або підслизова оболонка на ≤1 см. | Залучено лише власну пластину або підслизову оболонку на ≤1 см. |
| Т2 | Розповсюджується на власну м’язову оболонку або становить >1 см | Розповсюджується на власну м’язову оболонку або становить >1 см |
| Т3 | Вражає підшлункову залозу або періпанкреатичну жирову тканину. | Проростає через власну мускулатуру в підсерозну тканину, не проникаючи у серозну оболонку, що лежить вище. |
| Т4 | Проростає в вісцеральну очеревину (серозну оболонку) або інші органи | Проростає у вісцеральну очеревину (серозну оболонку) чи інші органи чи сусідні структури |
| Регіонарний лімфатичний вузол (N) | ||
| Nx | Регіональні лімфатичні вузли не можуть бути оцінені | Регіональні лімфатичні вузли не можуть бути оцінені |
| N0 | Відсутність ураження регіонарних лімфатичних вузлів | Відсутність ураження регіонарних лімфатичних вузлів |
| N1 | Залучення регіонарних лімфатичних вузлів | Метастази у регіонарні лімфатичні вузли менше 12 вузлів |
| N2 | Н/Д | Н/Д |
| Віддалені метастази (М) | ||
| M0 | Відсутність віддалених метастазів | Відсутність віддалених метастазів |
| M1 | Віддалені метастази | Віддалені метастази |
| M1a | Обмежені печінкою | Обмежені печінкою |
| M1b | Принаймні, в одному позапечінковому місці | Принаймні, в одному позапечінковому місці |
| M1c | Печінкові та позапечінкові метастази | Печінкові та позапечінкові метастази |
| Групи прогностичних стадій AJCC | ||
| Стадія 1 | T1, N0, M0 | T1, N0, M0 |
| Стадія 2 | T2, N0, M0 | T2, N0, M0 |
| T3, N0, M0 | T3, N0, M0 | |
| Стадія 3 | T4, N0, M0 | Любая T, N1/N2, M0 |
| Будь-яка T, N1, M0 | T4, N0, M0 | |
| Стадія 4 | Будь-яка T, будь-який N, M1 | Будь-яка T, будь-який N, M1 |
Таблиця 2:
| Мітотичний індекс (мітози/HPF) | Індекс Ki-67 (%) | |
| GX | Оцінка не може бути проведена | Оцінка не може бути проведена |
| G1 | <2 | <3 |
| G2 | 2-20 | 3-20 |
| G3 | >20 | >20 |
Оцінка НЕП часто включає комбінацію біохімічних, візуалізаційних та ендоскопічних методів. Біохімічні маркери можуть включати гастрин (дуоденальні НЕП), 5-гідроксиіндолоцтову кислоту (для порожньокишечних/клубових НЕО) і хромогранін А, тоді як візуалізація може включати комп’ютерну томографію (КТ), магнітно-резонансну томографію (МРТ) та як 68Ga- дотація ПЕТ/КТ.
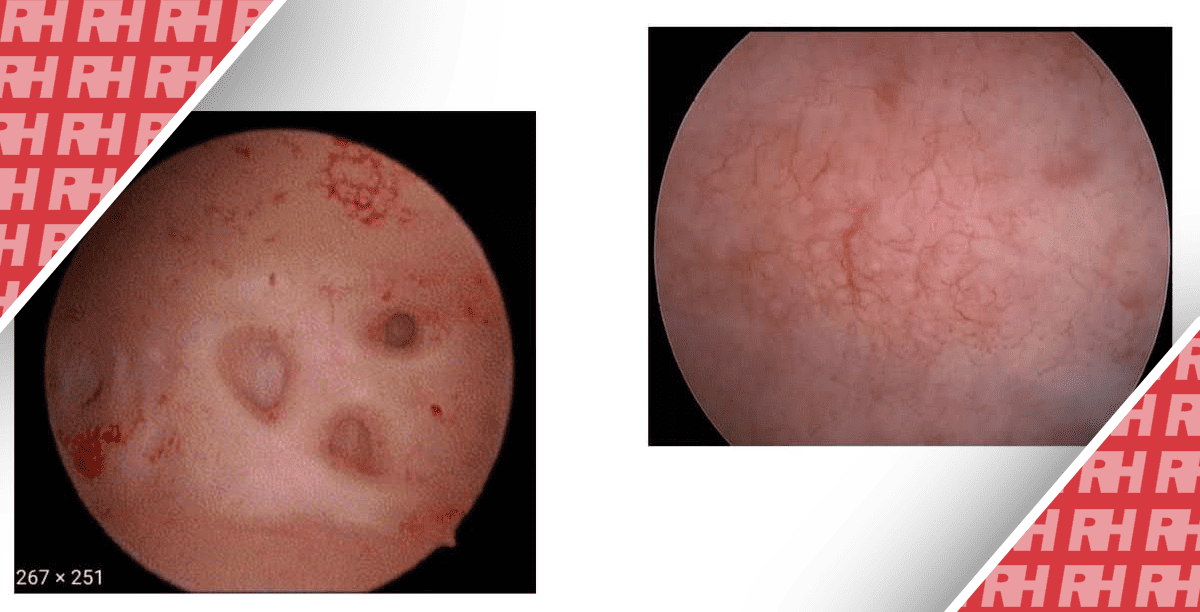
При ендоскопії НЕП-ТК зазвичай виглядають як круглі, іноді тонкі субепітеліальні ураження. Ендоскопічні методи, такі як відеокапсульна ендоскопія та ендоскопічне ультразвукове дослідження (ЕУЗД), можуть бути корисні в діагностиці НЕП, в той час як передові ендоскопічні методи, такі як ендоскопічна резекція слизової оболонки (ЕРСО) та ендоскопічна підслизова диссекція (ЕПСД), можуть стаити наріжним каменем лікування НЕП-ТК. У цьому огляді ми прагнули підкреслити роль ендоскопічних методів у діагностиці та лікуванні НЕП-ТК.
Нейроендокринні пухлини дванадцятипалої кишки
Дуоденальні НЕП часто виявляються випадково при ендоскопії верхніх відділів шлунково-кишкового тракту. Хоча вони найчастіше є нефункціонуючими пухлинами (тобто не пов’язані з клінічним синдромом), НЕП дванадцятипалої кишки також можуть бути пов’язані з синдромом Золлінгера-Еллісона з його клінічною тріадою рефлюксу, виразкової хвороби та діареї. Оскільки дванадцятипала кишка знаходиться в межах досяжності звичайної ендоскопії, її розташування дозволяє проводити гістологічну оцінку, оцінку стадії пухлини та навіть лікувальну ендоскопічну резекцію.
Ендоскопічна УЗД
Розмір та глибина інвазії є важливими факторами ризику, пов’язаними з лімфатичними вузлами та віддаленими метастазами. Ендоскопічне ультразвукове дослідження (ЕУЗД) пропонує метод точної оцінки розміру та глибини інвазії НЕП дванадцятипалої кишки перед резекцією, що необхідно для визначення методу резекції: ендоскопічного або хірургічного.
При ураженнях розміром менше 10 мм ризик залучення лімфатичних вузлів або віддалених метастазів та рецидивів низький. Якщо інвазія власної м’язової оболонки виключена під час ЕУЗД, ендоскопічна резекція підходить для пухлин такого розміру.
Дуоденальна НЕП розміром понад 20 мм пов’язана з більш високим ризиком рецидиву та зниженою виживаністю за конкретним захворюванням і є показанням до хірургічної резекції для отримання більш широких країв.
Для НЕП між 10 та 20 мм дані менш чіткі. За відсутності інвазії м’язової оболонки на ЕУЗД можна розглядати початкову ендоскопічну резекцію. Хірургічну резекцію слід розглядати, якщо при патологоанатомічному дослідженні виявляються ознаки високого ризику, такі як лімфоваскулярна інвазія, високий рівень, високий мітотичний індекс або інвазія власної м’язової оболонки.
Ендоскопічна резекція
Повідомлялося про тенденцію до ендоскопічної резекції порівняно з хірургічною резекцією НЕП дванадцятипалої кишки з перевагою запобігання хірургічним ускладненням. НЕП є підслизовими ураженнями; таким чином, проста поліпектомія не вважається ефективною. Описано різні методи резекції; однак єдиної думки щодо оптимальної техніки немає.
Були вивчені ендоскопічна резекція слизової оболонки (ЕРСО), ендоскопічна підслизова дисекція (ЕПСД) та варіанти цих методик – ендоскопічна резекція на всю товщину (ЕРВТ). Вибраний метод резекції повинен мати найбільшу ймовірність резекції єдиним блоком та резекції R0 (гістологічно чисті бічні та глибокі краї).
Слід також враховувати частоту небажаних явищ, оскільки дванадцятипала кишка має тонкі стінки та має більш високий ризик перфорації, ніж інші області шлунково-кишкового тракту (таблиця 3). Дані про віддалені результати та рецидиви обмежені через короткі періоди спостереження в доступних дослідженнях.
Таблиця 3:
| Техніка | Вибір процедури | Переваги | Недоліки |
| ЕРСО | • Ураження < 10 мм без інвазії м’язової оболонки
• Розглянути при ураженнях розміром 10–20 мм без інвазії у м’язову оболонку. |
• Проста техніка, короткий час процедури
• Низький ризик небажаних явищ |
• Може бути важко виконати резекцію єдиним блоком та резекцію R0, особливо для глибокого краю
• Коагуляційне пошкодження зразка може обмежувати гістологічну оцінку країв |
| ЕПСД | • Ураження ≤20 мм без інвазії м’язової оболонки.
• Розглянути під час уражень > 20 мм без інвазії м’язової оболонки. |
• Вища частота резекції єдиним блоком і R0 порівняно з ЕРСО | • Висока частота ускладнень у дванадцятипалій кишці (перфорація, відстрочена кровотеча)
• Тривалий час процедури |
| ЕРВТ | • Ураження ≤20 мм без інвазії м’язової оболонки
• Розглянути при ураженнях розміром 10–20 мм без інвазії у м’язову оболонку. • Може розглядатися як рятувальна процедура для рецидивуючих/залишкових НЕП після інших технік |
• Можна досягти резекції на всю товщину
• Висока швидкість резекції R0 |
• Висока частота ускладнень (перфорація, відстрочена кровотеча)
• Більш тривалий час процедури, ніж ЕРСО |
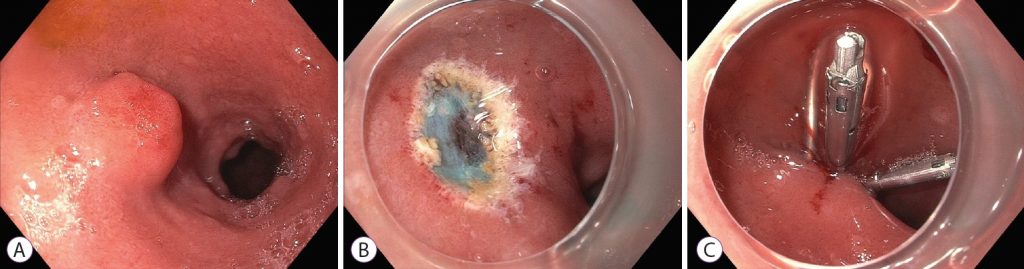
ЕРСО використовує підслизову ін’єкцію, щоб підняти та відокремити ураження від власної м’язової оболонки. Це створює піднесене ураження, яке можна резктувати за допомогою припікання у вигляді петлі (зобр. 1). Однак ЕРСО може призвести до розмозження та коагуляції країв зразка, що може обмежити патологічну оцінку. Крім того, може бути важко досягти резекції єдиним блоком та чіткого глибокого краю навіть при ін’єкційній підтяжці ураження.
ЕРСО з лігуванням смуг (band-ЕРСО або ЕРСО-ligation; ЕРСО-L) був запропонований як альтернативний метод, який дозволяє уникнути цих недоліків. При band-ЕРСО тканина відсмоктується в ковпачок, а під ним розгортається бандаж, утворюючи псевдополіп.
Зображення 1: Ендоскопічна резекція слизової оболонки дванадцятипалої кишки при нейроендокринній пухлині. (A) Нейроендокринна пухлина цибулини дванадцятипалої кишки. (B) Після ендоскопічної резекції слизової оболонки. (C) Закриття дефекту слизової оболонки кліпсами.
При НЕП дванадцятипалої кишки за допомогою ЕРСО досягається резекція єдиним блоком у 88-97% випадків, а резекція R0 – у 63-97% випадків. Так само band-ЕРСО забезпечує резекцію єдиним блоком у 100% випадків, а резекцію R0 – у 61–92% випадків.
Зареєстровані ускладнення аналогічні для обох методів, включаючи інтрапроцедурну кровотечу, відстрочену кровотечу та перфорацію у 10-12%, 0-6% та 0-6% випадків відповідно.
ЕПСД продемонструвала більш високу частоту резекцій єдиним блоком і R0 порівняно з ЕРСО, проте дванадцятипала кишка є технічно складним місцем з більш високим рівнем ускладнень. ЕПСД включає маркування межі ураження перед виконанням кругового розрізу слизової оболонки за допомогою електрохірургічного ножа. Потім ножем проводять підслизову диссекцію якомога ближче до власної м’язової оболонки. Потім дефект можна закрити за допомогою затискачів. Середній час процедури становить близько 15 хвилин.
ЕПСД забезпечує резекцію єдиним блоком у 80-100% випадків, а резекцію R0 у 88-100% випадків для дванадцятипалої кишки. Хоча ці дослідження обмежені невеликим числом, мабуть, висока частота небажаних явищ, при цьому в деяких дослідженнях повідомляється про перфорацію в 23-25% випадків і відстрочену кровотечу в 7% випадків. Середній час процедури складає близько 90 хвилин.
Ендоскопічна повношарова резекція за допомогою кліпс (ЕПР) також була запропонована як метод поліпшення краю зразка при глибокій резекції. Спочатку відзначають межу ураження за допомогою аргоноплазмової коагуляції або електрохірургічного ножа. Потім ураження всмоктується в ковпачок, іноді з використанням тризубцевого анкера для подальшого втягування тканини в ковпачок. На відтягнуту тканину накладається кліпса поза ендоскопом, створюючи псевдополіп. Тканина над кліпсою потім резектується за допомогою електрокаутерної петлі.
Розгортання кліпси поза ендоскопом дозволяє проводити глибоку резекцію із закриттям дефекту, що теоретично мінімізує ризик перфорації. Використання цієї методики в дванадцятипалій кишці обмежене, але в дослідженнях на сьогоднішній день повідомлялося про резекцію R0 у 100% випадків. ЕПР також успішно використовується як рятувальна процедура для рецидивуючих або залишкових НЕП після інших технік.
Повідомлення про небажані явища були різними через обмежену кількість у кожному дослідженні. В одному дослідженні, яке включало 6 НЕП дванадцятипалої кишки, перфорація, мікроперфорація та крововилив відбулися в 1/6, 3/6 та 1/6 випадків відповідно. У двох інших дослідженнях, з такою ж кількістю, побічних ефектів не було зареєстровано. Повідомлений час процедури становив приблизно 50 хвилин.
Нейроендокринні пухлини порожньої та клубової кишки
НЕП середньої частини кишечника класично пов’язані з карциноїдним синдромом і часто пов’язані зі значними симптомами, включаючи шлунково-кишкову кровотечу, біль у животі та діарею. НЕП клубової кишки зустрічаються набагато частіше, ніж НЕП порожньої кишки, і часто пов’язані з мультифокальним захворюванням.
Іноді НЕП клубової кишки виявляються випадково при інтубації ілеоцекального клапана під час скринінгової колоноскопії. Через менш доступне розташування порожньокишкові та клубові НЕП можуть представляти діагностичну проблему.
Відеокапсульна ендоскопія
Роль відеокапсульної ендоскопії (ВКЕ) у діагностиці НЕП-ТК ще чітко не встановлена, і рекомендації щодо її використання залежать від місцевого досвіду. ВКЕ може бути корисною для виявлення мультифокальних НЕП, які можуть виникати у 30-50% пацієнтів і потенційно давати гірший прогноз, ніж при одиночних пухлинах.
Хоча чутливість візуалізації та сцинтиграфії для виявлення первинної пухлини тонкої кишки в останні роки підвищилася, чутливість візуалізації при виявленні багатоцентрових карциноїдних пухлин не оцінювалася. У цьому контексті використання ВКЕ у передопераційній оцінці може допомогти у визначенні ступеня резекції.
Використання ВКЕ також може бути розглянуте у пацієнтів із метастатичними НЕП невідомого походження перед хірургічним дослідженням. Метастатичне розповсюдження (зазвичай печінка) виявляється у 11% пацієнтів з добре диференційованими НЕП, але первинна пухлина залишається невідомою. При хірургічному дослідженні більшість метастатичних НЕП виявляються у тонкій кишці і не виявляються при візуалізації у поперечному перерізі чи сцинтиграфії.
Ідентифікація первинної пухлини важлива, оскільки деякі дані свідчать про те, що резекція первинної пухлини може покращити прогноз навіть за метастатичного захворювання.
У цілому нині діагностична цінність ВКЕ при виявленні пухлин тонкої кишки низька (2–9%). У пацієнтів з НЕП з невідомими первинними пухлинами ВКЕ мала чутливість 75% та специфічність 38% порівняно з діагностичною хірургією.
ВКЕ може бути обмежена хибнопозитивними об’ємними утвореннями, що візуалізуються через скорочення тонкої кишки та зовнішньої компресії. Коли видно справжнє утворення, ендоскопічна картина не є остаточною, а локалізація неточною. Для виявлення підозрілих випинань, що вимагають подальшого дослідження, була запропонована система оцінки ендоскопічних даних, але вона не була підтверджена у великій когорті. Після ідентифікації за допомогою ВКЕ потрібна додаткова інвазивна процедура, така як балонна ентероскопія, для підтвердження результатів та отримання патологічного підтвердження. Сцинтиграфія рецептора соматостатину з використанням 68Ga-DOTATATE покращила виявлення порівняно з попередніми агентами. Проте за його відсутності ВКЕ все ще може мати значення, враховуючи її низький ризик, особливо перед діагностичною операцією.
Балонна ентероскопія
З моменту появи в 2004 році балонна ентероскопія (БЕ) розширила сферу застосування ендоскопічних методів до раніше недоступної тонкої кишки за різними показаннями, включаючи оцінку пухлин тонкої кишки. Діагностична цінність БЕ при пухлинах тонкої кишки за всіма показаннями оцінюється у 4-14%. У пацієнтів із підозрою на НЕП, але негативним вихідним обстеженням діагностична цінність становить до 33%.
В одному дослідженні БЕ мала чутливість 88% для первинної НЕП-ТК порівняно з 60% для КТ, 54% для МРТ та 56% для візуалізації рецепторів соматостатину.
БЕ також можна розглядати для виявлення мультифокальних НЕП до операції. В одному ретроспективному дослідженні пацієнтів, які перенесли резекцію тонкої кишки, БЕ до операції виявила додаткові ураження у 54% пацієнтів порівняно з 18% після ВКЕ. В іншому дослідженні з аналогічним анамнезом ентероскопія тонкої кишки дала лише 10% вихід у порівнянні з ВКЕ з виходом 83%. Однак ВКЕ визначила правильну кількість пухлин лише у 21% цих випадків.
Використання БЕ може бути обмежене довідковими центрами. Враховуючи ці обмеження, мультифокальні пухлини можуть бути найнадійніше виявлені під час операції при дослідженні всього кишечника, як наголошується в рекомендаціях NANETS. Хоча було показано, що ендоскопічні втручання, включаючи біопсію, кліпування і резекцію (включаючи резекцію карциноми), здійсненні через БЕ з мінімальними ускладненнями, ця практика не набула широкого поширення, і хірургічна резекція залишається основою для НЕП порожньої та клубової кишки.
Ендоскопічна резекція НЕП порожньої та клубової кишки не рекомендується, оскільки навіть невеликі (менше сантиметра) ураження тонкої кишки можуть бути пов’язані з інвазією та лімфатичним поширенням, що потребує більшої хірургічної резекції.
Висновки
Ендоскопія є наріжним каменем діагностики та лікування НЕП-ТК. У дванадцятипалій кишці ЕУЗД є важливим методом, який дозволяє оцінити розмір пухлини та глибину інвазії, що необхідно для вибору відповідних кандидатів для ендоскопічної резекції.
Для резекції НЕП у дванадцятипалій кишці було вивчено кілька ендоскопічних методів, у тому числі EMR, band-EMR, EFTR, та ESD. За допомогою EMR для НЕП може бути важко досягти чистого результату; проте в даний час немає єдиної думки про оптимальну техніку. При порожньокишкових та клубових НЕП ендоскопія призначена в основному для діагностики, виявлення мультифокальних пухлин перед хірургічною резекцією або локалізації первинного ураження в метастатичних НЕП, де початкове обстеження не дозволяє виявити пухлину.
Запитання та відповіді
Що таке нейроендокринні пухлини тонкої кишки (НЕП-ТК)?
- НЕП-ТК є гетерогенною групою новоутворень шлунково-кишкової системи, які відрізняються за поведінкою залежно від локалізації, гістології та стадії.
- Вони стають все більш поширеними, і станом на 2000 рік були найпоширенішим злоякісним новоутворенням тонкої кишки.
- Часто НЕП-ТК є безсимптомними і виявляються випадково під час візуалізаційних досліджень або ендоскопії за іншими показаннями.
- Симптоми можуть бути неспецифічними, такими як дискомфорт у животі та діарея, що з’являються за роки до встановлення діагнозу.
Як класифікуються нейроендокринні пухлини тонкої кишки?
- НЕП-ТК класифікуються за стадіями відповідно до системи стадіювання TNM Американського об’єднаного комітету з раку (AJCC).
- Також використовується система оцінок Європейського товариства нейроендокринних пухлин/Всесвітньої організації охорони здоров’я (СНП/ВООЗ) для прогнозування, яка враховує мітотичний індекс та індекс Ki-67.
Які ендоскопічні методи використовуються для діагностики та лікування НЕП-ТК?
- Для діагностики НЕП-ТК можуть використовуватися відеокапсульна ендоскопія та ендоскопічне ультразвукове дослідження (ЕУЗД).
- Для лікування застосовуються передові ендоскопічні методи, такі як ендоскопічна резекція слизової оболонки (ЕРСО), ендоскопічна підслизова дисекція (ЕПСД) та ендоскопічна повношарова резекція (ЕПР).
Яка роль ендоскопічного ультразвукового дослідження (ЕУЗД) у веденні НЕП дванадцятипалої кишки?
- ЕУЗД дозволяє точно оцінити розмір та глибину інвазії НЕП дванадцятипалої кишки, що є критично важливим для вибору методу резекції (ендоскопічної чи хірургічної).
- При ураженнях менше 10 мм з відсутньою інвазією м’язової оболонки, визначеною за допомогою ЕУЗД, ендоскопічна резекція є доцільною.
- Для пухлин розміром понад 20 мм або при наявності ознак високого ризику, виявлених під час ЕУЗД, рекомендується хірургічна резекція.
Які переваги та недоліки різних ендоскопічних технік резекції НЕП дванадцятипалої кишки?
- ЕРСО є простою технікою з низьким ризиком ускладнень, але може ускладнити досягнення резекції R0 та гістологічну оцінку країв.
- ЕПСД забезпечує вищу частоту резекції єдиним блоком та R0, але пов’язана з вищим ризиком ускладнень у дванадцятипалій кишці.
- ЕПР може покращити якість краю зразка при глибокій резекції та використовується як рятувальна процедура, але дані щодо її ефективності та ускладнень обмежені.
Яке значення має відеокапсульна ендоскопія (ВКЕ) при НЕП тонкої кишки?
- ВКЕ може бути корисною для виявлення мультифокальних НЕП, які можуть впливати на прогноз.
- Вона також може використовуватися для передопераційної оцінки та виявлення первинної пухлини у пацієнтів з метастатичними НЕП невідомого походження.
- Однак, діагностична цінність ВКЕ при виявленні пухлин тонкої кишки загалом низька, а для підтвердження результатів потрібні подальші інвазивні процедури.