Автори: P. Sladkevicius, L. Jokubkiene, D. Timmerman, D. Fischerova, C. Van Holsbeke, D. Franchi, L. Savelli, E. Epstein, R. Fruscio, J. Kaijser, A. Czekierdowski, S. Guerriero, M. A. Pascual, A. C. Testa, L. Ameye, L. Valentin
Зміст:
- Данні
♦ Цілі
♦ Методи
- Пацієнти та методи
♦ Популяція вивчення
♦ Збір інформації
♦ Ультразвукове обстеження
♦ Аналіз тривимірних об’ємів і аудіо-відео файлів
♦ Еталонний стандарт
♦ Статистичний аналіз
- Результати
Данні
Цілі
Оцінити, чи покращує морфологія судин, що відображається за допомогою тривимірного (3D) ультразвукового допплерівського дослідження, відмінності доброякісності і злоякісності утворень придатків, які важко класифікувати при використанні в якості тесту другого етапу.
Методи
Це було проспективне міжнародне наглядове багатоцентрове дослідження точності діагностики. Послідовні пацієнти з пухлиною придатків пройшли стандартизоване трансвагінальне двомірне (2D) дослідження в градаціях сірого, а також кольорове або енергетичне доплерівське дослідження і 3D-ультразвукове дослідження в області енергетичного доплера, проведене досвідченим лікарем, а пацієнти зі «складною» пухлиною були включені в поточний аналіз.
Складна пухлина була визначена як пухлина, в якій модель 1 логістичної регресії Міжнародного аналізу пухлин яєчників (IOTA) (LR-1) дала неоднозначний результат (ризик злоякісності від 8,3% до 25,5%), або як пухлина, при якій ультразвукове дослідження було не однозначним в класифікації як доброякісний або злоякісний при використанні суб’єктивної оцінки.
Для кожної складної пухлини один дослідник створив обертальне на 360° тривимірне зображення за допомогою енергетичного доплера судинної мережі в усій пухлині, а інший – судинної мережі в сферичному об’ємі 5 см³, обраному з найбільш васкуляризованної частини пухлини.
Два інших дослідника, які не знають історії хвороби пацієнта, результатів 2D-ультразвукового дослідження та гістологічного діагнозу, незалежно один від одного описали судинну мережу, використовуючи заздалегідь певні характеристики судини. Використовувалася їх узгоджена класифікація.
Пацієнти та методи
Популяція вивчення
В нашу досліджувану популяцію увійшли пацієнти в дослідженні IOTA-3, у яких була важка пухлина придатків (визначення нижче).
Дослідження IOTA-3 – це проспективне міжнародне наглядове багатоцентрове перехресне діагностичне дослідження точності. У період з жовтня 2009 р по травень 2012 р пацієнти були набрані в IOTA-3 в 18 центрах в шести країнах (Швеція, Бельгія, Італія, Польща, Іспанія та Чехія). Ці центри були або онкологічними центрами (тобто спеціалізованими центрами з певним гінекологічним онкологічним відділенням), або іншими лікарнями або відділеннями, що спеціалізуються на гінекологічному УЗД.
Пацієнти, спрямовані в один з центрів для ультразвукового дослідження, у яких було виявлено утворення придатків, підходили для включення в IOTA-3. Послідовні пацієнти з принаймні однією пухлиною придатка, визнанною не функціональню кістою, дослідженої за допомогою трансвагінального ультразвукового дослідження досвідченим ультразвуковим експертом, були включені в IOTA-3 за умови, що вони дали письмову і / або усну інформовану згоду перед ультразвуковим скануванням.
Якщо було виявлено більше одного утворення, для статистичного аналізу використовувалося утворення з найскладнішою ультразвукової морфологією.
Критеріями виключення пацієнтів з IOTA-3 були вагітність на момент ультразвукового дослідження, хірургічне видалення новоутворення більш ніж через 120 днів після ультразвукового дослідження, невідповідності даних, які зберігалися після остаточної ручної перевірки даних, і випадки з неповною гістологією.
Збір інформації
Спеціальна безпечна електронна система збору даних була розроблена для дослідження IOTA-3 (IOTA-3 Study Screen; astraia Software, Мюнхен, Німеччина).
Пацієнти автоматично отримують унікальний ідентифікатор. Безпека даних забезпечувалася за рахунок шифрування всіх даних, що передаються. Цілісність і повнота даних забезпечувалися перевірками на стороні клієнта в системі.
Програмне забезпечення astraia автоматично розрахувало ризик злоякісного новоутворення з використанням моделі IOTA LR-16, і результат був відображений на екрані комп’ютера.
Ультразвукове обстеження
Всі пацієнти, включені в дослідження IOTA-3, пройшли стандартизоване трансвагінальне ультразвукове обстеження гінекологом або радіологом, які мають великий досвід в гінекологічному ультразвуковому дослідженні, з використанням ультразвукових систем високого класу.
Для отримання інформації про більш ніж 40 ультразвукових змінних, щоб охарактеризувати кожне утворення придатків, використовували відтінки сірого і кольоровий або потужний доплерівський ультразвук.
Після завершення ультразвукового дослідження лікар класифікував кожну пухлину як доброякісну або злоякісну на основі його / її суб’єктивної оцінки результатів ультразвукового дослідження в відтінках сірого і кольорового або енергетичного доплера.
Крім того, дослідник заявив рівень своєї впевненості, класифікуючи кожну пухлину як:
- безумовно доброякісну
- можливо доброякісну
- невизначену
- можливо злоякісну
- визначено злоякісну.
Це означає, що навіть коли дослідник не був упевнений, доброякісна пухлина або злоякісна, він / вона був зобов’язаний класифікувати її як найбільш ймовірно доброякісну або найбільш ймовірно злоякісну.
Ультразвукова інформація була попередньо введена в електронну систему збору даних (див. Вище), була заблокована під час обстеження і не могла бути згодом змінена. Рішення про операцію з приводу пухлини придатків приймав лікуючий лікар на підставі клінічної інформації, такої як симптоми, вік, операційний ризик і супутнє захворювання, а також данні на ультразвуковому звіті, який був складений з використанням результатів суб’єктивної оцінки.
На додаток до виконання двовимірного (2D) ультразвукового дослідження, як описано вище, фахівці з ультразвукового обстеження в центрах з доступом до ультразвукової системі Voluson 730 Expert або GE E8 (GE Healthcare, Zipf, Австрія) з конвексним датчиком частотою 5-9 МГц або внутрішньопорожнинним датчиком з частотою 6-12 МГц, була проведена тривимірна ультразвукова доплерографія всіх новоутворень придатків.
Пацієнтів просили лежати нерухомо під час обстеження і, при необхідності, затримувати дихання. Об’єми складних пухлин, тобто пухлин, в яких фахівець з ультразвукового дослідження не був упевнений, чи є пухлина доброякісною або злоякісною на підставі суб’єктивної оцінки, або ті, в яких модель IOTA LR-1 дала неоднозначний ризик злоякісності (від 8,3% до 25,5%) 8, були відправлені на компакт-дисках у університетську лікарню Сконе в Мальме для аналізу. Використовувалася та ж методологія аналізу тривимірних об’ємів, яка описана раніше, і коротко викладена нижче.
Аналіз тривимірних об’ємів і аудіо-відео файлів
Для кожної пухлини другим автором були підготовлені обертальні на 360° тривимірні енергетичні доплерівські зображення (файли AVI) судин у всій пухлині, а також в сферичному об’ємі 5 см³, обраному з найбільш васкуляризованної частини пухлини (LJ) за допомогою програми візуалізації Virtual Organ Computer-Aided AnaLysis (4D-View, версія 7.0, GE Healthcare) на персональному комп’ютері.
Перед створенням обертового зображення сітки судин була відрегульована прозорість кольору, щоб оптимізувати обриси судин.
Потім всі файли AVI були проаналізовані незалежно двома членами дослідницької групи Мальме (L.V., P.S.), які не знали історії хвороби, результатів 2D ультразвукового дослідження або гістологічного діагнозу.
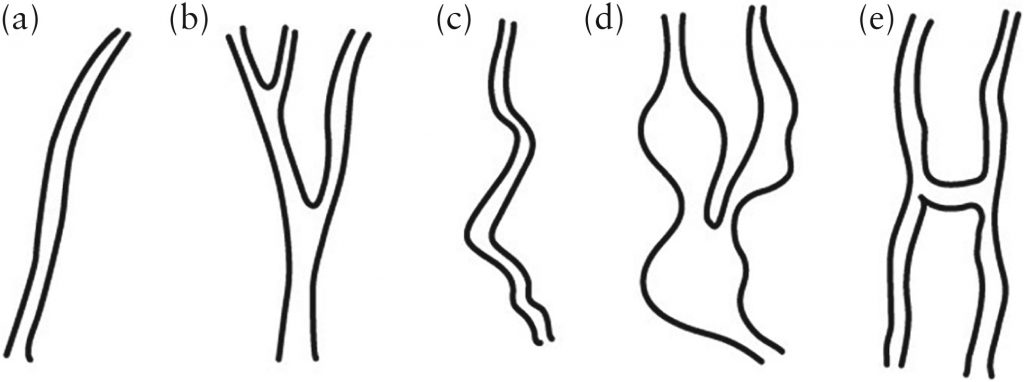
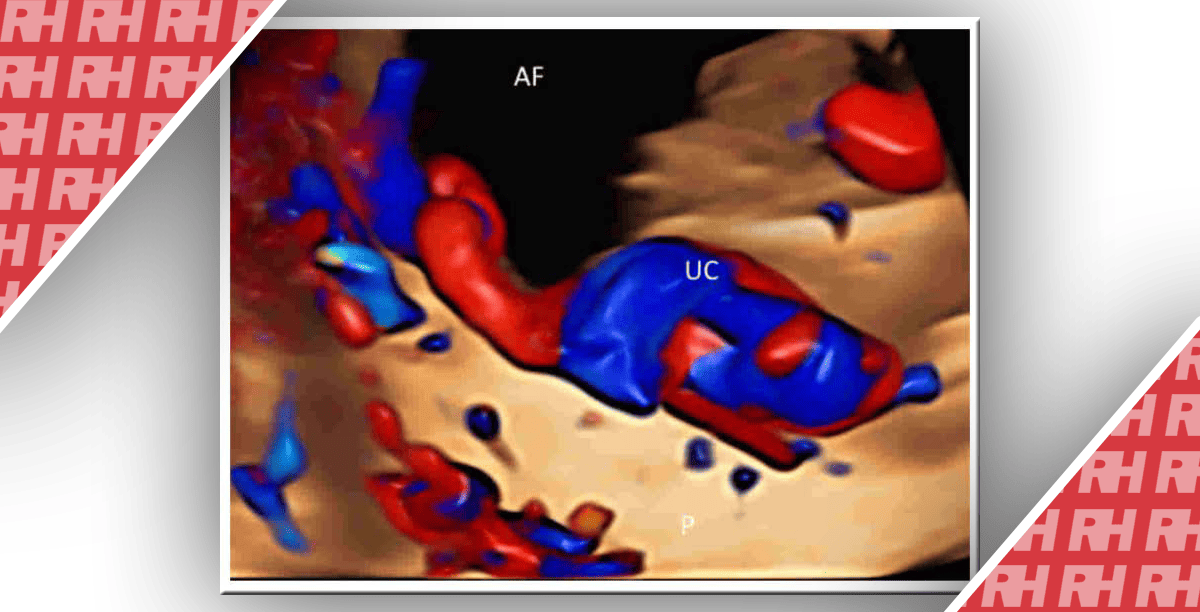
Судинна мережа у всьому об’ємі пухлини, а також в зразку об’ємом 5 см³ була охарактеризована з використанням тієї ж класифікації, що і описана раніше (зображення 1):
- розгалуження, тобто поділ судини на дві або більше гілок;
- зміни діаметра, тобто зміни ширини судини від вузького до широкого і від широкого до вузького;
- «Бризки», тобто ділянки кольору, що контрастують з чітко окремими судинами;
- звивистість;
- ділянки з щільно упакованими судинами;
- «Мости», тобто прямі з’єднання між двома сусідніми судами.
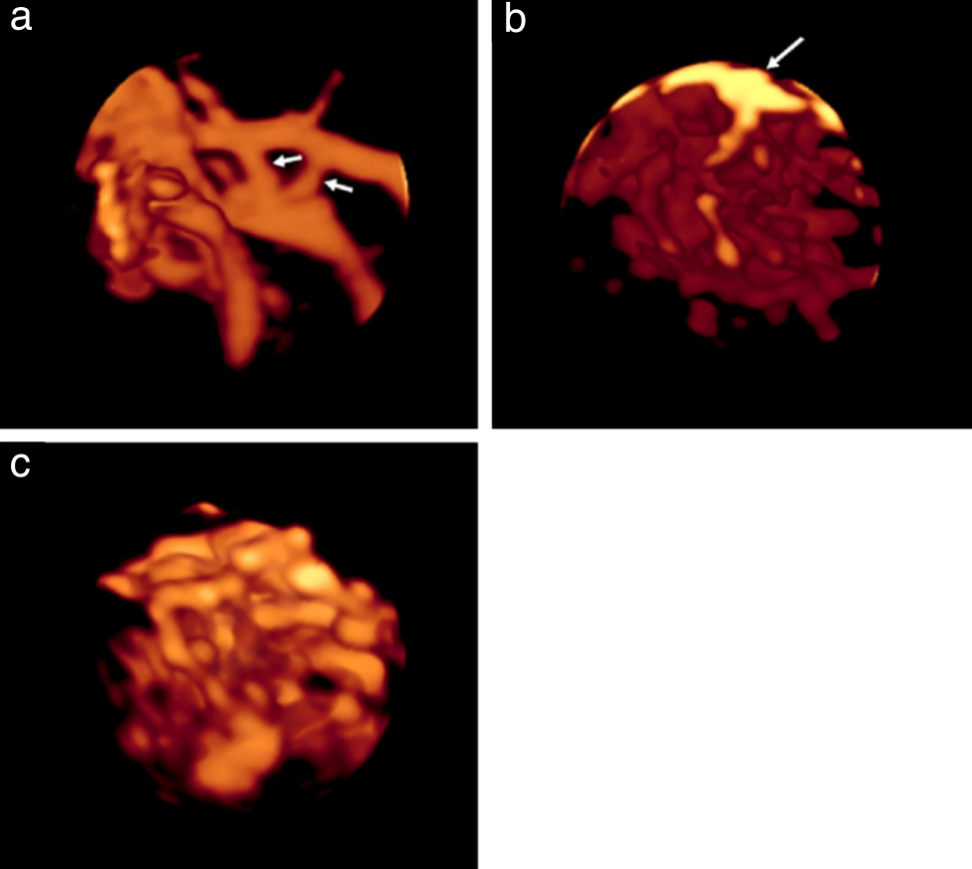
Наявність перемичок оцінювалася тільки в зразках об’ємом 5 см³, а наявність щільно упакованих судин – тільки в повному об’ємі пухлини. У разі розбіжностей між двома спостерігачами консенсус досягався шляхом обговорення, і узгоджена класифікація використовувалася для статистичного аналізу; це було зроблено, щоб знизити ризик упередженості, якщо покладатися на одного-єдиного спостерігача. Ультразвукові зображення судинних особливостей показані на зображеннях 2 і 3.
Зображення 1: Схематичні діаграми, що ілюструють судинні особливості, які оцінюються в придаткових масах в нашому дослідженні: (а) пряма судина без розгалуження; (b) розгалужена; (с) звивиста судина; (d) судина зі зміною діаметра; і (e) мости (короткі прямі з’єднання між двома сусідніми судинами).
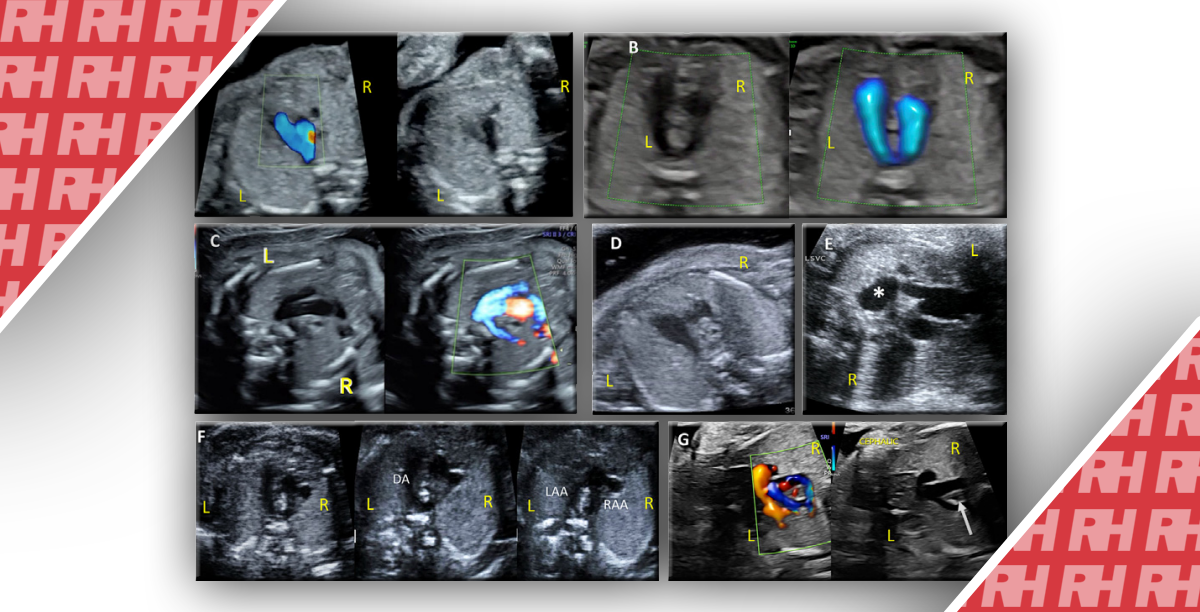
Зображення 2: Тривимірні ультразвукові зображення за допомогою енергетичної доплерографії судинного русла у всьому об’ємі пухлин яєчників, що показують: (а) розосереджені (на відміну від щільно упакованих), прямі (на відміну від звивистих), розгалужені судини в доброякісній муцинозній цистаденомі; (b) розосереджені, розгалужені, звиті судини (товста стрілка) зі змінами діаметра (тонка стрілка) в муцинозній прикордонній пухлині; (с) щільно упаковані, розгалужені, звиті судини зі зміною діаметра і кольоровими плямами (стрілкою показані плями) у функціональній кісті; і (d) щільно упаковані, розгалужені, звивисті судини зі змінами діаметра при світлоклітинному ракові яєчників.
Зображення 3: Тривимірні ультразвукові зображення судинних гілок в зразках пухлин яєчників об’ємом 5 см³, що показують: (а) мости (стрілки), тобто прямі з’єднання між двома сусідніми судинами в яєчниковому зобі; (б) розгалужені звиті судини зі зміною діаметра і колірних плям (стрілка) при доброякісній фібромі яєчника; (с) розгалужені звивисті судини зі зміною діаметра при ендометріоїдній карциномі яєчників.
Еталонний стандарт
Еталонним стандартом була гістологічна класифікація посічених утворень на злоякісні або доброякісні. Гістологічне дослідження проводилося в місцевих центрах. Огляд центральної патології не проводився, тому що в попередньому дослідженні IOTA не спостерігалося клінічно значущих відмінностей між звітами про місцеві та центральні патології.
Злоякісні пухлини були класифіковані відповідно до критеріїв, рекомендованих Міжнародною федерацією гінекології та акушерства. Прикордонні пухлини яєчників були класифіковані як злоякісні. Патологоанатоми не бачили результатів УЗД.
Статистичний аналіз
Ми прагнули зібрати інформацію про 300 складних новоутвореннь, з яких, як ми очікували, мінімум 30% (n = 90) будуть злоякісними. 90 злоякісних новоутворень дадуть нам розумні 95% довірчі інтервали навколо точкових оцінок чутливості.
Оскільки близько 7% всіх утворень придатків важко класифікувати як доброякісні або злоякісні за допомогою суб’єктивної оцінки, і оскільки модель IOTA LR-1 може дати неоднозначний результат тесту в 10% всіх утворень придатків, ми підрахували, що нам необхідно досліджувати близько 2000 жінок з пухлиною придатків .
Дослідження опубліковане з використанням керівних принципів «Стандарти звітності з досліджень діагностичної точності» (STARD).
Результати
Всього для включення в IOTA-3 була включена 2541 жінка з пухлиною придатків, 138 з яких були виключені. Причинами виключення були> 120 днів між ультразвуковим дослідженням і операцією (n = 66), вагітність (n = 31), помилки даних, які не могли бути усунені шляхом звернення до провідних дослідників (n = 28), і неповна остаточна гістологія (n = 13)).
Остаточний набір даних IOTA-3 включав 2403 пацієнта, з яких 376 (16%) мали важку пухлину; невизначений результат щодо злоякісності був отриманий для 168 (7%) пухлин при суб’єктивній оцінці, для 259 (11%) пухлин з використанням моделі LR-1 і для 51 (2%) пухлин з використанням обох методів.
Серозні і муцинозні цистаденоми / цистаденофіброми, фіброми і прикордонні пухлини були значно більш поширені серед складних пухлин, ніж серед інших, в той час як ендометріоми, доброякісні тератоми (дермоїдна кісти), первинний рак яєчників і метастази в яєчники з іншої первинної пухлини були значно рідше.
Розподіл гістологічних діагнозів був подібним в пухлинах, в яких ультразвуковий експерт не був упевнений в діагнозі при суб’єктивній оцінці, і в тих, в яких LR-1 дав неоднозначний результат, за винятком того, що в останніх частіше зустрічалися доброякісні тератоми і ендометріоми.
Ультразвукові характеристики пухлин, які досліднику було важко класифікувати при суб’єктивній оцінці, були аналогічні тим, в яких LR-1 давав неоднозначний результат, за винятком того, що асцит був більш поширений, а одногокулярні кісти були менш поширені в пухлинах, які досліджувач вважав важкими.
Об’єми тривимірного УЗД були доступні для 138 з 376 складних пухлин. Шість центрів не надали об’єми для будь-якого зі своїх складних утворень (0/55), чотири центри надали об’єми для більш 80% (73/87), чотири центри для від 40% до 57% (47/96), три центри від 11% до 18% (16/107) і один центр для 6% (2/31).
У трьох центрах причиною надання томів ні для однієї або тільки невеликої частини складних пухлин (6/78) було те, що об’єми, що зберігаються в ультразвукової системі, були видалені і не було резервних, а в одному центрі – необхідна ультразвукова система GE не завжди була доступна для дослідження.
Один центр (з 33 складними пухлинами) не мав доступу до ультразвукової системи Voluson 730 Expert або GE E8 і тому не міг надати будь-які об’єми.
Сім центрів повідомили, що забудькуватість або тимчасові технічні проблеми є поясненням того, що не пропонують об’єми для всіх їх важких утворень, а шість центрів не дали ніяких пояснень.
| Діагноз | Кількість (n/%) |
| Доброякісна пухлина | 100 (72) |
| Ендометріома | 7 (5) |
| Тератома | 5 (4) |
| Проста кіста чи парасальпінгіальна кіста | 3 (2) |
| Функціональна кіста | 3 (2) |
| Гідросальпінкс чи сальпінгіт | 3 (2) |
| Псевдокіста очеревини | 2 (1) |
| Абсцес | 2 (1) |
| Фіброма | 18 (13) |
| Серозна цистаденома / цистаденофіброма | 30 (22) |
| Муцинозна цистаденома / цистаденофіброма | 23 (17) |
| Рідкісна доброякісна пухлина | 4 (3) |
| Прикордонна пухлина | 15 (11) |
| Стадія 1 | 14 (10) |
| Стадія 2 | 1 (1) |
| Стадія 3 чи 4 | 0 (0) |
| Первинна інвазивна пухлина | 22 (16) |
| Стадія 1 | 7 (5) |
| Стадія 2 | 1 (1) |
| Стадія 3 | 8 (6) |
| Стадія 4 | 0 (0) |
| Рідкісна злоякісна пухлина | 6 (4) |
| Метастаз в яєчник з іншої первинної пухлини | 1 (1) |
Наші результати показують, що якщо модель IOTA LR-1 дає неоднозначну оцінку ризику (від 8,3% до 25,5%), то суб’єктивна оцінка досвідченим фахівцем з ультразвукового обстеження перевершує використання морфології судин, відображеної за допомогою тривимірного ультразвукового доплера в якості другого етапу.
Однак, якщо новоутворення не може бути впевнено класифіковано як доброякісне або злоякісне досвідченим фахівцем з ультразвукового обстеження з використанням суб’єктивної оцінки, то оцінка морфології судин за допомогою тривимірної ультразвукової доплерографії може бути корисною.
Для розрізнення можна використовувати як щільно упаковані судини у всьому об’ємі пухлини, так і звиті судини при біопсії пухлини об’ємом 5 см³.
Ми рекомендуємо використовувати щільно упаковані судини, тому що надійність між спостерігачами була краще для цієї змінної, ніж для звивистих судин при біопсії пухлини. З іншого боку, аналіз всього об’єму пухлини займає більше часу, ніж біопсія пухлини. З нашого досвіду, висококваліфікованому фахівцеві з ультразвукового обстеження потрібно не менше 2,5 хвилин для створення обертового тривимірного зображення судинної мережі всієї пухлини, в той час як для створення зображення для біопсії об’ємом 5 см³ потрібно не менше 1 хвилини.
При оцінці морфології судин важливо знати про підводні камені ультразвукової доплерографії і переконатися, що настройки доплеру вірні. Якщо пухлина знаходиться далеко від ультразвукового датчика, можливо, буде неможливо виявити доплерівські сигнали від всієї пухлини або її частин. Це обмежує клінічну застосовність морфології судин для класифікації пухлин як доброякісних або злоякісних. Ще одним обмежуючим фактором є суб’єктивність методу. Оцінка морфології судин, включаючи «судини з щільною упаковкою», заснована на розпізнаванні образів, і тому її важко стандартизувати або визначити.