🤖 Краткий пересказ от ИИ
Целью исследования было оценить, улучшает ли 3D ультразвуковое допплеровское исследование морфологии сосудов дифференциацию доброкачественных и злокачественных образований придатков, которые трудно классифицировать стандартными методами. В исследовании изучались “сложные опухоли”, определенные по неоднозначным результатам модели IOTA LR-1 или субъективной оценки.
Результаты показали, что субъективная оценка опытного специалиста превосходит 3D УЗИ допплерографию как метод второго этапа при неоднозначных результатах IOTA LR-1. Однако, при неуверенной субъективной оценке, анализ морфологии сосудов с помощью 3D УЗИ допплерографии может быть полезным, особенно признаков “плотно упакованных сосудов” или “извитых сосудов” для улучшения диагностики. Узнать больше о возможностях современного оборудования можно на странице, посвященной УЗИ аппаратам.
✅ Ключевые тезисы из статьи:
- Диагностика: Для диагностики сложных образований придатков применялись 2D и 3D ультразвуковое исследование с допплерографией, а также модель IOTA LR-1 и субъективная оценка.
- Лечение: При неоднозначных случаях субъективная оценка считается более эффективной, однако при ее неуверенности рекомендуется 3D УЗИ допплерография, особенно для выявления признака “плотно упакованных сосудов”.
- Преимущества: Трехмерная ультразвуковая допплерография может быть полезным инструментом для улучшения дифференциации доброкачественных и злокачественных образований в сложных случаях, когда стандартные методы дают неоднозначный результат.
- Ограничения: Метод имеет ограничения, включая его субъективность, трудности стандартизации, зависимость от настроек допплера и потенциальную невозможность обнаружения сигналов от отдаленных частей опухоли.
Последнее обновление: 21 июля 2025 р.
Экспертная проверка: Материал проверен и отредактирован экспертами RH.ua
Примечание об ИИ: Этот блок создан с помощью генеративного ИИ для быстрого ознакомления с основными идеями статьи. Для полного понимания темы рекомендуем прочесть полный текст.
⚠️ Не заменяет медицинскую консультацию
Авторы: P. Sladkevicius, L. Jokubkiene, D. Timmerman, D. Fischerova, C. Van Holsbeke, D. Franchi, L. Savelli, E. Epstein, R. Fruscio, J. Kaijser, A. Czekierdowski, S. Guerriero, M. A. Pascual, A. C. Testa, L. Ameye, L. Valentin
Содержание:
- Данные
♦ Цели
♦ Методы
- Пациенты и методы
♦ Популяция изучения
♦ Сбор информации
♦ Ультразвуковое обследование
♦ Анализ трехмерных объемов и аудио-видео файлов
♦ Эталонный стандарт
♦ Статистический анализ
- Результаты
Данные
Цели
Оценить, улучшает ли морфология сосудов, отображаемая с помощью трехмерного (3D) ультразвукового допплеровского исследования, различия доброкачественности и злокачественности образований придатков, которые трудно классифицировать при использовании в качестве теста второго этапа.
Методы
Это было проспективное международное наблюдательное многоцентровое исследование точности диагностики. Последовательные пациенты с опухолью придатков прошли стандартизированное трансвагинальное двухмерное (2D) исследование в градациях серого, а также цветное или энергетическое допплеровское исследование и 3D-ультразвуковое исследование в области энергетического допплера, проводимое опытным врачом, а пациенты со «сложной» опухолью были включены в текущий анализ.
Сложная опухоль была определена как опухоль, в которой модель 1 логистической регрессии Международного анализа опухолей яичников (IOTA) (LR-1) дала неоднозначный результат (риск злокачественности от 8,3% до 25,5%), или как опухоль, при которой ультразвуковое исследование было не однозначным в классификации как доброкачественный или злокачественный при использовании субъективной оценки.
Для каждой сложной опухоли один исследователь создал вращающееся на 360° трехмерное изображение с помощью энергетического допплера сосудистой сети во всей опухоли, а другой – сосудистой сети в сферическом объеме 5 см³, выбранном из наиболее васкуляризированной части опухоли.
Два других исследователя, не знающие истории болезни пациента, результатов 2D-ультразвукового исследования и гистологического диагноза, независимо друг от друга описали сосудистую сеть, используя заранее определенные характеристики сосуда. Использовалась их согласованная классификация.
Пациенты и методы
Популяция изучения
В нашу исследуемую популяцию вошли пациенты в исследовании IOTA-3, у которых была тяжелая опухоль придатков (определение ниже).
Исследование IOTA-3 – это проспективное международное наблюдательное многоцентровое перекрестное диагностическое исследование точности. В период с октября 2009 г. по май 2012 г. пациенты были набраны в IOTA-3 в 18 центрах в шести странах (Швеция, Бельгия, Италия, Польша, Испания и Чехия). Эти центры были либо онкологическими центрами (т.е. специализированными центрами с определенным гинекологическим онкологическим отделением), либо другими больницами или отделениями, специализирующимися на гинекологическом УЗИ.
Пациенты, направленные в один из участвующих центров для ультразвукового исследования, у которых было обнаружено образование придатков, подходили для включения в IOTA-3. Последовательные пациенты с по крайней мере одной опухолью придатка, признанной не функциональной кистой, исследованной с помощью трансвагинального ультразвукового исследования опытным ультразвуковым экспертом, были включены в IOTA-3 при условии, что они дали письменное и / или устное информированное согласие перед ультразвуковым сканированием.
Если было обнаружено более одного образования, для статистического анализа использовалось образование с самой сложной ультразвуковой морфологией.
Критериями исключения пациентов из IOTA-3 были беременность на момент ультразвукового исследования, хирургическое удаление новообразования более чем через 120 дней после ультразвукового исследования, несоответствия данных, которые сохранялись после окончательной ручной проверки данных, и случаи с неполной гистологией.
Сбор информации
Специальная безопасная электронная система сбора данных была разработана для исследования IOTA-3 (IOTA-3 Study Screen; astraia Software, Мюнхен, Германия).
Пациенты автоматически получают уникальный идентификатор. Безопасность данных обеспечивалась за счет шифрования всех передаваемых данных. Целостность и полнота данных обеспечивались проверками на стороне клиента в системе.
Программное обеспечение astraia автоматически рассчитало риск злокачественного новообразования с использованием модели IOTA LR-16, и результат был отображен на экране компьютера.
Ультразвуковое обследование
Все пациенты, включенные в исследование IOTA-3, прошли стандартизированное трансвагинальное ультразвуковое обследование гинекологом или радиологом, имеющим большой опыт в гинекологическом ультразвуковом исследовании, с использованием ультразвуковых систем высокого класса.
Для получения информации о более чем 40 ультразвуковых переменных, чтобы охарактеризовать каждое образование придатков, использовали оттенки серого и цветной или мощный допплеровский ультразвук.
После завершения ультразвукового исследования врач классифицировал каждую опухоль как доброкачественную или злокачественную на основе его / ее субъективной оценки результатов ультразвукового исследования в оттенках серого и цветного или энергетического допплера.
Кроме того, исследователь заявил уровень своей уверенности, классифицируя каждую опухоль как:
- безусловно доброкачественную
- возможно доброкачественную
- неопределенную
- возможно злокачественную
- определенно злокачественную.
Это означает, что даже когда исследователь не был уверен, доброкачественная опухоль или злокачественная, он / она был обязан классифицировать ее как наиболее вероятно доброкачественную или наиболее вероятно злокачественную.
Ультразвуковая информация была предварительно введена в электронную систему сбора данных (см. Выше), была заблокирована во время обследования и не могла быть впоследствии изменена. Решение об операции по поводу опухоли придатков принимал лечащий врач на основании клинической информации, такой как симптомы, возраст, операционный риск и сопутствующее заболевание, а также на ультразвуковом отчете, который был составлен с использованием результатов субъективной оценки.
В дополнение к выполнению двумерного (2D) ультразвукового исследования, как описано выше, специалисты по ультразвуковому обследованию в центрах с доступом к ультразвуковой системе Voluson 730 Expert или GE E8 (GE Healthcare, Zipf, Австрия) с конвексным датчиком частотой 5–9 МГц или внутриполостным датчиком с частотой 6–12 МГц, была проведена трехмерная ультразвуковая допплерография всех новообразований придатков.
Пациентов просили лежать неподвижно во время обследования и, при необходимости, задерживать дыхание. Объемы сложных опухолей, то есть опухолей, в которых специалист по ультразвуковому исследованию не был уверен, является ли опухоль доброкачественной или злокачественной на основании субъективной оценки, или те, в которых модель IOTA LR-1 дала неоднозначный риск злокачественности (от 8,3% до 25,5%) 8 , были отправлены на компакт-дисках в университетскую больницу Сконе в Мальмё для анализа. Использовалась та же методология анализа трехмерных объемов, которая описана ранее, и кратко изложена ниже.
Анализ трехмерных объемов и аудио-видео файлов
Для каждой опухоли вторым автором были подготовлены вращающиеся на 360° трехмерные энергетические доплеровские изображения (файлы AVI) сосудов во всей опухоли, а также в сферическом объеме 5 см³, выбранном из наиболее васкуляризированной части опухоли (LJ) с помощью программы визуализации Virtual Organ Computer-Aided AnaLysis (4D-View, версия 7.0, GE Healthcare) на персональном компьютере.
Перед созданием вращающегося изображения сетки сосудов была отрегулирована прозрачность цвета, чтобы оптимизировать очертания сосудов.
Затем все файлы AVI были проанализированы независимо двумя членами исследовательской группы Мальмё (L.V., P.S.), которые не знали истории болезни, результатов 2D ультразвукового исследования или гистологического диагноза.
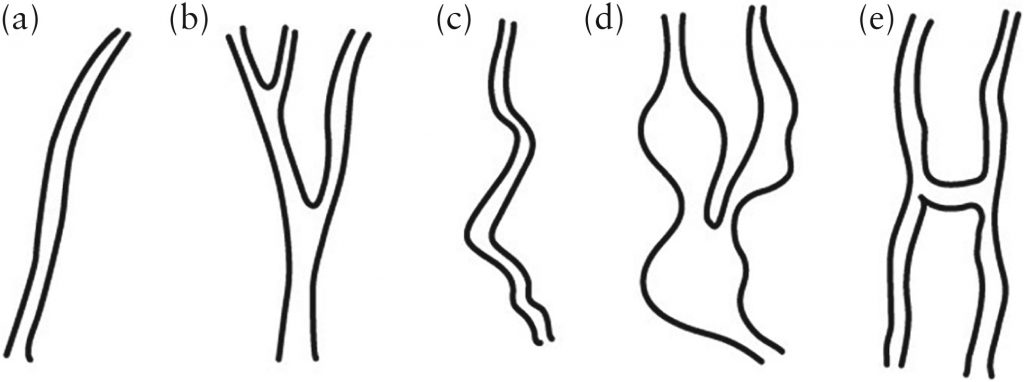
Сосудистая сеть во всем объеме опухоли, а также в образце объемом 5 см³ была охарактеризована с использованием той же классификации, что и описанная ранее (Рисунок 1):
- ветвление, то есть разделение сосуда на две или более ветвей;
- изменения диаметра, т.е. изменения ширины сосуда от узкого к широкому и от широкого к узкому;
- «Брызги», т.е. участки цвета, контрастирующие с четко отдельными сосудами;
- извилистость;
- участки с плотно упакованными сосудами;
- «мосты», то есть прямые соединения между двумя соседними судами.
Наличие перемычек оценивалось только в образцах объемом 5 см³, а наличие плотно упакованных сосудов – только во всем объеме опухоли. В случае разногласий между двумя наблюдателями консенсус достигался путем обсуждения, и согласованная классификация использовалась для статистического анализа; это было сделано, чтобы снизить риск предвзятости, если полагаться на одного-единственного наблюдателя. Ультразвуковые изображения сосудистых особенностей показаны на рисунках 2 и 3.
Рисунок 1: Схематические диаграммы, иллюстрирующие сосудистые особенности, оцениваемые в придаточных массах в нашем исследовании: (а) прямой сосуд без ветвления; (b) разветветвленный; (c) извилистый сосуд; (d) сосуд с изменением диаметра; и (e) мосты (короткие прямые соединения между двумя соседними судами).
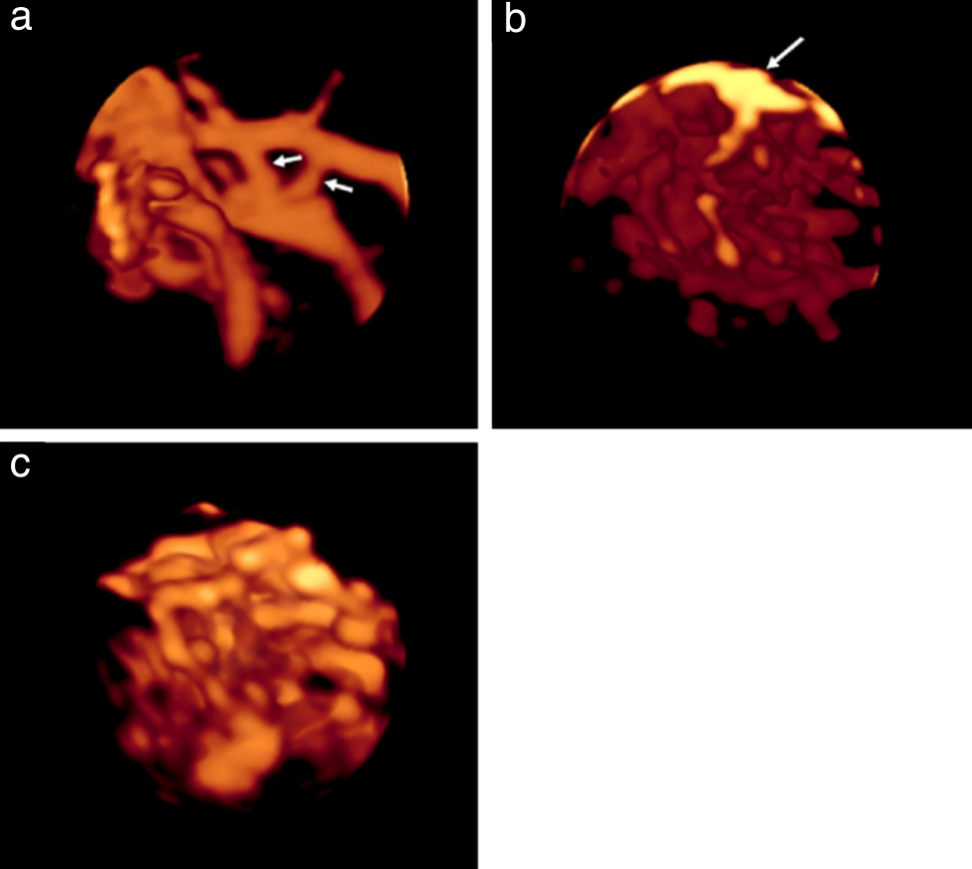
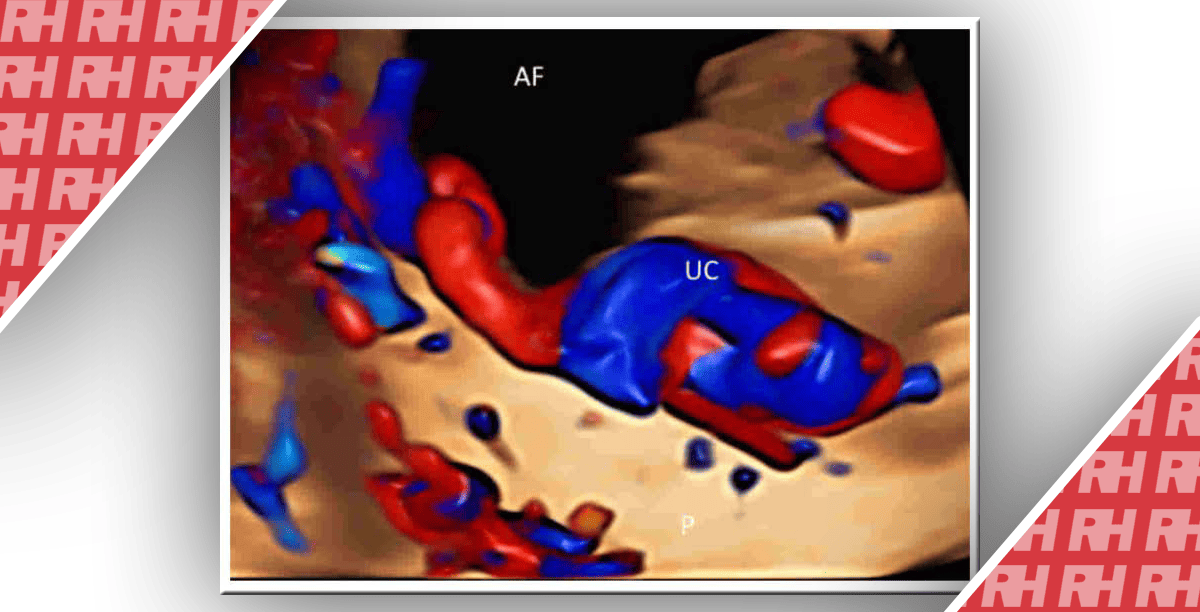
Рисунок 2: Трехмерные ультразвуковые изображения с помощью энергетической допплерографии сосудистого русла во всем объеме опухолей яичников, показывающие: (а) рассредоточенные (в отличие от плотно упакованных), прямые (в отличие от извилистых), ветвящиеся сосуды в доброкачественной муцинозной цистаденоме; (b) рассредоточенные, ветвящиеся, извитые сосуды (толстая стрелка) с изменениями диаметра (тонкая стрелка) в муцинозной пограничной опухоли; (с) плотно упакованные, ветвящиеся, извитые сосуды с изменением диаметра и цветными пятнами (стрелкой показаны пятна) в функциональной кисте; и (d) плотно упакованные, разветвленные, извилистые сосуды с изменениями диаметра при светлоклеточном раке яичников.
Рисунок 3: Трехмерные ультразвуковые изображения сосудистых ветвей в образцах опухолей яичников объемом 5 см³, показывающие: (а) мосты (стрелки), то есть прямые соединения между двумя соседними сосудами в яичниковом зобе; (b) ветвящиеся извитые сосуды с изменением диаметра и цветовых пятен (стрелка) при доброкачественной фиброме яичника; (c) ветвящиеся извилистые сосуды с изменением диаметра при эндометриоидной карциноме яичников.
Эталонный стандарт
Эталонным стандартом была гистологическая классификация иссеченных образований на злокачественные или доброкачественные. Гистологическое исследование проводилось в местных центрах. Обзор центральной патологии не проводился, потому что в предыдущем исследовании IOTA не наблюдалось клинически значимых различий между отчетами о местной и центральной патологиями.
Злокачественные опухоли были классифицированы в соответствии с критериями, рекомендованными Международной федерацией гинекологии и акушерства. Пограничные опухоли яичников были классифицированы как злокачественные. Патологоанатомы не видели результатов УЗИ.
Статический анализ
Мы стремились собрать информацию о 300 сложных новообразованиях, из которых, как мы ожидали, минимум 30% (n = 90) будут злокачественными. 90 злокачественных новообразований дадут нам разумные 95% доверительные интервалы вокруг точечных оценок чувствительности.
Поскольку около 7% всех образований придатков трудно классифицировать как доброкачественные или злокачественные с помощью субъективной оценки, и поскольку модель IOTA LR-1 может дать неоднозначный результат теста в 10% всех образований придатков, мы подсчитали, что нам необходимо исследовать около 2000 женщин с опухолью придатков.
Исследование опубликовано с использованием руководящих принципов «Стандарты отчетности по исследованиям диагностической точности» (STARD).
Результаты
Всего для включения в IOTA-3 была включена 2541 женщина с опухолью придатков, 138 из которых были исключены. Причинами исключения были> 120 дней между ультразвуковым исследованием и операцией (n = 66), беременность (n = 31), ошибки данных, которые не могли быть устранены путем обращения к ведущим исследователям (n = 28), и неполная окончательная гистология (n = 13) ).
Окончательный набор данных IOTA-3 включал 2403 пациента, из которых 376 (16%) имели тяжелую опухоль; неопределенный результат в отношении злокачественности был получен для 168 (7%) опухолей при субъективной оценке, для 259 (11%) опухолей с использованием модели LR-1 и для 51 (2%) опухолей с использованием обоих методов.
Серозные и муцинозные цистаденомы / цистаденофибромы, фибромы и пограничные опухоли были значительно более распространены среди сложных опухолей, чем среди других, в то время как эндометриомы, доброкачественные тератомы (дермоидные кисты), первичный рак яичников и метастазы в яичники из другой первичной опухоли были значительно реже.
Распределение гистологических диагнозов было сходным в опухолях, в которых ультразвуковой эксперт не был уверен в диагнозе при субъективной оценке, и в тех, в которых LR-1 дал неоднозначный результат, за исключением того, что в последних чаще встречались доброкачественные тератомы и эндометриомы.
Ультразвуковые характеристики опухолей, которые исследователю было трудно классифицировать при субъективной оценке, были аналогичны тем, в которых LR-1 давал неоднозначный результат, за исключением того, что асцит был более распространен, а одногокулярные кисты были менее распространены в опухолях, которые исследовал счел трудными.
Объемы трехмерного УЗИ были доступны для 138 из 376 сложных опухолей. Шесть центров не предоставили объемы для любого из своих сложных образований (0/55), четыре центра предоставили объемы для более 80% (73/87), четыре центра для от 40% до 57% (47/96), три центра для от 11% до 18% (16/107) и один центр для 6% (2/31).
В трех центрах причиной предоставления томов ни для одной или только небольшой части сложных опухолей (6/78) было то, что объемы, хранящиеся в ультразвуковой системе, были удалены и не было резервных, а в одном центре – требуемая ультразвуковая система GE не всегда была доступна для исследования.
Один центр (с 33 сложными опухолями) не имел доступа к ультразвуковой системе Voluson 730 Expert или GE E8 и поэтому не мог предоставить какие-либо объемы.
Семь центров сообщили, что забывчивость или временные технические проблемы являются объяснением того, что не предоставляют объемы для всех их трудных образований, а шесть центров не дали никаких объяснений.
| Диагноз | Количество (n/%) |
| Доброкачественная опухоль | 100 (72) |
| Эндометриома | 7 (5) |
| Тератома | 5 (4) |
| Простая киста или парасальпингеальная киста | 3 (2) |
| Функциональная киста | 3 (2) |
| Гидросальпинкс или сальпингит | 3 (2) |
| Псевдокиста брюшины | 2 (1) |
| Абсцесс | 2 (1) |
| Фиброма | 18 (13) |
| Серозная цистаденома / цистаденофиброма | 30 (22) |
| Муцинозная цистаденома / цистаденофиброма | 23 (17) |
| Редкая доброкачественная опухоль | 4 (3) |
| Пограничная опухоль | 15 (11) |
| Стадия 1 | 14 (10) |
| Стадия 2 | 1 (1) |
| Стадия 3 или 4 | 0 (0) |
| Первичная инвазивная опухоль | 22 (16) |
| Стадия 1 | 7 (5) |
| Стадия 2 | 1 (1) |
| Стадия 3 | 8 (6) |
| Стадия 4 | 0 (0) |
| Редкая злокачественная опухоль | 6 (4) |
| Метастаз в яичник из другой первичной опухоли | 1 (1) |
Наши результаты показывают, что если модель IOTA LR-1 дает неоднозначную оценку риска (от 8,3% до 25,5%), то субъективная оценка опытным специалистом по ультразвуковому обследованию превосходит использование морфологии сосудов, отображенной с помощью трехмерного ультразвукового допплера в качестве второго этапа.
Однако, если новообразование не может быть уверенно классифицировано как доброкачественное или злокачественное опытным специалистом по ультразвуковому обследованию с использованием субъективной оценки, то оценка морфологии сосудов с помощью трехмерной ультразвуковой допплерографии может быть полезной.
Для различения можно использовать как плотно упакованные сосуды во всем объеме опухоли, так и извитые сосуды при биопсии опухоли объемом 5 см³.
Мы рекомендуем использовать плотно упакованные сосуды, потому что надежность между наблюдателями была лучше для этой переменной, чем для извитых сосудов при биопсии опухоли. С другой стороны, анализ всего объема опухоли занимает больше времени, чем биопсия опухоли. По нашему опыту, высококвалифицированному специалисту по ультразвуковому обследованию требуется не менее 2,5 минут для создания вращающегося трехмерного изображения сосудистой сети всей опухоли, в то время как для создания изображения для биопсии объемом 5 см³ требуется не менее 1 минуты.
При оценке морфологии сосудов важно знать о подводных камнях ультразвуковой допплерографии и убедиться, что настройки допплера верны. Если опухоль находится далеко от ультразвукового датчика, возможно, будет невозможно обнаружить доплеровские сигналы от всей опухоли или ее частей. Это ограничивает клиническую применимость морфологии сосудов для классификации опухолей как доброкачественных или злокачественных. Еще одним ограничивающим фактором является субъективность метода. Оценка морфологии сосудов, включая «сосуды с плотной упаковкой», основана на распознавании образов, и поэтому ее трудно стандартизировать или определить.
Вопросы и ответы
Какова основная цель исследования, описанного в статье?
- Основная цель исследования – определить, улучшает ли визуализация сосудистой морфологии с помощью трехмерного (3D) ультразвукового допплеровского исследования различия между доброкачественными и злокачественными образованиями придатков, которые трудно классифицировать при использовании в качестве теста второго этапа.
Что означает термин “сложная опухоль” в контексте данного исследования?
- “Сложная опухоль” определяется как опухоль, для которой модель логистической регрессии Международного анализа опухолей яичников (IOTA) LR-1 дала неоднозначный результат (риск злокачественности от 8,3% до 25,5%), или опухоль, классификация которой как доброкачественной или злокачественной была неопределенной при субъективной оценке врачом.
Какие методы ультразвукового исследования применялись в исследовании?
- В исследовании использовались стандартизированное трансвагинальное двухмерное (2D) ультразвуковое исследование в градациях серого, цветное или энергетическое допплеровское исследование, а также трехмерное (3D) ультразвуковое исследование в области энергетического допплера.
Как анализировались трехмерные ультразвуковые изображения сосудистой сети?
- Анализ включал создание вращающихся на 360° трехмерных энергетических допплеровских изображений сосудов как во всей опухоли, так и в сферическом объеме 5 см³ из наиболее васкуляризированной части. Два независимых исследователя оценивали сосудистую сеть по заранее определенным характеристикам: ветвление, изменения диаметра, “брызги”, извилистость, участки с плотно упакованными сосудами и “мосты”.
Что являлось эталонным стандартом для классификации опухолей в данном исследовании?
- Эталонным стандартом была гистологическая классификация иссеченных образований, полученная в местных центрах. Пограничные опухоли яичников классифицировались как злокачественные. Патологоанатомы не имели доступа к результатам УЗИ.
Сколько женщин было включено в исследование IOTA-3 и сколько из них имели “сложные” опухоли?
- В исследование IOTA-3 была включена 2541 женщина с опухолью придатков. Из них 376 (16%) имели “сложную” опухоль, для которой диагноз был неопределенным при субъективной оценке, или модель LR-1 дала неоднозначный результат.
Какие причины были указаны для непредоставления трехмерных ультразвуковых объемов в некоторых центрах?
- Причинами непредоставления объемов были: удаление сохраненных в ультразвуковой системе объемов без резервных копий, недоступность требуемой ультразвуковой системы, забывчивость или временные технические проблемы, а также отсутствие доступа к необходимым ультразвуковым системам в одном из центров.