Частота преждевременных родов увеличилась в течение последних десятилетий и составляет примерно 10% от всех родов в мире. Около 70% преждевременных родов возникает спонтанно, без повреждения околоплодных оболочек или вследствие преждевременного разрыва плодных оболочек (ПРПО). Преждевременные роды приводят к 75% перинатальной смертности, а также к большинству кратко- и долгосрочных неонатальных заболеваний, вследствие инфекции и воспаления, которые являются основной причиной спонтанных преждевременных родов, и могут впоследствии привести к детскому церебральному параличу (ДЦП). Существует мнение, что неонатальная заболеваемость является продолжением внутриутробного воспалительного процесса, который получил название синдром воспалительного ответа плода (СВОП). Плоды, которые пострадали от этого синдрома, имеют клинические и лабораторные показатели системного воспаления.
АВТОРЫ: Yael Sciaky-Tamir, Reli Hershkovitz, Moshe Mazor, Ilan Shelef, Offer Erez
ВВЕДЕНИЕ
Частота преждевременных родов увеличилась в течение последних десятилетий и составляет примерно 10% от всех родов в мире. Около 70% преждевременных родов возникает спонтанно, без повреждения околоплодных оболочек или вследствие преждевременного разрыва плодных оболочек (ПРПО).
Преждевременные роды приводят к 75% перинатальной смертности, а также к большинству кратко- и долгосрочных неонатальных заболеваний, вследствие инфекции и воспаления, которые являются основной причиной спонтанных преждевременных родов, и могут впоследствии привести к детскому церебральному параличу (ДЦП). Существует мнение, что неонатальная заболеваемость является продолжением внутриутробного воспалительного процесса, который получил название синдром воспалительного ответа плода (СВОП). Плоды, которые пострадали от этого синдрома, имеют клинические и лабораторные показатели системного воспаления.
В настоящее время проведение диагностического амниоцентеза для пренатальной диагностики интраамниальной инфекции / воспаления и синдрома воспалительного ответа плода, проводится крайне редко, поэтому ультразвуковая диагностика может помочь в неинвазивной оценке плодов с риском преждевременных родов. Фетальный тимус является одним из самых интригующих органов в этом контексте. Недавно он был предложен в качестве маркера для диагностики внутриутробного воспаления плода. В данном обзоре будут описаны случаи преждевременных родов и развитие неинвазивной визуализации тимуса, как одного из методов оценки случаев с высоким уровнем спонтанных преждевременных родов.
ПРЕЖДЕВРЕМЕННЫЕ РОДЫ
Инфекция является причиной 25-40% преждевременных родов. Микробное инфицирование амниотической жидкости обнаруживается у 12,8% женщин с преждевременными родами с неповрежденными околоплодными оболочками, и у 32,4% женщин с ПРПО. Микробная инвазия амниотической жидкости (MИAЖ) диагностируется полимеразной цепной реакцией. Первыми по частоте выявления являются микоплазмы и Ureoplasma urealyticum. Также оказываются Streptococcus agalactiae, кишечная палочка, Fusibacterium species и Gardnerella vaginalis.
СИНДРОМ ВОСПАЛИТЕЛЬНОГО ОТВЕТЫ ПЛОДА (СВОП)
Синдром воспалительного ответа плода (СВОП) развивается по типу системной воспалительной реакции, что приводит к поражению органов, которое связано с повышением заболеваемости и смертности новорожденных. Около 39% случаев преждевременных родов осложнены СВОП.
Определение высокой концентрации в крови плода различных цитокинов (то есть IL-1, IL-6 и TNF-α) является признаком СВОП. Концентрация IL-6 выше 11 нг/мл в крови плода, было доказано, является предиктором тяжелой неонатальной заболеваемости и была установлена в качестве критерия для определения плодов с или без СВОП.
СВОП вызывает изменения во всех органах и системах плода, а также в амниотической жидкости, хориоамниотической мембране, шейке матки и миометрии. Процесс направлен на начало родовой деятельности, что объясняется изгнанием инфицированной ткани из организма матери.
ИМУННАЯ СИСТЕМА ПЛОДА
Инфекция/воспаление индуцирует ответ провоспалительных T-хелперов, что приводит к повышенному образованию TNFα и IL-1, оба увеличивают уровни матриксных металлопротеиназ (ММР), в результате чего продуцируются материнские простагландины. Они, как известно, связаны с патологической активацией процесса родоразрешения, что ведет к преждевременным родам, однако, они также могут влиять на развитие плода. Эти процессы могут привести к повреждению многих органов, включая альвеолы в легких (что приводит к бронхолегочной дисплазии (БЛД)), нейроны головного мозга (что может привести к неблагоприятным неврологическим результатам, таким как ДЦП), сердце (уменьшение диастолы приводит к снижению сердечного выброса, который может повторно способствовать гипоксическому/ ишемическому поражению головного мозга) и другие органы плода, такие как кожа, почки и надпочечники. Данные процессы свидетельствуют о том, что существует прямая связь между развитием СВОП и последующими осложнениями у новорожденных.
ТИМУС
Одним из основных органов, принимающим участие в развитии иммунной системы плода, является тимус – орган, который считается основным местом продукции Т-клеток. Развитие вилочковой железы начинается на ранней стадии беременности, и происходит с третьего мешка фарингеальной щели. Гемопоэтические стволовые клетки колонизируют эпителий тимуса на сроке гестации 7-8 недель. Морфологическое развитие тимуса завершается в 16-20 недель беременности, когда происходит его созревание. Кора тимуса содержит высокую концентрацию Т-клеток предшественников, также присутствуют эпителиальные клетки тимуса, мезенхимальные клетки, эндотелиальные клетки и дендритные клетки. У плода первые признаки тимоцитов негативной селекции появляются с 8 недель, признаки положительного отбора начинаются с конца 12 недели беременности. Размер тимуса коррелирует с массой тела при рождении, не отличается у плодов мужского и женского пола, и у доношенных новорожденных не имеет связи с методом родоразрешения. В конце первого года жизни тимус достигает максимального размера, и в достаточном объеме образует Т-клетки, в то время как периваскулярное пространство продолжает расти, с пиком в 10 и 25 лет. Тимопоэз происходит и у взрослых, хотя в меньшем количестве.
Размер тимуса
Уменьшенный размер тимуса может быть связан с увеличением смертности новорожденных. Хорошо известно, что дети с синдромом DiGeorge или с вело-кардио-фациальным-синдромом (VCFS), которые связаны с микроделецией 22q11 хромосомы, имеют гипоплазию или аплазию тимуса. Были проведены исследования, которые показали, что внутриутробная сонографическая диагностика уменьшенного тимуса у плодов с пороками сердца (особенно с дефектами конотрункуса) увеличивает вероятность того, что эти плоды имеют также патологию 22q11 хромосомы. Также описаны случаи уменьшенного тимуса у плодов с ЗВУР, и беременности, осложненные преэклампсией и в плодах с трисомией 21.
Изменения в тимусе во время воспаления / инфекции
De Felice и др. сообщают, что размер тимуса, который определяется путем измерения кардиотимического размера на рентгенограмме грудной клетки при рождении и оценивается как соотношение кардиотимического размера к грудной клетке (CT / T), значительно меньше у новорожденных с очень низкой массой тела, преждевременно рожденных от матерей с признаками субклинического хориоамнионита. Гистологические исследования подтвердили уменьшенный размер тимуса у плодов, которые умерли в результате преждевременных родов с признаками хориоамнионита.
Пренатальная диагностика тимуса
Пренатальная диагностика вилочковой железы описывалась в протоколах УЗ-диагностики с частотой 74% в конце 1980 годов. В начале 2000-х сонографистам удалось обнаружить фетальный тимус у> 99% плодов, во время первого и второго пренатального скрининга (рис.1).
Рис.1. Сонограмма плода на 28 неделе гестации, четко визуализируется ткань сниженной эхогенности тимуса (стрелки), на уровне кардиального среза трех сосудов.
Проведено измерение диаметра вилочковой железы и были опубликованы номограммы. Фетальная сонография позволяет визуализировать тимус в верхнем средостении, на уровне плоскости трех сосудов, как хорошо очерченный гипоэхогенный орган. Анатомическими ориентирами тимуса являются внутренние грудные артерии, определяющие боковые стенки железы, визуализирующиеся на цветовом доплере, и уровень плоскости среза трех сосудов (Рис.2).
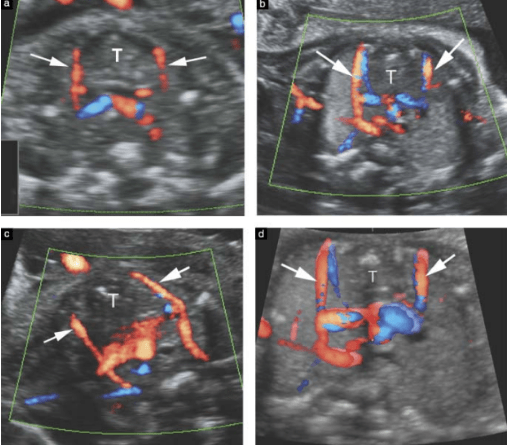
Рис.2. Сонограммы тимуса плодов в разные сроки гестации. 2D (а-с) и 3D (d) сонограммы с использованием доплера на уровне кардиального среза трех сосудов, грудных артерий, указывающих границы между тимусом и легкими. а) 22 недели гестации, b) 26 недель гестации, с и d) 31 неделя гестации.
Как правило, две грудные артерии имеют параллельный ход, было доказано, что в случаях гипоплазии тимуса изменяется ход артерий (Рис.3).
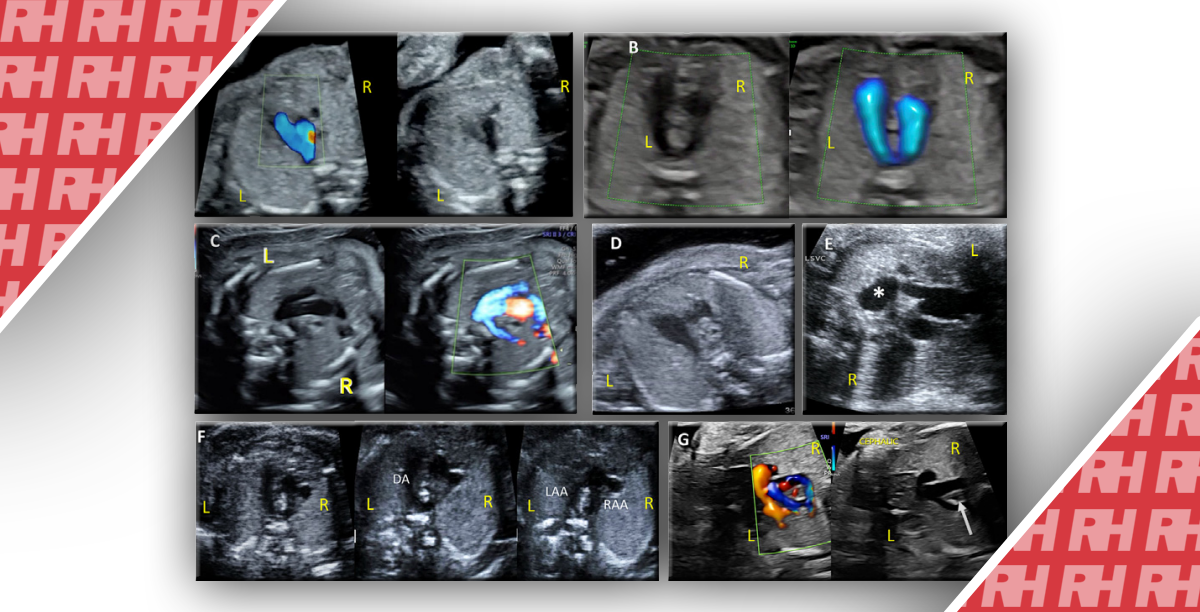
Рис.3. Цветовое доплеровское изображение грудных артерий а) нормальный размер тимуса (T), визуализируется параллельный ход сосудов, и b) изображения гипопластического тимуса (t), на что указывает изменение направления грудных артерий.
Оценить размер тимуса было предложено с помощью торакотимического соотношения (TT-Ratio) (Рис.4). Это отношение между передне-задним размером тимуса и средостением на уровне плоскости среза трех сосудов. Соотношение не коррелирует с гестационным возрастом или биометрией плода, и было установлено, что нормой является 0,44 ± 0,04.
Размер тимуса может быть измерен с помощью 3D ультразвука (рис.5).
Рис.4. Сонограмма поперечного среза грудной клетки на уровне кардиального среза трех сосудов, показано измерения торакотимического соотношения. Тимус измеряется от грудины до переднего края поперечного среза аорты (Caliper 1). Диаметр грудной клетки измеряется от задней поверхности грудины до грудного позвонка (Caliper 2).
Рис.5. Виртуальная реконструкция с измерением объема тимуса в 22 недели гестации. Для проведения исследований рекомендуем использовать аппарат от компании GE Voluson E8.
ЗАКЛЮЧЕНИЕ
Размер фетального тимуса был связан с тяжестью внутриутробной инфекции. Доказательства в поддержку этой точки зрения включают в себя следующее: (I) размер тимуса ниже 5-го процентиля был обнаружен во всех случаях внутриутробной инфекции. (II) Кроме того, уменьшенный размер вилочковой железы был обнаружен в 71% случаев преждевременных родов, которые имели гистологически подтвержденный хориоамнионит и только в 12% случаев преждевременных родов без признаков хорионамнионита.
Исследование показывает, что женщины, которые поступают в клинику с преждевременными родами с неповрежденными околоплодными оболочками и с ПРПО должны пройти детальное ультразвуковое исследование фетального тимуса, как маркера участия плода в процессе внутриутробного воспаления.