🤖 Короткий переказ від ШІ
Частота передчасних пологів зростає, і інфекції/запалення відіграють значну роль, призводячи до серйозних наслідків для новонароджених. Одним із перспективних методів неінвазивної оцінки внутрішньоутробного запалення є ультразвукова візуалізація фетального тимусу.
Дослідження показують, що зменшений розмір тимусу може корелювати з внутрішньоутробною інфекцією та передчасними пологами. Це робить його потенційним маркером для виявлення плодів з ризиком, хоча для точної діагностики інфекції може знадобитися амніоцентез. Для детальнішого ознайомлення з обладнанням, що використовується для таких досліджень, відвідайте УЗД апарати.
✅ Ключові тези зі статті:
- Діагностика: Фетальний тимус може слугувати маркером внутрішньоутробного запалення, що оцінюється за допомогою УЗД.
- Лікування: Акцент робиться на ранньому виявленні ризиків та неінвазивних методах дослідження.
- Переваги: УЗД тимусу є неінвазивним методом, що доповнює інші діагностичні процедури.
- Обмеження: Незважаючи на перспективність, УЗД тимусу не завжди повністю замінює прямі методи діагностики інфекції, такі як амніоцентез.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Частота передчасних пологів збільшилась протягом останніх десятиліть та становить приблизно 10% від усіх пологів у світі. Близько 70% передчасних пологів виникають спонтанно без пошкодження навколоплідних оболонок або внаслідок передчасного розриву плідних оболонок (ПРПО). Передчасні пологи призводять до 75% перинатальної смертності, а також до більшості коротко- і довгострокової неонатальної захворюваності, внаслідок інфекції та запалення, які є основною причиною спонтанних передчасних пологів, та можуть згодом призвести до дитячого церебрального паралічу (ДЦП). Існує думка, що неонатальна захворюваність є продовженням внутрішньоутробного запального процесу, якій отримав назву синдром запальної відповіді плоду (СЗВП). Плоди, які постраждали від цього синдрому мають клінічні і лабораторні показники системного запалення.
АВТОРИ: Yael Sciaky-Tamir, Reli Hershkovitz, Moshe Mazor, Ilan Shelef, Offer Erez
ВСТУП
Частота передчасних пологів збільшилась протягом останніх десятиліть та становить приблизно 10% від усіх пологів у світі. Близько 70% передчасних пологів виникають спонтанно без пошкодження навколоплідних оболонок або внаслідок передчасного розриву плідних оболонок (ПРПО).
Передчасні пологи призводять до 75% перинатальної смертності, а також до більшості коротко- і довгострокової неонатальної захворюваності, внаслідок інфекції та запалення, які є основною причиною спонтанних передчасних пологів, та можуть згодом призвести до дитячого церебрального паралічу (ДЦП). Існує думка, що неонатальна захворюваність є продовженням внутрішньоутробного запального процесу, якій отримав назву синдром запальної відповіді плоду (СЗВП). Плоди, які постраждали від цього синдрому мають клінічні і лабораторні показники системного запалення.
В даний час проведення діагностичного амніоцентезу для пренатальної діагностики інтраамніальньої інфекції/запалення і синдрому запальної відповіді плода, проводиться вкрай рідко, тому ультразвукова діагностика може допомогти в неінвазивній оцінці плодів з ризиком передчасних пологів. Фетальний тимус являється один з найбільш інтригуючих органів в цьому контексті, нещодавно був запропонований в якості маркера для діагностики внутрішньоутробного запалення плоду. В даному огляді будуть описані випадки передчасних пологів та розвиток неінвазивної візуалізації тимусу, як один із методів оцінки випадків з високим рівнем спонтанних передчасних пологів.
ПЕРЕДЧАСНІ ПОЛОГИ
Інфекція є причиною 25-40% передчасних пологів. Мікробне інфікування амніотичної рідини виявляється у 12,8% жінок з передчасними пологами з непошкодженими навколоплідними оболонками, і в 32,4% жінок з ПРПО. Мікробна інвазії амніотичної рідини (MIAР) діагностується полімеразно-ланцюговою реакцією. Першими по частоті виявлення являються мікоплазми та Ureoplasma urealyticum. Також виявляються Streptococcus agalactiae, кишкова паличка, Fusibacterium species та Gardnerella vaginalis.
СИНДРОМ ЗАПАЛЬНОЇ ВІДПОВІДІ ПЛОДА (СЗВП)
Синдром запальний відповіді плоду (СЗВП) розвивається по типу системної запальної реакції, що призводить до ураження органів, яке пов’язане з підвищенням захворюваності та смертності новонароджених. Близько 39% випадків передчасних пологів ускладнені СЗВП.
Виявлення високої концентрації в крові плоду різних цитокінів (тобто IL-1, IL-6 і TNF-α), являється ознакою СЗВП. Концентрація IL-6 вище 11 нг/мл в крові плоду було доказано, що є предиктором важкої неонатальної захворюваності та був встановлений в якості критерію для виявлення плодів з або без СЗВП.
СЗВП викликає зміни в усіх органах та системах плоду, а також в амніотичній рідині, хоріоамніотичній мембрані, шийці матки і міометрію. Процес спрямований на початок пологової діяльності, що пояснюється вигнанням інфікованої тканини з організму матері.
ІМУННА СИСТЕМА ПЛОДУ
Інфекція/запалення індукує відповідь прозапальних T-хелперів1, що призводить до підвищеного утворення TNFα та IL-1, обидва збільшують рівні матричних металопротеїназ (ММР), в результаті чого продукуються материнські простагландини. Вони, як відомо, пов’язані з патологічною активацією процесу пологорозрішення, що веде до передчасних пологів, проте, вони також можуть впливати на розвиток плода. Ці процеси можуть призвести до пошкодження багатьох органів, включаючи альвеоли в легенях (що призводить до бронхо-легеневої дисплазії (БЛД)), нейрони головного мозку (що може привести до несприятливих неврологічних результатів, такі як ДЦП), серця (зменшення діастоли призводить до зниження серцевого викиду, який може повторно сприяти гипоксическому / ішемічному ураженню головного мозку) та інших органів плоду, таких як шкіра, нирки та наднирники. Дані процеси свідчать про те, що існує прямий зв’язок між розвитком СЗВП та подальшими ускладненнями у новонароджених.
ТИМУС
Одним з основних органів, що приймає участь у розвитку імунної системи плоду є тимус, орган, який є основним місцем продукції Т-клітин. Розвиток вилочкової залози починається на ранній стадії вагітності, та походить з третього мішка фарингеальної щілини. Гемопоетичні стовбурові клітини колонізують епітелій тимусу в терміні гестації 7-8 тижнів. Морфологічний розвиток тимусу завершується в 16-20 тижнів вагітності, коли відбувається його дозрівання. Кора тимусу містить високу концентрацію Т клітин попередників, також присутні епітеліальні клітини тимусу, мезенхімальні клітини, ендотеліальні клітини та дендритні клітини. У плода перші ознаки тимоцитів негативної селекції появляються з 8 тижнів, ознаки позитивного відбору починаються з кінця 12 тижня вагітності. Розмір тимусу корелює з масою тіла при народженні, не відрізняється у плодів чоловічої та жіночої статі і в доношених новонароджених не має зв’язку з методом пологорозрішення. В кінці першого року життя тимус досягає максимального розміру, та в достатньому об’ємі утворює Т-клітини, в той час як периваскулярний простір продовжує рости, з піком в 10 та 25 років. Тимопоез відбувається і у дорослих, хоча в меньшій кількості.
Розмір тимусу
Зменшений розмір тимусу може бути пов’язаний зі збільшенням смертності новонароджених. Добре відомо, що діти з синдромом DiGeorge або вело-кардіо-фаціальним-синдромом (VCFS), які пов’язані з мікроделецією 22q11 хромосоми, мають гіпоплазію або аплазію тимусу. Були проведені дослідження, які показали, що внутрішньоутробна сонографічна діагностика зменшеного тимусу у плодів з вадами серця (особливо з дефектами конотрункусу) збільшує ймовірність того, що ці плоди мають також патологію 22q11 хромосоми. Також описані випадки зменшеного тимусу у плодів із ЗВУР, та вагітності ускладнені прееклампсією та в плодах з трисомією 21.
Зміни в тимусі під час запалення / інфекції
De Felice та ін. повідомляють, що розмір тимуса, який визначається шляхом вимірювання кардіотимічного розміру на рентгенограмі грудної клітки при народженні та оцінюється як співвідношення кардіотимічного розміру до грудної клітки (CT/T), значно менший у новонароджених з дуже низькою масою тіла, передчасно народжених від матерів з ознаками субклінічного хоріоамніоніту. Гістологічні досліджень підтвердили зменшений розмір тимусу у плодів, які померли внаслідок передчасних пологів з ознаками хоріоамніоніту.
Пренатальна діагностика тимусу
Пренатальна діагностика вилочкової залози описувалась в протоколах УЗ-діагностики з частотою 74% наприкінці 1980 років. На початку 2000-х сонографістам вдалося виявити фетальний тимус в >99% плодів, під час першого та другого пренатального скринінгу (рис.1).
Рис.1. Сонограма плода в 28тижнів гестації, чітко візуалізується тканина пониженої ехогенності тимусу (стрілки), на рівні кардіального зрізу трьох судин.
Проведено вимірювання діаметру вилочкової залози та були опубліковані номограми. Фетальна сонографія дозволяє візуалізувати тимус у верхньому середостінні, на рівні площини трьох судин, як добре окреслений гіпоехогенний орган. Анатомічними орієнтирами тимусу являються внутрішні грудні артерії, що визначають бокові стінки залози, які візуалізуються на кольоровому доплері, та рівень площини зрізу трьох судин (Рис.2).
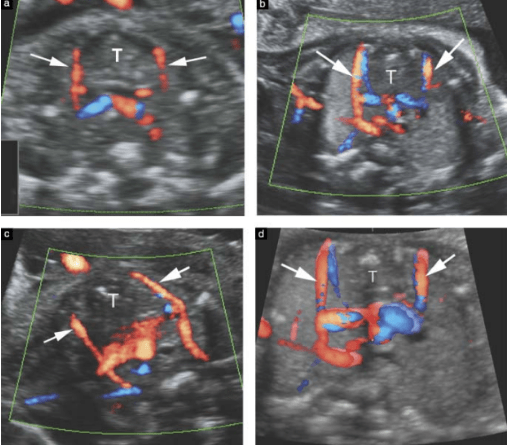
Рис.2. Сонограми тимусу плодів в різні терміни гестації. 2D (а-с) та 3D (d) сонограми з використанням доплеру на рівні кардіального зрізу трьох судин, грудних артерій, що вказують межі між тимусом та легенями. а) 22 тижні гестації, b) 26 тижнів гестації, с і d) 31 тиждень гестації.
Як правило, дві грудні артерії мають паралельний хід, було доказано, що у випадках гіпоплазії тимусу змінюється хід артерій (Рис.3).
Рис.3. Кольорове доплерівське зображення грудних артерій а) нормальний розмір тимусу (T), візуалізується паралельний хід судин, та b) зображення гіпопластичного тимусу (t), на що вказує зміна напрямку грудних артерій.
Оцінити розмір тимусу було запропоновано за допомогою а (TT-Ratio) (Рис.4). Це відношення між передньо-заднім розміром тимусу та середостінням на рівні площини зрізу трьох судин. Співвідношення не корелює з гестаційним віком або біометрією плоду, та було встановлено, що нормою являється 0,44 ± 0,04.
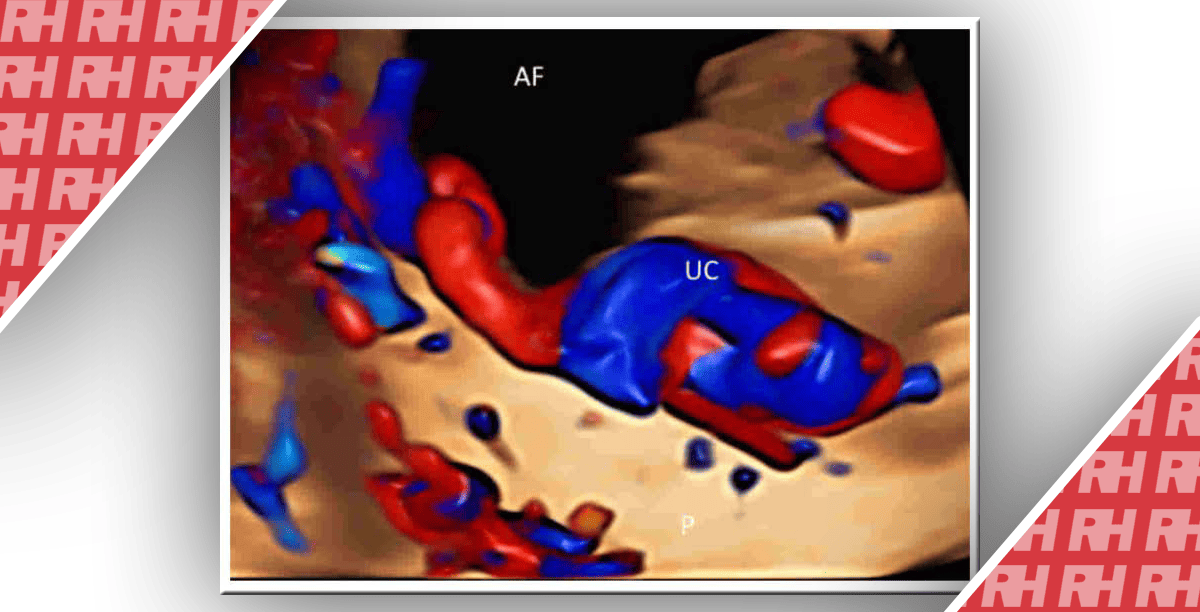
Розмір тимусу може бути виміряний за допомогою 3D ультразвуку (Рис.5).
Рис.4. Сонограма поперечного зрізу грудної клітки на рівні кардіального зрізу трьох судин, показано вимірювання торакотимічного співвідношення. Тимус вимірюється від грудини до переднього краю поперечного зрізу аорти (Caliper 1). Діаметр грудної клітки вимірюється від задньої поверхні грудини до грудного хребця (Caliper 2).
Рис.5. Віртуальна реконструкція з вимірюванням об’єму тимусу в 22 тижні гестації. Для проведення досліджень рекомендуємо використовувати апарат від компании GE Voluson E8.
ВИСНОВОК
Розмір фетального тимусу був пов’язаний з важкістю внутрішньоутробної інфекції. Докази на підтримку цієї точки зору включає в себе наступне: (I) розмір тимусу нижче 5 – го процентиля був виявлений у всіх випадках внутрішньоутробної інфекції. (II) Крім того, зменшений розмір вилочкової залози був виявлений в 71% випадків передчасних пологів, які мали гістологічно підтверджений хоріоамніоніт та тільки в 12% випадків передчасних пологів без ознак хоріонамніоніту.
Дослідження показує, що жінки, які поступають в клініку з передчасними пологами з непошкодженими навколоплідними оболонками та з ПРПО повинні пройти детальне ультразвукове дослідження фетального тимусу, як маркера участі плоду в процесі внутрішньоутробного запалення.
Питання та відповіді (FAQ)
Що таке синдром запальної відповіді плоду (СЗВП)?
- СЗВП – це системна запальна реакція плоду, що призводить до ураження органів та пов’язана з підвищенням захворюваності та смертності новонароджених. Він часто ускладнює передчасні пологи.
Які причини передчасних пологів?
- Інфекція є однією з основних причин (25-40%), а також передчасний розрив плідних оболонок (ПРПО).
Як тимус пов’язаний з внутрішньоутробним запаленням?
- Зменшений розмір тимусу може бути пов’язаний з внутрішньоутробною інфекцією та передчасними пологами. Дослідження показують його кореляцію з тяжкістю запалення.
Як проводиться пренатальна діагностика тимусу?
- Пренатальна діагностика тимусу проводиться за допомогою ультразвукового дослідження. Вимірюється його розмір та співвідношення з розміром грудної клітки.
Які показники використовуються для оцінки розміру тимусу?
- Використовується торакотимічне співвідношення (TT-Ratio) – відношення розміру тимусу до розміру грудної клітки на рівні площини трьох судин. Норма – 0,44 ± 0,04.
Чи є ультразвукова діагностика тимусу заміною амніоцентезу?
- Ультразвукова діагностика тимусу є неінвазивним методом оцінки, який може бути корисним додатковим інструментом, але не замінює амніоцентез для діагностики інтраамніальної інфекції/запалення.
Які наслідки СЗВП для новонародженого?
- СЗВП може призвести до ураження різних органів, включаючи легені (БЛД), головний мозок (ДЦП), серце та інші, що викликає підвищену захворюваність та смертність.