Автор: Luck J. Louis
Ви читаєте продовження статті. Щоб ознайомитись з першою частиною, переходьте за посиланням
ВНУТРІШНЬОСУХОЖИЛКОВІ ВТРУЧАННЯ
Кальцинований і некальцинований тендиноз – це два потенційно симптоматичних захворювання, які часто не піддаються консервативному лікуванню. Здатність ультразвукового сканування чітко візуалізувати і локалізувати аномалії сухожилків, робить аспірацію кальцифікатів під ультразвуковим наведенням і пролотерапію безцінними при лікуванні цих станів.
Лікування кальцинованого тендинозу
Кальцинований тендиноз ротаторної манжети (також відомий як кальцинуючий тендиніт) викликається осадженням кристалів карбонатного апатиту, найчастіше в критичній зоні надостьового сухожилля приблизно на 1 см проксимально від його місця фіксації. Uhthoff і Loehr описали три різних етапи в процесі розвитку хвороби, а саме: стадії прекальцифікації, кальцифікації і посткальцифікації. Залежно від фази захворювання значно різниться візуальна картина і фізичний стан кальцифікації, як і симптоми самого пацієнта. Стадія кальцифікації складається з трьох фаз. Фази формування і спокою – хронічні, і можуть бути пов’язані з різним ступенем больового синдрому в стані спокою або при русі. Однак у багатьох пацієнтів, захворювання протікає безсимптомно. Ці осередки кальцифікації часто чітко відмежовані і мають переривчасту структуру при рентгенографічних дослідженнях і, як правило, генерують значне акустичне затінення під час ультразвукового сканування (рис.11).
Рис.11. Тверді осередки кальцифікації при кальцинованому тендинозі. Приклади «твердої кальцифікації», які є типовими для фази формування кальцинованого тендинозу. (A) Рентгенограма в передньо-задній проекції пацієнта A показує велике, різко обмежене кальцинування всередині сухожилка підостьового м’язу (зафарбована стрілка). (B) У пацієнта B сухожилля надостьового м’язу візуалізується поздовжньо. Великий інтенсивний осередок кальцифікації (не зафарбована стрілка) створює виражений артефакт задньої акустичної тіні.
Аспірація вогнищ кальцифікації в цих двох фазах є досить важким завданням, оскільки такі осередки кальцифікації досить тверді і легко кришаться.
Фаза резорбції є останньою фазою стадії кальцифікації і супроводжується найбільшою симптоматикою. Потрапляння кристалів кальцію у поруч розташовану субакроміальну бурсу може привести до сильного болю і обмеження діапазону рухів. Ця фаза зазвичай триває 2 тижні або довше. Ці кальцифікати візуалізуються нечітко на рентгенограмах і практично не створюють акустичної тіні при ультрасонографії (рис. 12). При аспірації, ці кальциновані відкладення зазвичай м’які і мають консистенцію суспензії.
Рис. 12. М’які кальцифікати при кальцинованому тендинозі. Приклади «м’якої кальцифікації», які характеризують резорбтивну фазу кальцинованого тендинозу. (A) Слабка, нечітко виражена зона кальцифікації (зафарбована стрілка) зображена на рентгенограмі в передньозадній проекції у пацієнта А, який страждає від пекучого болю в плечовому суглобі. (B) У пацієнта B спостерігається нечітка гіперехогенна ділянка спереду в межах сухожилля надостьового м’язу, яка сканується уздовж короткої осі (НЕ зафарбована стрілка).
Кальцинований тендиноз зазвичай є станом, що самостійно відмежовується, при якому вогнища кальцифікації резорбуються після періоду загострення больового синдрому. Однак у деяких пацієнтів цей стан може призвести до хронічного болю і функціональних порушень. Резорбція кальцифікатів добре корелює з поліпшенням клінічної симптоматики, і тому для їх видалення були розроблені різні методи лікування. Не існує переконливих доказів ефективності ін’єкції стероїдів в осередок ураження, іонофорезу оцтової кислоти або імпульсної ультразвукової терапії. Екстракорпоральна ударно-хвильова літотрипсія використовує акустичні хвилі для фрагментації відкладень кальцію, при цьому значне або повне клінічне поліпшення було відзначено у 66% -91% пацієнтів. Однак доступ до такого устаткування як літотріптер обмежений, а ультразвукова техніка є доступною практично скрізь.
Відкрита або артроскопічна хірургія в даний час дає найкращі довгострокові результати з точки зору значного або повного клінічного поліпшення, при цьому численні дослідження повідомляють про хороші чи відмінні результати в 76,9% – 100% випадків. Однак хірургічне втручання може бути пов’язано з тривалими термінами втрати працездатності і рефлекторною симпатичною дистрофією.
Оскільки консервативні заходи ефективні приблизно у 90% пацієнтів, операція зазвичай показана тільки тим пацієнтам, у яких прогресує симптоматика, або прояви хвороби перешкоджають виконанню повсякденних завдань і при цьому не відзначається поява реакції на консервативну терапію.
Голкова іригація і аспірація (барботаж) під візуальним контролем при кальцифікації ротаційної манжети є ефективною мінімально інвазивною технікою, яка була вперше описана три десятиліття тому. У недавньому дослідженні аспірації під ультразвуковим контролем del Cura і колегами було показано, що 91% пацієнтів відзначили значне або повне поліпшення в обсягах рухів, больовому синдромі і працездатності. З огляду на потенційні ризики хірургічного втручання, перкутанну аспірацію кальцію слід розглядати в якості альтернативи, в разі неефективності консервативної терапії. Успішна аспірація може бути неможливою у випадках, коли вогнища кальцифікації візуалізуються у вигляді смуг, оскільки це вважається ознакою кальцифікації самих сухожильних волокон. Крім того, клінічні результати, при видаленні численних, дифузних, дрібних (<5 мм) кальцифікатів, як правило, незадовільні, навіть якщо застосовуються хірургічні методи лікування.
Методика барботажу під візуальним контролем сильно відрізняється, при цьому не існує загальноприйнятого стандарту. Розміри голок варіюють від 15-G, до 25-G. Деякі дослідники є прихильниками застосування двоголкової іригаційної системи, в той час як інші використовують тільки одну голку. З опублікованих даних за одними результатами лікування, виконувалося до 15 проходів через один і той же осередок кальцифікації, тоді як інші дослідники були прихильниками обмеження потенційного ятрогенного пошкодження манжети і виконували прокол тільки одноразово.
У нашому закладі ми регулярно проводимо повне ультразвукове дослідження перед будь-яким втручанням. Це робиться для того, щоб не пропустити супутні пошкодження, такі як розриви ротаторної манжети. Ми також дбаємо про те, щоб були виконані свіжі рентгенограми суглоба, для більш повної характеристики кальцифікатів і відправної точки для подальшого динамічного спостереження. Пацієнт вкладається на бік, протилежний ураженій стороні. Хоча процедура може бути виконана і сидячи, були відзначені випадки, коли пацієнти втрачали свідомість під час аспірації. Рука позиціонується, в залежності від місця розташування вогнища кальцифікації в манжеті. У разі розміщення його у ділянці сухожилка надостьового м’язу, використовується положення «рука в задній кишені». Перед дезінфекцією шкіри і обладнання проводиться ультразвукове сканування кальцифікатів. Голка 20-G, що приєднана до шприца із 2% лідокаїном, просувається в субакроміальну бурсу, куди вводиться невелика кількість анестетика до того, як голка продовжить рух в осередок кальцифікації. При цьому слід зазначити, що лідокаїн вводять в осередок кальцифікації без попередньої аспірації, щоб запобігти закупорці кінчика голки. Потім виконується кілька коротких ін’єкцій, після кожної з яких припиняється тиск на поршень. У разі успіху лідокаїн і фрагменти кальцинатів евакуюються в шприц. Шприц повинен утримуватися нижче горизонтальної лінії, щоб запобігти повторній ін’єкції аспірованого матеріалу. Крім того, коли необхідно, можна поміняти шприц на новий, наповнений лідокаїном. Барботаж слід продовжувати до тих пір, поки вогнище кальцифікації не буде аспіровано. Однак, існує ймовірність того, що відразу не вдасться аспірувати дуже тверді ділянки кальцифікації. В цьому випадку кальцифікат може бути обережно подрібнений наконечником голки під час обертання шприца (рис. 13).
Рис. 13. Неповна аспірація кальцифікатів сухожилка надостьового м’язу. (A) Сонограми сухожилка надостьового м’язу уздовж короткої осі показують розміщення голки (стрілка) біля краю «щільного» кальцифікованого відкладення. Відзначається виражене заднє акустичне затінення, яке прикриває кортикальну поверхню плечової кістки (зірочка). Була аспірована тільки невелика кількість кальцифікатів. На додаток до цього, вогнище кваліфікації було подрібнене кінчиком голки. (B) Подальша сонограма через 6 тижнів показує помітну зміну картини вогнища кальцифікації зі зникненням акустичної тіні, яка спостерігалася раніше (НЕ зафарбована стрілка). Симптоми пацієнта значно зменшилися за період між двома обстеженнями.
Вважається, що таке механічне подрібнення відкладень кальцію стимулює клітинну резорбцію. У хірургічній літературі існують узагальнені докази, що свідчать про те, що кальциновані відкладення не потрібно видаляти повністю для досягнення успішних результатів. По закінченню, голка підтягується до субакроміальної бурси, куди проводиться ін’єкція 1 мг 2% лідокаїну і 1 мл 40 мг / мл тріамцинолону для зниження ризику післяпроцедурного бурситу (рис. 14).
Пацієнтам рекомендується обмежити навантаження на плечовий суглоб протягом тижня і, в разі необхідності для зняття дискомфорту, приймати нестероїдні протизапальні препарати. Контрольний огляд проводиться через 6 тижнів після барботажа і включає в себе повторне ультразвукове дослідження і рентгенографію суглоба.
Рис.14. Ін’єкція в субакроміальну бурсу. Аксіальна сонограма сухожилка надостьового м’язу показує розміщення голки (не зафарбована стрілка) всередині субакроміальної бурси (зафарбована стрілка). Бурса частково розтягнута за рахунок ін’єкції лідокаїну і кортикостероїду по завершенню процедури барботажа.
Лікування некальцинованого тендинозу
Дегенерація сухожилків, так звана «тендинопатія» або «тендиноз», не характеризується запальною відповіддю, а скоріше інфільтрацією фібробластів і судин. Зазвичай вважається, що тендиноз розвивається в результаті постійних мікротравм з подальшими хронічними циклами дегенерації сухожилків і їх відновленням, що призводить до ослаблення сухожилля. На сонограмі ці зміни проявляються як гіпоехогенні ділянки (рис. 15).
Рис.15. Тендиноз загального сухожилля розгиначів. Сонограма в коронарній проекції загального сухожилля розгиначів в місці фіксації у ліктя, в пацієнта з клінічним латеральним епікондилітом. (A) Велика гіпоехогенна ділянка (зафарбована стрілка) визначається уздовж поверхневого краю сухожилля, що характерно для тендинозу. Нормальне сухожилля визначається глибше за місце ураження (зірочка). (B) Відповідна кольорова доплерограма тієї ж ділянки показує виражену гіперваскуляризацію, яка є звичайною, хоча і неспецифічною ознакою при тендинозі.
Описано кілька методів лікування тендинозу. Аутогенна кров, яка містить фактори росту фібробластів, успішно використовувалася при лікуванні рефрактерного медіального і латерального ліктьового епікондиліту. Ohberg і Alfredson повідомили про значне полегшення симптомів хронічної ахілодинії після облітерації неосудин з використанням полідоканолу як склерозуючого агенту.
Пролотерапія – ще один варіант лікування, який показав багатообіцяючі результати. Це метод, при якому ін’єкція подразнюючого розчину (проліферанта) в зв’язки або сухожилля викликає локальну запальну відповідь, який, в свою чергу, індукує проліферацію фібробластів і синтез колагену. Найбільш популярним і поширеним розчином, який був вивчений, є гіперосмолярна декстроза, яка володіє відмінним профілем безпеки і при цьому дешева. Експериментально було показано, що достатньо 0,6% позаклітинної D-глюкози (декстрози) для того, щоб стимулювати продукцію факторів росту клітинами людини від хвилин до годин. Концентрації глюкози більше 10% призводить до короткої запальної реакції. У нещодавньому літературному огляді щодо пролотерапії Rabago і колеги повідомили про позитивні результати лікування в порівнянні з контролем, як в нерандомізованих, так і в рандомізованих контрольованих дослідженнях. Хороші результати повідомлялися також після лікування сухожилків в зоні фіксації м’язів стегна і надлобкової зони фіксації абдомінальних м’язів, яке проводилося без візуального контролю. Внутрішньосуглобове введення глюкози також експериментально використовувалося для лікування остеоартриту і зниження міцності передніх хрестоподібних зв’язок.
Maxwell і його колеги значно вдосконалили цей метод, використовуючи ультразвук для лікування хронічного тендинозу ахілового сухожилля. Перш за все, точно візуалізувалися осередкові зони тендинозу і часткового розриву, а потім проводилася ін’єкція 25% розчину моногідрату декстрози (Рис. 16).
Рис. 16. Тендиноз ахілового сухожилля і пролотерапія. (A) На початковій сонограмі в поздовжній проекції в середній частині ахілового сухожилля виявлена зона вираженого веретеноподібного набряку. У сухожиллі є гіпоехогені дифузні ділянки, нормальна фібрилярна ехотекстура порушена, особливо вздовж поверхневого шару. (B) Сонограми сухожилля в коронарній проекції показують розміщення голки в максимальній зоні набряку (зафарбована стрілка) перед ін’єкцією гіперосмолярної глюкози. Симптоми пацієнта майже повністю усунені після проведення п’яти сеансів.
В ході дослідження пацієнти відмічали значне зниження болю в сухожилках в спокої (88%), при нормальній фізичній активності (84%) і після навантаження (78%). Кількість внутрішньотканинних розривів зменшилася на 78%, а ділянки неоваскуляризації зменшилися на 55%. При 1-річному спостереженні у 67% пацієнтів тривав безсимптомний період, у 30% були невиражені симптоми, і тільки у 3% були симптоми помірного ступеня. Як і при всіх інтервенційних процедурах, спочатку проводилося стандартне ультразвукове дослідження всієї ділянки, щоб встановити ступінь і характер захворювання, а також виключити іншу патологію. 25% розчин глюкози отримують шляхом змішування 1 мл 50% моногідрату глюкози і 1 мл 2% лідокаїну. Після планування траєкторії голки і проведення дезінфекційних заходів, використовують голку 25-G і лідокаїн для проведення місцевої анестезії. Потім голка просувається безпосередньо в сухожилки в зону тендинозу або розриву (рис. 17). Ділянки неоваскуляризації навмисно не є метою втручання, проте неосудини часто супроводжують зони тендинозів і, як правило, зменшуються на тлі проведеного лікування (рис. 18).
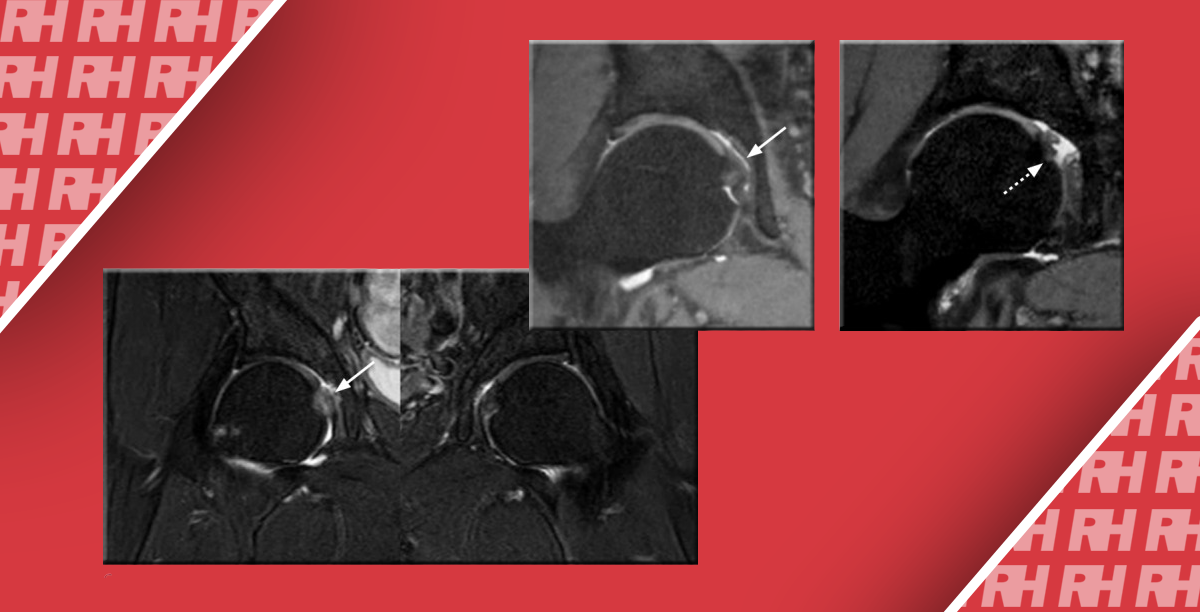
Рис. 17. Пролотерапія загального сухожилля розгиначів. (A) На сонограмі перед процедурою в коронарній площині загального сухожилля розгиначів в зоні ліктя визначаються два помітних часткових розриви (зафарбовані стрілки). (B) Голка розташовується нижче за ці два розриви (пунктирна стрілка), які розтягуються невеликою кількістю ін’єкційного розчину глюкози (не зафарбована стрілка). (C) Через 10 місяців (6 ін’єкцій) часткові розриви більше не визначаються, а симптоми пацієнта покращилися суб’єктивно на 90%. Однак сухожилля залишається дифузно гіпоехогенним і злегка потовщеним. З досвіду автора, сухожилля навіть після успішного лікування часто залишаються досить неоднорідними.
Рис. 18. Коліно стрибуна і пролотерапія. (A) Сонограма в сагітальній проекції початку сухожилку надколінка у водного лижника світового класу показує значну гіперваскуляризацію і потовщення сухожилля. (B) Повторна сонограма після кількох ін’єкцій пролотерапії показує значне скорочення кількості неосудин. Однак визначаються невеликі часткові розриви вздовж глибокої поверхні сухожилля (зафарбовані стрілки).
Як стверджує Maxwell і його колеги, зазвичай достатньо введення 0,5 мл або менше розчину в будь-які ураження. У той же час, можна проводити ін’єкції в кілька осередків ураження під час одного сеансу лікування.
Рекомендації після проведення процедури включають в себе уникнення будь-якого важкого навантаження на сухожилля протягом 2 тижнів. Крім того, для полегшення болю не повинні використовуватися нестероїдні протизапальні препарати, оскільки вони можуть пригнічувати стимулюючу декстрозою запальну реакцію. Пацієнти повторно оглядаються через 6 тижнів. Повторні ін’єкції виконуються до тих пір, поки у пацієнта не пройдуть всі симптоми або більше не буде визначатися ефект від лікування. Варто відзначити, що сухожилля у деяких пацієнтів, які повідомляють про повну ліквідацію симптомів, при візуальному контролі залишаються потовщеними, гіпоехогенними, а також мають ознаки гіперваскуляризації (рис. 19).
Рис. 19. Пролотерапія підошовного фасціїту. (A) Сонограма в сагітальній проекції правої підошовної фасції показує виражене потовщення і великий частковий розрив (стрілка) в порівнянні з безсимптомною лівою стороною. (B) Після декількох ін’єкцій декстрози частковий розрив значно зменшився в розмірі (НЕ зафарбована стрілка), при цьому симптоми пацієнта повністю ліквідовані. Незважаючи на це, сухожилля залишається потовщеним і неоднорідним.
У нашій серії неопублікованих результатів, більшість пацієнтів, які повідомляють про позитивний ефект пролотерапії, відзначають це тільки після чотирьох або п’яти ін’єкцій. Ми повідомляємо це нашим пацієнтам до початку лікування, щоб уникнути розчарування від отриманого результату.
ВТРУЧАННЯ ПРИ СИНОВІАЛЬНИХ КІСТАХ І БУРСИТАХ
Ультрасонографія – ідеальний метод для візуального контролю при пункції і аспірації більшості кіст і бурс кістково-м’язової системи. Здатність ультрасонографії візуалізувати навіть дуже невеликі скупчення рідини, уникаючи при цьому суміжних критичних структур в реальному часі, необхідна для успішного лікування цих уражень.
Лікування бурситів
Бурси – це заповнені рідиною мішки, які сприяють зменшенню тертя між сусідніми структурами і, як правило, покриті синовіальною оболонкою. Запалення бурси може бути викликано повторюваними рухами, інфекцією, системними запальними процесами і травмою. При лікуванні бурситу важливо встановити ймовірну причину його розвитку. Кортикостероїди, які зазвичай використовуються для лікування бурситу, який розвивається в результаті надмірного повторюваного навантаження (рис. 20), протипоказані при септичному бурситі (рис. 21).
Рис. 20. Фрикційний бурсит на ділянці кістка-сухожилля-кістка в зоні трансплантації. (A) Горизонтальна проекція надколінка у пацієнта, який раніше переніс відновлення передньої хрестоподібної зв’язки коліна. Ділянка надколінка в зоні трансплантації оточена кістковими фрагментами (зафарбована стрілка). (B) Сонограми в сагітальній проекції надколінка показують скупчення рідини (позначене хрестиками), яке сконцентровано над одним з таких фрагментів (НЕ зафарбована стрілка). У пацієнта через кілька тижнів після операції розвинувся прогресуючий набряк та біль при згинанні і розгинанні коліна.
Рис. 21. Септичний бурсит ліктьового відростка. Сонограма в поперечній проекції бурси ліктьового відростка. Синовіальні стінки бурси помітно потовщені і гіперваскуляризовані. Виявляється невелика кількість анехогенної рідини в центрі (зірочка). Дана ознака є неспецифічною, а диференціальна діагностика септичного і асептичного бурситу за даними ультразвукового дослідження ненадійна.
Слід також бути обережними при ін’єкції кортикостероїдів в порожнину бурси, яка з’єднується з суглобом, щоб запобігти можливому стероїд-опосередкованому ушкодженню хряща. Тому при лікуванні субакроміально-субдельтоподібного бурситу, перед ін’єкцією слід виключити розрив ротаторної манжети.
У разі розвитку бурситу з вираженим розтягненням бурси за рахунок великої кількості рідини, шляхом ретельної аспірації може бути досягнуто значне покращення і полегшення симптомів (рис. 22).
Рис. 22. Бурсит напівперетинчастого м’язу. (A) Сонограма в поперечній проекції задньомедіальної поверхні коліна. Нерівномірне скупчення рідини визначається по медіальному краю сухожилля напівперетинчастого м’язу (SM), що характерно для бурситу напівперетинчастого м’язу. (B) Голка (зафарбована стрілка) введена в бурсу, вміст якої було майже повністю аспіровано. Пацієнт одразу ж зазначив полегшення симптомів.
Однак, якщо ви виконуєте ін’єкцію кортикостероїдів в дуже маленьку зону скупчення рідини, іноді буває доцільна неповна аспірація вмісту бурси, що сприяє неповному колапсу потенційного простору її порожнини, до введення в неї ліки (рис. 23).
Рис. 23. Клубово-гребінчастий (вертлюговий) бурсит. Сонограма стегна в сагітальній проекції показує невелику кількість рідини (позначено хрестиками) поряд з великим вертлюгом. Пацієнт перебуває в положенні лежачи на боці. Тонка голка може бути легко введена в рідинне утворення (пунктирна лінія).
Лікування синовіальних кіст (гігром, гангліона)
Синовіальні кісти є найбільш поширеною причиною новоутворень м’яких тканин дистальної третини верхньої кінцівки. Етіологія синовіальних кіст суперечлива. Широко поширена думка про те, що утворення кісти відбувається в результаті травми або подразнення тканин, в результаті чого продукується муцин модифікованими синовіальними клітинами, що вистилають синовіально-капсулярну поверхню. Муцин в кінцевому підсумку заповнює клапаноподібні структури, утворені капсульними протоками, що призводить до утворення синовіальної кісти.
Багато уражень безсимптомні і не потребують лікування. За даними літератури, 40-60% гангліїв спонтанно проходять. Однак в інших випадках симптоми, які пов’язані безпосередньо з розвитком новоутворення, є показанням до проведення втручання (рис. 24).
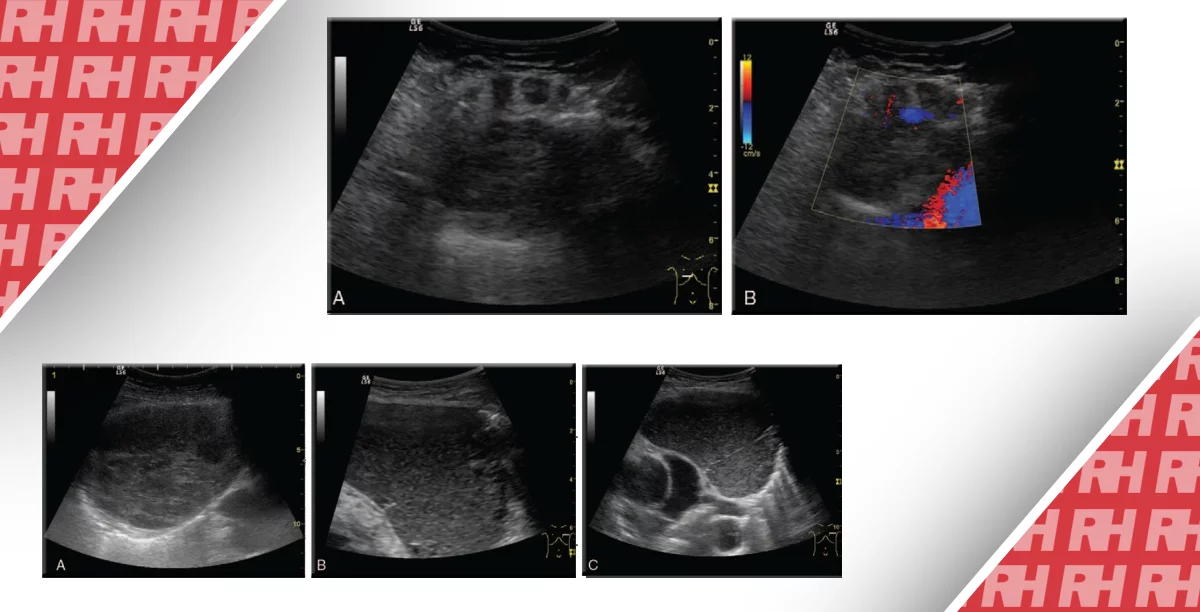
Рис.24. Аспірація синовіальної кісти вирізки лопатки. (A) Сонограма в поперечній проекції вирізки лопатки (не зафарбована стрілка) відображає невелику синовіальну кісту, що імовірно здавлює надлопатковий нерв. Голка 18-G просувається в кісту, але вона тільки частково візуалізується уздовж своєї траєкторії (зафарбовані стрілки). (B) Сонограма в поперечній проекції вирізки лопатки після аспірації 2 мл желатиноподібного матеріалу. Порожнина кісти повністю колабована (зірочка). Хронічний, тупий біль в задній частині плеча, яку відчував пацієнт протягом декількох місяців, значно зменшився до завершення процедури.
Пацієнти можуть скаржитися на обмеження діапазону рухів, біль, парестезії або м’язову слабкість. Крім того, кісти, які дренуються назовні, піддаються ризику інфікування глибоких м’яких тканин і суглобів.
Незважаючи на те, що хірургічна операція досягає 99% позитивних результатів, можливий розвиток таких ускладнень, як нестабільність суглоба, післяопераційна ригідність, зниження обсягу рухів, пошкодження нервів і судин створюють необхідність в мінімально інвазивних альтернативних методах лікування у симптоматичних пацієнтів. Ефективність сліпої черезшкірної аспірації сильно варіює – від 33% до 85%. В одному з великих опублікованих досліджень нехірургічного лікування синовіальних кіст зап’ястя, 85 пацієнтів були рандомізовані на дві групи: перша група – тільки аспірація, друга – аспірація з наступною ін’єкцією 40 мг метилпреднізолону. Дослідники не виявили різниці в частоті позитивних результатів між цими двома групами. Примітно, що 96% кіст, які згодом не рецидивували, були успішно пунктовані з однієї спроби. У тих випадках, коли потрібна була друга або третя аспірація, тільки 4% кіст в кінцевому підсумку були вилікувані. У цьому дослідженні багаторазові аспірації були малоефективні. Основним обмеженням цього дослідження було те, що всі пункції виконувались без візуального контролю.
Breidahl і Adler були першими, хто описали використання ультразвукового наведення в лікуванні синовіальних кіст. У своїй невеликій групі дослідження, дев’ять з десяти пацієнтів отримали значне або повне полегшення симптомів після аспірації голкою 20-G і ін’єкції 40-80 мг триамцинолону. Однак використання кортикостероїдів при лікуванні синовіальних кіст залишається неоднозначним.
При ультрасонографії синовіальні кісти проявляють себе як кістозні утворення і зазвичай мають овальну або часточкову форму (рис. 25). Внутрішній вміст кіст може бути анехогенним або містити низькоамплітудні ехо-сигнали і перетинки. Для аспірації всіх підозрюваних синовіальних кіст рекомендується голка 18-G, тому що вміст кісти завжди густий і желатиноподібний.
Рис. 25. Аспірація синовіальної кісти, яка викликає парез ліктьового нерва. Сонограма в поперечній проекції долонної поверхні ліктьового краю зап’ястя. (A) Часточкова синовіальна кіста (зірочка) визначається більш поверхнево за гачок (HAM) і впирається в ліктьовий нерв (зафарбована стрілка). (B) Голка (не зафарбована стрілка) частково викликала декомпресію кісти, яка відразу відійшла від ліктьового нерва (зафарбована стрілка) і ліктьової артерії (UA). Симптоми пацієнта поступово пройшли протягом кількох тижнів після аспірації.
РЕЗЮМЕ
В даний час в Північній Америці втручання під ультразвуковим контролем використовуються не в достатньому обсязі. Однак динамічні, багатоплощинні властивості ультрасонографії роблять цей метод привабливою альтернативою процедурам, які в іншому випадку виконувалися б за допомогою рентгеноскопії або комп’ютерної томографії. Насправді, більшість суглобів, кіст і бурс можна стандартно візуалізувати під контролем сонографії. У випадках барботажу і пролотерапії, ультрасонографія дала новий поштовх старим концепціям і надала радіологам нові можливості для лікування складних і хронічних проблем з сухожилками. Слід сподіватися, що цей огляд послужив трампліном для читачів, які продовжать дослідження важливої і різноманітної ролі, яку відіграє ультразвукова візуалізація при втручаннях на скелетно-м’язовому апараті.
Провести якісну ультразвукову діагностику Вам допоможе сучасний УЗД апарат TOSHIBA Aplio 500. Швидкодія та відмінна якість візуалізації роблять УЗД апарат зручним інструментом в клінічних обстеженнях. Переходьте за посиланням, щоб ознайомитись із перевагами системи!































14.10.2019
Оля