У 2004 році приблизно 1,7 млн. осіб померли від серцево-судинних захворювань (ССЗ). Атеросклероз визнано патологічною причиною більшості серцево-судинних проявів, для виявлення якого пропнують використовувати неінвазійні МРТ, КТ серця, КТА та УЗД, замість ангіографії, яка є інвазійною та дорогою процедурою.
У 2004 році приблизно 1,7 млн. осіб померли від серцево-судинних захворювань (ССЗ), що становить 29% від усіх смертей у світі. Із них майже 7,2 млн. були спричинені ішемічною хворобою серця (ІХС), а 5,7 млн. – інфарктом міокарда. Статистичні дані смертності, надані ВООЗ, вказують на те, що ССЗ стали основною причиню смерті 37,3 % осіб у США станом на 2003 рік, й що 32% всіх смертей через ССЗ стались передчасно, або ж до настання 75-річного віку (приблизна середня тривалість життя у США). Атеросклероз визнано патологічною причиною більшості серцево-судинних проявів. Враховуючи те, що атеросклероз починається на ранньому етапі життя і може приховано прогресувати протягом десятиліть, з’явилась потреба виявляти індивідів без наявних симптомів, проте із високим ризиком, допоки не стався сам напад, який може мати фатальні наслідки. Куріння, гіпертонія, цукровий діабет, а також підвищений рівень фібриногену, ліпопротеїну низької щільності та холестерину у плазмі, є одними із найпоширеніших факторів ризику для розвитку атеросклерозу та ССЗ. Щоправда, дані фактори не обов’язково вказують на існування атеросклерозу та його серйозність на рівні артеріальної стінки. Їх також не можна використати для визначення ані прогресування хвороби, ані реакції пацієнта на терапію. Однак, вдалось виявити, що зміни у товщині комплекса інтима-медіа сонної артерії (ТКІМСА) пов’язані із змінами у кількості атеросклеротичних бляшок. Окрім того, результати декількох паралельних спостережень виявили, що товщина шару інтима-медіа являє собою незалежний фактор ризику для появи латентних ССЗ, гострого інфаркту міокарда та інсульту. Саме у зв’язку із цим, задля вимірювання ТКІМСА і було запропоновано використовувати В-режим ультразвукової діагностики, як неінвазійну, високочутливу методику, яка б визначила та кількісно відобразила ранні симптоми судинного захворювання, а також ризик появи ССЗ. У даній статті розглянуто основи патологічної фізіології атерогенезу, дані що підтверджують значення ТКІМСА як сурогатного маркера для серцево-судинних хвороб, а також існуючі суперечки стосовно методології для оптимального вимірювання ТКІМСА.
АТЕРОГЕНЕЗ
На мікроскопічному рівні гіперліпідемія виступає одним із провокаторів розвитку атеросклерозу. Вважається, що окислення ЛНЩ (ліпопротеїнів низької щільності), які проникають у інтиму артеріальної стінки, спричиняє запальну реакцію, результатом чого є ендотеліальна дисфункція. Вона виражається вивільненням речовин, які сприяють приєднанню тромбоцитів, моноцитів, та лімфоцитів до ендотеліальної поверхні та переміщенню лейкоцитів у субендотеліальний шар. Тут моноцити проникають у запальні клітини, включаючи також і макрофаги, які поглинають або фагоцитують ЛНЩ, розташовані у межах інтими, за допомогою фагоцитарних та toll-подібних рецепторів. Холестерин та ЛНЩ, які моноцит не в змозі мобілізувати і знищити, накопичуються у цитоплазмі у формі цитозольних крапель, перетворюючи, у кінцевому результаті, макрофагоцит на ксантомну (пінну) клітину, яка є прототипом атеросклеротичної бляшки. Окрім того, toll-подібні рецептори, начебто, провокують нову хвилю запальної реакції, у якій беруть участь цитокіни, хемокіни, протеази, а також вільні радикали. Тучні клітини й інфільтрати Т-клітин (Т-лімфоцитів) завжди наявні у атеросклеротичних бляшках, що вкотре доводить важливість запалення у атерогенезі. Взагалі, вважається, що баланс між запальною так протизапальною дією визначає швидкість прогресування атеросклеротичної бляшки. Зараження хламідозом та цитомегаловірусом (ЦМВ) може також впливати на прогресування атеросклерозу; таким чином, зараження або колонізація ЦМВ мають особливо важливе значення для розвитку атеросклерозу, який може проявлятись дуже агресивно, у пацієнтів після трансплантації.
Коли атеросклероз прогресує, а фізіологічна компенсація спричиняє потовщення комплексу інтима-медіа артеріальної стінки, перевищується поріг дифузії кисню, спричиняючи гіпоксію та ішемію, що, в свою чергу, провокує появу цілої низки факторів, які посилюють запальну реакцію. Як наслідок, відбувається неоваскуляризація бляшок, ріст дрібних судин у адвентиціальній оболонці, що є гістологічною ознакою симптоматичного атеросклерозу. Окрім того, запальна реакція стимулює переміщення та збільшення клітин гладеньких м’язів всередині бляшки. У шарі інтими, або ж у м’язовому, медіальному шарі може відбутись потовщення стінки (Рис. 1 та 2). Однак, м’язовий медіальний шар є тонким у сонній артерії, тому потовщення артеріальної стінки сонної артерії спричинено передусім потовщенням інтими.
На макроскопічному рівні атеросклеротичні бляшки складаються із трьох типів клітин (ендотеліальні, гладком’язові та запальні клітини), елементів сполучної тканини, ліпідів, а також сторонніх речовин, які знаходяться в основному у інтимі артеріальної стінки. Тучні клітини разом із ліпідними краплями формують ядро, покрите оболонкою із гладком’язових клітин та збагаченої колагеном міжклітинної речовини сполучної тканини. Неоваскуляризація часто притаманна для бляшки. Окрім того, мережа дрібних кровоносних судин розростається у адвентиції – зовнішньому шарі стінки кровоносних судин, що розташований під бляшкою, яка зазвичай є запальною. Внутрішній крововилив у бляшці не обов’язково проявлятиметься. Атероми з’являються, як правило, у плечовому районі, де найбільш поширені запальні клітини, зокрема Т-клітини, тучні клітини та макрофаги. Найчастіше атеросклероз та бляшки розвиваються у зонах турбулентної течії із великою деформацією зсуву, наприклад у точках біфуркації аорти.
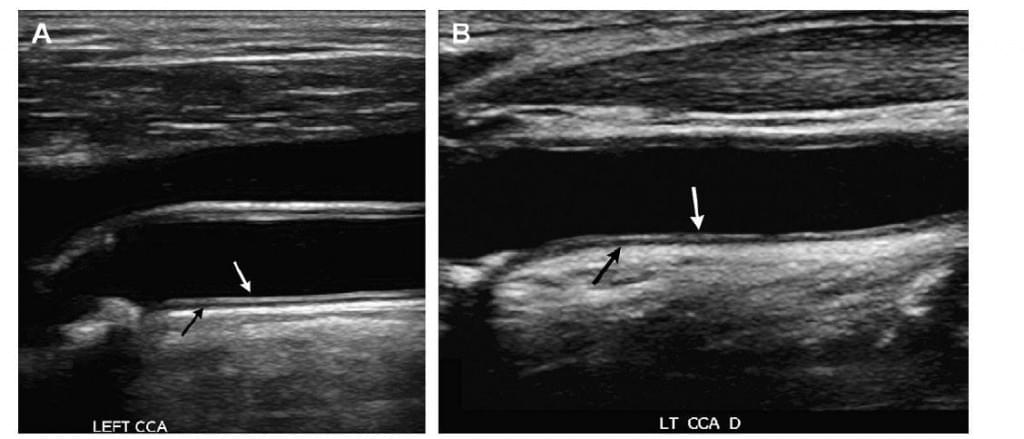
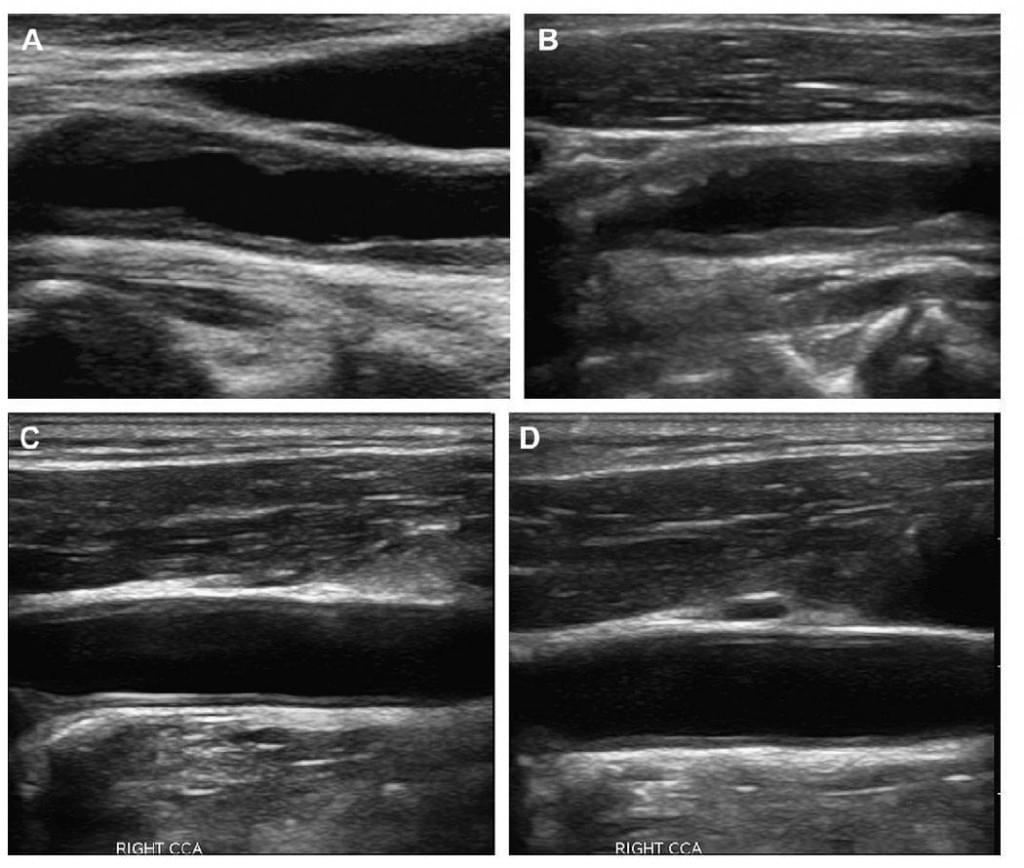
Рис. 1. (А, В) Звичний вигляд комплексу інтима-медіа сонної артерії. Сірошкальні ультразвукові зображення загальної сонної артерії у сагітальній площині двох різних пацієнтів, що показують нормальну товщину комплексу інтима-медіа, який добре видно на дальній стінці судини. Верхня ехогенна лінія (білі стрілки) являє собою інтиму та межу між інтимою і просвітом артерії. Одразу під нею знаходиться гіпоехогенний шар (чорні стрілки), що є шаром медіа судинної стінки. Ехогенний лінійний шар, що розташований внизу, – це адвентиція та межа із м’якими такнинами, які її оточують.
Рис. 2. (А, В) Потовщений комплекс інтима-медіа сонної артерії. Сірошкальні ультразвукові зображення двох різних пацієнтів у сагітальній площині, які показують потовження копмлексу інтима-медіа загальної сонної артерії (стрілки), що добре видно на дальній стінці загальної сонної артерії. Окрім потовження також помітна гетерогенність ехоструктури стінки та втрата звичної шарової структури, описаної на Рис. 1
Реагуючи на утворення бляшок й потовщення судинної стінки, судина починає розширюватись, задля того, аби вмістити зростаючу бляшку. Цей процес носить назву «позитивне ремоделювання» і полягає у розширенні діаметру судини без значного звуження просвіту. Таким чином, ми можемо спостерігати наявність великої кількості бляшок у мінімально звуженій судині. Проте, не зважаючи на відсутність стенозу, поява цих великих за розміром бляшок пов’язана із гострим коронарним синдромом. Вважається, що розрив стінки такої бляшки і/або її ендотеліальна ерозія, спричиняє виділення у кровоток тромбогенних речовин, зосереджених у ядрі, як от фосфоліпіди, фактори згортання крові та молекули клітинної адгезії. Це призводить до формування тромбу на поверхні бляшки, з можливим закупорюванням просвіту судини і появою клінічно значимих серцево-судинних ускладнень. Окрім того, активовані мікрофаги у бляшці також вивільняють протеїнази, викликаючи внутрішню кровотечу з дрібних судин у бляшці, або ж неоваскуляризацію і поступове набрякання бляшки, що призводить до розривів на її поверхні. Згодом позитивне ремоделювання не зможе забезпечити подальше збільшення бляшки, а на останніх стадіях захворювання спостерігатиметься цілковите заповнення просвіту судини. Тромб, який розвивається на поверхні бляшки із гемодинамічнозначимим стенозом, є особливо нестабільним. Це пов’язано із тим, що висока кінетична енергія від збільшеної швидкості і турбулентної циркуляції крові у точці стенозу підвищує ризик відриву тромбу та периферійної емболізації.
Низка досліджень спрямована на те, щоб заздалегідь виявити такі вразливі (активні) бляшки, які на мікроскопічному рівні характеризуються збільшеною кількістю запальних клітин (активних макрофаг і Т-лімфоцитів), неоваскуляризацією й стоншенням, або ж руйнуванням фіброзної капсули. Більшість із цих особливостей не можливо візуалізувати за допомогою теперішніх технологій. Однак, іноді на зображеннях ультразвукової діагностики (УЗД) чи магнітно-резонансної томографії (МРТ) із великою роздільною здтаністю можна побачити внутрішню кровотечу у бляшці, спричинену чи розривом капсули, чи тріщинами у маленьких та великих судинах всередині бляшки. На УЗД-зображенні геморагічна бляшка є, як правило, гіпоехогенною, а іноді навіть анехогенною і гетерогенною (Рис. 3). Більш стабільними є гомогенна та ехогенна бляшки (Рис.4). Декілька спостережень виявили, що наявність гетерогенних бляшок із гіпоехогенними/анехогенними ядрами, або ж бляшок із нестандартними властивостями поверхні, пов’язана із підвищеним ризиком нейрологічних проявів. Проте, у ході оцінки і/чи розгляду гіпоехогенної бляшки, помічені розбіжності у даних, отриманих кожним дослідником у ході особистого обстеження та показниками усіх залучених науковців. Окрім того, фіброзні та багаті на ліпіди бляшки можуть також виявитись гіпоехогенними. Саме тому їх виявлення під час УЗД не вказує на конкретні відхилення. З огляду на це, можливості УЗД апарата із сірошкальним зображенням у визначенні вразливих бляшок є обмеженими. Висновки декількох актуальних досліджень припускають, що виявлення підвищеної неоваскуляризації бляшок за допомогою внутрішньовенного ультразвукового контрастування може також слугувати маркером для вразливих бляшок (дивіться продовження обговорення).
ВИКОРИСТАННЯ ТОМОГРАФІЇ ДЛЯ ОБСТЕЖЕННЯ НА НАЯВНІСТЬ АТЕРОСКЛЕРОЗУ
Звуження коронарних артерій, виявлене за допомогою ангіографії, є передвісником появи серцевих захворювань. Однак, початкова стадія атеросклерозу, коли атероми (атеросклеротичні бляшки) ще не проходять у просвіт судини, не може бути відображена на звичайних чи цифрових ангіограмах, адже видимою є лише просвіт, а не сама судинна стінка. Тому, як показали дослідження, що поєднували посмертну гістологію із ангіографічними вимірюваннями, сама по собі ангіографія не в змозі точно відобразити наявні захворювання. До того ж, коронарна ангіографія є інвазійною та дорогою процедурою, яка піддає пацієнта ризикам, пов’язаним із перебуванням під впливом іонізуючої радіації та йодовмісткого контрастного препарату. У зв’язку із цим, використання коронарної ангіографії для обстеження пацієнтів без наявних симптомів не є доцільним. Існує зацікавленість у розвитку неінвазійних апаратів, серед яких МРТ, комп’ютерна томографія серця (КТ), комп’ютерна томографічна ангіографія (КТА) та УЗД, для отримання зображення та для виявлення безсимптомного атеросклерозу й оцінки його прогресування.
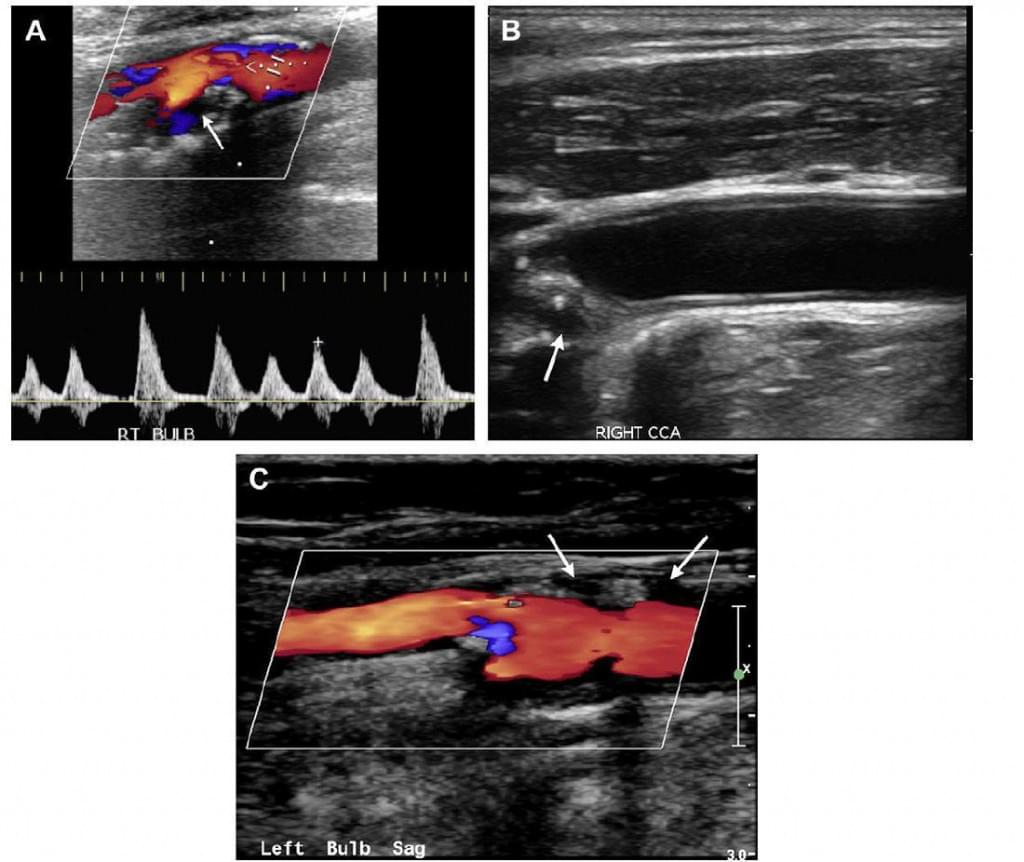
Рис. 3. Гіпоехогенна бляшка. (А) Зображення дуплексного сканування правого каротидного синусу у сагітальній площині, де показана гетерогенна бляшка із гіпоехогенною зоною у центрі (стрілка). (В) Сірошкальне зображення дистального відділу та ділянки біфуркації правої загальної сонної артерії в сагітальній площині з гетерогенною бляшкою, яка містить як гіперехогенні фокуси (ймовірно кальцинати), так і гіпоехогенну ділянку (стрілка). (С) Зображення кольорової доплерографії лівого каротидного синусу у сагітальній площині із гетерогенною бляшкою вздовж передньої стінки із двома окремими гіпоехогенними ділянаками (стрілки). Гіпоехогенна бляшка, особливо за умови, що вона розташована у центрі гетерогенної бляшки, вказує на можливий крововилив всередині бляшки. Однак, це не є специфічним симптомом, адже проявляється і у випадку фібро-ліпідної бляшки також.
У якості сурогатного маркера для перевірки наявності коронарного атеросклерозу було запропоновано використовувати вимірювання ТКІМСА. Американська Сердечна Асоціація (The American Heart Association) рекомендує проводити його із метою визначення ризику появи атеросклерозу та ССЗ. Вимірювання ТКІМСА за допомогою УЗД є неінвазійною, недорогою процедурою, яка не наражає пацієнтів на контакт із іонізуючим випромінюванням чи йодовмісними контрастними препаратами. Окрім того, завдяки вимірювання ТКІМСА можливо виявити атеросклероз у судинах ще до того, як розпочнеться звуження судинної порожнини. На повздовжніх зображеннях сонної артерії, ТКІМСА вимірюється від ехогенної перетинки між інтимою та анехогенною просвітом судини, до ехогенної адвентиції. Гіпоехогенна медіа, яка розташована між двома паралельними ехогенними лініями, також включена у вимірювання (Рис.5). Стало відомо, що нещодавні вдосконалення обладнання та вимірювальної техніки, до яких також належить програма для виділення границь (Рис.6), пов’язано із співпадінням даних, отриманих кожним дослідником у ході особистого обстеження та показниками усіх залучених науковців, принаймні у добре контрольованому дослідному середовищі. Вони підтверджують, що періодичні вимірювання ТКІМСА є дієвим методом для моніторингу змін у прогресуванні атеросклерозу із плином часом, та/або як реакції на лікування.
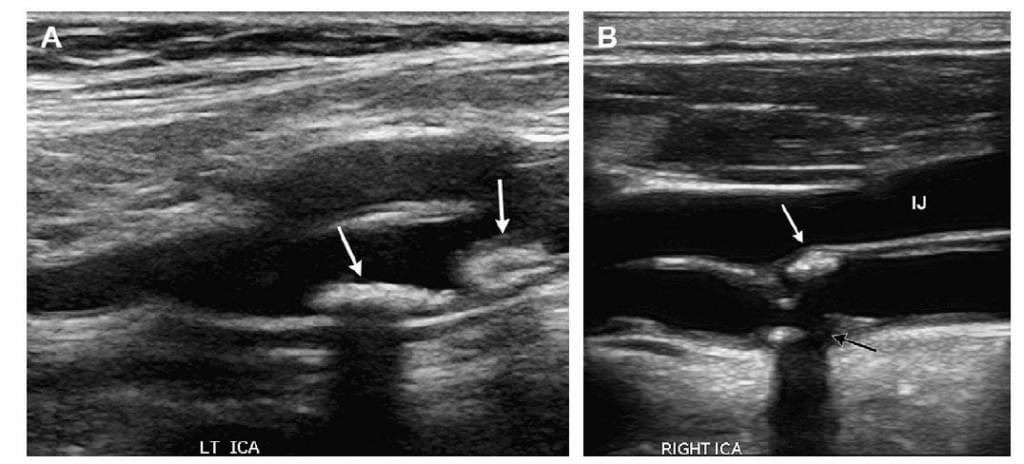
Рис. 4. Ехогенна бляшка (А) На даному сірошкальному зображенні ділянки біфуркації лівої внутрішньої сонної артерії (ВСА) позначено дві гіперехогенні бляшки (стрілки). Дистальне затемнення помітне під вищою бляшкою. (В) На цьому зображенні у сагітальній площині виявлено численні фокуси ехогенних бляшок, які знаходяться у ділянці біфуркації правої ВСА. Видима центральна частина гіпоехогенної бляшки вздовж дальної стінки (чорна стрілка) є дефектом, спричиненим затемненням від бляшки, яка розташована вище (біла стрілка). Доведено, що ехогенна бляшка не використовується для прогнозування у більшості досліджень, й не вказує на наявність кальцинатів, хоча останні є більш імовірними при виявленні затемення. IJ/internal jugular vein – внутрішня яремна вена
ДАНІ, ЩО ПІДТВЕРДЖУЮТЬ ЗНАЧЕННЯ ТКІМСА ДЛЯ ВИЯВЛЕННЯ СЕРЦЕВО-СУДИННИХ ЗАХВРЮВАНЬ
У 1986 році Pignoli разом із колегами вперше повідомив про зв’язок між товщиною стінки аорти та атеросклерозом. Починаючи із того періоду, численні клінічні випробування довели, що ТКІМСА відіграє значну роль у передбаченні майбутніх серцево-судинних захворювань. У ході дослідження The Cardiovascular Health Study із залученням 4476 пацієнтів віком понад 65 років, яке тривало 6 років і було оприлюднено у 1999 році O’Leary та колегами, виявлено, що ризик отримання інфаркту міокарда (ІМ) чи серцевого нападу у різних за віком та статтю пацієнтів був пропорційним до ТКІМСА. Згідно із результатами даного дослідження, кількість серцевих нападів та ІМ у найвищій квінтильній групі сягала більше 25%, якщо порівнювати із найнижчою квінтильною групою, де вона дорівнювала менше 5%. Відповідно, ризик у найвищій квінтильній групі на 3,87 рази поступався останній. У рамках Дослідження ризику появи атеросклерозу у різних груп населення (The Atherosclerosis Risk in Communities Study), опублікованого у 1997 році Chambliss та колегами, було обстежено понад 15 тис. пацієнтів й також доведено, що збільшена ТКІМСА була пов’язана із підвищеним ризиком можливих симптомів ССЗ та серцевого нападу. Подібних висновків дійшли й у Роттердамському Дослідженні (Rotterdam Study). Мета-аналіз 8-и праць, які були опубліковані Lorenz та колегами у 2007 році, повторно підтвердив, що збільшена ТКІМСА виступала серйозним передвісником майбутніх серцево-судинних ускладнень. Зокрема, потовщення на 0,1 мм збільшувало майбутній ризик серцевого нападу на 13-18%, а ІМ – 10-15%. Нещодавно проведений аналіз 33 досліджень виявив, що у 29 із них прослідковується позитивна залежність між ТКІМСА та ССЗ, із кореляцією між 0,12 та 0,51. Інші намагались співвіднести показники ТКІМСА із кількістю сонних артерій, вражених атеросклерозом. Атеросклероз однієї сонної артерії у пацієнтів віком понад 65 років відповідав ТКІМСА приблизно 0,9 мм, двох – 1,2 мм, і трьох – 1,3 мм.
Окрім того, виявилось, що показник ТКІМСА виступає не лише як незалежний фактор ризику, але й як аналогічний за здатністю передбачення серцево-судинних ускладнень поряд із традиційними факторами ризику, тобто, віком, расою, діабетом, холестерином, гіпертонією та курінням. Збільшення показників ТКІМСА на одне Стандартне відхилення (СВ) пов’язано із відносним ризиком 1,36 для ІМ або серцевого нападу. На противагу, зі збільшенням віку на 1 СВ (5,5 років) відносний ризик дорівнював 1,34, а систолічного (максимального) артеріального тиску на 1 СВ – 1,21.
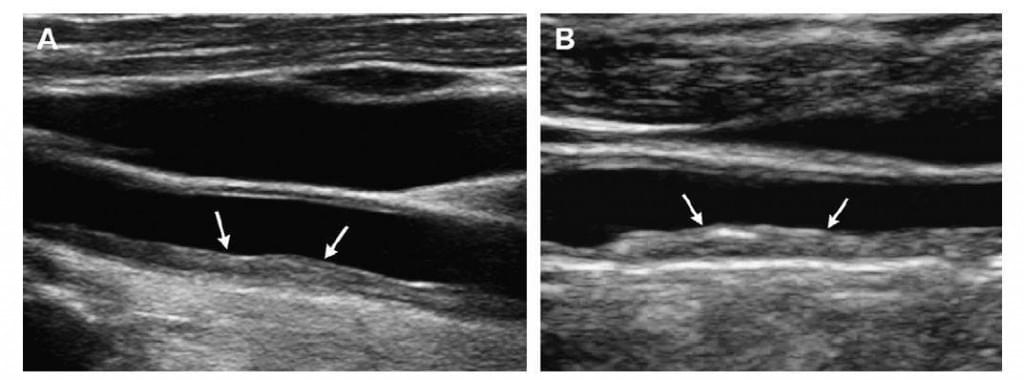
Рис. 5. Оцінка ближньої стінки комплексу інтима-медіа сонної артерії. (А, В) У двох пацієнтів комплекс інтима-медіа сонної артерії є значно товщим та більш нестандартної форми у ближній (передній) стінці. Досі чітко не визначено, чи варто робити вимірювання передньої та задньої стінок й, якщо так, то чи слід повідомляти показники ТКІМСА окремо, визначати їх середнє значення або ж максимальні результати. (С, D) Хоча деякі дослідники вважають, що ТКІМСА зазвичай вища у ближній (передній) стінці, аніж у дальній (задній), більшість повідомляють про те, що ТКІМСА не настільки чітко видно у ближній стінці у зв’язку із дефектами ближнього поля, що прослідковується у цих пацієнтів. Тому більшість дослідників, включаючи представників Американської Спілки Ехокардіографії (АСЕ – the American Society of Echocardiography/ASE), рекомендують робити вимірювання ТКІМСА від дальної стінки.
Збільшена ТКІМСА виступає не лише незалежним фактором ризику для розвитку ССЗ, вона також може бути єдиним видимим фактором ризику для деяких пацієнтів, чим може допомогти виявити ССЗ у осіб без наявних симптомів й традиційних факторів ризику. У дослідженні, оприлюдненому Khot та колегами у 2003 році, розглядалось переважання 4 стандартних факторів ризику появи ССЗ (куріння, діабет, гіпертонія та гіперліпідемія) у понад 120 тис. пацієнтів, які брали участь у клінічних серцево-судинних випробуваннях. Отримані дані показують, що приблизно у 15% жінок та 19% чоловіків не було виявлено жодних із стандартних факторів ризику. Більше того, кількість пацієнтів із ССЗ, у яких жоден із чотирьох факторів ризику не проявлявся, збільшувалась із віком і перевищила 20% для жінок віком від 75 років та чоловіків старше 65 років. Саме тому, використання ТКІМСА для виявлення ризику виникнення ССЗ є особливо доцільним серед літніх осіб, для яких притаманне граничне збільшення різноманітних факторів ризику. Окрім того, виявилось, що зв’язок між традиційними факторами ризику та ССЗ послаблюється у останні роки життя, що ускладнює можливість виявлення старших пацієнтів із субклінічними (прихованими) серцево-судинними захворюваннями лише за допомогою традиційних факторів ризику.
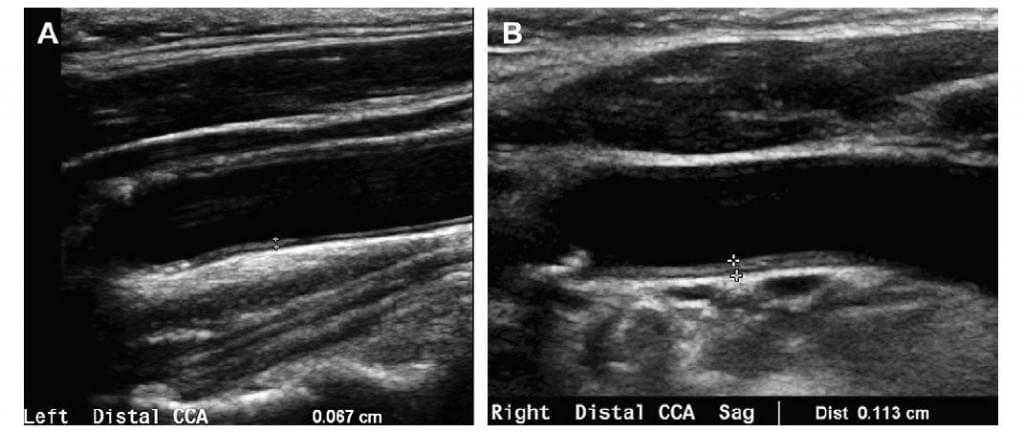
Рис. 6. Вимірювання товщини комплексу інтима-медіа сонної артерії вручну. (А) Сірошкальне зображення дистального відділу загальної сонної артерії у сагітальній площині з розмірами нормальної ТКІМСА. Зазвичай вимірювання роблять від дальної (задньої) стінки на відстані приблизно 1 см від каротидного синусу. Судина повинна знаходитись якомога паралельніше до поверхні датчика. Слід використовувати каліпери форми «+», ставлячи перехрестя на ехогенну інтиму на межі інтими із аехогенним просвітом артерії та ехогенну межу адвентиції із гіпоехогенною медіа. ТКІМСА у цього пацієнта дорівнює 0,67 мм. (В) На сірошкальному зображенні дистального відділу правої загальної сонної артерії у сагітальній площині видно збільшення ТКІМСА, що дорівнює 1, 13 мм.
У ході трохи меншого дослідження із залученням 118 молодих пацієнтів (віком від 35 до 59 років), у яких проявлявся лише один фактор ризику, проте не було самого ССЗ, встановлено, що у 13% ТКІМСА перевищувала 75-й процентиль (що вважаться високим ризиком). Це вказує на те, що навіть молоді люди зі, здавалося б, низьким ризиком можуть страждати на важке, проте безсимптомне, атеросклерозне захворювання. Тому, включення вимірювання ТКІМСА до оцінки факторів серцево-судинного ризику може допомогти ідентифікувати молодих людей без наявних симптомів, яким агресивні превентивні заходи принесуть користь. Висновки декількох інших досліджень говорять про можливість ефективного використання даних ТКІМСА для модифікації Шкали Ризику Фремінгема (Framingham Risk Score) та покращення класифікації факторів ризику ССЗ.
Подана вище інформація, що доводить значення вимірювань ТКІМСА для передбачення ризику появи ССЗ, зумовила їх використання у якості сурогатного маркера для визначення ефективності лікування атеросклерозу за допомогою антигіпертонічних ліків, ніацину, статину та інших ліпідознижуючих препаратів, та зміни способу життя. Існує величезний потенціал для вдосконалення процесу виробництва препаратів, шляхом створення легковимірювальних маркерів, які б на декілька років випереджали аналіз даних, здійснений у ході випробувань клінічних маркерів. Одне із перших досліджень, присвячених оцінці впливу статину на прогресування субклінічного атеросклерозу показало, що лікування розувастатином (Crestor) не лише стримувало прогресування атеросклерозу, але й зменшувало розміри ТКІМСА на 0,0014 мм щорічно, на відміну від збільшення на 0,0131 мм, спричиненого вживанням препаратів плацебо. У результаті, Управлінням із санітарного нагляду за якістю харчових продуктів та медикаментів США (the US Food and Drug Administration) розувастатин було визнано як препарат, який сповільнює прогресування атеросклерозу. Дослідження ARBITER (Arterial Biology for the Investigation of the Treatment Effects of Reducing Cholesterol/Використання Артеріальної Біології для Виявлення Впливу Лікування на Скорочення Кількості Холестерину) із подальшим звітом, показують, що помітне скорочення ЛНЩ (< 100 мг/дл) за допомогою статину призвело до зменшення ТКІМСА за 13-тимісячний період. Актуальний мета-аналіз 7 досліджень статину виявив статистичний зв’язок між прогресуванням ТКІМСА та ступенем сердечно-судинних проявів.
ДИСКУСІЇ СТОСОВНО ВИМІРЮВАННЯ ТКІМСА
Медіа – це гіпоехогенна лінійна структура, між ехогенною межею інтими із порожниною просвіту судини та ехогенною адвентицією зовнішньої артеріальної стінки (див. Рис.1). Отримання зображення у В-режимі за допомогою високочастотного лінійного датчика перпендикулярно до повздовжньої осі судин, забезпечує чітку візуалізацію шарів інтима-медіа у сонній артерії у більшості пацієнтів (див. Рис. 1 та 2). Однак, стабільний моніторинг ТКІМСА у якості загальноприйнятої практики поза дослідницьким середовищем ускладнюється через брак стандартизованих протоколів.
Методології, що використовувались у ході раніше згаданих багатоцентрових досліджень, були достатньо суперечливими. Дехто із дослідників отримав максимальні виміри, інші – середній коефіцієнт, а решта – низькі показники. Окрім того, не було встановлено загальноприйнятої шкали оцінки факторів ризику. У ході певних досліджень пацієнтів розділили на квінтилі; інші ж використовували квантилі; деякі дослідники надають перевагу використанню абсолютних величин окремо для віку, статі та етнічного походження; інші ж досліджували темпи росту.
Згоди стосовно того, який сегмент сонної артерії потрібно вимірювати, ще не досягнуто. Вимірювання загальної сонної артерії (ЗСА) є більш сталими та простішими у відтворенні, у зв’язку із тим, що судина є великою за розмірами, неглибоко розташованою й простягається паралельно до шкіри. Внутрішня сонна артерія (ВСА) в основному розташована навскіс від шкіри й, зазвичай, не має аналогічної до ЗСА прямолінійної форми, що ускладнює здійснення сталих розрахунків. У дослідженнях із залученням вимірів ЗСА та ВСА, дані стосовно того, у якій судині прослідковується найбільший взаємозв’язок між ТКІМСА та серцево-судинними ускладненнями, виявились суперечливими. Було використано виміри як передньої, так і задньої артеріальних стінок, а також середнє арифметичне із двох. Feinstein схиляється думки, що доцільніше робити сканування передньої стінки, зважаючи на її товщину та більшу схильність до атеросклерозу (див. Рис. 5). Однак, спотворення «ближнього поля» часто ускладнює можливість її відображення (див. Рис. 5), тому деякі дослідники дійшли висновків, що УЗД постійно применшує виміри ТКІМСА передньої стінки на 20%, є більш складною у технічному плані та для подальшого відтворення, а також не забезпечує помітного вдосконалення передбачення ризику. Вимірювання ТКІМСА передньої стінки також вважаються не настільки точними, у зв’язку із тим, що ультразвуковий промінь переходить із більш ехогенних до менш ехогенних шарів на перетині між адвентицією і медіа, та інтимою і порожниною у передній стінці. Деякі дослідження надають перевагу одностороннім вимірюванням, коли ж інші вимагають середнє арифметичне від вимірів ТКІМСА лівої та правої сторони.
Існують також суперечки стосовно того, чи правильно вимірювати ТКІМСА ручним способом (див. Рис. 6), чи можливо краще робити це автоматизовано, за допомогою програми виділення границь на артеріальній стінці довжиною в 1 см (див. Рис.7). Сьогодні більшість схиляється до використання автоматичних вимірювань із можливостями для ручного коригування. Проте, хоча автоматизовані вимірювання і є простішими у здійсненні, вони мають більші масштаби, аніж ручні вимірювання. У зв’язку із цим, стандартизовані таблиці від останніх не підходять для автоматизованих вимірювань.
Ще одне поширене занепокоєння, пов’язане із вимірюванням ТКІМСА, стосується залежності від оператора. Лікар повинен вимірювати ТКІМСА у долях міліметра, що дорівнює максимальному розширенню навіть найкращого УЗД обладнання (0,1 – 0,2 мм просторове розширення). Саме тому, у ході вимірювання настільки дрібної структури існує значна імовірність припуститись помилки при вимірюванні процентилів (див. Рис. 8). Розбіжності у даних, отриманих усіма залученими науковцями, що стосувались коефіцієнтів взаємовідношення Спірмена, коливалась у межах між 0,75 та 0,86. Розбіжності у даних, отриманих кожним дослідником у ході особистого обстеження, також є значними і варіювались між 0,69 та 0,73. Це ускладнює визначення ризику, тому що різниця між категоріями є дуже малою. До прикладу, у одному дослідженні розходження між окремими картелями дорівнювало менше 0,1 мм, а різниця між найнижчим та найвищим картелем – менше 0,3 мм.
Поява програми для виділення границь (країв) сприяла скороченню розходжень у тлумаченнях зображень. У ході її застосування Gepner та колеги повідомили, що лікарі (досвідчені, або ж новачки) змогли виявити розходження у вимірах ТКІМСА, що дорівнювали 0,011 мм (± 0,004 мм) та 0,022 мм (± 0,004 мм), у порівнянні із вимірюваннями тих же зображень, здійсненими у контрольній лабораторії. Подібність результатів, отриманих кожним дослідником у ході особистого обстеження, була високою, із середнім абсолютним відхиленням у 0,003 мм та 0,040 мм для досвідчених лікарів та новачків, відповідно.
Додатковими факторами, які потрібно брати до уваги під час інтерпретації вимірів ТКІМСА, є вплив віку, статі та етнічного походження. В загальному, ТКІМСА постійно збільшується приблизно на 0,008 мм у рік серед всього населення віком від 45 до 85 років. Однак, у пацієнтів із підвищеним рівнем холестерину сироватки крові та клінічно видимим атеросклерозом, ТКІМСА збільшується ще активніше протягом року. До того ж, у чоловіків зазвичай збільшена ТКІМСА у порівнянні із жінками. До прикладу, виявлено, що середня величина ТКІМСА для афро-американок у віці 65 років дорівнює 0,86 мм. Комплекс інтима-медіа сонної артерії є помітно товщим у афро-американок, у порівнянні із білими чи азіатками. Паління, підвищений систолічний тиск, чи підвищений рівень ЛНЩ також пов’язані із збільшеною ТКІМСА. Проте, не зважаючи на добре відомі розбіжності у вимірах ТКІМСА серед різних груп населення, у ході численних досліджень для спрощення були апріорі обрані певні лімітні точки (cutoff points).
Хоча ТКІМСА тісно пов’язана із атеросклерозом, її збільшення не являється особливим симптомом. Потовщення комплексу інтима-медіа сонної артерії може бути спричинено запальними хворобами, зокрема ревматоїдним артритом чи синдромом Такаясу.
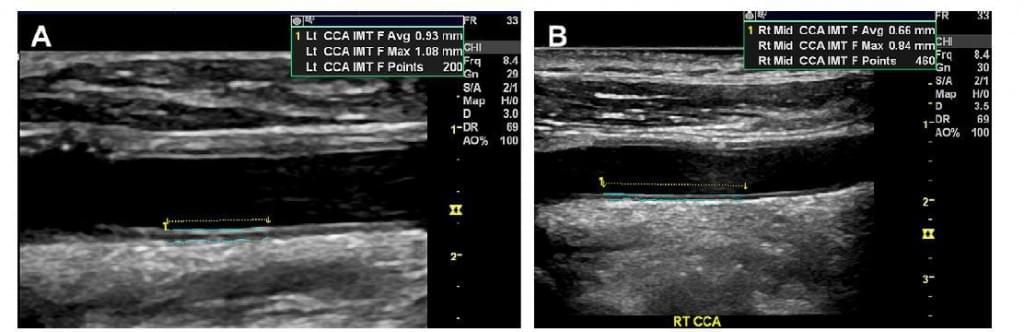
Рис. 7. Напівавтоматичне вимірювання товщини комплексу інтима-медіа сонної артерії. (А) Напіватоматичне вимірювання середнього відділу правої загальної сонної артерії розміром 1,4 см. ТКІМСА є нормальною і дорівнює 0,69 мм. (В) У цього пацієнта ТКІМСА трохи збільшена та становить 0, 9 см, із максимальним показником – 1,16 мм. (С) ТКІМСА даного пацієнта помітно збільшилось, становлячи 1,85 мм для 1, 21 см середнього відділу правої загальної сонної артерії. (Права на А та С у Philips Healthcare; дозвіл на використання.)
Рис. 8. Розбіжності у даних, отриманих кожним дослідником у ході особистого обстеження та показниками усіх залучених науковців. Ручне вимірювання. (А) Сірошкальне зображення лівої загальної сонної артерії у сагітальній площині показує неправильне розташування каліперів для вимірювання ТКІМСА. Не лише перехрестя переднього каліпера помилково знаходиться над ехогенною межею між інтимою та просвітом судини, але і він також не стоїть прямо над нижнім каліпером. (В) Повторне вимірювання ТКІМСА у лівій загальній сонній артерії того ж пацієнта що й у (А) показує, що ТКІМСА дорівнює 1,01 мм, а не 1, 62 мм.
АКТУАЛЬНІ РЕКОМЕНДАЦІЇ СТОСОВНО ВИМІРЮВАННЯ ТКІМСА
У 2000 році на V Превентивній Конференції Американської Сердечної Асоціації (the Prevention Conference V of the American Heart Association) дійшли висновку, що проведення ретельного ультразвукового обстеження сонної артерії та вимірювання ТКІМСА у осіб віком понад 45 років, дозволить отримати нову інформацію, якою можна буде скористатись при звичному визначенні факторів ризику. У 2006 році Спеціальна Комісія для Обстеження з Метою Запобігання Серцевому Нападу та Навчання (the Screening for Heart Attack Prevention and Education Task Force) порекомендувала лікувальні стратегії, серед яких більш активне скорочення ЛНЩ, на основі оцінки факторів ризику у пацієнтів із дуже високим ризиком (ТКІМСА ≥ 1 мм або 75-а процентиль) на противагу пацієнтам із помірним ризиком (ТКІМСА<1 мм або 50-75-а процентиль). Зараз Американська Сердечна Асоціація рекомендує вимірювати ТКІМСА як складову клінічного обстеження ризику появи атеросклерозу. У декількох публікаціях обговорюються підходи щодо запровадження традиційних розрахунків для класифікації ризику, і, зокрема, використання Шкали Ризику Фремінгема, в основі якої лежать виміри ТКІМСА. Однак, дані підходи не були визнані у тривалих когортних дослідженнях. До того ж, використання вимірювань ТКІМСА як маркера можливого ризику появи ССЗ зазнало найбільше критики з огляду на те, що хоча це і чудовий епідеміологічний інструмент, проте його застосування для окремих пацієнтів у лікувальній практиці, поза середовищем дослідження, викликає певні труднощі. Останні пов’язані із браком стандартизованих протоколів та критеріїв для звітності. Не зважаючи на це, у даній справі уже відбулись певні зрушення, а консенсусні заяви щодо стандартів для отримання, вимірювання та звітування про дані ТКІМСА вже були опубліковані або ж розглядаються.
У 2008 році Спеціальна Комісія для Вимірювання Комплексу Інтима-Медіа Сонної Артерії (Carotid Intima-Media Thickness Task Force) Американської Спілки Ехокардіографії (АСЕ – the American Society of Echocardiography/ASE) опублікувала консенсусні настанови, в основі яких лежать 4 великі епідеміологічні дослідження, що представили показники ТКІМСА у процентилях за віком, статтю та расою. У даних настановах ідеться про те, що вимірювання ТКІМСА та виявлення атеросклерозу могли б сприяти покращенню у визначенні ризиків появи ССЗ у пацієнтів із середніми показниками. У цих пацієнтів є від 6% до 20% шансів отримати ІМ чи померти від ССЗ протягом 10 років, проте у них немає зареєстрованого ССЗ чи симптомів ризику появи коронарної недостатності. Зокрема, спеціальна комісія визначила наступні клінічні випадки, за яких було б найбільш доцільно здійснювати вимірювання ТКІМСА: особи із сімейною історією ранніх ССЗ у родичів першого покоління; особи віком до 60 років із значним порушенням одного із факторів ризику, які б у іншому випадку не проходили медикаментозне лікування; або жінки віком до 60 років, із щонайменше двома факторами ризику можливого ССЗ. Спеціальна комісія дійшла висновку, що наявність атеросклерозу або ж розмір ТКІМСА ≥ 75 процентиля віку, статі чи раси пацієнта, вказує на збільшений ризик появи ССЗ й, можливо, на необхідність більш активних заходів для зниження ризику.
Спеціальна комісія не радить проводити ультразвукове обстеження лише із метою виявлення ризику появи ССЗ у пацієнтів із вираженим атеросклерозом, або ж якщо від його результатів не очікується позитивного впливу на терапію. Окрім того, періодичні вимірювання ТКІМСА для визначення прогресування чи регресу атеросклерозу не рекомендувались для використання у теперішній клінічній практиці [66]. Хоча, деякі дослідники радять проводити щорічні огляди, у випадку, якщо помічено аномалії, а якщо результати нормальні, то перевірку проводити кожні 2 – 5 років.
Відповідно до настанов АСЕ, вимірювання ТКІМСА повинно здійснюватись як складова ретельного сканування екстракраніальних відділів сонної артерії на наявність атеросклерозу, з метою досягнення максимальної чутливості для виявлення субклінічного судинного захворювання. Вимірювання сонної артерії повинно проводитись за допомогою лінійного датчика із частотою щонайменше 7 мГц, скануванні у В-режимі та за допомогою найсучаснішого обладнання, що відповідає стандартизованим протоколам (див. нормативи Американського Інституту з Використання Ультразвуку у Медицині/ American Institute of Ultrasound in Medicine, Американського Коледжу Рентгенології/ American College of Radiology або ж Міжсуспільної Комісії з Акредитації судинних Лабораторій/Intersocietal Commission for the Accreditation of vascular Laboratories). Сірошкальні ультразвукові зображення із високою резолюцією показують на стінці ЗСА (Загальної сонної артерії) 3 чітко виражені шари (див. Рис.1). Посередині бачимо ехогенний лінійний шар, що являє собою інтиму та межу інтими із просвітом артерії. Знизу знаходиться гіпоехогенний шар – медіа. Під нею розташований ще один ехогенний лінійний шар, який виступає у ролі адвентиції та перетину із м’якими тканинами, що оточують стінку. Тобто, відображаються 2 паралельні ехогенні лінії, які розділені більш гіпоехогенною зоною. Хоча атеросклероз та ТКІМСА активніше прогресують у каротидній залозі та сегментах внутрішньої сонної артерії, проте вимірювання ТКІМСА потрібно здійснювати починаючи із віддаленої стінки у дистальному відділі загальної сонної аретрії, сегментом довжиною 1 см. На зображенні судина повинна бути прямою та горизонтальною (тобто, перпендикулярною до направленого УЗД променю).
При можливості, пацієнтів потрібно сканувати використовуючи стандартну 4-сантиметрову глибину. За таких умов звичний розмір у пікселях становить приблизно 0,11 мм. У зв’язку із тим, що виміри ТКІМСА є надзвичайно маленькими, різниця у 1 цифровий піксель може віднести пацієнтів до різних категорій ризику. Саме тому, увага до використовуваного обладнання, стандартизованого зображення, техніки вимірювання (див. Рис. 8), а також правильної інтерпретації отриманих даних, має вирішальне значення. З огляду на те, що товщина каротидної стінки не є сталою, показники, отримані при ручному вимірюванні (див. Рис.6), можуть не зовсім точно відображати артеріальні зміни. Для цього здійснюють повторні вимірювання декількох розширених сегментів, довжиною щонайменше 1 см. Використання методу «від одного краю, до іншого» (leading-edge-to leading-edge methodology) (див. Рис. 7) не лише сприяє кращій загальній оцінці ТКІМСА, але також є простішими у відтворенні, із меншими розбіжностями у даних, отриманих кожним дослідником у ході особистого обстеження та показниками усіх залучених науковців. У більшості із раніше згаданих досліджень вимірювання ТКІМСА здійснювалось вручну. Проте, спеціальна комісія АСЕ, з метою покращення відтворюваності та скорочення тривалості обстеження безпосередньо рекомендувала використання схваленої напівавтоматизованої комп’ютерної програми із виділення границь, де можливе ручне корегування ( див. Рис. 9). Хоча дослідники й розуміють, що виміри ТКІМСА, виконані комп’ютерними програмами, є трохи більшими, аніж виміри, виконані вручну, до яких також відноситься метод «від одного краю, до іншого» (leading edge measurements). Сегменти потрібно вимірювати тричі та із трьох різних площин (латеральної, передньої і задньої, відстань між якими дорівнює 45°). Будь-який показник, що відрізняться більше, аніж на 0,05 мм, потрібно вилучити. Таким чином, виміри ТКІМСА – це середні значення від отриманих показників. У деяких лабораторіях рекомендують вимірювати ТКІМСА у декількох сегментах, повідомляючи лише максимальну величину, або також і середнє арифметичне із декількох максимальних величин (див. Рис. 10), хоча у нормативах АСЕ конкретно про це не йшлось. Виміри ТКІМСА із задніх стінок лівої та правої СЗА визначаються окремо. Будь яка фокальна площина у бляшці сегменту, який вимірюють, також повинна враховуватись. Окрім того, усі лікарі, які здійснюють вимірювання ТКІМСА, повинні пройти спеціальну підготовку.
Рис. 9. Ручне налаштування комп’ютерної програми виділення границь (країв). Хоча більшість науковців вважають, що автоматизоване вимірювання ТКІМСА для загальної сонної артерії довжиною 1 см знижує розбіжності у даних, отриманих кожним дослідником у ході особистого обстеження та показниками усіх залучених науковців, проте комп’ютеризоване вимірювання ТКІМСА все ж залишається недосконалим стандартом, результати якого у більшості випадків трохи перевищують показники, отримані у ході ручного вимірювання. Окрім того, можливість ручної корекції рекомендована для підвищення точності. Наприклад, у випадку (А) лінія, що відповідає перетину між адвентицією та медіа має неправильну форму. Повторне вимірювання із ручною корекцією у випадку (В) довзоляє вирівняти цю лінію та отримати більш точні показники ТКІМСА.
Не зважаючи на помилкове враження, що виконання точних вимірювань ТКІМСА є легким завданням, більшість дослідників повідомляють про значні розбіжності у даних, отриманих кожним дослідником у ході особистого обстеження та показниками усіх залучених науковців. Далі будуть описані одні із найпоширеніших помилок, та спроби їх мінімізації. Не слід робити вимірювання у тому випадку, якщо чітко не видно межі між інтимою та просвітом артерії (див. Рис. 11). Задля покращення видимості, найефективнішими прийомами будуть: регулювання зони фокусу, збільшення підсилення, а також перевірка, чи судина дійсно знаходиться горизонтально по відношенню до датчика, що допоможе покращити роздільну здатність. Окрім того, ТКІМСА варто вимірювати лише, якщо дві ехогенні лінії, які являють собою межі між інтимою й медіа та адвентицією, видно як у передній, так і у задній стінці, навіть якщо передню стінку зазвичай і не вимірюють; це гарантуватиме, що сканується центр судини і будуть отримані реальні виміри ТКІМСА, не перебільшені включенням згину бокової стінки. Якщо можливо побачити чітко лише сегмент ТКІМСА розміром менше, ніж 1 см, то можна виміряти коротший сегмент. Якщо ЗСА занадто глибока (>4 см), можна спробувати легке стиснення м’яких тканин над нею, або ж інший кут спостереження. Якщо судина занадто поверхнево розташована ( 4 см), є шанс отримати погіршене зображення, що спричинено викривленням товщини зрізу чи артефактом у ближньому полі, тому можна спробувати скористатись гелевою подушкою, або нанесенням товстого шару гелю. У випадку, якщо судина звивиста, для вирівнювання ЗСА можна витягнути шию, або ж попросити пацієнта повернутись на інший бік. Використання функції зближення не рекомендується. У даному випадку також не рекомендується здійснювати внутрішньосудинне ультразвукове сканування для обстеження ТКІМСА.
Спеціальна комісія АСЕ рекомендувала порівнювати показники ТКІМСА шляхом якісного опису різного роду процентилів. Виміри ТКІМСА ≥ 75 процентиля вважаються високими і вказують на збільшений ризик можливих ССЗ. Виміри між 25-м та 75-м процентилем вважаються середніми і вказують на те, що ризик появи ССЗ не змінився. Виміри ≤ 25 процентиля вважаються показником нижчого ступеню ризику ССЗ, проте, чи виправдовує це менш агресивну превентивну терапію аніж стандартний догляд залишається невідомим.
Центр із Забезпечення Медичного Догляду та Медичної Допомоги США (The United States Centers for Medicare and Medicaid) сформував Поточний код процедури (0126T) для «Загального дослідження ТКІМСА задля визначення розвитку атеросклеротичних бляшок й вивчення факторів ризику можливої появи ішемічної хвороби серця». Техас на сьогодні є єдиним штатом, де законодавчо передбачено страхове відшкодування за обстеження ТКІМСА, коли ж у інших лікарнях та клініках пацієнти повинні заплатити від 160$ до 325$ за характристику отриманого зображення.
МАЙБУТНІ ТРЕНДИ
Багато актуальних досліджень звертають основну увагу на виявлення вразливої/нестійкої бляшки, тобто геморагічної та/або запальної бляшки, у якої більше шансів прорватись і, тим самим, вивільнити тромбогенну речовину із свого ядра у кров. Це пришвидшує тромбоемболічні прояви (ускладнення), результатом чого може стати ІМ та/або серцевий напад. У нещодавно опублікованих гістологічних дослідженнях чітко видно, що прогресування неоваскуляризації у бляшці, так само як і збільшення концентрації мережі дрібних кровоносних судин у адвентиції, є характерними рисами вразливої бляшки. Декілька дослідників переконливо довели, що покращення візуалізації бляшки в пізній фазі обстеження з використанням УЗ контрастних речовин взаємопов’язано із збільшеною неоваскуляризацією у бляшці, і може слугувати сурогатним маркером на наявність вразливої бляшки. Окрім того, у 2006 році Feinstein припустив, що погіршення візуалізації бляшки в пізній фазі обстеження з використанням УЗД контрастних речовин могло проявлятись у пацієнтів, які реагували на лікування статином. Зовсім недавно декілька дослідників повідомили, що у пацієнтів із клінічним атеросклерозом прослідковується покращення візуалізації бляшки, на противагу пацієнтам із безсимптомним атеросклерозом в пізній фазі обстеження з використанням УЗД контрастних речовин. Вони також виявили, що покращення візуалізації бляшки відбувалось у тих зонах, які були гіпоехогенними на сірошкальному ультразвуковому зображенні, чим підтверджуються попередні висновки, що гіпоехогенна бляшка більш схильна до кровотечі. Окрім того, Staub із колегами дійшли висновків, що покращення візуалізації бляшки було прямо пов’язано із вираженістю стенозу сонної артерії. Не зважаючи на те, що у даному обстеженні брала участь лише невелика кількість пацієнтів, цілком можливо, що покращення візуалізації бляшки в пізній фазі обстеження з використанням УЗД контрастних речовин може використовуватись у обстеженні на наявність вразливої/нестійкої бляшки, або ж як оцінка факторів ризику у пацієнтів із гіпоехогенними чи обширними бляшками (extensive plaque). Можливо, покращення візуалізації бляшки допоможе у виявленні пацієнтів, які із стенозом ВСА ≥ 70% або із стенозами ВСА у межах 50-69% найбільше ризикують отримати серцевий напад, а тому лікування було б для них корисним.
Рис. 10. (А, В) Відхилення від норми розмірів комплексу інтима-медіа сонної артерії. Сірошкальні зображення у сагітальній площині, отримані від двох пацієнтів із аномальними потовженнями комплексу інтима-медіа. Точно не відомо чи більш правильним та клінічнозначимим буде визначення середнього показника для судинної стінки довжиною в 1 см, а чи максимальної товщини, яка у двох випадках буде відрізнятись. Для більшості великих досліджень характерна варіативність у методології оприлюднення результатів.
Рис. 11. Нечітке зображення комплексу інтима-медіа сонної артерії. Не зважаючи на те, що КІМСА у цього пацієнта здається потовщеним, ехогенна лінійна межа між інтимою та просвітом судини не є постійно видимою. Саме тому дане зображення не підходить для вимірювання ТКІМСА.
Еластографія також вважається одним із способів виявлення вразливої/нестійкої бляшки. Холестеринові та геморагічні бляшки можуть бути більш еластичними, аніж кальциновані, стабільні бляшки, хоча не настільки ж, як звичайна артеріальна стінка. Очікується, що еластична бляшка повинна проявляти більшу механічну напругу. Знижена еластичність бляшки може спричинити посилення зовнішньої напруги та стресу, призводячи тим самим до розриву. Клінічне значення еластографії (та отриманих за її допомогою показників стрейну та деформації/radial strain and shear distribution) на даний момент залишаються суперечливим та потребують подальшого вивчення.
Жорсткість артерій також можна визначити різними способами за допомогою УЗД, включаючи швидкість імпульсу; зміну у діаметрі під час серцевого циклу; розтяжність, еластичність та механічне напруження на окружності судинної стінки; індекс пульсативності; та перевірку реакційної здатності плечової артерії. Виявилось, що жорсткість артерії пов’язана із гіпертонією, діабетом, та проявами ССЗ. І все ж, поки ще не відомий найбільш оптимальний та надійний спосіб вимірювання жорсткості артерій, більшість із цих методів залишаються актуальними для проведення досліджень.
ВИСНОВКИ
Результати численних досліджень доводять доцільність використання ТКІМСА як сурогатного маркера наявності атеросклерозу або ризику проявів ССЗ. Окрім того, вимірювання ТКІМСА виявилось корисним в умовах дослідження задля вивчення прогресування хвороби. Його також можна використовувати як ефективний, легкий у вимірюванні маркер у клінічних дослідженнях, які оцінюватимуть терапевтичну ефективність препаратів та зміни у способі життя (втрата ваги, фізкультура), спрямовані на скорочення ризику появи ССЗ. Проте, хоча ТКІМСА і визнано незалежним фактором ризику можливої появи ССЗ, ще не було точно доведено, чи клінічна користь від застосування ТКІМСА має перевагу над традиційними моделями виявлення ризику ССЗ, серед яких Шкала Ризику Фремінгема або SCORE – Systematic COronary Risk Evaluation. Це пов’язано із необхідністю проведення аналізу результатів досліджень, щоб виявити, чи вдосконалення прогнозувань ризику, шляхом вимірювання ТКІМСА та ультразвуковому обстеженні сонної артерії, призведе до позитивних наслідків у виявленні ССЗ. Саме тому у основі рекомендацій щодо клінічної практики, запропонованих АСЕ, лежать виключно дані спостережень. Залишаються суперечності стосовно методології вимірювання та звітності. Не зважаючи на те, що численні великі дослідження із залученням багатьох вчених, повідомляють про тісний взаємозв’язок між збільшенням ТКІМСА та ризиком появи ССЗ, методи вимірювання та визначення результатів ТКІМСА у більшості відрізнялись, так само як і постійно наявна невідповідність між власними та спільними висновками спостерігачів, не залежно від протоколу, якого дотримувались під час вимірювання настільки маленьких структур, що розмір деяких із них сягав ліміту просторового розширення навіть найсучаснішого ультразвукового обладнання. У зв’язку із відсутністю уніфікованості, більшість клінічних центрів надає перевагу методології, запропонованій АСЕ. Однак, у найближчому майбутньому очікується, що Спілка із Обстеження та Запобігання Атеросклерозу (the Society of Atherosclerosis Imaging and Prevention) представить нові спільні норми, де буде визначено методологію та правила звітування, а також пацієнтів, які підлягають ультразвуковому обстеженню.
Toshiba Xario – тільки вигідні пропозиції від компанії RH.