🤖 Короткий переказ від ШІ
Ультразвукове дослідження з контрастним підсиленням (УЗКП) є значним кроком у діагностиці, використовуючи контрастні засоби (УКЗ) для покращення візуалізації кровопостачання органів. Метод демонструє високу ефективність у діагностиці та характеристиці уражень печінки, нирок, селезінки та інших органів, перевершуючи традиційну ультрасонографію та конкуруючи з КТ і МРТ у певних аспектах.
УЗКП дозволяє детально оцінити васкуляризацію тканин, що критично важливо для виявлення злоякісних утворень, запальних процесів та оцінки ефективності лікування. Його переваги включають безпеку, відсутність іонізуючого випромінювання та можливість проведення в режимі реального часу. Для оптимального використання УЗКП важливий досвід спеціаліста та використання сучасного обладнання, такого як УЗД апарати.
✅ Ключові тези зі статті:
- Діагностика: УЗКП значно підвищує точність діагностики уражень печінки та інших органів, порівняно зі стандартною ультрасонографією.
- Лікування: Метод допомагає оцінювати відповідь на лікування, наприклад, після абляції пухлин, та виявляти залишки пухлинної тканини.
- Переваги: УЗКП безпечне, доступне, забезпечує інформацію про перфузію в реальному часі та має меншу вартість порівняно з КТ/МРТ.
- Обмеження: Незважаючи на переваги, УЗКП не є панорамним методом і може бути складним для виконання у пацієнтів з певними станами (метеоризм, ожиріння).
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
MicheleBertolotto, MD, OrlandoCatalano, MD
Введення ультразвукових контрастних засобів (УКЗ) є важливим кроком вперед у сонографічних дослідженнях з моменту розвитку доплерівських методів. При цьому були впроваджені різні клінічні додатки, або принаймні запропоновані, для ультразвукового дослідження з контрастним підсиленням (УЗКП), у радіології та кардіологічних дослідженнях. Тим не менш, комерціалізація різних УКЗ в різних країнах і розвиток декількох технологій сканування створили плутанину, що потребує стандартизації методології та термінології.
У цій статті розглядаються історичні та фізичні основи УЗКП, потім ілюструються додатки, які застосовуються для дослідження печінки, позапечінкових досліджень і, нарешті, обговорюються основні перспективи розвитку.
ІСТОРИЧНА ПЕРСПЕКТИВА
Спроби використання фармакологічних речовин прийшли одночасно із застосуванням ультразвукових променів для діагностичної візуалізації. У 1960 році кардіологи все ще намагалися виявити скидання крові зліва направо шляхом введення речовини внутрішньовенно (які б не могли пройти легеневий фільтр) і позначали свою присутність в лівій камері серця. Транспульмональні частинки (діаметр 3-5 мкм), які б були здатні пройти у велике коло кровообігу, щоб досягти паренхіми всього тіла, були розроблені тільки в 90-ті роки. Ці УКЗ, так званого першого покоління, складалися з повітря, інкапсульованого в крихітну підтримуючу оболонку (білкову, ліпідну або полімерну), так звані мікропухирці. УКЗ першого покоління використовувалися в основному для поліпшення доплерівського сигналу з судин великого і проміжного діаметру, що дозволяло поліпшити виявлення артерій і вен, посилити зображення ходу судин і їх співвідношень і поліпшити відображення аномалій їх просвіту. Як приклад, важка доплерографічна диференціальна діагностика між обструктивним і необструктивним стенозом може бути проведена з більшою довірчою ймовірністю шляхом введення УКЗ. Крім того, для вузлів і пухлин, методи енергетичної і кольорової доплерографії з контрастним підсиленням дозволяють виявити структури з більш повільним кровотоком, судини малого калібру з поліпшеною візуалізацією ангіоархітектури і великою кількістю даних, доступних для характеристики пухлини. Перевага полягає у відсутності змін швидкості потоку при спектральному аналізі, яке виконується після введення УКЗ.
Тим не менш, особливо при болюсному введені, УКЗ викликали артефакти сигналу, зокрема артефакт надмірного посилення під назвою цвітіння, які могли б спричинити перешкоди сигналу при оцінці ураження. Крім того, УКЗ першого покоління не змогли істотно продемонструвати сигнал від малих судин, які розташовані всередині пухлини. Щоб відобразити внутрішньопухлинну мікроциркуляцію, кровотік повинен мати адекватну інтенсивність і швидкість. Використовуючи УКЗ можна збільшити інтенсивність сигналу, але при цьому неможливо поліпшити швидкість потоку.
У наступному десятилітті чутливість доплерівських сканерів для повільних потоків була поліпшена, і потреба в посиленні сигналу зменшилася. З часом інтерес дослідників повернувся до напівтонових додатків. Різні технології були введені виробниками, що дозволяє визначати розрив мікропухирців, індукований пучком променів з наступним записом широкосмугового сигналу високої інтенсивності. Цей високий механічний індекс (МІ> 0,2), забезпечує напівтоновим додаткам інтермітуючі зображення під час різних фаз циркуляції УКЗ, подібно багатофазній комп’ютерній томографії (КТ) та магнітно-резонансній томографії (МРТ). Високий МІ УЗКП дозволяв отримувати найдрібніше зображення перфузії пухлини, виявляти сигнали від дрібних судин.
Використання високої інтенсивності спалахів, які необхідні для розриву мікропухирців, викликали зменшення кількості мікропухирців («деструктивне УЗКП»), що було істотно несумісне зі скануванням в режимі реального часу і що є фундаментальним аспектом сучасної ультрасонографічної візуалізації. Ця несумісність була подолана шляхом розробки так званого другого покоління УКЗ. Нові мікропухирці були заповнені ін’єкційними газами, на відміну від повітря, що поліпшило їх стабільність і еластичність (Таблиця 1). Друге покоління УКЗ могло бути використане з технологіями з високим МІ, але при стимуляції пучком малої потужності (МІ <0,2), ці мікропухирці могли також викликати значний перфузійований сигнал (в той час, як при тих же умовах УКЗ першого покоління були не в змозі визначити будь значимі зміни).
Низький МІ зображень, заснований на коливаннях мікропухирців без їх руйнування, дозволяє отримувати посилені напівтонові зображення органів у режимі реального часу. Це стало можливим у зв’язку з тим, що УКЗ другого покоління коливаються на частоті від 2 МГц до 3 МГц, що знаходиться в межах частоти, яка використовується в діагностичній сонографії, зокрема, для абдомінального дослідження (це також пояснює, чому УЗКП дослідження поверхневих структур має погану якість зображення). У випадку, коли потужність пучка встановлена досить низькою, мікропухирці піддаються резонансу, швидко скорочуються і розширюються у відповідь на зміни тиску звукових хвиль. Коли мікропухирці піддаються впливу променю відповідної потужності і частоти, коливання стають нелінійними (тобто діаметр у фазі розрідження акустичного циклу в значній мірі перевищує його стиснення у фазі здавлення). Асиметричні коливання призводять до нелінійного ехосигналу, який містить обертони або гармоніки, провідної частоти збудження. Це явище робить можливим виконання «недеструктивного» контрастного специфічного дослідження в режимі реального часу.
УЗКП вимагає контраст-спеціального програмного забезпечення, для придушення статичного сигналу від фонових тканин і виділення сигналу від циркулюючих мікропухирців. Ця методика доступна в різних модальностях. При техніці інвертування імпульсу, 2 імпульси направляються уздовж кожної лінії сканування, другий – дзеркальне відображення першого. Обидва ехосигнали підсумовуються датчиком, несуттєвий сигнал, який формується від статичних лінійних об’єктів, таких як фонові тканини (сума 2 ехосигналів дорівнює нулю) і інтенсивні сигнали, які виникають через нелінійні об’єкти, такі як мікропухирці (сума 2 ехосигналів відрізняється від нуля).
Напівтонова сонографія з низьким МІ в режимі реального часу в даний час є стандартною процедурою, яка заснована на УКЗ і, ймовірно, є єдиним методом, до якого акронім УЗКП слід застосовувати.
Таблиця 1.
УКЗ доступні для клінічного використання в Європейському Союзі (ЄС), США та інших країнах. Назви генериків дані в дужках.
|
Найменування |
Хімічна природа |
Наявність |
|
Imagent (AF0150) |
Перфторгексан і стиснутий азот, стабілізовані в мікропухирці |
США, ЄС |
|
SonoVue (БР1) |
Стиснутий сірчастий гексафторид в полімері з фосфоліпідами |
ЄС, кілька азіатських країн за винятком Японії |
|
Definity (ImaRx) |
Ліпідні мікросфери перфлутрену в ін’єкційній суспензії |
Канада |
|
Albunex |
Заповнена повітрям білкова оболонка |
США |
|
Optison (FSO 69) |
Мікросфери з перфлутрен протеїном типу А |
США, ЄС |
|
Echovist (SHU 454) |
Газові пухирці на основі галактози |
ЄС |
|
Levovist (SHU 508A) |
Газові пухирці, стабілізовані пальмітиновою кислотою на основі галактози |
ЄС, Канада, Японія |
|
Echogen (QW3600) |
Додекафторпентан у розчині сахарози |
ЄС |
|
Sonazoid (DD723 /NC100100) |
Мікропухирці на основі перфлюбутану |
ЄС |
ЗАГАЛЬНІ АСПЕКТИ
На даний час УКЗ використовуються рутинно в більшості європейських і країнах Східної Азії, принаймні в основних університетах і лікарнях, хоча реальне поширення досі відсутнє. У США досі немає дозволу від Foodand Drug Administration для радіологічного використання, і їх використання обмежене деякими кардіологічними дослідженнями.
УКЗ значно відрізняються від КТ та МРТ контрастних засобів. УКЗ є внутрішньосудинними речовинами («кровоносного басейну») з недостатнім інтерстиціальним поширенням; їх період напіврозпаду в крові, як правило, становить кілька хвилин. Отже, знахідки при УКЗ перекриваються КТ та МРТ результатами під час артеріальної фази візуалізації, але розрізняються при переході до венозної фази. УКЗ рециркулюють кілька разів до їх розчинення, КТ та МРТ контрастні речовини (які значно менші, ніж УКЗ) проникають через стінку судини і поширюються в інтерстиції. Через відсутність позасудинної дифузії, УКЗ теоретично підходять для функціонального трасування органного кровообігу. Ще одна відмінність КТ та МРТ контрастних речовин, що УКЗ змінюються під дією скануючого променю, хоча цього і не відбувається при рентгенографії або під дією радіочастот. Сама енергія сканування змінює структуру мікропухирців, які використовуються при сонографії, але не змінює контрастні середовища для КТ та МРТ (проблема ускладнюється тим, що кожне УКЗ веде себе по-різному, коли стимулюється ультразвуковими променями з різним МІ). Остаточна істотна відмінність відноситься до фаз візуалізації. У той час, як фази сканування для КТ та МРТ відзначаються на піку підвищення для кожної фази, це не відноситься до УЗКП. Артеріальна фаза для УКЗ починається в момент надходження мікропухирців в артеріальну ніжку органу, який сканується (10-15 секунд після внутрішньовенної [intravenous – IV] ін’єкції) і триває близько 40 секунд, коли венозна фаза стає домінуючою. Венозна і кінцева фаза тривають від 3 до 6 хвилин, залежно від паренхіми, яку сканують (див. нижче обговорення). У зв’язку з можливостями проведення дослідження УЗКП в режимі реального часу з низьким МІ, необхідний орган постійно сканується протягом кожної фази контрастування. Неправильний вибір часу отримання зображення фаз КТ або МРТ може призвести до пропусків у виявленні осередкових уражень або неправильної/неможливої характеристики, в той час як УКЗ дозволяє безперервно отримувати зображення осередків ураження протягом всіх судинних фаз. Деякі УКЗ першого і другого покоління мають більш-менш виражену постваскулярну фазу, при цьому вони утримуються в печінці і, більше того, і в селезінці. Це так звана постваскулярна або паренхіматозна фаза, яка слідує за судинною фазою.
Нирки мають найшвидше інтенсивне і транзиторне (як наслідок відсутності клубочкової фільтрації) посилення після в/в ін’єкції УКЗ, в той час, як селезінка має сильне, але стійке посилення (до 6-8 хвилин). Печінка і підшлункова залоза поводяться проміжно, з прогресивним і стійким підвищенням інтенсивності. У зв’язку з подвійним кровопостачанням печінки, печінкові фази після артеріальної фази включають в себе портальну фазу (40-120 секунд після ін’єкції контрасту) і синусоїдальну (або пізню) фазу (120-300 секунд після ін’єкції контрасту). Щоразу, коли є потреба в поліорганному дослідженні (наприклад, дослідження при травмі), то нирка або нирки повинні бути досліджені в першу чергу, підшлункова залоза або печінка – наступні, і селезінка – в останню чергу (також необхідно враховувати те, що в початковій фазі неоднорідного посилення селезінки [схожий шаблон «зебри» при КТ та МРТ] може призвести до неправильної інтерпретації зображення).
УКЗ є зручними засобами, які добре переносяться і про які-небудь серйозні реакції рідко повідомляється в літературі. У ретроспективному огляді європейського досвіду використання другого покоління УКЗ SonoVue (Бракко International BV, Амстердам, Нідерланди) було тільки два серйозних несприятливих випадки і жодного смертельного результату серед 23,188 досліджених хворих. Тим не менш, алергія до компонентів контрастної речовини або інших додаткових речовин завжди повинна бути врахована. Немає особливої необхідності в дотриманні дієти або попереднього лабораторного дослідження. Оскільки УКЗ не виділяються нирками, їх можна сміливо використовувати у пацієнтів з гострою або хронічною нирковою недостатністю. Щоразу, коли це необхідно, малий об’єм УКЗ може бути введений знову, щоб уточнити зону, яка спочатку була неясною або для сканування декількох органів. Об’єм також може бути фракціонований для того, щоб оцінити артеріальну фазу поведінки різних органів або множинних осередків ураження в різних місцях одного органу. Тим не менш, навіть з тими прийомами УКЗ не вистачає панорамної якості, типової для КТ і МРТ, і не дозволяє провести повне дослідження черевної порожнини. Крім того, УКЗ зазвичай не дозволяють врятувати недіагностичне ультразвукове дослідження. Складні пацієнти, наприклад, з метеоризмом, також важко піддаються скануванню за допомогою УКЗ. Так само важко повністю дослідити пацієнтів з тяжким стеатозом або фіброзом, оскільки проникнення ультразвукового променю в печінку обмежене.
Необхідність адекватної підготовки оператора також слід враховувати. Крім того, потрібні УКЗ сканери, які оснащені спеціальним програмним забезпеченням. Безліч різновидів датчиків доступні для УКЗ, в тому числі черезшкірні датчики для живота і поверхневих структур, трансвагінальні і трансректальні датчики, ендоскопічні датчики, внутрішньосудинні датчики і датчики для інтраопераційного УЗКП. Максимум інтенсивності проекції зображення дозволяє відслідковувати хід мікропухирців з винятковим відображенням морфології судин. Також можуть бути отримані значущі контрастні 3-вимірні зображення, а також зображення з розширеним полем зору.
При методиці УЗКП базовий фон істотно очищується, враховуючи відсутність значущого гармонійного сигналу для тканин при низькому МІ, і тільки визначається сигнал від циркулюючих мікропухирців. Внутрішня ехогенність локальних уражень на базовій ультрасонограмі не суттєво заважає отриманню діагностичних даних при УЗКП. Крім того, на відміну від КТ, ехогенність паренхіми, яка оточує вогнище, істотно не впливає на діагностичну точність УЗКП. Наприклад, осередкове ураження на яскравому фоні печінки можна охарактеризувати з тією ж ефективністю, як і ураження в паренхімі без стеатозу.
УЗКП повинне бути призначене в першу чергу як завершення ультразвукового обстеження, що забезпечує додатковими даними, які недосяжні при базовій сонографії. У практиці авторів, коли ураження печінки при виявленні залишається у нас неуточненим, виконується негайно УЗКП, що дозволяє в більшості випадків поставити остаточний діагноз і уникнути більш складних і дорогих методів дослідження. Ця практика можлива, тому що ультрасонографію використовують в Італії як первісний метод візуалізації у вирішенні більшості клінічних питань при патології черевної порожнини. В інших країнах, де КТ і МР виконується на початковому етапі, існує менший потенціал для УЗКП. Як додаток до поліпшення безрезультатного ультрасонографічного обстеження, УЗКП може виступати в якості методу вибору для вирішення такої проблеми. Часто, коли лікарі знаходять невідповідність між двома методами дослідження (наприклад, КТ, МРТ, позитронно-емісійної томографії ПЕТ), автори намагаються вирішити проблему шляхом використання УЗКП (іноді відразу, без планування дослідження). Типовий сценарій включає в себе невідповідність між негативним результатом КТ відносно вогнищевих уражень печінки (ВУП) і ПЕТ дослідженням, яке показує деяке фокусне поглинання препарату; ВУП неадекватно характеризується на КТ через відсутність багатофазного режиму дослідження або тому, що осередок ураження менше сантиметра; або неспецифічне поглинання в межах даного органу при ПЕТ.
ПЕЧІНКА
УЗКП в даний час розроблено для дослідження печінки, воно стандартизоване, відтворюване і спирається на певні діагностичні критерії і прості алгоритми. Обмеження і можливості УКЗ досить зрозумілі, а керівництва для використання контрастних речовин при сонографії печінки були опубліковані Європейською федерацією суспільства з використання ультразвуку в медицині та біології у 2004 році і у 2008 році (включаючи і інші організації).
ХАРАКТЕРИСТИКА ВОГНИЩЕВИХ УРАЖЕНЬ ПЕЧІНКИ
Можливість ультразвукової характеристики уражень є низькою. Існує значне накладення даних між ехоструктурою і васуляризацією доброякісних і злоякісних ВУП, і, таким чином, існують дані про широкий спектр відсоткового співвідношення точності для сірошкального дослідження і кольорового доплерівського аналізу. При використанні УЗКП, ВУП можна охарактеризувати більш точно, відповідно до діагностичних критеріїв, схожих на динамічне КТ і МРТ. Знаючи типову перфузійну модель кожного ураження печінки в різні судинні фази можна проводити диференційну діагностику більш адекватно. Можливість УЗКП в характеристиці уражень істотно не залежить від їх діаметру. Доброякісні ураження відображаються зі значним підвищенням контрастності під час портальної або синусоїдальної фаз, і відображаються як ізоехогенніа бо гіперехогенні вогнища, в той час, як протягом тих же фаз злоякісні ураження проявляються у вигляді гіпоехогенних утворень, через вимивання контрастної речовини. Однак, за кількома винятками, існують і погано васкуляризовані доброякісні ураження, такі як: мікрорегенеративні вузлики, тромбовані або фіброзні гемангіоми і запальні або некротичні ураження, які можуть проявитися у гіпоехогенному вигляді протягом портальної і синусоїдальної фаз, що імітує злоякісність. З іншого боку, високо диференційована гепатоцелюлярна карцинома (ГЦК) може мати значне посилення протягом портальної і синусоїдальної фаз. Історія хвороби пацієнта, клініка та картина УЗКП в артеріальній фазі можуть допомогти в диференціальній діагностиці.
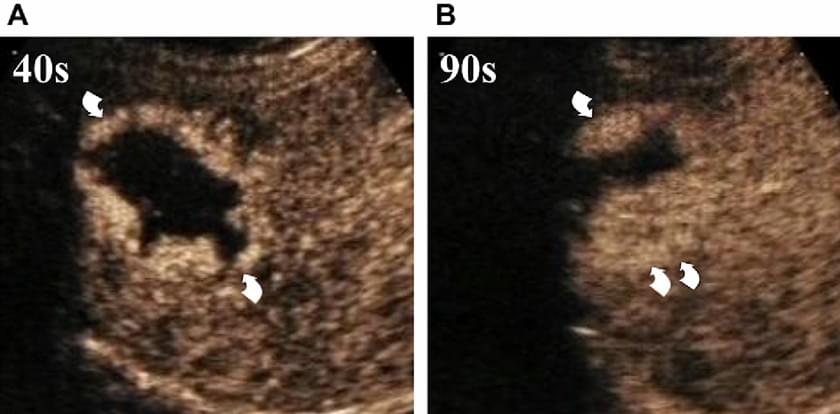
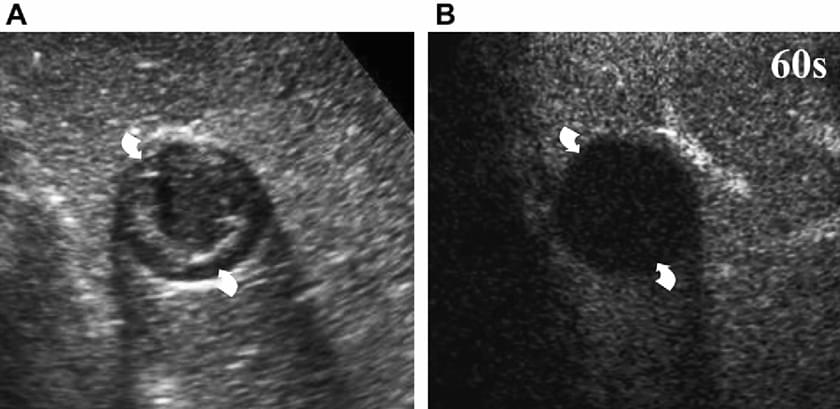
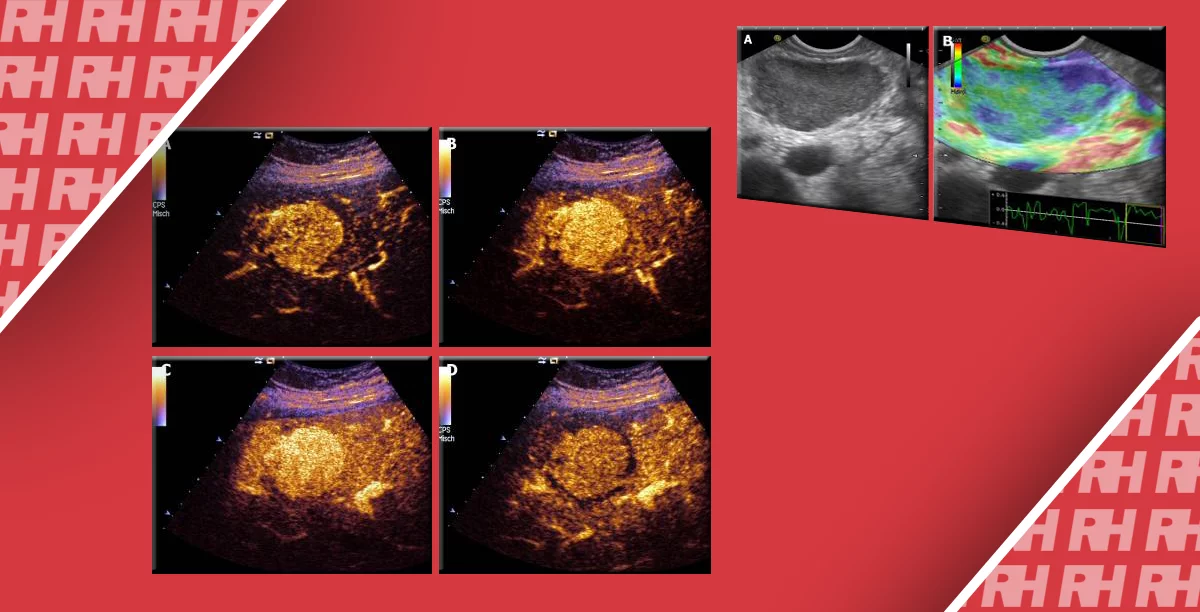
Близько 80% гемангіом печінки мають сферичне посилення малюнка (зобр.1) протягом артеріальної фази (глобуси [сфери] з периферичним посиленням, розмір яких поступово збільшується) і доцентровим накопиченням контрасту в портальній і синусоїдальній фазах.
Зображення 1. Типовий вид гемангіоми печінки (стрілки). УЗКП показує кулясте периферичне посилення через 40 секунд після ін’єкції мікропухирців (А) і прогресивне, доцентрове заповнення після 90 секунд (В). Центральна частина ураження залишається неконтрастованою через неповне заповнення.
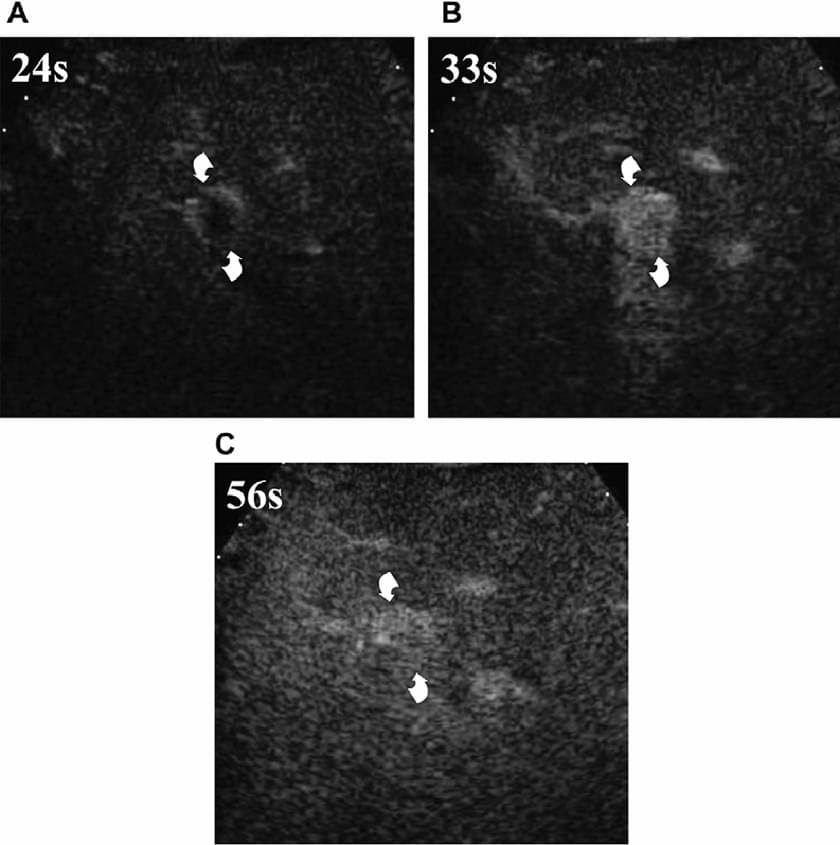
У гемангіомах з високим кровотоком сфери швидко зливаються в однорідне гіперехогенне ураження (зобр. 2).
Зображення 2. Гемангіома з високим кровотоком (стрілки). Зображення, які отримані в ході артеріальної фази через 24 секунди (А) і 33 секунди (В) після ін’єкції мікропухирців, відображають сферичне периферичне посилення відразу після надходження мікропухирців (А), з повним доцентровим заповненням протягом 9 секунд (В). Це ураження стає ізоехогенним до печінки через 56 секунд після ін’єкції (С).
Деякі гемангіоми, які заповнюються повільно, не показують значного центрального посилення в портальній і кінцевій фазах, але їх характеристика залишається адекватною, у зв’язку з їх сферичним посиленням. Існує невеликий відсоток гемангіом з незначним підвищенням контрастності або його відсутністю, що викликано масивним тромбозом або фіброзними змінами і це ускладнює адекватну діагностику. УЗКП здатна характеризувати 88% гемангіом печінки з атиповою ультразвуковою картиною.
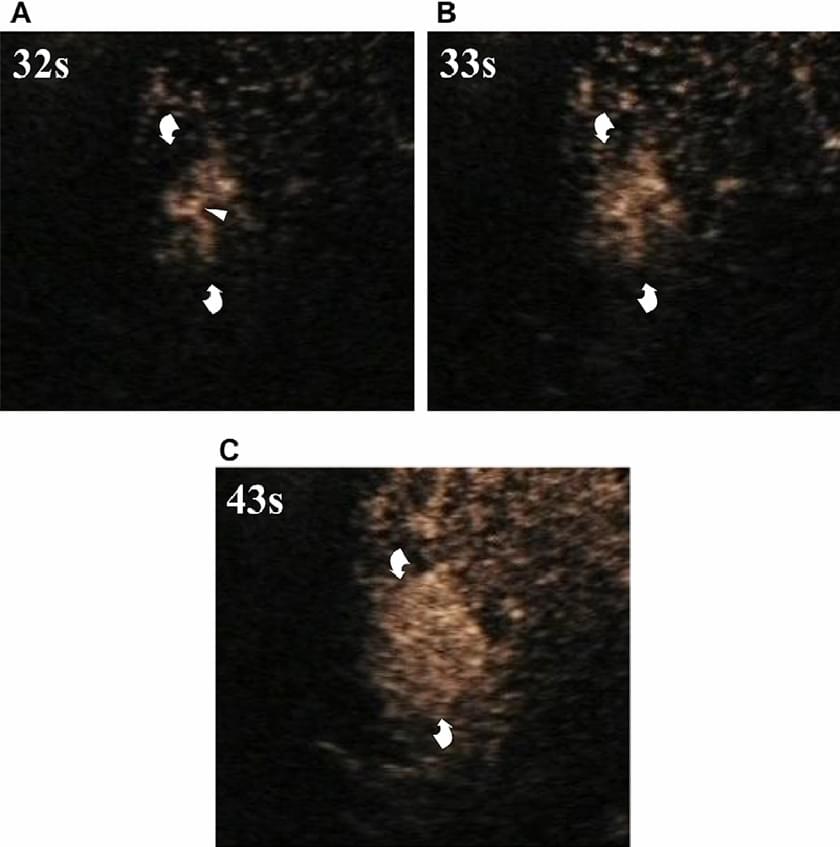
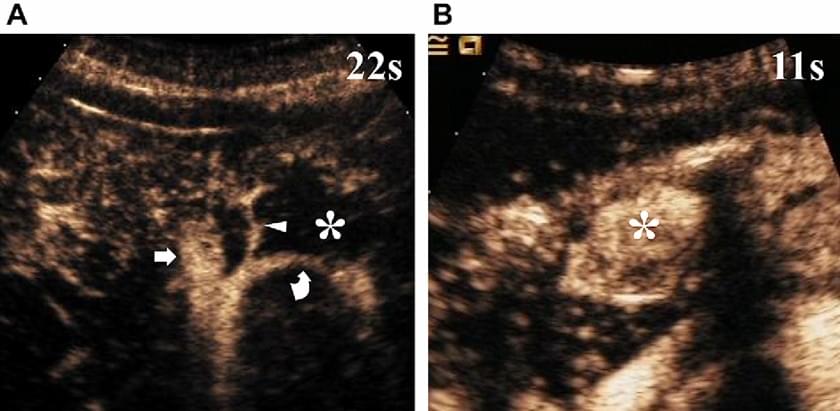
Ультразвукова картина осередкової вузлової гіперплазії (ОВГ) не є специфічною, хоча кольорова доплерографія дозволяє ефективно її охарактеризувати в 80% випадків, демонструючи центральну артеріальну судину, яка розгалужується у бік периферії самого ураження. ОВГ швидко посилюється від центру до периферії, і її картина змінюється кілька разів протягом декількох секунд. Центральна живильна артерія і радіальні гілочки можуть бути виключно оцінені в ранній артеріальній стадії через можливості УЗКП проводити аналіз в режимі реального часу (зобр. 3).
Зображення 3. ОВГ. (А) Центральна живляча артерія (наконечники стрілок) вузлика (вигнуті стрілки) віддає гілочки до периферії через 32 секунди після ін’єкції мікропухирців. Протягом 1 секунди посилення прогресує від центру до периферії (B). Повне однорідне посилення визначається протягом 10 секунд (С).
Протягом пізньої портальної стадії, ураження проявляється рівномірно гіперехогенним або ізоехогенним до печінки, за винятком очевидного гіпоехогенного центрального рубця (близько 25% випадків протягом синусоїдальної фази).
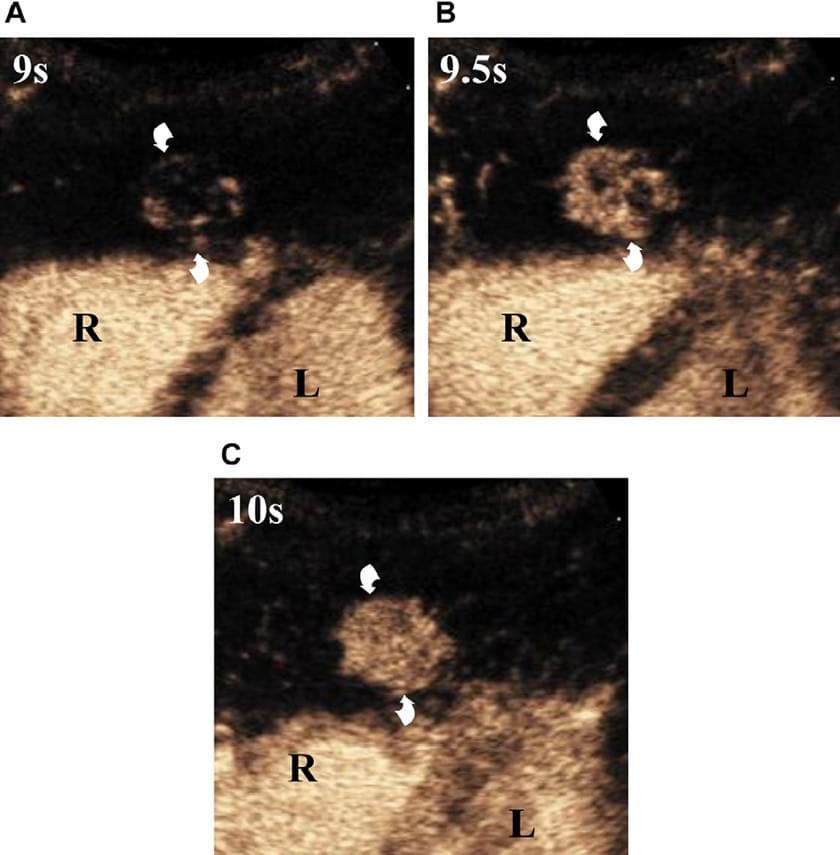
Аденома печінки (рис.4) очевидно підсилює свій малюнок доцентрово протягом ранньої артеріальної фази, і виявляється як гіперехогенне утворення, в порівнянні з навколишньою печінкою, а потім стає ізоехогенною, незначно гіпоехогенною або злегка гіперехогенною в портальній і в кінцевій фазах.
Зображення 4. Аденома печінки (вигнуті стрілки). Периферичні живлячі артерії визначаються через 9 секунд після ін’єкції мікропухирців (А). Посилення прогресує доцентрово з повним заповненням вузлика протягом 1 секунди (B, C).
R і L, правий і лівий шлуночки серця.
Посилення малюнка невеликої аденоми, як правило, однорідне, в той час як більш великі ураження мають гетерогенне підвищення контрастності, що викликано геморагічними і некротичними ділянками без накопичення контрасту. Відсутність центральної живлячої артерії і наявність ділянок без накопичення контрасту можуть допомогти в диференціальній діагностиці між аденомою і ВУП, хоча й існують перехресні симптоми для невеликих уражень.
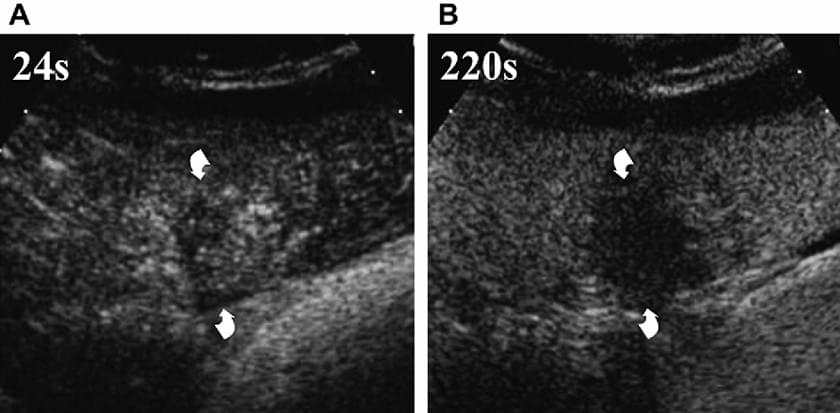
Метастази мають кровопостачання від неоангіогенних артеріальних судин, з невеликим або відсутністю портального компонента. Посилення артеріального компоненту відображає ступінь ангіогенезу пухлини, і таким чином деякі ураження проявляються як гіперваскуляризовані, а інші як гіповаскуляризовані. Метастатичні ураження можуть мати посилення малюнка у вигляді дифузного, гомогенного або гетерогенного зразку (зобр. 5), а також центральну некротичну ділянку без підсилення; дуже часто може бути виявлений типовий безперервний ободок різного розміру (зобр. 6) навколо ураження.
Зображення 5. Гіперваскуляризовані меастази раку легенів (вигнуті стрілки). 24 секунди після ін’єкції мікропухирців (А), показано гетерогенне посилення ураження, в основному по периферії. Посилення зникає під час наступних фаз, з вираженим вимиванням через 220 секунд (В).
Зображення 6. Гіповаскулярні метастази раку сечового міхура (стрілки). Артеріальна фаза сканування, показує посилення у вигляді обідка навколо ураження і кілька плям всередині.
Артеріальне посилення може бути транзиторним, і УЗКП виявляє значно більше гіповаскулярних уражень в порівнянні з КТ і МРТ, які не є методами дослідження в режимі реального часу. Навколоосередкове посилення може бути оцінене навколо ураження, яке, як правило, зберігається протягом від 30 до 60 секунд, і зникає в кінцевій фазі; це викликано перітуморальною десмопластичною реакцією, інфільтрацією запальних клітин і судинної проліферацією. Як правило, метастази в печінці «вимиваються» швидко – протягом артеріальної фази. На початку портальної фази зникає посилення ураження, і майже всі метастази стають більш гіпоехогенними в порівнянні з навколишньою паренхімою з посиленим малюнком, з більш-менш очевидними точками (які рясніють при оцінці в режимі реального часу), що, як вважається, є ознаками пухлинної мікроциркуляції. При правильній клінічній установці гіпоперфузійні ураження в порто-синусоїдальної фазі вважаються метастатичними, поки не доведено протилежне, незважаючи на їх гіперваскуляризовану або гіповаскуляризовану картину протягом артеріальної фази.
Посилення внутрішньо печінкової холангіоцелюлярної карциноми схоже на гіповаскуляризовані метастази; пухлина зазвичай представлена у вигляді точкового підсилення змінної інтенсивності протягом артеріальної фази і проявляється гіпоехогенним утворенням протягом портальної і кінцевої фаз. Також може спостерігатися навколоосередкове посилення, особливо у великих вузлах.
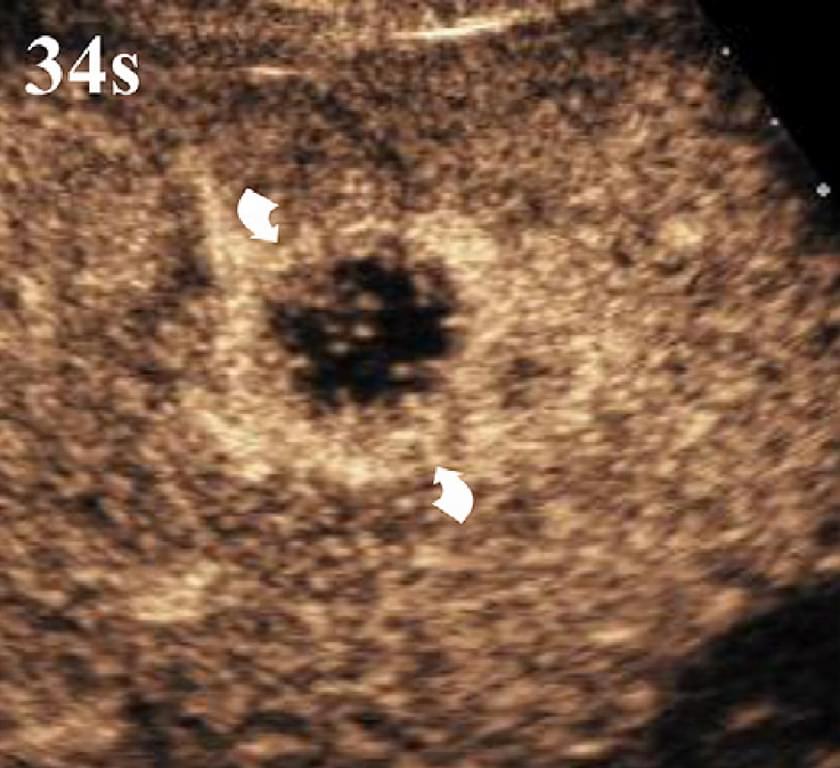
ГЦК, як правило, гіперваскуляризована пухлина. На початку артеріальної фази часто помітні периферичні живлячі судини, які розгалужуються до центру ураження у вигляді кошика (зобр. 7).
Зображення 7. ГЦК у пацієнта з цирозом (стрілки). Периферичні живлячі артерії визначаються на ранній артеріальній стадії, 15 секунд після ін’єкції мікропухирців (А). Наступні 5 секунд з інтенсивним і гетерогенним посиленням всього ураження (В).
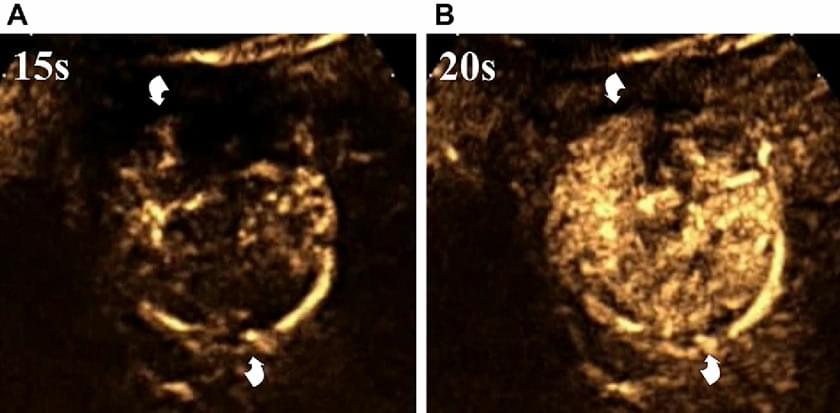
Посилення картини пухлини відбувається відразу, і воно зазвичай дифузне, інтенсивне і транзиторне. Посилення маленьких вузлів зазвичай однорідне, в той час як більш великі вузли, як правило, неоднорідні через некротичні зміни. Прогресивне вимивання спостерігається під час портальної і кінцевої фаз, при цьому воно, як правило, більш повільне, менш виражене і менш повне, ніж при метастазуванні (зобр. 8).
Зображення 8. ГЦК у пацієнта з цирозом (стрілки). Ураження має однорідне посилення контрастності під час артеріальної фази (А), яке зберігається протягом портальної фази (В). У кінцевій фазі (С) ураження майже ізоехогенне по відношенню до печінки.
У порівнянні з навколишньою паренхімою печінки, близько 60% ГЦК проявляються у вигляді гіпоехогенних утворень в портально-синусоїдальній фазі, в той час як 40% ГЦК, зокрема ті, які мають малий розмір або добре диференціюються, визначаються як ізоехогенні. Ця картина відрізняється від тієї, яку дає КТ та МРТ, при якій велика частина вузлів ГЦК проявляється гіперваскуляризацією в артеріальній фазі зображення і гіповаскуляризацією в портальній і, особливо, пізній стадії зображень. Отже, точність УЗКП в характеристиці дрібних вузлів ГЦК нижча, ніж при КТ та МРТ (якщо суворо дотримуватися діагностичних критеріїв з опублікованих керівництв). Близько 2% – 3% вузлів ГЦК погано васкуляризовані і мають точкове низьке контрастне посилення протягом різних судинних фаз. ГЦК, пов’язана із злоякісними тромбами в ворітній вені, як правило, посилюється в артеріальній фазі, в той час як цироз, пов’язаний з доброякісним тромбозом – ні.
Локальні області, позбавлені жирової тканини і локальні ділянки жирової тканини часто зустрічаються при жировій дистрофії печінки. Сумнівні пропущені області, а також локальні зміни ділянок жирової тканини можуть бути легко охарактеризовані за допомогою УЗКП. На відміну від вузлів печінки, ці псевдоураження посилюються зі швидкістю і інтенсивністю, рівними навколишнім тканинам печінки, і не відрізняються від неї (ізоехогенні) у всіх судинних фазах.
Абсцеси печінки, як правило, проявляються при сонографії, як неоднорідні і дещо гіпоехогенні утворення, з погано диференційованими полями. Після ін’єкції мікропухирців саме ураження і його внутрішня структура стають більш помітними. Периферія, як правило, посилюється, в той час як внутрішні, не посилені області, відповідають некротичним, розрідженим зонам. Мульфокальні абсцеси характеризуються посиленням сигналу перегородки із загальною картиною у вигляді бджолиних сот.
УЗКП може бути корисною в демонстрації істинного характеру солідної кісти печінки при звичайній ультрасонографії і в диференціальній діагностиці кістозних метастазів печінки від складних доброякісних кіст. Більшість доброякісних складних кіст не мають підвищення інтенсивності малюнка або навпаки, посилення у всіх судинних фазах, в той час як злоякісні кісти проявляються вимиванням контрасту в портальній і особливо синусоїдальній фазах (зобр. 9).
Зображення 9. Комплексна кіста печінки (вигнуті стрілки). (А) Базова сонографія показує гетерогенне округле ураження, яке має чітко окреслені поля, але без заднього посилення. (В) Після ін’єкції мікропухирців ураження не посилюється у всіх судинних фазах.
Всі дослідження, які порівнювали ефективність діагностики ультрасонографії і УЗКП, стверджують, що останнє покращує характеристику ВУП. Кількість правильних діагнозів збільшується з 60%-65% до 86%-95% після ін’єкції контрастної речовини, а диференціальна діагностика між злоякісними і доброякісними ураженнями покращується з 23%-68% до 92%-95%. У французькому перспективному багатоцентровому дослідженні 874 пацієнтів з 1034 вузлами, які не повною мірою були охарактеризовані при традиційній ультрасонографії або однофазній КТ, УЗКП дала чутливість 79% і специфічність 88% для диференціальної діагностики доброякісних і злоякісних уражень, і виявилася більш надійним дослідженням, ніж мультидетекторна КТ (МДКТ) і МРТ при оцінці внутрішньо- і міжспостережного узгодження. У німецькому багатоцентровому дослідженні 1349 пацієнтів з ураженням печінки з невизначеним діагнозом при традиційній ультрасонографії та енергетичній доплерографії, УЗКП показала 90% загальну точність, з 96% чутливістю до злоякісних уражень і 83% специфічність до доброякісних уражень. У серії з 88 гіпоехогенних ВУП при базовій ультрасонографії, УЗКП було точним в остаточній характеристиці 81% доброякісних уражень і 88% злоякісних уражень, що дозволило провести диференціальну діагностику між доброякісними і злоякісними ураженнями в 95% випадків.
Враховуючи високу специфічність, використання УЗКП дозволяє зменшити кількість біопсій печінки і досліджень другого рівня – КТ та МРТ, зокрема, для уражень з доброякісними ознаками. В аналізі досліджень на основі економічних витрат було показано, що УЗКП є найменш дорогим дослідженням другого рівня після базової ультрасонографії для діагностики доброякісних уражень печінки. УЗКП коштує менше, ніж КТ з контрастуванням, і особливо нижче ніж МРТ з контрастуванням. Алгоритм на основі УЗКП для діагностики ВУП, які не уточнені при базовій ультрасонографії є економічно більш ефективним, ніж алгоритм, який спирається на КТ або МРТ. Італійське багатоцентрове дослідження показало, що УЗКП є економічно ефективним для системи охорони здоров’я і шпиталів.
ВИЗНАЧЕННЯ ВУЗЛІВ У ХВОРИХ З ХРОНІЧНИМИ ЗАХВОРЮВАННЯМИ ПЕЧІНКИ
Розвиток ГЦК є найбільш серйозним ускладненням фіброзу і цирозу печінки. Ультрасонографія зазвичай розглядається як дослідження вибору для скринінгу ГЦК через її низьку вартість, доступність та неінвазивність. Кольорова доплерографія при оцінці васкуляризації ураження може бути ефективна, оскільки, як правило, ГЦК – гіперваскуляризоване утворення з переважанням периферичного артеріального кровотоку. Тим не менш, при використанні звичайних методів ультрасонографії виявляється високий відсоток ВУП у пацієнтів з хронічними захворюваннями печінки, природа яких не може бути чітко визначена.
УЗКП ефективне при оцінці васкуляризації вузлів, які виявляються випадково або під час динамічного спостереження за цирозом печінки. Канцерогенез печінки є багатостадійним процесом, який характеризується розвитком великої кількості доброякісних регенеруючих вузлів, які розвиваються в диспластичні вузли, і в кінцевому підсумку в ГЦК. Цей процес пов’язаний з поступовим зменшенням портального кровотоку і збільшенням неоангіогенного артеріального кровотоку. Близько 80% доброякісних регенеративних вузлів представлені у вигляді постійного точкового контрастного посилення і гіпоехогенних утворень в ході артеріальної фази, з подальшим посиленням, аналогічним навколишній паренхимі печінки. Решта 20% доброякісних вузлів, які, як правило, мають диспластичну будову при гістологічному аналізі, не можуть бути диференційовані від ГЦК. Коли ВУП виявляються при ультрасонографії у пацієнтів з хронічним захворюванням печінки, може бути виконана УЗКП для проведення диференціальної діагностики більшості випадків між передраковими і злоякісними вузлами, хоча й існують деякі перехресні ознаки.
УЗКП має обмежене значення при визначенні стадії у хворих з відомою ГЦК, і таким чином КТ або МРТ повинні завжди виконуватися для визначення поширення процесу і, зокрема, для виключення інших вузлів. Хоча більшість уражень, які видно при ультрасонографії, можна ефективно охарактеризувати за рахунок їх гіперваскуляризованого малюнка в артеріальній фазі, близько 40% з них ледь видно в портальній та пізній фазах. Отже, через коротку тривалість артеріальної фази провести дослідження всієї паренхіми печінки неможливо, тому завжди необхідне подальше дослідження для визначення стадії процесу.
ВИЯВЛЕННЯ МЕТАСТАЗІВ У ПАЦІЄНТІВ З ПОЗАПЕЧІНКОВИМИ ЗЛОЯКІСНИМИ ПУХЛИНАМИ
Сіро шкальна ультрасонографія і кольорова доплерографія мають обмежену точність, тому що ізоехогенні метастази і метастази менше одного сантиметра завжди важко виявити. Крім того, неметастатичні ураження іноді можна знайти у пацієнтів, які мають рак, і їх правильна характеристика є обов’язковою. УЗКП долає багато обмежень традиційної ультрасонографії у виявленні і характеристиці ВУП у онкологічних хворих.
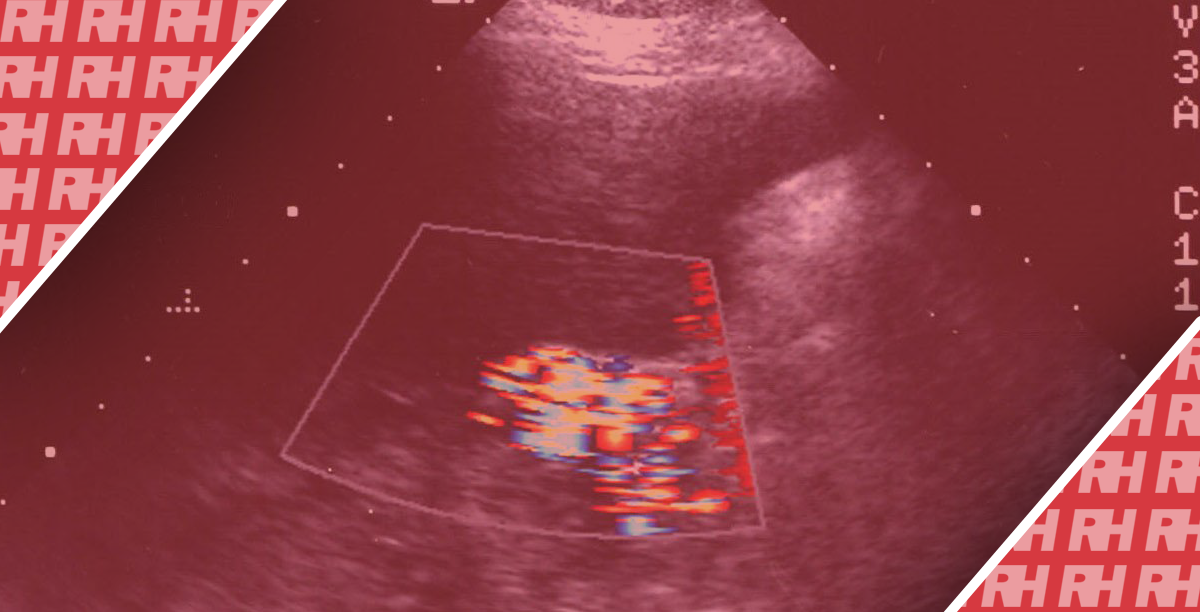
При використанні мікропухирців з низьким МІ режимом, печінку можна безперервно досліджувати протягом від 4 до 5 хвилин після болюсної ін’єкції. Практично всі метастази з’являються у вигляді гіпоехогенних утворень в порівнянні з навколишньою паренхімою в портальній та пізній фазах після ін’єкції мікропухирців, отже, при цьому достатньо часу для ретельного пошуку цих уражень (зобр. 10).
Зображення 10. Метастази раку товстої кишки. Ураження не видно при базовій ультрасонографії (А), тоді як воно добре визначається через 60 секунд після введення мікропухирців (В, стрілки).
Якщо всі відділи печінки будуть адекватно оглянуті при УЗКП, то дослідження в такому випадку є настільки ж ефективним, як КТ та МРТ у виявленні метастазів.
Quaia та ін. оцінювали 345 уражень за допомогою першого покоління УКЗ і деструктивного режиму, і 261 уражень за допомогою другого покоління УКЗ і недеструктивного режиму. Мікропухирці помітно підсилили чутливість для більшості виявлених уражень, при використанні обох модальностей УЗКП, від 40% до 46%, до 83% від 87% і, відповідно, при цьому не було знайдено статистично значущих відмінностей між діагностичною значимістю УЗКП і КТ. Konopke та ін. оцінювали 100 пацієнтів з підозрою на ураження печінки до лапаротомії і знайшли, що введення УКЗ поліпшили чутливість ультрасонографії для більшості виявлених пошкоджень з 53% до 86%, в той час як КТ досягло чутливості 76%. Oldenburg та ін. оцінювали 40 пацієнтів з відомим злоякісним процесом і принаймні 1 ураження печінки визначалося на базових ультрасонограмах. Ін’єкція УКЗ посилила чутливість ультрасонографії для виявлення уражень в порівнянні з еталонними процедурами від 69% до 90%. Крім того, УЗКП показала 13 уражень, які не були виявлені на вихідному зображенні.
Вартість гінералізованого використання мікропухирців для виключення метастазів у печінці у всіх пацієнтів з попереднім або поточним позапечінковим раком, ймовірно, надмірна. Тому необхідно виявляти субпопуляцію пацієнтів, які можуть отримати клінічну користь від цього дослідження. Наприклад, пацієнти, яким плануються хірургічні або інтервенційні процедури у зв’язку з метастазами печінки, можуть мати діагностичні переваги при комбінованому використанні КТ і УЗКП, оскільки оцінка метастатичного ураження у цих пацієнтів повинна бути якомога більш точною для того, щоб уникнути непотрібного лікування.
ОЦІНКА УРАЖЕННЯ ПЕЧІНКИ ПІСЛЯ ЛІКУВАННЯ
УЗКП ефективна для збільшення контрастності ураження і, отже, для наведення при діагностичних і терапевтичних пункціях ВУП, коли вони ледь помітні на сонограмі без посилення.
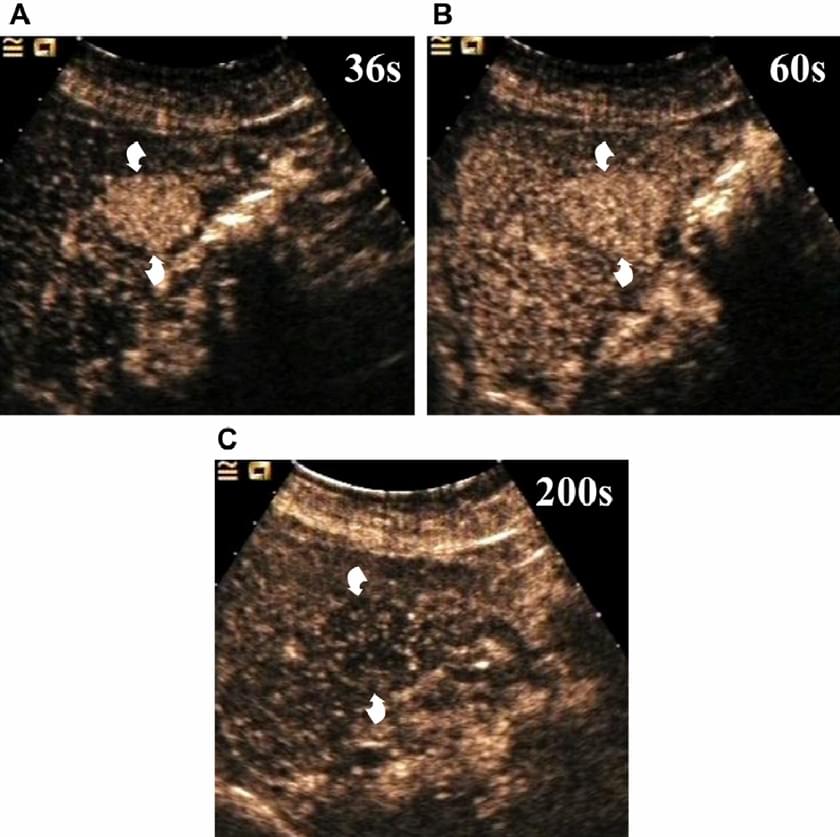
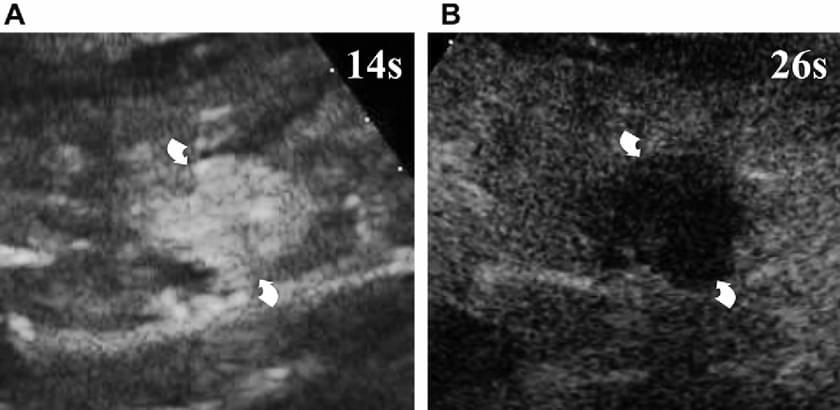
Черезшкірна абляція стала широко поширеним методом лікування неоперабельних пухлин печінки, особливо ГЦК і метастазів раку прямої кишки. У цих випадках оцінка утворень після лікування є важливою, тому що виявлення резидуальної, життєздатної пухлинної тканини, як правило, вказує на необхідність повторного лікування. КТ і МРТ, як правило, використовуються для оцінки реакції на абляцію. Однак, недавнє дослідження показало, що УЗКП є настільки ж ефективним, як і КТ у виявленні залишкової або рецидивуючої пухлини після абляції. У деяких установах УЗКП використовується під час самої процедури абляції, щоб негайно продемонструвати ефективність процедури. В інших установах УЗКП використовується через кілька днів після абляції (зобр. 11), для раннього виявлення залишкової пухлини і наступного планування повторного лікування.
Зображення 11. Вузли ГЦК (стрілки), оброблені за допомогою радіочастотної абляції. Ураження має інтенсивне і однорідне посилення (А – скани, отримані через 14 секунд після ін’єкції контрасту) до лікування, поступово воно стає повністю аваскулярним (В – скани, отримані через 26 секунд після ін’єкції контрасту) при УЗКП дослідженні, яке виконано через 25 днів після черезшкірної радіочастотної абляції.
УЗКП є особливо ефективною для наведення при прицільній абляції залишкового або рецидивуючого пухлинного утворення в некротичних вузлах.
УЗКП виявилася корисним методом для ранньої оцінки терапевтичного ефекту після внутрішньо артеріальної транскатетерної хемоемболізаціі. КТ широко використовується для оцінки цих пацієнтів, але при цьому необхідний мінімальний інтервал від 15 до 20 днів, і можуть виникати труднощі через артефакти маслянистих контрастних речовин. Разом з MРТ, УЗКП є ефективною альтернативою.
Ще одним важливим показанням для УЗКП є подальше динамічне спостереження за пацієнтами, які перенесли системну хіміотерапію стандартними препаратами. УЗКП може бути особливо корисною при використанні препаратів, які пригнічують ангіонеогенез пухлини. У цих хворих антиангіогенні препарати, як очікується, редукують кровотік в пухлині, що може бути виявлено за допомогою УЗКП, але не видно при базовій сонографії. Ураження, які піддавали впливу антиангіогенних препаратів, зменшувалися в розмірі повільно, але при УЗКП можна продемонструвати зменшену васкуляризацію вже через кілька днів після лікування, що дозволяє провести ранню диференціацію між пацієнтами, які відповідають на терапію, і які ні.
НИРКА
УЗКП нирки є новим полем дослідження для УКЗ. Мікропухирці можуть бути введені без урахування видільної функції нирок, а інтенсивне посилення ниркової паренхіми дозволяє легко виявити гіпоперфузійні ураження, такі як інфаркти або крововиливи.
НИРКОВА ІШЕМІЯ
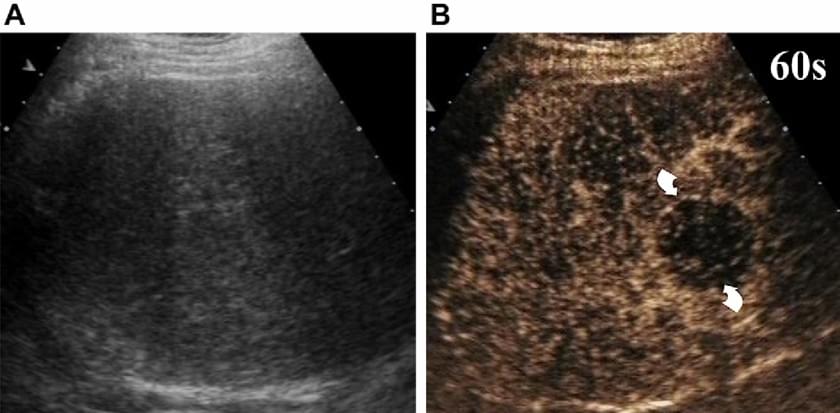
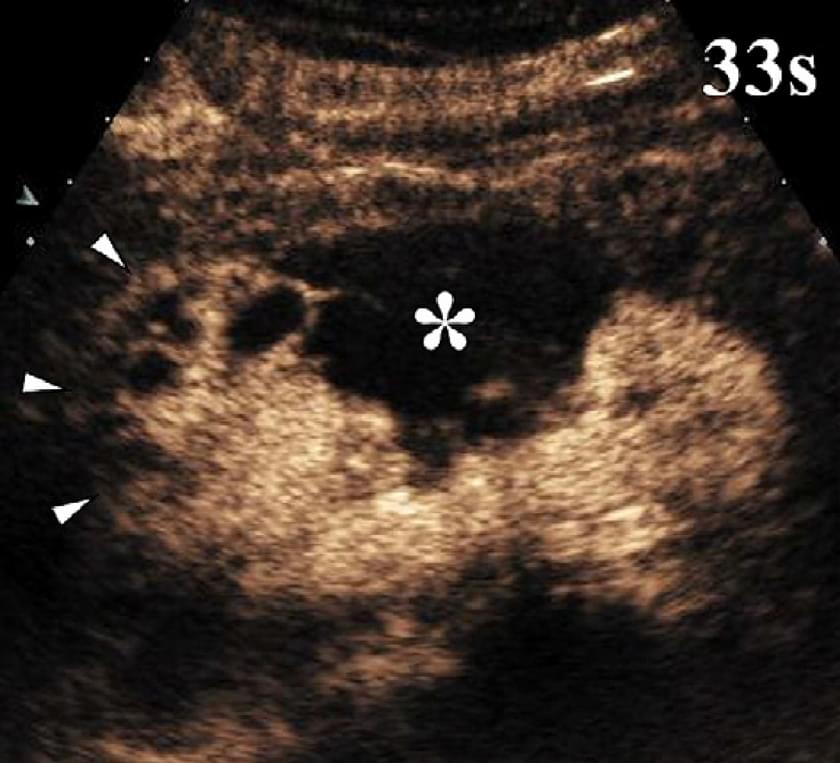
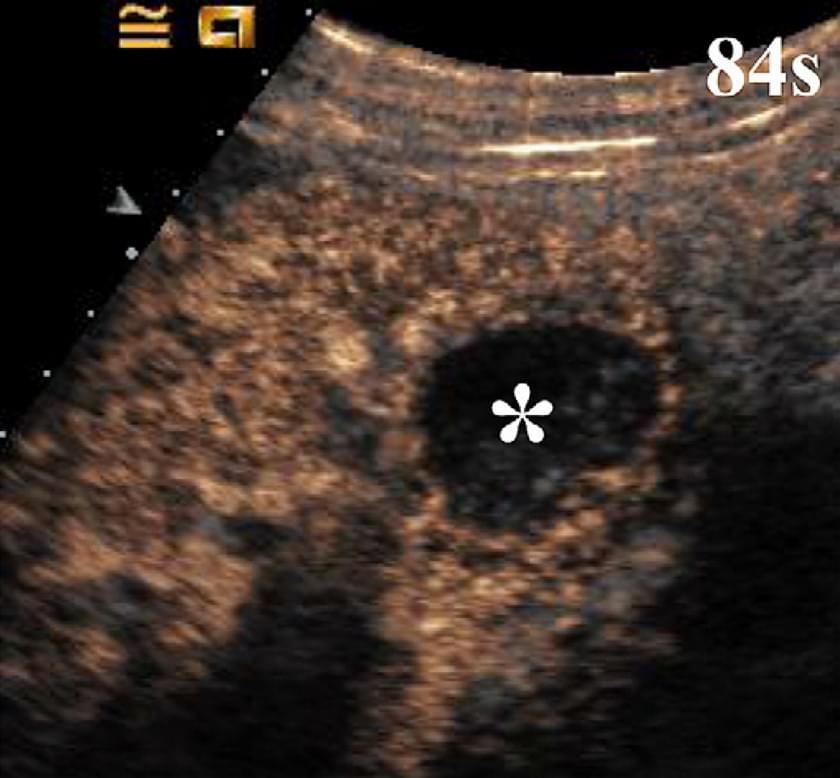
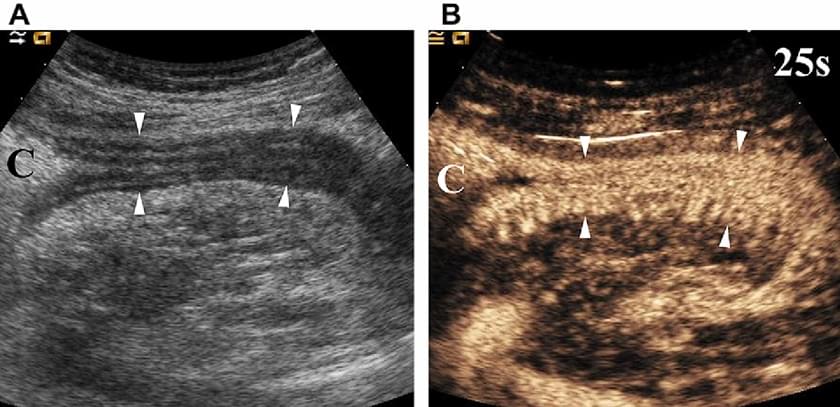
Доплерографія є методом першої лінії в виявленні дефектів ниркової перфузії, але вона має чіткі обмеження через нечутливість при низькій швидкості і низько амплітудних потоках. З’ясовано, що УЗКП є ефективне для відображення локальних дефектів перфузії нирок в експериментальних дослідженнях. Недавні дослідження показали діагностичну ефективність у виявленні ниркової ішемії, яка наближається до КТ з контрастуванням. Крім того, відмінна просторова роздільна здатність УЗКП дозволяє ефективно диференціювати ниркову ішемію і гострий кірковий некроз, який проявляється як непосилена область кори зі збереженою васкуляризацією у зоні воріт нирки (зобр. 12).
Зображення 12. Гостра ниркова ішемія після тромбоемболії у пацієнта з фібриляцією передсердь. УЗКП через тридцять три секунди після ін’єкції мікро пухирців показує непосилену область клиноподібної форми (*) в середній частині нирки. Маленькі, непосилені області кори (наконечники стрілки), також визначаються у верхньому полюсі нирки, що узгоджується з іншими зонами кіркового інфаркту.
Інше важливе застосування УЗКП у пацієнтів з нирковою ішемією – це диференціальна діагностика між неперфузійованими, інфарктними областями (необоротними) і гіпоперфузійованими зонами паренхіми (оборотними). Обидва ці стани проявляються при кольоровій доплерографії, як області зі слабким кольоровим сигналом, але тільки зони інфаркту мають слабке контрастне посилення після введення УКЗ.
ЩІЛЬНІ УРАЖЕННЯ НИРКИ ТА ПСЕВДОПУХЛИНИ
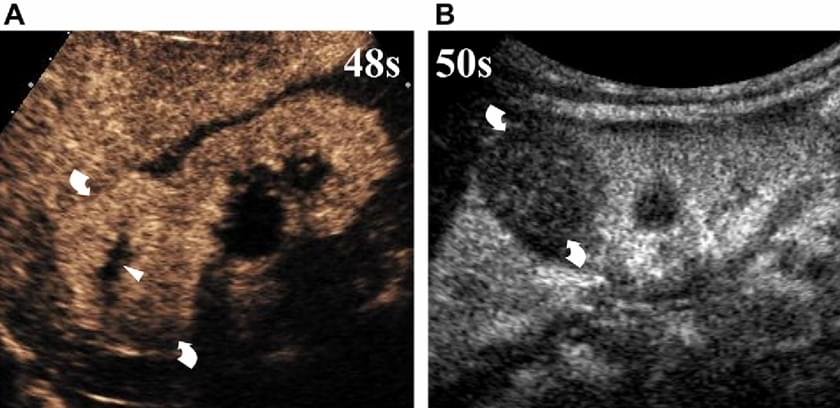
Після введення мікропухирців, щільні пухлини нирок проявляються у вигляді дифузного, гомогенного або гетерогенного посилення контрастності в початковій кортикомедулярній фазі, часто гіперваскуляризовані, і мають змінне контрастне посилення в інших фазах, як правило, подібно нормальній нирковій паренхімі. Посилення обмежене твердими життєздатними областями і виключає внутрішньо пухлинні аваскулярні некротичні, геморагічні або кістозні компоненти. Деякі ураження, як правило, папілярні або хромофобні пухлини, але також і метастази і приблизно 13% світлоклітинних карцином, посилюються менше, ніж навколишня паренхіма у всіх судинних фазах (зобр. 13).
Зображення 13. УЗКП картина щільних пухлин нирок (вигнуті стрілки). Зображення отримані через 48 секунд (А) і 50 секунд (В) після ін’єкції мікропухирців, відповідно. (А) Світлоклітинна карцинома має картину інтенсивного посилення і центральну некротичну область без посилення (стрілка). Посилення хромофорної пухлини (В) менш виражене, ніж навколишня ниркова паренхіма.
У зв’язку з тим, що посилення багатьох пухлин нирок аналогічно нирковій паренхімі в більшості судинних фаз, частота виявлення малих пухлин навряд чи буде значно поліпшена при введенні контрасту.
Ascenti та ін. припустили, що УЗКП ефективне для візуалізації псевдокапсули пухлини, яка проявляється після ін’єкції мікропухирців, як ободок посилення поблизу ураження, який збільшується в пізній фазі дослідження.
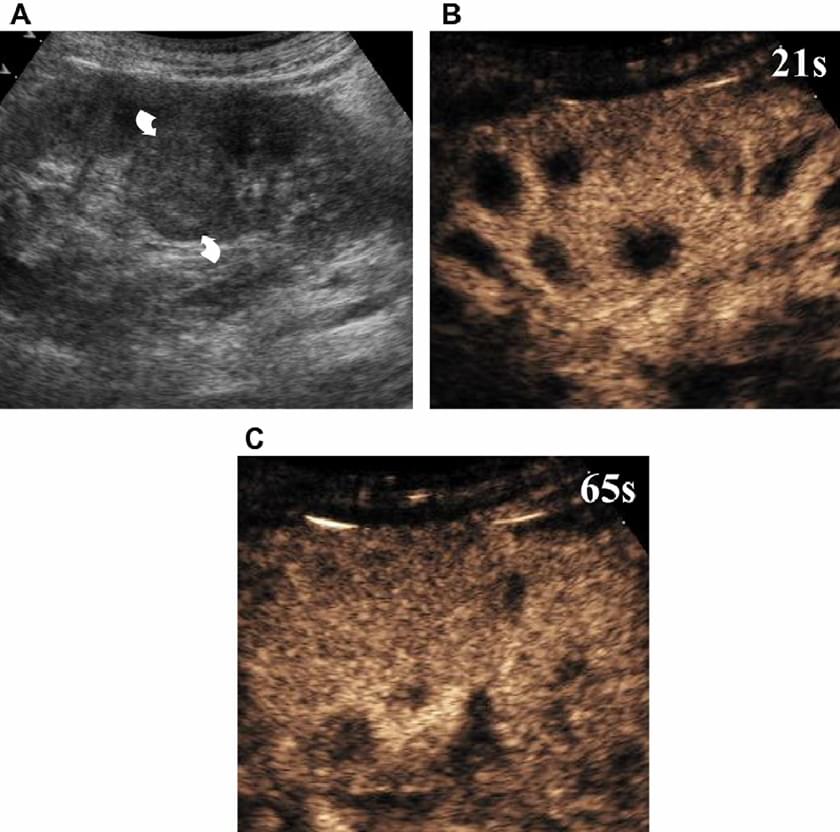
Незалежно від ступеня васкуляризації, судинний малюнок пухлин нирок відрізняється від ниркової паренхіми. Ця різниця може бути корисною для диференціальної діагностики нормальних варіантів від реальних вогнищевих уражень (зобр. 14).
Зображення 14. Псевдопухлина нирки. Базова ультрасонографія (А) показує сферичне зображення в середній частині нирки (стрілки), що припускає наявність пухлини нирки. УЗКП показує характеристики посилення ідентичні іншій частині ниркової паренхіми через 21 секунду (В) і 65 секунд (С) після ін’єкції мікропухирців, що підтверджує наявність псевдопухлини.
Попередні дослідження показують, що УЗКП більш чутлива, ніж КТ з контрастуванням для виявлення кровотоку в гіповаскуляризованих ураженнях. Tamai та ін. продемонстрували посилення в 5 гіповаскуляризованих пухлинах нирок з двозначним результатом при КТ з контрастуванням
УЗКП має обмеження: глибина місця ураження, переміщення газів кишківника, наявність кальцифікації стінки і великий розмір – все це перешкоджає повноцінній оцінці пухлини.
КІСТОЗНІ УРАЖЕННЯ НИРОК
Чутливість УЗКП у виявленні кровотоку в гіповаскуляризованих ниркових ураженнях дозволяє провести адекватну диференціальну діагностику між солідними пухлинами і атиповими кістозними ураженнями. УЗКП дозволяє охарактеризувати кістозні ураження нирок, як доброякісні або злоякісні з принаймні тією ж точністю, що і КТ з контрастуванням (зобр. 15).
Зображення 15. УЗКП характеристика кістозних уражень нирок (вигнуті стрілки) у 3-х різних пацієнтів. (А) Мінімально ускладнена доброякісна кіста характеризується тонкою, посиленою стінкою (пряма стрілка) з правильними краями і тонкою перегородкою (наконечники стріл). (В) Невизначене ураження нирок, яке вимагає хірургічного видалення через дещо потовщені нерівномірні перегородки і товсту посилену стінку. С – явна злоякісна кістозна пухлина з посиленою, неправильної форми стінкою і вегетації (*).
Quaia та ін. проаналізували серію з 40 складних кістозних ниркових утворень. Три радіологи отримали загальну діагностичну точність (80% -83%) при УЗКП вище, ніж КТ при визначенні злоякісності. Зокрема, УЗКП була більш чутливою, ніж КТ у виявленні посилення стінки кісти, перегородок і щільних компонентів. Park та ін. оцінили за допомогою КТ і УЗКП 31 патологоанатомічне підтверджене кістозне утворення нирок з використанням класифікації Bosniak. Діагностичний рівень точності УЗКП і КТ для злоякісного ураження був 74% і 90%, відповідно. У 26% ураженнях існувало розходження в балах класифікації Bosniak, що були скориговано при УЗКП. Крім того, для 6 уражень, щільні компоненти були виявлені при УЗКП, але не за допомогою КТ. Ascenti та ін. провели перспективне порівняння 40 послідовних кістозних утворень нирок за допомогою УЗКП і КТ з використанням класифікації Bosniak. Для УЗКП і КТ, міжспостережницьке узгодження було високим, і спостерігалося повне узгодження між УЗКП і КТ при диференціальній діагностиці хірургічних та нехірургічних кіст.
УЗКП повинна бути використана для характеристики пухлин нирок зі складною кістозною структурою, за умови, що ураження може бути досліджене адекватно. КТ і раніше необхідно з метою визначення стадії. Через свою доступність та відсутність іонізуючого випромінювання, УЗКП добре підходить для подальшого динамічного спостереження при нехірургічному випадку ураження.
НИРКОВІ ТРАВМИ
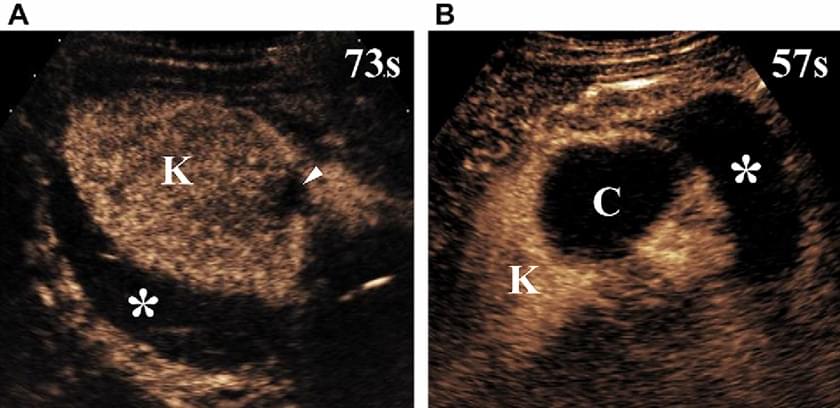
Після введення мікропухирців, ниркові пошкодження виглядають як дефекти васкуляризації в паренхімі, в яку добре постачається кров (зобр. 16).
Зображення 16. УЗКП картина травм нирок у 2 різних пацієнтів. Зображення отримані через 73 секунди (А) і 57 секунд (В) після ін’єкції мікропухирців, відповідно. (А) Невеликий розрив ниркової паренхіми представлений як дефект перфузії, який перериває нирковий профіль (стрілки) з відповідною періренальною гематомою (*). (В) Розрив ниркової кісти, яка проявляється у вигляді овалу і непосиленої зони з чітко окресленими межами, що сполучається з паранефральною гематомою (*).
К – нирка; С – кіста.
Переривання ниркового профілю узгоджується з розривом. Розрив ниркової артерії або тромбоз, представлені у вигляді відсутності перфузії паренхіми. Локальна екстравазація УКЗ передбачає активну кровотечу.
Хоча ін’єкції УКЗ покращують чутливість сонографії для ідентифікації ниркової травми, роль цього методу в клінічній практиці є спірною. Травма системи збірних канальців нирок може бути пропущена при УЗКП через відсутність сечової екскреції мікропухирців. Крім того, важка травма пацієнтів навіть при стабільній гемодинаміці, як правило, вимагає панорамної оцінки з застосуванням КТ всіх органів черевної порожнини. УЗКП може замінити або інтегруватися в ультрасонографічне дослідження при сортуванні гемодинамічно стабільних пацієнтів з незначними травмами черевної порожнини. Однак, Poletti та ін. виявили, що навіть в оптимальних умовах травми паренхіматозних органів можуть бути пропущені. Досвід авторів відповідає результатам Valentino і його колег, які не пропустили жодного значного пошкодження нирок у їх дослідженні. Невеликі та невиражені травми можуть бути іноді втрачені з уваги, особливо у пацієнтів з ожирінням, і коли паранефральна гематома невелика або відсутня. УЗКП можуть бути використані в подальшій оцінці ниркових ушкоджень, які ведуться консервативно для того, щоб зменшити частоту використання КТ.
НИРКОВА ІНФЕКЦІЯ
Ниркові абсцеси відображаються ефективно після ін’єкції УКЗ, оскільки вони не мають внутрішньопорожнинних судин, які руйнуються або зміщуються в результаті процесу розплавлення (зобр. 17).
Зображення 17. Нирковий абсцес (*) представлений як округле, гіпоехогенне ураження з тонким внутрішнім дебрісом (продукти деструкції), але при цьому визначається слабке посилення через 84 секунди після ін’єкції контрасту.
Фокальний гострий пієлонефрит може поліпшити свою візуалізацію після ін’єкції мікропухирців, якщо ниркові судини здавлені при супутньому набряку, що виявляє гіпоперфузійовані зони. Mitterberger та ін. оцінювали проспективно 100 послідовних пацієнтів з клінічними симптомами, які вказували на гострий пієлонефрит і показали, що УЗКП і КТ мають майже однакову чутливість та специфічність для виявлення ниркових змін.
УЗКП І НИРКОВА АБЛЯЦІЯ
Радіочастотна абляція стає альтернативною терапією у хворих з нирково-клітинною карциномою, які не є кандидатами на операцію. Попереднє дослідження припускає, що УЗКП може бути корисним у виявленні залишкової пухлини після видалення. Meloni та ін. оцінили за допомогою УЗКП і КТ або МРТ 29 пацієнтів з 30 пухлинами нирок до і після радіочастотної абляції. Вони виявили, що при гіперваскулярних пухлинах, точність УЗКП у виявленні локальних зон рецидиву пухлини або прогресії, є аналогічною для КТ і МРТ.
ПЕРЕСАДЖЕНА НИРКА
Fischer та ін. визначили затримку в посиленні ниркової кори у пацієнтів з відторгненням трансплантата. Цей висновок, однак, був також підтверджений у пацієнтів з великими паранефральними гематомами. Ще одне попереднє дослідження показало, що при гострому тубулярному некрозі кортикально/мозкове співвідношення ниркового об’єму крові і середній час проходження, були значно нижчі, порівняно з контрольною групою. Вплив на виявлення цих змін гемодинаміки в лікуванні цих пацієнтів з функціонуючою трансплантованою ниркою не встановлено.
СЕЛЕЗІНКА
Деякі УКЗ виявляють специфічне гепатолієнальне поглинання після їх зникнення з кровоносного басейну. SonoVue – мікропухирці, які найбільш широко використовується в Європі, викликають специфічне посилення селезінки, яке триває довше, ніж в кровоносному басейні і посилення печінкової фази.
ЕКТОПІЧНА ТКАНИНА СЕЛЕЗІНКИ
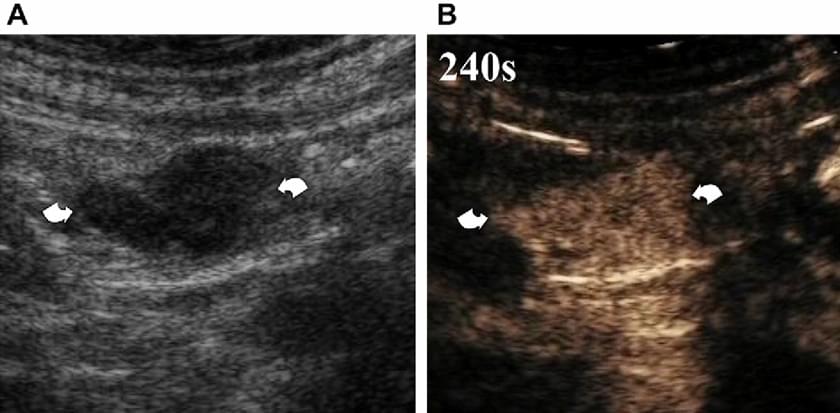
Кілька досліджень показали, що УЗКП ефективна для характеристики ектопічної тканини селезінки. Диференціальна діагностика між злоякісними і доброякісними ураженнями особливо проблематична, коли перитонеальний вузол визначається у пухлинних хворих, які піддалися спленектомії. SonoVue має властивості характеризувати тканину селезінки через його здатність до специфічного поглинання селезінкою (зобр. 18).
Зображення 18. Острівець перитонеального спленозу (стрілки) у пацієнта з множинним ендокринним непластичним синдромом, у якого в анамнезі спленектомія після травми. (А) Базова ультрасонографія показує овальний, часточковий вузлик з неспецифічним проявом. (В) Після введення мікропухирців вузлик, як правило, показує картину поглинання мікропухирців протягом 240 секунд після ін’єкції.
Лімфатичні вузли воріт селезінки, ураження надниркових залоз, пухлини хвоста підшлункової залози, метастатичні депозити та інші ураження мають знижене посилення в кінцевій фазі.
ДЕФЕКТИ ПЕРФУЗІЇ СЕЛЕЗІНКИ
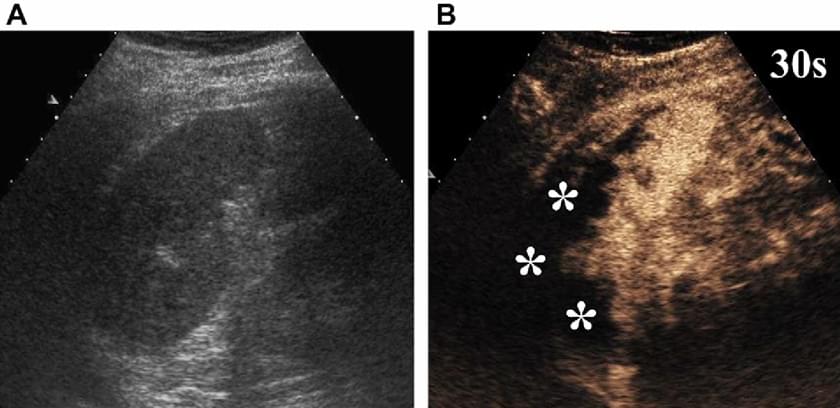
При гострому інфаркті селезінки УЗКП точно демонструє форму і протяжність ішемічної області, як зону зі слабким накопиченням контрасту. УЗКП ефективна тоді, коли інфаркт ледь впізнаний на базовій ультрасонограмі, або коли він імітує осередкове ураження (зобр. 19).
Зображення 19. Гострий інфаркт селезінки в результаті септичної емболії у пацієнта з інфекцією протезу аортального клапана і бактеріальним ендокардитом. (А) На базовій ультрасонограмі не визначаються аномалії паренхіми селезінки. (В) УЗКП зображення, отримане через 30 секунд після ін’єкції мікропухирців, показує більшу, неперфузійовану область (*) за участю купола селезінки.
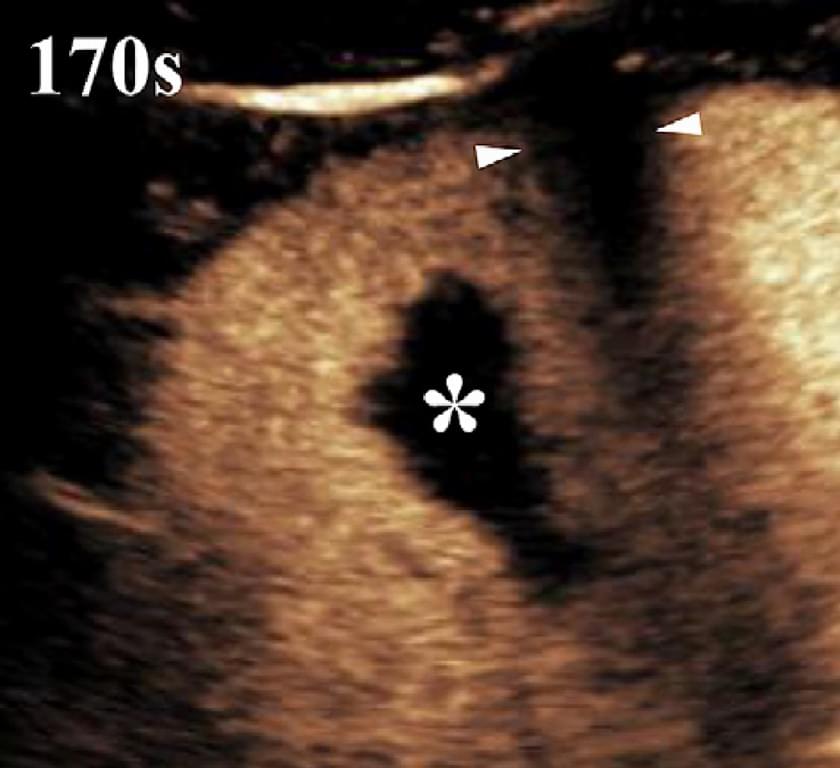
За даними Valentino та ін. чутливість УЗКП для виявлення пошкоджень селезінки наближається до 100%, а відповідно до Poletti та ін., однак, чутливість нижче, і хірургічні травми селезінки можуть бути пропущені. Травми селезінки з’являються, як паренхіматозні ділянки зі слабким контрастуванням. Розриви проявляються, як гіпоехогенні смуги, лінійні або розгалужені, перпендикулярні до капсули селезінки, хоча рвані і забиті зони та гематоми паренхіми виявляються, як неоднорідні гіпоехогенні області без ефекту пухлини або зсуву судин (зобр. 20).
Зображення 20. Гематома селезінки після тупої черевної травми представлена, як нерівномірна частина селезінкової паренхіми (*) з недостатнім накопиченням контрасту через 170 секунд після введення мікропухирців. Наконечники стріл вказують на акустичні тіні, що утворюються ребрами.
У пацієнтів з селезінковою травмою УЗКП може також відображати дані, які не проявляються при звичайній візуалізації на ультрасонограмі, у тому числі дефекти перфузії і екстравазація контрасту. Згідно досвіду авторів, як неінвазивна методика біля ліжка хворого і легко відтворена техніка, УЗКП ідеально підходить для подальшого динамічного спостереження при консервативному лікуванні травм селезінки, особливо у молодих пацієнтів, оскільки це зменшує кількість КТ.
ЛОКАЛЬНІ УРАЖЕННЯ СЕЛЕЗІНКИ
Контрастні мікропухирці можуть бути ефективні у визначенні тонкостінної кісти селезінки і в підтвердження відсутності посилення в осередку ураження. Гемангіома може бути представлена у вигляді сферичного посилення, так само як і в печінці або частіше з однорідним, постійним посиленням. Великі ураження з кістозним/некротичним/тромботичним компонентом, однак, можуть також мати гетерогенне посилення. Гамартома селезінки проявляється з варіабельним посиленням і часто не відрізняється від гемангіом або іншої селезінкової патології. Нерівномірне периферичне посилення характерно для лімфоми, а саме ураження проявляється як чіткий дефект наповнення у пізній фазі. При метастазах в селезінці мікропухирці можуть показати змінне периферичне посилення, при цьому такі осередки виявляються як дефекти наповнення в оточенні звичайної паренхіми селезінки. Можуть бути виявлені метастази, які не видимі на вихідних ультрасонограмах, за рахунок збільшення їх контрастності.
ПЕРЕДМІХУРОВА ЗАЛОЗА
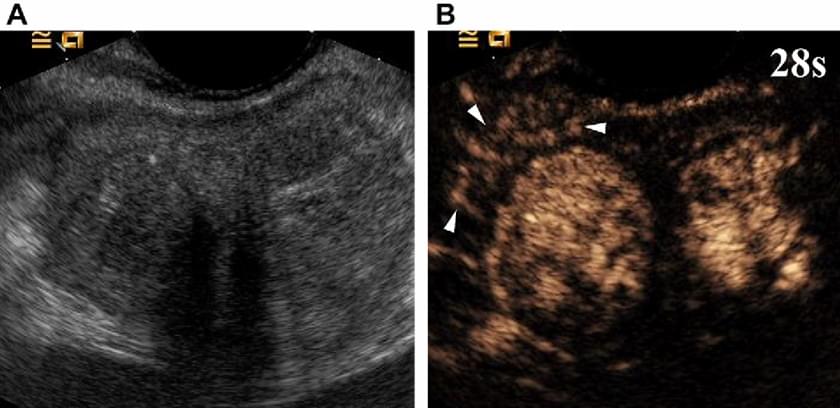
Наявність явного зв’язку між зростанням мікроваскуляризації і раком простати припускає, що використання УЗКП має значно поліпшити виявлення пухлини (зобр. 21).
Зображення 21. Зовнішній вигляд раку простати при УЗКП. (А) Базове трансректальне ультразвукове дослідження простати не вказує на локальні зміни у периферійній частині залози. (В) через 28 секунд після ін’єкції мікропухирців виявлена гіперваскуляризована зона в правій частці простати (стрілки). При біопсії був знайдений рак.
Крім того, оскільки збільшена щільність мікросудин корелює з метастатичним процесом і специфічним виживанням, рак, який виявлено за допомогою техніки візуалізації з контрастним підсиленням, ймовірно є більш агресивним. Кілька досліджень показали поліпшення частоти виявлення клінічно значущого раку простати з використанням УЗКП в якості техніки наведення для прицільної біопсії і виявлення раку передміхурової залози у пацієнтів з попередньо негативною біопсією, але з впевнено зростаючим рівнем простат-специфічного антигену (ПСА). Остаточна чутливість техніки, однак, є змінною величиною і, отже, УЗКП не може бути рекомендована на даний час у якості рутинної процедури.
Попереднє дослідження показує, що УЗКП також може бути ефективна при оцінці гемодинаміки простати у відповідь на терапевтичне лікування. У пацієнтів з раком простати кількісний аналіз інтенсивності сигналу після введення мікро пухирців Levovist (Шерінг, Берлін, Німеччина) показав, що після гормонального лікування, зменшення інтенсивності сигналу корелює зі змінами середнього рівня ПСА. Призначення тадалафілу, інгібітора фосфодіестерази 5 типу, для пацієнтів з доброякісною гіперплазією призвело до збільшення піку посилення і площі під кривою, яка відображає зміни у кровопостачанні передміхурової залози.
НИЖНІ СЕЧОСТАТЕВІ ШЛЯХИ
Були розроблені методи оцінки везікоуретрального рефлюксу. Після катетеризації сечового міхура останній заповнюється фізіологічним розчином до тих пір, поки у пацієнта з’являється бажання мочитися, а потім додавалися УКЗ. Рефлюкс діагностується тоді, коли мікропухирці виявляються в сечоводі або нирковій мисці. Зареєстрована хороша кореляція із звичайною цистоуретрографію і радіонуклідними дослідженнями.
УЗКП дозволяє оцінити прохідність маткових труб без опромінення пацієнта іонізуючою радіацією. Після внутрішньоматкової ін’єкції можуть бути оцінені прохідність через труби і виливання в черевну порожнину. При цьому була показана значна кореляція з результатами звичайних методів дослідження.
Попередні дослідження показують, що у пацієнтів, з травмою калитки УЗКП допомагає в оцінці пошкодження тканин яєчок та ідентифікації розриву білкової оболонки. Крім того, УЗКП покращує оцінку ішемічних областей, перекрут яєчка і абсцедування. Гіповаскулярні пухлини яєчок, які необхідно видаляти хірургічно, можуть бути віддиференційовані від повністю безсудинних уражень, таких як складні кісти, які можуть лікуватися консервативно.
У візуалізації статевого члена УЗКП ефективна в оцінці вроджених аномалій, травм, ішемії, фіброзу і виявлення ізоехогенних метастазів. Методика також може бути використана для оцінки прохідності шунтів у пацієнтів з ішемічним приапізмом, які піддалися хірургічному шунтуванню.
Новоутворення сечового міхура мають явне посилення в артеріальній фазі, яке зберігається у наступних фазах. УЗКП може бути ефективне для виявлення пухлини в дивертикулі і для диференціальної діагностики гіпомобільності тромбу пухлинної тканини. У попередньому дослідженні Caruso та ін. з’ясували, що УЗКП дозволяє відрізняти різні шари стінки сечового міхура і, таким чином, допомагає диференціювати поверхневі пухлини сечового міхура від тих, які проникають в м’язовий шар.
ПІДШЛУНКОВА ЗАЛОЗА
ЗАПАЛЬНІ ЗАХВОРЮВАННЯ ПІДШЛУНКОВОЇ ЗАЛОЗИ
Koito та ін. визначили, що УЗКП покращує діагностику запальних захворювань підшлункової залози. Ідентифікація регіонарного некрозу паренхіми, який з’являється як аваскулярна область після ін’єкції УКЗ, є більш надійною при УЗКП, ніж при базовій ультрасонографії. УЗКП ефективна в диференціальній діагностиці запальних від пухлинних утворень підшлункової залози. Характеристики посилення, які схожі з прилеглою паренхімою підшлункової залози, є ознаками процесу запального походження. Ці характеристики особливо корисні у пацієнтів з формуванням пухлиноподібного панкреатиту, а також з аутоімунним панкреатитом.
СОЛІДНІ ПУХЛИНИ ПІДШЛУНКОВОЇ ЗАЛОЗИ
Протокова аденокарцинома, як правило, гіповаскулярна у всіх судинних фазах. У порівнянні з сіро шкальною ультрасонографією, за допомогою УЗКП виходить чітке відображення країв пухлини, та більш ефективне визначення величини і співвідношення з періпанкреатичними судинами (зобр. 22А).
Більшість ендокринних пухлин мають швидке інтенсивне посилення в ранніх фазах, за винятком некротичних областей всередині самого ураження (зобр. 22 В).
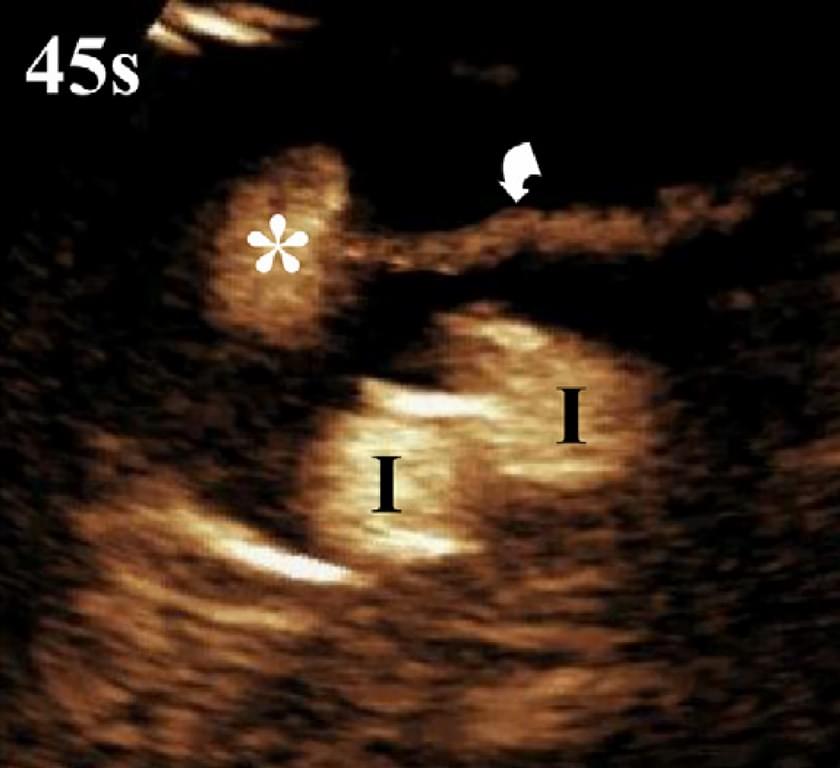
Зображення 22. Солідні пухлини підшлункової залози у 2-х різних пацієнтів. Зображення отримані через 22 секунди (А) і 11 секунд (В) після ін’єкції мікропухирців, відповідно. (А) Протокова аденокарцинома представлена як ураження зі слабким посиленням (*), що інфільтрує селезінкову артерію (вигнута стрілка) і ліву шлункову артерію (стрілка), просвіт якої звужений. Пухлина також контактує з печінковою артерією (пряма стрілка). (В) Гастринома являє собою овальний вузол (*) з інтенсивним і однорідним посиленням.
Функціонуючі нейроендокринні пухлини можуть бути гіповаскулярними. Здатність УЗКП у візуалізації васкуляризації ендокринної пухлини покращує ідентифікацію і характеристику цих ушкоджень, у порівнянні зі звичайною ультрасонографією і кольоровою доплерографією.
КІСТОЗНІ ПУХЛИНИ ПІДШЛУНКОВОЇ ЗАЛОЗИ
Диференціальна діагностика між серозною і муцинозною цистоаденомою підшлункової залози має вирішальне значення, оскільки перша, як правило, доброякісна, тоді як остання повинна бути видалена хірургічним шляхом. УЗКП покращує характеристику мікрокістозної серозної цистоаденоми, яка представлена кількома невеликими кістозними просторами, які розділені тонкими перегородками з чітко визначеними краями і центральним рубцем. Менш характерні олігокістозні і макрокістозні типи серозної цистоаденоми, які мають характеристики, що відрізняються від інших макрокістозних пухлин підшлункової залози.
У пацієнтів з внутрішньопротоковою папілярно-муцинозною пухлиною УЗКП може дозволити виявити внутрішньопротокові папілярні пухлинні вегетації. Однак, остаточний діагноз ставиться шляхом виявлення зв’язку між пухлиною і протокою підшлункової залози, що важко при традиційній ультрасонографії.
Псевдокісти слабо накопичують контраст і тому ефективно диференціюються від кістозних пухлин.
ТОНКА КИШКА
УЗКП дозволяє оцінити кровоносні судини стінки кишки при хворобі Крона. Спостерігаються різні типи посилення ураженої стінки кишки, в тому числі відсутність посилення, переважне посилення підслизового шару і посилення всієї стінки (зобр. 23).
Зображення 23. Хвороба Крона. (А) Базова ультрасонографія клубової кишки показує потовщену стінку кишки (наконечники стрілки) з пошаровим виглядом. (В) Через 25 секунд після ін’єкції мікропухирців показано дифузне посилення контрастності всієї стінки кишки. (С) сліпа кишка.
Serra та ін. виявили значну кореляцію між різними моделями посилення і індексом активності хвороби Крона (ІАХК). УЗКП може допомогти відрізнити запальні стенози, які значимо посилюються і більш чутливі до консервативного лікування, від фіброзних стенозів, які характеризуються поганою васкуляризацією. Крім того, УЗКП ефективна в диференціальній діагностиці абсцесів і флегмон, які викликані хворобою Крона, дивертикуліту і апендициту.
Попереднє дослідження показує, що УЗКП можна використовувати в моніторингу клінічного перебігу хвороби Крона. У пацієнтів з клінічною і біохімічною ремісією, відсутність посилення підтверджує стабільну ремісію, в той час як посилення контрастності потовщеної стінки кишки передбачає більш високий ризик рецидиву, і отже, необхідність суворого спостереження.
Quaia та ін. спробували співвіднести кількісне посилення стінки кишки і ІАХК під час консервативного лікування хвороби Крона. Вони прийшли до висновку, що кількісна оцінка васкуляризації стінки кишки при УЗКП може бути корисним і простим способом оцінки ефективності лікування. У попередньому дослідженні Guidi та ін. намагалися порівняти кількісно 8 пацієнтів з посиленням стінки кишки після 3 доз моноклональних антитіл до TNF (Інфліксіма б) з попередньою оцінкою, при цьому виявивши значне зниження васкуляризації стінки кишки.
ЧЕРЕВНА АОРТА
УЗКП дозволяє оцінити кілька видів патології аорти. У хворих з розшаруванням черевної аорти, істинний просвіт можна відрізнити від хибного по затримці надходження в останній болюса мікропухирців. Діагностика аортокавального шунта поліпшується, коли виявляється раннє синхронне, однорідне посилення аорти і нижньої порожнистої вени. Ендоваскулярне лікування аневризми черевної аорти є прийнятою альтернативою відкритій хірургії. Найбільш частим ускладненням цієї процедури є підтікання, яке визначається як збереження перипротезного кровотоку в межах випинання аневризми, закритого стентом-протезом. Оскільки підтікання є основною причиною збільшення і розриву аневризми після ендоваскулярного лікування, обов’язковим є суворе по життєве спостереження. КТ є процедурою вибору для візуалізації та виявлення походження перипротезного підтікання, прилеглих судин і ускладнень, пов’язаних з ендолюмінальним лікуванням аневризми аорти. Велика кількість клінічних даних показує, що використання УКЗ значно покращує здатність ультрасонографії у виявленні підтікання, долаючи обмеження, викликані кальцифікацією, ехосигналами від металевої частини стента-трансплантата і повільного кровотоку. Iezzi та ін. показали, що УЗКП має чутливість і негативну прогностичну цінність у виявленні підтікання, аналогічну КТ. Крім того, як виявляється, УЗКП більш специфічна, ніж КТ у виявленні невеликого підтікання з низьким рівнем потоку. На УЗКП підтікання проявляються, як посилена зона за межами трансплантата, але в межах випинання аневризми (зобр. 24).
Зображення 24. Підтікання після ендоваскулярного лікування аневризми аорти. Зображення отримане через 45 секунд після ін’єкції контрасту. Часткове заповнення випинання аневризми (*) за трансплантатом (I – протезовані клубові артерії) через колатеральну судину (вигнута стрілка).
Затримка сканування від 5 до 10 хвилин може поліпшити виявлення підтікання при повільному кровотоці. Особлива увага повинна бути приділена походженню та ідентифікації привідних і відвідних колатеральних судин, які можуть бути ідентифіковані на проксимальній і дистальній частини трансплантата, або зовні бічної стінки аортального трансплантата, що може бути пов’язано з колатеральними артеріальними гілками, порушенням цілісності трансплантата або його пористістю.
СОННА АРТЕРІЯ
УКЗ були використані для оцінки частини внутрішньої сонної артерії, яка розташована відразу за межами черепа, що важко оцінити звичайними доплерівськими методами і для поліпшення кількісного визначення стенозу внутрішньої сонної артерії. Зокрема, важкі стенози можуть бути диференційовані від повної оклюзії. Крім того, УЗКП чітко відображає атеросклеротичні бляшки і реканалізацію, які можуть бути не виявлені на зображеннях доплерографії через турбулентність, збурювання потоку або повільності потоку. Однак, за допомогою сучасних систем, сонні артерії ефективно оцінюються практично в будь-яких ситуаціях за допомогою кольорової доплерографії.
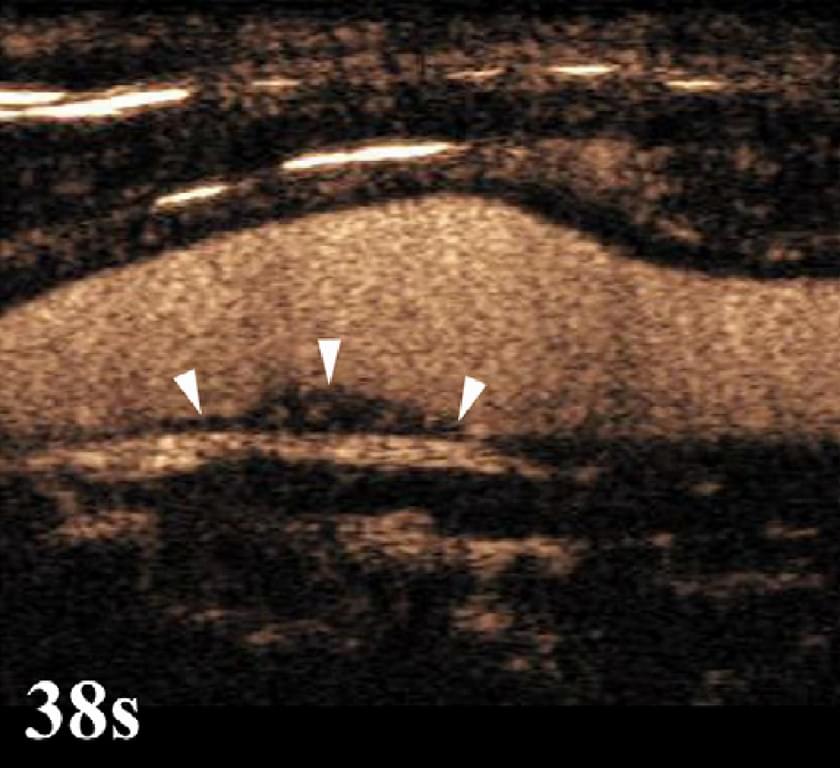
Зростає інтерес до застосування УЗКП для виявлення та візуалізації васкуляризації бляшок сонних артерій. Гістологічне дослідження показало, що запалення бляшки, ангіогенезінтіми, наявність адвентиційних ваза вазорум і неоваскуляризації бляшки – сильні предиктори нестабільності атероматозних уражень судин головного мозку та коронарних судин. УЗКП здатна безпосередньо візуалізувати адвентіційні ваза вазорум і неоваскуляризовані бляшки (зобр. 25).
Зображення 25. УЗКП сонної артерії у пацієнта, який страждав від гострої церебральної ішемії протягом 3 днів. Нестенозуюча бляшка з гіпоехогенним посиленням (наконечники стріл) виявлена в зоні початку внутрішньої сонної артерії через 38 секунд після введення контрасту.
Посилення бляшки визначається у 80% симптоматичних хворих і 30% безсимптомних пацієнтів. Крім того, інтенсивність контрастного підсилення значно більша у симптоматичних хворих.
Giannoni та ін. оцінили за допомогою УЗКП сонні артерії у 77 пацієнтів перед судинною операцією. У всіх 9 пацієнтів, які перенесли невідкладне хірургічне втручання у зв’язку з гострим неврологічним дефіцитом з геміпарезом УЗКП показала посилення контрастності бляшки, в той же час ця картина спостерігалася тільки в 1 з 64 безсимптомних пацієнтів. На хірургічних препаратах області контрастного підсилення відповідали зонам з підвищеною кількістю мікросудин при фарбуванні на наявність судинного ендотеліального фактору росту.
МОЗКОВИЙ КРОВООБІГ
УКЗ були використані для збільшення ефективності транс краніального доплерографічного дослідження. Мікропухирці надають новий підхід до вивчення Вілізієвого кола, серединної венозної системи і фронтальної паренхіми. Не так давно були введені методи перфузії з низьким МІ, що дозволило виявити УКЗ в церебральній мікроциркуляції. Висока частота кадрів може бути застосована з відмінною часовою роздільною здатністю для болюсних кінетиків. Недоліком цього методу є обмеження глибини дослідження через використання низького МІ.
СУГЛОБИ
Раннє виявлення панусу і моніторинг синовіальної васкуляризації є обов’язковими для відповідного лікування пацієнтів з ревматоїдним артритом. УЗКП показала багатообіцяючі результати в дослідженнях суглобів руки, ноги, коліна, і, останнім часом, крижово-клубових зчленувань. Зокрема, УЗКП дозволяє диференціювати між синовіальним панусом, який має перфузію і рідину. Ця диференційна діагностика важка при сіро шкальній ультрасонографії, оскільки обидва стани можуть мати і гіпоехогенну і гіперехогенну структуру і це клінічно дуже важливо, оскільки присутність панусу є прогностичним критерієм кісткових ушкоджень. УЗКП може мати значення для визначення наявності ерозивних уражень, оскільки васкуляризовані ерозії є ознакою прогресії активного захворювання. Нарешті, мікропухирці можуть бути корисними у виявленні гіперваскуляризації у пацієнтів з незначним або сумнівним об’ємом синовіальної проліферації, що не визначається при звичайній сонографії.
УЗКП значно ефективніше, порівняно з імпульсною доплерографією і ультрасонографією, в диференціальній діагностиці активного і неактивного синовіїту. Техніка дозволяє значно поліпшити вимірювання товщини активної синовіальної оболонки.
Об’єктивний кількісний аналіз синовіальної васкуляризації представляється перспективним для оцінки відповіді на лікування. Однак, для оптимальної роботи процедура отримання зображень повинна бути стандартизованою, а якість експертизи залежить від майстерності радіолога і використання оптимального устаткування.
ЛІМФАТИЧНИЙ ВУЗОЛ
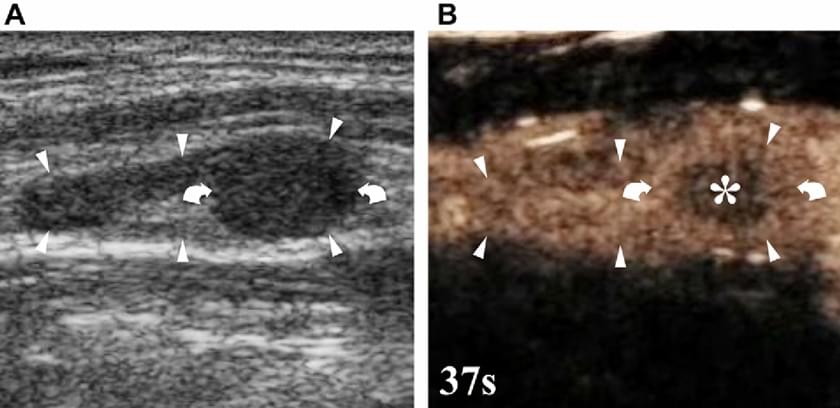
Після введення мікро пухирців Rubaltelli та ін. визначили різні характеристики посилення при патології лімфатичних вузлів. Реактивні лімфатичні вузли викликають дифузне інтенсивне і однорідне посилення. Вузлові метастази, як правило, менш васкуляризовані, ніж звичайна тканина вузла, і виявляються як дефекти перфузії (зобр. 26).
Зображення 26. Метастази раку молочної залози в пахвовий лімфатичний вузол. (А) Базова ультрасонографія показує лімфатичний вузол (наконечник стрілки) нормального розміру, але асиметричної форми, що викликано ексцентричною гіпоехогенною зоною (вигнуті стрілки). (В) Через 37 секунд після ін’єкції мікропухирців виявлене гіпоехогенне ураження (*) в цій зоні (вигнуті стрілки), відповідно до метастатичного ураження. Діагноз був підтверджений при прицільній біопсії.
Лімфоми можуть бути схожі на запалення лімфатичних вузлів або мати дифузне гетерогенне посилення контрастності з точковою картиною в ході артеріальної фази. Хоча ці попередні результати є перспективними, вони потребують подальшого підтвердження.
Використання УЗКП було запропоновано для того, щоб визначити сторожовий лімфатичний вузол при раку, після інтерстиційної ін’єкції УКЗ. Goldberg і його колеги, які використовували Sonazoid (Amersham, Бакінгемшир, Великобританія), показали можливість простежити лімфатичні судини від місця ін’єкції до дренуючого сторожового лімфатичного вузла, а також визначити інтранодальні метастази, представлені як перфузійні дефекти або у вигляді гетерогенного посилення. Попереднє клінічне дослідження показало схожі результати. Ці результати обнадіюють, але в даний час вони є експериментальними і їх прикладне значення, в основному, на тваринах. За допомогою SonoVueWang та ін. в режимі реального часу отримали картину лімфодренажу і визначили сторожові лімфатичні вузли у тварин, але не змогли виявити метастази в лімфатичних сторожових вузлах.
МОЛОЧНА ЗАЛОЗА
Молочна залоза була одним з перших органів, у якого було досліджено вплив УКЗ. Спочатку УЗКП була використана для диференціальної діагностики доброякісних і злоякісних захворювань. Контрастна кольорова доплерографія також була використана в складних випадках диференціальної діагностики між післяопераційним рубцем і рецидивом пухлини. Хоча деякі дослідження показують, що введення мікропухирців покращує здатність ультрасонографії в диференціальній діагностиці доброякісних уражень молочної залози від злоякісних, чутливість та специфічність методики не є достатніми для того, щоб уникнути біопсії. Таким чином, УЗКП не має клінічного значення для цієї мети.
Допплерівська ультрасонографія, навіть з контрастними засобами, дозволяє візуалізувати кровоносні судини на рівні артеріол і венул, але не виявляє кровотік через капілярні ложа, які можуть бути досліджені за допомогою контрастних специфічних режимів. Використовуючи ці методи, Liu та ін. показали, що висновки УЗКП корелюють з гістологічними особливостями пухлини молочної залози. Зокрема, області, що посилюються, відповідають внутрішньопротоковій карциномі, інвазивному раку, внутрішньопротоковій папіломі, фіброаденомі з підвищеною стромальною і епітеліальною клітинною гіперплазією, аденозу, багатому ацинарними і трубчастими структурами або запальному клітинному інфільтрату; не посилені області відповідають низькій кількості клітин, фіброзній реакції строми, розширеним протокам, фіброзу або некрозу. Du та ін. зіставили картину посилення і параметрів кривої часу інтенсивності ураження молочної залози, отримані в режимі реального часу при УЗКП, з щільністю мікросудин і виразністю судинного ендотеліального фактору росту. Вони виявили, що УЗКП має потенціал в оцінці щільності мікросудин для уражень молочної залози, але не дозволяє провести диференціальний діагноз між доброякісними і злоякісними гіперваскуляризованими пухлинами.
ПЕРСПЕКТИВИ
Специфічні мікропухирці є одним з найбільш перспективних додатків у майбутньому, з декількома діагностичними та терапевтичними точками прикладання.
Речовини, які зв’язуються з конкретною молекулою ендотеліальних маркерів ангіогенезу, такі як інтегрин avb3, яка вибірково експресується на ангіогенному ендотелії, можуть послужити основою для молекулярної візуалізації пухлин і таргетної доставки ліків. УЗКП може бути особливо ефективне для вивчення цих процесів через здатність селективно приєднуватися до необхідних судин з інформацією про перфузію та обсяг мікроциркулярного русла. Специфічні мікропухирці можуть бути виявлені після того, як циркулюючі мікропухирці зникли після внутрішньосудинної ін’єкції.
За допомогою специфічних мікропухирців може бути досягнута активація лейкоцитів, які задіяні в ендотелії судин в зоні травми або запалення, шляхом неспецифічної взаємодії між клітинами і мікропухирцями. Більш специфічний метод візуалізації запалення полягає у виявленні молекул клітинної адгезії, які експресовані на активованому ендотелії і беруть участь в лейкоцитарному поповненні пулу клітин.
Тромб-специфічні (таргетні) мікропухирці були розроблені для поліпшення діагностичної точності ультрасонографії у виявленні судинного або внутрішньосерцевого тромбозу на моделях у тварин. Крім виявлення тромбів, ці мікропухирці випробовувалися, як додаткова терапія для тромболізису.
Специфічні (таргетні) мікропухирці можуть переносити в конкретні місця біоактивні матеріали, такі як ліки або гени. Коли мікропухирці досягають місця призначення, надходження усередину клітини може відбуватися за участю процесу ендоцитозу для сполук з малою молекулярною масою, в той час як сонопорація (тобто, ультрасонографічно індуковане утворення пор в мембранах клітин) є переважаючим механізмом для більш великих молекул і плазмід.
Велика проблема для сонопораціі – це відкриття гематоенцефалічного бар’єру у зворотному порядку.
Деякі дослідники вивчають ультрасонографію з контрастуванням при генній терапії серцево-судинних захворювань з метою контролю гіперплазії інтими, відновлення функції судин або стимуляції ангіогенезу.
РЕЗЮМЕ
З появою контрастних агентів у вигляді мікропухирців і методів специфічного контрастування, УЗКП стала потужним додатковим інструментом променевої візуалізації, зокрема, для печінки. Коли мікропухирці вводять внутрішньовенно, чутливість та специфічність ультрасонографії в оцінці ВУП наближаються до КТ і МРТ, з перевагами відсутності випромінювання і низької вартості. Дані УЗКП в основному повторюють відомі результати КT і МРТ, хоча УКЗ поводяться по-різному. Функціональна (перфузійна) інформація може бути отримана на додаток до морфологічної інформації, і при цьому найчастіше відпадає необхідність у подальшому обстеженні. Тим не менш, УЗКП вимагає досвіду і адекватного ультразвукового устаткування. Крім того, суб’єкти та органи, непридатні для ультрасонографії, також не підходять і для УЗКП, методика не є панорамним методом візуалізації а, отже, не може бути заміною для всебічного вивчення всього тіла, як при КТ, МРТ або ПЕТ. Для проведення досліджень рекомендуємо використовувати апарат від компании GE Voluson E8.
Часті питання та відповіді (FAQ)
Що таке ультразвукове дослідження з контрастуванням (УЗКП)?
- УЗКП – це метод ультразвукової візуалізації, що використовує спеціальні контрастні засоби (УКЗ) для покращення якості зображення та отримання додаткової інформації про кровопостачання органів та тканин.
Які переваги УЗКП перед звичайною ультрасонографією?
- УЗКП дозволяє краще візуалізувати дрібні судини, покращуючи діагностику пухлин та інших уражень.
- Завдяки УЗКП можна оцінити кровотік в органах та тканинах, що важливо для функціональної діагностики.
- УЗКП дозволяє отримувати зображення в режимі реального часу, що спрощує дослідження.
Які типи контрастних засобів використовуються в УЗКП?
- Існують різні типи УКЗ, що відрізняються за хімічним складом та властивостями. У статті наведено таблицю з прикладами УКЗ, доступних в різних країнах.
Чи є УЗКП безпечною процедурою?
- УЗКП є загалом безпечною процедурою, і серйозні побічні ефекти трапляються рідко. Однак, перед проведенням дослідження необхідно враховувати можливу алергію на компоненти контрастної речовини.
В яких випадках застосовується УЗКП?
- УЗКП використовується для діагностики різних захворювань печінки, інших органів черевної порожнини та судин.
- Часто УЗКП застосовується як додатковий метод дослідження, коли результати звичайної ультрасонографії недостатньо інформативні.
Чим відрізняється УЗКП від КТ та МРТ?
- УКЗ є внутрішньосудинними речовинами, на відміну від контрастних засобів для КТ та МРТ, які проникають в інтерстицій. Це впливає на фази візуалізації та інтерпретацію результатів.
- УЗКП дозволяє отримувати зображення в режимі реального часу, чого неможливо досягти за допомогою КТ та МРТ.
Які обмеження УЗКП?
- УЗКП не забезпечує панорамного зображення, як КТ та МРТ.
- Якість зображення може бути знижена у пацієнтів з метеоризмом, стеатозом або фіброзом.
- Для проведення УЗКП необхідне спеціальне обладнання та підготовка персоналу.








14.10.2019
Такер Кристина Богдановна