R. Wunscha,∗, L. von Rohdenb,1, R. Cleavelanda, V. Aumannc,2aDepartment of Pediatric Radiology, Vestic Children’s Hospital Datteln, University of Witten/Herdecke, Dr.-Friedrich-Steiner-Strasse 5,D-45711 Datteln, GermanybDepartment of Pediatric Radiology, Otto-von-Guericke-University Magdeburg, Klinik f. Radiologie und Nuklearmedizin – Kinderradiologie,Leipziger Straße 44, D-39120 Magdeburg, GermanycDepartment of Pediatric Haematology and Oncology, Otto-von-Guericke-University Magdeburg, Universitätskinderklinik (H 10),Pädiatrische Hämatologie und Onkologie, Leipziger Straße 44, D-39120 Magdeburg, Germanya
Резюме. Ультразвукове дослідження (УЗД) поверхневих органів та структур – це відображення маленьких поверхневих структур за допомогою високочастотних лінійних датчиків. Традиційне застосування УЗД поверхневих органів включає візуалізацію та диференційну діагностику у випадках нечітких поверхневих структур з жорсткою, рідкою та змішаної текстурою, а також поверхневих органів, таких як щитовидна залоза і яєчка. Більше того, показами до УЗД ділянки голови та шиї є оцінка зовнішніх просторів цереброспинальної рідини (ЦСР) у немовлят, сонографія орбіти, стінок великих судин шиї, візуалізація поверхнево розташованих лімфовузлів і новоутворень.
За результатами проведених клінічних досліджень можна зробити висновок, що УЗД, котре з усіх методів візуалізації володіє найвищим просторовою роздільною здатністю у міліметровому та мікрометровому діапазоні (100-1000 мкм), може вважатися найбільш підходящим методом для дослідження поверхневих патологічних утворень і близько розташованих до поверхні органів. Також, воно забезпечує важливою інформацією про характерну, часто патогномонічну архітектуру тканини при різних паталогічних процесах.
ВСТУП
До УЗД поверхневих органів та структур відноситься візуалізація дрібних структур, розташованих близько до поверхні, за допомогою високочастотних лінійних датчиків (зазвичай в діапазоні 9 і 15-20 МГц).
Традиційне застосування УЗД поверхневих органів включає візуалізацію і диференціальну діагностику в наступних випадках:
– наявність нечітких поверхневих структур з жорсткою, рідкою або змішаною текстурою;
– такі ж структури в поверхневих органах, таких як щитовидна залоза та яєчка.
Виділяють такі покази до УЗД ділянки голови та шиї:
– оцінка зовнішніх просторів цереброспінальної рідини (ЦСР) у немовлят;
– сонографія орбіти;
– сонографія великих судин шиї;
– візуалізація поверхнево розташованих лімфовузлів і новоутворень;
– УЗД слинних залоз.
СТРУКТУРИ ДІЛЯНОК ГОЛОВИ ТА ШИЇ
Оцінка візуалізації та диференціальної діагностики, несподівано виявлених структур, що пальпуються – це завдання, яке часто зустрічається в практиці педіатричного радіолога. Батьки часто бояться, що утворення, яке пальпується, може виявитися пухлиною. УЗД – це доцільний, швидкий та широкодоступний інструмент в таких випадках, який дозволяє вибрати подальшу тактику.
Реактивний запальний набряк лімфатичних вузлів (НЛВ) частіше виникає в ділянці голови та шиї, але часто маніфестує в паху, під пахвами (axilla), у середостінні та в межах черевної порожнини (в брижі, в кишківнику) – тут найчастіше доброякісні (на відміну від злоякісних вісцеральних НЛВ у дорослих).
НЛВ у дітей, незалежно від локалізації, на УЗД незначно відрізняється від НЛВ в ділянці шиї, тому ми будемо обговорювати тільки останні. Основним завданням у всіх випадках НЛВ є диференціація між їх добро- і злоякісним утвореннями, наскільки це можливо за допомогою УЗД. У дитинстві розмір лімфовузлів грає невелику роль при оцінці утворень онкологічної природи. Однак, вони відіграють значну роль у відстеженні протікання запального процесу та моніторингу випадків підозрілої природи.
Нижче представлений перелік може стати додатковим способом оцінки та диференціальної діагностики добро- і злоякісних збільшень лімфовузлів за допомогою УЗД.
Перелік: параметри діагностики та оцінки
|
Критерій |
Властивості (множинні характеристики повинні враховуватися) |
Оцінка |
|
|
Д [1] |
З[1] |
||
|
1. Форма лімфовузла |
Овальна |
++ |
+ |
|
Еліпсоїдна, плоско-овальна |
+++ |
(+) |
|
|
Конусовидна |
(+) |
++ |
|
|
Кругла |
(+) |
++ |
|
|
Неправильна |
(+) |
+++ |
|
|
2. Внутрішньовузлова ехогенність = відносна яскравість зображення (виключаючи ворота і капсулу) |
Ізо- |
+ |
+ |
|
Гіпо- |
+ |
+ |
|
|
Значно гіпо- (чорне) |
+ |
+++ |
|
|
Гіпер- (біле) |
+ |
+ |
|
|
Змішана |
(+) |
+ |
|
|
3. Контури |
Гострі |
+ |
+ |
|
Більше 50% не гострі |
(+) |
+ |
|
|
Хвилясті, дуже неправильні |
(+) |
++ |
|
|
Екстранодулярні розтягнення або локальні обмежені протрузії |
– |
+++ |
|
|
4. Внутрішня структура |
Гомогенна, рівномірна |
++ |
+ |
|
Негомогенна, нерівномірна |
+ |
+++ |
|
|
5. Текстура внутрішніх структур (виключаючи ворота і капсулу) |
Гранулярна |
++ |
+ |
|
(дрібно або грубо гранулярна) |
+ |
+ |
|
|
Ретикулярна, «медові соти» |
(+) |
+ |
|
|
Смугаста (дрібна/груба) |
(+) |
++ |
|
|
Змішана |
+ |
+++ |
|
|
Інші незвичайні ознаки |
|||
|
6. Ворота |
Видно |
++ |
+ |
|
Не видно |
(+) |
+++ |
|
|
Ортотрофічні |
++ |
+ |
|
|
Дистрофічні |
+ |
++ |
|
|
Спотворені/деформовані |
+ |
+++ |
|
|
7. Капсула та перинодулярна тканина |
Цілі |
++ |
+ |
|
Переривчасті |
+ |
+++ |
|
|
Потовщені |
+ |
(+) |
|
|
Інші незвичайні ознаки |
+ |
+ |
|
|
8. Васкуляризація |
Ділянка воріт |
++ |
+ |
|
Периферична |
+ |
+++ |
|
|
Архітектура збережена |
+++ |
+ |
|
|
Архітектура порушена |
+ |
+++ |
|
|
Не визначається |
+ |
+ |
|
|
Розріджена |
+ |
++ |
|
|
Помірна (норма) |
++ |
+ |
|
|
Виражена |
+++ |
+ |
|
|
Інші незвичайні ознаки |
+ |
+++ |
Д = доброякісне; З = злоякісне.
Ці критерії можуть слугувати основними вказівками для діагностики в більшості випадків (зазвичай разом із клінічними спостереженнями), але не повинні вважатися всеохоплюючими, універсальними або негнучкими (Рис. 1 і 2).
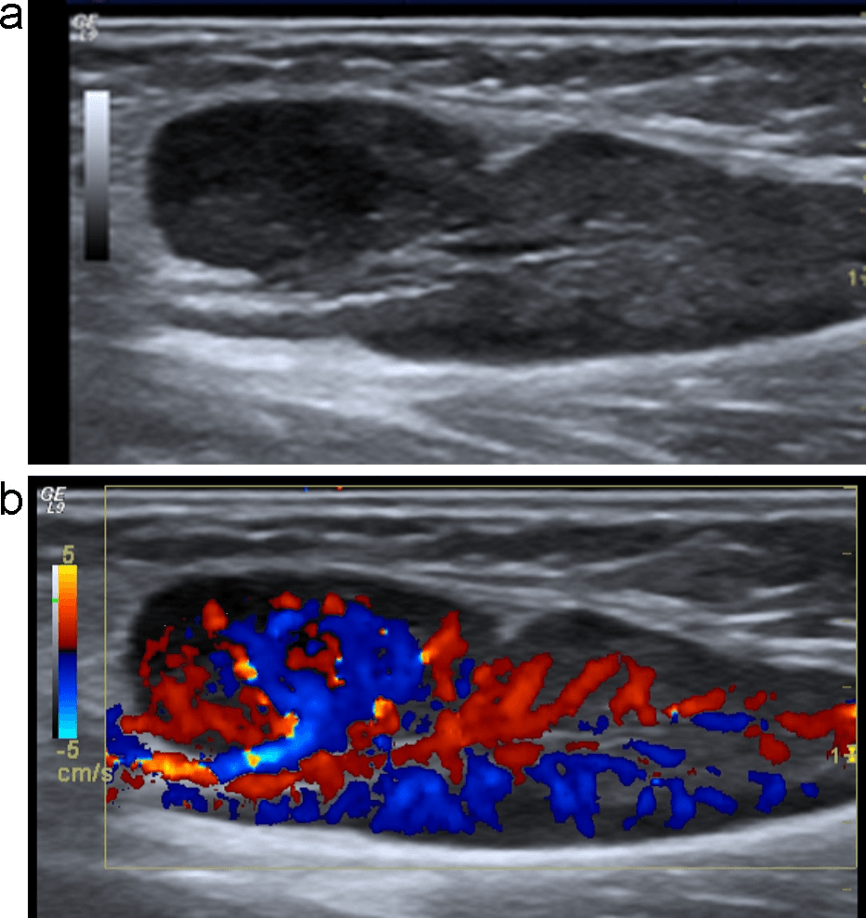
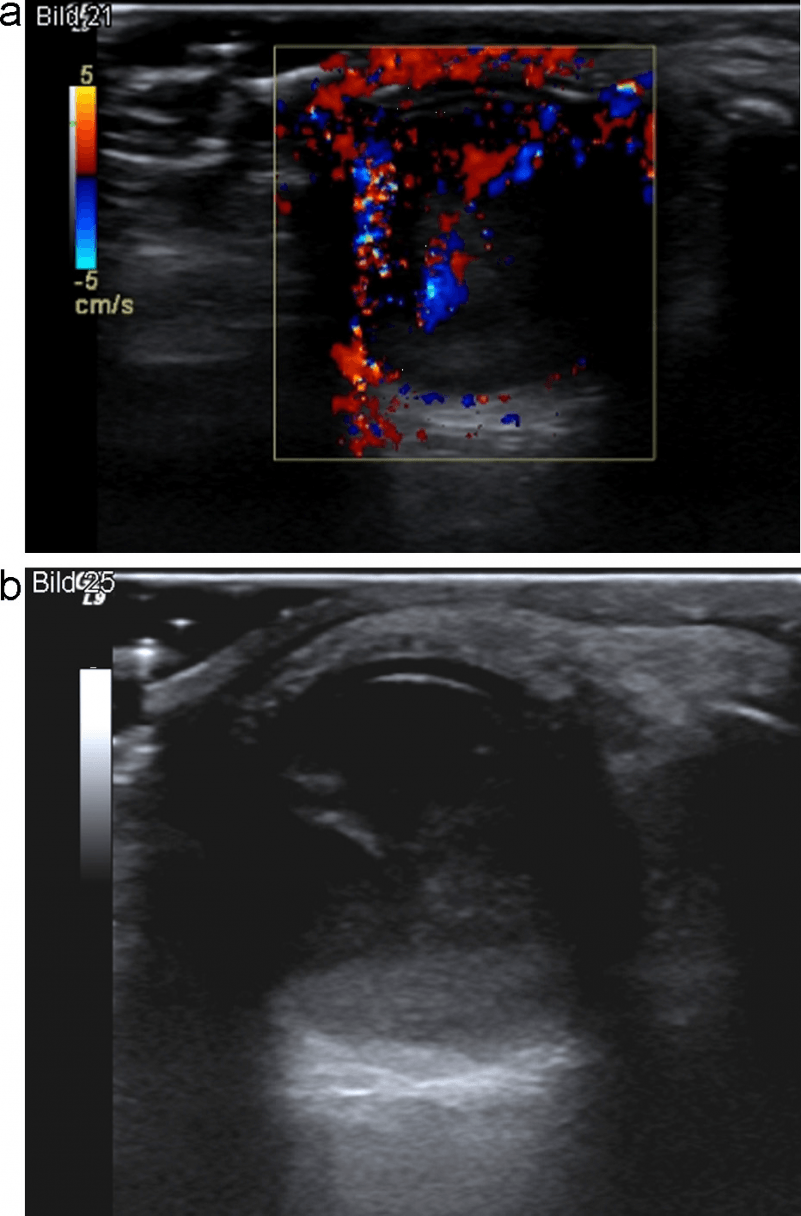
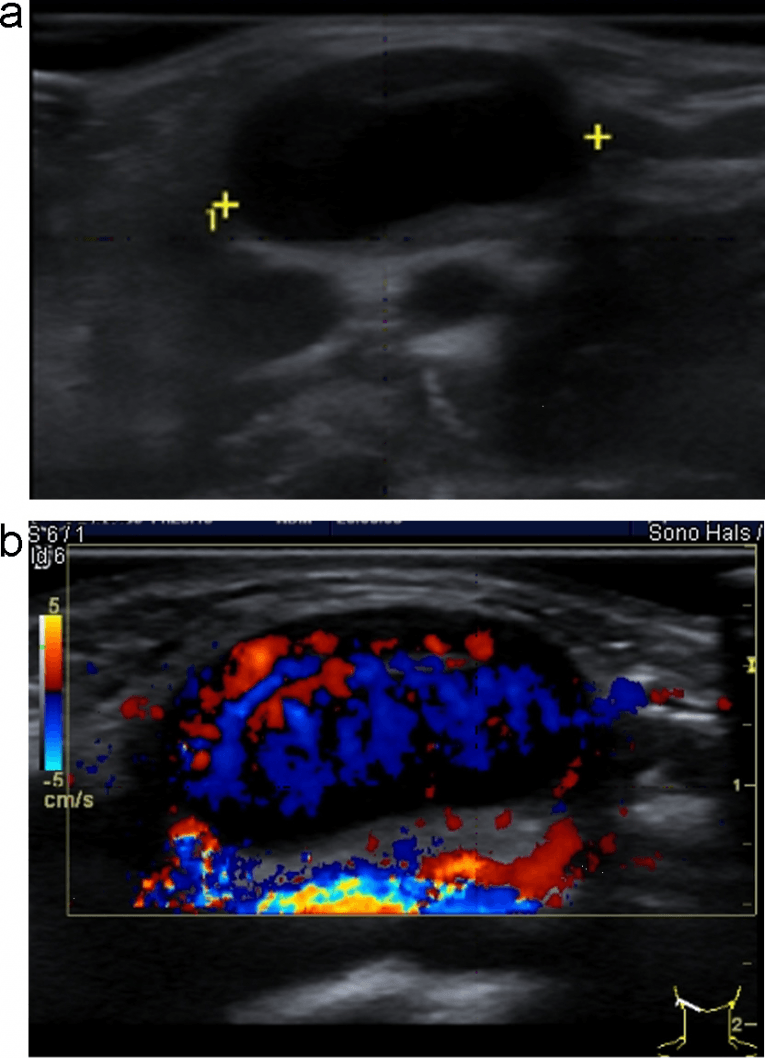
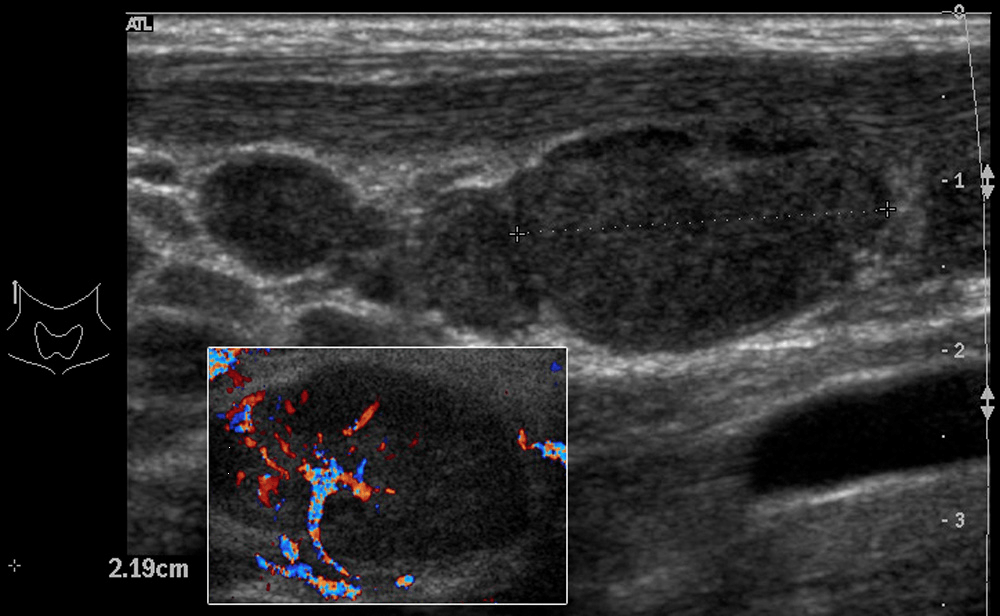
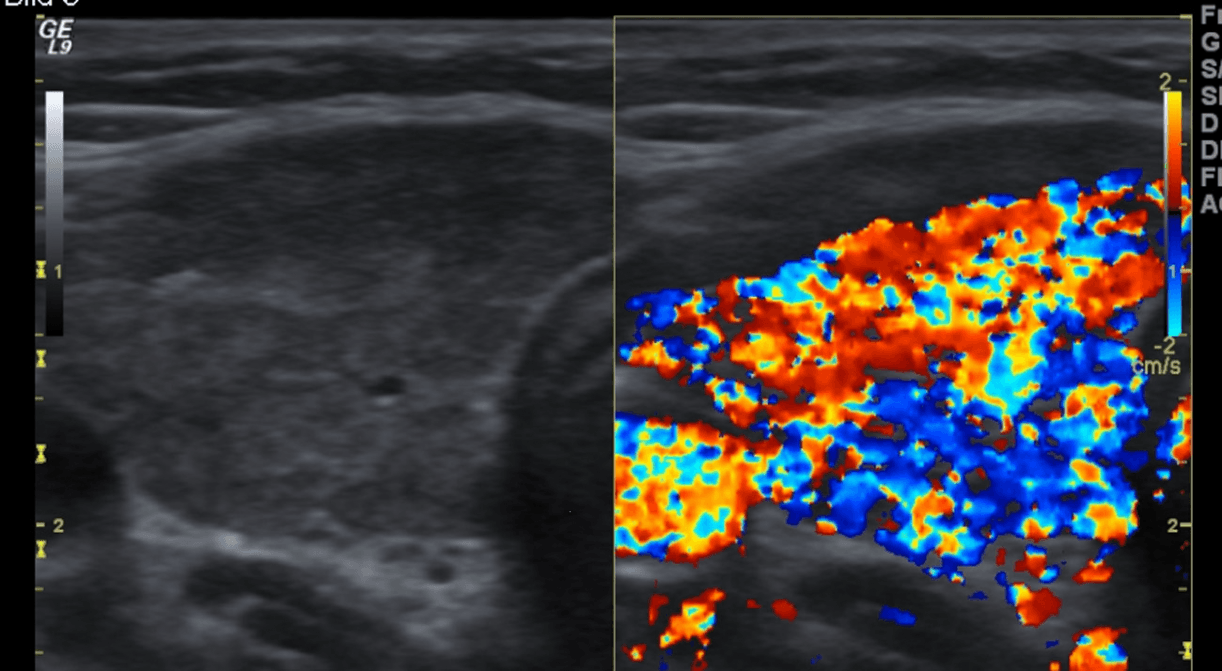
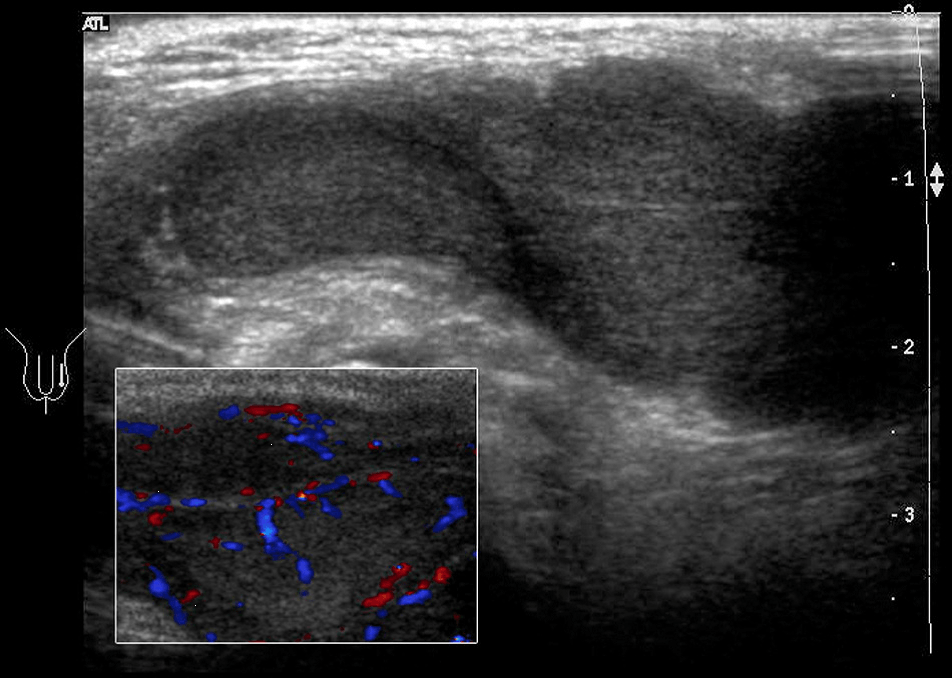
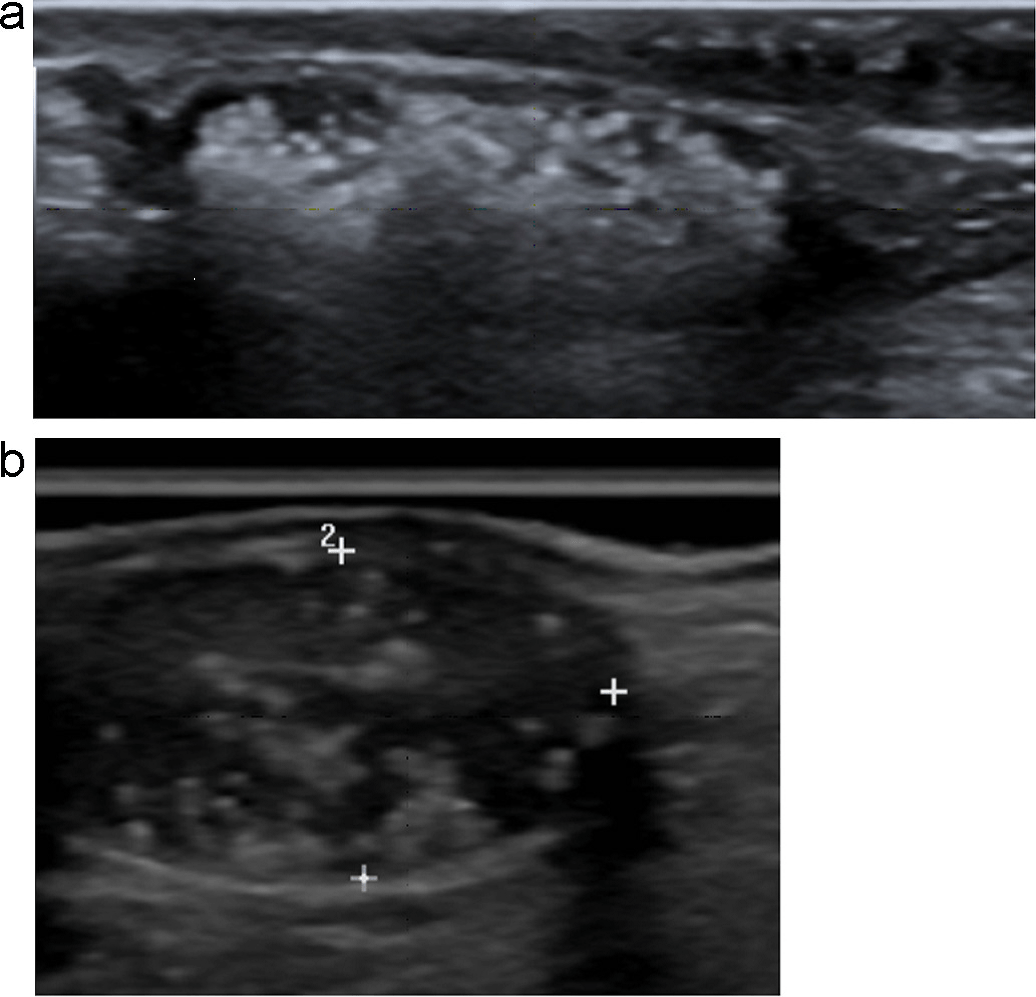
Рис. 1. (a і b) Звичайне УЗД і колірне доплерівське картування лімфовузла. Еліпсоїдна форма, ворота зі збереженою, нормальною архітектурою судин, гомогенним внутрішнім відлунням і незміненою капсулою, що вказує на реактивне запалення (доброякісне).
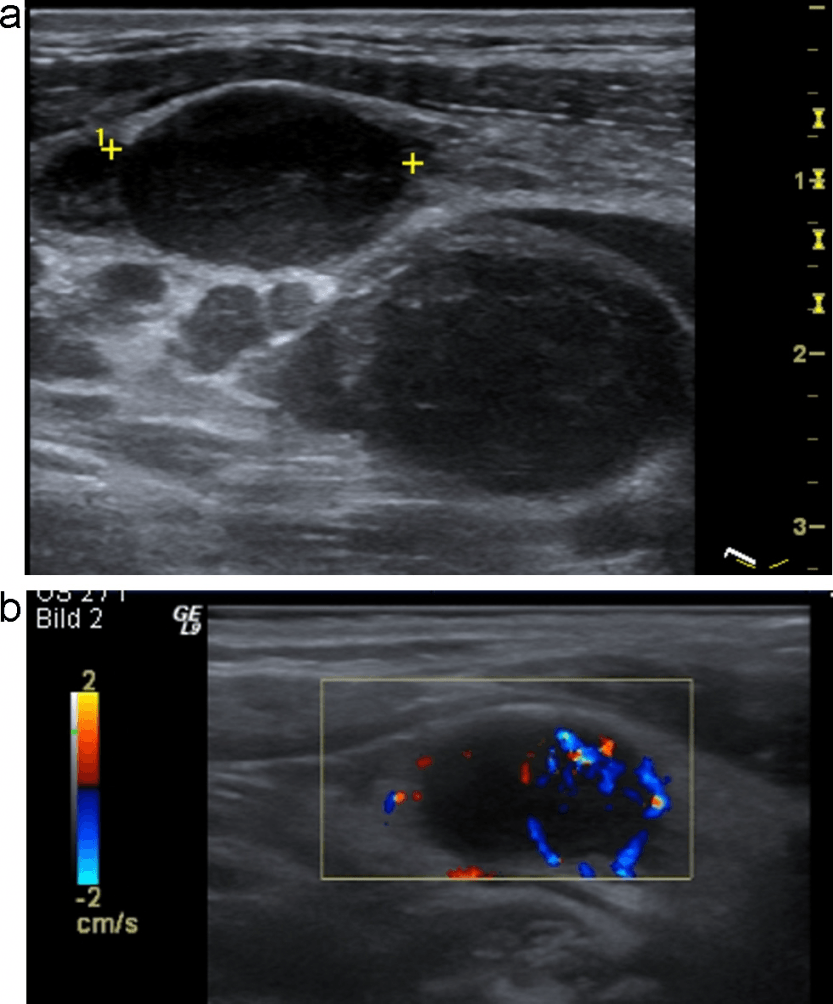
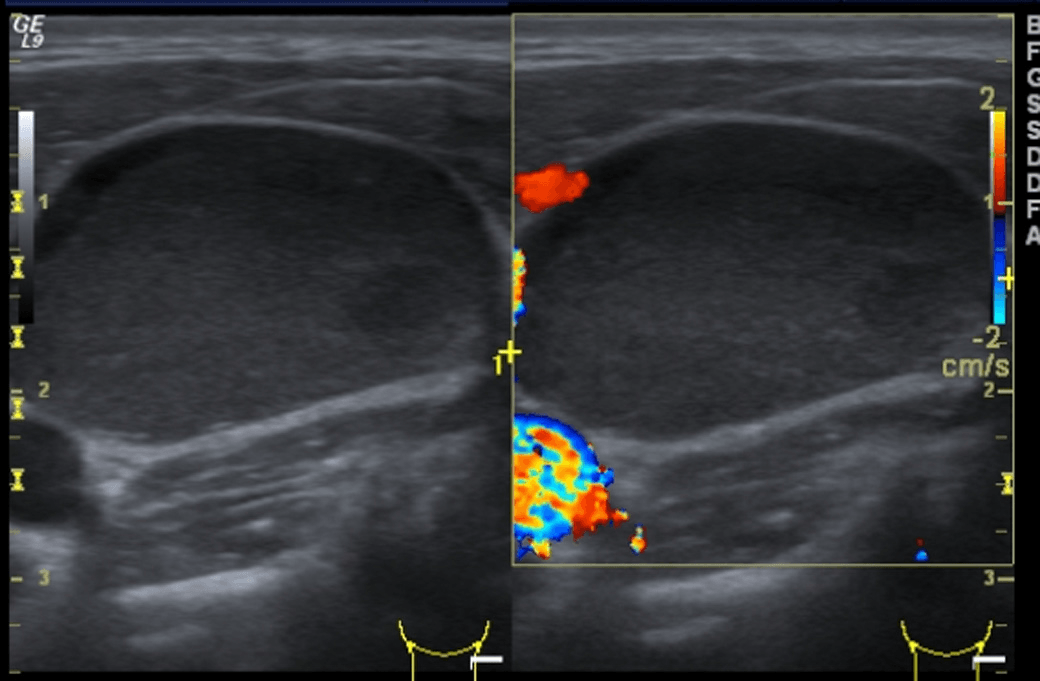
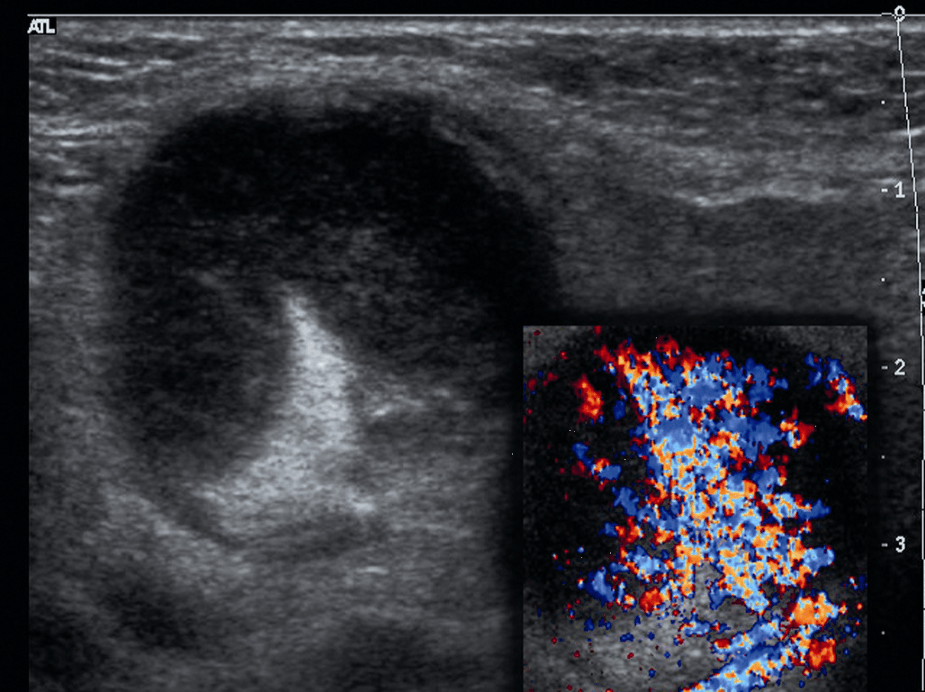
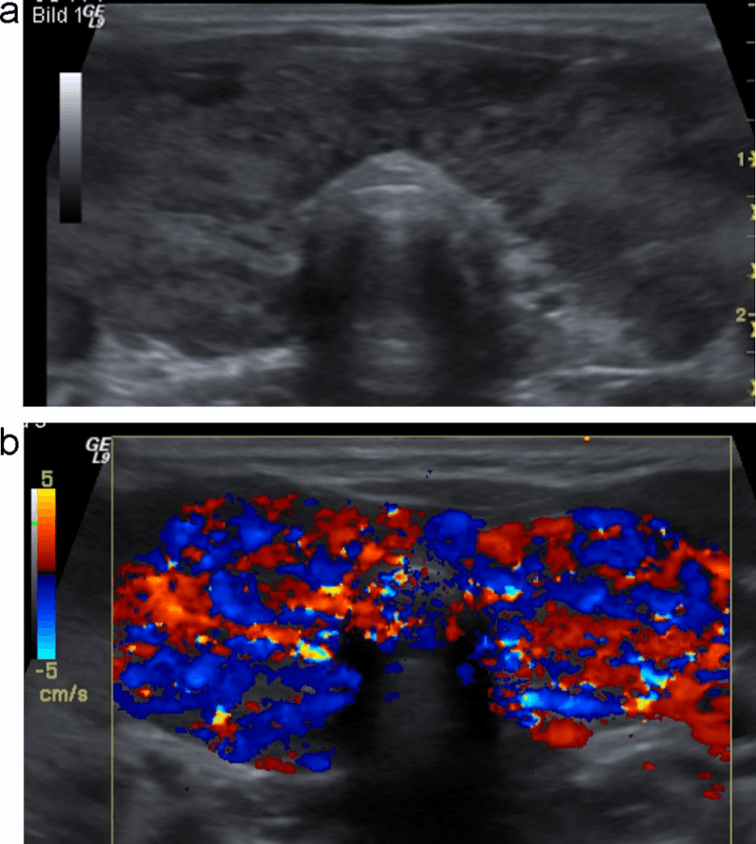
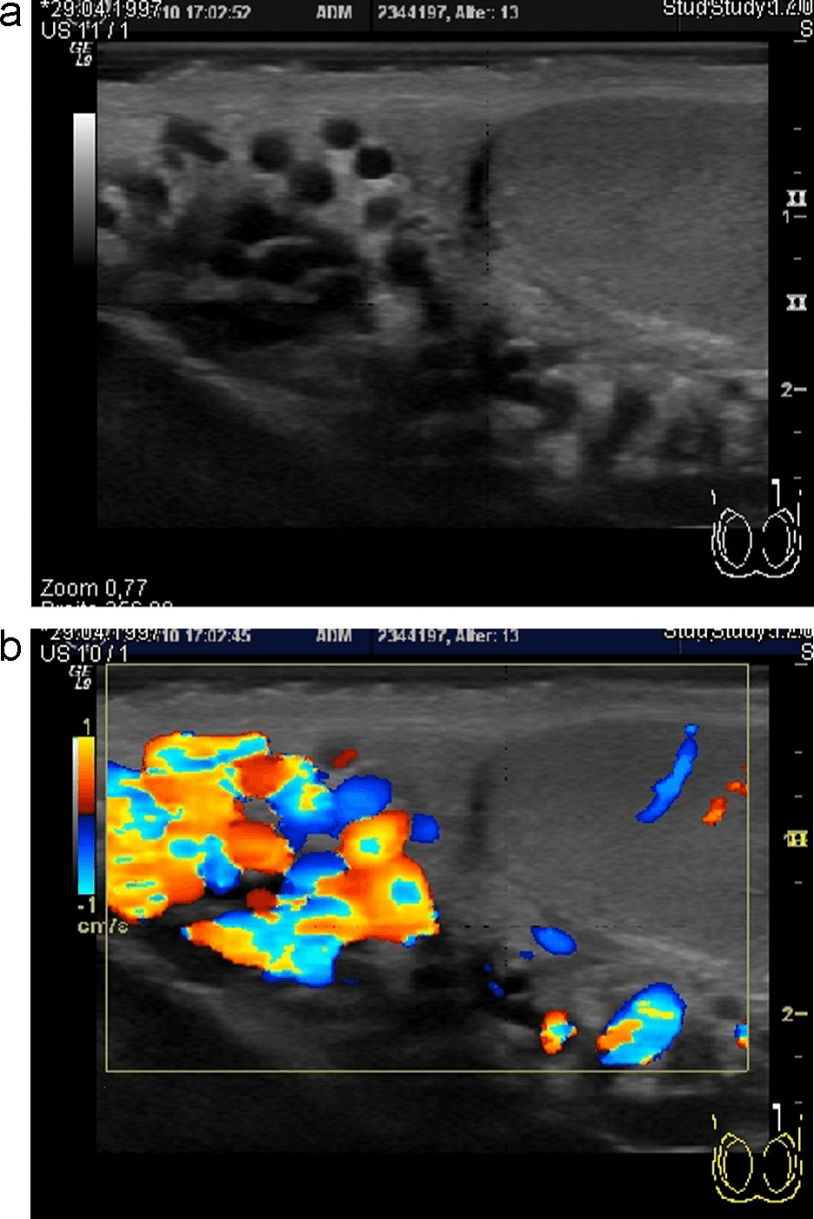
Рис. 2. (a і b) Звичайне УЗД і колірне доплерівське картування лімфовузла. Кругла форма, з чіткою внутрішньою гіпоехогенною текстурою, ворота не візуалізуються, порушена васкулярная архітектура з периферичним розташуванням судин і неправильною протрузією вказують на злоякісний процес в лімфовузлах.
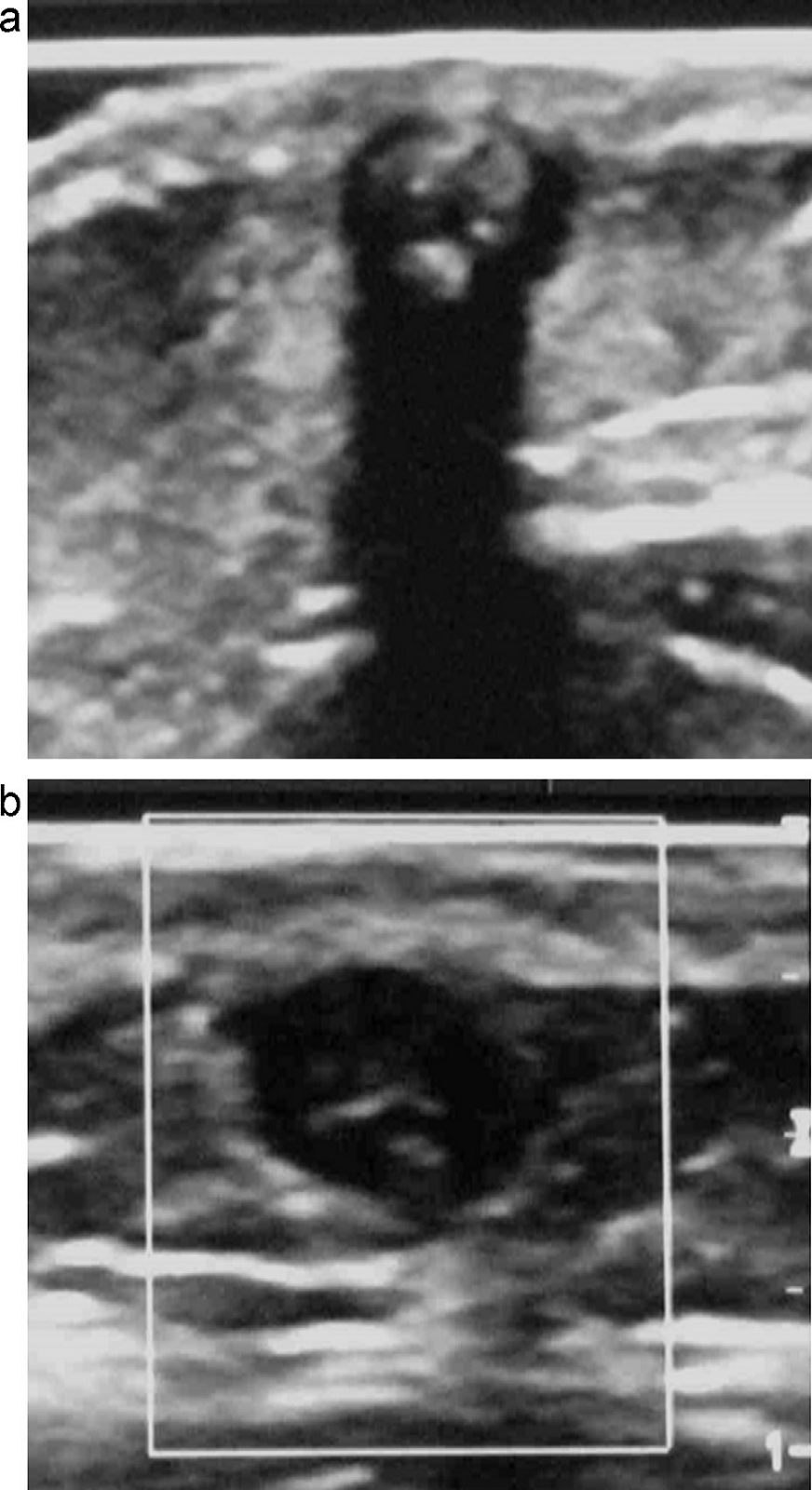
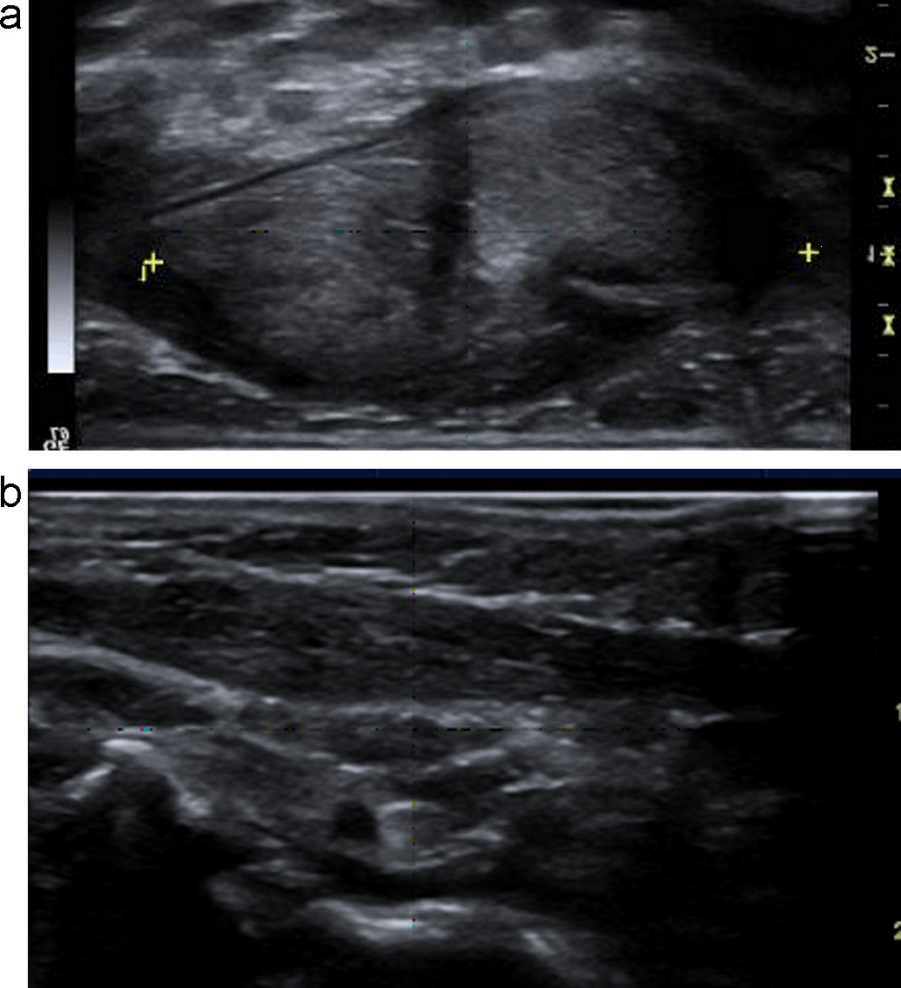
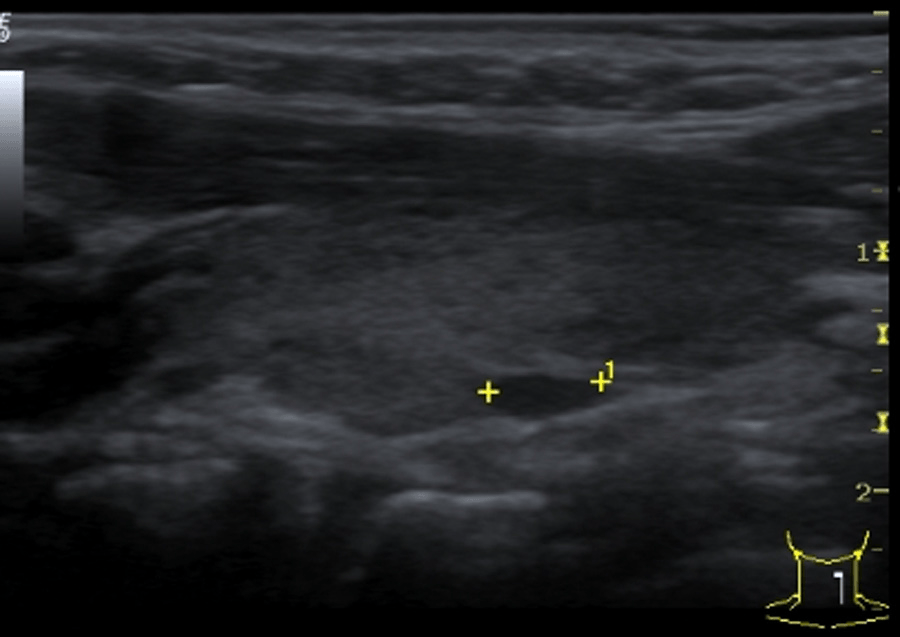
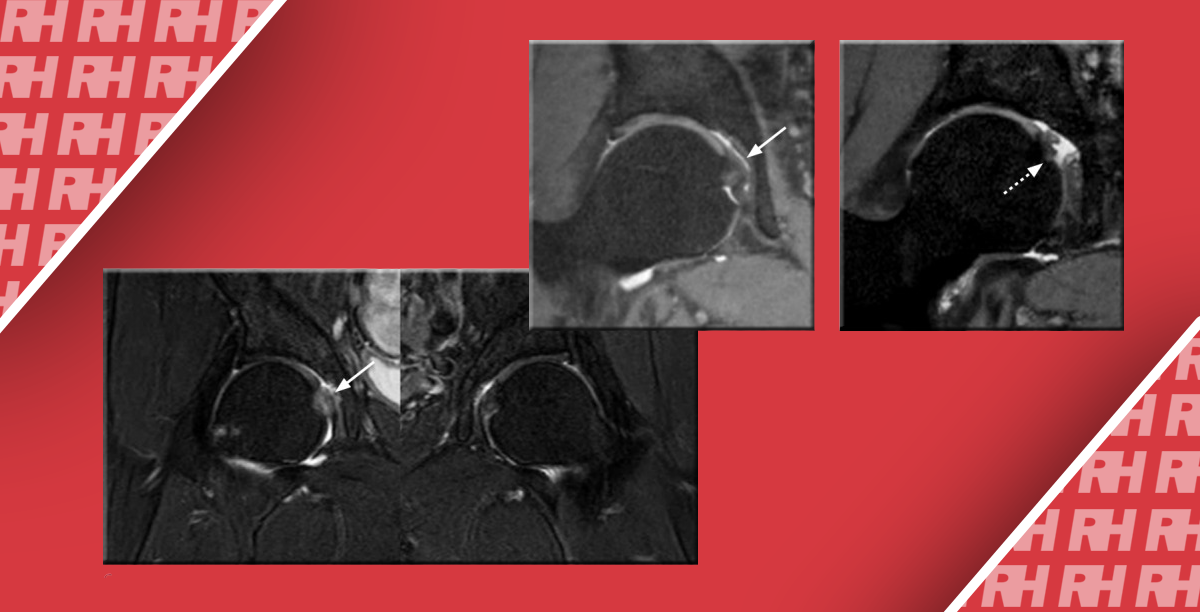
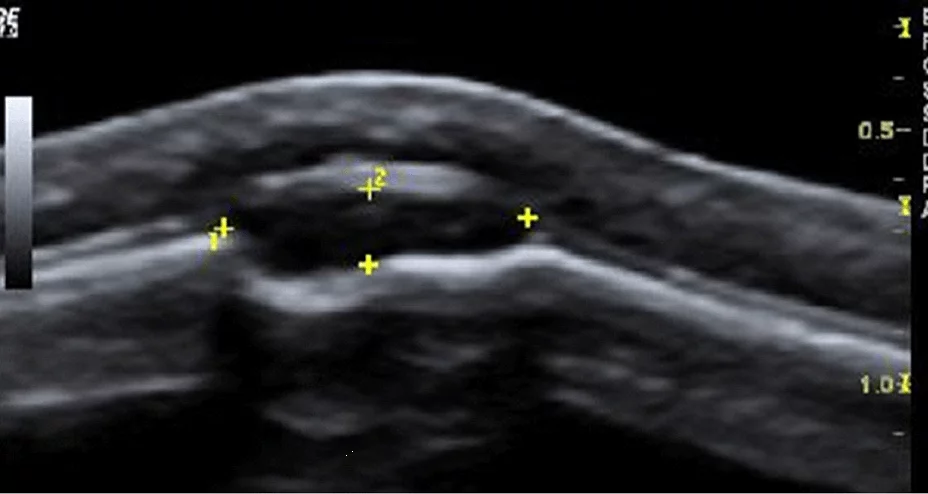
Епідермоїдні кісти виглядають як гіпоехогенні овоїдні структури без центральних кровоносних судин. Часто існує акустична передача через кісту, з так званим заднім ехо-підсиленням. Епідермоїдні кісти складаються з плоского епітелію, а дермоідні також можуть містити шкірні відростки. Ці пухлини можуть обмежуватися кістками (Рис. 3).
Рис. 3. Типовий УЗД знімок епідермоїдний кісти (+ … +).
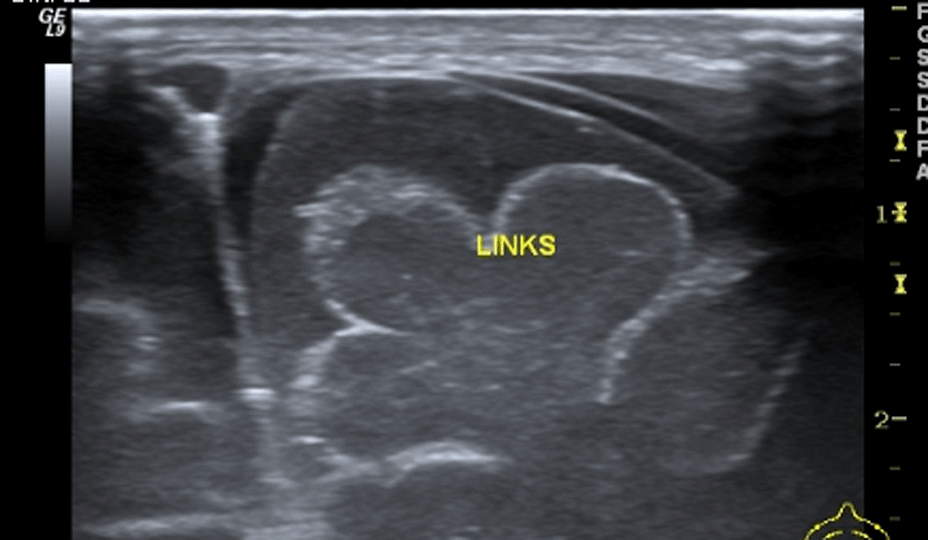
Піломатриксоми (кальцифікована епітеліома Малерба) складається з клітин подібних на матрицю волосного фолікула. Ці клітини можуть некротизуватися та кальцифікуватися. Маніфестація зазвичай відбувається до 20 років. Клінічно, при пальпації відчуваються глибокі дермальні або субкутанні (тверді, як камінь) вузли. Гістологічно, ці осередки відповідають доброякісній фолікулярній аднексальній пухлині. Центральні кальцифікації поширені, часто з гіперехогенною спицеподібною картиною в гіпоехогенній круглій або овальній структурі (Рис. 4).
Рис. 4. (a і b) піломатиксоми з різними ступенями кальцифікації. Центральні судини не візуалізуються.
ЕКСТРАЦЕРЕБРАЛЬНІ ПРОСТОРИ ЦСР У НЕМОВЛЯТ
У немовлят, екстрацеребральні простори ЦСР досліджуються лінійним датчиком, який здатний давати більш цінну інформацію, ніж секторний. Субдуральні гематоми можна особливо ефективно виявляти не лише в голові, але і в хребті. Випадок, представлений на рис. 5 демонструє можливість диференціації субдурального простору (гіпоехогенний) і значно розширеного субарахноїдального простору (злегка гіперехогенний).
Рис. 5. Збільшені екстрацеребральні простори ЦСР з гіперехогенною субдуральною гематомою.
УЗД ОРБІТИ
При проводенні цього дослідження пацієнт знаходиться в положенні лежачи на спині. Лінійний датчик ставлять на верхню повіку. Колобома формується при розщепленні в структурах ока (райдужна оболонка, сітківка, судинна оболонка або диск зорового нерва) в результаті недостатнього закриття ембріональної щілини судинної оболонки. Ця патологія візуалізується на УЗД як випинання склери від невеликого лійкоподібного до ретробульбарної кісти великого розміру.
Персистуюче гіперпластичне первинне склоподібне тіло (ПГПСТ)
При ПГПСТ на УЗД можна побачити гіперехогенну ділянку на проміжку від задньої частини кришталика до сосочка зорового нерва. Центральніше візуалізується персистуюча гіалоїдна артерія (Рис. 6).
Рис. 6. (a і b) УЗ зображення ПГПСТ.
За допомогою УЗД також можна візуалізувати крововилив у сітківку та набряк сосочка зорового нерва. Сонографічне дослідження зорового нерва та периневрію дозволяє оцінити внутрішньочерепний тиск, оскільки ЦСР в піхві зорового нерва взаємодіє з внутрішньочерепним простором. Цей метод набирає великої значущості, особливо при спостереженні за підвищенням внутрішньочерепного тиску (Рис. 7).
Рис. 7. Одинадцятирічний хлопчик з підвищеним внутрішньочерепним тиском; піхва зорового нерва виглядає розширеною.
ТОВЩИНА КОМПЛЕКСА ІНТИМА-МЕДІА (ТКІМ)
Сонографічна візуалізація, а також вимірювання товщини комплексу інтима-медіа (ТКІМ) і загальної сонної артерії (ЗСА) – добре відпрацьований неінвазивний метод для визначення преатеросклеротичних змін. Такі дослідження застосовуються у дітей та підлітків при необхідності точного вимірювання структур, менших ніж один міліметр.
Такі перспективні УЗД методи як візуалізація з придушенням спеклів (Speckle Reduction Imaging – SRI) та компаундна візуалізація значно покращують якість зображень, особливо для позначення меж тонких структур. Вони володіють високою вимірювальною точністю. Однак, візуалізації гармоніки тканин варто уникати при дослідженні тонких структур, оскільки роздільна здатність погіршується з цим методом. Вимірювання ТКІМ – це важливий діагностичний критерій, який пов’язаний з багатьма захворюваннями з підвищеним ризиком зміни васкулярної стінки. Цей метод особливо добре досліджували по відношенню до дітей та підлітків з проблемою ожиріння.
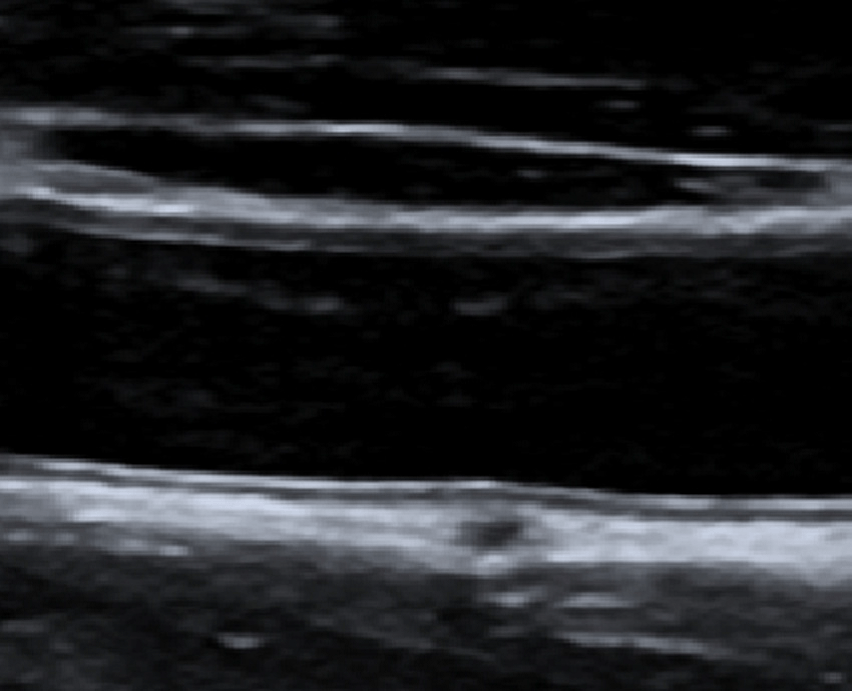
Діти з надлишковою вагою мають значно підвищену ТКІМ порівняно з дітьми з нормальною вагою. Підвищена ТКІМ значно корелює з підвищенням систолічного і діастолічного тиску, гіпертригліцеридемією, підвищенням рівня глюкози і С-реактивного білка (high-sensitivity C-reactive protein – hs-CRP) як параметра хронічного запального процесу. Істотне зниження ваги підлітків з пробемою ожиріння в програмі раннього втручання призводить до відповідного істотного зниження ТКІМ (Рис. 8).
Рис. 8. Візуалізація ТКІМ в стінці загальної сонної артерії (arteria carotis communis – ACC) на протилежній стороні від датчика
УЗД ДІЛЯНКИ ШИЇ
Для того, щоб зрозуміти суть патологій, котрі часто зустрічаються при УЗД шиї у дітей, необхідно згадати основні моменти розвитку плоду. У людському ембріоні зяброві (фарингеальні) дуги формують краніальний кінець первинного кишківника. До четвертого ембріонального тижня утворюються п’ять фарингеальних кишень з шістьма фарингеальними дугами і чотирма фарингеальними щілинами. Так звані «мембрани, що замикаються» відокремлюють внутрішні фарингеальні кишені від зовнішніх фарингеальной щілин. Щитовидна залоза розвивається біля основи (сліпий отвір – foramen caecum) первинної глотки, звідки щитовидно-язикова протока продовжується каудально, як канал для подальшого опущення щитовидної залози. До поширених патологічних процесів дитячого віку відносяться: фіброматоз шиї, серединні і латеральні цервікальні кісти, запальні зміни, пухлиноподібні вогнища і захворювання слинних залоз.
Фіброматоз шиї – це доброякісна проліферація фіброзної тканини в нижню третину грудино-ключично-соскоподібного м’яза. Типові клінічні зміни з тортиколізом з’являються незабаром після народження, причому підборіддя повернене в протилежну до ураження сторону. УЗД показує гіперехогенне, частково негомогенне утворення всередині запаленого грудино-ключично-соскоподібного м’яза. Етіологія не до кінця з’ясована. Докази вказують на мікрокрововиливи, пов’язані з пологами з подальшою фіброзно-рубцевою трансформацією (Рис. 9).
Рис. 9. (a і b) Фіброматоз шиї справа з нормальним грудино-ключично-соскоподібним м’язом зліва.
Бранхіогенна кіста (бічна кіста шиї) – локальна інтраепітеліальна адгезія (local inter-epithelial adhesion – LIAD), розвивається між внутрішніми фарингеальними кишенями (2, 3 або 4) та відповідними зовнішніми фарингеальними щілинами. Якщо процес тривалий – формується фістула (свищ); якщо фістула розривається з одного боку – утворюється пазуха; якщо з двох сторін – бранхіогенна кіста (Рис. 10).
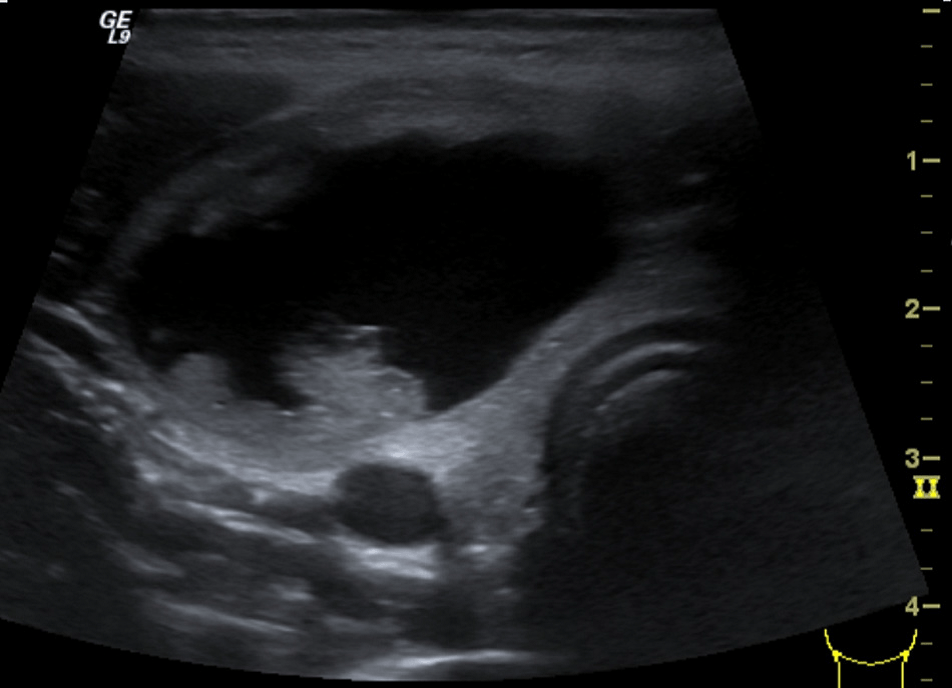
Рис. 10. Бранхіогенна кіста (бічна кіста шиї) з центральними ділянками середньої ехогенності, викликаними крововиливами в кісті.
Кіста щитовидно-язикової протоки (серединна кіста шиї) виникає при неповній регресії щитовидно-язикової протоки; ці кісти простелені циліндричним епітелієм і знаходяться посередині між основою язика та щитовидною залозою (Рис. 11).
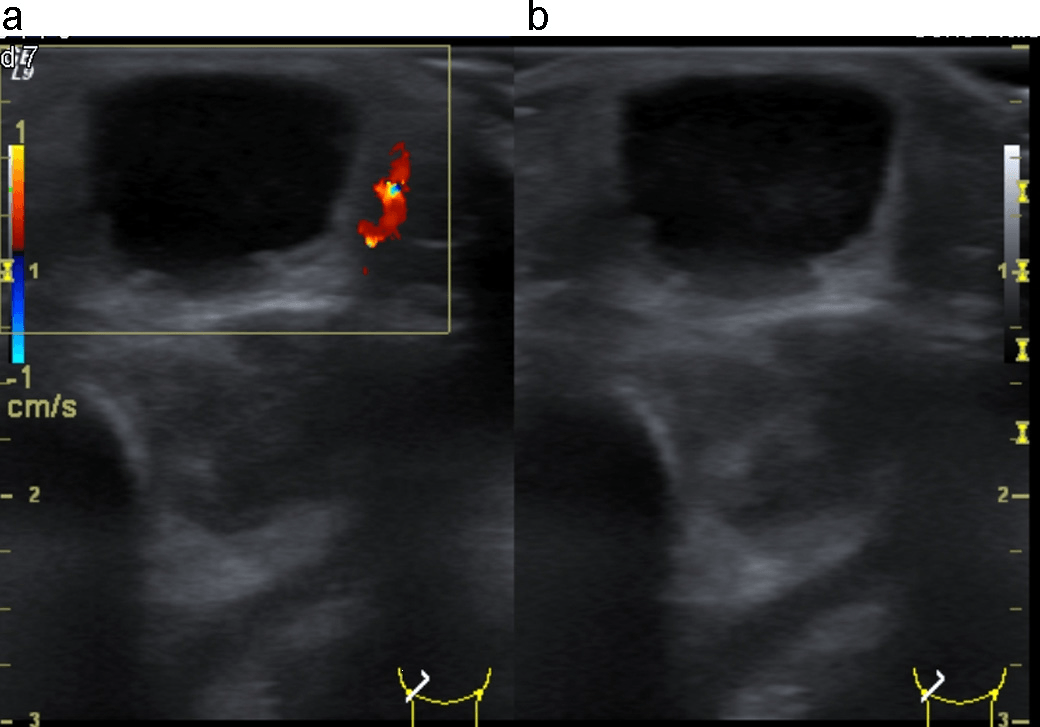
Рис. 11. Кіста щитовидно-язикової протоки (серединна кіста шиї), в даному випадку в правій частці щитовидної залози. Гіперехогенний осад по протилежному периметру, найочевидніше – залишки попереднього крововиливу або запалення.
Інфекційні процеси
Існує цілий ряд реактивних запальних процесів лімфовузлів, викликаних вірусними або бактеріальними інфекціями та чужорідними тілами. При ускладненні утворюються абсцеси (Рис. 12, 13).
Рис. 12. (a і b) Шестирічний хлопчик з абдомінальним болем і збільшеними шийними лімфовузлами. Серологічно доведена інфекція вірусом Епштейна-Барр. Збільшення лімфовузлів може тривати кілька тижнів, останні можуть бути болючими та неболючими.
Рис. 13. (a і b) Чотирьохрічна дівчинка з болючим підщелепним запаленням. Характерна картина підщелепного абсцесу на УЗД.
Варто відзначити три особливих запальних захворювання, для яких характерна специфічна морфологічна картина в лімфовузлах, а саме:
1. Синдром Кавасакі (слизисто-шкірний синдром з ураженням лімфовузлів);
2. Інфекція Bartonella henselae (хвороба котячих подряпин);
3. Інфекція атиповими мікобактеріями.
Синдром Кавасакі (слизисто-шкірний синдром з ураженням лімфовузлів) – це гарячкове, системне захворювання, яке характеризується васкулітом дрібних і середніх артерій. Крім того, може мати місце системне запалення інших органів. За даними літератури, частота даного захворювання складає 9 : 100000, найчастіше виникає в Азії.
Клінічно протікає в трьох фазах:
1. Гостра фебрильна стадія;
2. Підгостра стадія: 2-4 тижні з лущенням на ногах і руках;
3. Період одужання: протягом декількох місяців (Рис. 14).
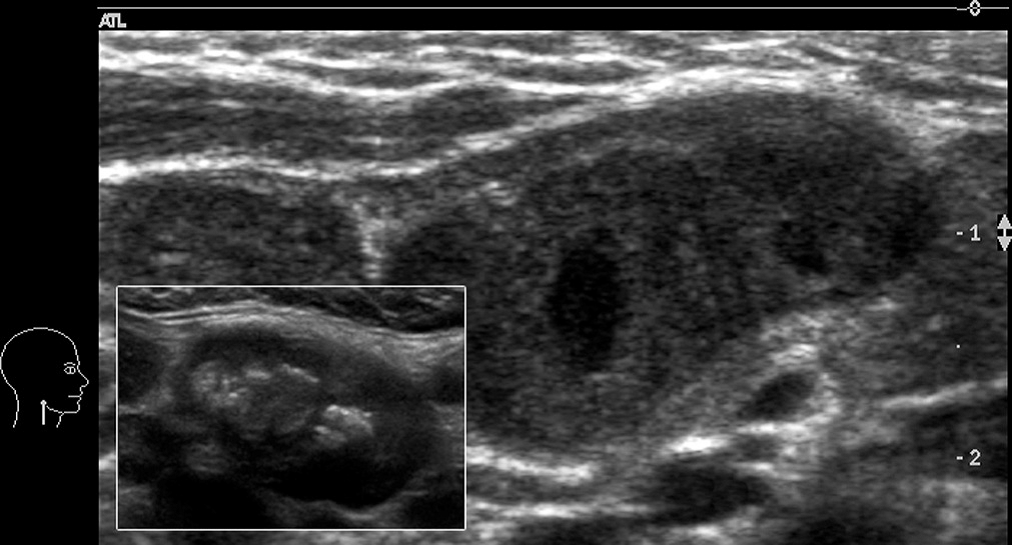
Рис. 14. Хвороба Кавасакі (васкуліт нез’ясованого генезу). Збільшені лімфовузли у вигляді ланцюга з недиференційованою, грубою гранулярною внутрішньою архітектурою. Вставка: внутрішньовузлове васкулярне дерево збережене, але є зміщена гіперперфузійна картина.
Хвороба котячих подряпин
Інфекційна хвороба, яка передається через пошкоджену шкіру (подряпини) або котячими блохами. Збудник: Bartonella henselae. Клінічно проявляється червоно-коричневими папулами, які з’являються від 2 до 10 днів, і зникають після декількох днів / тижнів.
Можливі ускладнення: енцефаліт, поліневрит, нейроретиніт, ураження паренхіми органу (Рис. 15).
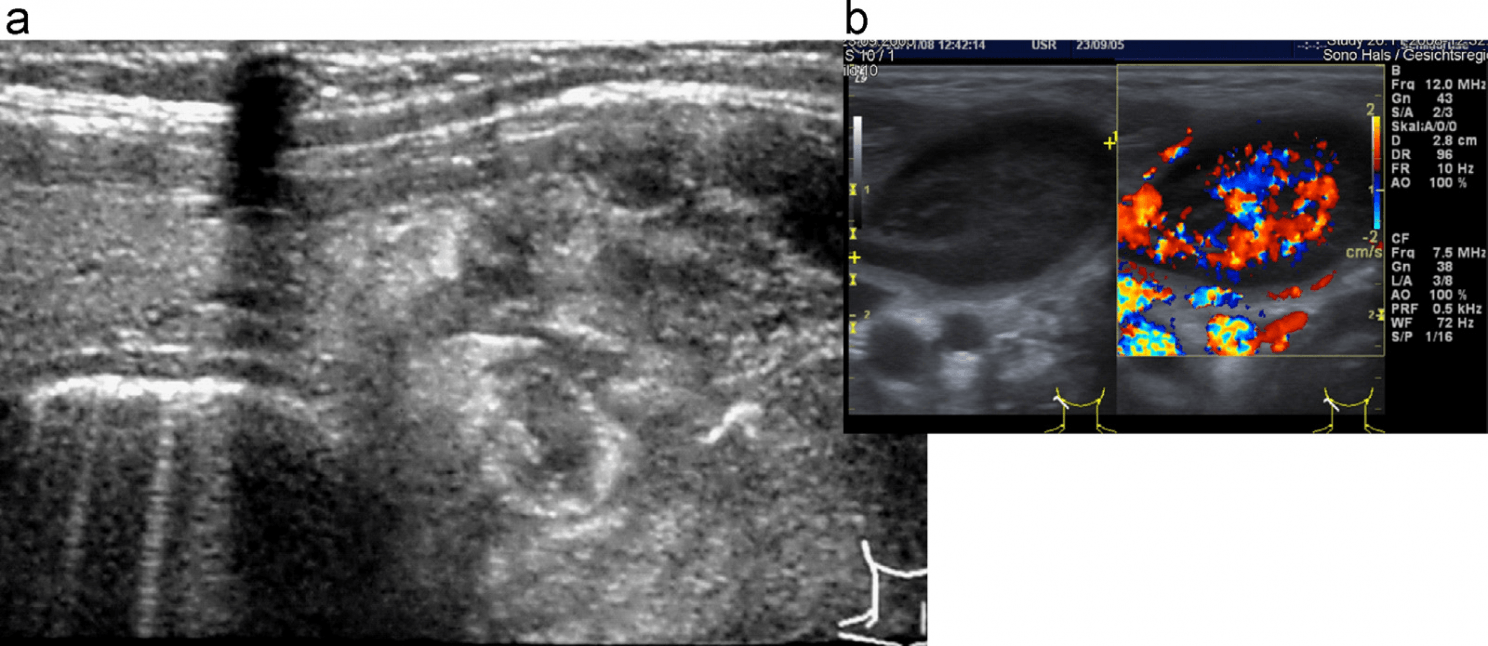
Рис. 15. Лівобічне запалення аксилярного лімфовузла (Bartonella henselae). Круглий, гіпоехогенний лімфовузол з лійкоподібними здавленими воротами. Значна запальна гіперваскуляризація на КДК. Вставка: характерні, майже патогномонічні УЗ дані.
Інфекція атиповими мікобактеріями (Рис. 16)
Злоякісні процеси, які часто зустрічаються в ділянці шиї (злоякісні лімфоми та метастази з нейробластомами) (Рис. 17).
Рис. 16. Атипова мікобактеріальна інфекція шийного лімфовузла (M. Avium). Гранулематозне запалення з двома центральними «холодними» абсцесами. Вставка: пізня стадія хвороби з накопиченням кальцинозних конкрементів. УЗД дані майже патогномонічні для мікобактеріозу.
Рис. 17. (a і b) Семирічний хлопчик із утворенням шиї і середостіння, яке швидко росте: неходжкінська лімфома (НХЛ).
УЗД ЩИТОВИДНОЇ ЗАЛОЗИ
До раннього шкільного віку паренхіма щитовидної залози (ЩЗ) відносно гомогенна. Під час пубертатного періоду, ЩЗ збільшується в розмірі і стає більш негомогенною (ювенільний зоб) (на УЗД гіпоехогенні ділянки в обох долях).
Ключовими для диференціації з аутоімунним тіреоїдитом є дані КДК, що не змінені в нормальній щитовидній залозі, але помітні (див. нижче) коли орган запалений.
Оскільки є тенденція до поліпшення при дієтичному забезпеченні йодом, середньостатистичні значення обсягу ЩЗ в загальній популяції зменшуються.
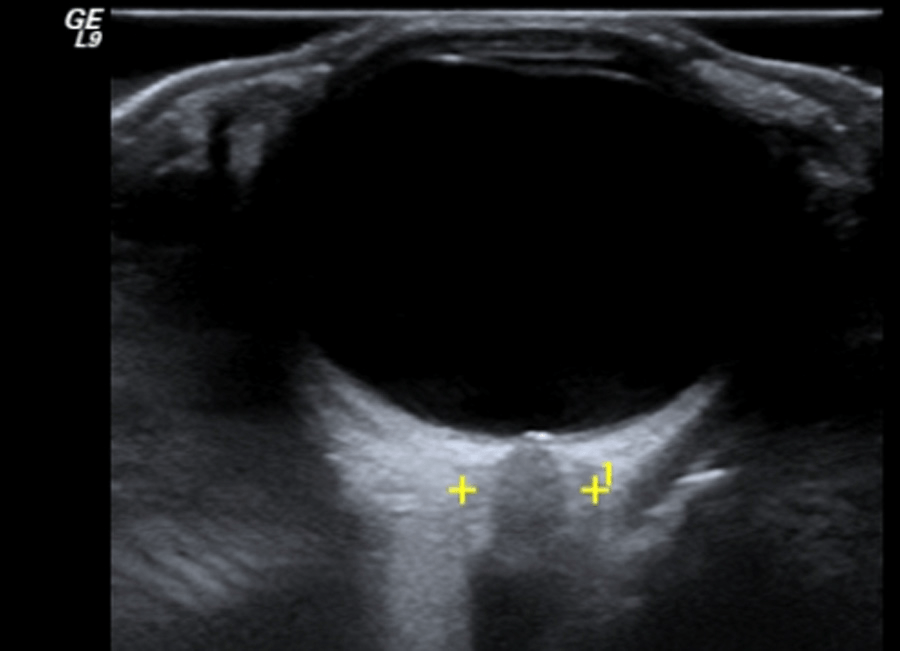
При природженому гіпотиреоїдизмі, обидві частки гіпопластичні та погано васкуляризовані. Раніше таких пацієнтів називали «атиреотиками». Паратиреоїдні залози можна зазвичай візуалізувати за допомогою УЗД з високою роздільною здатністю. Вони мають овоїдную форму та гіпоехогенну текстуру (Рис. 18).
Рис. 18. Паратиреоїдні залози в типовому місці розташування у 15-річної дівчинки.
Аденоми щитовидної залози мають нестабільну морфологію. Встановлення діагнозу за допомогою УЗД ускладнене, а дані можуть оцінюватися тільки в межах додаткового клінічного контексту. Швидке зростання та посилений кровотік з неправильними хвилястими судинами, вимагають негайного гістологічного дослідження.
Для карцином ЩЗ характерне відносно поступове, тривале збільшення в обсязі, негомегенні вузли з випучуванням поверхні ЩЗ, а також гіперперфузія з неправильними судинами різного діаметру, що є найважливішим критерієм злоякісності. Високочутливий спектральний доплер також може показати змішану картину артеріо-венозного кровотоку.
Аутоімунний тиреоїдит (Хашимото).
Прогресує, проходячи кілька стадій, кожна з типовою кореляцією на УЗД.
Для ранньої стадії (стадія 1) характерно всього лише помірне збільшення органу і злегка гіперехогенна текстура. Порівняно з ювенільним зобом, гіпоехогенні ділянки спостерігаються в основному по периферії паренхіми. Перфузія стає вище нормального рівня.
Для другої стадії характерна повна маніфестація (стадію 2 розділяють на 3 підстадії).
Стадія IIa – значне збільшення органу з явними змінами ехогенності: центральна негомогенна гіперехогенна паренхіма з ретикулярними септами та вузлами, периферія фокально-гіпоехогенна. КДК показує значно гіперваскуляризовану тканину.
Стадія IIb – протікає як клімакс хвороби. ЩЗ виражено запалена. Розвиваються множинні нодулярні гіперехогенні ділянки. Перфузія значно збільшується («палаюче пекло»). Швидкість кровотоку в нижній артерії ЩЗ (підходить для вимірювання) стає вище 25 см/с.
Стадія IIc – після декількох років маніфестації, обсяг органу зменшується з появою ундулюючих контурів на поверхні ЩЗ. Васкулярний просвіт зменшується. Тільки в гіпоехогенних периферійних ділянках можна виявити бурхливу перфузію.
Стадія III – являє собою перехід в класичну атрофічну форму дорослого Хашимото-тиреоїдиту, який рідко спостерігається у підлітків. ЩЗ значно зменшується та перетворюється на сполучну тканину з псевдо-кістами (рис. 19).
Рис. 19. Дівчинка з еутиреоїдним зобом і масивною гіперперфузією (стадія IIb аутоімунного тиреоїдиту Хашимото).
Гіпертиреоз Грейвса (Базедова-Грейвса)
Як і тиреоїдит Хашимото, хвороба Грейвса протікає в кілька стадій.
Стадія I проявляється збільшенням органу, фокально посиленою гіперехогенністю та натяком на нодулярне утворення. Гранулярна картина утворюється в паренхімі, а васкуляризація починає збільшуватися (рання гіперваскуляризація).
Стадія II – великий, жорсткий зоб з переважно гіперехогенною тканиною ЩЗ, з вкрапленнями кількох гіпоехогенних ділянок. Патогномонічною ознакою є значна гіперваскуляризація з випуклими, черв’якоподібними судинами («палаюче пекло»).
Стадія III – рідко зустрічається і часто є наслідком небажання пацієнта лікуватися. Масивна ЩЗ з великими кістами шиї і надмірно високою швидкістю кровотоку (вище 40 см/с). Особливою патологічною ознакою хвороби Грейвса є гіперехогенна, грубо-гранулярна псевдогіпертрофія скелетної мускулатури, яка спостерігається у всіх пацієнтів на пізніх стадіях. Такий вид ендокринної міопатії розвивається у всіх кінцівках, а також викликає (у зв’язку зі збільшенням ретробульбурних м’язів ока (Mm. Recti) і набряком ретробульбарной жирової тканини) добре відомий екзофтальм Базедова-Грейвса (Рис. 20).
Рис. 20. (a і b) Тринадцятирічна дівчинка з гіпертиреозом. Переважно гіперехогенна ЩЗ з великими черв’якоподібними судинами (хвороба Грейвса, стадія II). Судини більш об’ємні, ніж при аутоімунному тиреоїдиті (Хашимото).
УЗД ОРГАНІВ МОШОНКИ
Показами до обстеження чоловічих геніталій є гострі і хронічні зміни. У зв’язку з невідкладністю і важливістю адекватного обстеження у випадках гострої патології ми, в першу чергу, описуємо саме їх.
Клінічно, «гостра мошонка» проявляється запаленням, почервонінням і, зазвичай, болем. Однак, варто зауважити, що у немовлят клінічні симптоми можуть бути слабко виражені, що ускладнює клінічну ситуацію, тому існує ризик недооцінки і запізнілого лікування.
У дітей, гостра мошонка – це невідкладний стан, при якому через неадекватну діагностику втрачається час і, відповідно, внаслідок неадекватного лікування розвиваються безповоротні ушкодження тестикулярної паренхіми.
Диференціальна діагностика гострої мошонки з наступними захворюваннями необхідна для роз’яснення причини такого стану: перекрут яєчка, перекрут гідатіди, гострий епідидиміт, гострий орхіт, пурпура Шенлейн-Геноха, пухлина, травма і защемлена пахова грижа.
Для усунення непорозумінь номенклатури (термінології), три терміни, що характеризуються збором рідини в мошонці, повинні більш чітко описуватися, оскільки їх іноді плутають.
Гідроцеле – це накопичення рідини в мошонці через з’єднання черевної та мошонкової порожнини, яке виникає при неповному закритті вагінального відростка (рrocessus vaginalis). Фуніколоцеле – це накопичення рідини дистально від облітерованого вагінального відростка. Постпубертатне сперматоцеле виникає часто після травми, і проявляється як анехогенне кістозне утворення, яке зазвичай локалізується на головці придатка яєчка.
Нормальна анатомія на УЗД
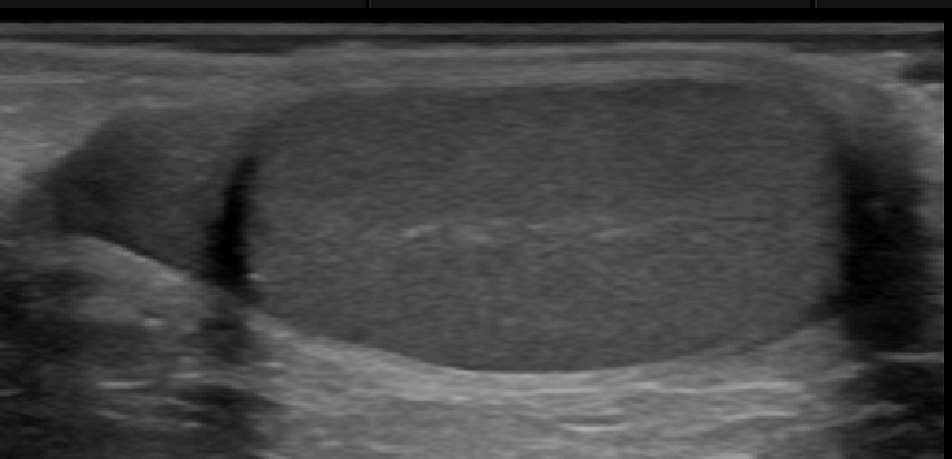
Ехогенність яєчка низька до пубертатного віку, а далі, після дев’яти років, поступово зростає. Ця зміна наймовірніше є причиною дозрівання тубулярного апарату і розвитку статевих клітин (Рис. 21).
Рис. 21. Гомогенна тестикулярна паренхіма з нормальною структурою воріт і делікатною стінкою мошонки.
Методика дослідження
Для адекватного дослідження ділянки мошонки необхідний близькофокусний лінійний датчик з високою роздільною здатністю, при цьому довжина хвилі повинна бути гранично низькою (9-15 МГц). КДК обов’язкове, включаючи можливість вимірювання повільних потоків (1‑2 см/с).
Перекрут яєчка
Перекрут яєчка – це ротація, яка виникає навколо поздовжньої осі канатика, і завжди повертається в медіальну сторону. Ми розрізняємо інтра- та екстравагінальний типи перекруту яєчка, які бувають у співвідношенні 9:1 (екстравагінальні відбуваються в основному в новонародженому періоді). Існують два вікові піки: перший – в дитячому, інший – в препубертатному періоді. Частота виникнення, за даними літератури, – приблизно 1 : 4000. Прогноз на збереження життєздатності тканин яєчка у великій мірі залежить від минулих годин з моменту появи клінічних симптомів і до встановлення діагнозу. Якщо перекрут звільняють протягом 6 годин, збереження органу буде майже в 100% випадків, а після 6 годин, відповідно, прогноз погіршується.
Інтравагінальний перекрут яєчка з яєчком, накрученим навколо сім’яного канатика в межах вагінальної оболонки, виникає тільки в тих випадках, коли яєчко вільно переміщається в цій оболонці. У нормі, вагінальна оболонка зростається з латеральними і передніми частинами яєчка і придатка яєчка, запобігаючи перекруту. Ця аномалія часто двостороння, тому дитячі хірурги рекомендують робити профілактичну фіксацію другого яєчка.
При екстра- або суправагінальному перекруті яєчко перекручується разом з вагінальної оболонкою навколо сім’яного канатика. У цьому випадку судини виглядають як спіраль закручена в напрямку до поверхневого пахового кільця. Порушення кровотоку залежить від ступеня перекрута та тривалості странгуляції. Венозний відтік може бути значно знижений, особливо у випадках з меншим ступенем перекрута, незважаючи на збережений артеріальний приплив. Ендокринний апарат (клітини Сертолі і Лейдіга) є набагато більш резистентним, ніж поверхневий епітелій яєчка, який безповоротно пошкоджується за декілька годин.
УЗД перекрута яєчка
До ранніх УЗ ознака перекрута яєчка відносяться збільшення яєчка і придатка з початковим зниженням ехогенності. Часто спостерігається невелике супутнє гідроцеле і практично завжди набряк стінки мошонки. Пізні УЗ ознаки перекрута яєчка включають руйнування текстури паренхіми яєчка з гіпоехогенними і гіперехогенними ділянками, що вказують на набряк, інфаркт і крововилив. Більше того, пізня фаза демонструє реактивну гіперемію стінки мошонки, що описується в англо-американській літературі як «ознака вінця пропущеного перекрута – Halo Sign of Missed Torsion» (Рис. 22).
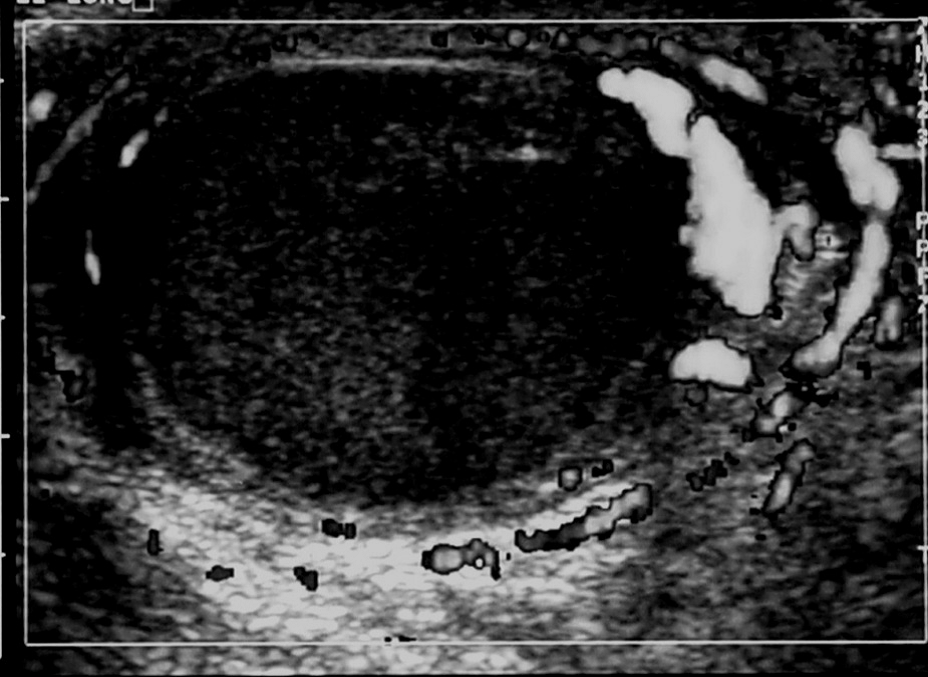
Рис. 22. Гіпоехогенне негомогенне яєчко з відсутністю доказів про наявність центральних судин. Значне запалення стінки мошонки є ознакою гострої патології.
На закінчення можна сказати, що УЗД пацієнтів з симптомами гострої мошонки, проведене досвідченим дослідником за допомогою високоякісної УЗ апаратури та відповідних датчиків – дуже надійний метод для підтвердження або виключення перекрута яєчка.
Це захищає пацієнта від непотрібних хірургічних втручань, а також знижує вартість лікування.
Перекрут гідатиди
Гідатида, більш відома як гідатида Морганьї (Appendix testis), є залишком Мюллерової протоки на верхній частині яєчка. Гідатида Галлера (Appendix epididymis) є залишком мезонефральних трубочок на голівці придатка яєчка. Перекрут цих структур викликає набряк стінки мошонки і реактивне гідроцеле. УЗД часто демонструє так звану «третю структуру», яка спостерігається тільки при наявності гідроцеле. Це звичайна гіперваскуляризована на периферії гидатида. Якщо супутнього гідроцеле немає, тоді перекрут гідатиди неможливо знайти при УЗД.
Орхіт/епідидиміт
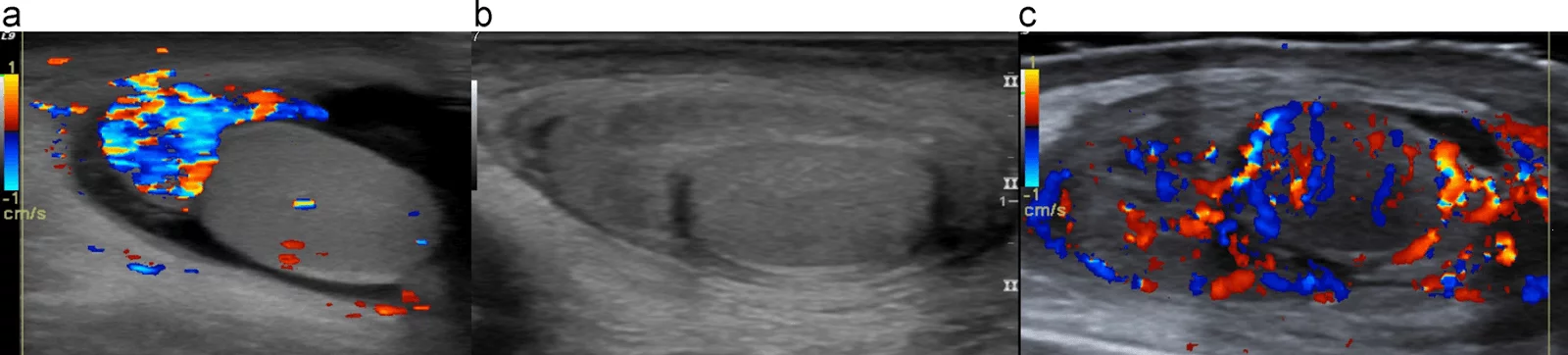
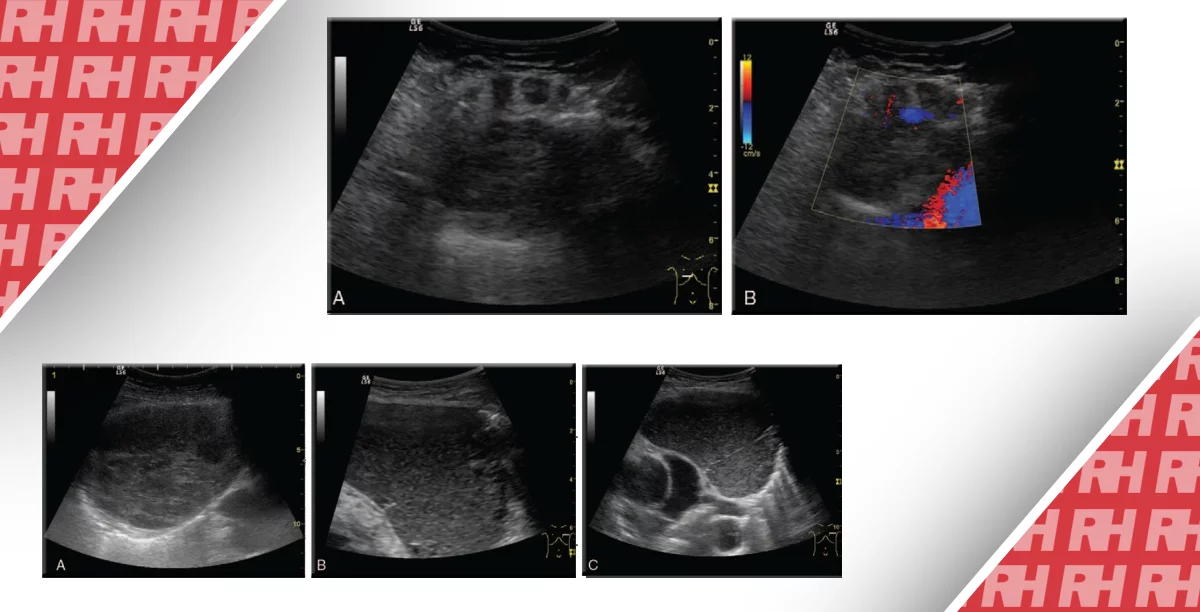
Ці запальні процеси часто виникають через вірусні інфекції. Тут варто згадати про епідемічний паротит, адено-, еховіруси та вірус Коксакі. До малопоширених причин відносять бактеріальні інфекції, алергічні, травматичні або автоімунні захворювання. На сучасному етапі запальні зміни набагато частіше зустрічаються, ніж раніше, часто в поєднанні з орхітом і епідидимітом (епідидиміт-орхіт). В органах спостерігається посилена перфузія крові і, як правило, втрата (або в окремих випадках, посилення) ехогенності. Також, як загальні ознаки може спостерігатися набряк стінки мошонки і реактивне гідроцеле (Рис. 23).
Рис. 23. (a – c) Ізольований епідидиміт (а), комбінований епідидиміт та орхіт (b і c).
Травмування
При травмах анамнез повинен орієнтувати вас на діагноз. Паренхіма негомогенна, тіло яєчка часто опухле. Реактивна гіперемія може виникати при легких травмах. Відсутність доказів перфузії може вказувати на розрив або авульсію васкулярної ніжки при більш важких травмах. Основне завдання – це диференціація вогнищ з і без розриву мембран, а також оцінка життєздатності тканин.
ПУХЛИНИ ЯЄЧКА
При пухлинах яєчка, орган переважно гіпоехогенний і збільшений. Інфільтрація виникає при лейкемії, нейробластомі і саркомі Юінга. Тератоми, як правило, часто супроводжуються змішаною ехогенністю з кістозними компонентами і неправильною структурою. Сімдесят відсотків пухлин є герміногенними (пухлина жовточного мішка), які відносяться до групи найпоширеніших, сюди також входять тератоми і семіноми. Тридцять відсотків пухлин відносяться до негерміногенних, разом з саркомами, пухлинами Лейдіга та Сертолі та лімфомами.
Рабдоміосаркома
Рабдоміосаркома – пухлина м’яких тканин, яка найчастіше зустрічається в дитинстві, розвивається від примітивних мезенхімальних клітин, які диференціюються в поперечнопосмуговані м’язи. Вони можуть виникати у всіх частинах тіла, але найчастіше зустрічається в урогенітальному тракті. Середній вік встановлення діагнозу становить 4-5 років. Клінічна маніфестація залежить від місця розташування пухлини.
Рабдоміосаркома – це жорстка або частково кістозна пухлина, яка має властивості місцевої інвазії і метастазує в легені, печінку і кістки. Вид пухлини при УЗД часто гетерогенний. У сечовому міхурі пухлина набуває більш гомогенного і гіперехогенного вигляду, тому її неможливо відрізнити від стінки сечового міхура. Якщо присутні кістозні компоненти, пухлина виглядає часточковою. На КДК для такої пухлини не характерна васкулярная інвазія (Рис. 24).
Рис. 24. Рабдоміосаркома каудального полюсу правого яєчка. Вставка: патологічні солітарні аморфні васкулярні залишки в саркоматозній осередковій тканині.
Варикоцеле
Варикоцеле – це збільшення лозоподібного венозного сплетіння. В першу чергу, УЗД показує множинні гіпоехогенні структури, які оточують і придаток яєчка. Такі структури чітко наповнюються і збільшуються під час проби Вальсальви. Варикоцеле частіше зустрічаються з лівого боку (Рис. 25).
Рис. 25. (a і b) Варикоцеле. Проба Вальсальви викликає значне збільшення обсягу судин лозовидного сплетення.
Адреногенітальний синдром (ВГКН – вроджена гіперплазія кори наднирників).
При адреногенітальному синдромі ВГКН – гіпоехогенна, ектопічна тканина наднирників може виявлятися в самому яєчку, часто з обох сторін і, в основному, невеликого розміру. Контур яєчка спотворений. Утворення ексцентричні і часто оточують середостіння яєчка.
Мікролітіаз
Мікролітіаз описують як гіперехогенне відображення в різних кількостях; етіологія не до кінця відома. У сучасній літературі перестали вважати біопсію потрібною в таких випадках. Частота мікролітіазу як супутнього захворювання при інших аномаліях яєчка становить від 1 до 20%. Частота виникнення у пацієнтів без клінічного прояву становить приблизно 2-3%. Частота мікролітіазу в тканині навколо пухлин яєчка – до 50%. У пацієнтів контрольної групи з мікролітіазом, менше ніж в 1% випадків утворюється пухлина. Таким чином, можна визначити наступні рекомендації: робити контралатеральну біопсію тільки тим пацієнтам, у яких є рак яєчка і мікролітіаз в контралатеральному яєчку. Отже, такі пацієнти повинні щорічно проходити УЗ контроль. Пацієнтам без пухлин із супутнім мікролітіазом не потрібно робити контрольного УЗД, тому що мікролітіаз яєчка вже не вважається фактором ризику розвитку раку яєчка при відсутності додаткових факторів (Рис. 26).
Рис. 26. (a і b) Мікролітіаз яєчка в різних ступенях розвитку у двох пацієнтів.
УЗД також є методом вибору для дослідження хронічних змін в яєчках, оскільки цей вид обстеження є широкодоступним, а коротка довжина хвилі перевершує всі інші методи діагностики органів мошонки в просторовому розрішенні.
ЗАКЛЮЧЕННЯ
Клінічні докази вказують на те, що УЗД має найкращу просторову роздільну здатність серед усіх методів візуалізації в міліметровому і мікрометровому діапазоні (100-1000 мкм), та може вважатися найкращим методом для дослідження поверхневих патологічних утворень органів, розташованих близько до поверхні. Також УЗД забезпечує важливою інформацією про характерну, часто патогномонічу архітектуру тканин при патологічних процесах. Жоден інший неінвазивний метод візуалізації не здатний надавати інформацію так швидко, надійно і точно.
УЗД видає актуальну діагностичну інформацію динамічно і візуалізує досліджувану патологію в реальному часі. В руках досвідченого дослідника – це відмінний, зручний для пацієнта інструмент, який дає неінвазивний доступ без випромінювання для швидкого і надійного встановлення діагнозу.
Ультразвукова діагностична система з технологією еластографії зсувної хвилі Siemens Acuson S2000. Кращі пропозиції від компанії RH.