🤖 Короткий переказ від ШІ
Трансректальне ультразвукове дослідження (ТРУЗД) є ключовим методом діагностики передміхурової залози, що надає важливу інформацію при доброякісних та злоякісних ураженнях, таких як ДГПЗ та РПЗ. Надійність та точність цих досліджень залежить від якості УЗД апаратів.
Застосування новітніх ультразвукових методів, таких як кольорова та енергетична доплерографія, а також УДКП та еластографія, значно покращує виявлення РПЗ та допомагає у виборі тактики лікування. Однак, попри прогрес, ТРУЗД залишається допоміжним методом, а біопсія під його контролем – “золотим стандартом” для остаточної діагностики.
✅ Ключові тези зі статті:
- Діагностика: ТРУЗД є основним методом візуалізації передміхурової залози, що допомагає у виявленні патологій, але його чутливість для РПЗ обмежена.
- Лікування: ТРУЗД відіграє важливу роль у наведенні для біопсії та моніторингу стану пацієнтів після лікування.
- Переваги: ТРУЗД дозволяє оцінити розміри, структуру, кровопостачання передміхурової залози та допомагає у проведенні біопсії.
- Обмеження: Сірошкальне ТРУЗД має низьку позитивну прогностичну цінність для діагностики РПЗ, а додаткові методи (доплерографія, контраст) покращують, але не повністю вирішують проблему виявлення.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
АВТОРИ: Ahmet T. Turgut, MD, Erkan Kismali, MD, Vikram S. Dogra, MD
Трансректальне ультразвукове дослідження (ТРУЗД) традиційно розглядається як ключовий тест для дослідження передміхурової залози, яке забезпечує клінічно важливу інформацію при доброякісних і злоякісних ураженнях, у тому числі доброякісній гіперплазії передміхурової залози (ДГПЗ), простатиті, обструктивному безплідді і раці передміхурової залози (РПЗ). На сьогоднішній день основними причинами для направлення пацієнтів на ТРУЗД є виявлення та оцінка РПЗ, а також ультразвукове наведення при біопсії передміхурової залози.
СОНОГРАФІЧНА АНАТОМІЯ
У зрілому віці нормальна передміхурова залоза має середні розміри від 4,0 до 4,5 см, від 2,5 до 3,0 см та від 3,0 до 4,0 см в поперечному, передньо-задньому і краніо-каудальному напрямках, відповідно. Ця залоза обмежена тонкою псевдокапсулою, яку практично не можна відрізнити від оточуючих фасціальних площин. Анатомічно, судинно-нервові пучки, які перфорують капсулу передміхурової залози мають вирішальне значення, тому що вони є основним місцем слабкості капсульного апарату і потенційно схильні впливати на пухлинний процес. Картина нормальної передміхурової залози при ТРУЗД залежить від віку. У молодих чоловіків гіперплазія залозистої тканини є незначною, в той час як у чоловіків у зрілому віці, передміхурова залоза перетворюється у велику залозу з більш округлою формою внаслідок розвитку ДГПЗ.
В середньому 70% нормальної передміхурової залози складається із залозистих елементів, а решта 30% – складаються із фіброзно-м’язової строми. Залозиста тканина передміхурової залози зазвичай складається з внутрішніх залоз, які мають перехідну зону і навколосечівникову залозисту тканину, і зовнішніх залоз, які займають периферичну і центральну зони. ТРУЗД, як правило, дозволяє відрізнити перехідну зону, яка розташована попереду, як гіпоехогенну область, від периферичної зони, яка є ехогенною і однорідною за своєю ехотекстурою, в порівнянні з іншою частиною залози. Центральна зона, з іншого боку, сумнівно, що відрізняється від периферичної зони у здорових дорослих чоловіків. Перехідна зона є основним місцем для гіперпластичних змін, становить більшу частину в пропорційному співвідношенні тканини передміхурової залози у літніх чоловіків, і може додатково бути місцем розвитку РПЗ приблизно в 20%. Слід зазначити, що від 1% до 5% РПЗ розташований в центральній зоні. Периферична зона є також основним місцем розвитку хронічного простатиту, призводить приблизно до 70% РПЗ. Ракове ураження в перехідній зоні, з іншого боку, навряд чи можна відрізнити від вузликів при ДГПЗ за даними ТРУЗД.
ТЕХНІКА СКАНУВАННЯ
На сьогодні, біпланові датчики в поєднанні з кінцевими і бічними датчиками дозволяють отримувати багатоплощинне зображення у напівкоронарній, осьовій, сагітальній проекціях при трансректальному скануванні передміхурової залози. Технічно, датчики з частотою від 5 до 8 МГц забезпечують більшу роздільну здатність для периферичної частини залози, що має вирішальне значення для точності вибору зразків в ході процедури біопсії. Повітряні бульбашки – артефакти, негативно впливають на якість зображення, і уникнути цього можна за допомогою ультразвукового гелю, який наноситься на латексний презерватив, одягнений на датчик. Самостійний прийом клізми перед процедурою допомагає у виведенні газу і калу, а це ще один фактор, який може призвести до спотворення зображення при ТРУЗД. Супутнє пальцеве ректальне дослідження може бути корисним для виявлення підозрілих знахідок при фізикальному обстеженні, які корелюють з аномаліями при ТРУЗД. Більшість експертів вважають, що кращим є положення пацієнта,який лежить на лівому боці. Насамкінець, повний сечовий міхур забезпечує чисте поле зору з основою передміхурової залози, що допомагає її кращій візуалізації. Тим не менш, за спостереженням авторів, клінічна практика така, що сечовий міхур не повинен бути перерозтягненим, бо це може призвести до нетримання сечі під час супутньої процедури біопсії.
ТРУЗД оцінка передміхурової залози починається із системного сканування в поперечній або напівкоронарній площині, починаючи від рівня сім’яних пухирців, які прилягають до основи передміхурової залози, і продовжуючи вниз до апікального рівня з візуалізацією залозистих зон. Потім проводиться сканування в сагітальній площині для виявлення будь–якої часткової асиметрії, а також і для підтвердження підозрілих утворень, виявлених при осьовому або коронарному скануванні. Простатичні і екстрапростатичні структури, які оцінюються при системному підході, перераховані в таблиці 1. Важливо зазначити, що формула еліпсоїда дозволяє обчислити об’єм передміхурової залози за допомогою діаметрів по ортогональних осях:
де td, apd і ccd представляють поперечний, передньо-задній і краніо-каудальний діаметри передміхурової залози, відповідно.
Таблиця 1.
Анатомічні структури, які оцінюються при ТРУЗД
|
Зовнішня залоза Внутрішня залоза Передні фіброзно-м’язові тканини Капсула Періпростатична жирова тканина Періпростатичні лімфатичні вузли Судинно-нервові пучки Еякуляторні протоки Сім’яні пухирці Стінка прямої кишки Сечівник |
У хворих з діагнозом РПЗ оцінка об’єму передміхурової залози може бути необхідна для проведення відповідної терапії. Правильна оцінка може бути також ефективна при лікуванні пацієнтів, яким не поставлений діагноз раку, оскільки це може допомогти у проведенні прямої терапії пацієнтам при лікуванні симптомів обструкції нижніх сечовивідних шляхів. Трансректальний ультразвуковий підхід до передміхурової залози також дозволяє оператору виконувати різні діагностичні та терапевтичні втручання при РПЗ завдяки більш високій роздільній здатності у порівнянні з іншими методиками ультразвукового сканування.
РАК ПЕРЕДМІХУРОВОЇ ЗАЛОЗИ
РПЗ є другою провідною причиною, що призводить до розвитку раку, пов’язаною зі смертністю у чоловіків. Крім того, що це захворювання зараховують до розряду основних медичних проблем, це також важливе питання у сфері суспільної охорони здоров’я, оскільки воно призводить до значних економічних витрат. Хоча раннє виявлення захворювання важливе для адекватного лікування, незначні вогнища раку також можуть бути виявлені на додаток до значного пухлинного ураження. На сьогоднішній день основними інструментами, які використовуються для діагностики захворювання є: пальцеве ректальне дослідження, сироваткові рівні простат-специфічного антигену (ПСА) і біопсія передміхурової залози під ТРУЗД контролем. В даний час позитивна прогностична цінність біопсії передміхурової залози на основі пальцевого ректального дослідження, ПСА та висновків ТРУЗД низька, і це призводить до значної кількості непотрібних біопсій. Отже, покращення точності діагностичних методів дослідження РПЗ є очевидною необхідністю.
Найбільш частим показанням для ТРУЗД дослідження передміхурової залози є діагностична оцінка при підозрі на РПЗ. Раннє виявлення РПЗ тісно пов’язане зі зниженням показника смертності, оскільки виявлення на ранній стадії захворювання є, найчастіше, єдиним шансом для лікування. До широкого впровадження діагностичних засобів, що дозволяють виявляти захворювання на ранніх стадіях таких, як: пальцеве ректальне дослідження, ТРУЗД і визначення рівня ПСА, РПЗ часто діагностувався в пізній стадії, в результаті чого пацієнти вмирали в більш короткі терміни. Хоча сироватковий рівень загального ПСА (ЗПСА) більший 4 нг/мл, а це означаєнаявність РПЗ, пацієнти з ДГПЗ і запальними розладами передміхурової залози також можуть мати підвищений сироватковий рівень загального ПСА. Відсутність специфічності сироваткового рівня загального ПСА для скринінгу РПЗ неминуче призвело до подальших зусиль, спрямованих на визначення ідеального протоколу, який би об’єднував ПСА, ТРУЗД і пальцеве ректальне дослідження для поліпшення специфічності без зниження чутливості. Незважаючи на те, що ТРУЗД визнається кращим методом для ультразвукового наведення при біопсії, його низька позитивна прогностична цінність в діагностиці злоякісних новоутворень розглядається як істотний недолік.
СІРОШКАЛЬНЕ УЛЬТРАЗВУКОВЕ ДОСЛІДЖЕННЯ
З моменту свого першого клінічного впровадження у 1960-х досягнуто стійке поліпшення технології ТРУЗД. Хоча існує консенсус щодо використання ТРУЗД для визначення розміру передміхурової залози і ультразвукового наведення при біопсії. Його обмежена цінність для точного виявлення стадії РПЗ і визначення локального пухлинного розповсюдження, як і раніше, представляє особливе клінічне питання про ефективність його використання. Тим не менш, сірошкальне ультразвукове дослідження дозволяє чітко виділити зональну анатомію передміхурової залози, при цьому залоза може бути легко окреслена при ТРУЗД від періпростатичних тканин, у тому числі прямої кишки, судинно-нервових пучків і жирової тканини.
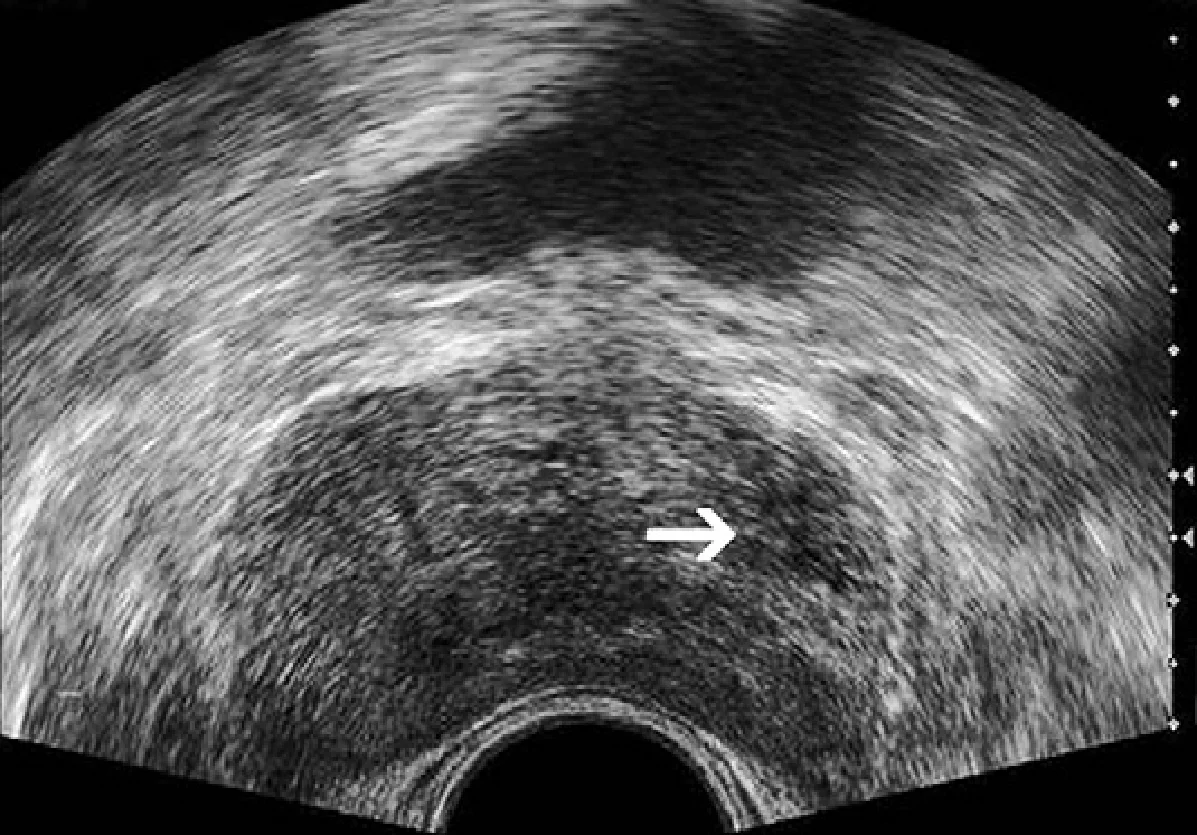
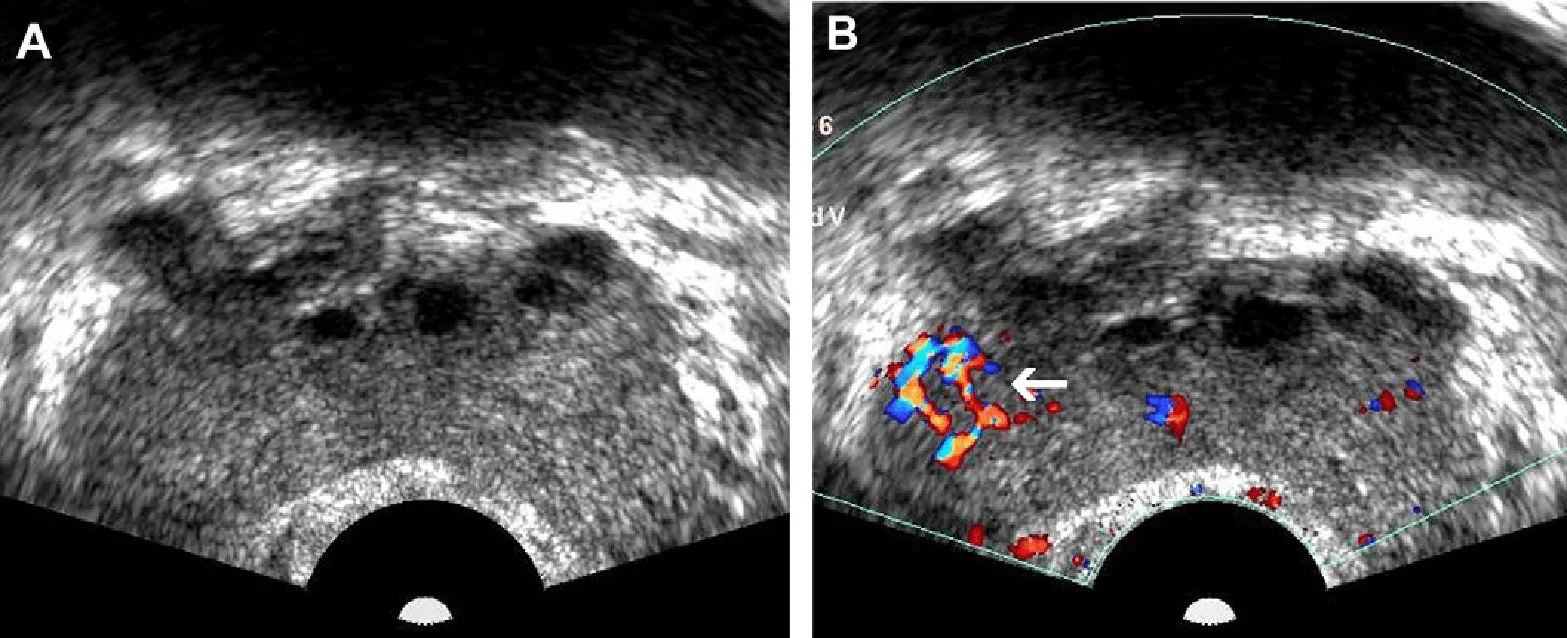
Класично, гіпоехогенне ураження в периферійній зоні може являти собою злоякісний процес, хоча РПЗ може рідше мати ізоехогенні або гіперехогенні характеристики (рис. 1 і 2А).
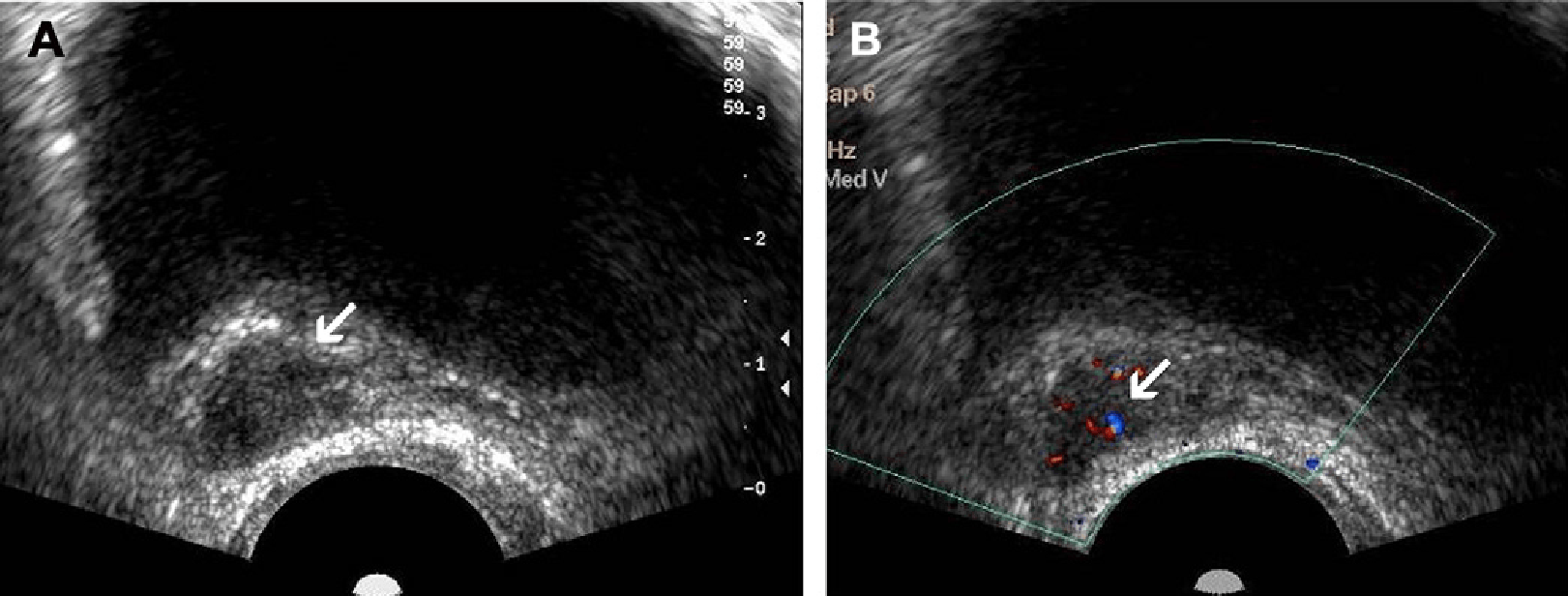
Рис. 1. Рак передміхурової залози. Зображення в поперечній проекції сірошкального ТРУЗД, яке показує нечітко визначене, злегка гіпоехогенне утворення в субкапсулярній зоні лівої частки (стрілка), яке було гістологічно верифіковано як аденокарцинома.
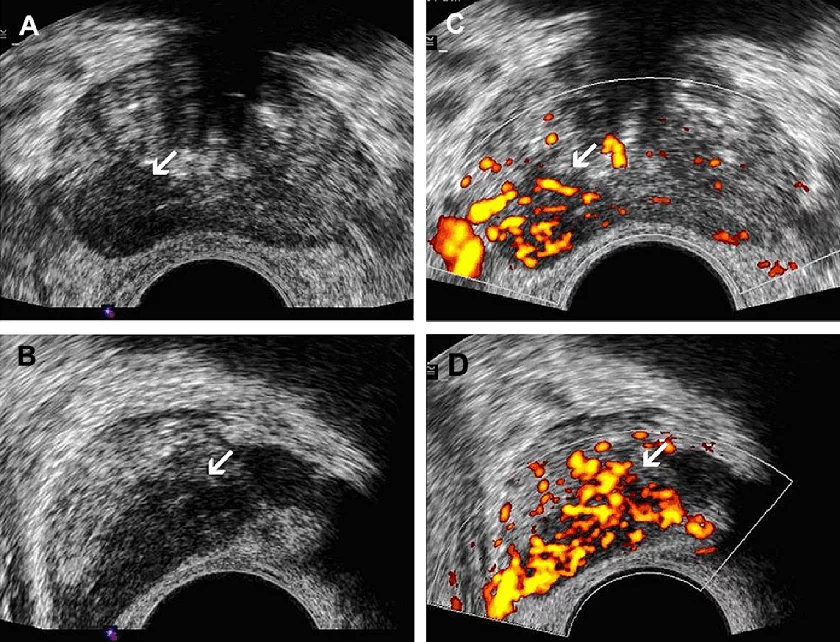
Рис. 2. Рак передміхурової залози. (А) Зображення у поперечній проекції сірошкального ТРУЗД без чіткого ураження в периферійній зоні. (В) Зображення в поперечній проекції кольорового доплерівського ТРУЗД того ж хворого показує область підвищеної васкуляризації в правій периферійній зоні (стрілка), що стало єдиною ознакою гістопатологічно виявленої аденокарциноми. Пухлину не було видно при сірошкальному ТРУЗД через її ізоехогенну природу.
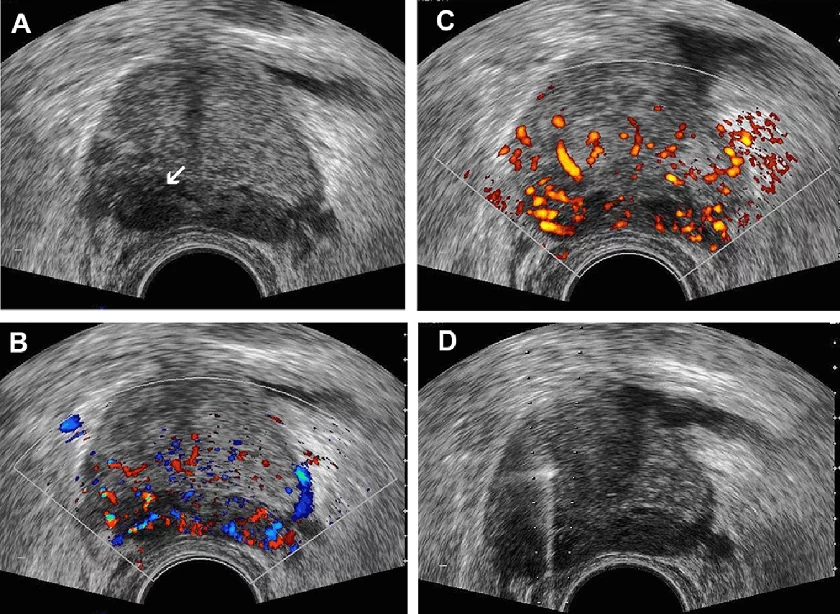
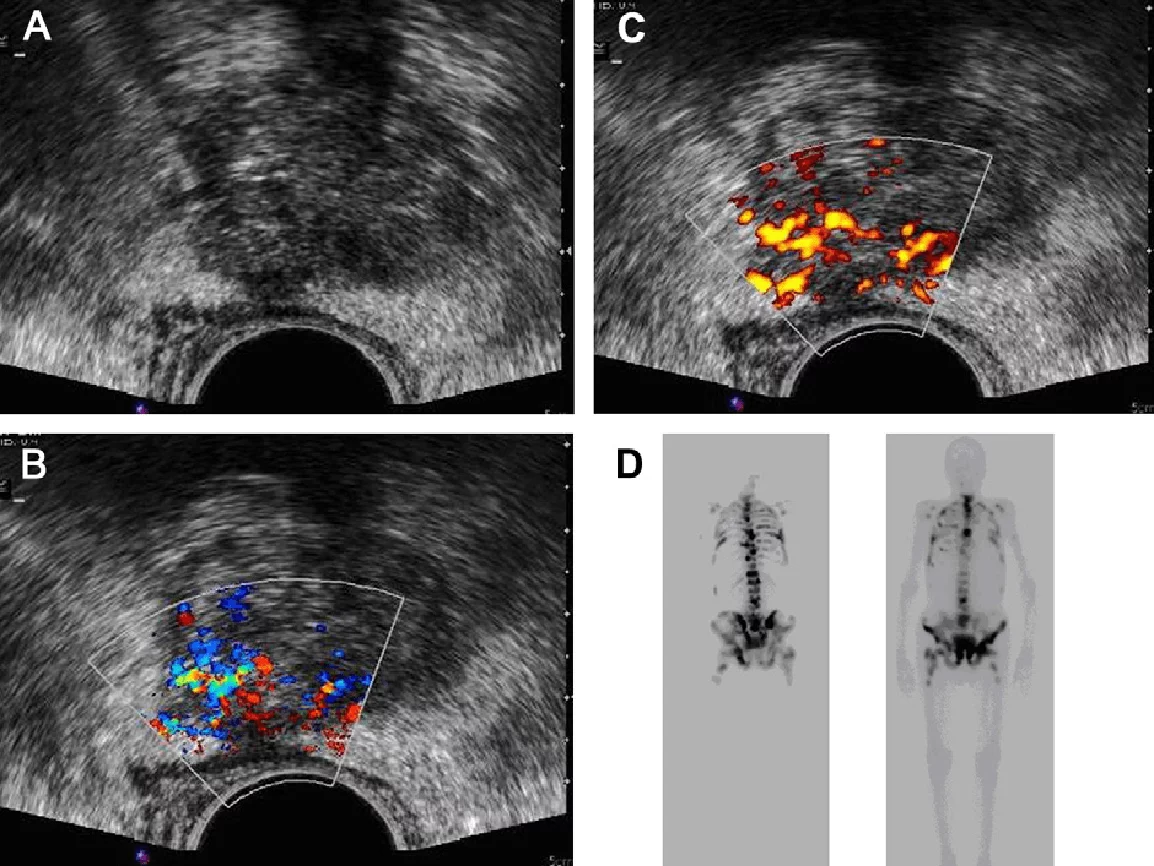
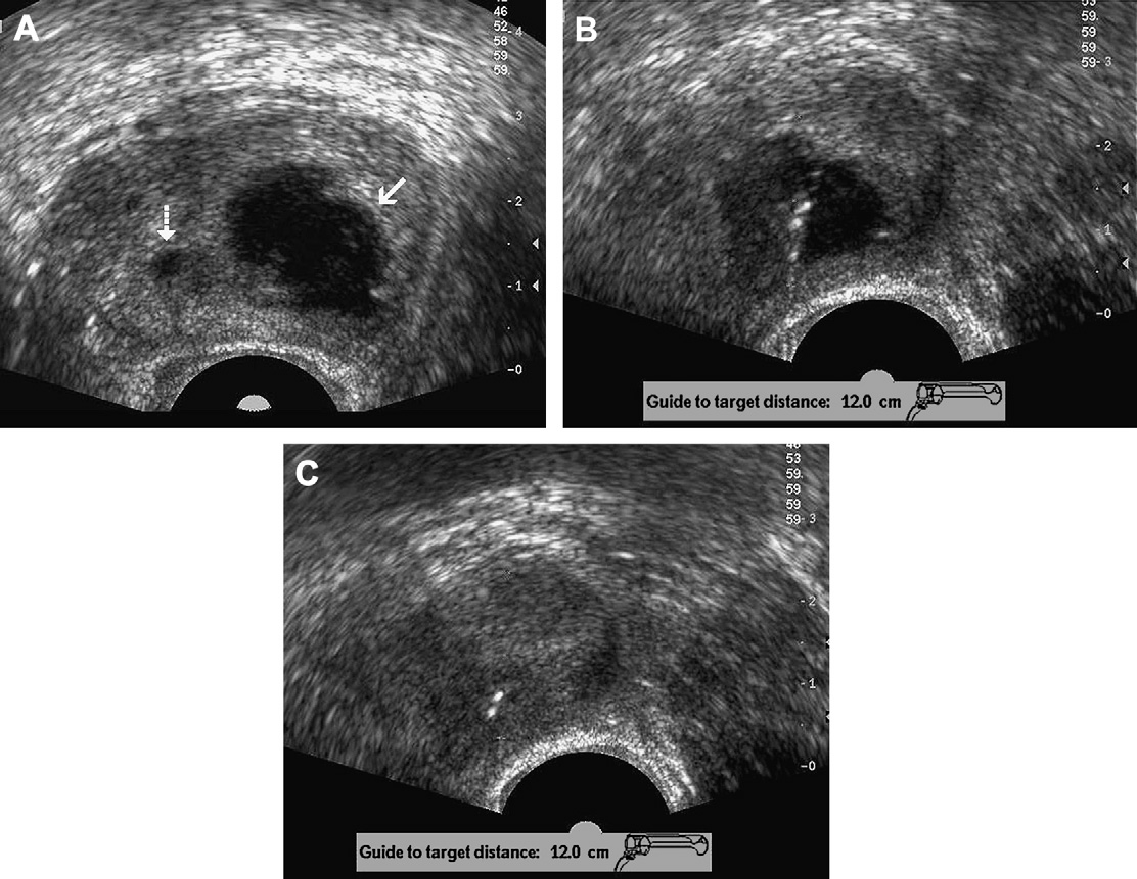
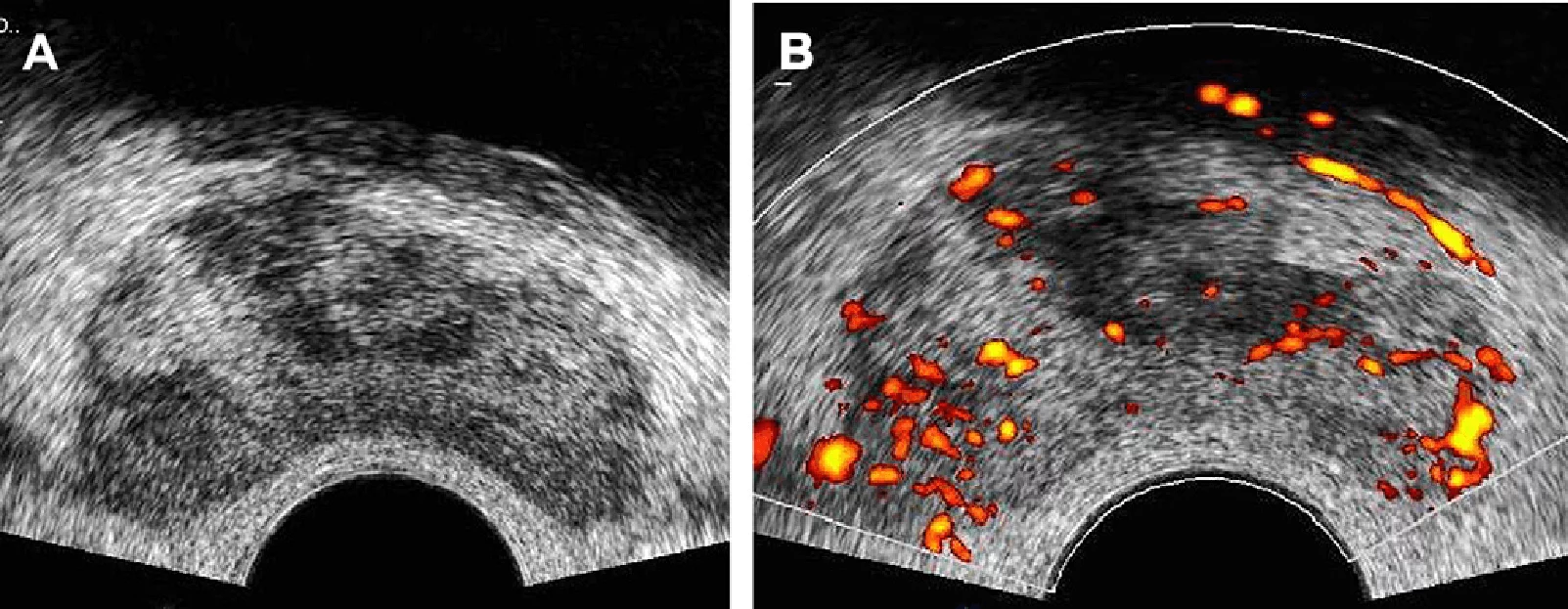
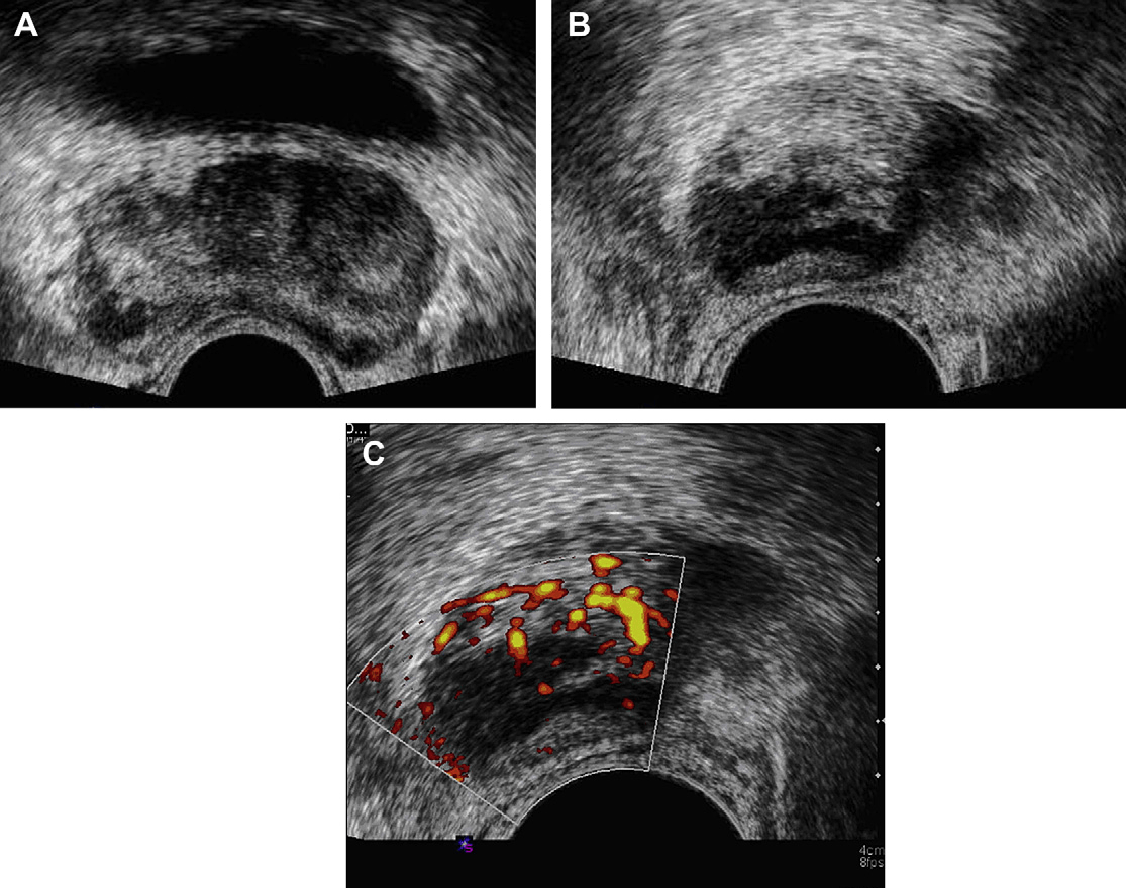
В даний час необхідне застосування інших, менш специфічних особливостей для діагностики РПЗ, бо значна частина виявлених РПЗ – ізоехогенні. У зв’язку з цим можуть бути корисними характеристики: асиметрія, ехотекстура або залозистий край. Відповідно до цього, неспецифічний нерівномірний ехосигнал, або опуклість, або переривчастий контур капсули може означати наявність РПЗ. Однак, близько половини уражень при РПЗ невидимі при сірошкальному ультразвуковому дослідженні. Більш того, деякі види патології, такі як: ДГПЗ, простатит, атрофія, гематома, ектазія проток і інтраепітеліальна неоплазія, можуть імітувати картину РПЗ при сірошкальному ультразвуковому дослідженні. Ще однією проблемою для оцінки РПЗ є те, що він в основному мультифокальний; поодиноке округле утворення також може мати місце, але така картина зустрічається рідше. Морфологічно, тільки 30% РПЗ може проявлятися в якості одиничного вузлика (рис. 3А), у той час як ураження, яке супроводжується інфільтративним компонентом, зустрічається приблизно у 50% пацієнтів (рис. 4А, В), а інфільтративна картина переважає в решти 20 %. Ультразвукова картина наводить на думку про поширений РПЗ при дифузно гіпоехогенній і гетерогенній ехотекстурі периферичної зони, яка або ізоехогенна, або гіперехогенна в порівнянні з внутрішньою залозистою тканиною нормальної передміхурової залози (рис. 5А).
Рис. 3. Рак передміхурової залози. (А) Зображення у поперечній проекції сірошкального ТРУЗД, що показує округле, гіпоехогенне утворення, яке розташоване в правій периферійній зоні (стрілка). Ні кольорове (B), ні енергетичне (С) доплерівське ТРУЗД не виявило помітного збільшення кровотоку, який би прогнозував неоваскуляризацію, характерну для РПЗ. (D) Поперечне ТРУЗД зображення відображає траєкторію голки, яка використовується для відбору проб при біопсії вищезгаданого ураження.
Рис. 4. Рак передміхурової залози. (A, B) Поперечні і повздовжні зображення сірошкального ТРУЗД, що відображають локальний вузлик управій периферійній зоні (стрілки в А і В). (С, D) Збільшення васкуляризації було виявлено в ураженні на поперечних і повздовжніх зображеннях енергетичного доплерівського ТРУЗД (стрілки C і D).
Рис. 5. Рак передміхурової залози. (А) Зображення у поперечній проекції сірошкального ТРУЗД, що відображає дифузно неоднорідну паренхіматозну ехотекстуру з нерівномірним контуром капсули і помітним заднім екстракапсулярним розповсюдженням. Ураження має помітне випинання і близьке до стінки прямої кишки, що означає інфільтрацію раковою тканиною. Поперечне кольорове (B) і енергетичне (С) доплерівське ТРУЗД зображення виявляють збільшене кровопостачання ураженої ділянки. (D) Сцинтіграфія всього тіла того ж пацієнта показує кілька областей підвищеного поглинання в осьовому скелеті, що представляє патологічну активність остеобластів і відповідає метастатичному ураженню.
Маленькі ракові пухлини, як правило, мають гіпоехогенний вигляд, в той час як збільшення пухлини може призвести до її трансформації в ізоехогенне ураження або в утворення з неоднорідним ехосигналом. Не існує специфічних ультразвукових характеристик для перехідних зон раку, хоча вони відрізняються від периферичної зони раку тим, що вони є менш агресивними клінічно. Отже, рутинна біопсія є єдиним засобом для виявлення перехідної зони раку. Наявність супутньої ДГПЗ може бути обмежуючим фактором при ТРУЗД оцінці передміхурової залози, тому що його змішаний відбитий сигнал або ефект компресії периферичної зони може маскувати РПЗ.
Крім аденокарциноми, яка найбільш часто зустрічається серед гістологічних типів РПЗ, ультразвукові особливості рідкісних пухлин передміхурової залози також описані. Аденоматозна кістозна карцинома передміхурової залози може проявлятися з декількома однорідними невеликими кістами. Комедокарцинома, як найбільш злоякісна форма PП, з’являється сонографічно як ракова гіпоехогенна зона, яка перемежовується з неоднорідними численними невеликими гіперехогенними вогнищами. Лімфома, з іншого боку, має ультразвукову картину великих гіпоехогенних утворень в перехідній зоні і периферичній зоні. Насамкінець, м’якотканні утворення, які проникають у сечовий міхур і передміхурову залозу можуть представляти картину рабдоміосаркоми – злоякісної пухлини, яка розвивається в дитинстві.
Хоча використання ТРУЗД і обмежене для постановки діагнозу РПЗ, деякі висновки ТРУЗД можуть виявляти екстракапсулярне поширення. Серед цих висновків є локальне випинання або нерівномірність капсули передміхурової залози і гіпоехогенні смужки в площині періпростатичної жирової тканини. Однак, ТРУЗД не може виявляти екстракапсулярне поширення малих мікроскопічних кластерів пухлинних клітин.
КОЛЬОРОВА ДОПЛЕРОГРАФІЯ
Доплерографія є засобом для оцінки місцевого кровотоку, який тісно пов’язаний з функцією тканини та її життєздатністю. При кольоровій доплерографії кольорова палітра пов’язана з напрямком потоку крові та орієнтацією датчика при прийомі сигналу, де потік до датчика зображено відтінком червоного кольору, а потік від датчика – відтінком синього. З іншого боку, збільшення потреби в кровопостачанні ракової тканини з прискореним темпом зростання більш виражено, ніж в нормальній тканині, що може призвести до значних змін в показниках місцевої гемодинаміки. Внаслідок цього відчутний вплив на здатність візуалізації та виявлення ракових утворень при кольоровій доплерографії (рис. 5B). У пухлинній тканині збільшення числа розширених і нетипових кровоносних судин, які відображають ангіогенез, і збільшення кровотоку, може бути виявлено при кольоровій доплерографії (рис. 2В). Технічно, збільшення кровотоку може бути показано або при спектральному аналізі при імпульсно-хвильовій доплерографії шляхом виявлення хвиль, що представляють зсув частоти або швидкості, або кольоровій доплерографії, при якій зображується спектр кольорів, що представляють середній діапазон зсуву частоти або швидкості еритроцитів в кровотоці.
Раніше вважалося, що кольорова доплерографія забезпечує кращу діагностику РПЗ, оскільки вона дозволяла визначити дифузний, локальний і навколишній характер кровотоку. Пізніше з’ясувалося, що специфічність техніки для відповідної оцінки була низькою. Крім того, було також зазначено, що гіпоехогенне ураження, яке передбачає РПЗ і гіперваскуляризація, не обов’язково корелюють (рис. 3B, C). Тим не менш, було показано, що кольоровий доплерівський сигнал має хорошу кореляцію зі стадією і типом РПЗ, а також із ризиком рецидиву після лікування, що є ключем до визначення поведінки і агресивності РПЗ. Відповідно, кольорова доплерографія була корисна в дифференційній діагностиці гіповаскулярних пухлин низького ризику від гіперваскулярних пухлин високого ризику, оскільки остання група пов’язана з гіперваскуляризацією, що представляє більш високий рівень пухлинної стадії за класифікацією Глісона, що означає більш високий ризик екстрапростатичного поширення пухлини (рис. 5). Прицільна біопсія, яка залежить виключно від високочастотного кольорового або енергетичного доплерівського зображення, не рекомендується через теоретичний ризик пропуску значної кількості пухлин. Крім кількісної оцінки кровотоку, за допомогою кольорової доплерографії можна провести розрахунок щільності мікросудин, який представляє розподіл мікросудин, що може бути корисним для оцінки кровотоку в передміхуровій залозі. Природно, що збільшена щільність мікросудин була вищою в метастатичних пухлинах, що є типовими для РПЗ. Через те, що кор-біопсія може недооцінювати гістологічну картину, яка відповідає шкалі Глісона, щільність мікросудин може бути використана як індикатор прогнозу захворювання. Серед технічних обмежень кольорової доплерографії для оцінки передміхурової залози є: кутова залежність доплерівського потоку, інтрапростатичний шум, що імітує посилення кровотоку і неадекватність методики виявлення при низьких швидкостях кровотоку.
ЕНЕРГЕТИЧНА ДОПЛЕРОГРАФІЯ
Енергетична доплерографія має меншу кутову залежність, ніж кольорова доплерографія та надає інформацію про наявність та інтенсивність сигналів потоку. Техніка має перевагу у виявленні повільного потоку і навіть незначних змін кровотоку в дрібних пухлинних судинах (рис. 4 і 5). Тим не менш, напрямок потоку не може бути визначений за допомогою цього методу. Енергетична доплерографія, яка має від 3-ьох до 4-ьохкратну чутливість для виявлення РПЗ, також допомагає в диференціальній діагностиці ДГПЗ і РПЗ. Тим не менш, про цей метод рідко повідомляється інформація про яку-небудь перевагу перед кольоровою доплерографією у виявленні РПЗ. Хоча енергетична доплерографія і може допомогти у визначенні необхідного місця для біопсії передміхурової залози шляхом виявлення області локальної гіперваскуляризація, вважається, що ця методика не перевершує кольорову доплерографію і тільки може бути корисною для прицільної біопсії в тому випадку, коли кількість біопсійних пункцій через залозу обмежена. Біопсія під комбінованим ультразвуковим наведенням сірошкальної сонографії і кольорової доплерографії при ТРУЗД не є достатньо чутливою для того, щоб виключити необхідність в рутинній біопсії. У недавньому дослідженні було опубліковано, що спектральне вимірювання форми сигналу капсулярних і уретральних артерій передміхурової залози при енергетичній доплерографії може бути корисним в диференціальній діагностиці РПЗ від доброякісної гіпертрофії. Дослідники також припускають, що збільшення числа біоптатів на межі з аномальними значеннями спектрального доплерівського індексу підвищить діагностичну цінність у виявленні РПЗ.
УЛЬТРАЗВУКОВЕ КОНТРАСТНЕ ДОСЛІДЖЕННЯ
Мікропухирці – контрастні речовини, які дозволяють візуалізувати мікросудинне русло передміхурової залози, що може поліпшити виявлення РПЗ, бо підвищена щільність мікросудин, яка асоціюється з ангіонеогенезом в раковій тканині передміхурової залози, менша, ніж рівень роздільної здатності звичайної доплерографії. У той же час, більшість ультразвукових контрастних речовин діаметром менше 10 мкм мають здатність проникати навіть у найдрібніші кровоносні судини. У зв’язку з цим, ультразвукове дослідження з контрастним підсиленням (УДКП) дозволяє оператору отримати зображення контрастних речовин у вигляді мікропухирців. Таким чином, невідповідність між акустичними властивостями мікропухирців і навколишньої крові призводить до інтенсифікації віддзеркалень ультразвукової хвилі.
Приблизно через 20 секунд після внутрішньовенного введення, число ультразвукових ехосигналів збільшується в судинному руслі передміхурової залози і це забезпечує поліпшення доплерівського зсувного сигналу, що підсилює чутливість вимірювань кольорової і енергетичної доплерографії. Максимальне контрастне посилення розвивається приблизно від 1 до 2 хвилин після одноразового внутрішньовенного болісного введення, хоча час посилення може бути розширений шляхом внутрішньовенної інфузії мікропухирців. Час пікового посилення, таким чином, показує частину передміхурової залози з раковим ураженням.
У цілому, УДКП покращує чутливість у виявленні РПЗ без зниження специфічності дослідження. УДКП може також сприяти зниженню кількості спроб відбору проб, що забезпечує прицільну біопсію. З іншого боку, 3-мірна енергетична доплерографія з контрастним підсиленням з 3-мірною реконструкцією зображення до і після введення контрастних речовин і рівні ПСА вважаються оптимальною прогностичною комбінацією для діагностики РПЗ. Тим не менш, основним недоліком для клінічного використання енергетичної та кольорової доплерографії з контрастним підсиленням є те, що кровотік при цьому методі в основному визначається у великих судинах, бо мікропухирці руйнуються при доплерографії до досягнення пухлинних неосудин.
Сірошкальне гармонійне ультразвукове дослідження є ще одним способом для візуалізації мікропухирцевих контрастних агентів. Метод передбачає використання більш низьких енергій для зображення контрастних речовин з меншим руйнуванням бульбашок і, відповідно, більшим їх проникненням у мікросудини. На відміну від кольорової доплерографії з контрастним підсиленням, гармонійні методи візуалізації включають виявлення нелінійних ехосигналів бульбашок. Технологія фазової інверсії (інверсія імпульсу) за допомогою зображення з широкою пропускною здатністю, покращує оцінку тканинної перфузії у зв’язку з кращим виявленням сигналів, відбитих від мікропухирців. Крім того, зображення з високою роздільною здатністю, які відтворюються цією технікою, на відміну від традиційної ультразвукової технології, з вузькою смугою пропускання призводить до втрати просторової роздільної здатності. Сірошкальне гармонійне ультразвукове дослідження може підвищити чутливість виявлення РПЗ. Крім того, більш високий ступінь посилення, як вже було показано, пов’язаний з більш високим ступенем за шкалою Глісона. Нещодавно було розроблено метод переміжної візуалізації, який забезпечує більш тривалий термін персистування мікропухирцевих контрастних агентів. У порівнянні з безперервним гармонійним дослідженням, метод переміжної гармонійної візуалізації забезпечує краще посилення паренхіми. Останнім часом було відзначено, що техніка флеш наповнення, на відміну від гармонійної методики, покращує прицільність зон з підвищеною мікросудинною васкуляризацією при біопсії передміхурової залози під ТРУЗД наведенням. У недавньому дослідженні, яке проводилося після премедикації дутастериду (подвійний інгібітор 5–а редуктази) до біопсії передміхурової залози, був продемонстрований обмежений кровотік в доброякісній тканині передміхурової залози, на відміну від ракової тканини. Зовсім недавно контраст-модульована послідовна імпульсна технологія поліпшила візуалізацію мікросудин, які пов’язані з РПЗ і, таким чином, покращилася частота виявлення РПЗ.
Загалом, УДКП покращує візуалізацію РПЗ завдяки розвитку нових специфічних ультразвукових методів і кращої візуалізації мікросудин, які асоціюються з РПЗ, хоча чутливість та специфічність досі залишається не досить високою для того, щоб уникнути рутинної біопсії. Хоча прицільна біопсія разом з рутинним відбором проб згідно протоколів збільшує частоту виявлення патології, роль УДКП в рутинній клінічній практиці залишається дискутабельною.
ЕЛАСТОГРАФІЯ
Еластографія оцінює еластичність досліджуваних тканин. Технічно, відбиті ультразвукові сигнали незначно змінюються в різному ступені, якщо досліджувана тканина злегка стискається і потім розтискається під час дослідження. Стисливість досліджуваної тканини змінюється в часі або просторі між зонами дослідження з різними коефіцієнтами стиснення. Спеціально розроблений ТРУЗД датчик необхідний для застосування методу при візуалізації передміхурової залози. Технічно, невеликі зміни в тиску датчиком, який прикладається до передміхурової залози при ТРУЗД дослідженні, призводить до змін у створюваному зображенні в режимі реального часу і показує тільки зміни в локальній компресії тканин. Відповідно, може бути проведена диференційна діагностика між раковими і доброякісними тканинами, залежно від градієнта щільності і зниження ступеня еластичності. РПЗ, який характеризується обмеженою пружністю або еластичністю, зображується сонографічно як темна зона. Отже, це дослідження можна вважати потенційним методом візуалізації для виявлення РПЗ. Хоча використання еластографії при ТРУЗД дослідженні допомагає збільшити діагностування РПЗ по маркуванню місць для біопсії, дана методика поки не може виключити потреби в рутинній біопсії передміхурової залози. Також було відзначено, що дана техніка потенційно ефективна в поліпшенні точності визначення стадії процесу при ТРУЗД.
БІОПСІЯ ПЕРЕДМІХУРОВОЇ ЗАЛОЗИ ПІД ТРУЗД НАВЕДЕННЯМ
Процедура біопсії передміхурової залози різко змінилася завдяки досягненням в галузі технології ТРУЗД. Було вирішено, що біопсія передміхурової залози під ТРУЗД наведенням є золотим стандартом для виявлення РПЗ. Комбіноване використання ТРУЗД і голкової біопсії дозволило направляти біопсійну голку саме в область ураження, що в результаті призвело до збільшення можливості виявлення РПЗ в порівнянні з біопсією під контролем пальця (рис. 3D). Крім того, біопсія передміхурової залози відіграє ключову роль у лікуванні РПЗ. Показання для проведення біопсії передміхурової залози під ТРУЗД наведенням наведені в таблиці 2.
Таблиця 2.
Показання для проведення біопсії передміхурової залози під ТРУЗД наведенням
|
• Патологічні результати пальцевого ректального дослідження • Підвищення рівня загального ПСА в сироватці крові • Рівень ПСА більше 0,75 нг/мл/год • Вільний ПСА менше 20%, ЗПСА в сірій зоні • Співвідношення про-ПСА до вільного ПСА більше 1,8% • Підозрілі результати ТРУЗД • Перед хірургічним лікуванням ДГПЗ • Для діагностики та стадіювання рецидивного раку передміхурової залози після відсутності ефекту від променевої терапії до проведення місцевої хіміотерапії |
Класично, зміни при пальцевому ректальному дослідженні, підвищений рівень ПСА (> 4 нг/мл) і підозрілі ознаки при ТРУЗД дослідженні є основними показаннями для проведення біопсії передміхурової залози під ТРУЗД наведенням, хоча до цих пір не існує консенсусу по верхній межі нормального значення ПСА. Процедура заснована на регіональному рутинному відборі проб тканини із зон передміхурової залози, де за даними дослідження, швидше за все, розташована пухлина. Але оскільки дана патологія має багатоцентровий характер, індивідуальна діагностична здатність ТРУЗД у виявленні раку обмежена. Залежно від дизайну датчика, відбір проб тканини передміхурової залози виконується або при сагитальному, або при аксіальному скануванні. Постріл з біопсійного пістолета повинен бути виконаний тільки після ідентифікації капсули передміхурової залози за допомогою біопсійної голки для того, щоб уникнути контамінації періпростатичних тканин і якомога більше тканини включити в зразок проби. Крім того, довжина траєкторії голки в межах залози повинна бути прорахована за допомогою лінії-траєкторії на ультразвуковому екрані, таким чином випадкове проникнення в структури сечівника і періпростатичних тканини може бути попереджено.
Оскільки РПЗ переважно виникає в периферійній зоні і агресивність раку периферичної зони вища, ніж в перехідній зоні, відбір проб для біопсії повинен бути зосереджений на периферійній зоні. Протокол класичної шеститочкової біопсії включає зразки тканини з точки посередині між бічною межею і серединною площиною на рівні основи, середньої частини залози і верхівки залози, відповідно. Був розроблений також розгорнутий протокол відбору проб для біопсії, який включає від 10-ти до 12-ти зразків тканини за участю додаткових бічних ділянок тканини на зазначених рівнях, хоча все ще існують суперечки щодо оптимальних зон і кількості біопсій. Як повідомлялося, збільшення об’єму передміхурової залози має негативний вплив на діагностичний результат, при такій же кількості ділянок тканини. В даний час, при виконанні первинної біопсії не виконується відбір проб з внутрішньої частини залози через низькевиявлення місць ураження раку і метастатичного потенціалу ураження внутрішньої частини залози. За допомогою біопсії передміхурової залози під ТРУЗД наведенням також може бути визначено стадію за шкалою Глісона, як оцінку агресивності РПЗ.
ПЕРЕДПРОЦЕДУРНА ПІДГОТОВКА І ЗНЕБОЛЕННЯ
Для того, щоб звести до мінімуму ризик інфікування, пов’язаний з процедурою, рекомендується антибіотикопрофілактику ципрофлоксацином починати за день до процедури і продовжувати протягом 3–ьох наступних днів. Крім того, застосування очищувальних ректальних клізм розглядається як міра профілактики проти інфекційних ускладнень, що дуже важливо в отриманні хорошого ТРУЗД зображення. У недавньому дослідженні повідомлялося, що пацієнти з уретральним катетером, з цукровим діабетом, або ті, хто піддавався біопсії з більш, ніж 10-ти зон залози, повинні спостерігатися, тому що вони мають більший ризик розвитку інфекції сечовивідних шляхів.
Через зростаючу увагу до полегшення дискомфорту пацієнта під час біопсії передміхурової залози під ТРУЗД наведенням, останнім часом стало популярним застосування декількох методів знеболення. Серед них періпростатична блокада нервів під ультразвуковим наведенням була найбільш ефективним методом, який застосовується більшістю лікарів. Після проникнення під фасцію Данонвілье, на рівні заднього півкола основи передміхурової залози з використанням голки 22 номеру, анестезуюча речовина (лідокаїн без адреналіну) вводиться латерально біля білої пірамідальної ділянки між передміхуровою залозою і сім’яними пухирцями, яку також називають ознака «гори Еверест» у зв’язку з її білим, загостреним зовнішнім виглядом через жирову тканину в цій зоні при сагитальному скануванні. Поступово з’являється ультразвукова картина скупчення рідини у вигляді гіпоехогенного заповнення зони «гори Еверест». Однак, все ще існує спір щодо точного місця ін’єкції, кількості та дози препаратів. Більш важливо те, що введення анестетика переважно здійснюють у період до процедури для того, щоб забезпечити достатньо часудля настання ефекту. Дана методика може мати деякі небажані ефекти, такі як: біль, спричинений проколом голкою, яка використовується для місцевої анестезії, необхідність повторних ін’єкцій протягом процедури біопсії, рутинна токсичність лідокаїну, нетримання сечі, спотворення або утворення артефактів на ТРУЗД зображеннях, періпростатична інфекція і еректильна дисфункція. Крім того, оператор-залежний характер і неефективність техніки у присутності факторів ризику, таких як: неспокій пацієнта, молодий вік, повторна біопсія або запальні захворювання анального каналу, існують також серед недоліків даного методу, при цьому седація з внутрішньовенним введенням мідазоламу є альтернативним і ефективним засобом анестезії.
ТРУЗД В ОЦІНЦІ МІСЦЕВИХ РЕЦИДИВІВ ПІСЛЯ РАДИКАЛЬНОЇ ПРОСТАТЕКТОМІЇ
Радикальна простатектомія (РПЕ) є ефективним засобом лікування клінічно локалізованого РПЗ. Після РПЕ, рецидивуючий РПЗ є важливою клінічною проблемою в довгостроковій перспективі приблизно у 40% пацієнтів, при цьому більш ніж 95% рецидивів відбувається в перші 5 років. Не дивно, що більш раннє виявлення місцевого рецидиву раку може дозволити пацієнтам почати місцеву променеву терапію в потенційно більш курабельній стадії захворювання. Добре відомо, що рівень ПСА повинен бути менше, ніж 0,4 нг/мл від 2 до 3 тижнів після РПЕ. У зв’язку з цим, підвищення рівня ПСА припускає місцевий рецидив РПЗ в області ямки передміхурової залози, метастатичне ураження або поєднання і того, й іншого. У цьому зв’язку, рівень ПСА є найкориснішим маркером пухлини для моніторингу пацієнтів з рецидивом РПЗ після РПЕ. Клінічно, діагноз місцевого рецидиву РПЗ ґрунтується на комбінованому використанні пальцевого ректального дослідження, ТРУЗД і біопсії передміхурової залози під ТРУЗД наведенням. У цілому, ТРУЗД вважається ефективною процедурою, тому що це дозволяє провести точну оцінку анатомії нормальної й патологічно зміненої ямки передміхурової залози. У пацієнтів без клінічних або біохімічних ознак місцевого рецидиву після РПЕ, ТРУЗД, як правило, відображає зовнішній вигляд щілиноподібного конічного профілю, що тягнеться від шийки сечового міхура до везікоуретрального анастомозу, який оточений змінною кількістю гіпоехогенної тканини. Зокрема, гіпоехогенна зона поблизу везікоуретрального анастомозу, шийки сечового міхура або позаду трикутника Льєто вважається патологічною, хоча асиметричне потовщення везікоуретрального анастомозу або відсутність цілісності ретроанастомотичної площини жирової тканини, також слід розглядати як підозрілі зони для місцевого рецидиву (рис. 6А, В).
Рис. 6. Місцевий рецидив після радикальної простатектомії. (А) Зображення у поперечній проекції сірошкального ТРУЗД, яке показує нечітко визначене, гіпоехогенне утворення в ямці передміхурової залози, яке прилягає до області анастомозу (стрілка), яка пізніше гістопатологічно виявилася рецидивуючою аденокарциномою. (В) Зображення поперечного кольорового доплерівського ТРУЗД, на якому в осередку ураження виявлені області підвищеної васкуляризації, що пов’язано з неоваскуляризацією пухлини (стрілка).
Тим не менш, сірошкальне ТРУЗД не може виключити необхідність у біопсії ямки передміхурової залози під ТРУЗД наведенням для диференціальної діагностики між післяопераційним фіброзом і рецидивом РПЗ. З іншого боку, енергетичне доплерівське ТРУЗД, яке полегшує ідентифікацію гіперваскуляризованих зон в межах пухлинної тканини під час біопсії передміхурової залози під ТРУЗД наведенням, вважається ефективним для раннього виявлення локальних рецидивів пухлини.
ДОБРОЯКІСНА ГІПЕРПЛАЗІЯ ПЕРЕДМІХУРОВОЇ ЗАЛОЗИ (ДГПЗ)
ДГПЗ є поширеним захворюванням серед літніх чоловіків, яка включає в себе вузлову гіперплазію фіброзної, м’язової і залозистої тканини в межах періуретральної залозистої зони і перехідної зони. Основна роль ультрасонографії при дослідженні пацієнтів з ДГПЗ полягає в оцінці розміру передміхурової залози і об’єму залишкової сечі (ОЗС) до лікування. Методика також може бути використана для оцінки об’єму перехідної зони, яка тісно пов’язана з тяжкістю ДГПЗ. Трансабдомінальне ультразвукове дослідження може відігравати роль при подальшому динамічному спостереженні за пацієнтами з ДГПЗ, тому що воно ефективне в розрахунку підвищення рівня ОЗС. Підвищення рівня ОЗС збільшує ризик затримки сечі. Крім того, верхні сечовивідні шляхи також повинні бути досліджені на предмет будь-яких змін.
Основні ТРУЗД зміни при ДГПЗ – дифузне або вузлове збільшення перехідної зони з гіпоехогенним або гетерогенним проявом, у порівнянні з периферичною зоною, випинання капсули передміхурової залози, кістозні зміни і кальцифікати в аденоматозних вузликах і компресія периферичної зони збільшеною перехідною зоною. Крім того, можуть бути виявлені відповідні зміни в проксимальних відділах сечовивідних шляхів, таких як: підйом основи сечового міхура, збільшення ОЗС, утворення трабекул сечового міхура і гідроуретеронефроз, які є вторинними по відношенню до тієї чи іншої міри інфравезикальної непрохідності. Хірургічний дефект може бути виявлений у центральній частині перехідної зони у пацієнтів з попередньою трансуретральною резекцією передміхурової залози у зв’язку з ДГПЗ, який не повинен бути невірно розтлумачений як кістозне ураження. Кісти, вторинні по відношенню до дегенерації гіперпластичних вузликів, пов’язаних з ДГПЗ, досить поширені в клінічній практиці. Найголовніше, випинання збільшеної перехідної зони не слід плутати з пухлинами, що розвиваються з основи сечового міхура. Точна диференціальна діагностика може бути проведена шляхом виявлення переривання контуру ураження і передміхурової залози при сагітальному ТРУЗД скануванні.
ПРОСТАТИТ
Термін простатит використовується на позначення різноманітних порушень передміхурової залози, які викликають біль в області тазу і в основному мають небактеріальну етіологію. Клінічно, дана патологія класифікується як гострий бактеріальний простатит, хронічний бактеріальний простатит, хронічний асептичний простатит, синдром хронічної тазової болі і асимптоматичний простатит. Роль ТРУЗД обмежена у хворих з гострим простатитом, бо діагноз в основному базується на клінічній картині. Пацієнти з гострим простатитом зазвичай скаржаться на лихоманку, біль, дизуричні розлади, емпіричні позиви і піурію, і навіть відчувають значний дискомфорт при введенні датчика в пряму кишку через сильний біль запаленої передміхурової залози. При ТРУЗД можна побачити такі запальні зміни, як округла, збільшена передміхурова залоза зі зменшеною ехогенністю і дифузною гіперваскуляризацією при кольоровій або енергетичній доплерографії. Тим не менш, основна роль ТРУЗД при гострому простатиті – виключити формування абсцесу у хворих, які не реагують на лікування.
Абсцес передміхурової залози, який розвивається в основному на п’ятому чи шостому десятилітті життя – рідкісне ускладнення гострого бактеріального простатиту. Типова ТРУЗД картина – чітко окреслене, товстостінне, одно- або багатокамерне рідинне утворення з внутрішнім ехосигналом і перегородками, які в основному розташовані в перехідній зоні (рис. 7А).
Рис. 7. Абсцес передміхурової залози. (А) Картина поперечної проекції сірошкального ТРУЗД, яка показує порожнину великого абсцесу в лівій внутрішній частині залози з внутрішніми ехосигналами (стрілки), з додатковим меншим рідинним скупченням в правій внутрішній частині залози. (В) Було виконано зовнішнє дренування вогнища ураження в лівій внутрішній частині залози під ультразвуковим наведенням. (С) ТРУЗД також може бути використано для оцінки ефективності інтервенційного лікування вищезгаданого абсцесу.
Крім проведення оцінки морфологічних особливостей абсцесу, ТРУЗД також забезпечує ультразвукове наведення для дренування ураження (рис. 7В). У зв’язку з цим, дренування рекомендується для абсцесу більше, ніж 1,5 см в діаметрі, в той час як лікування антибіотиками є кращим для абсцесів меншого розміру. Подальше динамічне спостереження для визначення ефективності або характеру лікування також може бути виконано за допомогою ТРУЗД (рис. 7С).
Хронічний простатит, як правило, представлений неспецифічними симптомами нижніх сечовивідних шляхів, що проявляється сонографічно, як плямисте, гіпоехогенне ураження або ділянками з гетерогенною, або підвищеною ехогенністю (рис. 8А). Збільшення кровопостачання вищезгаданого ураження при кольоровій доплерографії, дистрофічна кальцифікація, нерівномірність і потовщення капсули, дилатація періпростатичних вен і нерівномірність зони навколо сечоводу – також можуть бути виявлені у пацієнтів хронічним простатитом (рис. 8B).
Рис. 8. Хронічний простатит. (А) Картина поперечної проекції сірошкального ТРУЗД виявляє гетерогенну ехотекстуру паренхіми з гіпоехогенними областями, що мають неоднорідний розподіл. (В) Поперечна проекція енергетичної доплерографії при ТРУЗД того ж пацієнта показує збільшення васкуляризації всієї тканини залози. Рутинна біопсія під ТРУЗД наведенням гістопатологічно показала хронічний простатит.
Рідко, простатит може бути залучений до гранулематозного процесу, що призводить до збільшення передміхурової залози з локальними або мультифокальними гіпоехогенними ураженнями (рис. 9A-C).
Рис. 9. Гранульоматозний простатит. (AC) Картина поперечної і поздовжньої проекції сірошкального ТРУЗД показує збільшену передміхурову залозу з гетерогенною ехотекстурою паренхіми з кількома, випадково розподіленими, гіпоехогенними ураженнями. Кольорова доплерографія показує підвищену васкуляризацію. ТРУЗД біопсія гістопатологічно виявила гранульоматозний простатит.
Туберкульоз є найбільш поширеним типом інфекційного гранулематозного простатиту, який, як правило, розвивається вторинно при проходженні сечі через простатичну частину сечівника. Супутнє залучення еякуляторних протоків може призвести до утворення стриктур. Через відсутність конкретних ознак при ТРУЗД, біопсія є єдиним засобом для постановки правильного діагнозу.
КІСТИ ПЕРЕДМІХУРОВОЇ ЗАЛОЗИ
Маточкові кісти і кісти Мюлерової протоки – найбільш характерні серединні кісти передміхурової залози, які навряд чи можна віддиференціювати за клінічними даними або за допомогою методів візуалізації. Вони можуть бути безсимптомними, або рідко провокувати клініку обструктивної уропатії, або безпліддя. Кісти Мюлерової протоки, які, як правило, більші, ніж маточкові кісти, розташовані трохи збоку середньої лінії і можуть часто мати супрапростатичне розширення. Маточкові кісти, зазвичай, асоціюються з такими аномаліями, як гіпоспадії, крипторхізм або ниркова агенезія, і можуть бути діагностовані у чоловіків більш молодшого віку. Вкрай рідко РПЗ може бути виявлений при обох типах кіст. Кістозні порожнини, які розташовані по середній лінії і позаду від уретри є типовою знахідкою, хоча гіпоехогенний внутрішній інфекційний дебрис також може бути виявлений.
Менш характерні кісти еякуляційної протоки, що розвиваються вторинно по відношенню до обструкції еякуляторних проток, або вроджені, або вторинні до запальних процесів. Сонографічно вони проявляються округлої або овальної форми, тонкостінні, однокамерні кістозні ураження з парасерединною локалізацією. Вкрай рідко вони можуть викликати одностороннє розширення сім’яного пухирця. Для проведення досліджень рекомендуємо використовувати апарат від компании GE Voluson E8.
Часті питання та відповіді (FAQ)
Що таке трансректальне ультразвукове дослідження (ТРУЗД) передміхурової залози?
- Трансректальне ультразвукове дослідження (ТРУЗД) – це ключовий метод дослідження передміхурової залози, який забезпечує важливу клінічну інформацію при доброякісних та злоякісних ураженнях, таких як доброякісна гіперплазія передміхурової залози (ДГПЗ), простатит, обструктивне безпліддя та рак передміхурової залози (РПЗ).
Які основні причини для направлення пацієнтів на ТРУЗД?
- Основними причинами є виявлення та оцінка РПЗ, а також ультразвукове наведення при біопсії передміхурової залози.
Які розміри передміхурової залози вважаються нормальними?
- У зрілому віці нормальна передміхурова залоза має розміри від 4,0 до 4,5 см в поперечнику, від 2,5 до 3,0 см в передньо-задньому напрямку та від 3,0 до 4,0 см в краніо-каудальному напрямку.
Як проводиться ТРУЗД передміхурової залози?
- Сканування проводиться за допомогою біпланових датчиків з частотою від 5 до 8 МГц. Пацієнт, як правило, лежить на лівому боці з повним, але не перерозтягнутим сечовим міхуром. Перед процедурою рекомендується клізма для очищення прямої кишки.
Чи може ТРУЗД точно виявити рак передміхурової залози?
- ТРУЗД є корисним для ультразвукового наведення при біопсії, але його позитивна прогностична цінність в діагностиці РПЗ невисока. Багато РПЗ є ізоехогенними і невидимі на сірошкальному УЗД. Для діагностики часто потрібні додаткові методи дослідження.
Які додаткові методи використовуються для діагностики раку передміхурової залози?
- Для діагностики РПЗ використовуються пальцеве ректальне дослідження, визначення рівня простат-специфічного антигену (ПСА) та біопсія під контролем ТРУЗД.
Чи можна за допомогою ТРУЗД визначити розмір передміхурової залози?
- Так, за допомогою ТРУЗД можна визначити розміри передміхурової залози та розрахувати її об’єм за формулою еліпсоїда, використовуючи поперечний, передньо-задній та краніо-каудальний діаметри.