🤖 Короткий переказ від ШІ
Симптоматична аденокарцинома протоки підшлункової залози (АППЗ) часто діагностується на пізніх стадіях, проте рання діагностика безсимптомних випадків значно покращує прогноз. Ендоскопічна ультрасонографія (ЕУЗД), особливо з контрастним посиленням (C-EUS), виявилася ефективнішим методом для виявлення та диференціації утворень підшлункової залози порівняно з традиційними методами візуалізації.
C-EUS та ультразвукова еластографія дозволяють проводити диференційну діагностику солідних пухлин підшлункової залози з високою точністю, допомагаючи розрізняти АППЗ від нейроендокринних пухлин та інших утворень. Менші ураження частіше є доброякісними, тоді як жорсткі утворення можуть вказувати на злоякісність. Отримані дані свідчать, що гіповаскулярність (близько 90% випадків) та м’якість пухлин є ключовими маркерами для вибору подальшої тактики лікування, включаючи спостереження або біопсію. Ось посилання: УЗД апарати
✅ Ключові тези зі статті:
- Діагностика: ЕУЗД з контрастним посиленням (C-EUS) та еластографія є ключовими методами для точної діагностики солідних утворень підшлункової залози.
- Лікування: Етіологічна диференціація необхідна для вибору оптимальної тактики лікування – від радикальної хірургії до спостереження.
- Переваги: C-EUS забезпечує високу чутливість у виявленні дрібних утворень та допомагає диференціювати АППЗ від інших пухлин завдяки аналізу гіповаскулярності.
- Обмеження: Ультразвукова еластографія може мати обмеження у диференціації вогнищевого панкреатиту від АППЗ через схожу жорсткість тканин.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: Christoph F. Dietrich, Christian Jenssen
Введення: чим менше ураження, тим краще прогноз
Симптоматична аденокарцинома проток підшлункової залози (АППЗ), яка найбільш часто діагностується серед солідних злоякісних пухлин підшлункової залози, зазвичай діагностується на пізніх стадіях з метастазами або без них.
Більшість міжнародно визнаних посібників рекомендують радикальні операції при всіх невеликих солідних утвореннях підшлункової залози (СУПЗ), якщо немає підозр на етіологію іншого утворення або відсутні протипоказання.
Рання діагностика цієї пухлини в безсимптомних стадіях має вирішальне значення для поліпшення її прогнозу. Дані з японського реєстру раку підшлункової залози показують, що чим менше ураження під час діагностики, тим довше очікувана 5-річна виживаність.
Точність традиційних методів візуалізації, включаючи ультразвукове дослідження (УЗД), комп’ютерну томографію (КТ) та магнітно-резонансну томографію (МРТ), в диференціальній діагностиці утворень підшлункової залози виявилася невтішною.
КТ була рекомендованим методом діагностики для постановки стадії раку ПЗ, але показала незадовільні результати для виявлення невеликих солідних утворень (<20 мм).
Ендоскопічна ультрасонографія (ЕУЗД) вважається методом візуалізації, що виключає АППЗ. На підставі 22 досліджень, що включають 1170 випадків, сумарна чутливість ЕУЗД для виявлення солідних утворень склала 94%, що помітно вище, ніж відомі результати для мультидетекторної КТ, МРТ і трансабдомінальної УЗД. Крім того, ЕУЗД надає можливість виявити безсимптомні варіанти АППЗ.
Методи візуалізації з контрастом дозволяють поліпшити видимість характеристик пухлини перед радикальною операцією, а біопсія тонкою голкою успішно дозволяє проводити передопераційну диференціальну діагностику в багатьох випадках.
CEUS або C-EUS
Застосування контрастної ЕУЗД (C-EUS) поліпшило продуктивність ендоскопічної візуалізації. Багатоцентрове дослідження підшлункової залози в США за участю понад 1000 пацієнтів і інші дослідження, що використовують УЗД з контрастним посиленням (CEUS) і C-EUS, показали поліпшену діагностичну точність для характеристики вогнищевих утворень підшлункової залози.
Тільки 146 з 394 невеликих солідних новоутворень (37%) були остаточно діагностованими як АППЗ. У підгрупі солідних утворень розміром 15 мм (n = 83) 51 ураження виявилося АППЗ (62%).
Найбільш важливим диференціальним діагнозом АППЗ є нейроендокринні пухлини. Третьою за частотою етіології були метастази в підшлунковій залозі (n = 28,7%). Інші диференціальні діагнози включали нерідко гіперваскулярну серозну мікроцистну цистаденому, солідну псевдопапілярну пухлину, неходжкінську лімфому, вогнищевий панкреатит, внутрішньопанкреатичну додаткову селезінку і гамартоми.
Можна зробити висновок, що чим менше солідне новоутворення, тим менш імовірний діагноз АППЖ і тим частіше діагностуються нейроендокринні пухлини.
CEUS і/або C-EUS були виконані у 219 з 394 пацієнтів з використанням внутрішньовенної ін’єкції SonoVue 2,4 мл (CEUS) або 4,8 мл (CEUS) відповідно до рекомендацій Європейської федерації ультразвуку в медицині та біології.
Ізо-, гіпер- або гіпопосилення в порівнянні з навколишньою паренхімою підшлункової залози були задокументовані: у 57 з 62 пацієнтів (92%) АППЗ демонструвала гіпопосилення, в той час як у пацієнтів без АППЗ спостерігалося ізо- або гіперпосилення. Крім того, 91 з 102 нейроендокринних пухлин (89%) мала гіпер- або ізопосилення, що призвело до правильної диференціальної діагностики.
Результати з використанням CEUS були достовірнішими в порівнянні з КТ; КТ не окреслила осередкове ураження підшлункової залози у 14 з 38 пацієнтів (середній діаметр 8 мм [діапазон від 4 до 12 мм)])
Відповідно до опублікованої літературою, C-EUS і CEUS дозволяють проводити диференційну діагностику солідних пухлин підшлункової залози приблизно в 90% випадків.
ЕУЗД проти УЗД
УЗД проводилась до ЕУЗД у 45 пацієнтів (середній вік: 59 років; діапазон від 18 до 81 року; 20 чоловіків і 25 жінок) з 25 (56%) злоякісними і 20 (44%) доброякісними солідними утвореннями.
У 5 з 45 пацієнтів (11%) солідні пухлини не були виявлені під час УЗД. У 6 з 45 пацієнтів (13%) виявлення ураження при УЗД і CEUS було можливо тільки при відомих результатах ЕУЗД. У 34 з 45 пацієнтів (76%) солідні пухлини були виявлені під час УЗД до обстеження ЕУЗД.
Ми прийшли до висновку, що більшість солідних утворень може бути виявлено за допомогою УЗД, а оцінка CEUS можлива для подальшої характеристики (зобр. 1, 2).
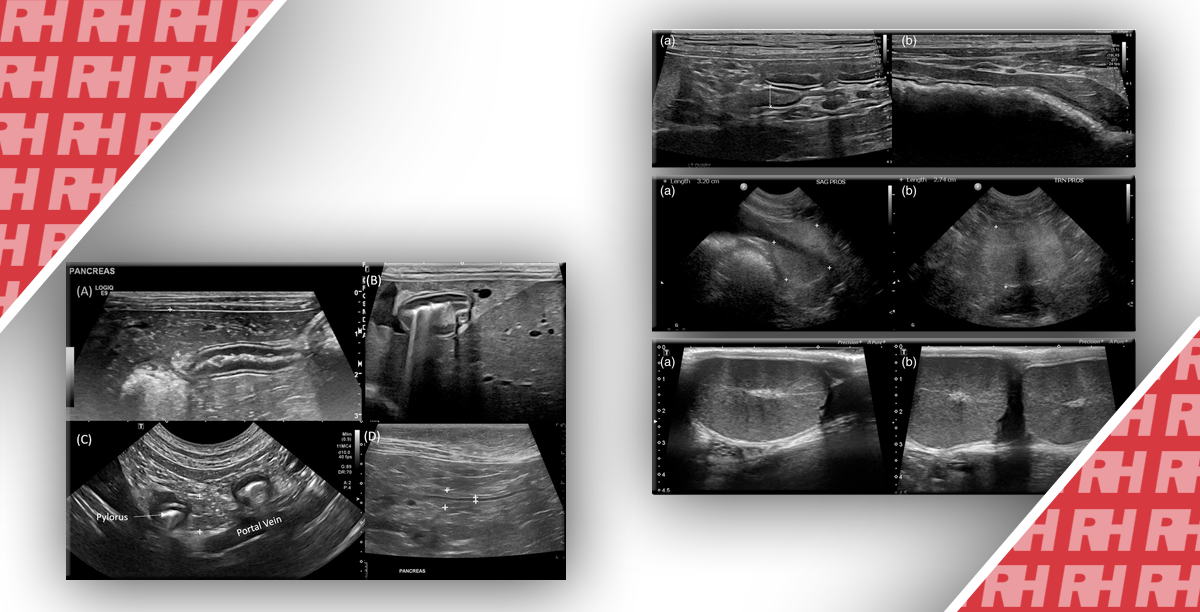
Зображення 1: Нейроендокринна неоплазія.
A, B. Показані вогнищеві ураження підшлункової залози, які були гіперцентрічнимі при використанні методів візуалізації з контрастним посиленням (7 × 6 мм, між маркерами) з використанням ендоскопічної ультрасонографії (A) і черезшкірної контрастної ультрасонографії (B). C. Також показано м’яке еластографічне зображення, яке вказує на доброякісний ураження.
Зображення 2: Нейроендокринна змішана солідно-кістозна неоплазія.
Показані солідно-кістозні вогнищеві ураження підшлункової залози (відзначені стрілками) з використанням B-режиму (A), які були гіперцентрічнимі при ендоскопічній ультрасонографії з контрастом (B) і B-режимі (C) і ультрасонографії з контрастом (D). Нейроендокринна неоплазія була діагностована за допомогою біопсії і гістопатологічної оцінки.
Ультразвукова еластографія
Ультразвукова еластографія дозволяє оцінити жорсткість тканини шляхом віртуальної пальпації. Для оцінки невеликих вогнищевих уражень підшлункової залози була розроблена ультразвукова тензометрична еластографія з використанням ЕУЗД.
М’які невеликі солідні утворення зазвичай доброякісні, тоді як більш жорсткі (більш тверді) в паренхімі підшлункової залози – злоякісні.
Можна сказати, що, особливо у пацієнтів з невеликими ураженнями підшлункової залози, ЕУЗД-еластографія може виключати злоякісні новоутворення з високим ступенем достовірності, якщо утворення відображається як м’яке. У більших (> 30 мм) результати менш переконливі, головним чином, через гетерогенність уражень, але також через супутні зміни навколишньої паренхіми підшлункової залози.
Еластографія не здатна остаточно диференціювати вогнищевий панкреатит від АППЗ, оскільки хронічний вогнищевий панкреатит також може бути більш жорстким, ніж в іншому здорова паренхіма підшлункової залози. Туберкульоз підшлункової залози також жорсткіше, ніж навколишня паренхіма, але застосування і правильна інтерпретація еластографії при хронічному панкреатиті є більш складними.
Висновок
У пацієнтів з солідними пухлинами етіологічна диференціація необхідна для прийняття обґрунтованих рішень про подальше лікування:
- радикальне хірургічне втручання у пацієнтів з резектабельними АППЗ
- онкологічне лікування у пацієнтів з неоперабельним злоякісним новоутворенням
- стратегії збереження панкреатичної паренхіми або спостереження при доброякісній нейроендокринній неоплазії
- подальше спостереження при невеликих доброякісних ураженнях (зобр. 3).
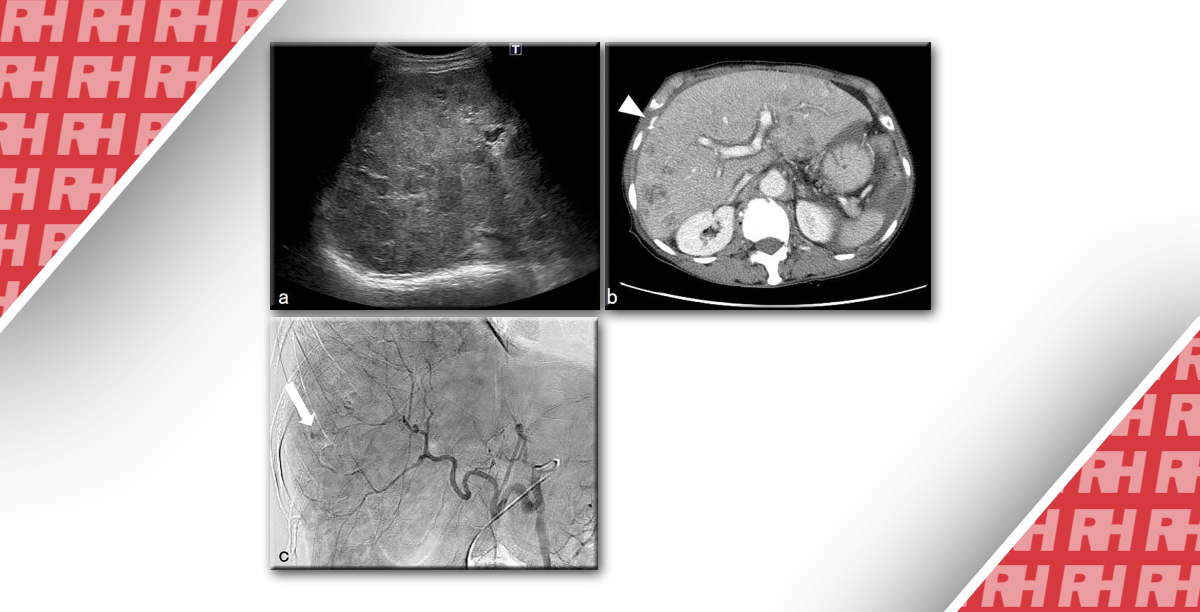
Зображення 3: Алгоритм діагностики.
На підставі паттерна поліпшення результатів CEUS і еластографії можлива подальша характеристика солідних новоутворень. Гіповаскулярність спостерігається приблизно в 90% випадків АППЗ. М’які солідні пухлини є доброякісними, за дуже невеликим винятком.
Таким чином, у пацієнтів з гіперваскулярними і/або м’якими утвореннями, біопсія тканини рекомендується до прийняття рішення про лікування, оскільки радикальна операція може бути недоцільною.
Пацієнтам з серозною цистаденомою, мезенхімальними ураженнями, і нефункціональними нейроендокринними пухлинами <10 мм з індексом Ki67 <3% можна рекомендувати подальше спостереження, тоді як НЕП> 10 мм з індексом Ki67> 3% часто вимагають спостереження через їх злоякіснийпотенціал.
Питання та відповіді (FAQ)
Які методи візуалізації використовуються для діагностики пухлин підшлункової залози?
- Для діагностики пухлин підшлункової залози використовуються ультразвукове дослідження (УЗД), комп’ютерна томографія (КТ), магнітно-резонансна томографія (МРТ) та ендоскопічна ультрасонографія (ЕУЗД). ЕУЗД, особливо з контрастним посиленням (C-EUS), демонструє високу точність у виявленні та характеристиці пухлин.
Наскільки ефективна ендоскопічна ультрасонографія (ЕУЗД) у виявленні пухлин підшлункової залози?
- ЕУЗД має високу чутливість (близько 94%) у виявленні солідних утворень підшлункової залози, що значно перевищує показники КТ, МРТ та трансабдомінального УЗД.
Які переваги використання контрастної ЕУЗД (C-EUS)?
- C-EUS покращує візуалізацію характеристик пухлини, дозволяючи краще диференціювати доброякісні та злоякісні утворення. Вона підвищує діагностичну точність, особливо у виявленні дрібних пухлин.
Як ультразвукова еластографія допомагає у діагностиці?
- Ультразвукова еластографія оцінює жорсткість тканини. М’які утворення частіше доброякісні, а жорсткі – злоякісні. Однак, еластографія не завжди може точно диференціювати вогнищевий панкреатит від аденокарциноми.
Які основні диференційні діагнози при солідних утвореннях підшлункової залози?
- Найважливішим диференціальним діагнозом аденокарциноми протоки підшлункової залози є нейроендокринні пухлини. Також можливі метастази, серозна мікроцистна цистаденомия, солідна псевдопапілярна пухлина та інші.
Що робити, якщо виявлено невелике солідне утворення підшлункової залози?
- Необхідна подальша диференціація етіології для прийняття рішення про лікування: хірургічне втручання, онкологічне лікування, спостереження або консервативна терапія. Біопсія тканини може бути необхідною для точної діагностики.
Чи завжди потрібне оперативне втручання при виявленні пухлини підшлункової залози?
- Рішення про оперативне втручання залежить від типу та розміру пухлини, її злоякісності, загального стану пацієнта та інших факторів. В деяких випадках може бути достатньо спостереження.