Резюме
Втрата вагітності може бути визначена як втрата до 20 або 24 тижнів вагітності (за першим днем останньої менструації) або втрата ембріона чи плода вагою менше 400 г, якщо термін вагітності невідомий. Щороку у світі відбувається приблизно 23 мільйони втрат вагітності, що становить 15-20% від усіх клінічно встановлених вагітностей. Втрата вагітності зазвичай пов’язана з фізичними наслідками, такими як кровотеча на ранніх термінах вагітності, що варіюється за ступенем тяжкості від кров’янистих виділень до геморагії. Однак це також може бути пов’язано з глибоким психологічним розладом, який можуть відчувати обидва партнери і який може включати почуття заперечення, шок, тривогу, депресію, посттравматичний стресовий розлад і суїцид. Прогестерон відіграє ключову роль у збереженні вагітності, і прийом прогестерону був оцінений як профілактичний захід у пацієнток з підвищеним ризиком втрати вагітності. Основна мета цієї статті – оцінити докази застосування різних форм прогестагенів у лікуванні загрозливої та рецидивуючої втрати вагітності, виходячи з припущення, що оптимальний план лікування повинен переважно включати валідований метод психологічної підтримки як доповнення до відповідного фармакологічного лікування.
Ключові слова: дидрогестерон; втрата вагітності; прогестерон; прогестаген; психологічна підтримка
1. Вступ
Втрата вагітності (ВВ) визначається як втрата вагітності до 20 або 24 тижнів вагітності (за першим днем останньої менструації) або втрата ембріона чи плода вагою менше 400 г, якщо термін вагітності невідомий [1,2,3,4]. Вагінальна кровотеча протягом перших 20 тижнів вагітності, з болем або без нього, з життєздатним плодом, що знаходиться всередині матки, без розширення або згладжування шийки матки, відома як загрозлива ВВ [2,3,5,6]. Рецидивуюча ВВ визначається як переривання двох або більше вагітностей, або трьох і більше вагітностей до досягнення плодом життєздатності [2,7,8,9,10,11]. Приблизно 23 мільйони втрат вагітності трапляються у світі щороку, що становить 15-20% від усіх клінічно визнаних вагітностей, причому 1-2% жінок, які намагаються завагітніти, зазнають повторних втрат, хоча реальна частота може бути набагато вищою [1,2,3,12,13].
З ВВ пов’язані як фізичні, так і психологічні наслідки. Кровотеча на ранніх термінах вагітності є типовою і може варіювати за ступенем тяжкості від кров’янистих виділень до геморагії [1,2,3,5,13]. Психологічний вплив може відчуватися обома партнерами і включати почуття заперечення, шок, тривогу, депресію, посттравматичний стресовий розлад і суїцид [2,13,14,15,16,17]. Наслідки ВВ є більш масштабними, якщо врахувати підвищений ризик акушерських ускладнень, таких як мертвонародження під час наступних вагітностей, потенційні довгострокові проблеми зі здоров’ям, такі як серцево-судинні захворювання та венозна тромбоемболія, а також економічні витрати для систем охорони здоров’я та суспільства: Лише у Сполученому Королівстві економічні витрати на ВВ становлять близько 471 мільйона фунтів стерлінгів на рік [13].
Важливість прогестерону на ранніх термінах вагітності та ймовірність того, що дефіцит прогестерону може призвести до ВВ, вже давно теоретично обґрунтована [18,19,20]. Як наслідок, екзогенні прогестагени широко використовуються для боротьби з дефіцитом, який може призвести до безпліддя та ВВ.
У цій статті ми обговорюємо лікування прогестагенами при ВВ та важливість його поєднання з психологічною підтримкою.
2. Стратегія пошуку та критерії відбору
Ми провели комплексний пошук літератури в PubMed та Кокранівській бібліотеці (з моменту створення бази даних до березня 2022 р.) щодо відповідних рандомізованих клінічних досліджень (РКД), систематичних оглядів та метааналізів, використовуючи комбінацію вільних текстових пошукових термінів та термінів і назв MeSH, пов’язаних з темою “Аборти, загроза переривання вагітності”, ‘Загроза передчасної вагітності’, ‘Загроза викидня’, ‘Загроза передчасних пологів’, ‘Ускладнення вагітності’, ‘Спонтанний аборт’, ‘аборт’, ‘викидень’, ‘прогестерон’, ’17-OHPC, ’17α-гідроксипрогестерону капроат’, ’17p’, ’17-альфагідроксипрогестерон’ та ‘прогестагени’. Крім того, ми вручну провели пошук у списках літератури всіх відповідних статей. Були відібрані лише англомовні публікації.
3. Прогестагени під час вагітності
Прогестерон – це жіночий статевий гормон з мультимодальною дією, який необхідний для успішної імплантації та збереження вагітності [1,2,5,21,22,23,24]. Дефіцит жовтого тіла разом з відповідним дефіцитом прогестерону був постульований як потенційний етіологічний фактор ВВ [2,3]. Як наслідок, для лікування ВВ було оцінено декілька фармакологічних втручань, включаючи прогестагени, з рекомендаціями, відображеними в більшості клінічних настанов (табл. 1).
Таблиця 1. Короткий виклад рекомендацій щодо лікування невиношування вагітності.
| Керівництво для загрозливих ВВ | |
| Міжнародні та регіональні рекомендації/цитування | Рекомендації/заяви |
| EPC guideline (2015 [5]) | У жінок з клінічним діагнозом загрози ВВ спостерігається зниження частоти спонтанних ВВ при застосуванні дидрогестерону |
| Australia and New Zealand, RANZCOG guidelines [25] | Прийом прогестагенів до другого триместру у жінок з клінічним діагнозом загрози переривання вагітності може знизити частоту мимовільних викиднів і може бути розглянутий |
| Національна настанова/цитата | Рекомендації/заяви |
| UK, NICE guidelines [26] | Запропонувати вагінальний мікронізований прогестерон 400 мг 2 р/д жінкам з внутрішньоматковою вагітністю, підтвердженою скануванням, якщо у них є вагінальна кровотеча і раніше був викидень. |
| Saudi Arabian guidelines [27] | Пероральні прогестагени, а саме дидрогестерон, добре переносяться і ефективно зменшують кількість викиднів у жінок з ризиком загрози переривання вагітності |
| Наявних доказів недостатньо, щоб рекомендувати використання вагінальних прогестагенів для лікування загрози переривання вагітності | |
| Malaysian guidelines [29] | Жінкам можна призначати:
Пероральним дидрогестероном (10 мг 2 р/д) від початку кровотечі до 1 тижня після її зупинки Пероральним дидрогестероном (10 мг р/д від початку кровотечі до 16-го тижня вагітності) або мікронізованим прогестероном (400 мг р/д вагінально/ректально), якщо в анамнезі жінки був ≥1 попередній викидень |
| FOGSI guidelines [30] | Жінки можуть лікуватися МВП (400 мг/добу до зупинки кровотечі) або пероральним дидрогестероном (початкова доза 40 мг, потім 20-30 мг/добу до 7 днів після зупинки кровотечі). |
| Chinese guidelines [31] | Пероральний дидрогестерон – перший вибір – 40 мг одразу, потім по 10 мг кожні 8 год до зникнення симптомів; потім продовжувати прийом перорального дидрогестерону протягом 1 – 2 тижнів |
| Vietnamese guidelines [32] | Ендокринні препарати, такі як прогестерон 25 мг × 2 ампули (внутрішньом’язова ін’єкція)/день, якщо є ознаки ендокринної недостатності або для розслаблення м’язів матки |
| Vietnamese Hung Vuong Hospital guidelines [33] | Лікувати симптоми після виключення інфекційного загрози переривання вагітності:
Прогестерон 25 мг/ампула (внутрішньом’язова ін’єкція); 1-4 ампули/день Напівсинтетичний (дидрогестерон), максимальна доза 40 мг/добу; Пероральний прогестерон, максимальна доза 600 мг/день |
| Taiwanese guidelines, Taiwan Society of Perinatology 2022 [34] | Єдиним рекомендованим лікарським засобом є пероральний дидрогестерон: 40 мг одразу, потім 10 мг 2 рази на день до повної ремісії симптомів; потім продовжувати прийом дидрогестерону по 10 мг 2 р/д протягом 1-2 тижнів |
| Indonesian guidelines [35] | Природні прогестагени можна використовувати як терапію при загрозі викидня
Рекомендації щодо лікування включають Дидрогестерон початкова доза 40 мг перорально, потім 3 × 10 мг до зупинки кровотечі. Потім зменшити дозу до 2 × 10 мг до 16 тижнів вагітності Прогестерон 2 × 400 мг перорально до 12 тижнів вагітності Песарій прогестерону 2 × 400 мг ректально Прогестерон гель 8%, 90 мг, 1-2 рази/день вагінально Дидроксипрогестерон 250 мг/тиждень, внутрішньом’язово |
| Mexican guidelines [36] | Існуючих доказів недостатньо для призначення прогестерону; однак використання прогестерону рекомендується для уникнення екстреної та непотрібної медичної процедури, а також для заспокоєння пацієнтки. |
| Philippines [37] | Дані обмежені і потребують подальших досліджень, однак є певні докази того, що лікування прогестероном може знизити ризик ВВ навіть у жінок без рецидивів ВВ у анамнезі.
Прогестерон доступний для застосування у трьох формах: пероральній, внутрішньом’язовій та інтравагінальній. Серед цих препаратів пероральний прогестерон є більш ефективним для лікування жінок із загрозою виникнення ВВ Прогестерон, особливо пероральний дидрогестерон, може призначатися для лікування загрози ВВ у жінок з рецидивами ВВ у анамнезі |
| Рекомендації щодо рецидивуючого ВВ | |
| Міжнародні та регіональні рекомендації/цитування | Рекомендації/заяви |
| EPC guideline [5] | У жінок з клінічним діагнозом повторного викидня (три або більше) спостерігається зниження частоти викиднів при застосуванні дидрогестерону |
| ESHRE guideline [7] | Вагінальний прогестерон на ранніх термінах вагітності не має позитивного ефекту у жінок з незрозумілим рецидивуючим ВВ. Існують деякі докази того, що дидрогестерон, який починають застосовувати, коли можна підтвердити роботу серця плода, може бути ефективним, але потрібні додаткові дослідження. |
| German (DGGG), Austrian (OEGGG), and Swiss (SGGG) Societies of Gynecology and Obstetrics guideline [10] | Синтетичні прогестагени b можна призначати жінкам з ідіопатичним рецидивуючим невиношуванням у першому триместрі вагітності для запобігання викидням |
| Лікування натуральним мікронізованим прогестероном у першому триместрі вагітності для запобігання невиношування не рекомендується жінкам з ідіопатичним рецидивуючим невиношуванням | |
| Національна настанова/цитата | Рекомендації/заяви |
| UK, Royal College of Obstetricians and Gynaecologists guidelines [11] | Існує недостатньо доказів для оцінки впливу добавок прогестерону під час вагітності для запобігання викидня у жінок з повторним невиношуванням вагітності |
| American Society for Reproductive Medicine [8] | У пацієнток з трьома або більше викиднями поспіль, що безпосередньо передували поточній вагітності, емпіричне призначення прогестагену може мати певну користь |
| Saudi Arabian guidelines [27] | Пероральні прогестагени, а саме дидрогестерон, добре переносяться та ефективно зменшують кількість викиднів у жінок з ризиком ідіопатичного рецидивуючого невиношування вагітності |
| Наявних доказів недостатньо, щоб рекомендувати використання вагінальних прогестагенів для лікування повторних викиднів | |
| Israeli guidelines [38] | Встановлено, що підтримка прогестероном має перевагу у жінок з рецидивуючими ВВ. Метааналізи та систематичні огляди виявили перевагу певних препаратів, таких як дидрогестерон |
| Malaysian guidelines [29] | Може розглянути терапію прогестероном у жінок з незрозумілими повторними викиднями: Існують певні докази того, що пероральний прийом дидрогестерону є ефективним, якщо його розпочати, коли підтверджено серцеву активність плода. |
| FOGSI guidelines [30] | Жінки можуть лікуватися пероральним дидрогестероном (10 мг 2 р/д до 20 тижнів вагітності) або МВП (400 мг/добу до 20 тижнів вагітності) |
| Chinese guidelines [31] | Пероральний дидрогестерон – перший вибір: 30 мг/день |
| Taiwanese guidelines, Taiwan Society of Perinatology 2022 [34] |
Пероральний дидрогестерон 10 мг 2 р/д або МВП 400 мг 2 р/д призначають при підтвердженні вагітності. Лікування слід продовжувати до 20-го тижня вагітності |
| Indonesian guidelines [41] |
Застосування дидрогестерону значно зменшує ризик повторного викидня та збільшує частоту настання вагітності (Рекомендація А)
Застосування дидрогестерону є більш ефективним і корисним, якщо його розпочинати, як тільки підтверджено серцеву діяльність плода/з лютеїнової фази, оскільки доведено, що він знижує ризик викидня (Рекомендація А). |
| Vietnamese guidelines [32] | Варіант лікування залежить від причини повторного викидня; у випадку ендокринної недостатності: ендокринні добавки, такі як прогестерон 25 мг × 2 ампули
(глибока внутрішньом’язова ін’єкція)/день, естроген 2 мг/день |
| Philippines [37] | Існує користь від застосування прогестагенів перорально (медроксипрогестерону ацетат 10 мг/добу або дидрогестерон 20-30 мг/добу до ≥12 тижнів) або внутрішньом’язово (гідроксипрогестерону капроат 500 мг/тиждень до 36 тижнів) для запобігання ВВ у жінок, які мали в анамнезі рецидивуючі ВВ.
Існує недостатньо доказів, щоб показати будь-який бажаний шлях, дозування або тривалість лікування |
aa Капсули, супозиторії, мікронізовані або гелі; bдопоміжний набір даних включає дидрогестерон у групі синтетичних прогестагенів [42]. 2 р/д – двічі на день; EPC – Європейський клуб прогестинів; ESHRE – Європейське товариство репродукції людини та ембріології; FOGSI – Федерація акушерських та гінекологічних товариств Індії; МВП – мікронізований вагінальний прогестерон; NICE – Національний інститут удосконалення охорони здоров’я та медичної допомоги; ВВ – втрата вагітності; RANZCOG – Королівський австралійський та новозеландський коледж акушерів-гінекологів; Великобританія – Сполучене Королівство.
Прогестагени – це стероїдні гормони, які зв’язуються з рецепторами прогестерону та активують їх [3,43,44,45]. Відмінності в хімічній структурі прогестагенів, що призводять до різної селективності зв’язування з рецепторами (андрогени, глюкокортикоїди, естрогени та мінералокортикоїди), ефективності та біодоступності, можуть призводити до різних побічних ефектів, включаючи потенційно шкідливий вплив на плід, що розвивається, а це означає, що не всі прогестагени придатні для використання під час вагітності [44,45,46]. Через перехресну реактивність з іншими рецепторами єдиними прогестагенами, дозволеними для застосування під час вагітності, є прогестерон, дидрогестерон та 17α-гідроксипрогестерону капроат [44,47,48]. Вони доступні в різних формах для клінічного застосування, включаючи пероральні, вагінальні та внутрішньом’язові препарати [44,49,50]. Дослідження показали, що для профілактики ВВ вагінальний прогестерон може бути більш ефективним, ніж внутрішньом’язові ін’єкції [51,52], а нещодавні метааналізи дійшли висновку, що пероральні прогестагени можуть бути настільки ж ефективними, як і прогестагени, що вводяться внутрішньом’язово або вагінально [1,2,3].
4. Використання прогестагенів при втраті вагітності
Застосування прогестерону оцінювали у жінок із загрозою ВВ або у жінок з рецидивами ВВ.
4.1. Загроза переривання вагітності
Багато досліджень вивчали здатність прогестагенів лікувати загрозливу ВВ. Wahabi та співавт. провели попарний метааналіз семи досліджень (за участю 696 учасниць) для вивчення ефективності прогестагенів у лікуванні загрози ВВ і виявили, що застосування прогестагенів порівняно з плацебо або відсутністю лікування знижує ризик ВВ (відношення ризиків [ВР] 0,64, 95% довірчий інтервал [ДІ] 0,47-0,87) [3]. Аналогічно, Wang та співавт. і Li та співавт. оцінили РКД, в яких порівнювали прогестаген з плацебо, без лікування або будь-яким іншим лікуванням, і повідомили про відносні ризики 0,64 (95% ДІ 0,48-0,85) [53] і 0,73 (95% ДІ 0,59-0,92) [54] відповідно. Висновок останнього дослідження Li та співавт. про те, що користь спостерігалася лише при застосуванні пероральних прогестагенів, а не вагінального прогестерону [54], був підданий критиці Devall та співавт., які дійшли висновку, що використані допоміжні дослідження мали високий ризик упередженості, і що для подальшої оцінки ефективності та безпечності пероральних прогестагенів необхідні більш якісні рандомізовані дослідження [55]. Li та співавт. згодом погодилися з цією оцінкою і підтвердили, що саме з цієї причини їхню оригінальну публікацію, яка підкреслює їхні висновки щодо пероральних прогестагенів, слід інтерпретувати з обережністю [56]. Нещодавно в мережевому метааналізі оцінювали ефективність і безпеку різних прогестагенів у лікуванні загрози ВВ і підтвердили, що прогестагени ефективні в зниженні ризику ВВ [57].
4.2. Повторна втрата вагітності
Ряд досліджень, включаючи РКД, оцінювали ефективність прогестагенів при рецидивуючих ВВ. Haas та співавт. провели попарний метааналіз 10 досліджень (із загальною кількістю учасниць 1684) для вивчення ефективності прогестагенів у лікуванні рецидивуючих ВВ. Вони порівнювали прогестаген з плацебо або відсутністю лікування і виявили, що застосування прогестагенів знижує ризик рецидиву ВВ (ВР 0,73, 95% ДІ 0,54-1,00) [2].
4.3. Який прогестаген слід використовувати при втраті вагітності?
Багато уваги приділяється здатності мікронізованого вагінального прогестерону (МВП) знижувати ризик майбутніх ВВ у жінок, які страждають на рецидивуючу ВВ. У дослідженні PROMISE – подвійному сліпому плацебо-контрольованому дослідженні, в якому 836 жінок з незрозумілими рецидивуючими ВВ були розподілені випадковим чоном на прийом супозиторіїв МВП двічі на день (n = 404) або відповідного плацебо (n = 432) з моменту отримання позитивного результату тесту на вагітність до 12 тижня вагітності – лікування МВП достовірно (p = 0. 45) покращити показник живонароджуваності (ПЖН) (65,8% МВП проти 63,3% плацебо [ВР 1,04, 95% ДІ 0,94-1,15]) [58]. Аналогічно, дослідження PRISM (ще одне подвійне сліпе, плацебо-контрольоване, рандомізоване дослідження з оцінки МВП порівняно з плацебо у 4153 жінок з вагінальними кровотечами на ранніх термінах вагітності) не виявило статистично значущої різниці в показниках ПЖН (первинна кінцева точка) між групами лікування: З 2079 жінок, які отримували МВП, і 2074 жінок, які отримували плацебо, ПЖН становив 75% у групі МВП порівняно з 72% у групі плацебо (ВР 1,03, 95% ДІ 1,00-1,07; p = 0,08) [59]. Попередньо визначений аналіз даних у підгрупах виявив значний підгруповий ефект у жінок, які перенесли ≥3 попередніх ВВ (ПЖН 72% у групі МВП порівняно з 57% у групі плацебо: ВР 1,28, 95% ДІ 1,08-1,51; р = 0,007) [59]. Подальший post hoc аналіз підгруп показав, що МВП був ефективним у жінок, які перенесли ≥ 1 попереднього ВВ (ВР 75% з МВП проти 70% з плацебо; ВР1,09, 95% ДІ 1,03-1,15; p = 0,003) [60].
Результати підгрупи PRISM підтверджують дані метааналізів, які дійшли висновку, що прогестагени можуть запобігати ВВ у жінок з рецидивуючими ВВ [2,42,61], що змусило Національний інститут охорони здоров’я та якості медичної допомоги переглянути свої настанови і рекомендувати використання МВП поза показаннями [26]. Однак перевага МВП над іншими формами прогестерону не є очевидною. Подвійне сліпе, рандомізоване, плацебо-контрольоване дослідження прогестагену дидрогестерону продемонструвало його ефективність у жінок з рецидивуючими ВВ [62], але подібних надійних досліджень для інших прогестагенів немає.
5. Шляхи введення прогестагенів та вподобання пацієнток і лікарів
Прогестагени відрізняються за своєю ефективністю, селективністю зв’язування з рецепторами, біодоступністю та способом введення, і ці фактори повинні визначати вибір найбільш підходящого лікування [44,46]. Незважаючи на мікронізацію, пероральному застосуванню прогестерону все ще перешкоджає низька біодоступність [44], а це означає, що потрібні високі дози, що призводить до побічних ефектів, таких як сонливість, нудота і головний біль [46,63,64,65]. Вагінальне введення мікронізованого прогестерону покращує концентрацію в матці, але може викликати подразнення, вагінальні виділення і кровотечу; часто є неприємним; або може призвести до вимивання препарату, якщо кровотеча сильна [64,66,67,68]. Оптимальний рівень прогестерону в крові досягається при внутрішньом’язовому введенні, але може спричинити утворення абсцесів і бути надзвичайно болючим [67].
Вагінальні та пероральні препарати є найбільш широко вивченими при ВВ, і дуже ймовірно, що пацієнтки надаватимуть перевагу тій чи іншій формі на основі зручності та переносимості. Хоча можна припустити, що зручність і відсутність вагінальних побічних ефектів можуть призвести до переваги перорального прийому, дослідження в цьому відношенні не проводилися в умовах рецидивуючого ВВ. Однак дослідження інших гінекологічних захворювань показали, що як пацієнтки, так і медичні працівники загалом надають перевагу пероральному застосуванню перед вагінальним [69,70,71,72], а пероральний дидрогестерон став широко застосовуватися під час вагітності.
6. Дидрогестерон
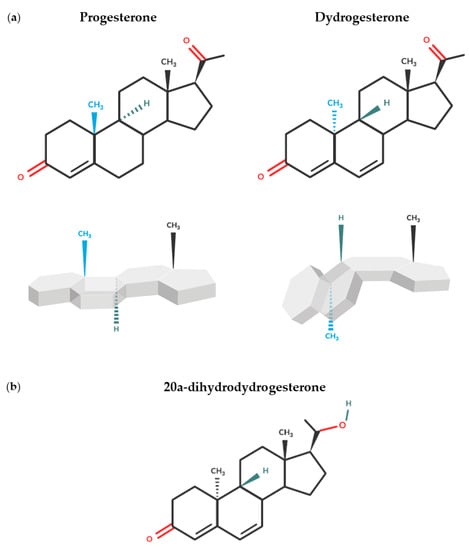
Дидрогестерон є ретропрогестероном та потужним і селективним пероральним агоністом рецепторів прогестерону [44,73]. Зміна просторової орієнтації метильної групи при 10-му карбоні та подвійний зв’язок між карбонами 6 та 7 відрізняють дидрогестерон від прогестерону та надають йому “зігнутої” форми (зобр. 1а) [46,64,73]. Ця унікальна структура зумовлює високу пероральну біодоступність, а висока селективність дидрогестерону до прогестеронового рецептора означає, що його можна застосовувати в дозах, у 10-20 разів нижчих, ніж у мікронізованого прогестерону для перорального застосування [44,64,74]. Крім того, на відміну від інших форм прогестерону, основний метаболіт дидрогестерону, 20α-дигідрогестерон (зобр. 1б), проявляє подібну прогестагенну селективність до вихідної молекули, що зводить до мінімуму небажані побічні ефекти (ПЕ) [44].
Зображення 1. Хімічні структури (а) прогестерону та дидрогестерону і пов’язана з цим різниця у просторовій конформації та (б) основного метаболіту дидрогестерону, 20α-дигідрогестерону.
6.1. Ефективність дидрогестерону при втраті вагітності
Існують публікації, які не є релевантними для обговорення через їхній вік, якість та дизайн [75]; однак останнім часом з’явилася велика кількість доказів (включаючи РКД, огляди та метааналізи), які підтверджують ефективність дидрогестерону як при загрозливому (табл. 2), так і при рецидивуючому (табл. 3) ВВ.
Таблиця 2. Дидрогестерон при загрозі переривання вагітності.
| Показник ВВ | ||||||
|---|---|---|---|---|---|---|
| РКД | Лікування дидрогестероном | Контрольне лікування | Дидрогестерон | Контрольна або нелікована група | ВР/ВШ (95% ДІ) |
p Value |
| [76] | Дидрогестерон 40 мг, потім 10 мг в/в (n = 74) до зупинки кровотечі або консервативна терапія з постільним режимом і фолієвою кислотою | Всі жінки отримували постільний режим та фолієву кислоту (n = 80) | 4.1% | 13.8% | – | p = 0.037 |
| [77] | Стандартна підтримуюча терапія та дидрогестерон 10 мг 2 р/д (n = 86) до 1 тижня після зупинки кровотечі | Усі жінки отримували стандартну підтримуючу терапію a (n = 60) | 17.5% | 25.0% | – | p < 0.05 |
| [78] | Дидрогестерон 40 мг (стандартна доза), потім 10 мг 2 р/д (n = 96) до 16-го тижня | Консервативне лікування з постільним режимом (n = 95) | 12.5% | 28.4% | – | p < 0.05 |
| [79] | Дидрогестерон 10 мг 2 р/д (n = 71) протягом 2 тижнів | Пероральний мікронізований прогестерон 200 мг 2 р/д (n = 70) протягом 2 тижнів | 15.2% | 10.2% | – | p = 0.581 |
| [80] | Дидрогестерон 40 мг (статична доза), потім 10 мг 3 р/д (n = 203) до 12-го тижня або через 1 тиждень після припинення кровотечі | Плацебо (n = 203) | 12.8% | 14.3% | ВР: 0.897 (0.548–1.467) |
p = 0.772 |
| Показник ВВ | ||||||
| Метааналіз | Набір даних | Основний результат | Дидрогестерон | Контроль | ВР/ВШ (95% ДІ) |
p Value |
| [67] | Дидрогестерон проти плацебо або консервативного лікування
П’ять досліджень (n = 660) |
Значнеb зниження частоти викиднів при застосуванні дидрогестерону | 13.0% | 24.0% | ВШ: 0.47 (0.31–0.70) |
не застосовується b |
| [6] | Дидрогестерон проти контролю
(консервативне лікування) Три дослідження (n = 491) |
Значне зниження частоти викиднів при застосуванні дидрогестерону | 11.7% | 22.6% | ВШ: 0.43 (0.26–0.71) |
p = 0.001 |
| Вагінальний прогестерон у порівнянні з контролем (плацебо або консервативне лікування)
Чотири дослідження (n = 286) |
Зниження частоти викиднів при застосуванні вагінального прогестерону (незначне) | 15.4% | 20.3% | ВШ: 0.72 (0.39–1.34) |
p = 0.3 | |
| [3] | Пероральний прогестаген проти відсутності лікування
Три дослідження (n = 408); дидрогестерон – два дослідження (n = 337) |
Значне зниження частоти викиднів при застосуванні пероральних прогестагенів (включаючи дидрогестерон) | не застосовується | не застосовується | ВР: 0.57 (0.38–0.85) |
p = 0.0059 |
| Вагінальний прогестерон проти плацебо
Чотири дослідження (n = 288) |
Незначний або відсутній ефект лікування вагінальним прогестероном | не застосовується | не застосовується | ВР: 0.75 (0.47–1.21) |
p = 0.24 | |
| [54] | Прогестагени порівняно з плацебо або без лікування
Десять досліджень (n = 5104); дидрогестерон порівняно з плацебо або без лікування, чотири дослідження (n = 563) |
Пероральні прогестагени можуть мати переваги щодо частоти ВВ: переваги спостерігаються лише при застосуванні перорального прогестагену, а не вагінального прогестерону | 18.5% | 21.9% | ВР: 0.73 (0.59–0.92) |
p = 0.01 |
| [57] | Прогестагени проти інших препаратів прогестерону або плацебо
59 досліджень (n = 10 424); дидрогестерон порівняно з іншими препаратами прогестерону або плацебо, 49 досліджень (n = 2793) |
Дидрогестерон достовірно знижував ризик викидня порівняно з вагінальним, в/м та пероральним мікронізованим прогестероном або плацебо | не застосовується | не застосовується | Вагінальний ВШ: 0.50 (0.34–0.74) |
p = 0.002 |
| В/м ВШ: 0.41 (0.32–0.54) |
p = Дидрогестерон 10 мг 2 р/д (n = 82) до тижня вагітності 120.006 | |||||
| Пероральний ВШ: 0.37 (0.28–0.48) |
p < 0.001 | |||||
| Плацебо ВШ: 0.42 (0.29–0.61) |
p < 0.001 | |||||
a Залізо, фолієва кислота, полівітамінні добавки та рекомендований постільний режим; bP value не вказано. 2 р/д – двічі на день; ДІ – довірчий інтервал; в/м – внутрішньом’язово; НЗ – не застосовується; ВШ – відношення шансів; ВВ – втрата вагітності; РКД – рандомізоване клінічне дослідження; ВР – відношення ризиків; 3 р/д – тричі на день.
Таблиця 3. Дидрогестерон при повторній втраті вагітності.
| Показник ВВ | ||||||
|---|---|---|---|---|---|---|
| РКД | Лікування дидрогестероном | Контрольне лікування | Дидрогестерон | Контрольна або нелікована група | ВР/ВШ (95% ДІ) |
p Value |
| [81] | Dydrogesterone 10 mg 2 р/д (n = 82) until gestation Week 12 | Без додаткового лікування (n = 48) | 13.4% | 29.0% | – | p = 0.028 |
| [62] | Дидрогестерон 20 мг/добу (n = 175) до 20-го тижня вагітності | Плацебо (n = 173) | 6.9% | 16.8% | – | p = 0.004 |
| Показник ВВ | ||||||
| Метааналіз | Набір даних | Основний результат | Прогестаген | Контроль | ВР/ВШ (95% ДІ) |
p Value |
| [82] | Дидрогестерон порівняно з плацебо або консервативним лікуванням (стандартне лікування)
Три дослідження (n = 509) |
Значне зниження частоти викиднів при застосуванні дидрогестерону | 10.5% | 23.5% | ВШ: 0.29 (0.13–0.65) |
не застосовується a |
| [42] | Прогестагени проти плацебо або відсутності лікування
Десять досліджень (n = 1586); дидрогестерон порівняно з плацебо або без лікування, три дослідження (n = 277) |
Нижчий ризик викидня при лікуванні прогестагенами | – | – | ВР: 0.72 (0.53–0.97) |
p = 0.03 |
| [2] | Прогестагени проти плацебо або
без лікування Десять досліджень (n = 1684); дидрогестерон порівняно з плацебо або без лікування, три дослідження (n = 518) |
Чисельне зниження частоти викиднів при лікуванні прогестагенами (несуттєве) | 20.1% | 27.5% | ВР: 0.73 (0.54–1.00) b |
p = 0.10 |
a p value не вказано; b два з трьох досліджень з використанням дидрогестерону показали чітке зниження ризику ВВ при лікуванні прогестагеном [62,81]. 2 р/д – двічі на день; ДІ – довірчий інтервал; НЗ – не застосовується; ВШ – відношення шансів; ВВ – втрата вагітності; РКД – рандомізоване клінічне дослідження; ВР – відношення ризиків.
Три РКД показали, що жінки із загрозою ВВ, які отримували дидрогестерон, мали достовірно (p < 0,05) нижчу частоту ВВ порівняно з жінками, які отримували постільний режим з підтримуючою терапією або без неї [76,77,78]. Це підтверджується різними метааналізами, які демонструють достовірне (p = 0,001) зниження частоти ВВ при застосуванні пероральних прогестагенів, включаючи дидрогестерон [3,6]. У кожному випадку препарати порівняння мали незначний або взагалі не мали лікувального ефекту і суттєво не знижували частоту ВВ (табл. 2). У більш пізньому метааналізі Zhao та співавт. оцінили ефективність і безпеку різних прогестагенів у 59 РКД, в яких брали участь 10 424 жінки, і також дійшли висновку, що пероральний дидрогестерон був більш ефективним у лікуванні загрози ВВ, ніж вагінальний прогестерон [57].
Основні дані щодо ефективності дидрогестерону при рецидивуючих ВВ наведені в таблиці 3. Два РКД продемонстрували, що жінки з рецидивуючими ВВ, які отримували дидрогестерон, мали достовірно (p < 0,05) нижчі показники ВВ, ніж ті, які отримували плацебо або не отримували додаткового лікування [62,81]. Два метааналізи повідомили про подібні позитивні ефекти дидрогестерону у жінок з рецидивуючими ВВ. Один з них оцінював три дослідження (n = 509) і дійшов висновку, що дидрогестерон спричиняє суттєве зниження частоти ВВ порівняно з плацебо або консервативним лікуванням [82]. В іншому дослідженні, яке оцінювало загалом 10 досліджень (n = 1684), що вивчали прогестагени порівняно з плацебо або відсутністю лікування [2], було зроблено висновок про чисельне зниження частоти ВВ при лікуванні прогестагенами, в тому числі і в дослідженнях з використанням дидрогестерону. Примітно, що в цьому останньому метааналізі два дослідження, які показали чітке зниження ризику ВВ при лікуванні прогестагенами, були двома з трьох, в яких використовувався дидрогестерон [2,62,81]. Ці результати підтверджуються ще одним РКД, в якому порівнювали дидрогестерон з вагінальним прогестероном у жінок з рецидивуючою ВВ, в якому було виявлено, що для повної зупинки кровотечі потрібно менше часу у пацієнток, які отримували дидрогестерон, порівняно з пацієнтками, які отримували вагінальний прогестерон (53,90 ± 9,09 проти 94,60 ± 7,29 год, р < 0,0001) [83].
Нещодавно Devall та співавт. провели мережевий метааналіз (який об’єднав прямі та непрямі докази відносних ефектів лікування для досягнення єдиного узгодженого аналізу) для оцінки прогестагенів з метою профілактики ВВ і дійшли висновку, що прогестагени, ймовірно, мають незначну або нульову різницю в ПЖН у жінок із загрозливою або рецидивуючою ВВ; однак, МВП можуть збільшувати ПЖН у жінок з ≥ 1 попередньою ВВ в анамнезі та кровотечею на ранніх термінах вагітності [1]. Вони також дійшли висновку, що все ще існує невизначеність щодо ефективності та безпеки альтернативних методів лікування прогестагенами при загрозі та рецидиві ВВ [1].
Цікаво відзначити, що мережевий метааналіз, проведений Devall та співавт., включав сім РКД, лише одна з яких була присвячена дослідженню дидрогестерону [1]. На противагу цьому, Zhao та співавт. включили значно більшу кількість РКД, з великою часткою тих, що досліджували дидрогестерон [57]. Фактично, сучасні настанови відображають сукупність доказів і підтримують застосування дидрогестерону як при загрозливому, так і при рецидивуючому ВВ, що свідчить про добрий профіль ефективності та безпеки, з низькою частотою ускладнень у матері та плода (табл. 1). Суб’єктивний характер рішення про виключення або включення досліджень до мережевих метааналізів ще раз підкреслює цінність і важливість постійного врахування первинних даних і проведення систематичних оглядів з метааналізом.
6.2. Безпека застосування дидрогестерону під час вагітності
Дидрогестерон продається і використовується з 1960-х років для лікування низки станів, пов’язаних з недостатністю прогестерону, і показаний для лікування як загрозливої, так і рецидивуючої ВВ у багатьох країнах світу [47,84]. На основі даних про кумулятивну експозицію дидрогестерону з квітня 1960 року по квітень 2021 року оцінюється, що постмаркетингова експозиція пацієнток становить 137,5 млн років лікування. У 2014 році, виходячи з даних про продажі, повідомлялося, що з квітня 1960 року по квітень 2014 року дидрогестерон внутрішньоутробно впливав на понад 20 мільйонів вагітностей [85]. У період з 1977 по 2005 рік дані фармаконагляду виявили лише 28 випадків вроджених вад розвитку, які потенційно можуть бути пов’язані з впливом дидрогестерону на плід [86]. Це може бути пов’язано з унікальною структурою дидрогестерону, яка забезпечує ефективність при пероральному застосуванні в низьких терапевтичних дозах, уникаючи проблем переносимості, пов’язаних з вагінальним введенням прогестерону. Крім того, висока селективність дидрогестерону до рецепторів прогестерону може допомогти обмежити ризик побічних ефектів [44], що підтверджується добре вивченим профілем безпеки дидрогестерону, який не викликає значних занепокоєнь щодо безпеки для матері або плоду, що розвивається, при застосуванні під час вагітності [87].
6.2.1. Материнська безпека
Доведено, що дидрогестерон має хороший профіль безпеки з низькою частотою материнських ускладнень. Крім того, він так само добре переноситься, як і вагінальний прогестерон, за результатами аналізу безпеки, проведеного в дослідженнях з оцінки застосування дидрогестерону для підтримки лютеїнової фази під час екстракорпорального запліднення (ЕКЗ), а також у дослідженнях з вивчення застосування дидрогестерону при загрозливому та рецидивуючому ВВ [74].
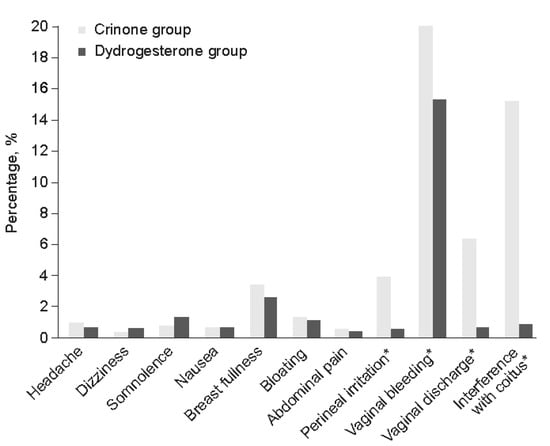
РКД, в якому порівнювали дидрогестерон та вагінальний прогестероновий гель для підтримки лютеїнової фази, підтвердило, що пацієнтки, які отримували прогестероновий гель, мали вищу частоту вагінального подразнення та виділень, вагінальних кровотеч та перешкод для статевої активності порівняно з пацієнтками, які отримували дидрогестерон (зобр. 2) [68]. Метааналіз індивідуальних даних учасниць досліджень підтримки лютеїнової фази Lotus I і II підтвердив, що частота материнських ПЕ була подібною між групами лікування дидрогестероном і МВП, причому найпоширенішою ПЕ була вагінальна кровотеча [88,89,90]. Ці результати підтверджуються нещодавнім ретроспективним когортним дослідженням, яке вивчало, чи впливає застосування дидрогестерону порівняно з МВП на результати вагітності при перенесенні заморожених ембріонів, і показало, що материнські ускладнення були подібними в обох групах пацієнток [91].
Зображення 2. Переносимість дидрогестерону порівняно з вагінальним гелем прогестерону (8%) для підтримки лютеїнової фази [68]. * p < 0,05 за критерієм хі-квадрат на користь групи Кринон. Передрук з Eur J Obstet Gynecol Reprod Bio, Vol 186, Tomic V, Tomic J, Klaic DZ та ін. Пероральний дидрогестерон порівняно з вагінальним гелем прогестерону в підтримці лютеїнової фази: рандомізоване контрольоване дослідження, стор. 49-53, Copyright 2015, з дозволу Elsevier.
Цей сприятливий профіль материнської безпеки був імітований у дослідженнях, що вивчали застосування дидрогестерону як при загрозі, так і при рецидиві ВВ, які не виявили суттєвих відмінностей у загальному рівні материнських ускладнень при застосуванні дидрогестерону порівняно з пероральним застосуванням мікронізованого прогестерону або плацебо [79,80].
6.2.2. Безпека плоду
Сприятливий профіль безпеки дидрогестерону також був відзначений при розгляді ускладнень для плода, таких як низька вага при народженні, неонатальна смертність і вроджені аномалії [2,74].
У дослідженнях Lotus I і II, а також у подальших мета- і субпопуляційних аналізах частота вроджених, сімейних і генетичних порушень була низькою і подібною між пероральним дидрогестероном і гелем МВП [74,84,88,89,90,92]. Ці результати були підтверджені більш пізніми ретроспективними когортними дослідженнями. В одному з таких досліджень оцінювали 3556 немовлят у Китаї після ЕКЗ з використанням протоколу дидрогестерон + людський менопаузальний гонадотропін (n = 1429) або короткого протоколу агоніста гонадотропін-рилізинг-гормону (n = 2127) і виявили, що ці два протоколи не мали відмінностей у характеристиках маси тіла при народженні і мали схожу частоту вроджених вад розвитку після впливу дидрогестерону [93]. В іншому, більш пізньому, ретроспективному когортному дослідженні вивчали, чи впливає застосування дидрогестерону порівняно з МВП на результати вагітності при екстракорпоральному заплідненні замороженими ембріонами, і виявили, що аномалій розвитку плода не спостерігалося в жодній з груп лікування [91]. Аналогічно, дослідження загрозливого та рецидивуючого ВВ також не виявили суттєвих відмінностей у плодових/неонатальних ускладненнях при застосуванні дидрогестерону порівняно з плацебо або МВП [74].
З’явилися публікації, в яких стверджується, що дидрогестерон має тератогенну дію. Через поганий дизайн і недотримання основних принципів епідеміологічних досліджень (відмінності в материнській популяції, що призводять до плутанини, відсутність підтвердженого впливу дидрогестерону, об’єднання різних вад серця під час оцінки, ігнорування супутніх захворювань і соціально-економічного статусу), причинно-наслідковий зв’язок між дидрогестероном і вадами серця не може і не повинен базуватися на дослідженні, проведеному Zaqout et al. та співавт. [94]. Аналогічно, в іншому дослідженні, опублікованому в 2020 році, стверджувалося, що дидрогестерон має тератогенні ефекти після впливу рекомендованих доз у вагітних жінок [95]; однак суттєві занепокоєння щодо дизайну дослідження, статистичного аналізу, непослідовності та неточності представлення даних і достовірності висновків спонукали журнал відкликати цю статтю.
Зважаючи на широке застосування, значний тератогенний ризик дидрогестерону без проблем з безпекою видається дуже малоймовірним [96]. Достовірність і подальше використання відкликаних і неякісних даних нещодавно поставили під сумнів Katalinic та співавт., які провели метааналіз шести РКД і дійшли висновку, що застосування дидрогестерону під час першого триместру вагітності не пов’язане зі значним підвищенням ризику вроджених аномалій (ВР 0,96, 95% ДІ 0,57-1,62). Більше того, вони підтримують використання дидрогестерону, за наявності показань, у лікуванні загрозливого або рецидивуючого ВВ [87].
7. Доповнення фармакологічного лікування психологічною підтримкою
7.1. Психологічний вплив ризикованих вагітностей на жінок та результати вагітності
Вагітність є ризикованою, коли існує підвищена ймовірність несприятливого результату для матері або плода, що може статися з різних причин, таких як: розвиток гіпертензивних розладів вагітності, гестаційний цукровий діабет, зміни шийки матки та відшарування плаценти, та/або серйозні аномалії, що виникають у дитини [97,98,99].
Добре задокументовано, що вагітність з високим ризиком може мати негативний вплив як на психологічний, так і на фізичний стан жінки, викликаючи негативні емоції, такі як страх, шок, горе, провину і дистрес [97,100,101]. З’являється все більше доказів того, що психологічне благополуччя може впливати на перебіг вагітності. Наприклад, підвищений рівень дистресу під час вагітності з високим ризиком може бути пов’язаний зі шкідливими наслідками для дитини, такими як низька вага при народженні та передчасні пологи, а нещодавні публікації загалом свідчать про те, що психологічні консультації, які можуть підвищити відчуття контролю, можуть допомогти покращити результати вагітності [97,99,101].
Хоча зараз все більше уваги приділяється необхідності вивчення емоційних і психологічних проблем, а також медичних аспектів під час вагітності з високим ризиком, метою цієї статті є зосередитися на тих дослідженнях, які оцінювали психологічне благополуччя жінок з високим ризиком ВВ.
7.2. Психологічні наслідки втрати вагітності
Глибокий емоційний дистрес і психологічну захворюваність зазвичай відчувають жінки з кровотечею при загрозі ВВ, а також жінки з рецидивуючими ВВ [1,2,3,102,103]. Однак повідомлялося про різницю між психологічним впливом одноразової втрати і багаторазових ВВ, коли було виявлено, що депресивні симптоми або ризик психологічного дистресу зростають зі збільшенням кількості попередніх втрат вагітності [104]. Дійсно, численні дослідження повідомляють про високий рівень тривоги і депресії у жінок, які пережили повторну втрату вагітності, причому повторюваний характер цієї втрати посилює емоційний вплив, а ранні етапи нової вагітності є особливо складним періодом для жінок через занепокоєння щодо можливості повторної втрати вагітності [9,14,15,17,102,103,105]. Про це свідчать результати фокус-групового дослідження, в якому повідомлялося, що жінки, які пережили повторні втрати вагітності, не могли впевнено відчувати надію або радість під час періоду очікування і часто використовували “підготовку до найгіршого” як стратегію подолання в цей час [106].
Замість того, щоб знову і знову переживати цей період невизначеності, за відсутності адекватної емоційної підтримки та/або навичок подолання, деякі жінки, які пережили рецидиви ВВ, вирішують більше не намагатися завагітніти [16,107], що підкреслює необхідність поєднання фармакологічного лікування загрозливого та рецидивуючої ВВ з певною формою психологічної підтримки або консультування як для жінок, так і для їхніх партнерів у цей вирішальний період [108,109,110].
7.3. Як психологічний стан жінки впливає на ризик втрати вагітності?
Вплив стресу на ризик ВВ вивчався в численних дослідженнях. У великому проспективному дослідженні стресу, пов’язаного з роботою, у майже 4000 вагітних жінок було виявлено, що стрес асоціюється з вищим ризиком ВВ у жінок старше 32 років (p = 0,04), жінок, які палять (p = 0,02), і під час перших вагітностей (p = 0,06) [111]. Аналогічно, в когортному дослідженні 1098 вагітних жінок повідомлялося, що вищий рівень сприйманого стресу був пов’язаний з наступними ВВ (p = 0,024) [112]. На підтримку цих даних метааналіз восьми досліджень “випадок-контроль” і когортних досліджень показав, що психологічний стрес асоціюється з підвищеним ризиком ВВ (співвідношення шансів 1,42) [113], а нещодавно ці результати були підтверджені проспективним когортним дослідженням 293 жінок, які відвідували відділення ранньої діагностики вагітності, в якому повідомлялося, що відсутність емоційного благополуччя пов’язана з підвищеним ризиком ВВ [114].
7.4. Чи може психологічна підтримка допомогти покращити благополуччя пацієнта та його партнерів?
Раніше було висловлено припущення, що існує недостатньо доказів на підтримку консультування після раннього ВВ [115]. Тим не менш, нещодавно з’явилися повідомлення про те, що жінки та їхні партнери висловили незадоволену потребу в психологічних консультаціях, які забезпечать емоційну підтримку та стратегії, що допоможуть їм впоратися з ситуацією під час і після ВВ, під час наступної вагітності, а також при прийнятті рішення про те, чи варто намагатися завагітніти знову [105,116,117]. Незважаючи на відомі психологічні та емоційні наслідки ВВ і потенційний вплив стресу на результати вагітності, на ранніх стадіях нової вагітності доступна обмежена підтримка і консультування [9]; однак, що обнадіює, в останні роки ця сфера почала повільно розвиватися, щоб зосередитися на досвіді пацієнтки, і все більше досліджень тепер повідомляють про думки і почуття не тільки жінок, але і їхніх партнерів, і підтверджують, що як жінки, так і їхні партнери схильні до ризику розвитку тривоги і депресії [118,119,120,121,122].
Хоча психологічна та підтримуюча допомога після ВВ не була широко вивчена, ряд психологічних втручань, таких як консультування, психотерапія на основі усвідомленості, когнітивно-поведінкова терапія та заходи з позитивної переоцінки (ЗПП), були досліджені в контексті рецидивуючих ВВ і дали багатообіцяючі результати; отримано попередні докази переваг щодо стресу, депресії та тривоги, причому ЗПП отримала позитивні відгуки від пацієнтів щодо простоти застосування та впливу на мислення [9,107,123,124,125,126]. Підтвердженням ефективності цих втручань стало нещодавнє дослідження за участю 294 жінок, в якому 72,7% (n = 176) народили живих дітей, і в якому, як повідомлялося, підтримуюча терапія була, ймовірно, єдиним найбільш ефективним методом лікування [127]. Інше дослідження, проведене серед жінок, які перенесли повторні ВВ, підтвердило, що пацієнт-орієнтована допомога може мати значний вплив на ймовірність народження живої дитини під час наступної вагітності; загалом, ПЖН для цих пар становила близько 80% [103]. Пізніші дослідження підтвердили, що медичні працівники також визнають необхідність кращого догляду після ВВ і усвідомлюють, що необхідно вжити термінових заходів для покращення можливостей, які вони надають, включаючи збільшення інформації про ВВ, більш емоційно чутливий догляд під час ВВ і більше варіантів психологічної підтримки [108,109,110,128]. Важливо, що незалежно від втручання, більшість настанов підкреслюють цю незадоволену потребу і важливу роль підтримуючої допомоги [7,8,11].
8. Майбутні дослідження та висновки
Ми підкреслили, що прогестагени, такі як дидрогестерон, можуть бути корисними в лікуванні загрозливого та рецидивуючого ВВ. Тривають дослідження для поглиблення нашого розуміння факторів, пов’язаних з пацієнтками, таких як різноманітність репродуктивного мікробіому та його зв’язок з наслідками вагітності [129,130,131], а також факторів, пов’язаних з лікуванням, таких як: як комбіноване лікування внутрішньоутробних патологій, імунного статусу та функції щитоподібної залози – так звана стратегія лікування “OPTIMUM” (OPtimization of Thyroid function, IMmunity, and Uterine Milieu) – може потенційно покращити результати вагітності [132]; оптимальна тривалість лікування прогестагенами; вплив початку лікування прогестагенами до зачаття і продовження під час вагітності (практика, яка вже використовується в Росії і рекомендована в національних клінічних настановах) [39]; генетичне різноманіття рецепторів прогестерону і конкретних популяцій пацієнток, які можуть отримати найбільшу користь від прийому прогестагенів під час вагітності [133,134,135]. Іншим фактором є потенційний зв’язок екзогенних прогестагенів з побічними ефектами, пов’язаними з настроєм, наприклад, тривожними та депресивними симптомами. Дослідження використання гормональної контрацепції визнали, що існує підгрупа жінок, які страждають від побічних ефектів, пов’язаних з настроєм, незважаючи на впровадження таблеток з меншою дозою та альтернативних методів введення [136,137]. Зовсім недавно використання гормональних контрацептивів було пов’язано з посиленням депресії та погіршенням розпізнавання емоцій, з припущенням, що прогестаген, який міститься в гормональних контрацептивах, викликає проблеми з настроєм [138,139]. У поєднанні з деякими даними, що вказують на зв’язок між рівнем ендогенного прогестерону і тривожністю [140], а також на роль алопрегнанолону (3-альфа-відновленого метаболіту прогестерону) у зміні настрою [139], це означає, що можуть бути підстави для занепокоєння щодо використання прогестагенів при ВВ, особливо з огляду на те, що пацієнтки і без того вразливі до підвищеного рівня тривожності і депресії. Однак дослідження етіології гормонально індукованих афективних симптомів залишаються непереконливими, і лише деякі з них можуть безпосередньо пов’язати рівень гормонів з психопатологією [137,139]; необхідно провести набагато більше досліджень, щоб визначити групи жінок, які можуть мати більший ризик виникнення афективних побічних ефектів після лікування прогестагенами. Дійсно, більш глибоке розуміння всіх цих факторів може поглибити наше розуміння механізму дії прогестагенів і допомогти оптимізувати та персоналізувати лікування майбутніх пацієнтів.
Враховуючи емоційну травму, яку багато жінок переживають після ВВ, ми також припустили, що структурована психологічна підтримка має вирішальне значення для збереження благополуччя пацієнтки, щоб запевнити її, що вона робить все можливе для підтримки вагітності, допомогти їй та її партнеру впоратися з емоційним впливом ВВ і підтримати їх під час стресового періоду очікування наступних вагітностей. Необхідні подальші дослідження для визначення найбільш ефективної форми психологічної допомоги таким пацієнткам, а також рекомендації щодо її впровадження. Оскільки ми намагаємося з’ясувати, як результати нових досліджень можуть вплинути на результати лікування, було б розумно розглянути реконцептуалізований, цілісний підхід до лікування загрозливого та рецидивуючого ВВ, щоб забезпечити оптимальний догляд та підтримку для жінок та їхніх партнерів. Хоча для підтвердження того, що комбіноване фармакологічне та психологічне лікування є більш ефективним, ніж кожен з цих підходів окремо, необхідні нові дослідження, бажано, щоб переосмислений план лікування поєднував валідований інструмент психологічної підтримки як доповнення до відповідного фармакологічного лікування. Приділяючи особливу увагу побажанням пацієнтки, цей план також повинен бути спрямований на вирішення деяких різноманітних аспектів, які можуть сприяти ВВ, таким чином, максимізуючи майбутні шанси на народження живої дитини.
Посилання на джерела
- Devall, A.J.; Papadopoulou, A.; Podesek, M.; Haas, D.M.; Price, M.J.; Coomarasamy, A.; Gallos, I.D. Progestogens for preventing miscarriage: A network meta-analysis. Cochrane Database Syst. Rev. 2021, 4, CD013792.
- Haas, D.M.; Hathaway, T.J.; Ramsey, P.S. Progestogen for preventing miscarriage in women with recurrent miscarriage of unclear etiology. Cochrane Database Syst. Rev. 2019, 2019, CD003511.
- Wahabi, H.A.; Fayed, A.A.; Esmaeil, S.A.; Bahkali, K.H. Progestogen for treating threatened miscarriage. Cochrane Database Syst. Rev. 2018, 8, CD005943.
- Zegers-Hochschild, F.; Adamson, G.D.; de Mouzon, J.; Ishihara, O.; Mansour, R.; Nygren, K.; Sullivan, E.; Vanderpoel, S.; International Committee for Monitoring Assisted Reproductive Technology (ICMART); World Health Organization (WHO). International Committee for Monitoring Assisted Reproductive Technology (ICMART) and the World Health Organization (WHO) revised glossary of ART terminology, 2009. Fertil. Steril. 2009, 92, 1520–1524.
- Schindler, A.E.; Carp, H.; Druckmann, R.; Genazzani, A.R.; Huber, J.; Pasqualini, J.; Schweppe, K.W.; Szekeres-Bartho, J. European Progestin Club Guidelines for prevention and treatment of threatened or recurrent (habitual) miscarriage with progestogens. Gynecol. Endocrinol. 2015, 31, 447–449.
- Lee, H.J.; Park, T.C.; Kim, J.H.; Norwitz, E.; Lee, B. The influence of oral dydrogesterone and vaginal progesterone on threatened abortion: A systematic review and meta-analysis. Biomed. Res. Int. 2017, 2017, 3616875.
- European Society of Human Reproduction and Embryology Early Pregnancy Guideline Development Group. Recurrent Pregnancy Loss. November 2017. Available online: https://www.eshre.eu/Guidelines-and-Legal/Guidelines/Recurrent-pregnancy-loss.aspx (accessed on 24 January 2023).
- Practice Committee of the American Society for Reproductive Medicine (ASRM). Evaluation and treatment of recurrent pregnancy loss: A committee opinion. Fertil. Steril. 2012, 98, 1103–1111.
- Bailey, S.; Boivin, J.; Cheong, Y.; Bailey, C.; Kitson-Reynolds, E.; Macklon, N. Effective support following recurrent pregnancy loss: A randomized controlled feasibility and acceptability study. Reprod. Biomed. Online 2020, 40, 729–742.
- Toth, B.; Würfel, W.; Bohlmann, M.; Zschocke, J.; Rudnik-Schöneborn, S.; Nawroth, F.; Schleussner, E.; Rogenhofer, N.; Wischmann, T.; von Wolff, M.; et al. Recurrent Miscarriage: Diagnostic and Therapeutic Procedures. Guideline of the DGGG, OEGGG and SGGG (S2k-Level, AWMF Registry Number 015/050). Geburtshilfe Frauenheilkd. 2018, 78, 364–381.
- Royal College of Obstetricians and Gynaecologists (RCOG). The Investigation and Treatment of Couples with Recurrent First-trimester and Second-Trimester Miscarriage. Green-Top Guideline No. 17. April 2011. Available online: https://www.rcog.org.uk/media/3cbgonl0/gtg_17.pdf (accessed on 24 January 2023).
- Cohain, J.S.; Buxbaum, R.E.; Mankuta, D. Spontaneous first trimester miscarriage rates per woman among parous women with 1 or more pregnancies of 24 weeks or more. BMC Pregnancy Childbirth 2017, 17, 437.
- Quenby, S.; Gallos, I.D.; Dhillon-Smith, R.K.; Podesek, M.; Stephenson, M.D.; Fisher, J.; Brosens, J.J.; Brewin, J.; Ramhorst, R.; Lucas, E.S.; et al. Miscarriage matters: The epidemiological, physical, psychological, and economic costs of early pregnancy loss. Lancet 2021, 397, 1658–1667.
- He, L.; Wang, T.; Xu, H.; Chen, C.; Liu, Z.; Kang, X.; Zhao, A. Prevalence of depression and anxiety in women with recurrent pregnancy loss and the associated risk factors. Arch. Gynecol. Obstet. 2019, 300, 1061–1066.
- Tavoli, Z.; Mohammadi, M.; Tavoli, A.; Moini, A.; Effatpanah, M.; Khedmat, L.; Montazeri, A. Quality of life and psychological distress in women with recurrent miscarriage: A comparative study. Health Qual. Life Outcomes 2018, 16, 150.
- Venema, V. ‘I Faced Miscarriage Alone—My Partner had to Wait in the Car Park’. Available online: https://www.bbc.co.uk/news/uk-53613348 (accessed on 24 January 2023).
- Kolte, A.M.; Olsen, L.R.; Mikkelsen, E.M.; Christiansen, O.B.; Nielsen, H.S. Depression and emotional stress is highly prevalent among women with recurrent pregnancy loss. Hum. Reprod. 2015, 30, 777–782.
- Csapo, A.I.; Pulkkinen, M.O.; Wiest, W.G. Effects of luteectomy and progesterone replacement therapy in early pregnant patients. Am. J. Obstet. Gynecol. 1973, 115, 759–765.
- Couzinet, B.; Le Strat, N.; Ulmann, A.; Baulieu, E.E.; Schaison, G. Termination of early pregnancy by the progesterone antagonist RU 486 (Mifepristone). N. Engl. J. Med. 1986, 315, 1565–1570.
- Silvestre, L.; Dubois, C.; Renault, M.; Rezvani, Y.; Baulieu, E.E.; Ulmann, A. Voluntary interruption of pregnancy with mifepristone (RU 486) and a prostaglandin analogue. A large-scale French experience. N. Engl. J. Med. 1990, 322, 645–648.
- Corner, G.W.; Csapo, A. Action of the ovarian hormones on uterine muscle. Br. Med. J. 1953, 1, 687–693.
- Okada, H.; Tsuzuki, T.; Murata, H. Decidualization of the human endometrium. Reprod. Med. Biol. 2018, 17, 220–227.
- Polikarpova, A.V.; Levina, I.S.; Sigai, N.V.; Zavarzin, I.V.; Morozov, I.A.; Rubtsov, P.M.; Guseva, A.A.; Smirnova, O.V.; Shchelkunova, T.A. Immunomodulatory effects of progesterone and selective ligands of membrane progesterone receptors. Steroids 2019, 145, 5–18.
- Maurya, V.K.; DeMayo, F.J.; Lydon, J.P. Illuminating the “black box” of progesterone-dependent embryo implantation using engineered mice. Front. Cell Dev. Biol. 2021, 9, 640907.
- Royal Australian and New Zealand College of Obstetricians and Gynaecologists (RANZCOG). Progesterone Support of the Luteal Phase and in the First Trimester. March 2018. Available online: https://ranzcog.edu.au/wp-content/uploads/2022/05/Progesterone-Support-of-the-Luteal-Phase-and-in-the-First-Trimester.pdf (accessed on 24 January 2023).
- National Institute for Health and Care Excellence (NICE). Ectopic Pregnancy and Miscarriage: Diagnosis and Initial Management. Guideline NG126 (Update). 24 November 2021. Available online: https://www.nice.org.uk/guidance/ng126 (accessed on 24 January 2023).
- Arab, H.; Alharbi, A.J.; Oraif, A.; Sagr, E.; Al Madani, H.; Abduljabbar, H.; Bajouh, O.S.; Faden, Y.; Sabr, Y. The role of progestogens in threatened and idiopathic recurrent miscarriage. Int. J. Womens Health 2019, 11, 589–596.
- Sinthamoney, E.; Hamdan, M.; Yan, V.H.; Bhaskaran, V.; Karalasingam, S.D.; Peraba, P.; Dass, S.G.S.; Daud, S.; Shen, V.C.B.; Aznal, S.S.S.; et al. Progestogens in the management of miscarriage and preterm labour. 12 May 2020. Available online: https://www.ogsm.org.my/docs/Clinical-Practice-Guidelines-on-Miscarriage-Management.pdf (accessed on 24 January 2023).
- Patki, A.; Pandit, S.N. FOGSI Position Statement on the Use of Progestogens. 2015. Available online: https://www.fogsi.org/wp-content/uploads/2015/11/Progesterone-position-paper-Oct-2015.pdf (accessed on 24 January 2023).
- Chinese Society of Reproductive Medicine and Chinese Medical Doctor Association. Clinical practice guidelines for progestogens in pregnancy maintenance and luteal phase support. Chin. J. Reprod. Contracep. 2021, 41, 95–105. (In Mandarin)
- Vietnam Ministry of Health. Vietnam Guideline for Obstetrics and Gynecology Disease Management. 2015. Chapter 1: Obstetrics. Threatened Miscarriage. Available online: https://thuvien.benhvienhungvuong.vn/index.php?language=vi&nv=laws&op=detail/Huong-dan-chan-doan-va-dieu-tri-cac-benh-san-phu-khoa-90 (accessed on 24 January 2023). (In Vietnamese)
- Hung Vuong Hospital. Hung Vuong Guideline of Obstetrics and Gynecology Disease Management. Miscarriage: Threatened Miscarriage; Hung Vuong Hospital: Ho Chi Minh City, Vietnam, 2016; pp. 48–53. (In Vietnamese)
- Lai, T.J.; Teng, S.W.; Chang, C.K.; Huang, C.Y. Evidence-Base Recommendation of Progesterone in Early Pregnancy. 2022. Available online: https://www.tsop.org.tw/upload/magazine/20220312150908_magazine_0.pdf (accessed on 24 January 2023). (In Taiwanese).
- Indonesian Society of Reproductive Endocrinology and Fertility (HIFERI). Indonesian National Guidelines for Health Services: Consensus of Threatened Miscarriage; HIFERI: Jakarta Pusat, Indonesia, 2015. (In Indonesian)
- CENETEC. Prevention, Diagnosis, Treatment, and Referral of Patients with Threatened Abortion in Primary and Secondary Levels of Care. Clinical Practice Guidelines: Evidence and Recommendations. Mexico. 2020. Available online: http://www.cenetec-difusion.com/CMGPC/GPC-SS-026-20/ER.pdf (accessed on 24 January 2023). (In Spanish)
- Philippine Obstetrical and Gynecological Society. Clinical Practice Guidelines on Abortion. 2017. Available online: https://pogsinc.org/clinical-practice-guidelines/ (accessed on 24 January 2023).
- Bashiri, A.; Orbito, R.; Carp, H.; Laufer, N.; Blickstein, D.; Vardimon, D.; Yaron, Y.; Solt, I.; Baris-Feldman, H.; Halevy, R.; et al. Recurrent Pregnancy Loss. Position Paper Number 215. 2021. Available online: https://ima-contentfiles.s3.amazonaws.com/Ne167_pregnencyLost.pdf (accessed on 24 January 2023).
- Indonesian Society of Reproductive Endocrinology and Fertility (HIFERI); Indonesian Society of Obstetrics and Gynecology (POGI). Consensus of Recurrent Miscarriage; HIFERI: Jakarta Pusat, Indonesia, 2018. (In Indonesian)
- Saccone, G.; Schoen, C.; Franasiak, J.M.; Scott, R.T., Jr.; Berghella, V. Supplementation with progestogens in the first trimester of pregnancy to prevent miscarriage in women with unexplained recurrent miscarriage: A systematic review and meta-analysis of randomized, controlled trials. Fertil. Steril. 2017, 107, 430–438.e433.
- Evans, R.M. The steroid and thyroid hormone receptor superfamily. Science 1988, 240, 889–895.
- Griesinger, G.; Tournaye, H.; Macklon, N.; Petraglia, F.; Arck, P.; Blockeel, C.; van Amsterdam, P.; Pexman-Fieth, C.; Fauser, B.C. Dydrogesterone: Pharmacological profile and mechanism of action as luteal phase support in assisted reproduction. Reprod. Biomed. Online 2019, 38, 249–259.
- Kuhl, H. Pharmacology of estrogens and progestogens: Influence of different routes of administration. Climacteric 2005, 8 (Suppl.. 1), 3–63.
- Stanczyk, F.Z.; Hapgood, J.P.; Winer, S.; Mishell, D.R., Jr. Progestogens used in postmenopausal hormone therapy: Differences in their pharmacological properties, intracellular actions, and clinical effects. Endocr. Rev. 2013, 34, 171–208.
- Abbott, B.V. Duphaston 10 mg Film-Coated Tablets, Summary of Product Characteristics; Abbott B.V.: Hoofddorp, The Netherlands, 2020.
- Besins Healthcare Ltd. Utrogestan Vaginal 200mg Capsules; Summary of Product Characteristics; Besins Healthcare (UK) Ltd.: London, UK, 2020.
- Sator, M.; Radicioni, M.; Cometti, B.; Loprete, L.; Leuratti, C.; Schmidl, D.; Garhofer, G. Pharmacokinetics and safety profile of a novel progesterone aqueous formulation administered by the s.c. route. Gynecol. Endocrinol. 2013, 29, 205–208.
- Vaisbuch, E.; Leong, M.; Shoham, Z. Progesterone support in IVF: Is evidence-based medicine translated to clinical practice? A worldwide web-based survey. Reprod. Biomed. Online 2012, 25, 139–145.
- Oler, E.; Eke, A.C.; Hesson, A. Meta-analysis of randomized controlled trials comparing 17alpha-hydroxyprogesterone caproate and vaginal progesterone for the prevention of recurrent spontaneous preterm delivery. Int. J. Gynaecol. Obstet. 2017, 138, 12–16.
- Saccone, G.; Khalifeh, A.; Elimian, A.; Bahrami, E.; Chaman-Ara, K.; Bahrami, M.A.; Berghella, V. Vaginal progesterone vs intramuscular 17alpha-hydroxyprogesterone caproate for prevention of recurrent spontaneous preterm birth in singleton gestations: Systematic review and meta-analysis of randomized controlled trials. Ultrasound Obstet. Gynecol. 2017, 49, 315–321.
- Wang, X.X.; Luo, Q.; Bai, W.P. Efficacy of progesterone on threatened miscarriage: Difference in drug types. J. Obstet. Gynaecol. Res. 2019, 45, 794–802.
- Li, L.; Zhang, Y.; Tan, H.; Bai, Y.; Fang, F.; Faramand, A.; Chong, W.; Hai, Y. Effect of progestogen for women with threatened miscarriage: A systematic review and meta-analysis. BJOG 2020, 127, 1055–1063.
- Devall, A.J.; Gallos, I.D.; Khalaf, Y.; Mol, B.W.; Ross, J.; Shennan, A.; Horne, A.W.; Small, R.; Goddijn, M.; van Wely, M.; et al. Re: Effect of progestogen for women with threatened miscarriage: A systematic review and meta-analysis. BJOG 2020, 127, 1303–1304.
- Li, L.; Zhang, Y.; Fang, F. Authors’ reply re: Effect of progestogen for women with threatened miscarriage: A systematic review and meta-analysis. BJOG 2020, 127, 1304.
- Zhao, H.; He, W.; Yang, Z. A pairwise and network meta-analysis comparing the efficacy and safety of progestogens in threatened abortion. Int. J. Gynaecol. Obstet. 2022, 156, 383–393.
- Coomarasamy, A.; Williams, H.; Truchanowicz, E.; Seed, P.T.; Small, R.; Quenby, S.; Gupta, P.; Dawood, F.; Koot, Y.E.; Bender Atik, R.; et al. A randomized trial of progesterone in women with recurrent miscarriages. N. Engl. J. Med. 2015, 373, 2141–2148.
- Coomarasamy, A.; Devall, A.J.; Cheed, V.; Harb, H.; Middleton, L.J.; Gallos, I.D.; Williams, H.; Eapen, A.K.; Roberts, T.; Ogwulu, C.C.; et al. A randomized trial of progesterone in women with bleeding in early pregnancy. N. Engl. J. Med. 2019, 380, 1815–1824.
- Coomarasamy, A.; Harb, H.M.; Devall, A.J.; Cheed, V.; Roberts, T.E.; Goranitis, I.; Ogwulu, C.B.; Williams, H.M.; Gallos, I.D.; Eapen, A.; et al. Progesterone to prevent miscarriage in women with early pregnancy bleeding: The PRISM RCT. Health Technol. Assess. 2020, 24, 1–70.
- Rasmark Roepke, E.; Hellgren, M.; Hjertberg, R.; Blomqvist, L.; Matthiesen, L.; Henic, E.; Lalitkumar, S.; Strandell, A. Treatment efficacy for idiopathic recurrent pregnancy loss—A systematic review and meta-analyses. Acta Obstet. Gynecol. Scand. 2018, 97, 921–941.
- Kumar, A.; Begum, N.; Prasad, S.; Aggarwal, S.; Sharma, S. Oral dydrogesterone treatment during early pregnancy to prevent recurrent pregnancy loss and its role in modulation of cytokine production: A double-blind, randomized, parallel, placebo-controlled trial. Fertil. Steril. 2014, 102, 1357–1363.e1353.
- Paulson, R.J.; Collins, M.G.; Yankov, V.I. Progesterone pharmacokinetics and pharmacodynamics with 3 dosages and 2 regimens of an effervescent micronized progesterone vaginal insert. J. Clin. Endocrinol. Metab. 2014, 99, 4241–4249.
- Mirza, F.G.; Patki, A.; Pexman-Fieth, C. Dydrogesterone use in early pregnancy. Gynecol. Endocrinol. 2016, 32, 97–106.
- Di Renzo, G.C.; Tosto, V.; Tsibizova, V.; Fonseca, E. Prevention of preterm birth with progesterone. J. Clin. Med. 2021, 10, 4511.
- Chakravarty, B.N.; Shirazee, H.H.; Dam, P.; Goswami, S.K.; Chatterjee, R.; Ghosh, S. Oral dydrogesterone versus intravaginal micronised progesterone as luteal phase support in assisted reproductive technology (ART) cycles: Results of a randomised study. J. Steroid Biochem. Mol. Biol. 2005, 97, 416–420.
- Carp, H. A systematic review of dydrogesterone for the treatment of threatened miscarriage. Gynecol. Endocrinol. 2012, 28, 983–990.
- Tomic, V.; Tomic, J.; Klaic, D.Z.; Kasum, M.; Kuna, K. Oral dydrogesterone versus vaginal progesterone gel in the luteal phase support: Randomized controlled trial. Eur. J. Obstet. Gynecol. Reprod. Biol. 2015, 186, 49–53.
- Ashok, P.W.; Hamoda, H.; Nathani, F.; Flett, G.M.; Templeton, A. Randomised controlled study comparing oral and vaginal misoprostol for cervical priming prior to surgical termination of pregnancy. BJOG 2003, 110, 1057–1061.
- Arvidsson, C.; Hellborg, M.; Gemzell-Danielsson, K. Preference and acceptability of oral versus vaginal administration of misoprostol in medical abortion with mifepristone. Eur. J. Obstet. Gynecol. Reprod. Biol. 2005, 123, 87–91.
- Saxena, P.; Sarda, N.; Salhan, S.; Nandan, D. A randomised comparison between sublingual, oral and vaginal route of misoprostol for pre-abortion cervical ripening in first-trimester pregnancy termination under local anaesthesia. Aust. N. Z. J. Obstet. Gynaecol. 2008, 48, 101–106.
- Song, T.; Kim, M.K.; Kim, M.L.; Jung, Y.W.; Yoon, B.S.; Seong, S.J. Effectiveness of different routes of misoprostol administration before operative hysteroscopy: A randomized, controlled trial. Fertil. Steril. 2014, 102, 519–524.
- Schindler, A.E. Progestational effects of dydrogesterone in vitro, in vivo and on the human endometrium. Maturitas 2009, 65 (Suppl.. 1), S3–S11.
- Ott, J.; Egarter, C.; Aguilera, A. Dydrogesterone after 60 years: A glance at the safety profile. Gynecol. Endocrinol. 2022, 38, 279–287.
- MacDonald, R.R.; Goulden, R.; Oakey, R.E. Cervical mucus, vaginal cytology and steroid excretion in recurrent abortion. Obstet. Gynecol. 1972, 40, 394–402.
- Omar, M.H.; Mashita, M.K.; Lim, P.S.; Jamil, M.A. Dydrogesterone in threatened abortion: Pregnancy outcome. J. Steroid Biochem. Mol. Biol. 2005, 97, 421–425.
- El-Zibdeh, M.Y.; Yousef, L.T. Dydrogesterone support in threatened miscarriage. Maturitas 2009, 65 (Suppl.. 1), S43–S46.
- Pandian, R.U. Dydrogesterone in threatened miscarriage: A Malaysian experience. Maturitas 2009, 65 (Suppl. 1), S47–S50.
- Siew, J.Y.S.; Allen, J.C.; Hui, C.Y.Y.; Ku, C.W.; Malhotra, R.; Ostbye, T.; Tan, T.C. The randomised controlled trial of micronised progesterone and dydrogesterone (TRoMaD) for threatened miscarriage. Eur. J. Obstet. Gynecol. Reprod. Biol. 2018, 228, 319–324.
- Chan, D.M.K.; Cheung, K.W.; Ko, J.K.Y.; Yung, S.S.F.; Lai, S.F.; Lam, M.T.; Ng, D.Y.T.; Lee, V.C.Y.; Li, R.H.W.; Ng, E.H.Y. Use of oral progestogen in women with threatened miscarriage in the first trimester: A randomized double-blind controlled trial. Hum. Reprod. 2021, 36, 587–595.
- El-Zibdeh, M.Y. Dydrogesterone in the reduction of recurrent spontaneous abortion. J. Steroid Biochem. Mol. Biol. 2005, 97, 431–434.
- Carp, H. A systematic review of dydrogesterone for the treatment of recurrent miscarriage. Gynecol. Endocrinol. 2015, 31, 422–430.
- Kale, A.R.; Kale, A.A.; Yelikar, K. A comparative, randomized control trial in patients of per vaginal bleeding comparing efficacy of oral dydrogesterone versus vaginal progesterone in successful pregnancy outcome for patients with recurrent pregnancy loss. J. Obstet. Gynaecol. India 2021, 71, 591–595.
- Griesinger, G.; Blockeel, C.; Tournaye, H. Oral dydrogesterone for luteal phase support in fresh in vitro fertilization cycles: A new standard? Fertil. Steril. 2018, 109, 756–762.
- Podzolkova, N.; Tatarchuk, T.; Doshchanova, A.; Eshimbetova, G.; Pexman-Fieth, C. Dydrogesterone treatment for menstrual-cycle regularization in routine clinical practice: A multicenter observational study. Gynecol. Endocrinol. 2016, 32, 246–249.
- Queisser-Luft, A. Dydrogesterone use during pregnancy: Overview of birth defects reported since 1977. Early Hum. Dev. 2009, 85, 375–377.
- Katalinic, A.; Shulman, L.P.; Strauss, J.F.; Garcia-Velasco, J.A.; Anker, J. A critical appraisal of safety data on dydrogesterone for the support of early pregnancy: A scoping review and meta-analysis. Reprod. Biomed. Online, 2022; online ahead of print.
- Tournaye, H.; Sukhikh, G.T.; Kahler, E.; Griesinger, G. A Phase III randomized controlled trial comparing the efficacy, safety and tolerability of oral dydrogesterone versus micronized vaginal progesterone for luteal support in in vitro fertilization. Hum. Reprod. 2017, 32, 2152.
- Griesinger, G.; Blockeel, C.; Sukhikh, G.T.; Patki, A.; Dhorepatil, B.; Yang, D.Z.; Chen, Z.J.; Kahler, E.; Pexman-Fieth, C.; Tournaye, H. Oral dydrogesterone versus intravaginal micronized progesterone gel for luteal phase support in IVF: A randomized clinical trial. Hum. Reprod. 2018, 33, 2212–2221.
- Griesinger, G.; Blockeel, C.; Kahler, E.; Pexman-Fieth, C.; Olofsson, J.I.; Driessen, S.; Tournaye, H. Dydrogesterone as an oral alternative to vaginal progesterone for IVF luteal phase support: A systematic review and individual participant data meta-analysis. PLoS ONE 2020, 15, e0241044.
- Atzmon, Y.; Aslih, N.; Estrada, D.; Bilgory, A.; Ellenbogen, A.; Shalom-Paz, E. Comparable outcomes using oral dydrogesterone vs. micronized vaginal progesterone in frozen embryo transfer: A retrospective cohort study. Reprod. Sci. 2021, 28, 1874–1881.
- Yang, D.Z.; Griesinger, G.; Wang, W.; Gong, F.; Liang, X.; Zhang, H.; Sun, Y.; Kahler, E.; Pexman-Fieth, C.; Olofsson, J.I.; et al. A Phase III randomized controlled trial of oral dydrogesterone versus intravaginal progesterone gel for luteal phase support in in vitro fertilization (Lotus II): Results from the Chinese mainland subpopulation. Gynecol. Endocrinol. 2020, 36, 175–183.
- Huang, J.; Xie, Q.; Lin, J.; Lu, X.; Wang, N.; Gao, H.; Cai, R.; Kuang, Y. Neonatal outcomes and congenital malformations in children born after dydrogesterone application in progestin-primed ovarian stimulation protocol for IVF: A retrospective cohort study. Drug Des. Devel. Ther. 2019, 13, 2553–2563. [Google Scholar] [CrossRef] [PubMed][Green Version]
- Zaqout, M.; Aslem, E.; Abuqamar, M.; Abughazza, O.; Panzer, J.; De Wolf, D. The impact of oral intake of dydrogesterone on fetal heart development during early pregnancy. Pediatr. Cardiol. 2015, 36, 1483–1488.
- Koren, G.; Gilboa, D.; Katz, R. Expression of concern to: Fetal safety of dydrogesterone exposure in the first trimester of pregnancy. Clin. Drug Investig. 2020, 40, 681.
- Medicines and Healthcare Products Regulatory Agency (MHRA). Efficacy of Progestogens in the Maintenance of Early Pregnancy in Women with Threatened Miscarriage or Recurrent Miscarriage. February 2008. Available online: https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/852391/Efficacy_of_progestogens_in_the_maintenance_of_early_pregnancy_in_women_with_threatened_miscarriage_or_recurrent_miscarriage.pdf (accessed on 24 January 2023).
- Williamson, S.P.; Moffitt, R.L.; Broadbent, J.; Neumann, D.L.; Hamblin, P.S. Coping, wellbeing, and psychopathology during high-risk pregnancy: A systematic review. Midwifery 2023, 116, 103556.
- Isaacs, N.Z.; Andipatin, M.G. A systematic review regarding women’s emotional and psychological experiences of high-risk pregnancies. BMC Psychol. 2020, 8, 45.
- Yu, X.; Liu, Y.; Huang, Y.; Zeng, T. The effect of nonpharmacological interventions on the mental health of high-risk pregnant women: A systematic review. Complement. Ther. Med. 2022, 64, 102799.
- Dawes, L.; Waugh, J.J.S.; Lee, A.; Groom, K.M. Psychological well-being of women at high risk of spontaneous preterm birth cared for in a specialised preterm birth clinic: A prospective longitudinal cohort study. BMJ Open 2022, 12, e056999.
- Aliabadi, S.; Shayan, A.; Refaei, M.; Tapak, L.; Moradveisi, L. The effect of individual counseling based on the GATHER principles on perceived stress and empowerment of the mothers with high-risk pregnancies: An experimental study. BMC Psychiatry 2022, 22, 396.
- Mevorach-Zussman, N.; Bolotin, A.; Shalev, H.; Bilenko, N.; Mazor, M.; Bashiri, A. Anxiety and deterioration of quality of life factors associated with recurrent miscarriage in an observational study. J. Perinat. Med. 2012, 40, 495–501.
- Lachmi-Epstein, A.; Mazor, M.; Bashiri, A. Psychological and mental aspects and “tender loving care” among women with recurrent pregnancy losses. Harefuah 2012, 151, 633–637, 654.
- Neugebauer, R. Depressive symptoms at two months after miscarriage: Interpreting study findings from an epidemiological versus clinical perspective. Depress. Anxiety 2003, 17, 152–161.
- Bailey, S.L.; Boivin, J.; Cheong, Y.C.; Kitson-Reynolds, E.; Bailey, C.; Macklon, N. Hope for the best …but expect the worst: A qualitative study to explore how women with recurrent miscarriage experience the early waiting period of a new pregnancy. BMJ Open 2019, 9, e029354.
- Ockhuijsen, H.D.; Boivin, J.; van den Hoogen, A.; Macklon, N.S. Coping after recurrent miscarriage: Uncertainty and bracing for the worst. J. Fam. Plann. Reprod. Health Care 2013, 39, 250–256.
- Bailey, S.; Bailey, C.; Boivin, J.; Cheong, Y.; Reading, I.; Macklon, N. A feasibility study for a randomised controlled trial of the Positive Reappraisal Coping Intervention, a novel supportive technique for recurrent miscarriage. BMJ Open 2015, 5, e007322.
- Dimitriadis, E.; Menkhorst, E.; Saito, S.; Kutteh, W.H.; Brosens, J.J. Recurrent pregnancy loss. Nat. Rev. Dis. Primers 2020, 6, 98.
- Chichester, M.; Harding, K.M. Early pregnancy loss: Invisible but real. Nursing 2021, 51, 28–32.
- Yang, J.; Dowell, A.; Filoche, S. Views of health professionals on the impact of early miscarriage on women’s mental health and the accessibility of services and support. N. Z. Med. J. 2022, 135, 54–64.
- Fenster, L.; Schaefer, C.; Mathur, A.; Hiatt, R.A.; Pieper, C.; Hubbard, A.E.; Von Behren, J.; Swan, S.H. Psychologic stress in the workplace and spontaneous abortion. Am. J. Epidemiol. 1995, 142, 1176–1183.
- Arck, P.C.; Rücke, M.; Rose, M.; Szekeres-Bartho, J.; Douglas, A.J.; Pritsch, M.; Blois, S.M.; Pincus, M.K.; Bärenstrauch, N.; Dudenhausen, J.W.; et al. Early risk factors for miscarriage: A prospective cohort study in pregnant women. Reprod. Biomed. Online 2008, 17, 101–113.
- Qu, F.; Wu, Y.; Zhu, Y.H.; Barry, J.; Ding, T.; Baio, G.; Muscat, R.; Todd, B.K.; Wang, F.F.; Hardiman, P.J. The association between psychological stress and miscarriage: A systematic review and meta-analysis. Sci. Rep. 2017, 7, 1731.
- San Lazaro Campillo, I.; Meaney, S.; Corcoran, P.; Spillane, N.; O’Donoghue, K. Risk factors for miscarriage among women attending an early pregnancy assessment unit (EPAU): A prospective cohort study. Ir. J. Med. Sci. 2019, 188, 903–912.
- Murphy, F.A.; Lipp, A.; Powles, D.L. Follow-up for improving psychological well being for women after a miscarriage. Cochrane Database Syst. Rev. 2012, 3, CD008679.
- van den Berg, M.M.J.; Dancet, E.A.F.; Erlikh, T.; van der Veen, F.; Goddijn, M.; Hajenius, P.J. Patient-centered early pregnancy care: A systematic review of quantitative and qualitative studies on the perspectives of women and their partners. Hum. Reprod. Update 2018, 24, 106–118
- Koert, E.; Malling, G.M.H.; Sylvest, R.; Krog, M.C.; Kolte, A.M.; Schmidt, L.; Nielsen, H.S. Recurrent pregnancy loss: Couples’ perspectives on their need for treatment, support and follow up. Hum. Reprod. 2019, 34, 291–296.
- Voss, P.; Schick, M.; Langer, L.; Ainsworth, A.; Ditzen, B.; Strowitzki, T.; Wischmann, T.; Kuon, R.J. Recurrent pregnancy loss: A shared stressor—couple-orientated psychological research findings. Fertil. Steril. 2020, 114, 1288–1296.
- Riggs, D.W.; Due, C.; Tape, N. Australian heterosexual men’s experiences of pregnancy loss: The relationships between grief, psychological distress, stigma, help-seeking, and support. Omega 2021, 82, 409–423.
- Harty, T.; Trench, M.; Keegan, O.; O’Donoghue, K.; Nuzum, D. The experiences of men following recurrent miscarriage in an Irish tertiary hospital: A qualitative analysis. Health Expect. 2022, 25, 1048–1057.
- Miller, E.J.; Temple-Smith, M.J.; Bilardi, J.E. ‘There was just no-one there to acknowledge that it happened to me as well’: A qualitative study of male partner’s experience of miscarriage. PLoS ONE 2019, 14, e0217395.
- Obst, K.L.; Due, C.; Oxlad, M.; Middleton, P. Men’s grief following pregnancy loss and neonatal loss: A systematic review and emerging theoretical model. BMC Pregnancy Childbirth 2020, 20, 11.
- Nakano, Y.; Akechi, T.; Furukawa, T.A.; Sugiura-Ogasawara, M. Cognitive behavior therapy for psychological distress in patients with recurrent miscarriage. Psychol. Res. Behav. Manag. 2013, 6, 37–43.
- Patel, A.; Dinesh, N.; Sharma, P.S.V.N.; Kumar, P.; Binu, V.S. Outcomes of structured psychotherapy for emotional adjustment in a childless couple diagnosed with recurrent pregnancy loss: A unique investigation. J. Hum. Reprod. Sci. 2018, 11, 202–207.
- Jensen, K.H.K.; Krog, M.C.; Koert, E.; Hedegaard, S.; Chonovitsch, M.; Schmidt, L.; Kolte, A.M.; Nielsen, H.S. Meditation and mindfulness reduce perceived stress in women with recurrent pregnancy loss: A randomized controlled trial. Reprod. Biomed. Online 2021, 43, 246–256.
- Elsharkawy, N.B.; Mohamed, S.M.; Awad, M.H.; Ouda, M.M.A. Effect of happiness counseling on depression, anxiety, and stress in women with recurrent miscarriage. Int. J. Womens Health 2021, 13, 287–295.
- Green, D.M.; O’Donoghue, K. A review of reproductive outcomes of women with two consecutive miscarriages and no living child. J. Obstet. Gynaecol. 2019, 39, 816–821
- Yu, A.Y.; Temple-Smith, M.J.; Bilardi, J.E. Health care support following miscarriage in Australia: A qualitative study. How can we do better? Aust. J. Prim. Health 2022, 28, 172–178.
- Kuon, R.J.; Togawa, R.; Vomstein, K.; Weber, M.; Goeggl, T.; Strowitzki, T.; Markert, U.R.; Zimmermann, S.; Daniel, V.; Dalpke, A.H.; et al. Higher prevalence of colonization with Gardnerella vaginalis and gram-negative anaerobes in patients with recurrent miscarriage and elevated peripheral natural killer cells. J. Reprod. Immunol. 2017, 120, 15–19.
- Sirota, I.; Zarek, S.M.; Segars, J.H. Potential influence of the microbiome on infertility and assisted reproductive technology. Semin. Reprod. Med. 2014, 32, 35–42.
- Zhang, F.; Zhang, T.; Ma, Y.; Huang, Z.; He, Y.; Pan, H.; Fang, M.; Ding, H. Alteration of vaginal microbiota in patients with unexplained recurrent miscarriage. Exp. Ther. Med. 2019, 17, 3307–3316.
- Kuroda, K.; Ikemoto, Y.; Horikawa, T.; Moriyama, A.; Ojiro, Y.; Takamizawa, S.; Uchida, T.; Nojiri, S.; Nakagawa, K.; Sugiyama, R. Novel approaches to the management of recurrent pregnancy loss: The OPTIMUM (OPtimization of Thyroid function, Thrombophilia, Immunity, and Uterine Milieu) treatment strategy. Reprod. Med. Biol. 2021, 20, 524–536.
- Li, J.; Hong, X.; Mesiano, S.; Muglia, L.J.; Wang, X.; Snyder, M.; Stevenson, D.K.; Shaw, G.M. Natural selection has differentiated the progesterone receptor among human populations. Am. J. Hum. Genet. 2018, 103, 45–57.
- Zeberg, H.; Kelso, J.; Pääbo, S. The neandertal progesterone receptor. Mol. Biol. Evol. 2020, 37, 2655–2660.
- Bahia, W.; Finan, R.R.; Al-Mutawa, M.; Haddad, A.; Soua, A.; Janhani, F.; Mahjoub, T.; Almawi, W.Y. Genetic variation in the progesterone receptor gene and susceptibility to recurrent pregnancy loss: A case-control study. BJOG 2018, 125, 729–735.
- Lewis, C.A.; Kimmig, A.S.; Zsido, R.G.; Jank, A.; Derntl, B.; Sacher, J. Effects of hormonal contraceptives on mood: A focus on emotion recognition and reactivity, reward processing, and stress response. Curr. Psychiatry Rep. 2019, 21, 115.
- Standeven, L.R.; McEvoy, K.O.; Osborne, L.M. Progesterone, reproduction, and psychiatric illness. Best Pract. Res. Clin. Obstet. Gynaecol. 2020, 69, 108–126.
- Shirazi, T.N.; Rosenfield, K.A.; Cardenas, R.A.; Breedlove, S.M.; Puts, D.A. No evidence that hormonal contraceptive use or circulating sex steroids predict complex emotion recognition. Horm. Behav. 2020, 119, 104647.
- Sundstrom-Poromaa, I.; Comasco, E.; Sumner, R.; Luders, E. Progesterone—Friend or foe? Front. Neuroendocrinol. 2020, 59, 100856.
- Reynolds, T.A.; Makhanova, A.; Marcinkowska, U.M.; Jasienska, G.; McNulty, J.K.; Eckel, L.A.; Nikonova, L.; Maner, J.K. Progesterone and women’s anxiety across the menstrual cycle. Horm. Behav. 2018, 102, 34–40.
- McEvoy, K.; Osborne, L.M. Allopregnanolone and reproductive psychiatry: An overview. Int. Rev. Psychiatry 2019, 31, 237–244.