🤖 Короткий переказ від ШІ
Дослідження порівнює гістеросальпінго-контрастну сонографію (ГСКС) з гістеросальпінгографією (ГСГ) як методи оцінки прохідності маткових труб. Результати показали, що ГСКС є більш безпечним, ефективним та економічним методом, який корелює з кращою функцією яєчників та вищою частотою настання вагітності.
ГСКС продемонструвала нижчий індекс резистентності (ІР) та більшу товщину ендометрію порівняно з ГСГ, що є важливими показниками для фертильності. Загальна частота настання вагітності у групі ГСКС становила 68.8%, тоді як у групі ГСГ – 25%. Ось посилання: УЗД апарати
✅ Ключові тези зі статті:
- Діагностика: ГСКС є безпечнішим, простішим та дешевшим методом оцінки прохідності маткових труб порівняно з ГСГ.
- Лікування: ГСКС асоціюється з покращенням оваріального кровотоку, ендометріального кровотоку та вищою частотою зачаття.
- Переваги: ГСКС показала нижчий ІР та більшу товщину ендометрію, що може позитивно впливати на результати фертильності.
- Обмеження: Хоча обидва методи ефективні, ГСГ може мати незначний вплив на оваріальний кровотік; однак, клінічне значення цього потребує подальших досліджень.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Резюме
Мета: Дослідити гістеросальпінго-контрастну сонографію (ГСКС) як безпечний, ефективний, простий і дешевший метод вимірювання прохідності маткових труб, ніж гістеросальпінгографія (ГСГ), а також кореляцію між покращенням функції яєчників, ендометріального та яєчникового кровотоку і частотою зачаття у безплідних жінок.
Методологія: У цьому перехресному дослідженні взяли участь 40 безплідних жінок віком від 22 до 42 років; 20 з них проводили ГСГ на 6-й або 7-й день циклу, а 20 – ГСКС зі звичайним фізіологічним розчином і 100 мг гідрокортизону. Усім було проведено процедуру ФСК з препаратом IU Gnonal 75 за протоколом на 2-й і 3-й дні, з кломіфеном 50 мг двічі на день з 2-го по 7-й день або летризолом 2,5 двічі на день з 3-го по 8-й день (приблизно на 14-й день). Критерії оцінки: індекс резистентності (ІР) та індекс перфузії (ІП) судин яєчників за даними допплерометрії, кількість та розмір фолікулів по групах, товщина ендометрію, малюнок ендометрію, зони кровотоку до ендометрію. Потім HCG для стимуляції овуляції та прогестерон для підтримки лютеїнової фази.
Результати: Середній вік групи ГСГ становив 29,7 років 6 Вік групи ГСКС становив 29,6 років. 82,1% жінок, які отримували ГСГ, і 90,1% жінок, які отримували ГСКС, мали 2-е безпліддя. У 42,9% жінок, які проходили ГСГ, була І зона і у 65,6% – IV зона. Жінки, які отримували ГСГ та ГСКС, мали 1 фолікул відповідно. 68,8% жінок, які проходили ГСГ, завагітніли. ГСГ і ГСКС мали різний ІР, товщину. ГСКС мав більшу товщину і менший ІР, ніж ГСГ. ГСГ і ГСКС показали однакову кількість і розміри фолікулів.
Висновок: ГСКС виявився безпечнішим, ефективнішим, простішим і дешевшим способом оцінки прохідності маткових труб, ніж ГСГ, з меншим ІР і більшою товщиною ендометрію.
Ключові слова: Прохідність труб, оваріальний кровотік, функція, гістеросальпінгографія, ГСКС.
Вступ
Поширеною гінекологічною проблемою є безпричинна кровотеча з матки. Такі проблеми можуть бути викликані чимось нешкідливим, наприклад, матковою кровотечею, яка не працює належним чином, або чимось серйознішим, наприклад, серйозним основним захворюванням. Найчастіше причиною аномальних кровотеч є поліпи ендометрію, лейоміома матки, гіперплазія ендометрію або рак ендометрію. Коли кровотеча не є нормальною, поліпи ендометрію виявляються в матці в 10-30% випадків.1,2
На сьогоднішній день найпоширенішим типом пухлини органів малого тазу у жінок є лейоміома матки. Коли субмукозна міома росте в напрямку до ендометрію, вона викликає випинання в порожнині ендометрію. Здебільшого, щоб з’ясувати, чому у жінки аномальна кровотеча, використовують ТВУЗД, СІФ, Г/С, біопсію ендометрію та дилятацію і вишкрібання (Д/В).3 Соногістерографія, яку також називають сонограмою з інфузією фізіологічного розчину, щоб не робити гістерограму, при якій рідина вводиться трансцервікально в порожнину матки, щоб легше було побачити ендометрій під час трансвагінального ультразвукового дослідження.4,5 Цей метод полегшує діагностику проблем з ендометрієм, таких як поліпи, гіперплазія, рак, лейоміоми та спайки, за допомогою сонографії.
Процес визначення того, які жінки потребують лікування перед операцією, можна покращити, а деяким пацієнткам може не знадобитися так багато інвазивних діагностичних тестів. Це можна зробити швидко і дешево, і це рідко викликає якісь проблеми. Американський коледж акушерів-гінекологів (ACOG), Американський коледж радіології та Американський інститут ультразвуку в медицині спільно працювали над документом з оцінки технології соногістерографії з інфузією фізіологічного розчину.6,7 У випадку гістеросальпінгографії (ГСГ) було багато розмов про те, чи впливає тип контрастної речовини, що використовується, на здатність жінки завагітніти в майбутньому, навіть якщо вона не отримує ніяких інших методів лікування.
Коли йдеться про те, наскільки здорові репродуктивні органи жінки,8,9 ГСГ є стандартом лікування і найбільш економічно ефективним вибором. Більшість людей вважає, що Ріндфлейш був першою людиною, яка застосувала інтервенційну радіологію, коли в 1910 році вперше ввів розчин вісмуту в порожнину матки. Основною клінічною причиною для проведення ГСГ є безпліддя, з повторною втратою або без неї. ГСГ може виявити ряд проблем з маткою, таких як вроджені вади розвитку, синехії, лейоміоми, поліпи та аденоміоз. За допомогою цього методу можна виявити ряд проблем з трубами, таких як сальпінгіт, оклюзія труб, гідросальпінкс і перитубарний спайковий процес. Якщо ГСГ виконано правильно, за його допомогою можна визначити форму порожнини матки та розмір цервікального каналу.10,11
За допомогою додаткової ін’єкції досліджують рогову оболонку, перешийок і ампулу труби, щоб побачити, скільки часу минуло з моменту витоку.12 Якщо ГСГ показує, що порожнина матки в нормі, інші методи візуалізації, такі як трансабдомінальне, ендовагінальне та гістерографічне ультразвукове дослідження (УЗД), а також магнітно-резонансна томографія (МРТ), з меншою ймовірністю виявлять проблеми. Ми вважаємо, що це перше дослідження такого роду в нашій області, яке вивчає вплив ГЗГ на кількість пологів.13 Це дослідження мало на меті оцінити ГКС як безпечний, ефективний, простий і дешевший спосіб оцінки прохідності маткових труб, ніж ГЗГ, і встановити кореляцію між кращою сприйнятливістю ендометрію, нижчим RI і вищою перфузією яєчників та кращою функцією яєчників, а також поліпшенням кровотоку в ендометрії і яєчниках у безплідних жінок з точки зору частоти настання вагітності.
Методологія
У цьому перехресному дослідженні взяли участь 40 безплідних жінок у віці від 22 до 42 років, які страждали на первинне або вторинне безпліддя від одного до 14 років. Критерії включення вимагали, щоб учасниці були безплідними жінками у віці від 22 до 42 років, мали прохідні маткові труби, здорову матку (без набутих або вроджених аномалій) і здоровий ендометрій. Критерії виключення передбачали запальні захворювання органів малого тазу, ендокринні розлади, такі як діабет, гіперпролактинемія або захворювання щитовидної залози, здорові яєчники (без кіст, без полікістозу яєчників і не оперовані раніше з будь-якої причини), відсутність впливу хіміотерапії або опромінення, а також ІМТ не вище 30. Також виключалися нездорові яєчники, в тому числі з кістами або ті, що були раніше прооперовані. Усі повнолітні учасники та їхні законні опікуни або батьки дали усну згоду на участь у дослідженні. Протокол та форма згоди були затверджені локальним етичним комітетом [Документ 177 (7/7/2022)].
З 40 пацієнток 20 пройшли процедуру ГСГ, а іншим 20 – процедуру ГСКС на 6-й або 7-й день циклу із застосуванням фізіологічного розчину та 100 мг гідрокортизону. Всі пацієнтки проходили протокол, який включав 75 IU of Gonal F підшкірно на 2-й і 3-й дні, а також Кломіфен 50 мг двічі на день з 2-го по 7-й день або Летризол 2,5 двічі на день з 3-го по 8-й день в середині циклу (приблизно на 14-й день). ІР та ІП судин яєчників оцінювали за допомогою допплерівського ультразвуку, кількість та розмір фолікулів для групи, товщину ендометрію, малюнок ендометрію та зони кровотоку до ендометрію. Потім усім пацієнткам призначали ХГЛ для запуску овуляції та прогестерон для підтримки лютеїнової фази. Барвник, що використовувався при ГСГ, був контрастним засобом на масляній основі. Ми оцінювали ІР і ІП в різні фази циклу, включаючи лютеїнову фазу після середини циклу, день зрілих фолікулів (між 12 і 18 днем наступного циклу), деякі з загальним і деякі з Прегнілом, але всі параметри оцінювалися до тригера, а не після нього.
Таблиця 1: Зона, кількість фолікулів і тест на вагітність в обох групах.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Статистичний аналіз: Для категоріальних даних використовували SPSS версії 22, для неперервних даних – частоту та відсоток, а для категоріальних – середнє, медіану та стандартне відхилення. Для оцінки зв’язку між змінними використовували критерій хі-квадрат, а для оцінки відмінностей між середнім і медіаною безперервних змінних – T-тести. Значущим вважалося значення p, менше або рівне 0,05.
Результати
Середній вік жінок у групі ГСГ становив 29,7 ± 6 років, а в групі ГСКС – 29 ± 6 років. 82,1% жінок, які проходили процедуру ГСГ, мали 2-е безпліддя, тоді як 90,1% жінок, які проходили процедуру ГСКС, мали 2-е безпліддя. 42,9% жінок, які пройшли ГСГ, мали І зону, тоді як 65,6% жінок, які пройшли ГСКС, мали IV зону. 82,1% і 90,6% жінок, які пройшли процедуру ГСГ і ГСКС, мали 1 фолікул відповідно. 68,8% жінок, які застосовували ГСКС, мали позитивні результати тестів на вагітність (Таблиця 1). Як показано в Таблиці 2, між ГСГ і ГСКС була значна різниця за показниками ІР, товщини. ГСКС мали менший ІР та більшу товщину, ніж ГСГ. У той час як за кількістю та розміром фолікулів достовірної різниці між ГСГ та ГСКС не виявлено.
Як видно з таблиці 3, 75,9% жінок з позитивним тестом на вагітність проходили процедуру ГСКС порівняно з жінками, які проходили процедуру ГСГ, 24,1% з достовірним зв’язком. 84% жінок з IV зоною при застосуванні ГСКС зі значущим зв’язком. Не виявлено значущого зв’язку між анамнезом безпліддя, кількістю фолікулів та процедурою ГСГ і ГСКС.
Таблиця 2: Відмінності між ГСГ та ГСКС за показниками ІР, товщини, кількості та розміру фолікулів, а також їх розмірів.
| Змінна | Тип | N | Середнє | СВ | P-value |
| ІР | ГСГ | 28 | 0.79 | 0.04 | 0.003 |
| ГСКС | 32 | 0.75 | 0.03 | ||
| Товщина | ГСГ | 28 | 8.07 | 1.08 | 0.005 |
| (мм) | ГСКС | 32 | 8.90 | 1.14 | |
| Фолікули | ГСГ | 28 | 0.82 | 0.39 | 0.3 |
| ГСКС | 32 | 0.91 | 0.29 | ||
| Розмір | ГСГ | 28 | 14.78 | 7.27 | 0.1 |
| ГСКС | 32 | 17.40 | 4.81 |
p ≤ 0.05 (значущий)
Обговорення
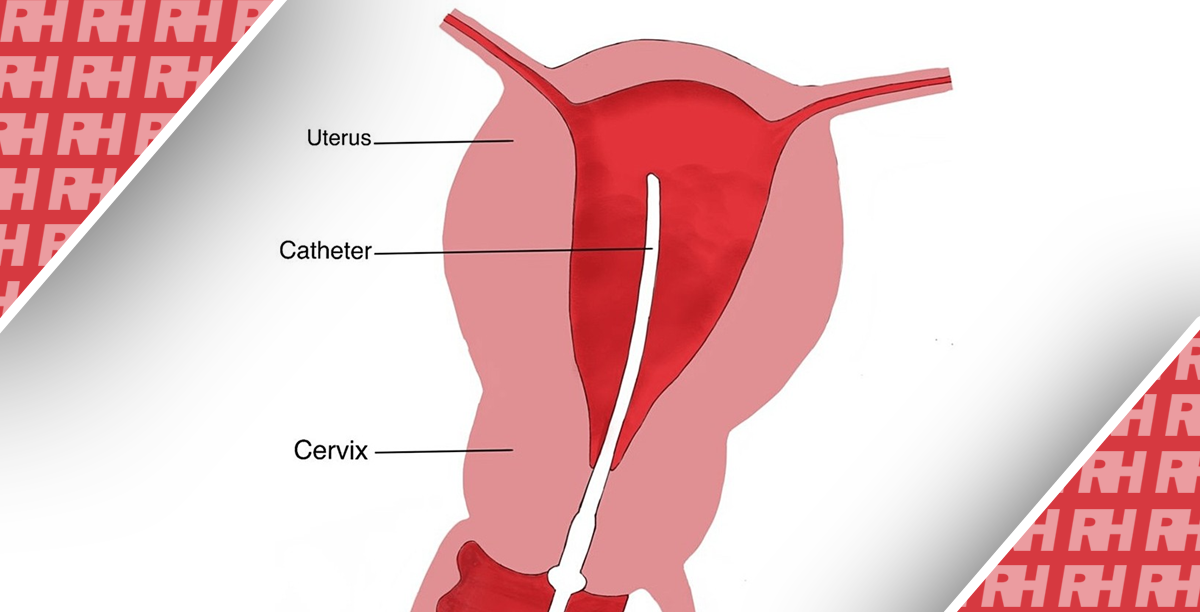
Оцінка прохідності маткових труб є важливим діагностичним інструментом в оцінці жіночої фертильності. Два найпоширеніші методи оцінки прохідності труб – це ГСГ та ГСКС. ГСГ передбачає ін’єкцію контрастного барвника в матку з подальшою рентгенівською візуалізацією для оцінки розтікання барвника по маткових трубах. ГСКС, з іншого боку, передбачає ін’єкцію контрастної речовини в матку з подальшим трансвагінальним ультразвуковим дослідженням для оцінки витоку контрастної речовини через маткові труби.
У низці досліджень порівнювали діагностичну точність ГСГ і ГСКС в оцінці прохідності труб.14,15 Деякі дослідження виявили, що ГСКС має вищу чутливість і специфічність, ніж ГСГ, тоді як інші виявили, що ГСГ і ГСКС мають подібну діагностичну точність. Що стосується впливу на кровотік і функцію яєчників, то деякі дослідження припускають, що ГСГ може тимчасово зменшувати оваріальний кровотік і, можливо, впливати на функцію яєчників. Однак клінічне значення цих даних незрозуміле, і для повного розуміння потенційного впливу ГСГ і ГСКС на оваріальний кровотік і функцію яєчників необхідні додаткові дослідження.
Загалом, як ГСГ, так і ГСКС є ефективними методами оцінки прохідності труб, і вибір методу для використання може залежати від ряду факторів, включаючи переваги пацієнтки, доступність та вартість. Важливо обговорити ризики та переваги кожного методу з лікарем, щоб визначити, який підхід найкраще підходить для кожного окремого пацієнта.14–16
ІР слугує мірою судинного опору в певній ділянці, наприклад, в яєчниковій артерії, а товщина відноситься до товщини ендометрію, який є вистиланням матки. У деяких дослідженнях повідомлялося про відмінності в ІР і товщині ендометрія між ГСГ і ГСКС. Деякі дослідження припускають, що проходження ГСКС може бути пов’язане з нижчими значеннями ІР і більшою товщиною ендометрія порівняно з застосуванням ГСГ. Ці дані можуть вказувати на потенційну перевагу ГСКС над ГСГ з точки зору оваріального кровотоку та рецептивності ендометрія, які є важливими факторами фертильності.
Таблиця 3: Зв’язок між безпліддям в анамнезі, кількістю фолікулів, тестом на вагітність та зоною між ГСГ та ГСКС.
|
Змінна |
Група |
Загалом |
p- value | ||
| ГСГ | ГСКС | ||||
|
Безпліддя в анамнезі |
Первинне |
5 | 3 | 8 |
0.4 |
| 62.5% | 37.5% | 100.0% | |||
|
Вторинне |
23 | 29 | 52 | ||
| 44.2% | 55.8% | 100.0% | |||
|
Фолікули |
0 |
5 | 3 | 8 |
0.45 |
| 62.5% | 37.5% | 100.0% | |||
|
1 |
23 | 29 | 52 | ||
| 44.2% | 55.8% | 100.0% | |||
|
ІП |
Негативний |
21 | 10 | 31 |
0.001 |
| 67.7% | 32.3% | 100.0% | |||
|
Позитивний |
7 | 22 | 29 | ||
| 24.1% | 75.9% | 100.0% | |||
|
Зона |
I |
12 | 0 | 12 |
0.0001 |
| 100.0% | 0.0% | 100.0% | |||
|
II |
10 | 4 | 14 | ||
| 71.4% | 28.6% | 100.0% | |||
|
III |
2 | 7 | 9 | ||
| 22.2% | 77.8% | 100.0% | |||
|
IV |
4 | 21 | 25 | ||
| 16.0% | 84.0% | 100.0% | |||
p ≤ 0.05 (Значущий)
Однак важливо зазначити, що ці відмінності в ІР та товщині ендометрія не були послідовно виявлені у всіх дослідженнях, і клінічне значення цих результатів не є чітким. Тому для повного розуміння потенційного впливу цих відмінностей на результати фертильності необхідні додаткові дослідження. Щодо кількості та розміру фолікулів, то не було виявлено суттєвих відмінностей між ГСГ та ГСКС. Обидва методи можна використовувати для оцінки розміру та кількості фолікулів, які є важливими показниками функції яєчників.
Хоча можуть існувати деякі відмінності в ІР і товщині ендометрія між ГСГ і ГСКС, клінічне значення цих результатів не до кінця зрозуміле. Однак обидва методи є ефективними для оцінки прохідності маткових труб та оцінки функції яєчників, і вибір методу для використання може залежати від різних факторів, включаючи переваги пацієнтки, доступність та вартість.17–20 Представлені тут результати свідчать про те, що існує значна різниця у частоті настання вагітності між жінками, які пройшли ГСКС та жінками, які проходили ГСГ. Зокрема, 75,9% жінок, які мали позитивний тест на вагітність, проходили курс ГСКС, тоді як лише 24,1% – курс ГСГ.
Ця різниця є статистично значущою, що вказує на те, що ГСКС може бути ефективнішим за ГСГ для досягнення вагітності. Крім того, дослідження виявило, що у 84% жінок з IV зоною (що вказує на наявність контрасту у фімбріальному кінці труби) під час проходження ГСКС спостерігався значний зв’язок з позитивним тестом на вагітність. Цей висновок підтверджує думку про те, що ГСКС може бути більш ефективним методом оцінки прохідності маткових труб і виявлення потенційних перешкод для вагітності.
ВИСНОВОК
ГСКС був безпечнішим, ефективнішим, простішим і дешевшим способом оцінки прохідності маткових труб, ніж ГСГ, з меншим ІР і збільшеною товщиною ендометрію. У групі ГСКС у 90,6% було виявлено більше одного фолікула, тоді як у групі ГСГ – лише у 82,1%. Середній розмір фолікула в групі ГСКС становив 17,9 порівняно з 14,7 у групі ГСГ. Середня товщина ендометрію становила 8,9 мм у групі ГСКС порівняно з 8 мм у групі ГСГ. Всі процедури показали кращу овуляцію, кількість фолікулів і товщину ендометрію в групі ГСКС, ніж в групі ГСГ, що призвело до 25% позитивних вагітностей в групі ГСГ в порівнянні з 68,8% в групі ГСКС.
Посилання на джерела
- Pereira N, Petrini AC, Lekovich JP, Elias RT, Spandorfer SD. Surgical Management of Endometrial Polyps in Infertile Women: A Comprehensive Review. Surg Res Pract 2015;2015:914390.
- Wynants L, Verbakel JYJ, Valentin L, De Cock B, Pascual MA, Leone FPG, et al. The Risk of Endometrial Malignancy and Other Endometrial Pathology in Women with Abnormal Uterine Bleeding: An Ultrasound-Based Model Development Study by the IETA Group. Gynecol Obstet Invest 2022;87:54-61.
- Seshadri S, El-Toukhy T, Douiri A, Jayaprakasan K, Khalaf Y. Diagnostic accuracy of saline infusion sonography in the evaluation of uterine cavity abnormalities prior to assisted reproductive techniques: asystematicreview andmeta-analyses. Hum Reprod Update 2015;21:262-74.
- Parsons AK, Lense JJ. Sonohysterography for endometrial abnormalities: preliminary results. J Clin Ultrasound 1993;21:87-9.
- Syrop CH, Sahakian V. Transvaginal sonographic detection of endometrial polyps with fluid contrast augmentation. Obstet Gynecol 1992;79:1041-5.
- American College of Obstetricians and Gynecologists. ACOG Technology Assessment in Obstetrics and Gynecology No. 5: sonohysterography. Obstet Gynecol 2008;112:1467-88.
- Katz VL. Diagnostic procedures: Imaging, endometrial sampling, endoscopy: indications and contraindications, complications. In: Katz VL, Lentz GM, Lobo RA, Gershenson DM, eds. Comprehensive Gynecology. 5th ed. Philadelphia, Pa: Mosby Elsevier; 2007.
- Fang F, Bai Y, Zhang Y, Faramand A. Oil-based versus water-based contrast for hysterosalpingographyin infertile women: a systematic review and meta-analysis of randomized controlled trials. Fertil Steril 2018;110:153- 160.e3.
- Rosielle K, Kamphuis D, van Welie N, Roest I, Mozes A, van Santbrink EJP, et al. Oil-based versus water-based contrast media for hysterosalpingography in infertile women of advanced age, with ovulation disorders or a high risk fortubal pathology: study protocol of a randomized controlled trial (H2Oil2 study). BMC Womens Health 2022;22:123-7.
- Bisogni FA, Galanti F, Riccio S, Yacoub V, Carletti V, Morgani C, et al. 4D-ГСКС performed in are productive center: retrospective analysis of pain perception, complications and spontaneous pregnancy rate after the technique. Eur Rev Med Pharmacol Sci 2021;25:7468-75.
- Eng CW, Tang PH, Ong CL Hysterosalpingography: current applications. Singapore Med J 2007;48:368-73
- Marci R, Marcucci I, Marcucci AA, Pacini N, Salacone P, Sebastianelli A, et al. Hysterosalpingo contrast sonography (ГСКС): evaluation of the pain perception, side effects and complications. BMC Med Imaging 2013;13:28-31.
- Schankath AC, Fasching N, Urech-Ruh C, Hohl MK, Kubik-Huch RA. Hysterosalpingography in theworkup of female infertility: indications, technique and diagnostic findings. Insights Imaging 2012;3:475-83.
- Grimbizis GF, Tsolakidis D, Mikos T, Anagnostou E, Asimakopoulos E, Stamatopoulos P, et al. Aprospective comparison of transvaginal ultrasound, saline infusion sonohysterography, and diagnostic hysteroscopy in the evaluation of endometrial pathology. Fertility Sterility 2010;94:2720-5.
- Chawla I, Tripathi S, Vohra P, Singh
- To Evaluate the Accuracy of Saline Infusion Sonohysterography (SIS) for Evaluation of Uterine Cavity Abnormalities in Patients with Abnormal Uterine Bleeding. J Obstetr Gynecol India 2014;64:197-201.
- Luterek K, Szymusik I, Bartkowiak R, Wielgos M. Sonohysterography in peri-and postmenopausal women with abnormal uterine bleeding or abnormal endometrial appearance. Neuro Endocrinol Letters 2014;35:297-300.
- Erdem M, Bilgin U, Bozkurt N, Erdem A. Comparison of transvaginal ultrasonography and saline infusion sonohysterography in evaluating the endometrial cavity in pre-and postmenopausal women with abnormal uterine bleeding. Menopause 2007;14:846-52.
- Bingol B, Gunenc Z, Gedikbasi A, Guner H, Tasdemir S, Tiras B. Comparison of diagnostic accuracy of saline infusion sonohysterography, transvaginal sonography and hysteroscopy. J Obstetr Gynaecol 2011;31:54-8.
- Soguktas S, Cogendez E, Kayatas SE, Asoglu MR, Selcuk S, Ertekin A. Comparison of saline infusion sonohysterography and hysteroscopy in diagnosis of premenopausal women with abnormal uterine bleeding. Euro J Obstetr Gynecol Reprod Biol 2012;161:66-70.
- Fleischer AC, Shappell HW. Color Doppler sonohysterography of endometrial polyps and submucosal fibroids. J Ultrasound Med 2003;22:601-4.
- Tamura-Sadamori R, Emoto M, Naganuma Y, Hachisuga T, Kawarabayashi T. The sonohysterographic difference in submucosal uterine fibroids and endometrial polyps treated by hysteroscopic surgery. J Ultrasound Med 2007;26:941-6.
- Cil A, Tulunay G, Kose M, Haberal A. Power Doppler properties of endometrial polyps and submucosalfibroids: a preliminary observational study in women with known intracavitary lesions. Ultrasound Obstetr Gynecol 2010;35:233-7.
- Omidiji OA, Toyobo OO, Adegbola O, Fatade A, Olowoyeye OA. Hysterosalpingographic findings in infertility – what has changed over the years? Afr Health Sci 2019;19:1866-74.
Найпоширеніші запитання та відповіді
Що таке гістеросальпінгографія (ГСГ) та гістеросальпінго-контрастна сонографія (ГСКС)?
- Гістеросальпінгографія (ГСГ) – це рентгенологічний метод дослідження прохідності маткових труб, який передбачає введення контрастної речовини в матку та подальшу візуалізацію за допомогою рентгенівських променів.
- Гістеросальпінго-контрастна сонографія (ГСКС) – це ультразвуковий метод дослідження прохідності маткових труб, який використовує контрастну речовину (наприклад, фізіологічний розчин з гідрокортизоном) та трансвагінальне ультразвукове дослідження для оцінки проходження контрасту через труби.
Які переваги ГСКС порівняно з ГСГ згідно з дослідженням?
- Згідно з дослідженням, ГСКС виявилася безпечнішим, ефективнішим, простішим і дешевшим методом оцінки прохідності маткових труб порівняно з ГСГ.
- Також відзначається, що ГСКС асоціюється з меншим індексом резистентності (ІР) та більшою товщиною ендометрію, що може позитивно впливати на кровотік і функцію яєчників.
Як ГСГ та ГСКС впливають на кровотік та функцію яєчників?
- Деякі дослідження припускають, що ГСГ може тимчасово зменшувати оваріальний кровотік та впливати на функцію яєчників, хоча клінічне значення цього не до кінця зрозуміле.
- ГСКС, за результатами дослідження, показала менший ІР (опору судин) та більшу товщину ендометрію, що може свідчити про потенційну перевагу щодо оваріального кровотоку та рецептивності ендометрію.
Чи є різниця у частоті настання вагітності між жінками, які проходили ГСГ та ГСКС?
- Так, результати дослідження показали значну різницю у частоті настання вагітності.
- У групі, яка проходила ГСКС, 68.8% жінок мали позитивні тести на вагітність, тоді як у групі ГСГ цей показник становив 25%. Більше того, 75.9% жінок з позитивним тестом на вагітність проходили курс ГСКС.
Які критерії оцінювалися в дослідженні для порівняння методів?
- У дослідженні оцінювалися такі критерії:
- Індекс резистентності (ІР) та індекс перфузії (ІП) судин яєчників за даними допплерометрії.
- Кількість та розмір фолікулів.
- Товщина ендометрію та його малюнок.
- Зони кровотоку до ендометрію.
- Частота настання вагітності.
Чи виявлено різницю у кількості та розмірі фолікулів між групами ГСГ та ГСКС?
- Ні, дослідження не виявило достовірної різниці між ГСГ та ГСКС за кількістю та розміром фолікулів. Обидва методи однаково підходять для оцінки цих показників функції яєчників.
Які висновки можна зробити щодо безпеки та ефективності ГСКС?
- На основі проведеного дослідження зроблено висновок, що ГСКС є безпечнішим, ефективнішим, простішим і дешевшим методом для оцінки прохідності маткових труб порівняно з ГСГ.
- Також відзначається, що ГСКС асоціюється з покращенням показників кровотоку яєчників та ендометрію, що може сприяти підвищенню шансів на вагітність.