🤖 Короткий переказ від ШІ
Дослідження описує соногістерографію з інфузією фізіологічного розчину (СІФ) як ефективний метод для оцінки уражень матки, який має значні переваги над традиційними методами візуалізації завдяки своїй простоті, економічній ефективності та точності.
СІФ відзначається як цінний інструмент у діагностиці широкого спектра гінекологічних захворювань, включаючи аномальні маткові кровотечі та безпліддя. Хоча метод має свої переваги, важливо враховувати його обмеження, зокрема, меншу чутливість у повній оцінці маткових труб порівняно з гістеросальпінгографією (ГСГ). Для повного розуміння теми рекомендуємо ознайомитися з УЗД апаратами, які є основою цього методу.
✅ Ключові тези зі статті:
- Діагностика: СІФ забезпечує високоякісну візуалізацію патологій ендометрію, допомагаючи диференціювати їх від патологій міометрію.
- Лікування: Метод використовується для точної діагностики, що є першим кроком до вибору оптимальної тактики лікування гінекологічних захворювань.
- Переваги: СІФ є економічно вигідною, простою у використанні, мінімально інвазивною та має порівнянну або вищу точність порівняно з іншими методами.
- Обмеження: До недоліків належить менша чутливість у повній візуалізації маткових труб порівняно з ГСГ та потенційний дискомфорт для пацієнтки.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Резюме
Метою цього дослідження було описати роль соногістерографії з інфузією фізіологічного розчину СІФ для оцінки уражень матки. Інфузійна соногістеросальпінгографія забезпечує тривимірні (3D) зображення з високою роздільною здатністю, що, в свою чергу, дає хорошу орієнтацію клініцистам і радіологам, в більшості випадків, про основну патологію ендометрія і труб. Інфузійна соногістеросальпінгографія з фізіологічним розчином є недостатньо використовуваним методом візуалізації, який має деякі переваги над іншими традиційними методами візуалізації. Він може бути використаний для діагностики гінекологічних захворювань. Соногістеросальпінгографія з інфузією фізіологічного розчину має перевагу над іншими методами завдяки простоті використання, економічній ефективності та неінвазивності, при цьому має порівнянну або навіть кращу точність, ніж більшість методів візуалізації, що застосовуються при гінекологічних захворюваннях. Економічна ефективність і відмінна патологічна характеристика роблять цей метод візуалізації вигідним для індійських закладів охорони здоров’я в цілому і для сільських медичних установ зокрема, де пацієнти не можуть дозволити собі дорогі дослідження. Цей огляд охоплює показання та протипоказання, техніку візуалізації, недоліки візуалізації, використання СІФ при різних патологіях матки і, в кінці, порівняння СІФ з іншими методами візуалізації. Інфузійна соногістеросальпінгографія з фізіологічним розчином показана при більшості поширених гінекологічних захворювань в Індії, а повідомлень про післяпроцедурні ускладнення дуже мало. Існує також кілька протипоказань, про які слід пам’ятати, і які згадуються нижче. Під час процедури слід дотримуватися асептичних заходів. Порівняння між методами візуалізації дозволить визначити найкращий метод для конкретного випадку відповідно до потреб пацієнта.
Категорії: Акушерство/гінекологія, Радіологія, Епідеміологія/громадське здоров’я
Ключові слова: сіф при вроджених аномаліях, сіф при синехіях матки, сіф при аденоміозі, сіф при карциномі ендометрія, сіф при субмукозній міомі, сіф при аденоміозі, соногістеросальпінгографія, соногістерографія з інфузією фізіологічного розчину.
Вступ та передумови
Ультрасонографія, також відома як ультразвукове дослідження, є дуже поширеним неінвазивним методом діагностики, який використовується для візуалізації структур, що лежать під шкірою, і майже не має протипоказань. Ультразвуковий апарат складається з датчика, підключеного до екрану комп’ютера. Датчик випромінює хвилі, які відбиваються від підлеглих структур і приймаються датчиком. Інформація від відбитих хвиль інтерпретується в комп’ютері і представляється у вигляді зображення на екрані в режимі реального часу. Це дуже широко використовуваний метод візуалізації органів черевної порожнини і тазу та інших структур, що лежать під шкірою, в режимі реального часу [1]. Соногістерографія з інфузією фізіологічного розчину (СІФ), яку також називають соногістеросальпінгографією з інфузією фізіологічного розчину, – це метод радіологічної візуалізації, який використовується для візуалізації різних патологій ендоцервіксу та ендометрію. Використовуючи ті ж принципи, що і ультразвук, цей метод візуалізує порожнину ендометрія, яка попередньо заповнюється фізіологічним розчином. Найбільшу користь СІФ приносить у виявленні та оцінці уражень ендометрію та диференціації їх від патологій міометрію. Точність СІФ не поступається гістероскопії в оцінці уражень ендометрія [2]. Інфузійна соногістерографія з фізіологічним розчином може одночасно оцінювати прохідність маткових труб з точністю на рівні з гістеросальпінгографією (ГСГ) [3,4].
Інфузійна соногістерографія з фізіологічним розчином виконується шляхом введення стерильного фізіологічного розчину в порожнину матки за допомогою катетера для розтягнення порожнини ендометрію і одночасної візуалізації органів малого тазу за допомогою трансабдомінальної або трансвагінальної сонографії. Під час виконання процедури вживаються асептичні заходи. Асептичні заходи включають використання стерильних рукавичок та інструментів, а також очищення шийки матки ватним тампоном з антисептичним розчином. Для процедури використовується 10-20 мл теплого фізіологічного розчину, який вводиться повільно. Техніка візуалізації передбачає розтягнення порожнини матки, що дозволяє рентгенологам або гінекологам візуалізувати один шар порожнини матки. Це дозволяє краще охарактеризувати патологію [5]. Показана при більшості гінекологічних захворювань, єдиними протипоказаннями до проведення СІФ є наявність активної інфекції органів малого тазу, вагітність та наявність внутрішньоматкової спіралі [6]. Інфузійна соногістерографія з фізіологічним розчином є відносно неінвазивною процедурою, ускладнень, про які повідомляється, дуже мало, найпоширенішим ускладненням є постпроцедурна інфекція [7]. Недоліки СІФ нечисленні, більшість з них можна усунути шляхом ретельного планування та виконання процедури. Ці кілька недоліків легко перекриваються чудовими результатами візуалізації, які дає СІФ.
Інфузійна соногістерографія з сольовим розчином є менш поширеним методом візуалізації, тому радіологи, клініцисти та студенти недостатньо добре ознайомлені з цією методикою, а також з отриманими зображеннями. Відсутність досвіду у більшості радіологів та недостатня обізнаність клініцистів про вищу діагностичну цінність СІФ є причиною того, що в Індії вона виконується переважно в лікарнях третинного рівня. Описано найпоширеніші гінекологічні захворювання, а також традиційно використовувані методи візуалізації для їх дослідження. Результати візуалізації за допомогою СІФ порівнюються з традиційним методом візуалізації, який при більшості патологій матки виявляється кращим. Проведено детальне порівняння між СІФ та іншими методами візуалізації, а саме: трансвагінальною сонографією (ТВС), гістероскопією, гістеросальпінгографією та магнітно-резонансною томографією (МРТ). МРТ є найбільш чутливим методом візуалізації, але не може використовуватися як основний, оскільки він є дуже дорогим і трудомістким, а також займає багато часу. Методи візуалізації мають свої переваги та недоліки, порівняльне дослідження дозволить виявити найкращий метод візуалізації для конкретної патології матки.
Огляд
Показання та протипоказання
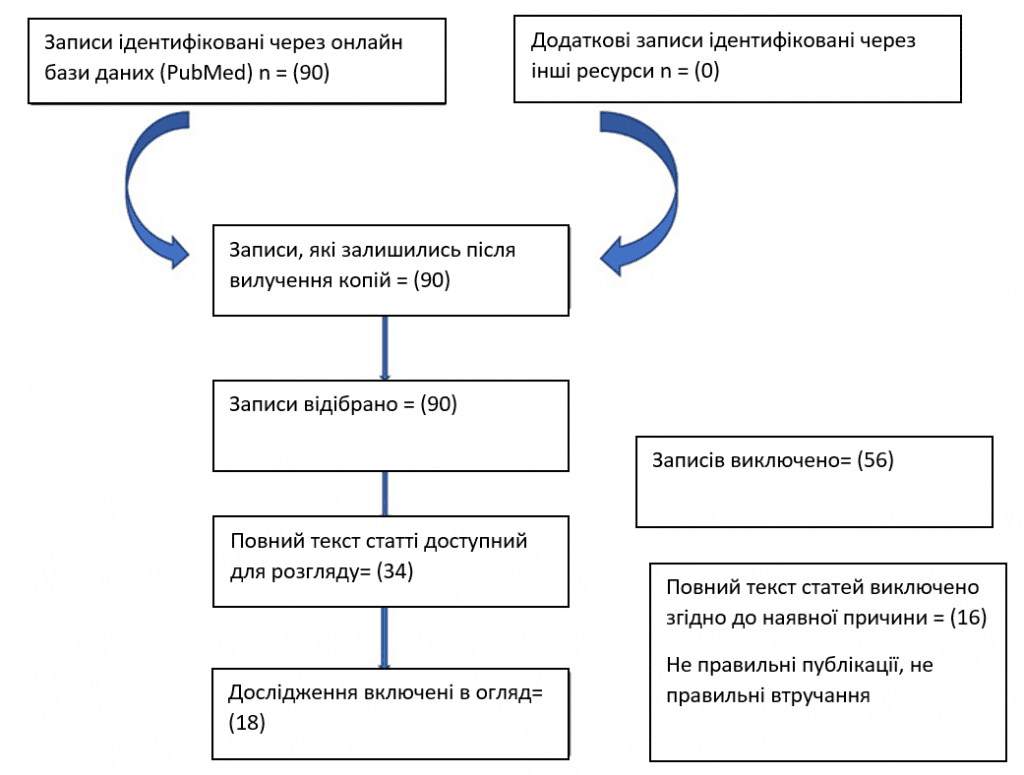
Аномальні маткові кровотечі (АМК) є найпоширенішим показанням до СІФ. АМК є дуже поширеним гінекологічним захворюванням, яке потребує повного обстеження, особливо у віковій групі перименопаузи та постменопаузи, оскільки воно прогресує до раку ендометрію, частота якого становить 10-15%. Злоякісна пухлина ендометрія, що викликає АМК, діагностується за допомогою гістероскопічної біопсії ендометрія. Відносно неінвазивні методи, такі як ТВС, зазвичай виконуються як попередні дослідження. Однак при скринінгу патологій ендометрія корисність ТВС обмежена [2]. Соногістерографія з інфузією фізіологічного розчину забезпечує кращу диференціацію вогнищевих і дифузних патологій, оскільки дозволяє оцінити один шар ендометрію за рахунок адекватного розтягнення порожнини ендометрію під час ультразвукового дослідження. Це дозволяє проводити прицільний і точний забір зразків вогнищевих уражень з високою діагностичною ефективністю. Соногістерографія з інфузією фізіологічного розчину є другим за частотою показань методом візуалізації при безплідді. Тридцять сім відсотків випадків безпліддя пов’язані з жіночими факторами, а ще 35% – з комбінованими жіночими та чоловічими факторами. Жіночі фактори безпліддя поділяються на цервікальні, маткові, яєчникові, трубні та перитонеальні [8]. Для первинної оцінки основним методом візуалізації є ТВС. Прохідність труб і порожнини матки оцінюють за допомогою ГСГ. Інфузійна соногістерографія з фізіологічним розчином поєднує можливості ГСГ та ТВС і може одночасно візуалізувати прохідність труб, порожнину матки та інші патології (зображення 1).
Зображення 1: Пошукова методика, яка використовувалась щоб відібрати найбільш релевантні статті.
Повторні аборти, передопераційна оцінка підслизової або внутрішньопорожнинної міоми матки, моніторинг після терапії тамоксифеном, підозра на синехії матки та вроджені аномалії розвитку матки є іншими показаннями для проведення СІФ [9,10]. Протипоказаннями до проведення СІФ є вагітність, активна інфекція органів малого тазу та наявність внутрішньоматкових контрацептивів [6].
Техніка візуалізації
Найкращий час для проведення СІФ – між п’ятим і 10-м днями менструального циклу в ранній проліферативній фазі, коли оболонка ендометрія є найтоншою [9]. Планування таким чином дозволяє уникнути помилкового сприйняття поліпа або утворення ендометрія за потовщений ендометрій секреторної фази, що є фізіологічним [11]. Час візуалізації також запобігає витісненню заплідненої яйцеклітини під час секреторної фази промиванням фізіологічним розчином. Через наявність залишкових згустків крові в порожнині матки протягом перших чотирьох днів менструального циклу процедуру уникають, оскільки вона може бути помилково прийнята за патологію. У жінок в постменопаузі, які страждають на АМК, її можна проводити в будь-який час циклу. Пацієнткам, які отримують замісну гормональну терапію, її призначають наприкінці прогестеронової фази менструального циклу [5].
Однак, не можна пропускати допроцедурну базову ультразвукову візуалізацію. Скринінгу таких патологій, як гідросальпінкс, може допомогти УЗД, оскільки під час СІФ його можна помилково прийняти за ін’єкційну рідину. Скринінг активних запальних захворювань органів малого тазу, які абсолютно протипоказані для проведення СІФ, можливий за допомогою передпроцедурної базової візуалізації. Визначення розміру та положення матки і шийки матки для кращої оцінки необхідної кількості фізіологічного розчину і кращого позиціонування катетера допомагає перед процедурою [5]. Техніка візуалізації зображена на зображенні 2.
Зображення 2: Техніка візуалізації при соногістерографії з інфузією фізіологічного розчину.
Недоліки СІФ при діагностиці
Очевидною передумовою для проведення СІФ є адекватне розтягнення порожнини матки; для цього використовується безехогенний фізіологічний розчин. Може виникнути кілька проблем, пов’язаних з пацієнткою та технікою виконання. Найпоширенішою проблемою є неможливість доступу до шийки матки [5]. Цього можна уникнути, правильно розташувавши пацієнтку та підібравши дзеркало відповідно до розміру піхви. Проблему змінної орієнтації шийки матки можна вирішити, попросивши пацієнтку лягти на спину після маневрування дзеркалом до відомого положення зовнішнього вічка або використовуючи тенакулум для тракції шийки матки [5,11]. Для просування катетера за межі стенозованої шийки матки можна використовувати цервікальні розширювачі або провідники. Для зменшення болю на інструменти можна наносити нестероїдні протизапальні препарати (НПЗП) та місцевоанестезуючі змащувальні гелі.
Затінення відповідної патології, що підлягає візуалізації, може бути спричинене повітрям, що міститься в порожнині матки. Візуалізації можуть заважати механічні перешкоди через наявність згустків крові в порожнині ендометрію, особливо у пацієнток з нерегулярним менструальним циклом, оскільки складно запланувати процедуру на правильний час. Згусток крові може бути помилково прийнятий за поліп ендометрію або інші вогнищеві ураження ендометрію. Згустки крові можна відрізнити від поліпів ендометрію за допомогою доплерографії, яка показує відсутність кровотоку. Адекватне роздування балона має важливе значення для запобігання зміщення катетера [5].
Однак слід уникати надмірного розтягування, щоб запобігти затемненню патології. Іншим недоліком є те, що процедура передбачає розтягнення матки і може бути болючою для деяких пацієнток. Процедура також може призвести до занесення інфекції в порожнину матки, якщо не дотримуватися відповідних асептичних заходів.
Ускладнення СІФ
Інфузійна соногістерографія з фізіологічним розчином, як процедура з мінімальною інвазією, є порівняно безпечною і добре переноситься пацієнтками, а кількість повідомлень про ускладнення є дуже малою. Dessole та співавт. провели проспективне дослідження, в якому описали ускладнення приблизно у 8,8% з 1153 пацієнток, яким проводили СІФ [7]. Менше ніж у 0,2% пацієнтів повідомлялося про постпроцедурну інфекцію [7].
Діагностична ефективність СІФ при різних патологіях матки
Підслизова фіброміома
Це доброякісні пухлини матки з фіброзної тканини і гладких м’язів, які класифікуються на підслизові, інтрамуральні та серозні залежно від їх локалізації. Часто безсимптомні підслизові міоми є випадковими знахідками при візуалізації; однак симптоматичні міоми є найпоширенішим показанням до гістеректомії [12,13]. Біль у ділянці таза, АМК, повторні втрати вагітності та безпліддя є поширеними проявами симптоматичної міоми [9,10].
Фіброміоми виглядають як гіпоехогенні, круглі та широкопрофільні утворення при візуалізації, тоді як поліпи ендометрію виглядають як гіперехогенні утворення порівняно з міометрієм. На СІФ при міомі матки спостерігається втрата ендометріально-міоматозної межі, і вона утворює тупий кут з ендометрієм. На противагу цьому, при поліпах ендометрія інтерфейс ендометрій-міометрій інтактний і має гострий кут з ендометрієм [6].
Хоча одна живильна артерія зустрічається менш ніж у половині випадків, вона залишається патогномонічною ознакою поліпів ендометрія [9,14,15], тоді як міома матки живиться розгалуженою судинною мережею [16]. Як правило, на УЗД міома матки демонструє рефракційне заднє затінення [16].
Існують як хірургічні, так і гормональні методи лікування. Консервативне лікування зазвичай проводиться в більшості випадків, але підслизові фіброміоми, що супроводжуються АМК, можуть бути видалені хірургічним шляхом. Соногістерографія з інфузією фізіологічного розчину може бути використана для визначення кількості, локалізації та об’єму проекції в порожнину фіброміоми [16]. У пацієнток з множинними міомами на УЗД органів малого тазу можна побачити викривлений або затемнений ендометрій.
Поліп ендометрію
Це локалізована доброякісна проліферація залоз ендометрія та стромальної тканини, яка проростає в порожнину ендометрія. Залежно від популяції та методу діагностики, що використовується, поширеність поліпів ендометрія становить від 16% до 34% [17]. Поліп ендометрія є важливою етіологічною причиною АМК у жінок в пре- та постменопаузі. У деяких випадках можливе співіснування дифузної гіперплазії ендометрія та поліпів [18]. Трансформація в злоякісну пухлину відбувається рідко; поширеність становить менше 5% [19].
На УЗД виглядає як гомогенно-ехогенне поліпозне ураження, яке може зазнавати крововиливів, некрозу та інфаркту [9,16]. При ТВС важко диференціювати поліп ендометрія та дифузну гіперплазію ендометрія, оскільки обидва виглядають як неспецифічне потовщення ехогенного ендометрія. При СІФ стінки ендометрія розділені безехогенним фізіологічним розчином, а ураження краще окреслене, що допомагає краще охарактеризувати ураження ендометрія. У більшості випадків ендометріальний поліп має ніжку з однією живильною судиною [17]. Ехогенні утворення з рівними контурами також можна диференціювати від злоякісних. Поліпи ендометрія необхідно видаляти хірургічним шляхом, оскільки візуалізація не може класифікувати їх як доброякісні або злоякісні [6].
Гіперплазія ендометрію
Це аномальна дифузна проліферація строми і залоз ендометрія на відміну від вогнищевої проліферації, яка спостерігається при поліпах ендометрія. Залежно від кількості, наявності та ступеня атипії розрізняють три типи – просту, складну та атипову гіперплазію.
На СІФ гіперплазія ендометрія виглядає як гомогенне потовщення ендометрія. Потовщення ендометрію може бути гетерогенним з кістозною дегенерацією. Вогнищеві ураження, такі як фіброміома, поліпи або карцинома, можуть імітуватися асиметричним потовщенням ендометрія. Основними методами лікування гіперплазії ендометрія з атипією або без неї є циклічна прогестеронова терапія або гістеректомія відповідно [20].
Карцинома ендометрію
Ендометрій Жінки в постменопаузі найчастіше страждають від карциноми ендометрію і на них припадає 10% випадків постменопаузальних кровотеч [15]. Основними факторами ризику розвитку карциноми ендометрія є відсутність естрогенів, такі як синдром полікістозних яєчників (СПКЯ), безпліддя, раннє менархе, пізня менопауза, ожиріння та метаболічний синдром.
На УЗД вона виглядає як поліпозне утворення, вогнищеве потовщення ендометрія або гетерогенне дифузне потовщення ендометрія, а також порушена межа між ендометрієм і міометрієм. Ранню стадію раку ендометрія та гіперплазію ендометрія неможливо відрізнити лише за допомогою візуалізації, тому для підтвердження діагнозу необхідне гістологічне дослідження. Гетерогенна ехотекстура, спотворена межа ендометрій-міометрій, рідина в порожнині ендометрію та нерівні краї ендометрію вказують на злоякісну пухлину [9,15]. На противагу цим результатам, гомогенна ехоструктура, чітко окреслена межа між ендометрієм та міометрієм, кістозні зміни та рівні краї ендометрію вказують на доброякісну патологію. Основним методом хірургічного лікування є тотальна абдомінальна гістеректомія разом з двосторонньою сальпінгоофоректомією. За показаннями можуть також застосовуватися хіміотерапія та променева терапія [21].
Синехії матки
Синехії матки, також відомі як маткові спайки, є однією з важливих причин повторних абортів та безпліддя. Під час звичайного ТВС ці спайки важко візуалізувати, оскільки ендометрій часто виглядає нормальним [22,23]. Соногістерографія з інфузією фізіологічного розчину забезпечує кращу візуалізацію ехогенних смуг, розділяючи стінки матки. Кінетографія в реальному часі забезпечує найкращу візуалізацію маткових спайок, які виглядають як нерегулярні ехогенні смуги, присутні вздовж викривленої порожнини ендометрія. На пізніх стадіях синехій матки адекватне розтягнення порожнини матки стає складним. Погане розтягнення порожнини ендометрія свідчить про синехії матки. Синехії або спайки ендометрія можуть обмежувати розтягнення порожнини ендометрія внаслідок попередніх процедур або введення маткових інструментів, або ж інфекції можуть призвести до скріплення слизової оболонки ендометрія між собою. Основним методом лікування є гістероскопічний керований адгезіоліз. Реадгезії можна запобігти шляхом введення внутрішньоматкової спіралі [22,23].
Аденоміоз
Це доброякісна патологія ендометрія з наявністю ектопічної строми та ендометріальних залоз у міометрії з гіпертрофією гладких м’язів [24]. Вона може бути безсимптомною або проявлятися тазовим болем, АМК або дисменореєю [25]. На сонографії він виглядає як асиметричне потовщення стінки міометрія з кулястим збільшенням матки, неоднорідною ехоструктурою міометрія, розширеним злуковим комплексом, кістами міометрія, ехогенними лінійними смугами та заповненням тріщин міометрія рідиною в порожнині ендометрія [25,26]. Першим методом візуалізації, який часто використовується, є ТВС, але діагноз може бути неспецифічним. У порівнянні з УЗД, особливості МРТ є більш специфічними. Соногістерографія з інфузією фізіологічного розчину також долає недоліки ТВС і дозволяє точно локалізувати субендометріальні кістозні зміни [25].
Крім того, краща візуалізація ендометрію забезпечується розтягненням порожнини матки фізіологічним розчином, який при інших методах візуалізації може бути затушований аденоміозом, що лежить в основі. Інші нехірургічні методи лікування включають абляційну терапію ендометрія, гормональну терапію та емболізацію маткових артерій [27].
Вроджені аномалії матки
Вроджені аномалії матки, такі як дворога матка або перегородка матки, можуть бути краще охарактеризовані за допомогою СІФ. Точна візуалізація перегородки, її товщини та типу можлива завдяки розтягненню порожнини матки фізіологічним розчином. Диференціювати перегородку від дворогій матки також можливо за допомогою СІФ. Післяопераційна оцінка вроджених аномалій матки для визначення адекватності лікування також може бути проведена за допомогою СІФ.
Терапія тамоксифеном
Тамоксифен – це препарат з антиестрогенними властивостями. Антиестрогенний вплив тамоксифену на молочну залозу використовується для лікування раку молочної залози. Спостерігається підвищена частота захворювань ендометрію, таких як кісти, поліпи, гіперплазія та злоякісні пухлини ендометрію. При візуалізації гіперплазія ендометрія, що супроводжується кістозними змінами, є найбільш поширеною знахідкою [10]. Для моніторингу патологій ендометрія, що розвиваються вторинно на фоні терапії тамоксифеном, СІФ є корисним методом діагностики. Він має вищу специфічність, ніж ТВС, в оцінці патології ендометрія у жінок у постменопаузі з раком молочної залози на терапії тамоксифеном, які не мають симптомів захворювання [28].
Порівняння СІФ з іншими методами візуалізації
СІФ проти ТВС
В оцінці стану матки та придатків матки ТВС є основним методом. Однак він обмежений у виявленні невеликих уражень внутрішньоматкової порожнини та диференціації дифузних і вогнищевих уражень ендометрія. Різні фази менструального циклу ускладнюють точну діагностику викривлень ендометрію, спричинених матковими утвореннями. Нормальну вистилку ендометрія іноді можна помилково прийняти за гіперплазію ендометрія при ТВС через те, що шари знаходяться в безпосередній близькості один від одного. На відміну від ТВС, СІФ можна використовувати для візуалізації як вогнищевих, так і дифузних уражень ендометрію, оскільки він дозволяє оцінити один шар ендометрію [2].
СІФ проти ГСГ
Безпліддя оцінюється за допомогою тестів на трубні фактори та прохідність маткових труб. На сьогоднішній день скринінговим методом дослідження прохідності труб є ГСГ [29]. СІФ є ефективним і безпечним замінником оцінки прохідності труб. Перевагами СІФ над ГСГ є економічність, простота використання, відсутність іонізуючого випромінювання та можливість одночасної візуалізації всієї порожнини матки. До недоліків
СІФ є неможливість візуалізації всієї довжини маткової труби та впевненого визначення прохідності однієї або обох маткових труб [3,4]. Різні дослідження Christianson та співавт., Socolov та співавт. і Campbell та співавт. показали, що СІФ не поступається ГСГ у виявленні уражень матки, єдиним недоліком є менша чутливість у визначенні прохідності труб [4,30–32].
СІФ проти гістероскопії
Гістероскопія є референтним стандартом в оцінці уражень порожнини матки. Однак її недоліки полягають у тому, що вона є інвазивною і дорогою, а також може призвести до ускладнень, таких як кровотеча і перфорація, через свою інвазивну природу [33]. Роль гістероскопії в оцінці уражень аднексису та міометрію обмежена.
Дослідження Scwarzler та співавт. і Epstein та співавт. показали порівнянну специфічність і чутливість гістероскопії та СІФ в оцінці внутрішньоматкових уражень і вогнищевих уражень ендометрія. Хоча гістероскопія мала перевагу в диференціації доброякісних і злоякісних уражень ендометрія, жоден з цих методів не був надійним [34,35].
Таким чином, СІФ як неінвазивний і економічно ефективний метод візуалізації з чутливістю, порівнянною з чутливістю діагностичної гістероскопії, може бути використаний як замінник первинного скринінгу при обстеженні жінок з АМК. Перевагою гістероскопії є можливість проведення біопсії одночасно з візуалізацією для гістопатологічної діагностики, що є неможливим при СІФ.
СІФ проти МРТ органів малого тазу
Використання МРТ для оцінки стану жіночого тазу зростає завдяки кращій візуалізації м’яких тканин, вищій контрастній роздільній здатності та можливостям мультипланарної візуалізації. МРТ є найкращим методом візуалізації міоми. МРТ має більше поле зору і також використовується для передопераційного картування аденоміозу [36].
Після проведення емболізації маткових артерій МРТ надає можливість виявити зміни інтенсивності сигналу та об’єму фіброміоми [37]. МРТ також краще підходить для стадіювання та оцінки раку ендометрія, оскільки дозволяє визначити передопераційне стадіювання та оцінити ступінь інвазії міометрія [38]. Здатність МРТ демонструвати розширену зону з’єднання робить МРТ органів малого тазу набагато точнішим методом оцінки аденоміозу [39]. В оцінці вроджених аномалій Мюллерової протоки МРТ є референтним стандартом [40,41].
Перевагами СІФ є одночасна оцінка прохідності труб та оцінка трубних факторів безпліддя. У пацієнтів, які не можуть пройти МРТ через протипоказання, такі як ниркова недостатність, металеві імплантати та клаустрофобія, може бути виконана СІФ. Порівняння СІФ з іншими методами візуалізації, що застосовуються в гінекології, наведено в таблиці 1.
ТАБЛИЦЯ 1: Підсумок порівняння СІФ з іншими методами візуалізації.
| СІФ проти ТВС | |
| СІФ | ТВС |
| Краща диференціація між дифузними та вогнищевими ураженнями ендометрію. Можлива одношарова оцінка матки. |
Поступається щодо точності. |
| СІФ проти ГСГ | |
| СІФ | ГСГ |
| Безпечно, ефективно, економічно вигідно і без радіаційного опромінення. | Краща та повніша візуалізація маткових труб. |
| СІФ проти гістероскопії | |
| СІФ | Гістероскопія |
| СІФ Безпечна, неінвазивна, недорога і з меншою кількістю ускладнень. Хоча обидва методи є надійними, гістероскопія дещо краща для скринінгу, оскільки дозволяє диференціювати доброякісні та злоякісні утворення. | |
| СІФ проти МРТ органів малого тазу | |
| СІФ | МРТ органів малого тазу |
| Недорога, її можна використовувати у пацієнтів з металевими імплантатами. | Краща візуалізація в декількох площинах, вища роздільна здатність і більше поле зору. |
СІФ: соногістеросальпінгографія з інфузією фізіологічного розчину
Висновок
СІФ забезпечує кращу візуалізацію патологій ендометрію порівняно з деякими рутинними методами візуалізації в гінекології і допомагає диференціювати їх від субендометріальних чинників, забезпечуючи тим самим кращі результати діагностики. Додатковою перевагою є одночасна оцінка прохідності маткових труб з порівнянною точністю. Однак, при дослідженні випадків безпліддя ГСГ є скринінговим методом вибору. Його здатність візуалізувати всю довжину маткової труби дає йому перевагу над СІФ. У випадках, пов’язаних з безпліддям та аномальними матковими кровотечами, СІФ відіграє важливу роль у діагностиці. Недоліки СІФ
Процедура СІФ є дещо болючою і може призвести до занесення інфекції, якщо не дотримуватися адекватних асептичних заходів. СІФ може ефективно використовуватися як додатковий метод скринінгу перед візуалізацією органів малого тазу. Перш за все, його економічна ефективність і порівнянна точність дають йому перевагу над іншими методами візуалізації, де ураження не є чітко візуалізованими. У таких країнах, як Індія, де багато сільського населення страждає від безлічі гінекологічних захворювань, СІФ, будучи дешевим, але ефективним, може використовуватися для скринінгу, а також для діагностики деяких захворювань.
Посилання на джерела
- Ihnatsenka B, Boezaart AP: Ultrasound: basic understanding and learning the language . Int J Shoulder Surg. 2010, 4:55-62. 10.4103/0973-6042.76960
- Aslam M, Ijaz L, Tariq S, Shafqat K, Meher-Un-Nisa, Ashraf R, Kazmi T: Comparison of transvaginal sonography and saline contrast sonohysterography in women with abnormal uterine bleeding: correlation with hysteroscopy and histopathology. Int J Health Sci (Qassim). 2007, 1:17-24.
- Sankpal RS, Confino E, Matzel A, Cohen LS: Investigation of the uterine cavity and fallopian tubes using three-dimensional saline sonohysterosalpingography. Int J Gynaecol Obstet. 2001, 73:125-9. 10.1016/s0020-7292(01)00363-0
- Christianson MS, Legro RS, Jin S, et al.: Comparison of sonohysterography to hysterosalpingogram for tubal patency assessment in a multicenter fertility treatment trial among women with polycystic ovary syndrome. 2023 Kumar et al. Cureus 15(2): e35424. DOI 10.7759/cureus.35424 7 of 9 J Assist Reprod Genet. 2018, 35:2173-80. 10.1007/s10815-018-1306-2
- Allison SJ, Horrow MM, Kim HY, Lev-Toaff AS: Saline-infused sonohysterography: tips for achieving greater success. Radiographics. 2011, 31:1991-2004. 10.1148/rg.317115074
- Frost AV, Routon SG, Angtuaco TL: Saline infusion sonohysterography: key findings and how to perform the examination. Contemp Diag Radiol. 2016, 39:1-5. 10.1097/01.CDR.0000482101.07628.03
- Dessole S, Farina M, Rubattu G, Cosmi E, Ambrosini G, Nardelli GB: Side effects and complications of sonohysterosalpingography. Fertil Steril. 2003, 80:620-4. 10.1016/s0015 0282(03)00791-x
- Recent advances in medically assisted conception . (1990). https://apps.who.int/iris/bitstream/handle/10665/38679/WHO_TRS_820_eng.pdf?sequence=1&isAllowed=y.
- Berridge DL, Winter TC: Saline infusion sonohysterography: technique, indications, and imaging findings . J Ultrasound Med. 2004, 23:97-115. 10.7863/jum.2004.23.1.97
- Yang T, Pandya A, Marcal L, Bude RO, Platt JF, Bedi DG, Elsayes KM: Sonohysterography: principles, technique and role in diagnosis of endometrial pathology. World J Radiol. 2013, 5:81-7. 10.4329/wjr.v5.i3.81
- Lindheim SR, Sprague C, Winter TC 3rd: Hysterosalpingography and sonohysterography: lessons in technique. AJR Am J Roentgenol. 2006, 186:24-9. 10.2214/ajr.05.0836
- Parker WH: Etiology, symptomatology, and diagnosis of uterine myomas . Fertil Steril. 2007, 87:725-36. 10.1016/j.fertnstert.2007.01.093
- Wallach EE, Vlahos NF: Uterine myomas: an overview of development, clinical features, and management . Obstet Gynecol. 2004, 104:393-406. 10.1097/01.AOG.0000136079.62513.39
- Bhaduri M, Tomlinson G, Glanc P: Likelihood ratio of sonohysterographic findings for discriminating endometrial polyps from submucosal fibroids. J Ultrasound Med. 2014, 33:149-54. 10.7863/ultra.33.1.149
- Bree RL, Bowerman RA, Bohm-Velez M, Benson CB, Doubilet PM, DeDreu S, Punch MR: US evaluation of the uterus in patients with postmenopausal bleeding: a positive effect on diagnostic decision making. Radiology. 2000, 216:260-4. 10.1148/radiology.216.1.r00jl37260
- Lane BF, Wong-You-Cheong JJ: Imaging of endometrial pathology. Top Magn Reson Imaging. 2010, 21:237-10.1097/RMR.0b013e31823d8045
- Rahimi S, Marani C, Renzi C, Natale ME, Giovannini P, Zeloni R: Endometrial polyps and the risk of atypical hyperplasia on biopsies of unremarkable endometrium: a study on 694 patients with benign endometrial polyps. Int J Gynecol Pathol. 2009, 28:522-8. 10.1097/PGP.0b013e3181a42228
- Grasel RP, Outwater EK, Siegelman ES, Capuzzi D, Parker L, Hussain SM: Endometrial polyps: MR imaging features and distinction from endometrial carcinoma. Clin Obstet Gynecol. 2000, 214:47-52. 10.1148/radiology.214.1.r00ja3647
- Tabrizi AD, Vahedi A, Esmaily HA: Malignant endometrial polyps: report of two cases and review of literature with emphasize on recent advances. J Res Med Sci. 2011, 16:574-9.
- Chandra V, Kim JJ, Benbrook DM, Dwivedi A, Rai R: Therapeutic options for management of endometrial hyperplasia. J Gynecol Oncol. 2016, 27: 10.3802/jgo.2016.27.e8
- Braun MM, Overbeek-Wager EA, Grumbo RJ: Diagnosis and management of endometrial cancer. Am Fam Physician. 2016, 93:468-74.
- Conforti A, Alviggi C, Mollo A, De Placido G, Magos A: The management of Asherman syndrome: a review of literature. Reprod Biol Endocrinol. 2013, 11: 10.1186/1477-7827-11-118
- AAGL practice report: practice guidelines for management of intrauterine synechiae . J Minim Invasive Gynecol. 2010, 17:1-7. 10.1016/j.jmig.2009.10.009
- Byun JY, Kim SE, Choi BG, Ko GY, Jung SE, Choi KH: Diffuse and focal adenomyosis: MR imaging findings. Radiographics. 1999, 19:161-70. 10.1148/radiographics.19.suppl_1.g99oc03s161
- Verma SK, Lev-Toaff AS, Baltarowich OH, Bergin D, Verma M, Mitchell DG: Adenomyosis: sonohysterography with MRI correlation. AJR Am J Roentgenol. 2009, 192:1112-6. 10.2214/AJR.08.1405
- Reinhold C, Tafazoli F, Mehio A, Wang L, Atri M, Siegelman ES, Rohoman L: Uterine adenomyosis: endovaginal US and MR imaging features with histopathologic correlation. Radiographics. 1999, 19:147-60. 10.1148/radiographics.19.suppl_1.g99oc13s147
- Siskin GP, Tublin ME, Stainken BF, Dowling K, Dolen EG: Uterine artery embolization for the treatment of adenomyosis: clinical response and evaluation with MR imaging. AJR Am J Roentgenol. 2001, 177:297-302. 10.2214/ajr.177.2.1770297
- Fong K, Kung R, Lytwyn A, et al.: Endometrial evaluation with transvaginal US and hysterosonography in asymptomatic postmenopausal women with breast cancer receiving tamoxifen. Radiology. 2001, 220:765-10.1148/radiol.2203010011
- Saunders RD, Shwayder JM, Nakajima ST: Current methods of tubal patency assessment. Fertil Steril. 2011, 95:2171-9. 10.1016/j.fertnstert.2011.02.054
- Socolov D, Lupaşcu IA, Danciu E, et al.: Sonohysterosalpingography versus hysterosalpingography in the evaluation of uterine and tubal infertility. [Article in Romanian]. Rev Med Chir Soc Med Nat Iasi. 2009, 113:803-8.
- Holz K, Becker R, Schürmann R: Ultrasound in the investigation of tubal patency. A meta-analysis of three comparative studies of Echovist-200 including 1007 women. Zentralbl Gynakol. 1997, 119:366-73.
- Campbell S, Bourne TH, Tan SL, Collins WP: Hysterosalpingo contrast sonography (HyCoSy) and its future role within the investigation of infertility in Europe. Ultrasound Obstet Gynecol. 1994, 4:245-53. 10.1046/j.1469-0705.1994.04030245.x
- Aas-Eng MK, Langebrekke A, Hudelist G: Complications in operative hysteroscopy – is prevention possible? Acta Obstet Gynecol Scand. 2017, 96:1399-403. 10.1111/aogs.13209
- Schwärzler P, Concin H, Bösch H, Berlinger A, Wohlgenannt K, Collins WP, Bourne TH: An evaluation of sonohysterography and diagnostic hysteroscopy for the assessment of intrauterine pathology. Ultrasound Obstet Gynecol. 1998, 11:337-42. 10.1046/j.1469-0705.1998.11050337.x
- Epstein E, Ramirez A, Skoog L, Valentin L: Transvaginal sonography, saline contrast sonohysterography and hysteroscopy for the investigation of women with postmenopausal bleeding and endometrium >5 mm. Ultrasound Obstet Gynecol. 2001, 18:157-62. 10.1046/j.1469-0705.2001.00472.x
- Dueholm M, Lundorf E, Hansen ES, Ledertoug S, Olesen F: Accuracy of magnetic resonance imaging and 2023 Kumar et al. Cureus 15(2): e35424. DOI 10.7759/cureus.35424 8 of 9 transvaginal ultrasonography in the diagnosis, mapping, and measurement of uterine myomas. Am J Obstet Gynecol. 2002, 186:409-15. 10.1067/mob.2002.121725
- Jha RC, Ascher SM, Imaoka I, Spies JB: Symptomatic fibroleiomyomata: MR imaging of the uterus before and after uterine arterial embolization. Radiology. 2000, 217:228-35. 10.1148/radiology.217.1.r00se49228
- Yamashita Y, Mizutani H, Torashima M, et al.: Assessment of myometrial invasion by endometrial carcinoma: transvaginal sonography vs contrast-enhanced MR imaging. AJR Am J Roentgenol. 1993, 161:595-9. 10.2214/ajr.161.3.8352114
- Ascher SM, Arnold LL, Patt RH, et al.: Adenomyosis: prospective comparison of MR imaging and transvaginal sonography. Radiology. 1994, 190:803-6. 10.1148/radiology.190.3.8115630
- Troiano RN: Magnetic resonance imaging of mullerian duct anomalies of the uterus . Top Magn Reson Imaging. 2003, 14:269-79. 10.1097/00002142-200308000-00002
- Pellerito JS, McCarthy SM, Doyle MB, Glickman MG, DeCherney AH: Diagnosis of uterine anomalies: relative accuracy of MR imaging, endovaginal sonography, and hysterosalpingography. Radiology. 1992, 183:795-800. 10.1148/radiology.183.3.1584936
Питання та відповіді (FAQ)
Що таке соногістерографія з інфузією фізіологічного розчину (СІФ) і як вона використовується в гінекології?
- СІФ, або соногістеросальпінгографія з інфузією фізіологічного розчину, — це радіологічний метод візуалізації, що використовується для оцінки патологій ендоцервіксу та ендометрію. Він застосовує принципи ультразвуку для візуалізації порожнини матки, попередньо заповненої фізіологічним розчином, що допомагає у виявленні та диференціації уражень ендометрію від патологій міометрію.
Які основні переваги СІФ порівняно з іншими методами візуалізації?
- СІФ є простою у використанні, економічно ефективною та відносно неінвазивною процедурою. Її точність порівнянна або навіть краща, ніж у багатьох традиційних методів візуалізації, що застосовуються при гінекологічних захворюваннях. Вона також може одночасно оцінювати прохідність маткових труб.
При яких гінекологічних захворюваннях найчастіше застосовується СІФ?
- Найчастішим показанням до СІФ є аномальні маткові кровотечі (АМК). Також СІФ ефективна при оцінці безпліддя, повторних викиднів, передопераційній оцінці підслизової або внутрішньопорожнинної міоми матки, моніторингу після терапії тамоксифеном, а також при підозрі на синехії матки та вроджені аномалії розвитку матки.
Які протипоказання до проведення СІФ?
- Основними протипоказаннями до проведення СІФ є вагітність, активна інфекція органів малого тазу та наявність внутрішньоматкових контрацептивів (спіралі).
Коли найкраще проводити процедуру СІФ?
- Найкращий час для проведення СІФ – це між п’ятим і десятим днями менструального циклу, в ранню проліферативну фазу, коли оболонка ендометрію найтонша. Це дозволяє уникнути помилкового сприйняття фізіологічних змін як патології. У жінок в постменопаузі, які страждають на АМК, процедуру можна проводити в будь-який час.
Які можливі недоліки або ускладнення при проведенні СІФ?
- Серед можливих недоліків – труднощі з доступом до шийки матки, затінення патології повітрям у порожнині матки або згустками крові, а також можливий дискомфорт або біль під час процедури через розтягнення матки. Ускладнення, такі як постпроцедурна інфекція, зустрічаються рідко (менше 0,2% випадків) за умови дотримання асептичних заходів.
Як СІФ допомагає у діагностиці таких станів, як підслизова міома матки або поліп ендометрію?
- При підслизовій міомі матки СІФ дозволяє визначити кількість, локалізацію та об’єм її виступу в порожнину матки, а також оцінити втрату ендометріально-міоматозної межі. Для поліпів ендометрію СІФ забезпечує краще окреслення ураження завдяки розділенню стінок ендометрію фізіологічним розчином, що полегшує диференціацію від дифузної гіперплазії ендометрію.