З моменту відкриття вільної фетальної ДНК (cell-free fetal DNA, cffDNA) в плазмі матері, з 1997 року спостерігається швидкий прогрес в освоєнні цього методу в якості джерела генетичного матеріалу плоду для пренатальної діагностики. Більшість вільної фетальної ДНК (cffDNA) є материнською за походженням, тільки 10% є cffDNA плоду, яка походить із плаценти та появляється в материнскому кровотоці з 5 тижня вагітності. Спочатку cffDNA були використані для визначення статі плоду за допомогою алелі Y-хромосоми, визначення фетального резус D (RHD) генотипу в резус-негативних матерів та для діагностики деяких генетичних захворювань, таких як ахондроплазії, які в більшості випадків виникають в результаті нової мутації.
АВТОРИ: T. R. Everett, L. S. Chitty
Введення
З моменту відкриття вільної фетальної ДНК (cell-free fetal DNA, cffDNA) в плазмі матері, з 1997 року спостерігається швидкий прогрес в освоєнні цього методу в якості джерела генетичного матеріалу плоду для пренатальної діагностики. Більшість вільної фетальної ДНК (cffDNA) є материнською за походженням, тільки 10% є cffDNA плоду, яка походить із плаценти та появляється в материнскому кровотоці з 5 тижня вагітності. Спочатку cffDNA були використані для визначення статі плоду за допомогою алелі Y-хромосоми, визначення фетального резус D (RHD) генотипу в резус-негативних матерів та для діагностики деяких генетичних захворювань, таких як ахондроплазії, які в більшості випадків виникають в результаті нової мутації. Технологічні досягнення, пов’язані з розробкою наступного покоління секвенування (NGS), привели до точного підрахунку послідовностей ДНК, які пов’язані з конкретними хромосомами, присутніми в материнській крові, що удосконалило розвиток неінвазивної пренатальної діагностики (NIPT) для анеуплоїдій. Крім того, кількісне визначення cffDNA також може бути корисним в ранньому виявленні вагітностей з ризиком інших несприятливих ускладнень, таких як прееклампсія та синдром затримки розвитку плоду (СЗРП).
Х-зчеплені розлади та аномалії розвитку статевих органів
Найбільш раннє клінічне застосування cffDNA було для визначення статі плоду. Це залежить від виявлення послідовностей, SRY або DYS14 в плазмі матері, що з’являються з Y-хромосоми. Техніка вже включена в стандартну пренатальну діагностику в ряді європейських країн, включаючи Великобританію, для ведення вагітностей з підвищеним ризиком важких генетичних порушень, зчеплених з Х-хромосомою, наприклад, м’язової дистрофії Дюшена. Точне визначення статі плода у вагітних з ризиком вродженої гіперплазії кори наднирників може забезпечити раннє припинення лікування стероїдами, при виявленні плода чоловічої статі. Тестування являється єдиним надійним методом визначення статі плоду вже з 7 тижнів вагітності, хибно-позитивні результати можливі у випадку багатоплідних вагітностей.
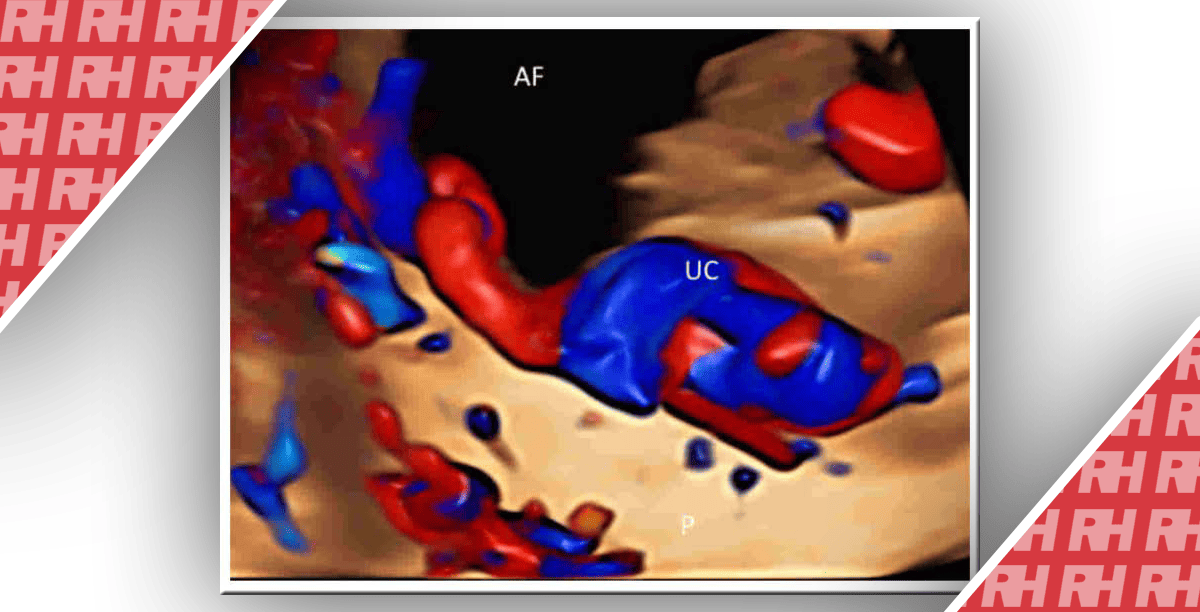
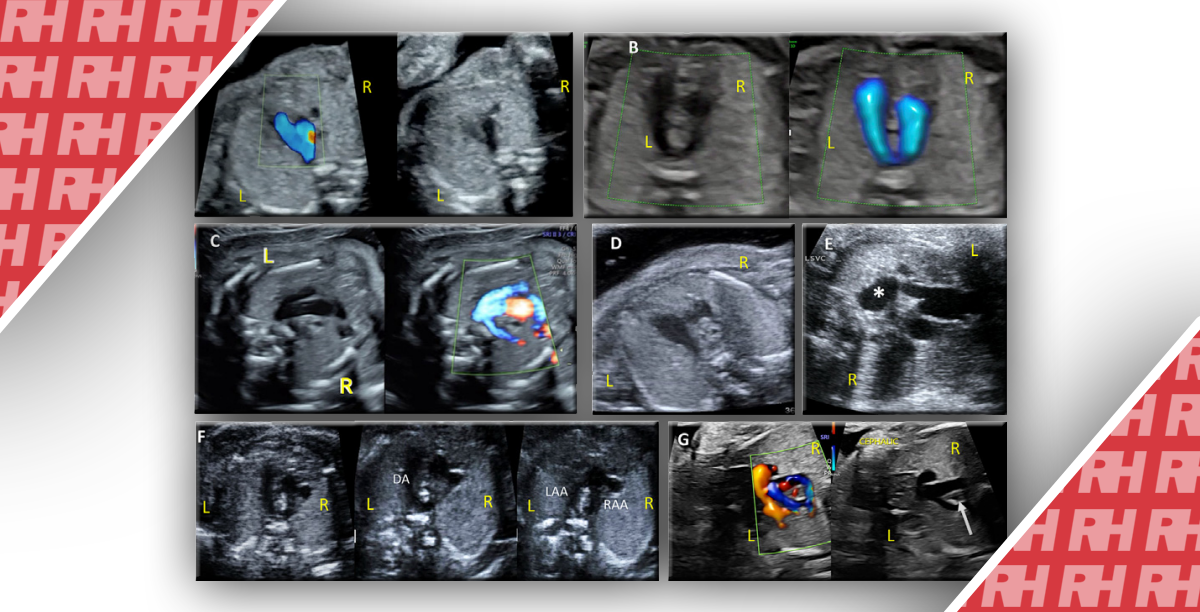
Неоднозначність розвитку геніталій є рідкісною знахідкою на УЗД, проте навіть з появою вдосконалених тривимірних методів (3D) візуалізації, диференціація між кліторомегалією у плода жіночої статі та гіпоспадією у хлопчиків залишається складною (Рис.1). У тих випадках, коли є генітальна невизначеність і тестування cffDNA показує, що плід чоловічої статі, найбільш ймовірний діагноз гіпоспадія, хоча деякі рідкісні ендокринні розлади не можуть бути виключені повністю без секвенування гена рецептора андрогену (Рис.1).
Рис.1 Патологія розвитку статевих органів. а) випадок гіпоспадії у плода чоловічої статі, підтверджений cffDNA аналізом, b) кліторомегалія, жіноча стать підтверджена cffDNA.
cffDNA та Rh-D негативна мати
Друге клінічне застосування тесту cffDNA – визначення резусналежності плода у RhD-негативних матерів. Як і в разі визначення статі плоду, це можливо тому, що резус-негативна мати не виробляє ніяких копій гена RhD (RHD), і, таким чином визначення RHD в материнській крові походить від плоду, який успадкував ген від батька. За останнє десятиліття, фетальне RHD генотипування в резус-негативних жінок зі значними титрами анти-RhD імуноглобуліну, було можливо з використанням полімеразної ланцюгової реакції (ПЛР). Такий підхід до ведення цих вагітних високого ризику призводить до уникнення необхідності інвазивного тестування, яке було потрібно раніше. NIPT обходить необхідність оцінки батьківського фенотипу, який може не бути відомим. Якщо плід резус позитивний, необхідно посилене спостереження за можливим розвитком анемії або набряку плоду.
Впровадження високопродуктивних технологій для масового RHD генотипування може забезпечити цільове введення анти-D імуноглобуліну. В даний час багато країн пропонують допологову імунну профілактику для всіх резус-негативних матерів, в терміні гестації 26-28 тижнів, що значно знижує частоту резус-сенсибілізації, але це призводить до непотрібного введенню анти-D імуноглобуліну приблизно у 38% RhD-негативних жінок, які несуть резус-негативний плід. Рутинне RHD генотипування плода може покращити імунопрофілактику, орієнтовану на жінок з найвищим ризиком, в результаті знижується темп алоімунізації, а згодом і необхідність внутрішньоутробного переливання крові.
Неінвазивне пренатальне тестування для моногенних розладів
Використання cffDNA у виявленні моногенних розладів є значно складнішою технічно, ніж генотипування RHD або визначення статі плоду, та в даний час використовується в клінічній практиці тільки для виявлення аллелів, які виникли в момент запліднення, наприклад ахондроплазії або захворювання які передаються у спадок від батька.
Остаточний діагноз ахондроплазії та летальної дисплазії по NIPT був доступним на дослідницькій основі з 2007 року та схваленим для використання у звичайній клінічній практиці в Великобританії в 2012 році. NIPT може поставити остаточний діагноз без необхдності інвазивного тестування, забезпечити диференціацію між летальною дисплазією та ахондроплазією, обидва з яких виникають із-за мутацій в гені рецептора фактора росту фібробластів 3 (FGFR3). Різниця між цими двома станами під час ультразвукової пренатальної діагностики може бути складним завданням, оскільки вони мають багато спільних рис, таких як вип’ячування лобової кістки, відносна макроцефалія, короткі кінцівки та короткі фаланги пальців, зменшення грудної клітки, дані ознаки є більш виражені при летальній дисплазії. NIPT також може запропонувати більш точний діагноз у випадку багатоплідної вагітності, з одним нормальним плодом, та НЕ допустити при цьому викидня нормального плода. Діагностика NIPT здійснюється в 9 тижнів вагітності, що раніше, ніж інвазивне тестування, яке не може бути виконане до 11 тижнів, та набагато раніше, ніж постановка діагнозу на УЗД.
Використання cffDNA для діагностики моногенних розладів має великий потенціал. У Великобританії він був схвалений для використання в Національній службі охорони здоров’я (NHS) для скринінгу мутацій в FGFR3 (ахондроплазії та летальної дисплазії) та FGFR2 (Apert syndrome) генів та виключення розповсюджених мутацій муковісцидозу. З введенням цих безпечних випробувань ми спостерігаємо різке зниження використання інвазивних тестів для виявлення моногенних розладів, з подальшим зниженням післяманіпуляційних ускладнень.
Cell-free DNA тест для анеуплоїдії
Використання тестування cfDNA для анеуплоїдії призводить до радикальних змін в практиці фетальної медицини.
Для виявлення трисомії 21 використовується NGS для NIPT, що є доступним в приватному секторі в більш ніж 50 країн, з рівнем виявлення понад 99% для трисомії 21 та дещо вище для трисомії 18 і 13, на рівні близько 96% і 92% відповідно.
Хоча NIPT є більш точним, ніж звичайний комбінований скринінг (УЗД-скринінг, визначення РАРР-А та ХГ) в першому триместрі вагітності, NIPT слід розглядати як високочутливий скринінг, а не остаточний діагноз. Будь-який позитивний результат повинен бути підтверджений інвазивним тестуванням, в ідеалі амніоцентезом або, як мінімум, каріотипуванням на культивованих ворсинах хоріону, щоб уникнути випадків плацентарного мозаїцизму, материнських хромосомних перебудов або мозаїчності.
Хибні результати NIPT діагностуються в 5% випадків. Вони, як правило, викликані низькою ембріональною фракцією cffDNA, найчастіше на ранніх термінах вагітності, так як кількість cffDNA збільшується з плацентарною масою та терміном гестації, або високим індексом маси тіла матері, коли низька фетальна фракція була оцінена як патологія, хоча це сталося на фоні високого рівня материнської cffDNA, отриманої з жирової тканини. У ситуаціях, пов’язаних з невеликим плацентарним об’ємом, наприклад, трисомії 13 і 18, рівень фетальної фракції буде нижчим.
NIPT для анеуплоїдії тепер доступний широко по всій земній кулі, хоча, на даний час тільки в приватному секторі. Вартість тестування залишається високою, але вона вже значно знизилася, ведуться переговори щодо того, як це може бути реалізовано в охороні здоров’я на державному рівні.
Висновок
В даний час NIPT може надійно використовуватися тільки для виявлення основних трисомій та хромосомних аномалій, зчеплених зі статтю. Незважаючи на це, ряд компаній почали комерційні тести для обмеженого кола мікроделеційних синдромів, в тому числі Di George (22q-), Wolf–Hirschhorn (4p-), Cri-du-Chat (5p-), Prader–Willi. Ці тести, в основному, були розроблені з використанням штучно отриманих зразків, проте, обгрунтовані дані по валідизації, що характеризують чутливість, специфічність і прогностичну цінність в зразках материнської плазми ще не опубліковані. Хоча такий підхід може підвищити виявлення патогенних мутацій, існує побоювання, що за допомогою розширеного NIPT може збільшитись кількість хибнопозитивних результатів.


















14.10.2019
Карпенко Юрій