Авторы: Carla Serra, Cristina Felicani, Elena Mazzotta, Veronica Gabusi, Valentina Grasso, Antonio De Cinque, Lydia Giannitrapani, Maurizio Soresicor
Введение
Серошкальное УЗИ очень точное в диагностике заболеваний желчного пузыря, но в некоторых случаях оно не имеет решающего значения. Одним из основных ограничений этого инструмента является его неспособность дифференцировать густой желчный осадок и опухоли.
На УЗИ осадок от застоя проявляется в виде эхо-сигналов низкого уровня, которые наслоены в прилегающей к печени части желчного пузыря без акустического затенения; как правило, они медленно сдвигаются с изменением положения пациента. Когда осадок откладывается в нижней стенке желчного пузыря или в воронке или на дне и является слишком плотным, движение не наблюдается, что может ввести в заблуждение.
В последние годы внедрение CEUS внесло значительный вклад в диагностику многих заболеваний брюшной полости. Это также верно для заболеваний желчного пузыря. Поскольку, в отличие от опухолей, осадок не является васкуляризированным, CEUS может фактически улучшить диагностическую точность УЗИ при дифференцировке опухолей от осадка.
Материалы и методы
Мы ретроспективно рассмотрели УЗ-изображения 4137 пациентов (2653 Ж, 1484 M) с положительными симптомами на заболевания желчного пузыря в отделении ультразвуковой диагностики и интервенции, отделении внутренней медицины и трансплантологии, Болонский университет (больница Св. Орсола Мальпиги). У 43 пациентов (1,04%) , средний возраст 54 ± 12 лет – на УЗИ с использованием классических критериев (образование в желчном пузыре, подвижность с изменениями положения тела) не проводилось различий между осадком и новообразованием.
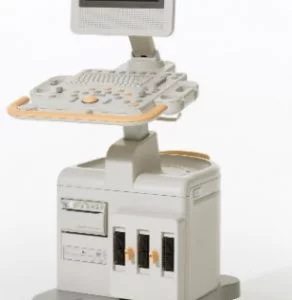
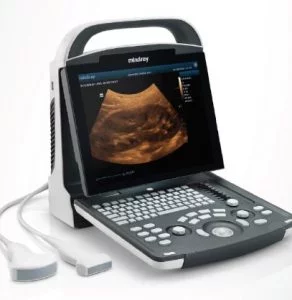
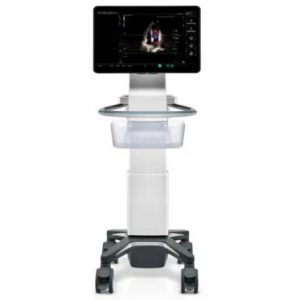
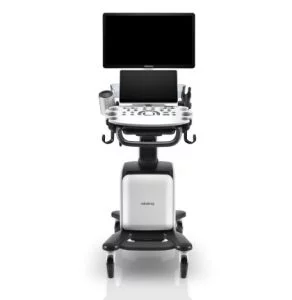
Ультразвуковые исследования проводились с помощью системы Philips IU 22. Использовались конвексный 1–5 МГц и линейный 3–9 МГц датчики.
Сканирование выполняли у пациентов утром после голодания в течение не менее 10 часов; CEUS был выполнен врачом с более чем 10-летним опытом, который также выполнил предварительное традиционное ультразвуковое исследование для каждого пациента.
CEUS: SonoVue (Бракко, Италия) – контрастный агент с микропузырьками, наполненный SF6, стабилизированный фосфолипидами. Контрастный болюс объемом 2,4 мл с последующим 10-мл промыванием физиологическим раствором. Исследование в реальном времени проводилось в течение 5 минут после введения контрастного вещества.
Процесс усиления поражений желчного пузыря с использованием CEUS классифицируется на две сосудистые фазы: «ранняя / артериальная фаза» (через 10–30 с после введения контрастного вещества) и «поздняя / венозная фаза» (через 31–180 с после введения контрастного вещества).
В 4 случаях, CEUS не был доступен из-за камней с большой тенью, которые мешали увидеть весь просвет желчного пузыря.
Поражения были классифицированы следующим образом:
- Серошкальное УЗИ:
• Полипоидные поражения: сидячие или с ножкой. Эхогенность была разделена на: (а) гиперэхогенную; (б) гипоэхогенную; (в) изоэхогенную
• Утолщение стенок при неровной поверхности: при этом стенки желчного пузыря просматриваются очагово и нерегулярно утолщенными с неровной поверхностью и неоднородной внутренней текстурой.
- CEUS:
• Аваскулярные поражения: без усиления.
• Сосудистые поражения: с усилением.
Результаты были определены как:
- Осадок: поражения, направленные просвет желчного пузыря или утолщенные без признаков увеличения или инфильтрации в печень.
- Поражения: поражения желчного пузыря или утолщение с признаками усиления.
Они в свою очередь были определены как:
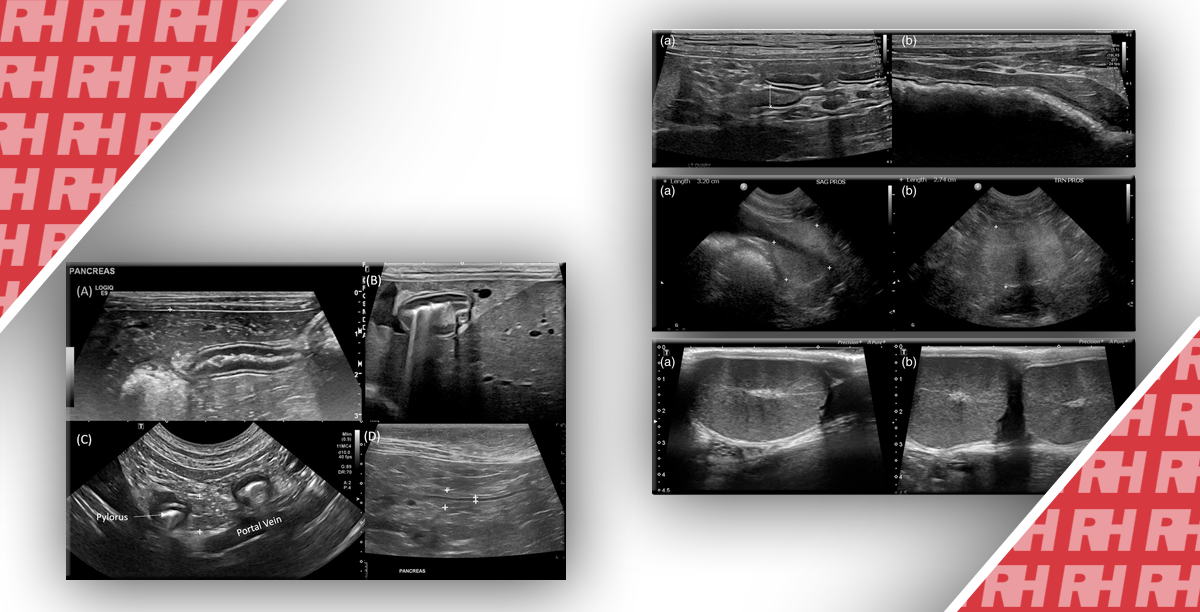
- Доброкачественные образования: поражения, направленные в просвет ЖП или утолщенные без вымывания в течение 60с и инфильтрации в печень (Рис. 1)
Рисунок 1: a При CEUS однородное усиление полипа, выступающего в просвет ЖП во время артериальной фазы, b то же самое поражение демонстрирует стойкое усиление в поздней фазе (60 с).
- Рак: поражения, направленные в просвет ЖП с вымыванием в течение 60с при наличии или отсутствии инфильтрации в печень (Рис. 2 и 3).
Рисунок 2: В-режим УЗИ демонстрирует гипоэхогенное поражение диаметром 2,29 см в желчном пузыре и без явного слияния с печенью.
Рисунок 3: a На ранней стадии CEUS (23 с) поражение желчного пузыря (стрелка) показало гомогенное гипер-усиление, b поражение (стрелка) показало гипо-усиление через 40 с после введения контрастного вещества; c поражение показало непрерывное гипо-усиление во время поздней фазы (120 с).
Выбор лечения:
- Последующее наблюдение: поражения ≤ 1 см, без клинических, лабораторных и УЗ-признаков холестаза.
- Хирургия:
• поражения любого размера с клиническими, ультразвуковыми или лабораторными признаками холестаза,
• поражения > 1 см, даже без признаков холестаза,
• увеличение размера поражения во время наблюдения> 1 см;
Диагностика осадка
Таблица 1 показывает некоторые характеристики УЗИ и CEUS исследуемой популяции с осадком при застое желчи.
| Осадок (16 пациентов) | |
| Возраст | 43.2 ± 12 |
| Ж/М | 7/9 |
| Размер(мм) | 14 (10-24) |
| Эхогенность | |
| Гипоэхогенные | 2 (12.5%) |
| Гиперэхогенные | 2 (12.5%) |
| Изоэхогенные | 12 (75%) |
Пациенты с осадком имели значительно меньший возраст. Не было различий по полу или размеру, форме, эхогенности и текстуре.
Диагностика доброкачественных / злокачественных образований
Двадцать пациентов получили хирургическое лечение; гистопатологический диагноз выявил рак желчного пузыря у 9, аденому у 2, полипы у 5 и желчный осадок с микролитиазом у 4.
| Рак | Доброкачественные | |
| Возраст | 68 ± 9 | 60 ± 11 |
| Ж/М | 3/6 | 5/9 |
| Размер(мм) | 20 (10–60) | 12 (10–24) |
| Эхогенность | ||
|
Гипо-, / гипер- эхогенные |
7/2 | 2/12 |
| Изоэхогенные | 0 (0%) | 0 (0%) |
Все поражения показали усиление, но вымывание в течение 60с присутствовало у 100% карцином и 14,3% доброкачественных образований. При использовании порога вымывания 60с для диагностики карциномы желчного пузыря чувствительность CEUS составила 100%, а специфичность – 85%, поскольку было 2 ложноположительных результата, но нет ложноотрицательных.
Итоги
Ограничением УЗИ являлось то, что они не изучают васкуляризацию. По этой причине в прошлом использовался цветной допплер. Однако надежность этого метода, особенно для небольших поражений, была неудовлетворительной. CEUS позволяет наблюдать за микроциркуляцией и, следовательно, способен обнаруживать васкуляризацию, таким образом различая осадок при застое (аваскулярный) и опухоли желчного пузыря (васкулярные). Более того, благодаря улучшению он может помочь дифференцировать хронический холецистит от рака желчного пузыря.
Предыдущие исследования разделили поражения желчного пузыря на четыре типа:
- тип 1 с сосудистым рисунком, характеризующимся «ветвистым» расположением;
- тип 2 с «гетерогенным» сосудистым рисунком;
- тип 3 – поражения с «однородным» сосудистым рисунком;
- тип 4, поражения без сигналов васкуляризации.
При определении карциномы желчного пузыря как поражений типа 1 или типа 2 чувствительность и специфичность составили 86% и 97% соответственно. При определении осадка как сосудистого рисунка типа 4 чувствительность и специфичность составляли 100% и 98% соответственно. При определении неопухолевых полипов как поражений типа 3 чувствительность и специфичность составили 92% и 97% соответственно.
Эта классификация, однако, особенно применима к изображениям, размер которых превышает 2–3 см, поэтому эти схемы будут малопригодны для ранней диагностики, которая имеет большое значение, учитывая агрессивность рака желчного пузыря.