🤖 Короткий переказ від ШІ
Сірошкальна УЗД ефективна в діагностиці захворювань жовчного міхура, але має обмеження у розрізненні густого жовчного осаду та пухлин. Контрастна ультразвукова еластографія (CEUS) значно покращує цю диференціацію, візуалізуючи васкуляризацію, що відсутня в осаді, але присутня в пухлинах.
Дослідження показало, що CEUS здатна розрізняти доброякісні та злоякісні утворення з високою чутливістю та специфічністю, особливо за критерієм вимивання контрасту. Зокрема, чутливість CEUS для діагностики раку жовчного міхура склала 100%, а специфічність – 85%. Завдяки цій технології можна покращити діагностику та вибір тактики лікування, забезпечуючи своєчасне виявлення патологій. Для ознайомлення з різними типами УЗД апаратів, що використовуються в таких дослідженнях, відвідайте наш сайт.
✅ Ключові тези зі статті:
- Діагностика: CEUS допомагає диференціювати пухлини жовчного міхура від осаду завдяки візуалізації васкуляризації.
- Лікування: Вибір тактики лікування залежить від розміру ураження, наявності симптомів холестазу та динаміки зростання.
- Переваги: CEUS підвищує точність УЗД, дозволяючи спостерігати за мікроциркуляцією та розрізняти аваскулярні (осад) та васкулярні (пухлини) ураження.
- Обмеження: Класичні УЗД методи не завжди можуть диференціювати осад від пухлин, особливо при щільному осаді.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: Carla Serra, Cristina Felicani, Elena Mazzotta, Veronica Gabusi, Valentina Grasso, Antonio De Cinque, Lydia Giannitrapani, Maurizio Soresicor
Вступ
Сірошкальна УЗД дуже точна в діагностиці захворювань жовчного міхура, але в деяких випадках вона не має вирішального значення. Одним з основних обмежень цього інструмента є його нездатність диференціювати густий жовчний осад і пухлини.
На УЗД осад від застою проявляється у вигляді ехо-сигналів низького рівня, які нашаровані в прилеглій до печінки частині жовчного міхура без акустичного затінення; як правило, вони повільно зсуваються зі зміною положення пацієнта. Коли осад відкладається в нижній стінці жовчного міхура або в воронці або на дні і є дуже щільним, рух не спостерігається, що може ввести в оману.
В останні роки впровадження CEUS зробило значний внесок в діагностику багатьох захворювань черевної порожнини. Це також вірно для захворювань жовчного міхура. Оскільки, на відміну від пухлин, осад не є васкуляризованним, CEUS може фактично поліпшити діагностичну точність УЗД при диференціюванні пухлин від осаду.
Матеріали та методи
Ми ретроспективно розглянули УЗ-зображення 4137 пацієнтів (2653 Ж, 1484 Ч) з позитивними симптомами на захворювання жовчного міхура у відділенні ультразвукової діагностики та інтервенції, відділенні внутрішньої медицини та трансплантології, Болонський університет (лікарня Св. Орсола Мальпігі). У 43 пацієнтів (1,04%), середній вік 54 ± 12 років – на УЗД з використанням класичних критеріїв (утворення в жовчному міхурі, рухливість зі змінами положення тіла) не виявлялося відмінностей між осадом і новоутворенням.
Ультразвукові дослідження проводились за допомогою системи Philips IU 22. Використовувалися конвексний 1-5 МГц і лінійний 3-9 МГц датчики.
Сканування виконували у пацієнтів вранці після голодування протягом не менше 10 годин; CEUS був виконаний лікарем з більш ніж 10-річним досвідом, який також виконав попереднє традиційне ультразвукове дослідження для кожного пацієнта.
CEUS: SonoVue (Бракко, Італія) – контрастний агент з мікробульбашками, наповнений SF6, стабілізований фосфоліпідами. Контрастний болюс об’ємом 2,4 мл з наступним 10-мл промиванням фізіологічним розчином. Дослідження в реальному часі проводилося протягом 5 хвилин після введення контрастної речовини.
Процес посилення уражень жовчного міхура з використанням CEUS класифікується на дві судинні фази: «рання / артеріальна фаза» (через 10-30 секунд після введення контрастної речовини) і «пізня / венозна фаза» (через 31-180 секунд після введення контрастної речовини).
У 4 випадках, CEUS не був доступний через каміння з великою тінню, які заважали побачити весь просвіт жовчного міхура.
Ураження були класифіковані в такий спосіб:
- Сірошкальних УЗД:
• Поліпоїдні ураження: сидячі або з ніжкою. Ехогенність була розділена на: (а) гіперехогенну; (б) гіпоехогенну; (в) неоднорідну
• Потовщення стінок при нерівній поверхні: при цьому стінки жовчного міхура проглядаються вогнищево і нерегулярно потовщеними з нерівною поверхнею і неоднорідною внутрішньої текстурою. - CEUS:
• Аваскулярні ураження: без посилення.
• Судинні ураження: з посиленням.
Результати були визначені як:
- Осад: ураження, спрямовані в просвіт жовчного міхура або потовщені без ознак збільшення або інфільтрації в печінку.
- Поразки: ураження жовчного міхура або потовщення з ознаками посилення.
Вони в свою чергу були визначені як:
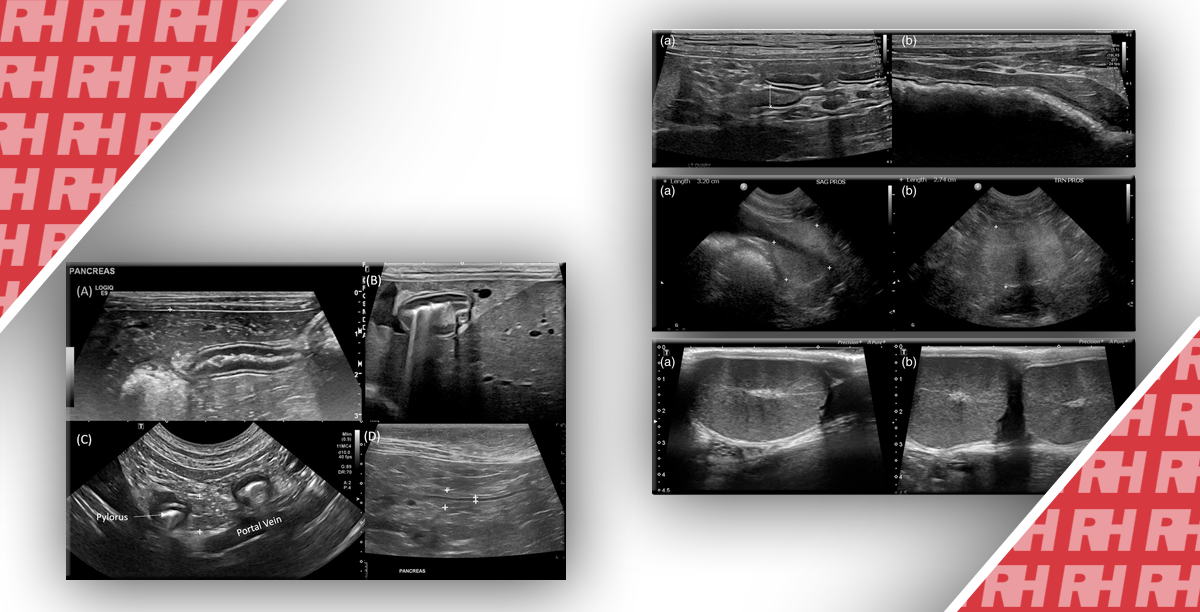
- Доброякісні утворення: ураження, направленні в просвіт ЖМ або потовщені без вимивання протягом 60 с і інфільтрацією в печінку (Зобр. 1)
Зображення 1: a При CEUS однорідне посилення поліпа, який виступає в просвіт ЖМ під час артеріальної фази, b те ж саме ураження демонструє стійке посилення в пізній фазі (60 с).
- Рак: ураження, спрямовані в просвіт ЖМ з вимиванням протягом 60с при наявності або відсутності інфільтрації в печінку (Зобр. 2 і 3).
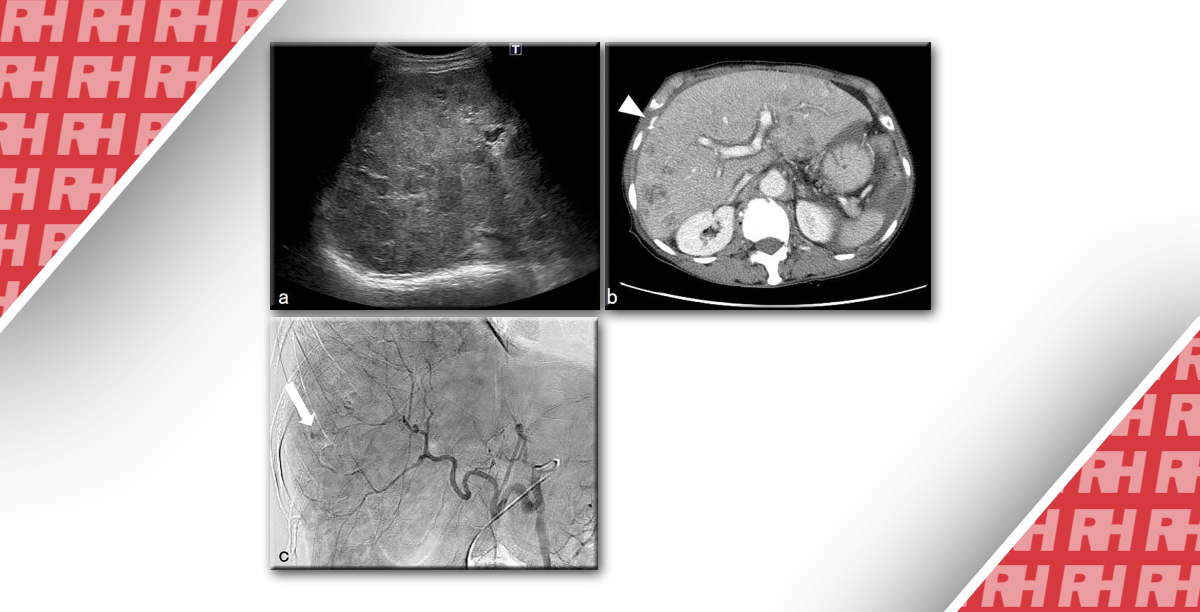
Зображення 2: В-режим УЗД демонструє гіпоехогенне ураження діаметром 2,29 см в жовчному міхурі і без явного злиття з печінкою
Зображення 3: a На ранній стадії CEUS (23 с) ураження жовчного міхура (стрілка) показало гомогенне гіпер-посилення, b ураження (стрілка) показало гіпо-посилення через 40 секунд після введення контрастної речовини; c ураження показало безперервне гіпо-посилення під час пізньої фази (120 с).
Вибір лікування:
- Подальше спостереження: ураження ≤ 1 см, без клінічних, лабораторних та УЗ-ознак холестазу.
- Хірургія:
• ураження будь-якого розміру з клінічними, ультразвуковими або лабораторними ознаками холестазу,
• ураження> 1 см, навіть без ознак холестазу,
• збільшення розміру поразки під час спостереження> 1 см;
Діагностика осаду
Таблиця 1 показує деякі характеристики УЗД і CEUS досліджуваної популяції з осадом при застої жовчі.
| Осад (16 пацієнтів) | |
| Вік | 43.2 ± 12 |
| Ж/Ч | 7/9 |
| Розмір(мм) | 14 (10-24) |
| Ехогенність | |
| Гіпоехогенні | 2 (12.5%) |
| Гіперехогенні | 2 (12.5%) |
| Ізоехогенні | 12 (75%) |
Пацієнти з осадом мали значно менший вік. Не було відмінностей за статтю або розміром, формою, ехогенністю і текстурою.
Діагностика доброякісних/злоякісних утворень
Двадцять пацієнтів отримали хірургічне лікування; гістопатологічний діагноз виявив рак жовчного міхура у 9, аденому у 2, поліпи у 5 і жовчний осад з мікролітіазом у 4.
| Рак | Доброякісні | |
| Вік | 68 ± 9 | 60 ± 11 |
| Ж/Ч | 3/6 | 5/9 |
| Розмір(мм) | 20 (10–60) | 12 (10–24) |
| Ехогенність | ||
|
Гіпо-, / гіпер- ехогенні |
7/2 | 2/12 |
| Ізоехогенні | 0 (0%) | 0 (0%) |
Всі ураження показали посилення, але вимивання протягом 60с присутнє у 100% карцином і 14,3% доброякісних утворень. При використанні порога вимивання 60с для діагностики карциноми жовчного міхура чутливість CEUS склала 100%, а специфічність – 85%, оскільки було 2 хибнопозитивних результати, але не було хибнонегативних.
Підсумки
Обмеженням УЗД було те, що воно не вивчають васкуляризацию. З цієї причини в минулому використовувався кольоровий доплер. Однак надійність цього методу, особливо для невеликих уражень, була незадовільною. CEUS дозволяє спостерігати за мікроциркуляцією і, отже, здатний виявляти васкуляризацію, таким чином розрізняючи осад при застої (аваскулярні) і пухлини жовчного міхура (васкулярні). Більш того, завдяки поліпшенню він може допомогти диференціювати хронічний холецистит від раку жовчного міхура.
Попередні дослідження розділили ураження жовчного міхура на чотири типи:
- тип 1 з судинним малюнком, що характеризується «гіллястим» розташуванням;
- тип 2 з «гетерогенним» судинним малюнком;
- тип 3 – ураження з «однорідним» судинним малюнком;
- тип 4 – ураження без сигналів васкуляризації.
При визначенні карциноми жовчного міхура як уражень типу 1 або типу 2 чутливість і специфічність склали 86% і 97% відповідно. При визначенні осаду як судинного малюнка типу 4 чутливість і специфічність становили 100% і 98% відповідно. При визначенні непухлинних поліпів як уражень типу 3 чутливість і специфічність склали 92% і 97% відповідно.
Ця класифікація, однак, підходить для зображень, розмір яких перевищує 2-3 см, тому ці схеми будуть малопридатні для ранньої діагностики, яка має велике значення, враховуючи агресивність раку жовчного міхура.
Часті питання (FAQ)
Які обмеження має сірошкальна УЗД в діагностиці захворювань жовчного міхура?
- Одним з основних обмежень сірошкальної УЗД є нездатність диференціювати густий жовчний осад і пухлини.
Як CEUS покращує діагностичну точність УЗД при диференціюванні пухлин від осаду?
- Оскільки осад не є васкуляризованим, на відміну від пухлин, CEUS може поліпшити точність, візуалізуючи мікроциркуляцію.
Які фази судинного посилення розрізняють при використанні CEUS?
- «Рання/артеріальна фаза» (10-30 секунд після введення контрастної речовини) та «пізня/венозна фаза» (31-180 секунд).
Як класифікуються ураження жовчного міхура за допомогою CEUS?
- На аваскулярні (без посилення) та судинні (з посиленням).
Який критерій використовувався для визначення раку жовчного міхура за допомогою CEUS в дослідженні?
- Вимивання контрастної речовини протягом 60 секунд.
Які показники чутливості та специфічності CEUS при діагностиці раку жовчного міхура за дослідженням?
- Чутливість 100%, специфічність 85% (при використанні порога вимивання 60с).
Коли показано хірургічне лікування уражень жовчного міхура?
- Ураження будь-якого розміру з ознаками холестазу, ураження >1 см навіть без холестазу, збільшення розміру ураження під час спостереження >1 см.