Акустична променева візуалізація є новим методом еластографії, який може аналізувати жорсткість тканин якісно та кількісно. ARFI оцінює жорсткість тканини, забезпечує додатковою інформацією при традиційній ультрасонографії, таким чином потенційно покращує характеристику тканин і вогнищевих уражень.
Feng-Juan Zhang, Ruo-Ling Han, Xin-Ming Zhao
В статті описується технологія еластографії зсувної хвилі ARFI на апараті Siemens Acuson S2000.
Мета. Вивчити значення Virtual Touch Tissue Imaging (VTI) і Virtual Touch Tissue Quantification (VTQ) в диференційній діагностиці вузлових утворень щитоподібної залози.
Методи. Сто семи хворим з 113 вузлами щитоподібної залози проводилось звичайне ультразвукове дослідження і акустична променева імпульсна візуалізація (acoustic radiation force impulse (ARFI)) еластографія. Була класифікована жорсткість вузлів при Virtual Touch Tissue Imaging (VTI), а також були обчислені співвідношення площі (СП) вузлів на зображеннях VTI порівняно із зображеннями у В-режимі. Була виміряна швидкість зсуву хвилі (ШЗХ) у вузлових утвореннях щитоподібної залози за допомогою техніки Virtual Touch Tissue Quantification (VTQ). Патологоанатомічний діагноз використовувався як золотий стандарт побудови кривої робочої характеристики приймача (receiver-operating characteristic curve (ROC)) для визначення порогових значень класів VTI, співвідношення площі і ШЗХ для прогнозування розвитку раку щитоподібної залози.
Результати. Різниця в класах VTI злоякісних і доброякісних вузлів, а також в показниках СП і ШЗХ була статистично значущою (P <0,05). Не виявлено жодних суттєвих відмінностей в СП вузлів або ШЗХ вузлів у групі доброякісних вузлів або в групі злоякісних. Була вивчена чутливість, специфічність, точність, позитивна прогностична цінність (positive predictive value (ППЦ)) та негативна прогностична цінність (negative predictive value (НПЦ)) класів VTI, співвідношення площі і ШЗХ в диференційній діагностики вузлів щитоподібної залози. Не було виявлено жодних суттєвих відмінностей в діагностичній точності серед усіх трьох методик.
Висновки. Класи VTI, СП вузлів на VTI зображеннях порівняно з подібними в B-режимі і ШЗХ в межах вузла допомагають провести диференційну діагностику вузлових утворень щитоподібної залози.
ВСТУП
Акустична променева візуалізація (Acoustic radiation force impulse (ARFI)) є новим методом еластографії, який може аналізувати жорсткість тканин якісно та кількісно. ARFI оцінює жорсткість тканини, забезпечує додатковою інформацією при традиційній ультрасонографії, таким чином потенційно покращує характеристику тканин і вогнищевих уражень. Попередня версія компресійної еластографії є напівкількісним методом оцінки жорсткості (еластичності) тканин. Дані компресійної еластографії значною мірою залежать від ступеня стиснення тканин, що застосовується, а рівень досвіду прямо пропорційний відтворюваності еластограми, у зв’язку з чим її надійність ставиться під сумнів.
В даний час, ARFI – це новітній режим візуалізації для виявлення механічних властивостей тканини без застосування зовнішнього стиснення. ARFI технологія включає в себе Virtual Touch Tissue Imaging (VTI) і Virtual Touch Tissue Quantification (VTQ). Mікрозміщення генерується в тканини в межах області, що цікавить оператора (поле зору (ПЗ)) за допомогою наявного у продажу ультразвукового датчика, який запускає в тканини короткочасні акустичні імпульси (<100 мс) високої інтенсивності. Зсув тканини залежить від її еластичності. Чим більше еластична тканина, тим більше вона піддається зміщенню. Зсув тканини всередині ПЗ, викликаного ARFI реєструють і представляють як напівтонове зображення, яке називається Virtual Touch візуалізацією тканин (VTI). Чим жорсткішою є тканина, тим темнішим – зображення. Тканини в межах ПЗ генерують горизонтальні зміщення хвилі внаслідок поширення поздовжнього імпульсу, що генерується датчиком. Швидкість зсуву хвилі розраховується і виражається в одиницях “м/с” (м/с), що називається Virtual Touch квантифікацією тканин (VTQ). Чим жорсткішою є тканина, тим швидше поширюються хвилі. Швидкість поширення хвилі є внутрішнім і відтворюваним параметром самої тканини, так що ARFI квантифікація тканини видає об’єктивні та відтворювані дані. VTQ забезпечує числові вимірювання швидкості зсуву хвилі, а сама швидкість зсуву хвилі пропорційна квадратному кореню з еластичності тканини, тому VTQ – кількісна технологія оцінки еластичності тканини.
ARFI технологія вперше була застосована в діагностиці захворювань черевної порожнини і захворювань молочної залози. Публікацій про застосування ARFI технології при захворюваннях щитоподібної залози, особливо з використанням лінійного датчика, небагато, і ця проблема, як і раніше потребує подальшого дослідження. У цих дослідженнях вивчалася різні типи зображень VTI і значення VTQ, а також порівнювалася діагностична точність між VTQ та якісною еластографією в режимі реального часу. Це дослідження присвячене визначенню класів зображень VTI, співвідношення площі (СП) вузлів на VTI і в B-режимі, а також швидкості зсуву хвилі (ШЗХ), що необхідно для оцінки ефективності вищезазаначених методів в диференційній діагностиці вузлів щитоподібної залози. Всі діагнози були підтверджені гістологічно.
МАТЕРІАЛИ І МЕТОДИ
Характеристики пацієнтів
Це дослідження було схвалено етичним комітетом Fourth Hospital – медичного університету Хебея. Між липнем 2012 і січнем 2013, 185 пацієнтів з направленням на ультразвукове дослідження були включені в це дослідження. Всі учасники підписали інформовану згоду, необхідну для включення у дослідження «Комітетом з вивчення прав людини». Сімдесят вісім з них були втрачені під час динамічного спостереження (50 пацієнтів з очевидними ознаками доброякісних вузлів надали перевагу тонкоголковій аспіраційній біопсії щорічному ультразвуковому дослідженню, а 28 – зробили операцію в інших лікарнях, у зв’язку з тим, що у них були отримані підозрілі патологоанатомічні результати). Критерії включення в дослідження пацієнтів були наступні: (1) стабільні зображення вузлів в двох площинах (2D) під час затримки дихання пацієнтами; (2) розмір вузлів в діапазоні від 0,6 до 2,0 см; (3) жорсткі або майже жорсткі (<20% кістозності) вузли при ультразвуковому дослідженні (УЗД); (4) достатньо щитоподібної тканини, навколо вузла на тій же глибині; (5) хірургічне лікування щитоподібної залози проводилося після ультразвукового дослідження. Не кожен вузол міг бути включений у дослідження для пацієнтів з множинними вузликами через обмеження розміру і характеру компонентів вузлів. У дослідженні багато пацієнтів мали множинні вузлики, але тільки один або два задовольняли критерії включення. Зрештою, 107 пацієнтів (середній вік 35,56 ± 10,34 років, діапазон 21-75 років) з 113 вузлами (середній розмір – 1,5 ± 0,3 см, діапазон 0,5-2,0 см) відповідали критеріям включення, і всі ці вузлики були видалені і отримані патологоанатомічні результати.
Техніка візуалізації
Стандартна ультрасонографія і ARFI техніка проводилася на ультразвуковій системі Acuson S2000 (Siemens Medical Solutions), оснащеної 9L4 лінійним датчиком (з частотою 4-9 МГц) і ARFI програмним забезпеченням. Пацієнти знаходилися в положенні на спині з повністю розігнутою шиєю. Морфологічні характеристики вузлів: розмір, межі, ехоструктури і ознаки на кольоровому доплері були оцінені за допомогою звичайної стандартної ультрасонографії. При переході на VTI техніку датчик злегка торкався шкіри, регулювався розмір ПЗ для того, щоб переконатися, що вузол і достатня кількість навколишньої тканини залози були включені в ПЗ. Максимальний подовжній перетин вузлів відображали в центрі екрану, а потім просили пацієнтів затримати дихання, одночасно натискали на кнопку оновлення. Потім VTI зображення, що відповідало зображенню в В-режимі з’являлося в правій частині екрана. Дослідження виконувалося п’ять разів поспіль і вибиралося три зображення з найбільш чіткою межею, котрі і зберігалися як дослідні дані. Були виміряні площі вузла на VTI і на B-режимі сонографії. Площа вузла щитоподібної залози на VTI була обрана в якості А1, а відповідна ділянка в B-режимі сонографії – як A2, таким чином обчислювали співвідношення площі (СП). Середнє значення трьох вимірів співвідношення площі кожного вузлика використовувалося для подальшого статистичного аналізу. Всі ультразвукові дослідження були проведені експертами з більш ніж десятирічним досвідом в звичайному ультразвуковому дослідженні і трьохрічним досвідом роботи з ARFI, всі вони не знали гістопатологічних результатів.
Відповідно до класифікації VTI методу Tian та ін., VTI зображення вузлових утворень щитоподібної залози розділили на чотири класи згідно сірої шкали:
-
клас I: зображення білі або білі за типом бджолиних стільників;
-
клас II: зображення були сірі або світло-сірі, схожі на навколишні тканини;
-
клас III: зображення були темно-сірі або з невеликою кількістю білих точок, які дуже відрізнялися від навколишніх тканин;
-
клас IV: зображення були абсолютно чорного кольору.
Чим жорсткіше тканини, тим темніше зображення.
У режимі VTQ поле зору (ПЗ) з фіксованою роздільною здатністю 6 мм × 5 мм було розміщено всередині вузлів, коли вузли були того ж розміру, що й ПЗ. Вузли вимірювалися п’ять разів, потім розраховувалася середня величина п’яти вимірювань, що і використовувалося для подальшого аналізу. Діапазон руху ПЗ у вузлі був незначний, коли розмір вузла був близький до такого у ПЗ. Відтворюваність п’яти вимірювань була дуже високою, а результати мали високу узгодженість. Діапазон руху ПЗ був більшим в більшому за розміром вузлі. Тканина може мати зовсім різні значення при дослідженні, тому дані вимірювання можуть не відповідати один одному. Таким чином, великі вузли були розділені на чотири частини, кожна частина була виміряна двічі, середнє з восьми вимірів було більш надійним показником для великих вузлів, ніж середня величина їх п’ятикратного вимірювання. Діапазон вимірювань значень VTQ (швидкості зсуву хвилі) для цього ультразвукового устаткування – 0-9 м/с. Значення поза цим діапазоном були представлені як “X.XX м/с”, а також результати реєструвалися як 9 м/с, коли вузол був абсолютно твердим.
Патологоанатомічний діагноз
Операція (резекція вузла щитоподібної залози) була проведена для всіх пацієнтів, включених у це дослідження. Природа всіх вузлів була підтверджена гістологічно. Всі патологоанатомічні діагнози були зроблені патологоанатомом з багаторічним досвідом в дослідження патології щитоподібної залози. Вузли були в першу чергу класифіковані як доброякісні або злоякісні, а потім вони були розділені на дві підгрупи, як описано в таблиці 1.
Таблиця 1. Кількість доброякісних і злоякісних вузлів щитоподібної залози при Virtual Touch візуалізації тканин
|
Патогістологічні результати |
Кількість при Virtual Touch візуалізації тканин |
|||
|
I (n) |
II (n) |
III (n) |
IV (n) |
|
|
Вузли з аденоматозною гіперплазією |
22 |
31 |
4 |
3 |
|
Аденома |
3 |
4 |
0 |
0 |
|
Папілярний рак |
0 |
1 |
27 |
6 |
|
Папілярна аденокарцинома фолікулярного типу |
0 |
1 |
4 |
5 |
|
Медулярна карцинома |
0 |
0 |
2 |
0 |
Статистичний аналіз
Оцінка співвідношення площі і VTQ мала ненормальний розподіл, тому вони виражалися як середнє значення. Співвідношення площі і ШЗХ були різні між доброякісною групою і злоякісної групою. Був також проведений порівняльний аналіз всередині доброякісної групи, а також всередині злоякісної, а оцінка класів VTI була виконана з використанням непараметричного U-теста Манна-Уїтні. Непараметричний критерій Крускала-Уолліса був використаний для визначення значущої різниці в СП або ШЗХ серед різних патологічних типів злоякісних вузлів. Була оцінена ефективність класів VTI, значення співвідношення площі і значення VTQ (ШЗХ) в диференційній діагностиці злоякісних вузлів від доброякісних за допомогою аналізу кривої помилок (характеристичної кривої), або ROC-аналізу (receiver operating characteristic). Кращі порогові значення для класів VTI, співвідношення площі і показників VTQ були отримані при використанні індексу Youden (чутливість + специфічність – 1) з даних ROC-аналізу. Чутливість, специфічність, точність, позитивна прогностична цінність (ППЦ) і негативна прогностична цінність (НПЦ) були розраховані за допомогою тесту хі-квадрат (χ2-тест). Р значення <0,05 вважалося статистично значущим. Наведені вище дані були проаналізовані за допомогою статистичної програми (SPSS для Microsoft Windows, версії 13.0).
РЕЗУЛЬТАТИ
Гістологія
Патогістологічні результати виявили 46 з 113 (40.71%) злоякісних вузлів (34 папілярних карцином, 10 папілярних аденокарцином фолікулярного типу, 2 мозкових карцином) і 67 з 113 (59,29%) доброякісних вузлів (60 – вузли з аденоматозною гіперплазією, 7 аденом) (Таблиця 1).
Розподіл класів VTI
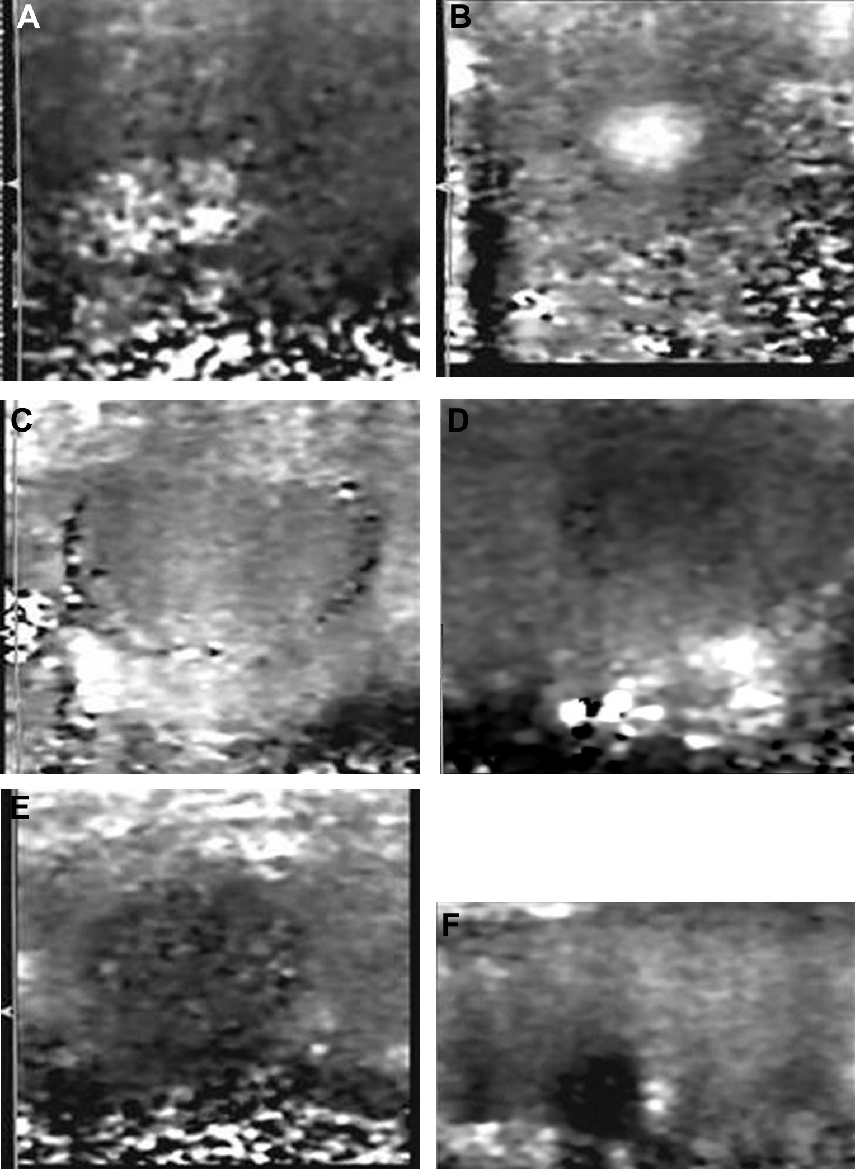
Зображення доброякісних вузлових утворень щитоподібної залози на VTI в основному були I класу (зображення були по типу білих стільників (Рис. 1 А)) або повністю білі (Рис. 1 В), або II класу (зображення були світло-сірими (Рис. 1 В), або сірими (Рис. 1 D), так само, як навколишні тканин). Зображення злоякісних вузлів щитоподібної залози на VTI в основному були III класу (темно-сірі або з невеликою кількістю білих точок, які значно відрізняються від навколишніх тканин (Рис. 1 E)), або IV класу (зображення були чорними (Рис. 1 F)).
Рис. 1. Класи Virtual Touch візуалізації тканин: (A) вузол за типом аденоматозної гіперплазії відображається у вигляді білих стільників (Клас I); (B) чисто білий вузол за типом аденоматозної гіперплазії (Клас I); (C) Аденома щитоподібної залози відображається світло-сірим кольором (клас II); (D) вузол за типом аденоматозної гіперплазії відображається сірим кольором (клас II); (Е) Папілярна карцинома щитоподібної залози – темно-сірого кольору з невеликою кількістю білих крапок (клас III); (F) Папілярний рак щитоподібної залози – абсолютно чорного кольору (клас IV).
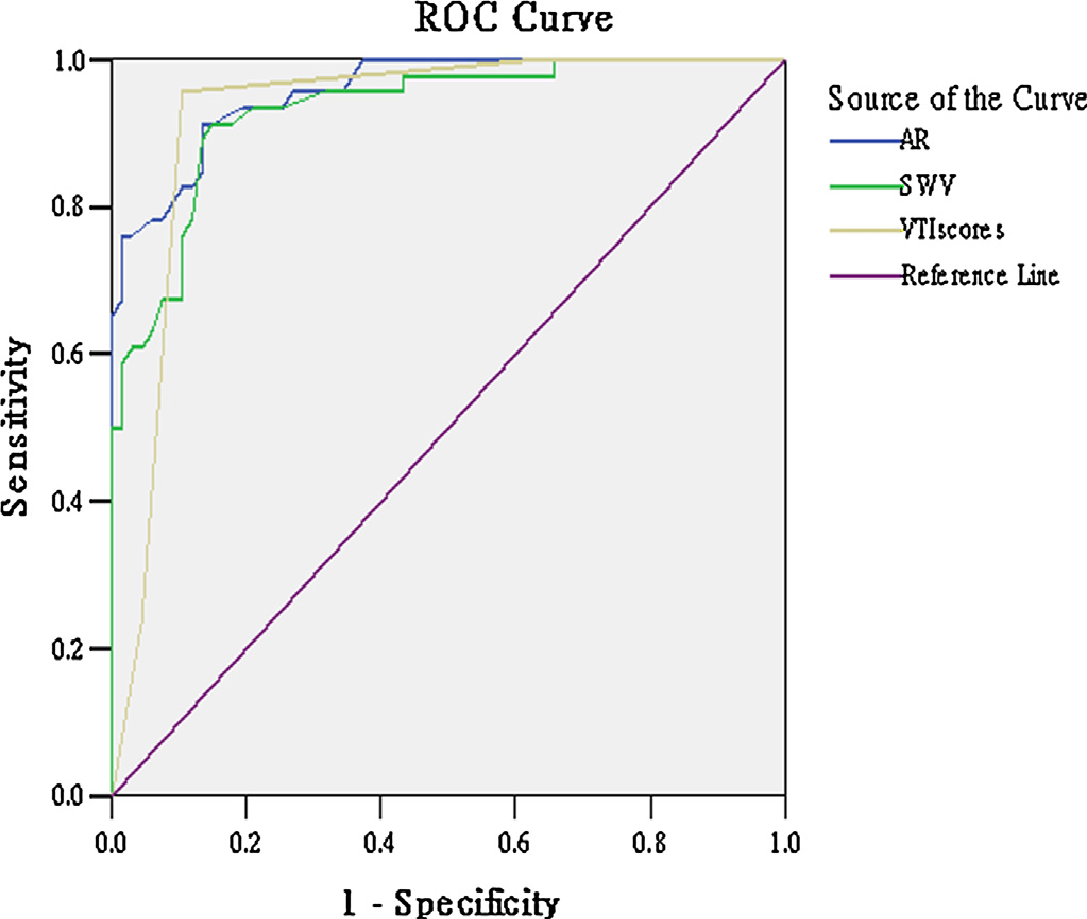
60 доброякісних вузлів при VTI (60 з 67) мали клас менший ніж III, і 44 злоякісних вузлів (44 з 46) мали клас більший або рівний III. Різниця в класі VTI злоякісних і доброякісних вузлів була статистично значущою (P <0,05; Таблиця 2). Якщо прийняти значення більше або рівне III класу в якості діагностичного стандарту злоякісного утворення, то чутливість, специфічність, точність, ППЦ, і НПЦ буде 95.65 (44/46), 89,55 (60/67), 92,04 (104 / 113), 86,27 (44/51) і 96,77% (60/62) відповідно (Рис. 2, Таблиця 2).
Рис. 2. Характеристичні криві (ROC-криві) для класів Virtual Touch візуалізації тканин, співвідношення площі і швидкості зсуву хвилі.
Таблиця 2. Чутливість, специфічність, точність, ППЦ і НПЦ VTI класів, СП і VTQ в диференційній діагностики вузлів щитоподібної залози.
|
Метод |
Порогові значення |
Чутливість (%) |
Специфічність (%) |
Точність (%) |
ППЦ (%) |
НПЦ (%) |
|
VTI клас |
III |
95,7 |
89,6 |
92,04 |
86,27 |
96,77 |
|
VTI СП |
1,08 |
91,3 |
89,6 |
88,5 |
82,35 |
93,55 |
|
VTQ ШЗХ |
2,9 |
91,3 |
85,1 |
87,61 |
80,77 |
93,44 |
Співвідношення площі доброякісних і злоякісних вузлів
Вимірювання СП доброякісних і злоякісних вузлів показано в таблиці 3.
Таблиця 3. Співвідношення площі характеристик доброякісних і злоякісних вузлів щитоподібної залози
|
Патологічні типи |
Співвідношення площі |
|||
|
Середнє ± стандартне відхилення |
Медіана |
Мінімум |
Максимум |
|
|
Доброякісні вузли |
0,97 ± 0,11 |
0,96 |
0,70 |
1,25 |
|
Вузли з аденоматозною гіперплазією |
0,98 ± 0,11 |
0,96 |
0,70 |
1,25 |
|
Аденома |
0,94 ± 0,09 |
0,97 |
0,78 |
1,04 |
|
Злоякісні вузли |
1,46 ± 0.36 |
1.39 |
1.00 |
2.62 |
|
Папілярний рак |
1,46 ± 0,39 |
1,39 |
1,00 |
2,62 |
|
Папілярна аденокарцинома фолікулярного типу |
1,36 ± 0,23 |
1,38 |
1,00 |
1,75 |
|
Медулярна карцинома |
1,68 ± 0,45 |
1,68 |
1,36 |
2,00 |
P – значення: P = 0,000 між злоякісними і доброякісними вузлами; P = 0,637 між аденоматозною гіперплазією вузлів і аденомою; P = 0,601 між папілярним раком, папілярною аденокарциномою фолікулярного типу та медулярним раком.
Не було ніяких істотних відмінностей в середньому значенні між аденоматозною гіперплазією вузлів і аденомами в групі доброякісних процесів і між папілярними карциномами, папілярними аденокарциномами фолікулярного типу та медулярним раком в групі злоякісних захворювань. Медіана співвідношення площі злоякісних вузлів була вищою, ніж в доброякісних утвореннях (1,39 проти 0,96, P <0,001). Площа під ROC-кривою (area under ROC curve (AUROC)) для співвідношення площі вузлових утворень щитоподібної залози для діагностики злоякісних вузлів – 0,957. Порогове значення співвідношення площі злоякісних вузлів – 1,08. Використання ROC-кривої з цим граничним значенням, чутливість, специфічність, точність, ППЦ і НПЦ показника співвідношення площі для діагностики злоякісних вузлів були наступними: 91,30 (42/46), 86,60 (58/67), 88,50 (100 / 113), 82,35 (42/51) і 93,55% (58/62) відповідно (Рис. 2, Таблиця 2).
Швидкість зсуву хвилі доброякісних і злоякісних вузлів
Вимірювання ШЗХ доброякісних і злоякісних вузлів наведені у таблиці 4.
Таблиця 4. ШЗХ доброякісних і злоякісних вузлів щитоподібної залози
|
Патологічні типи |
Співвідношення площі |
|||
|
Середнє ± стандартне відхилення |
Медіана |
Мінімум |
Максимум |
|
|
Доброякісні вузли |
2.37 ± 0.74 |
2.34 |
1.00 |
5.50 |
|
Вузли з аденоматозною гіперплазією |
2.37 ± 0.76 |
2.35 |
1.00 |
5.50 |
|
Аденома |
2.34 ± 0.58 |
2.15 |
1.75 |
3.50 |
|
Злоякісні вузли |
6.20 ± 2.84 |
6.65 |
2.08 |
9.00 |
|
Папілярний рак |
6.18 ± 2.91 |
6.90 |
2.08 |
9.00 |
|
Папілярна аденокарцинома фолікулярного типу |
6.32 ± 2.89 |
7.15 |
3.20 |
9.00 |
|
Медулярна карцинома |
6.00 ± 2.83 |
6.00 |
4.00 |
8.00 |
P-значення: P = 0,000 між злоякісними і доброякісними вузлами; P = 0,830 між аденоматозною гіперплазією вузлів і аденомою; P = 0,974 між папілярним раком, папілярною аденокарциномою фолікулярного типу та медулярним раком.
Не було ніяких істотних відмінностей в медіані ШЗХ між аденоматозною гіперплазією вузлів і аденомами в групі доброякісних процесів і між папілярними карциномами, папілярними аденокарциномами фолікулярного типу та медулярним раком в групі злоякісних захворювань. Медіана ШЗХ злоякісних вузлів була вищою, ніж доброякісних вузлів (6,65 м / с в порівнянні з 2,34 м / с, P <0,001). Кращим пороговим значенням для ШЗХ було 2,9 м / с. Використання ROC-кривої з цим граничним значенням, ШЗХ прогнозувала малігнізацію з чутливістю 91,30 (42/46), специфічністю 85,10% (57/67), точністю 87.61% (99/113), ППЦ 80,77% (42 / 52), НПЦ 93,44% (57/61) і видавало значення AUROC – 0,932 (Рис. 2, таблиця 2).
Не було ніякого істотного розходження в діагностичній ефективності між класом VTI, показниками співвідношення площі і ШЗХ (P = 0,521).
ОБГОВОРЕННЯ
Частота вузлових утворень щитоподібної залози значно зросла в останні роки через забруднення навколишнього середовища, особливостей їжі і генетичних факторів. Особливо це стосується раку щитоподібної залози, який збільшився з 3,6 на 100 тисяч в 1973 році до 8,7 на 100 000 в 2002 р.. Глобальна захворюваність на рак щитоподібної залози також збільшується на 4% на рік і займає восьме місце серед найпоширеніших пухлин у жінок. Тому рання діагностика доброякісних і злоякісних вузлів щитоподібної залози особливо важлива. Ультразвуковий метод є кращим для діагностики вузлів щитоподібної залози, тому що він неінвазивний, має низьку вартість, точний, легко відтворюваний. Оскільки китайські дослідники приділяють більше уваги фізикальному обстеженню, в останні роки було виявлено багато випадків типових форм раку щитоподібної залози та проведена їх хірургічна резекція. В даний час, все більше і більше випадків раку щитоподібної залози з ультразвуковою картиною доброякісних вузлів виявляється за допомогою ультразвуку. Одне і те ж зображення може бути при різній патології, одна і та ж патологія може мати різне візуальне відображення, що ще більше збільшує число помилкових діагнозів при вузлах щитоподібної залози.
Жорсткість пухлин певною мірою може відображати їх характер. Чим жорсткіше тканини, тим вищий ризик злоякісного переродження. Як правило, злоякісні вузлики щитоподібної залози мають тенденцію бути жорсткішими, ніж доброякісні. Жорсткість вузлів зазвичай визначається шляхом пальпації самим лікарем, але вузли меншого розміру, особливо глибокі, не можуть бути пропальповані. Допоміжний метод компресійної еластографії – напівкількісний метод оцінки еластичності тканин, який використовується клінічно. При його використанні були отримані перспективні результати для диференційної діагностики вузлів щитоподібної залози. Але існують деякі суб’єктивні фактори, які можуть вплинути на результати: досвід і сила стиснення тканин, яка застосовується дослідником. Ці навички впливають на відтворюваність результатів еластографії. Це дослідження розглядає передовий метод візуалізації – ARFI еластографію, яка не залежить від досвіду виконавця і правильної вібрації або стиснення тканини. ARFI надає кількісну та якісну інформацію про еластичність тканин об’єктивним і простим способом.
Технологія VTI проста в експлуатації і отримані зображення легко відтворюються. Дослідники завжди будуть отримувати однакові зображення, незалежно від їх досвіду роботи. Хоча не існує конкретного значення у відтінках сірого, легко класифікувати зображення щитоподібної залози на VTI на чотири класи, які помітні неозброєним оком. Здатність класифікації зображення не вимагає спеціальної підготовки. 95,65% (44/46) злоякісних вузлів щитоподібної залози в цьому дослідженні були III-IV класу VTI і це свідчило про те, що злоякісні вузлики є жорсткішими. 89,55% (60/67) доброякісних вузлів щитоподібної залози були I-II класу VTI і це вказувало на те, що доброякісні вузлики були м’якішими. Ці результати свідчать про те, що жорсткість тканини, виявлена при VTI може чудово відображати природу вузла.
Тільки два злоякісних вузла показали зменшення величини класу жорсткості: один з них – мікрофокальна папілярна аденокарцинома фолікулярного типу. При цьому VTI вузол мав світло-сірий колір (клас II, Рис. 3).
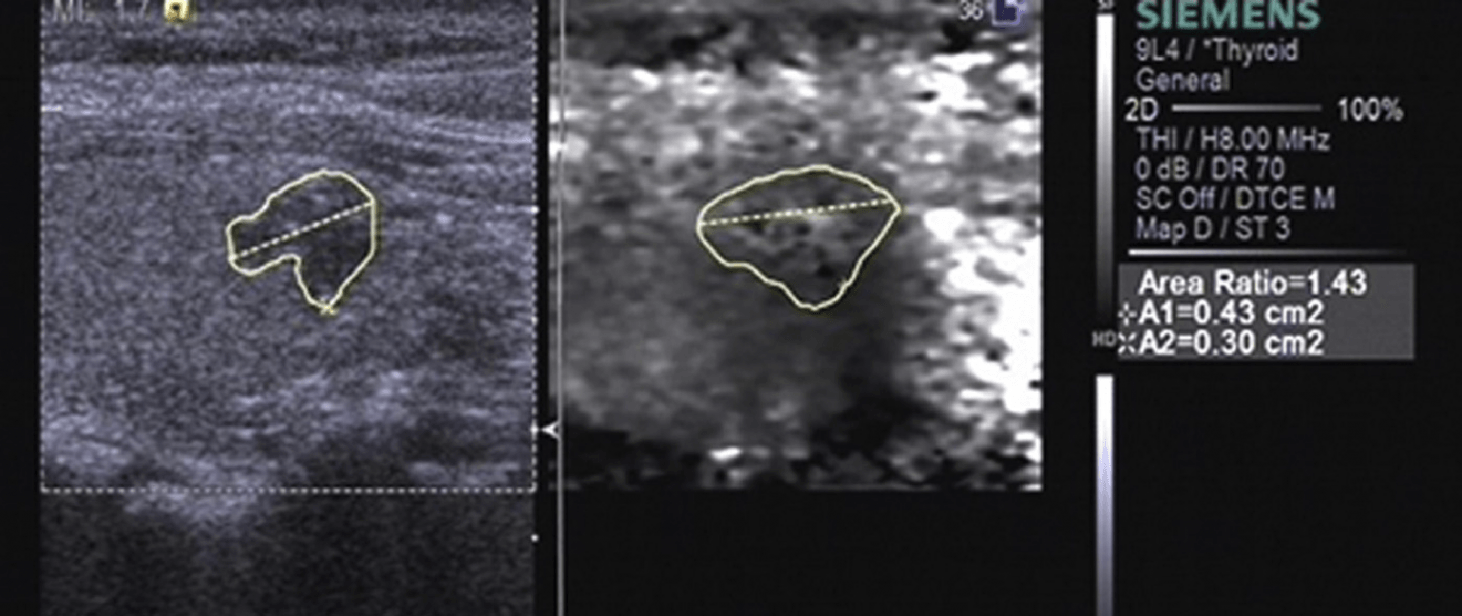
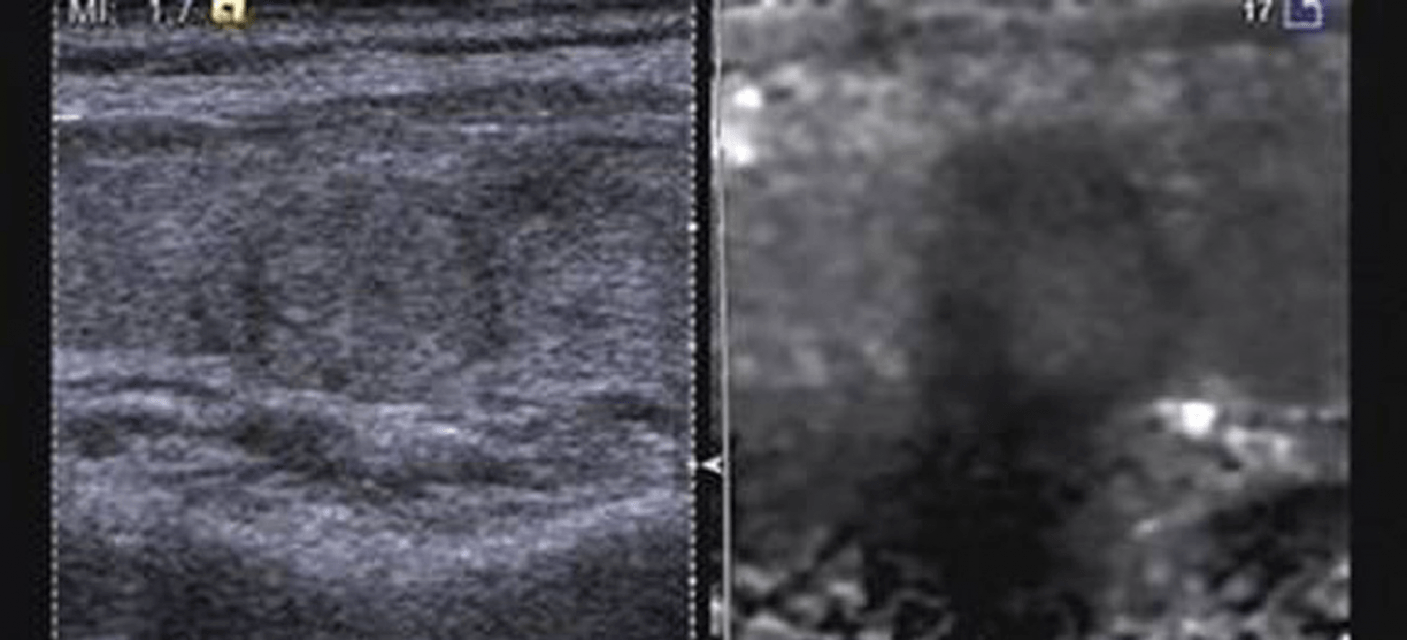
Рис. 3. Acoustic radiation force impulse (ARFI) зображення мікрофокальної папілярної аденокарциноми фолікулярного типу. При дослідженні вузла в B-режимі показаний неправильний гіпоехогенний вузол (ліворуч). Зображення тканини при VTI показало, що вузол має світло-сірий колір (клас II), який був помилково діагностований як доброякісний, але при цьому дослідженні він мав більший показник співвідношення площ (праворуч).
При іншій нетиповій аденомі зі злоякісним переродженням, VTI показала, що внутрішня основна частина вузла була білою, і тільки її край був чорного кольору, при цьому зображення було класифіковано, як клас II (Рис. 4).
Рис. 4. VTI зображення нетипової аденоми зі злоякісним переродженням. B-режим зображення – ехогенність вузла однорідна, але капсула має переривчастий контур (ліворуч). VTI показує світло-сірий вузол з чорними лініями по краю (клас II, праворуч), цей вузол був помилково діагностовано, як доброякісний.
У випадку розвитку фокального раку у вузлі, наприклад, мінімальний рак або локальне злоякісне переродження доброякісного вузла, основна маса вузла залишається доброякісною і VTI зображення доброякісної основної частини легко перекриває місце локального злоякісного переродження і, отже, це призводить до постановки помилкового діагнозу. Сім доброякісних вузлів у цьому дослідженні показали вищий клас еластичності: два аденоматозних гіперпластичних вузла (Рис. 5), два аденоматозних гіперпластичних вузла з еозинофільними змінами та три аденоматозних гіперпластичних вузла з кальцифікацією (Рис. 6).Жорсткість доброякісних вузлових утворень збільшувалася помітно, коли розвивався некроз, фіброз, гіалінізація і кальцифікація. Ці зміни додають клас еластичності при VTI і обумовлюють постановку помилкового діагнозу.
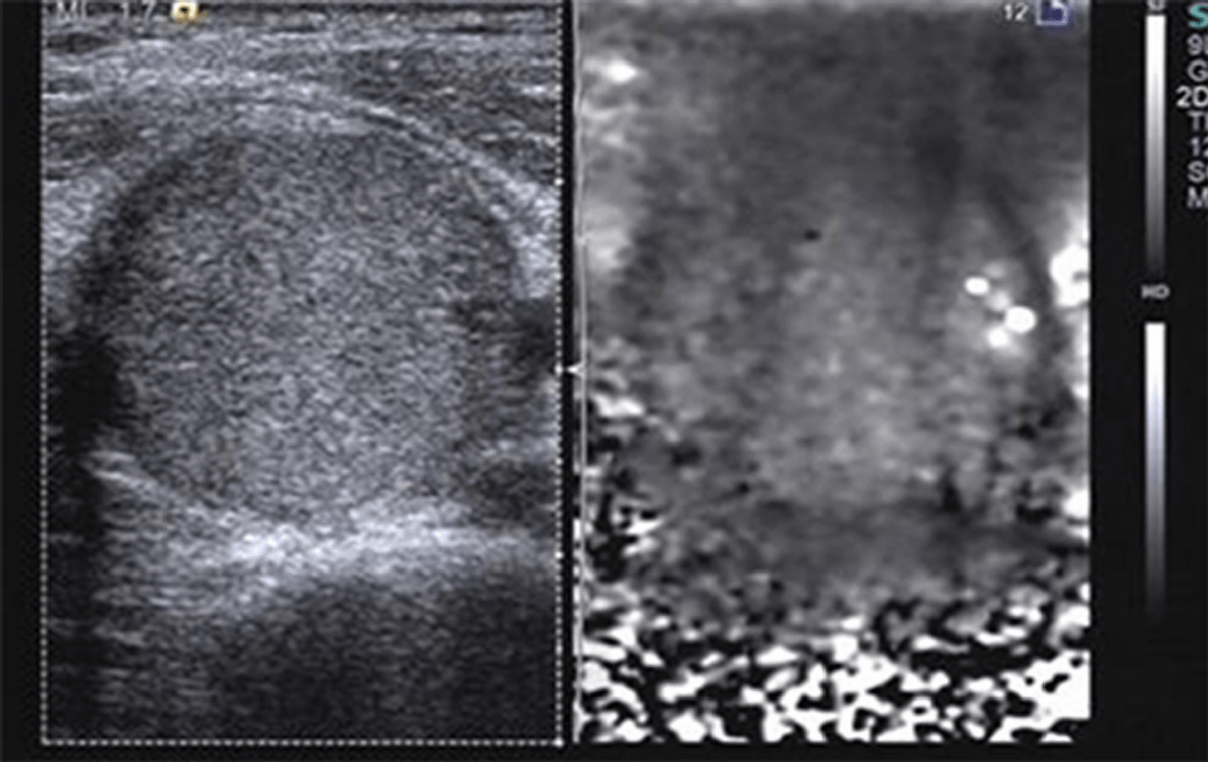
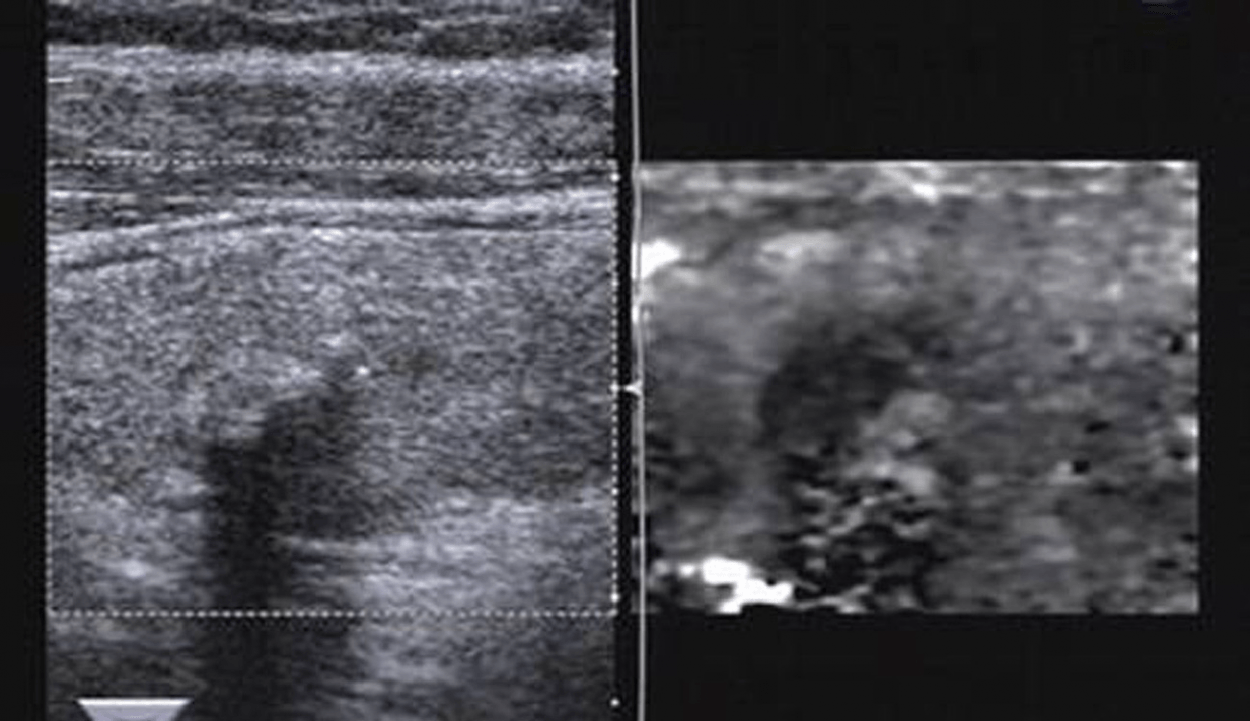
Рис. 5. VTI зображення аденоматозної гіперплазії вузла. B-режим зображення показав вузол з однорідним ехосигналом правильної форми (ліворуч). VTI показала світло-сірий колір в центрі вузла і темно-сірий – на периферії (клас III, праворуч), який був помилково діагностований як злоякісний.
Рис. 6. VTI зображення аденоматозної гіперплазії вузла з кальцифікацією. B-режим зображення показує множинну кальцифікацію (ліворуч). При VTI виявлено, що кальцифікована частина має темно-сірий колір (клас III, праворуч).
СП 78,26% (36/46) злоякісних вузлів була більшою або дорівнювала 1,19, в той час як тільки 16,41% (11/67) доброякісних вузлів мали подібні параметри. Таким чином, СП показує очевидні відмінності між злоякісними і доброякісними вузлами. Більшість доброякісних вузлів були білими або світло-сірими, особливо при розвитку множинних голчастих дрібних кістозних змін у внутрішній частині вузлів, в цьому випадку зображення мали вигляд білих бджолиних стільників, при цьому на VTI не визначалося чіткої межі між вузлами та оточуючими тканинами. Співвідношення площі вузлів часто було менше, ніж 1, при виборі контурів вузлів відповідно до білої межі. На VTI навколо вузла визначалися чіткі чорні ореоли в тому випадку, коли розвивався множинний фіброз у вузлах і формувалася потовщена псевдокапсула навколо вузла (Рис. 5). Співвідношення площі цих доброякісних вузлів часто була більшим або дорівнювало 1 (при виборі контурів вузлів відповідно до чорного ореолу). СП 78,26% (36/46) злоякісних вузлів ≥ 1,19; 95,65% (44/46) ≥ 1. СП тільки двох злоякісних вузлів було меншим 1 і, відповідно, було 0, 94 і 0.97.
Площі більшості злоякісних вузлів на VTI були більшими, ніж доброякісних, що пов’язано з характером росту злоякісної пухлини. Пухлинні клітини проникають в навколишні тканини нерівномірно і, отже, злоякісні вузли часто мають нечіткі межі. Атипова потенційна інфільтрація часто не виводиться при стандартному ультразвуковому дослідженні, але проявляється на VTI, тому що вона, як правило, є жорсткішою, ніж периферичні тканини. Це пояснює той феномен, що злоякісне ураження має більший об’єм на VTI, ніж на відповідному B-режимі ультразвукового дослідження. Два злоякісних вузла правильної форми і з чіткими межами мали маленький розмір, при патогістологічному дослідженні було підтверджено діагноз мікрофокальної карциноми. Розміри цих двох вузлів на VTI були аналогічні розмірам в B-режимі. Основною причиною цього може бути те, що ці два вузли не мали жодних очевидних ознак інфільтративного росту в периферичні тканини.
У нашому дослідженні ми виявили, що медіана ШЗХ злоякісних вузлових утворень щитоподібної залози була значно вищою, ніж доброякісних вузлів. Ці результати узгоджуються з патологоанатомічною характеристикою доброякісних і злоякісних вузлів. Гіперпластичні вузлики щитоподібної залози й аденоми, як правило, складаються з гомогенних фолікулів, які наповнені колоїдом. Таким чином, вони, як правило, є м’якішими і мають більш низький показник ШЗХ. Але коли мають місце такі дегенеративні процеси, як: некроз, гіалінізація і кальцифікація в доброякісних вузла, їх жорсткість значно збільшується. Також, відповідно, збільшиться і ШЗХ. Папілярна карцинома щитоподібної залози, як правило, має ознаки фіброзу, кальцифікації і псамозні тіла в мезенхімі. Згідно злоякісного типу зростання, папілярний рак часто має погано окреслені межі, інфільтрує периферичні тканини і має слабку рухливість. При проведенні даного дослідження в двох вузлах медулярної карциноми щитоподібної залози були виявлені очевидні кальциновані бляшки. Ці патологічні ознаки сприяють розвитку більш високої жорсткості і більш високої ШЗХ в карциномі щитоподібної залози.
Тонкоголкова аспіраційна (FNA) біопсія є кращим нехірургічним методом диференційної діагностики злоякісних вузлів, але використання цього методу призводить до певної частоти хибно-негативних і хибно-позитивних результатів, і, більше того, FNA дає неадекватні зразки для дослідження в 10-20% процедур. Коротко кажучи, FNA є інвазивною процедурою, що може призвести до помилок вибірки, забирає багато часу та економічних ресурсів, а також пов’язана з незначними ускладненнями. Таким чином, FNA біопсія вузлів щитоподібної залози не користується популярністю в нашій лікарні. Пацієнти, які мають рак щитоподібної залози або підозрілі вузли вибирають хірургічну резекцію замість біопсії. Пацієнти з типовими доброякісними ознаками при ультразвуковому дослідженні неохоче погоджуються на біопсію, надаючи перевагу динамічному спостереженню. Оскільки ці пацієнти не мали результатів FNA, вони були виключені з дослідження. Таким чином, всі пацієнти, включені в дослідження, були прооперовані. Деякі доброякісні вузли в цьому дослідженні були видалені у зв’язку з співіснуючим раком щитоподібної залози, підозрілих вузлів або співіснуючих великих доброякісних вузлів, що викликають симптоми здавлення. Ці причини могли привести до високого відсотку захворюваності на рак щитоподібної залози в даному дослідженні. Таким чином, ця вибірка не може бути репрезентативною, а результати не можуть бути застосовні для західних країн.
Наше дослідження має деякі обмеження. Фіксований розмір і форма ПЗ VTQ впливали на розміщення ПЗ. Занадто великі або занадто маленькі вузлики були виключені з цього дослідження, оскільки VTQ-ПЗ вимірює площу 6 × 5 мм, а ширина VTI була 2,6 см. Для великих вузлів є потреба у вимірі в декількох позиціях для отримання середнього значення. Іноді рідинна частина вузла або навколишніх тканин неминуче була включена в ПЗ за рахунок фіксованої форми VTQ-ПЗ.VTQ-ПЗ буде включати в себе навколишню тканину залози, якщо розмір вузла є меншим 0,6 см. Ці умови можуть вплинути на точність VTQ. Багато злоякісних вузлів не можуть бути оцінені кількісно, якщо значення перевищує верхню межу детекції 9 м / с. Необхідна оптимізація програмного забезпечення підвищення виявлення швидкості для показників, що перевищують 9 м / с для того, щоб подолати це обмеження. Максимальна ширина VTI-ПЗ була 2,6 см, тому ми рекомендуємо верхню межу 2,0 см для вузла, тому що в ПЗ необхідно включати достатньо нормальної тканини залози, навколишнього вузла. VTI методика не ефективна, коли розмір вузла є занадто великим для відображення на VTI, або коли мало навколишніх тканин. Вузлики зі змішаною ехогенністю і з кістозним компонентом (> 20%) були виключені з дослідження, осківльки поперечні хвилі не поширюються в нев’язкій рідині, а реакція рідкого компонента на швидкість зсуву хвилі твердого компонента ще не визначена. Таким чином, результати цього дослідження не можуть робити які-небудь висновки про значення швидкості зсуву хвилі для переважно кістозних вузлів щитоподібної залози. Не кожен вузол міг бути включений у дослідження, а саме: пацієнти з множинними вузлами через обмеження розміру і компонентів вузла. Папілярні аденокарциноми і гіперпластичні вузли були головними патологічними типами, при цьому інші патологічні типи були рідкісними спостереженнями. Необхідні додаткові дослідження з великою різноманітністю злоякісних вузлів і більшою вибіркою для визначення значення ARFI для характеристики різних патологічних типів раку щитоподібної залози. Застосування FNA для вузлових утворень щитоподібної залози не поширене в нашій лікарні, і цей метод вимагає більш інтенсивного розвитку.
ВИСНОВКИ
У підсумку, наша попередня робота показала, що VTQ може забезпечити кількісний вимір еластичності; VTI класифікація забезпечує напівкількісний аналіз еластичності; співвідношення площ вузла на VTI і в B-режимі може показати ступінь інвазії злоякісної пухлини, що може відігравати важливу роль в диференційній діагностиці злоякісних і доброякісних вузлів щитоподібної залози. Тим не менш, ця вибірка не може бути репрезентативною для скринінгу населення. Тому необхідно проведення більш проспективного вивчення населення без хірургічного втручання, з більшою кількістю вибірки і більшої варіацією патології. Необхідно порівняння з іншими подібними еластографічними методами для оцінки справжнього потенціалу кількісної еластографії в диференційній діагностиці вузлів щитоподібної залози.












14.10.2019
Юрий