Автори: Jia Zhan, Hong Ding
Вступ
- УЗД з контрастним посиленням (CEUS) вважається ефективним методом оцінки мікроваскулярізаціі, що важливо, оскільки ангіогенез є основою зростання пухлини.
- Параметри CEUS допомагають характеризувати ураження і оцінювати ангіогенез пухлини.
- CEUS був вперше використаний при діагностиці вогнищевих уражень печінки, і міжнародні керівні принципи УЗД рекомендують CEUS як метод вибору при дослідженні вогнищевих уражень печінки, якщо B-режим і доплерографія непереконливі.
- Згодом CEUS був додатково застосований для дослідження нирок, простати, молочних залоз і яєчок.
Вузли щитовидної залози (ЩЗ) є поширеним явищем серед населення в цілому, і їх частота виявлення збільшується з широким використанням УЗД. Більшість вузлів щитовидної залози доброякісні, і менше 5% є злоякісними. В останнє десятиліття CEUS для захворювань, пов’язаних з щитовидною залозою, значно покращилися завдяки розробці більш сучасного УЗ-обладнання та впровадження контрастних агентів другого покоління (SonoVue, Bracco Imaging, Мілан, Італія). SonoVue складається з мікропухирців гексафториду сірки (2-10 мкм); він вводиться внутрішньовенно у вигляді невеликого болюса. Мікропухирці залишаються в кровотоці протягом деякого часу, протягом якого ультразвукова система фокусується на області інтересу (ОІ). Коли мікропухирці в кровотоці проходять повз вікна візуалізації, вони відображають унікальне ехо, яке контрастує з навколишньою тканиною через невідповідність декількох порядків між ехогенністю мікропухирців і тканини. Ультразвуковий пристрій перетворює зразки сильної ехогенності в контрастне зображення області інтересу. Таким чином, ехо кровотоку посилюється, що дозволяє динамічно виявляти мікросудини.
CEUS дослідження вузлів щитовидної залози
Більшість CEUS проводили для вузлів щитовидної залози у відповідності з наступними критеріями:
- гістопатологічно підтверджені вузли щитовидної залози (хірургічне втручання або біопсія),
- тверді або майже тверді (<25% кістозні) вузлики на звичайних УЗД,
- вузли щитовидної залози із злоякісними тенденціями (наприклад, система звітів і зображень щитовидної залози [TI-RADS], категорія 4 в звичайних УЗД),
- вузли діаметром більше 0,5 см.
Загальними критеріями виключення є:
- вузлики з грубою кальцифікацією,
- переважно кістозні вузлики,
- діаметр вузликів <5 мм,
- вагітність.
Загальний процес CEUS для вузлів щитовидної залози полягає в наступному. До переходу зі звичайного режиму УЗД в CEUS вибирається найбільший кут огляду вузлів. Зона фокусування завжди розташовується на нижньому рівні вузла, а CEUS виконується з використанням низького механічного індексу (MИ) (<0,10). SonoVue вводиться внутрішньовенно у вигляді болюса в дозі від 1,2 до 4,8 мл з наступним 5-мл промиванням фізіологічним розчином. Запускається таймер і зображення, отримані протягом наступних 2-3 хвилин, зберігаються в цифровому вигляді як необроблені дані.
Діагноз вузлових утворень щитовидної залози включає як якісний аналіз, так і кількісний. Включаючи ступінь посилення (тобто ізо-. гіпо-, або гіперчутливість) вузлика щитовидної залози визначають як пікову інтенсивність, що перевищує, рівну або меншу, ніж перинодулярна тканина, відповідно. Гомогенні ураження визначаються як ураження, при яких повне ураження демонструє повне посилення, незалежно від ступеня посилення, тоді як гетерогенні ураження являють собою посилені ураження, які містять ділянки без будь-якого посилення. Під «вимиванням» розуміється посилення, яке з’являється або зникає раніше, одночасно або пізніше, ніж перинодулярна тканина, відповідно. Кільцеве посилення визначається як розширений край тканини, який з’являється в ранній фазі і стає більш виразним в пізній фазі.
Під час кількісного аналізу лікар вручну малює ОІ, що підлягає дослідженню, і автоматично створюється колірна карта з допомогою вбудованого пакету аналізу або за допомогою програмного забезпечення для кількісного визначення. Потім на кольоровій карті всередині утворення малюються додаткові і менші області інтересу аналогічного розміру, і автоматично розраховуються такі кількісні параметри:
- пікова інтенсивність,
- максимальна інтенсивність кривої час-інтенсивність,
- час до піку,
- час, необхідний для досягнення максимальної інтенсивності,
- середній час проходження,
- часу, за яке інтенсивність перевищує середнє значення,
- площі під кривою час-інтенсивність, пропорційної загальному обсягу крові в області інтересу і сумі площ омивання.
Характеристика патернів CEUS для злоякісних вузлів щитовидної залози
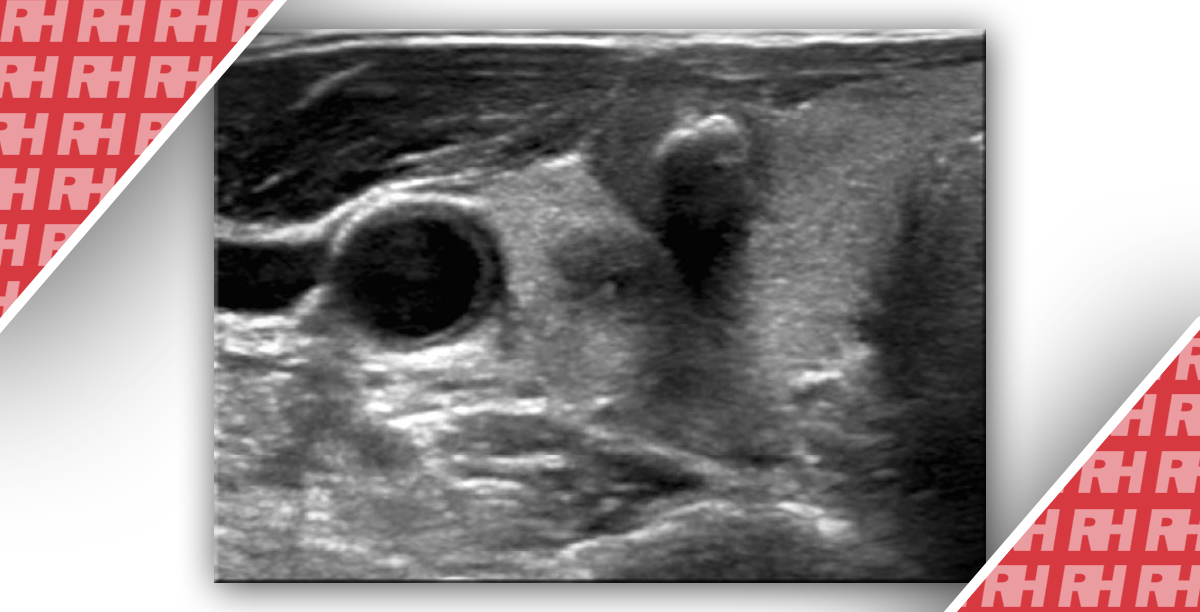
Вважається, що гіпопосилення є основною картиною CEUS, характерною для злоякісних вузлів щитовидної залози (зобр. 1), особливо для пухлин щитовидної залози діаметром 10 мм або менше. Це відкриття суперечить здоровому глузду, тому що злоякісні пухлини в інших органах добре забезпечуються кровоносними судинами. Підвищення частоти розвитку злоякісних вузлів щитовидної залози в деяких дослідженнях також називають «відсутнім» патерном. Основна причина того, що злоякісні пухлини щитовидної залози демонструють брак кровопостачання, полягає в тому, що пухлини ростуть зі складною неоваскуляризацією всередині; як тільки зростання переважає неоваскуляризації, в пухлини відбувається некроз і утворення емболії, що в кінцевому підсумку призводить до гіпопосилення на CEUS.
Зображення 1:Звичайна ультрасонографія (УЗД) і УЗД з контрастним посиленням (CEUS) папілярної карциноми щитовидної залози у 32-річного чоловіка.
A. Сіра шкала показує гіпоехогенний твердий вузлик в правій частці щитовидної залози з погано видимим краєм, оцінюваний як Категорія 4C. B. Кольоровий доплер показує розгалуження судин (стрілка) в межах утворення. C. CEUS показує гіпопосилення з проникаючими судинами (стрілка).
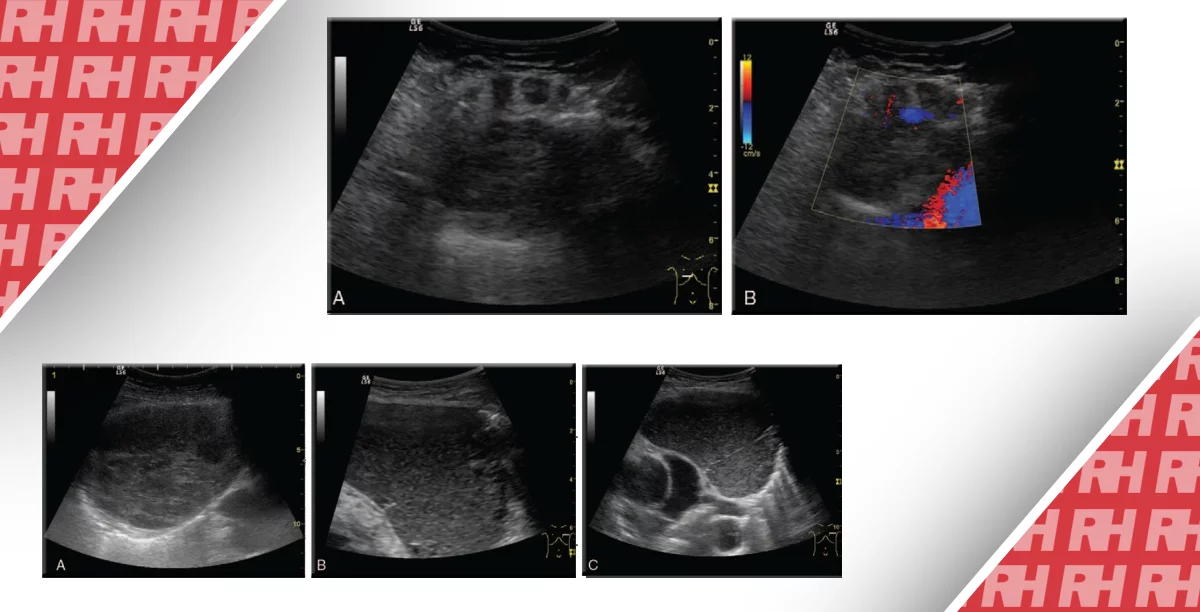
Гетерогенне посилення є ще одним важливим паттерном CEUS, характерним для злоякісних вузлів щитовидної залози (зобр. 2). Дослідники відзначили, що кровоносні судини злоякісних вузликів зазвичай аберрантні і звивисті. Більшість злоякісних вузликів містять області фіброзу, кальцифікації або осередкового некрозу, що може пояснити тенденцію до гетерогенного посилення. Крім того, гетерогенне посилення було визнано найкращим показником для прогнозування злоякісності в багатовимірному логістичному регресійному аналізі.
Зображення 2: Звичайна ультрасонографія і CEUS візуалізація папілярної карциноми щитовидної залози у 64-річного чоловіка.
A. Сіра шкала показує вузлик зі змішаною текстурою (стрілка) в лівій долі щитовидної залози з кальцифікацією, оціненою як система 4B. LCCA, ліва загальна сонна артерія. В. Кольоровий доплер показує периферичний і внутрішній кровотік. C. CEUS показує гетерогенне посилення в утворенні.
Гетерогенність зазвичай вважається суб’єктивною, якісною характеристикою CEUS.
Крім кількісної оцінки гетерогенності посилення, CEUS може також використовуватися для оцінки вузлів щитовидної залози з використанням інших показників, зокрема, часу прибуття речовини і часу піку накопичення. Деякі опубліковані дослідження показали, що раннє вимивання і час до піку були пов’язані зі злоякісним новоутворенням. Це може бути пов’язано зі зменшенням мікроваскулярізаціі в карциномі в результаті некрозу.
Немек і співавтори виявили, що відносне посилення під час кривої вимивання (відношення посилення через 20 секунд після пікового посилення до базової інтенсивності) було нижче в злоякісних вузлах, ніж в доброякісних вузлах, і 2,35 було оптимальним порогом цього параметра для диференціації на доброякісних і злоякісні вузли щитовидної залози.
Характеристики CEUS для доброякісних вузлів щитовидної залози
На відміну від різних патернів CEUS, характерних для злоякісних вузликів, консенсус по діагностичним критеріям для доброякісних вузликів полягає в тому, що гомогенність і посилення країв є двома найбільш цінними індикаторами CEUS для прогнозування доброякісності (зобр. 3), і ці параметри часто оцінювалися в дослідженні .
Зображення 3: Звичайна УЗД і CEUS зображення аденоми щитовидної залози у 35-річної жінки.
A. Сіра шкала показує ізоехогенний вузлик в лівій долі щитовидної залози з чітко визначеним краєм, який оцінюється як категорія 3. В. Кольорова доплерографія показує в основному внутрішній кровотік з відсутністю периферичного кровотоку. C. CEUS показує гомогенність і збільшення кільця країв в утворенні.
Підводячи підсумок, можна сказати, що CEUS є багатообіцяючим неінвазивним методом диференціальної діагностики доброякісних і злоякісних вузлів щитовидної залози. Згідно метааналізу, його чутливість становить від 85% до 88%, а його специфічність – від 88% до 90%. Тим не менш, деякі дослідження виявили, що патерн посилення контрасту може перекриватися між злоякісними і доброякісними вузлами щитовидної залози. Деякі вузлики з типовим доброякісним контрастним посиленням проявляли злоякісну поведінку; наприклад, деякі доброякісні вузлики мали неоднорідне посилення через некроз. Тому багато вчених об’єднали CEUS з іншими методами УЗД для підвищення точності діагностики.
CEUS в поєднанні з еластографією в реальному часі і звичайними УЗД
Еластографія в реальному часі – це відтворена сонографична оцінка консистенції тканин з використанням зовнішнього стиснення. Аналогічно пальпації, обгрунтування еластографії полягає в тому, що ракові вузлики більш жорсткі, з менш пружною деформацією, ніж навколишні тканини або доброякісні вузли щитовидної залози (зобр. 4).
Зображення 4: Звичайне УЗД, еластографія і візуалізація аденоми щитовидної залози в CEUS у 35-річного чоловіка.
A. Сіра шкала показує гіпоехогенний твердий вузлик в правій частці щитовидної залози з кальцифікацією, оцінений як 4C. B. Картина еластографії в основному червона і злегка жовта, що означає, що вузлик, ймовірно, твердий. C. CEUS показує гетерогенне ізопосилення в утворенні.
У попередньому дослідженні повідомлялося, що комбінація цих трьох методів може підвищити як чутливість, так і специфічність діагностики. Що стосується порівнянь між окремими методами, більшість досліджень показали, що еластографія була найбільш цінним інструментом.
CEUS в поєднанні з акустичною радіаційно-імпульсноїю візуалізацією
Акустична радіаційно-імпульсна візуалізація (ARFI) – це новий метод еластографії на основі УЗ-діагностики, що дозволяє кількісно виміряти жорсткість тканини, отриману з якісної еластографії. Комбінація традиційних методів і ARFI і CEUS значно поліпшила діагностичну точність в порівнянні з будь-якою з цих модальностей окремо або комбінацією традиційних (зобр. 5).
Зображення 5: Звичайне УЗД, ARFI і CEUS аденоми щитовидної залози у 35-річного чоловіка.
A. Сіра шкала показує гіпоехогенний твердий вузлик в перешийку з контактом капсули, оцінений як 4C. B. ARFI в основному червоний і злегка жовтий, а середня швидкість поперечної хвилі становила 7,82 м / с, що означає, що вузлик був дуже твердим. C. CEUS показує гіпопосилення в утворенні.
Жан і співавтори використовували ARFI як інструмент попереднього скринінгу для диференціальної діагностики вузлів щитовидної залози, в той час як CEUS використовувався в якості доповнення до вузлів, які було важко розрізнити по ARFI. CEUS може бути об’єднаний з технологією обробки для подання 3-мірного (3D) виду внутрішнього потоку.
На додаток до диференціальної діагностики доброякісних і злоякісних вузлів щитовидної залози, CEUS був застосований для оцінки інших захворювань, пов’язаних з щитовидною залозою.
Висновок
Даний огляд показав, що жодна особливість CEUS не здатна прогнозувати злоякісні утворення в вузлах щитовидної залози з прийнятною діагностичною точністю. Проте, наявність деяких функцій CEUS, таких як гіпопосилення і гетерогенність, можна використовувати для виявлення вузликів з підвищеним ризиком злоякісності; крім того, однорідність і посилення країв вказують на доброякісність.
Більш того, завдяки подальшим дослідженням, CEUS може потенційно грати більш важливу роль у виявленні екстранодулярних злоякісних вузликів і в оцінці відповіді на лікування.