🤖 Короткий переказ від ШІ
Фіброз печінки у дітей є прогресуючим захворюванням, що вимагає ефективних методів діагностики. Дослідження оцінює взаємозв’язок між швидкістю зсуву ультразвукової хвилі (SWS) та ступенем фіброзу печінки у дітей, використовуючи методи Virtual Touch Quantification (VTQ) та Virtual Touch IQ (VTIQ).
Результати показали значну позитивну кореляцію між SWS та ступенем фіброзу, а також запаленням печінки. Методи SWE продемонстрували здатність диференціювати легкий фіброз від помірного/тяжкого, але не можуть точно розрізняти сусідні стадії. Для моніторингу фіброзу печінки у дітей рекомендується використовувати УЗД апарати, наприклад, від компанії GE Voluson E8.
✅ Ключові тези зі статті:
- Діагностика: Швидкість зсуву ультразвукової хвилі (SWS) корелює зі ступенем фіброзу та запалення печінки у дітей.
- Лікування: SWE може допомогти у диференціації ступенів фіброзу, що важливо для подальшого моніторингу.
- Переваги: УЗД зсувнохвильова еластографія є неінвазивною, швидкою, доступною та безпечною альтернативою біопсії.
- Обмеження: SWE може мати труднощі з розрізненням певних стадій фіброзу та може бути менш ефективним у пацієнтів з вищою вагою.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Jonathan R. Dillman, Amer Heider, Jacob L. Bilhartz, Ethan A. Smith, Nahid Keshavarzi, Jonathan M. Rubin, M. James Lopez
Резюме
Тільки в невеликій кількості опублікованих досліджень показаний взаємозв‘язок між неінвазивним вимірюванням швидкості зсуву ультразвукової хвилі (shear wave speed – SWS) і ступенем фіброзу печінки за даними черезшкірної біопсії у дітей.
Мета дослідження – оцінити взаємозв‘язок між вимірюванням швидкості зсуву ультразвукової хвилі в печінці і фіброзом паренхіми у дітей.
Матеріали та методи.
Шістдесят дві дитини (віком від 0-18 років) з відомим або прогнозованим захворюванням печінки піддалися ультразвуковій зсувнохвильовій еластографії (shear wave elastography – SWE) і клінічно показаної черезшкірної товстоголкової біопсії (всі дослідження виконувалися в один день). SWE виконувалася перед біопсією печінки в зоні, яка відбиралася для проведення біопсії, з використанням системи Acuson S3000 з датчиком 9L4; при цьому проводилося шість вимірювань SWS з використанням режимів Virtual Touch Quantification (VTQ) and Virtual Touch IQ (VTIQ). Зразки біопсії вивчали для гістологічної оцінки фіброзу і запалення. Двомірний аналіз проводився з використанням кореляції Пірсона, в той час як множинна лінійна регресія була використана для виявлення взаємозв‘язку між SWS і предикторами. Криві робочої характеристики приймача (receiver operating characteristic – ROC) будували для оцінки здатності VTQ і VTIQ розрізняти помірний проти вираженого фіброзу печінки (гістологічний фіброз 0-2 балів проти 3-6 балів).
Результати.
Була виявлена значна позитивна кореляція між кількістю балів гістологічного фіброзу печінки і середніми значеннями швидкості зсуву хвилі при VTQ (n = 49) і VTIQ (n = 48) (r = 0,68 і r = 0,73; P-значення <0,0001). Також була виявлена значна позитивна кореляція між кількістю балів гістологічного запалення печінки і середніми значеннями швидкості зсуву хвилі при VTQ і VTIQ (r = 0,47 і r = 0,44, а P = 0,0006 і р = 0,0016 відповідно). Для VTQ, кількість балів, як для гістологічного фіброзу (Р <0,0001), так і для запалення (Р = 0,04) були значущими показниками-предикторами для швидкості зсуву хвилі (скоригована модель R2 = 0,49). Для VTIQ тільки кількість балів для гістологічного фіброзу (Р <0,0001) була значущим предиктором швидкісті зсуву хвилі (скоригована модель R2 = 0,56). ROC площі під кривою були 0,84 і 0,86 для VTQ і VTIQ, відповідно.
Висновки.
Показники швидкості зсуву ультразвукової хвилі в печінці збільшуються зі збільшенням фіброзу паренхіми у дітей.
ВСТУП
Існує багато причин хронічної патології печінки у дітей. З часом, регулярне пошкодження гепатоцитів може призвести до розвитку фіброзу паренхіми, або рубцювання. Фіброз печінки у дітей – часто прогресуюче захворювання, зі збільшенням ступеню фіброзу (часто непередбачуване) з часом, що іноді призводить до цирозу печінки. Найбільш поширені причини розвитку включають в себе такі патологічні стани: біліарна атрезія (як без лікування, так і після портоентеростоміі по Касаі), захворювання печінки, пов’язані з повністю парентеральним харчуванням, кістозний фіброз, неалкогольна жирова хвороба печінки (НЖХП), склерозуючий холангіт, аутоімунний гепатит, різні метаболічні порушення і криптогенний цироз.
Декількома методами візуалізації, у тому числі ультрасонографія, МРТ і КТ, можна визначити термінальну стадію фіброзу печінки або явний цироз. Цироз може бути запідозрений при анатомічній візуалізації на основі зміни морфології печінки (наприклад, печінка зазвичай виглядає зморщеною і має горбисту поверхню) або зміни в інтенсивності сигналу з використанням звичайних методів МРТ. МР еластографія недавно була вивчена у дітей і дорослих з хронічними захворюваннями печінки, у тому числі у педіатричних хворих з НАХП і після паліативного лікування хвороби Фонтану – вродженого захворювання серця. При цьому, документально підтверджено підвищення жорсткості печінки при наявності фіброзу. Однак, МР еластографія має обмеження, у тому числі: високу вартість (ціна самого дослідження і пов’язана з ним необхідна інфраструктура), обмежена доступність, потреба в седації, або загальній анестезії у деяких пацієнтів, втрата МР сигналу в установці при надлишку заліза.
Не існує доступних у використанні пристроїв візуалізації, які могли б виявити і точно кількісно визначити ступені від легкого до помірного фіброзу печінки, або оцінити прогресування фіброзу протягом довгого часу. Отже, біопсія печінки, часто з використанням лапароскопічної техніки або черезшкірного товстоголкового доступу під ультразвуковим контролем, зазвичай необхідна для того, щоб підтвердити наявність і виміряти кількісно фіброз печінки у дітей. Ця процедура має обмеження, такі як: відсутність згоди на процедуру пацієнта і батьків, вкрай обмежені зразки печінки, потреба в седації або загальній анестезії, і різні процесуальні ризики, у тому числі небезпечний для життя гемоперитонеум.
Нещодавно, кількісні ультразвукові методики, на основі зсувнохвильової еластографії (SWE), стали доступними в Сполучених Штатах, що дозволило проводити неінвазивну оцінку жорсткості печінки. Ці методи мають численні переваги у дітей, тому що вони дозволяють провести швидку оцінку, не використовують іонізуюче випромінювання, все більше і більше інтегруються в сучасні ультразвукові системи, коштують менше, ніж МР еластографія, і не вимагають седації або загальної анестезії. Крім того, ультразвукова зсувнохвильова еластографія являє собою портативний метод, який дозволяє отримувати зображення у відділі радіології або клініці, а також біля ліжка пацієнта. В даний час, проведено відносно невелике число досліджень по використанню ультразвукової зсувнохвильової еластографії для виявлення фіброзу печінки у дітей. Акустична променева імпульсна візуалізація (ARFI) – метод SWE, який використовує ультразвуковий імпульс для генерування транзиторної деформації тканини, яка в природних умовах призводить до зсуву хвилі в органі мішені (наприклад, печінки). Швидкість зсуву хвилі (shear wave speed – SWS) можна виміряти (в м/с), використовуючи той же датчик, який забезпечує оцінку жорсткості (твердості) тканини. SWS збільшується зі збільшенням жорсткості тканини і може бути безпосередньо пов’язаний з Модулем Юнга (кПа). КПа, властивість матеріалу, яке описує еластичну жорсткість матеріалу, і надається деякими постачальниками, що приблизно складає 3 × (швидкість зсуву хвилі в м/с) 2.
Мета нашого дослідження полягала в перспективній оцінці співвідношення між показниками швидкості зсуву ультразвукової хвилі в печінці і фіброзом паренхіми (на основі часового та анатомічного зв’язку з гістологічною структурою) у дітей для двох різних SWE методів. Крім того, ми прагнули змоделювати співвідношення між SWS печінки і різними предикторами, у тому числі гістологічний фіброз, гістологічне запалення, вік і стать.
МАТЕРІАЛИ І МЕТОДИ
Це дослідження було схвалено інституціональним контрольним органом і відповідає нормативам медичного страхування.
Шістдесят дві дитини (віком 0-18 років), яким була виконана клінічно показана черезшкірна пункційна товстоголкова біопсія печінки для відомого або ймовірного (непухлинного) захворювання печінки, були включені в це проспективне дослідження. Діти були включені між листопадом 2012 і липнем 2014 року. Ми отримали батьківську/опікунську інформовану згоду всіх учасників дослідження; ми отримали згоду самого суб’єкта для дітей старше 10 років. Деякі дані 11 дітей у цьому дослідженні були раніше представлені в попередньому дослідженні, в якому використовується зсувнохвильова еластографія для диференціальної діагностики біліарної атрезії від інших причин неонатальної/малюкової жовтяниці.
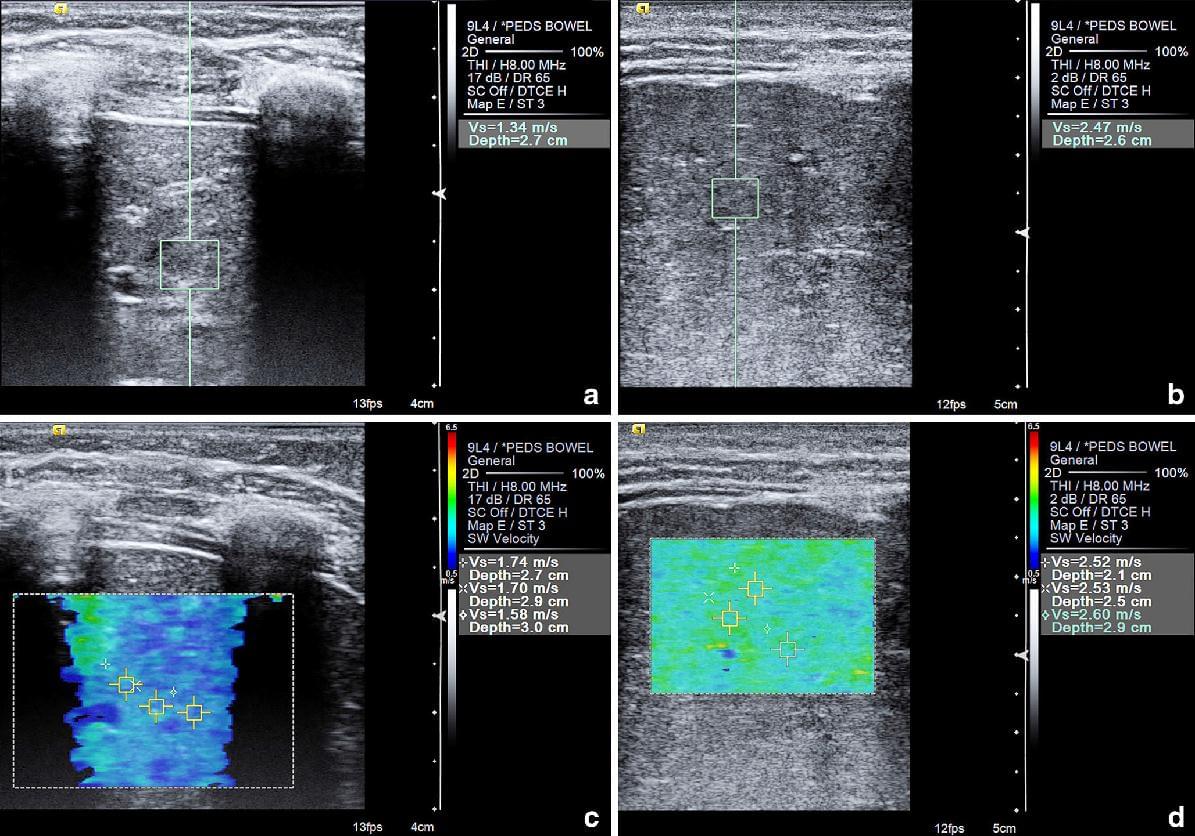
Після ініціації седації або індукції загальної анестезії, ультразвукова зсувнохвильова еластографія виконувалася або в палаті інтервенційної радіології, або прямо в операційній перед проведенням черезшкірної товстоголкової біопсії печінки під ультразвуковим наведенням. SWE проводили в зоні печінки, яка визначена для біопсії. Всі ультразвукові дослідження проводилися невеликою групою дослідників, які спеціалізувалися на педіатричній ультразвуковій техніці зсувнохвильової еластографії під наглядом керівника дослідження. Всі дослідження були проведені з використанням системи Acuson S3000 і датчика 9L4 (Siemens Medical Solutions USA, Malvern, PA). SWE виконувалася в положенні дитини лежачи на спині при спонтанному диханні, якщо дитина була достатньо доросла і в змозі виконати команду затримати дихання. Ми використовували два методи: Virtual Touch Quantification (VTQ) and Virtual Touch IQ (VTIQ) (Рис. 1).
Рис. 1. Зсувнохвильова еластографія. Virtual Touch Quantification (VTQ) зображення у (а) 5-річного хлопчика і (b) 17-річної дівчинки. Режим зображення Virtual Touch IQ (VTIQ) зсувнохвильової еластографії (c) та ж сама дівчинка і (d) той же хлопчик, як (а, b). Високий показник швидкості зсуву хвиль (і неоднорідність еластограми на зображенні VTIQ) корелюють зі збільшенням фіброзу паренхіми.
VTQ і VTIQ є специфічними термінами від виробника для двох методів зсувнохвильової еластографії, також відомі, як акустична променева імпульсна візуалізація (ARFI). Точний доступ для правильної візуалізації (наприклад, права чи ліва частка, міжребір’я або підребір’я) для даної дитини був визначений гастроентерологом або інтервенційним радіологом, який виконував процедуру біопсії печінки. Так як всі процедури біопсії проводилися під седацією або загальною анестезією, пацієнти нічого не вживали перорально протягом SWE дослідження, відповідно до принципів відділення анестезії.
Для VTQ зсувнохвильової еластографії використовується встановлюваний оператором режим 4.0 МГц ARFI, або “поштовховий імпульс” для віддаленого отримання зсувних хвиль в межах поля зору, в той час як режим VTIQ використовує декілька ARFI імпульсів (4.0-5.7 МГц, що виникають з різних точок вздовж поверхні датчика і зосереджені на різних глибинах) для відтворення зсувних хвиль і створення кольорового зображення (еластограми) жорсткості тканин. VTQ використовує датчик 9L4, що дозволяє розмістити єдине, фіксованого розміру 5-мм2 поле зору (region of interest – ROI) в отриманому зображенні для вимірювання швидкості зсуву хвилі (м/с), у той час як VTIQ дозволяє розмістити кілька ROI фіксованого розміру – 1,5 мм2 в отриманому зображенні для вимірювання швидкості зсуву хвилі. Зсувнохвильова еластографія виконувалася з використанням ультразвукової системи з настройками за замовчанням; шкала VTIQ кольорової еластограми варіювала швидкість в діапазоні від 0,5 м/с (синій) до 6,5 м/с (червоний).
При використанні режиму VTQ, поле зору було розміщено в печінці в зоні, яка була визначена для біопсії, уникаючи видимих кровоносних судин і, принаймні, на 10 мм нижче поверхні печінки. Шість VTQ вимірювань швидкості зсуву хвилі були отримані у кожної дитини, з повторним розташуванням датчика для кожної спроби. При використанні режиму VTIQ, два зображення еластограми печінки були отримані в зоні, яка була визначена для біопсії. Шість VTIQ вимірювань швидкості зсуву хвилі також були отримані у кожної дитини (три виміри на еластограмі, з полем зору, розміщеним на розсуд ультразвукового техніка в зонах “повного заповнення кольором”). Всі зображення SWE були отримані з найменшим тиском датчика, що необхідно для проведення діагностичної візуалізації.
Вік, стать і індекс маси тіла (ІМТ) були задокументовані для кожної дитини. Ми вивчили всі електронні медичні записи для того, щоб отримати клінічні показання для проведення біопсії печінки та отримання гістологічного діагнозу.
ГІСТОЛОГІЧНИЙ АНАЛІЗ ПЕЧІНКИ
Всі діти в нашому дослідженні піддалися клінічно обгрунтованій процедурі товстоголкової біопсії печінки під ультразвуковим контролем з використанням або 16-го, або 18-го калібру пристроя для біопсії (одноразова пункційна голка для біопсії Bard Monopty; Bard Biopsy Systems, Tempe, AZ).
Як мінімум два зразки тканин були отримані від кожної дитини. Після звичайної обробки тканини, зразки були поміщені на предметне скло і пофарбовані гематоксиліном і еозином, а також і Масон тріхромом. Зразки тканини були піддані вивченню для бальної оцінки гістологічного фіброзу (система визначення стадії фіброзу Ishak, 0-6, де 0 вказує на відсутність фіброзу, а 6 показує наявність цирозу) і запалення (модифікований індекс активності гепатиту, 0-18, де 0 означає – немає запалення, а 18 вказує на важке запалення і некроз); скоринг був проведений сертифікованим педіатричним патологоанатомом (3,5 років досвіду), який не знав результатів ультразвукової зсувнохвильової еластографії. Ці гістологічні скорингові системи були задіяні тому, що вони використовуються і затверджені в численних дослідженнях у дорослих; при цьому не існує схожих спеціальних педіатричних розробок для скорингу гістологічного запалення і фіброзу.
СТАТИСТИЧНИЙ АНАЛІЗ
Безперервні дані були узагальнені за допомогою середніх величин і стандартного відхилення, в той час як категоріальні дані були узагальнені за допомогою графіків і відсотків. Двоваріантне співвідношення, в тому числі VTQ і швидкість зсуву хвилі VTIQ (індивідуальне для суб’єкта середнє, медіана і максимум) проти кількості балів гістологічного фіброзу та запалення були оцінені з використанням кореляції Пірсона. Аналіз дисперсії (ANOVA) був використаний для порівняння VTQ і VTIQ середніх значень швидкості зсуву хвилі у дітей з відсутністю, або легким, проти помірного і проти значного фіброзу (гістологічний фіброз 0-1 балів, проти 2-3 балів, проти 4-6 балів). Ці середні також були зіставлені попарним способом, використовуючи багаторазове порівняння – тест Тьюки з відповідним коригуванням значення Р.
Ми використовували множинний лінійний регресійний аналіз для оцінки співвідношення між SWS і предикторами (кількість балів для гістологічного фіброзу і запалення, а також вік і стать) як для VTQ, так і VTIQ. Критерій інформації Akaike був використаний для остаточного вибору моделі. Криві робочої характеристики приймача (ROC) були побудовані для оцінки діагностичної значимості VTQ і VTIQ для диференціальної діагностики легкого (кількість балів гістологічного фіброзу 0-2) проти значного (гістологічний фіброз – 3-6 балів) фіброзу. Всі статистичні тести проводилися за допомогою SAS версії 9.3 (SAS Institute, Cary, NC). Р-значення <0,05 вважали значущим.
РЕЗУЛЬТАТИ
Характеристики об’єктів дослідження
Шістдесят дві дитини були включені в наше дослідження, 29 (47%) дівчаток і 33 (53%) хлопчика. Середній вік пацієнтів склав 8,0 ± 5,8 років (діапазон, 4 тижня-18 років). Клінічні показання для біопсії печінки, а також гістологічні діагнози представлені в таблиці 1.
Таблиця 1. Клінічні показання для біопсії печінки і остаточні діагнози у 62 дітей.
|
Показання для біопсії |
n |
Остаточні діагнози |
n |
|
Первинна ортотопічна трансплантація печінки (OLT) |
24 |
OLT відторгнення |
11 |
|
Підвищені печінкові проби (рідна печінка) |
21 |
Неспецифічна аномалія розвитку печінки |
10 |
|
Холестаз |
11 |
Нормальна печінка |
9 |
|
Підвищені печінкові проби (після процедури Kasai) |
1 |
Біліарна атрезія/біліарна обструкція |
5 |
|
Відомий аутоімунний гепатит |
1 |
Аутоімунний гепатит |
5 |
|
Відомий криптогенний цироз |
1 |
Склерозуючий холангіт |
5 |
|
Відома хвороба накопичення глікогену |
1 |
Медикаментозний гепатит |
2 |
|
Відомий дефіцит піруваткінази |
1 |
Хвороба накопичення глікогену |
2 |
|
Відомий склерозуючий холангіт |
1 |
Неонатальний гепатит |
2 |
|
Неалкогольний стеатогепатит |
2 |
||
|
Недостатність жовчних проток |
2 |
||
|
Криптогенний цироз |
1 |
||
|
Природжений фіброз печінки |
1 |
||
|
Лейкемія |
1 |
||
|
Вірусний гепатит |
1 |
VTQ було успішним (це означає, що вимірювання швидкості зсуву хвилі можуть бути проведені) у 49 дітей, у тому числі 24 (49%) дівчинки і 25 (51%) хлопчиків, при використанні датчика 9L4. Середній вік був 7,2 ± 5,5 років. Діти (5 дівчаток і 8 хлопчиків) з недостовірними зображеннями VTQ мали середній вік -11,1 років. Середній індекс маси тіла (ІМТ) для дітей з успішними зображеннями VTQ склав 18,4 ± 4,7 кг/м2, проти 30.4 ± 6.4 кг/м2 для дітей з невдалими зображеннями (Р <0,0001).
VTIQ було успішним (це означає, що більш ніж дві третини еластограми заповнені кольоровими даними на основі суб’єктивної оцінки) у 48 дітей, у тому числі 21 (44%) дівчинка і 27 (56%) хлопчиків. Середній вік дітей був 6.7 ± 5.5 років. Діти (8 дівчаток і 6 хлопчиків) з недостовірними зображеннями VTIQ мали середній вік 12,4 років. Середній ІМТ для дітей з успішною візуалізацією при VTIQ був 17,6 ± 4,1 кг/м2, проти 27,8 ± 7,1 кг/м2 для дітей з невдалим дослідженням (Р = 0,0001).
Двовимірний аналіз
Виявлено значну позитивну кореляцію між окремими середніми значеннями для суб’єктів, медіаною і максимумом VTQ вимірювань зсувнохвильової швидкості і кількістю балів для гістологічного фіброзу та запалення паренхіми (Таблиця 2) (Рис. 2). Точно так само, існує значна позитивна кореляція між окремими середніми значеннями для суб’єктів, медіаною і максимумом VTIQ вимірювань зсувнохвильової швидкості і кількістю балів для гістологічного фіброзу та запалення паренхіми (Таблиця 2), (Рис. 2).
Таблиця 2. Кореляція Пірсона (R) між показниками швидкості зсуву хвилі окремих суб’єктів (в м/с, n=6) і прогнозованими змінними (предикторами), у тому числі кількістю балів гістологічного фіброзу (0-6), гістологічного запалення (0- 18) і віком.
|
r (P-значення) (n) |
VTQ – середне SWS |
VTQ – медіана SWS |
VTQ – максимум SWS |
VTIQ – середне SWS |
VTIQ – медіана SWS |
VTIQ – максимум SWS |
|
Бали фіброзу |
0.68 |
0.63 |
0.65 |
0.73 |
0.72 |
0.68 |
|
(<0.0001) |
(<0.0001) |
(<0.0001) |
(<0.0001) |
(<0.0001) |
(<0.0001) |
|
|
(49) |
(49) |
(49) |
(48) |
(48) |
(48) |
|
|
Бали запалення |
0.47 |
0.45 |
0.52 |
0.44 |
0.44 |
0.48 |
|
(0.0006) |
(0.001) |
(0.0001) |
(0.0016) |
(0.002) |
(0.0006) |
|
|
(49) |
(49) |
(49) |
(48) |
(48) |
(48) |
|
|
Вік |
0.02 |
−0.02 |
0.07 |
−0.28 |
−0.27 |
−0.26 |
|
(0.87) |
(0.86) |
(0.63) |
(0.057) |
(0.06) |
(0.08) |
|
|
(49) |
(49) |
(49) |
(48) |
(48) |
(48) |
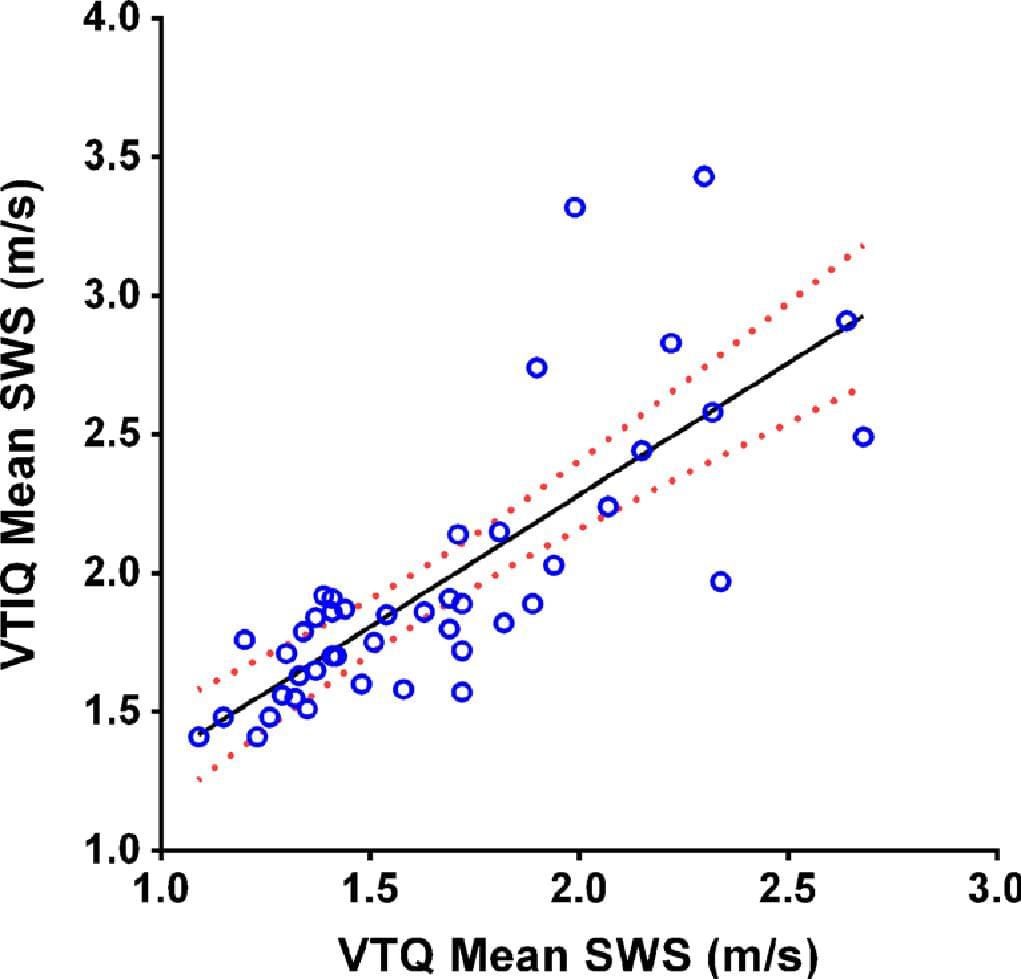
Середні показники VTQ і VTIQ швидкості зсуву хвилі мали також сильну позитивну кореляцію, як і очікувалося (r = 0.79; Р <0,0001) (Рис. 3).
Рис. 2. Порівняння швидкості зсуву хвилі (SWS) і фіброзу. Бокс-графіки показують збільшення показників SWS печінки одночасно зі збільшенням фіброзу паренхіми при (а) VTQ і (b) VTIQ режимах зсувнохвильової еластографії. VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification.
Рис. 3. Кореляція між показниками швидкості зсуву хвилі при Virtual Touch Quantification (VTQ) і Virtual Touch IQ (VTIQ). Діаграма розкиду (з усередненою кривою і 95% довірчим інтервалом) показує взаємозв’язок між середніми значеннями швидкості зсуву хвилі (SWS) при VTQ і VTIQ у 44 дітей (r = 0,79; p <0,0001).
Не було виявлено значимої кореляції між значеннями SWS (середнє, медіана і максимум) і віком при VTQ. Виявлена незначна негативна кореляція між значеннями SWS (середнє, медіана і максимум) і віком при VTIQ (P-значення = 0.057-0.08).
Дисперсійний аналіз (ANOVA)
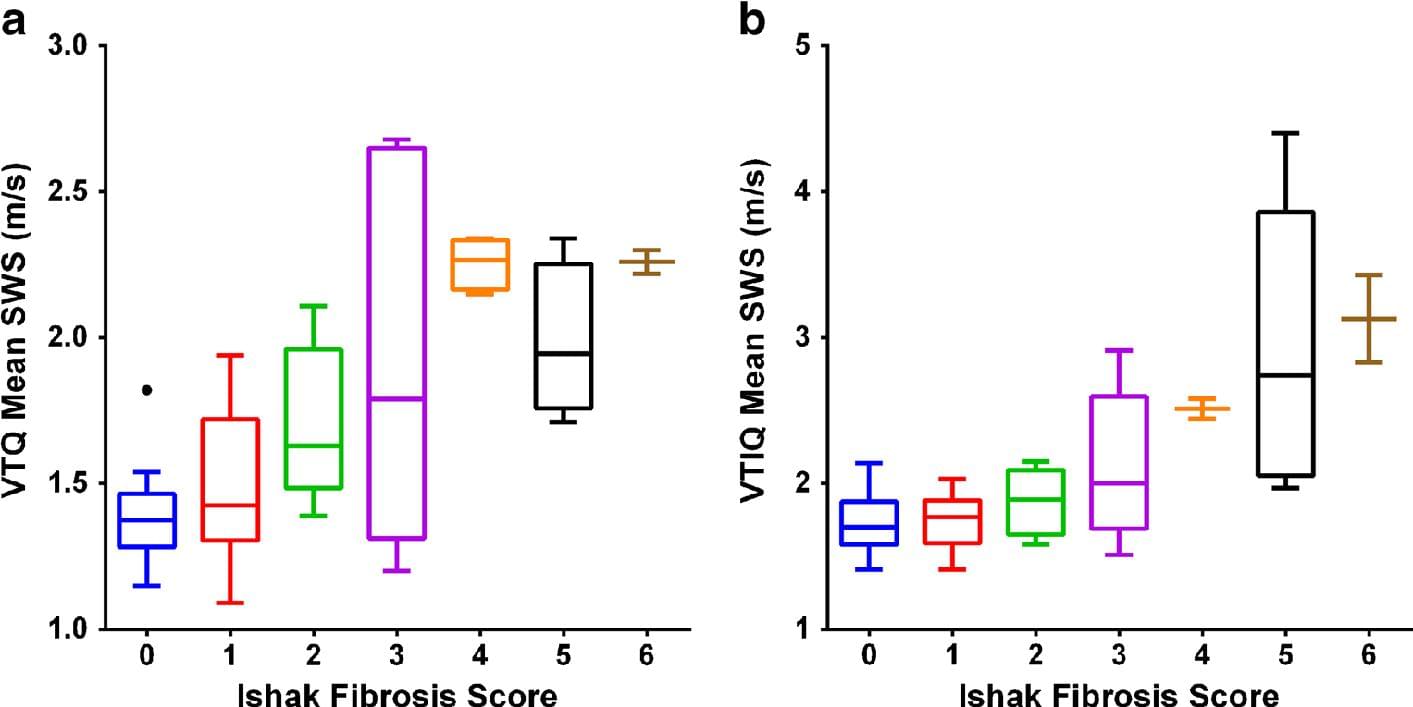
Виявлено значну різницю середніх значень SWS серед дітей з Ishak 0-1 (n = 28, 1,46 ± 0,23 м/с), 2-3 (n = 11, 1,82 ± 0,50 м/с) і 4-6 (n = 10, 2,15 ± 0,21 м/с) кількістю балів гістологічного фіброзу при VTQ (P <0,0001) (Рис. 4). Аналогічно, існувала значна різниця середніх значень SWS серед дітей з Ishak 0-1 (n = 29, 1,74 ± 0,18 м/с), 2-3 (n = 10, 2,02 ± 0,44 м/с ) і 4-6 (n = 9, 2,87 ± 0,75 м/с) та кількістю балів гістологічного фіброзу при VTIQ (P <0,0001) (рис. 4).
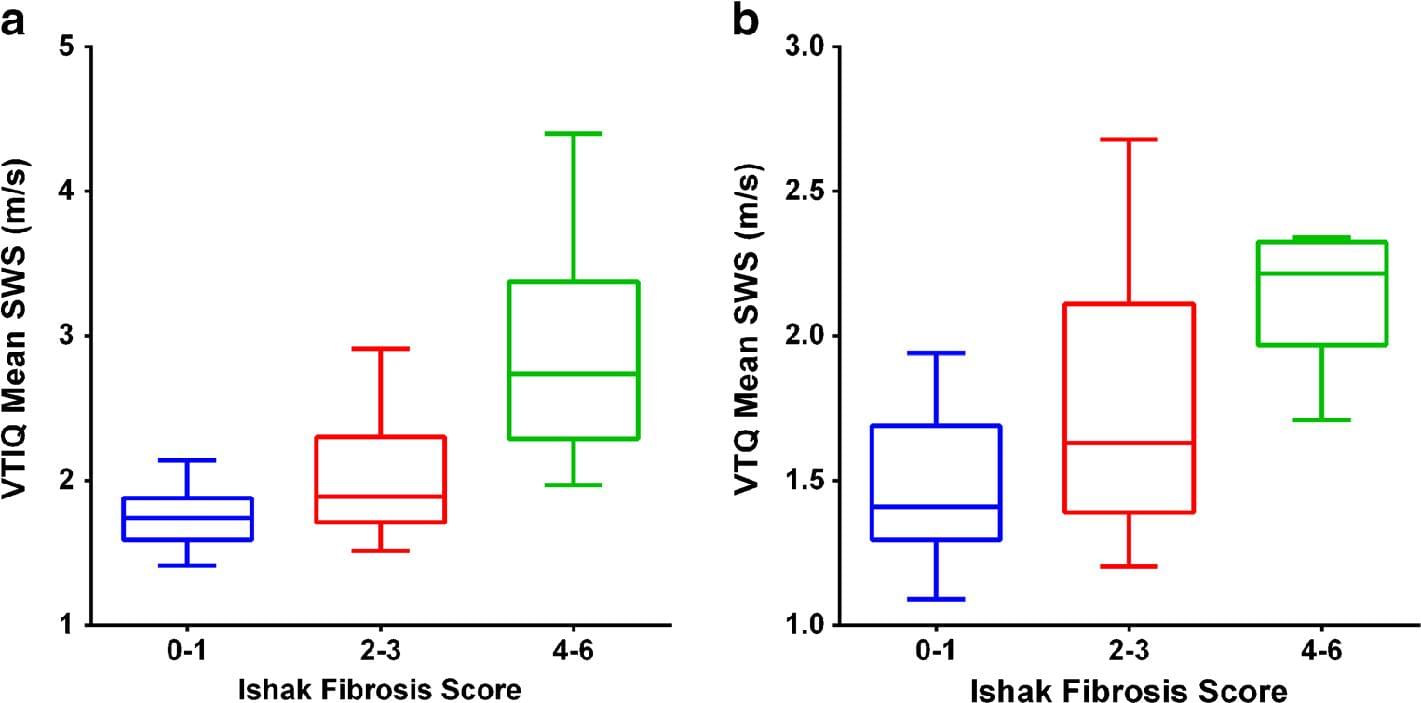
Рис. 4. Порівняння показників швидкості зсуву хвилі і кількості балів гістологічного фіброзу. Бокс-графіки показують середнє значення швидкості зсуву хвилі (SWS) у дітей з різною вираженістю фіброзу печінки, з використанням (а) VTIQ і (b) VTQ режимів. Обидва режими зображення демонструють збільшення SWS зі збільшенням балів гістологічного фіброзу (Р <0,0001 для обох режимів VTQ і VTIQ). VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification.
Парне порівняльне тестування середнього значення швидкості зсуву хвилі серед груп з різною кількістю балів гістологічного фіброзу з Туки-корекцією P-значень, представлені в таблиці 3.
Таблиця 3. Парні порівняння значень середньої швидкості зсуву хвилі в печінці у дітей з легким, помірним і вираженим гістологічним фіброзом.
|
Групи порівняння пацієнтів з гістологічним фіброзом |
Середні значення різниці SWS (м с) |
Значимість? |
Скориговане значення Р * |
|
VTQ |
|||
|
0–1 vs. 2–3 |
0.36 |
Так |
0.006 |
|
0–1 vs. 4–6 |
0.69 |
Так |
<0.0001 |
|
2–3 vs. 4–6 |
0.33 |
Так |
0.045 |
|
VTIQ |
|||
|
0–1 vs. 2–3 |
0.27 |
Ні |
0.15 |
|
0–1 vs. 4–6 |
1.13 |
Так |
<0.0001 |
|
2–3 vs. 4–6 |
0.86 |
Так |
<0.0001 |
SWS – швидкість зсуву хвилі, VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification
* P-значення, скориговані з використанням методу Тьюки
Прогнозування швидкості зсуву хвилі в печінці
Ми використовували множинну лінійну регресію для оцінки співвідношення між значенням SWS печінки (середнім) і предикторами (кількістю балів гістологічного фіброзу печінки і запалення, а також віком і статтю), як для VTQ, так і VTIQ.
VTQ
Для VTQ, кількість балів гістологічного фіброзу печінки та запалення були значущими предикторами середнього значення швидкості зсуву хвилі (P <0,0001 і P = 0,04 відповідно). Вік та стать не були значущими прогностичними факторами, і вони привели до небажаного збільшення інформаційного критерію Akaike.
Остаточна модель була наступною: SWS (м/с) = 1,32 + (0,13 × бали гістологічного фіброзу) + (0,025 × бали гістологічного запалення) (Р <0,0001; скориговане R2 = 0,49).
VTIQ
Для VTIQ, бали гістологічного фіброзу були єдиним значущим предиктором середньої швидкості зсуву хвилі (Р <0,0001). Бали гістологічного запалення (Р = 0,09) і вік (Р = 0,10) були незначущими прогностичними факторами і були включені в остаточну модель, тому що вони призвели до зменшення інформаційного критерію Akaike. Стать не була значущим предиктором, що сприяло небажаному збільшенню інформаційного критерію Akaike. Остаточна модель була наступною: SWS (м/с) = 1,65 + (0,20 × бали гістологічного фіброзу) + (0,028 × бали гістологічного запалення) + (- 0,018 × вік) (Р <0,0001; скориговане R2 = 0,56).
Аналіз кривої робочої характеристики приймача (ROC)
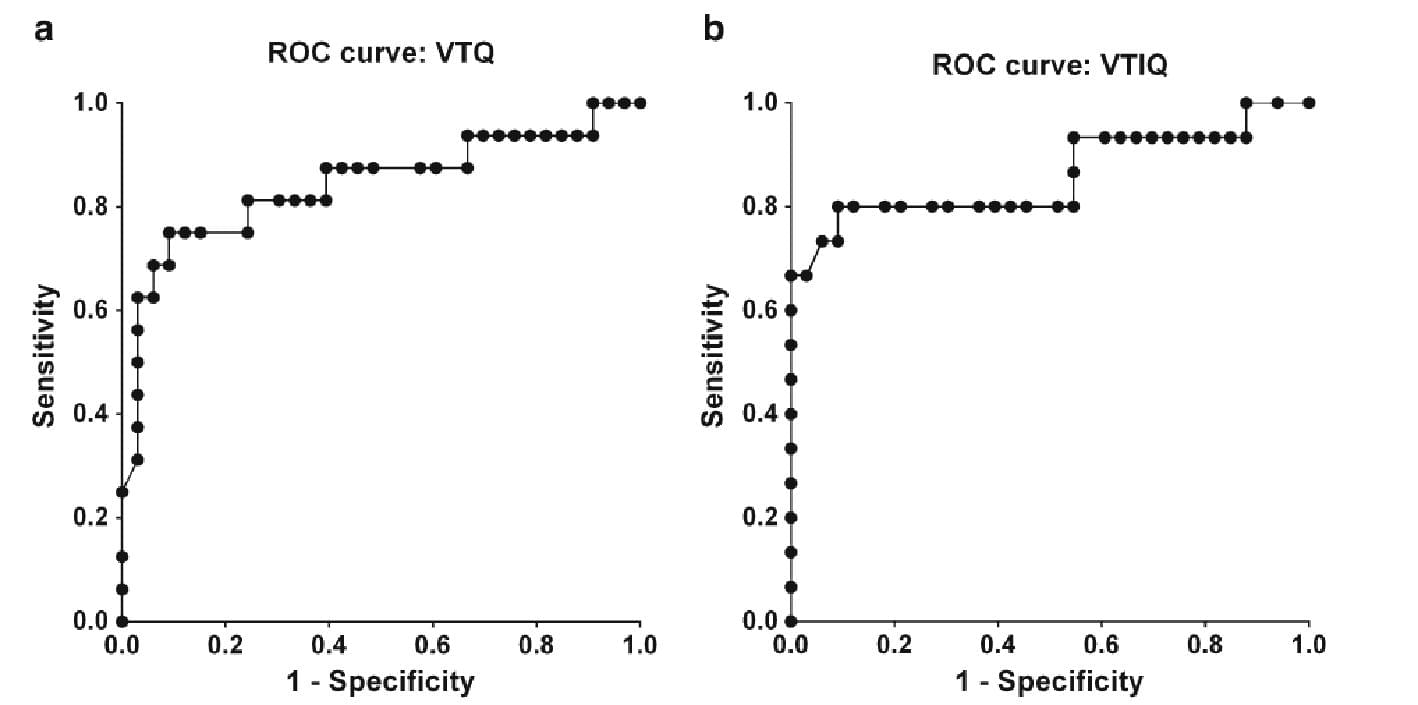
Аналіз кривої робоча характеристики приймача (ROC) провели з метою оцінки можливостей використання показників швидкості зсуву хвилі для диференціальної діагностики дітей з незначним гістологічним фіброзом печінки і вираженого фіброзу в балах. Для VTQ, площа під кривою була 0,84 (95% ДІ: 0.70-0.98; Р = 0,0001) (Рис. 5). Порогове значення швидкості зсуву хвилі 2,07 м/с сприяло відмінному позитивному значенню ймовірності (20,6) для виявлення вираженого гістологічного фіброзу (відповідно з балами), з чутливістю 63% і специфічністю 97%. Для VTIQ, площа під кривою була 0,86 (95% ДІ: 0.72-1.0; Р <0,0001) (Рис. 5).
Рис. 5. Криві робочої характеристики приймача (ROC) для диференціальної діагностики легкого (гістологічний фіброз 0-2 бали) і вираженого (гістологічний фіброз 3-6 балів) фіброзу печінки за допомогою показника середньої швидкості зсуву хвилі. А. Площа під кривою для VTQ становить 0,84 (95% ДІ: 0.70-0.98). В. Площа під кривою VTIQ становить 0,86 (95% ДІ: 0.72-1.0). VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification.
Порогове значення SWS 2,15 м/ссприялоотриманнювідмінногопозитивногозначенняймовірності (22,0) длявиявленнявираженогогістологічногофіброзу (відповіднозбалами), зчутливістю67% і специфічністю 97%.
ОБГОВОРЕННЯ
Діагностичні значення SWS можуть бути отримані у 49 з 62 (79%) дітей за допомогою VTQ і у 48 з 62 (77%) дітей, при VTIQ. При аналізі невдалих випадків (тобто дітей, у яких не могли бути отримані вимірювання швидкості зсуву хвилі для VTQ – дисплей виводить повідомлення про помилку в цьому випадку, або у випадку, коли менше як дві третини еластограми заповнені кольоровими даними для VTIQ) було показано, що ці діти, як правило, були старші і мали більшу статуру, в порівнянні з дітьми з вдалою діагностичною візуалізацією SWE. Цікаво, що деякі діти з невдалою візуалізацією VTQ мали успішні VTIQ зображення, і навпаки, це явище, для якого ми не маємо певного пояснення. Збільшення жирової тканини черевної стінки може послаблювати звукові хвилі і, як результат, зменшувати силу акустичного імпульсу. Погіршення сигналу призводить до нездатності діагностичної оцінки швидкості зсуву хвилі. Невеликий відсоток недіагностичних випадків, ймовірно, був результатом виражених дихальних рухів, які, ймовірно, перешкоджають можливості реєстрації зсуву хвилі. У разі невдалої ультразвукової SWE печінки, альтернативою є MР еластографія, особливо у великих педіатричних хворих, таких, як діти з НАХП. Для дослідження дітей ми навмисно обрали тільки 9L4 лінійний датчик, щоб мінімізувати похибку вимірювання, тому що зображення з більш, ніж одним датчиком є потенційним джерелом варіабельності при спробах кореляції вимірювань SWS з гістологічними результатами, враховуючи той факт, що вимірювання швидкості зсуву хвилі в якійсь мірі залежать від датчика. Тим не менш, слід зазначити, що VTQ SWE також може бути виконано за допомогою конвексного датчика 4C1, який має режим силового імпульсу низької частоти і оптимізований для візуалізації печінки у великих дітей і дорослих. В даний час, тільки лінійний датчик 9L4 сумісний з SWE в режимі VTIQ.
Двовимірний аналіз показав значну позитивну кореляцію між вимірами SWS, як гістологічного фіброзу, так і запалення для VTQ і VTIQ. Хоча співвідношення між SWS і бальною оцінкою гістологічного фіброзу були достатньо сильні для обох режимів SWE, співвідношення між SWS і бальною оцінкою гістологічного запалення були суттєвими. Наші багатовимірні регресійні моделі припускають, що гістологічне запалення впливає на SWS печінки, коли враховується кількісний ступінь фіброзу печінки. Цікаво, що дуже схожі сильні кореляції виявили між середнім значенням окремих суб’єктів, медіаною і максимумом значень SWS і кількістю балів гістологічного фіброзу та запалення для обох режимів VTQ і VTIQ.
Тестування ANOVA також показало, що SWS печінки збільшується зі збільшенням фіброзу печінки. Тим не менш, бокс-графік, побудований з використанням трьох ступенів фіброзу печінки (гістологічний фіброз 0-1 балів, 2-3 балів і 4-6 балів) показав деяке перекриття значень SWS для кожної гістологічної категорії. Таким чином, малоймовірно, що SWE (або, принаймні, VTQ і VTIQ в їх нинішньому вигляді) можуть диференціювати певний ступінь гістологічного фіброзу з високою часткою достовірності (наприклад, шкала фіброзу Ishak: 1 проти. 2, 2 проти 3, або 3 проти 4).
Аналізи ROC кривої показують, що певні порогові значення SWS можуть давати достатню чутливість і дуже високу специфічність для диференціальної діагностики відсутність/легкий фіброз від помірний/важкий (виражений) фіброз. ROC площі під кривою були схожі для VTQ і VTIQ (0,84 і 0,86, відповідно). Слід зазначити, що порогові значення SWS для диференціальної діагностики гістологічних ступенів фіброзу можуть залежати від конкретного виробника, що показано в якійсь мірі на основі останніх експериментів отримання даних на фантомі Альянсом кількісної візуалізації біомаркерів (Quantitative Imaging Biomarker Alliance). Це спільне групове дослідження показало, що «існує статистично значуща різниця в значеннях SWS серед [різних ультразвукових] систем». У кінцевому рахунку, SWE, ймовірно, буде найбільш корисним маркером для визначення наявності або відсутності істотного фіброзу печінки і для моніторингу прогресування фіброзу протягом довгого часу (на відміну від точного кількісного визначення фіброзу).
Множинний лінійний регресійний аналіз був використаний для оцінки співвідношення між SWS печінки і різних предикторів, у тому числі кількості балів гістологічного фіброзу, гістологічного запалення, віку і статі. Для VTQ, як гістологічний фіброз, так і запалення були значущими предикторами; вплив гістологічного запалення є важливим спостереженням і припускає, що й інші фактори, крім фіброзу, можуть впливати на зміни показників швидкості зсуву хвилі в печінці. Якщо провести корекцію по відношенню до кількості балів гістологічного запалення, то збільшення балу гістологічного фіброзу на 1 одиницю (наприклад, зміни за шкалою фіброзу Ishak від 3 до 4 балів) викликає збільшення середньої SWS на 0,13-м/с. Для VTIQ, бальна оцінка гістологічного фіброзу стала єдиним значущим предиктором, хоча бальна оцінка гістологічного запалення і вік в цілому поліпшили якість моделі. Якщо провести корекцію по відношенню до кількості балів гістологічного запалення і віку, то збільшення балу гістологічного фіброзу на 1 одиницю викликає збільшення середнього значення SWS на 0,20м/с.
Для VTIQ, остаточна модель множинної лінійної регресії мала скориговане R2-значення 0,56. Це означає, що приблизно 56% значень середньої SWS, зареєстрованих у дітей в нашому дослідженні, можна пояснити нашою моделлю і її предикторами; однак, 44% значень залишаються незрозумілими. Ця незрозуміла варіабельність, ймовірно, є результатом кількох факторів, у тому числі варіабельність вимірювання, пов’язана з використовуваною технікою SWE, (наприклад, варіабельність, притаманна VTIQ), варіабельність вибірки тканини і гістологічного скорингу та індивідуальна біологічна варіабельність об’єкта. Крім того, ми припустили лінійну залежність між SWS і кількістю балів гістологічного фіброзу і запалення. При цьому ці співвідношення можуть бути складнішими, ніж ми їх оцінили, наприклад, з нелінійним збільшенням SWS збільшується фіброз паренхіми або запалення.
Одним з основних переваг нашого дослідження є те, що воно є першим у своєму роді, яке безпосередньо порівнює режими VTQ і VTIQ SWE для дослідження фіброзу печінки у дітей. VTIQ, на відміну від VTQ, забезпечує кольорове зображення жорсткості печінки, що дозволяє виявити найжорсткіші області печінки та оцінити неоднорідність паренхіми. Наші результати показують, що в середньому у дітей, значення SWS при VTIQ трохи вище, ніж значення VTQ у тієї ж дитини. Джерело цієї систематичної різниці недостатньо вивчено, хоча, ймовірно, пов’язано з технічними відмінностями між режимами VTQ і VTIQ. Забігаючи вперед, при клінічному застосуванні SWE у дітей і дорослих, буде важливо враховувати відмінності в значеннях SWS, які отримані з використанням різних режимів SWE і різних ультразвукових систем для того, щоб правильно інтерпретувати результати. У зв’язку з тим, що в наше дослідження включено майже 30 дітей з відсутністю або дуже мінімальним фіброзом печінки (гістологічний фіброз 0-1 бал), наші результати повинні допомогти встановити характерне нормативне або навколонормативне значення SWS для конкретної ультразвукової системи, яку ми використовували в педіатричній популяції (приблизно 1,46 м/с [95% ДІ: 1.37-1.55 м/с] для VTQ і 1,74 м/с [95% ДІ: 1.67-1,81 м/с] для VTIQ). Ці значення SWS трохи вищі, ніж повідомлялося в деяких опублікованих дослідженнях. Наприклад, в недавньому дослідженні Matos і ін.за допомогою VTQ і датчиком 4С1 визначено нормальне значення SWS дитячої печінки як 1.07 м/с, в середньому, в той час як дослідження Fontanilla та ін. за допомогою датчика 9L4 знаходить, що нормальне значення SWS дитячої печінки повинно бути 1,15 м/с, в середньому. Ще одне недавнє дослідження Tütar та ін., з використанням іншої ультразвукової системи (SuperSonic Imagine, Aix-en-Provence, France), визначило нормальне значення SWS дитячої печінки як 1,56 м/с, що цілком схоже на наші результати.
Наше дослідження має кілька обмежень. По-перше, близько половини дітей у нашому дослідженні не мали, або мали дуже мінімальний фіброз печінки, в той же час був мінімальний відсоток дітей з більш високими ступенями фіброзу (наприклад, тільки восьмеро дітей мали бал 5 або 6 за шкалою фіброзу Ishak). Незважаючи на це, ми чітко показали, що значення SWS печінки зростають зі збільшенням запалення і фіброзу. Більше число дітей з помірним і важким фіброзом печінки дозволило б нам ще точніше змоделювати співвідношення між SWS і кількістю балів гістологічного фіброзу. По-друге, наші результати можуть мати похибки, так як в нашому дослідженні був тільки один патологоанатом, який підраховував бали гістологічного запалення і фіброзу. Гістологічне визначення стадії фіброзу та запалення – суб’єктивне, незважаючи на використання перевірених напівкількісних скорингових систем, і, потенційно, схильне до систематичних і випадкових помилок вимірювання. Нарешті, хоча ми проводили SWE в зоні відбору проб тканини в момент біопсії, як і раніше майже неможливо досягти ідеальної кореляції 1: 1 – зображення до гістології.
ВИСНОВКИ
Показники SWS печінки зростають зі збільшенням фіброзу печінки у дітей. Параметри швидкості зсуву хвилі при VTQ і VTIQ мають сильну кореляцію, і показники SWS печінки можуть ефективно диференціювати дітей з відсутністю або слабким фіброзом печінки, від дітей з помірним або тяжким фіброзом печінки. При використанні декількох видів лінійного регресійного аналізу, ми також показали, що і гістологічний фіброз, і запалення є предикторами збільшення показників SWS при ультразвуковому дослідженні. Необхідні додаткові дослідження для поліпшення діагностичної точності ультразвукового методу SWE, а також розуміння того, як показники SWS змінюються з часом у дітей з хронічним захворюванням печінки, як набряк і закрепи впливають на вимірювання SWS печінки, і, як результати ультразвукової SWE, співвідносяться з такими, отриманими при використанні МР еластографії. Для проведення досліджень рекомендуємо використовувати апарат від компании GE Voluson E8.
Питання та відповіді (FAQ)
Що таке фіброз печінки у дітей?
- Фіброз печінки – це рубцювання печінки, яке виникає внаслідок хронічного пошкодження гепатоцитів. Це часто прогресуюче захворювання, що може призвести до цирозу.
Які методи використовуються для вимірювання швидкості зсуву ультразвукової хвилі (SWS)?
- У дослідженні використовувалися два методи ультразвукової зсувнохвильової еластографії: Virtual Touch Quantification (VTQ) та Virtual Touch IQ (VTIQ).
Який зв’язок між SWS та ступенем фіброзу печінки?
- Дослідження показало значну позитивну кореляцію між показниками SWS та ступенем фіброзу печінки. SWS зростає зі збільшенням фіброзу.
Які переваги ультразвукової зсувнохвильової еластографії перед іншими методами?
- SWE – неінвазивний, швидкий, не використовує іонізуюче випромінювання, більш доступний та дешевший ніж МРТ еластографія, не потребує седації або анестезії.
Яка точність методів VTQ та VTIQ у визначенні ступеня фіброзу?
- Площа під кривою ROC для VTQ та VTIQ склала 0,84 та 0,86 відповідно, що вказує на високу діагностичну точність.
Чи враховувалися інші фактори, окрім фіброзу, при аналізі даних?
- Так, у множинній лінійній регресії враховувалися також гістологічне запалення, вік та стать.
Скільки дітей взяло участь у дослідженні?
- У дослідженні взяли участь 62 дитини віком від 0 до 18 років.













14.10.2019
Дядченко Святослав Андреевич