АВТОРИ: Ji Yang Kim a,b, Soo Young Kim b, Ki Ra Yang b
а – відділення радіології, Університет Луїсвілля, Кентуккі, США
b – відділення радіології Сеульського національного університетського госпіталю, Сеул, Південна Корея
Ключові слова: рак щитоподібної залози, ультразвукове дослідження щитоподібної залози, тонкоголкова аспіраційна біопсія
Скорочення: FNA (fine needle aspiration) – тонкоголкова аспіраційна біопсія, PFI (positive FNA indication) – А, якщо вузол має 2 або більше злоякісні сонографічні ознаки, це позитивне показання для FNA; PFI – B, якщо вузол має 1 або більше злоякісних сонографічних ознак, це позитивне показання для FNA; NFI (negative FNA indication), якщо вузол має комірчасту структуру, або не має злоякісних сонографічних ознак, це негативне показання для біопсії.
Резюме
Мета. Дослідити ультразвукові (УЗ) характеристики вузлів щитоподібної залози (ЩЗ), що не пальпуються, 1-2 см в діаметрі і оцінити рекомендації для проведення FNA з точки зору ультразвукових даних.
Матеріали та методи. У період з червня 2005 року по листопад 2006 року радіологами була проведена FNA в 919 вузлах щитоподібної залози. З усіх обстежених вузлів в остаточний аналіз було включено 51 вузол злоякісної етіології і 72 – доброякісної. Всі 123 вузла були проаналізовані 3 радіологами при наявності наступних ультразвукових характеристик: виражена гіпоехогенність, гіпоехогенність, ізоехогенність, гіперехогенність, наявність мікрокальцифікатів, груба кальцифікація, кальцифікація обідка, загострений край, розмір більше в довжину, ніж в ширину, неправильна форма, гіпоехогенний обідок і комірчаста структура. Були виміряні максимальні діаметри вузлів і товщина гіпоехогенного обідка. Значимі ультразвукові характеристики, як предиктори, були ідентифіковані за допомогою критеріїв хі-квадрат, критерію Фішера або відношення шансів. Ми порівняли діагностичну ефективність трьох УЗ критеріїв для визначення показань до FNA.
Результати. Мікрокальцифікація, розмір більше в довжину, ніж в ширину, виражена гіпоехогенність, гіпоехогенність, груба кальцифікація, неправильна форма і загострений край були значущими характеристиками злоякісних вузлів. Ізоехогенність, гіпоехогенний обідок і комірчаста структура були значущими характеристиками доброякісних вузлів. Обідкова і дугоподібна кальцифікація, гіперехогенність і товщина гіпоехогенного обідка були незначними ознаками. Серед трьох УЗ критеріїв для визначення показань для FNA, NFI показало найвищу діагностичну ефективність – 98,0% чутливість і 75,0% специфічність, а відношення шансів – 150.0.
Висновок. Ультразвукові характеристики вузлів щитоподібної залози, що не пальпуються, 1-2 см в діаметрі можуть бути використані для диференціальної діагностики злоякісних і доброякісних вузлів. Ультразвукові характеристики для злоякісних вузлів і комірчаста структура мають вагоме значення при виборі вузлів для біопсії і зниження частоти виконання FNA.
Введення
Вузлові утворення щитоподібної залози – дуже поширена патологія. Вона зустрічається у 4-7% дорослого населення і діагностується за допомогою пальпації. Протягом останніх 2-х десятиліть, широке використання ультразвукового дослідження для оцінки патології щитоподібної залози та шиї призвело до різкого збільшення поширеності захворювань щитоподібної залози без клінічних проявів, які, за оцінками літератури, складають від 20 до 76% в загальній популяції. Поширеність патології аналогічна тій, яка повідомляється в даних аутопсії у 50% у пацієнтів без анамнезу захворювань щитоподібної залози. Багато з цих вузлів додатково оцінювалися за допомогою FNA під ультразвуковим наведенням. Для того, щоб уникнути небажаного використання FNA у значної частини популяції в цілому, вкрай важливо визначити потенціал злоякісності уражень щитоподібної залози на основі їх ультрасонографічних особливостей.
Проте, на даний момент не існує рекомендацій показань до проведення FNA, тобто коли необхідно досліджувати вузол. Суспільство радіологів в звітах Ультразвукового Консенсусу і Американська асоціація патології щитоподібної залози (American Thyroid Association (ATA)) пропонують однакові принципи для вузлів щитоподібної залози менших 1 см, і більших 2 см: всі вузли щитоподібної залози, розміром менше 1 см не повинні піддаватися аспіраційної біопсії, а всі вузли більше, ніж 2 см повинні піддаватися FNA для цитологічної верифікації. З іншого боку, для вузлів розміром понад 1 см і рівним, або менше, ніж 2 см (1-2 см), показання для проведення FNA у цих двох організацій різні: товариство радіологів передбачає, що аспіраційна біопсія повинна бути виконана, якщо вузол щонайменше розміром 1 см з мікрокальціфікацією при ультразвуковому дослідженні, або вузол щонайменше розміром 1,5 см, переважно щільний або містить грубі кальцифікати. ATA рекомендує все вузли розміром понад 1 см піддавати FNA.
У багатьох дослідженнях доведено ефективність УЗ характеристик вузлів ЩЗ для диференціальної діагностики і прогнозування злоякісності. Однак, наскільки нам відомо, основні попередні дослідження були зосереджені на принципах проведення FNA під ультразвуковим наведенням для вузлів щитоподібної залози 1-2 см в діаметрі, що є спірним питанням. Таким чином, це дослідження було проведено з метою вивчення ультразвукових характеристик і оцінки відповідних рекомендацій для проведення FNA в вузлах ЩЗ, що не пальпуються, 1-2 см в діаметрі.
2. Матеріали та методи
2.1. Характеристика пацієнтів
У період з червня 2005 року по листопад 2006 року, проводився УЗ скринінг щитоподібної залози у 13,607 пацієнтів без клінічних симптомів у медичному скринінговому центрі Сеульського національного університетського госпіталю. Серед цих пацієнтів, FNA проведена в цілому в 919 вузлах щитоподібної залози сертифікованими радіологами. Патогістологічні результати FNA показали 588 доброякісних вузлів, 109 недетермінованих вузла, 120 недіагностованих вузла і 102 злоякісних вузла.
До групи злоякісних вузлів були включені 47 пацієнтів з 51 вузлом розміром 1-2 см. Всі діагнози були підтверджені після тиреоїдектомії в нашій лікарні (n = 29) та іншими лікарнями (n = 12), або тільки FNA без операції (n = 10). Всі двадцять дев’ять злоякісних вузлів, які видалені в нашому центрі, були раки папілярного типу. Серед пацієнтів було 20 чоловіків (42,6%) і 27 жінок (57,4%), їх вік становив від 31 до 77 років (середній вік 52,1 років).
До групи доброякісних вузлів були включені 66 пацієнтів з 72 вузлами ЩЗ розміром 1-2 см. Доброякісна природа вузлів була підтверджена як FNA, так і подальшим динамічним УЗ наглядом або FNA протягом 12 місяців. Обстежено 22 чоловіки (33,3%) і 44 жінки (66,6%), їх вік становив від 36 до 74 років (середній вік 55,4 років).
2.2. FNA (тонкоголкова аспіраційна біопсія)
FNA в нашій установі проводили для всіх вузлів ЩЗ 1-2 см в діаметрі, за винятком повністю кістозних вузлів. Для локалізації вузла для проведення біопсії проводили ультразвукове дослідження високочастотним лінійним датчиком (7-13 МГц) (GE Logic 9, системи GE Healthcare, Milwaukee, WI, і Philips IU 22, Philips Medical Systems, Bothell, WA). Вузли вимірювалися в 3-х площинах. FNA проводили за допомогою голки 23-25-го розміру на 10 мл шприці. УЗ наведення було використано для підтвердження правильності розміщення голки в вузлі. У вузол здійснювалося від одного до 3 проходів в залозу. Для частково кістозних вузлів, відбір тканини проводився в їх твердій частині. Зразки наносилися на предметне скло, негайно фіксувалися в 95% етанолі і забарвлювалися за допомогою методу Папаніколау. Радіологи визначали адекватність зразка тканини і число проходів. Два патогістологи з 7 і 6-річним досвідом роботи у відділенні патології щитоподібної залози, відповідно, інтерпретували результати цитології.
2.3. Аналіз зображень
Три радіолога з 8, 7 і 7-річним досвідом роботи в діагностиці патології щитоподібної залози, відповідно, вивчали ультразвукові зображення і обговорювали дані, поки не приходили до консенсусу. Всі УЗ особливості вивчалися на 21-дюймовому моніторі робочої станції Picture Archiving and Communication System (PACS).
Проаналізовано всі 123 вузла з тієї метою, щоб визначити існування будь-яких характерних УЗ особливостей злоякісних або доброякісних вузлів, про які повідомлялося в попередніх дослідженнях: виражена гіпоехогенність, гіпоехогенність, ізоехогенність, гіперехогенність, наявність мікрокальцифікатів, груба кальцифікація, кальцифікація обідка, загострений край, розмір більше в довжину, ніж в ширину, неправильна форма, гіпоехогенний обідок і коміркова структура. Гіпоехогенність визначалася, як зниження ехогенності вузла, в порівнянні з нормальною паренхімою щитоподібної залози, в той час як виражена гіпоехогенність визначалася, як зниження ехогенності в порівнянні з м’язом (рис. 1). Вузли розміром більше в довжину, ніж в ширину, визначалися, коли розмір у передньозадній площині був більше, ніж в поперечній площині (рис. 1).
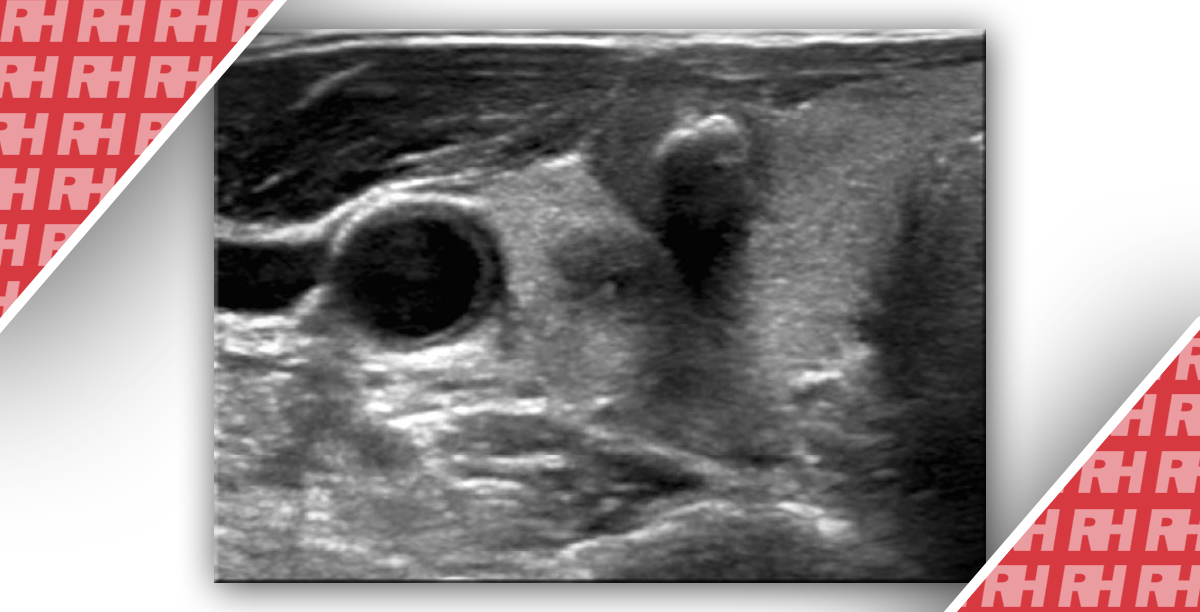
Рис. 1. Типовий злоякісний вузол щитоподібної залози у 50-річної пацієнтки. Сонограма показує 12-мм, з вираженою гіпоехогенністю вузол, з розміром більше в довжину, ніж в ширину, з нерівними і загостреними краями в правій частці. Видно інтранодулярні мікрокальцифікати (стрілка). Вузол має 5 ультразвукових характеристик, які характерні для злоякісного ураження. Після тиреоїдектомії було підтверджено наявність папілярного раку.
Коміркова структура визначалася як структура, що має безліч невеликих кістозних просторів з тонкими ехогенними стінками (рис. 2).
Рис. 2. Доброякісний вузол щитоподібної залози з комірчастою структурою у 56-річного пацієнта чоловічої статі. Поздовжня сонограма показує 11-мм, гіпоехогенний, вузол з комірчасткою структурою. У вузлі визначається кілька маленьких анехогенних кістозних порожнин. Цитологічне дослідження після FNA показало, що це доброякісне ураження.
Ми уникали області акустичного затінення при аналізі ехогенності вузлів, які мали осередки кальцифікації. Максимальні діаметри вузлів і товщина гіпоехогенного обідка вимірювалися за допомогою програмного забезпечення.
2.4. Статистичний аналіз
Максимальний діаметр вузлів і товщину гіпоехогенного обідка порівнювали за допомогою Т-критерію Стьюдента. Одновимірний аналіз індивідуальних УЗ характеристик між доброякісними і злоякісними групами проводили з використанням критерію хі-квадрат і критерію Фішера. Були проаналізовані специфічність і чутливість кожної з УЗ характеристик і 3 УЗ критеріїв для визначення показань для виконання FNA. Також було розраховано відношення шансів. Робоча характеристика приймача (Receiver operating characteristic – ROC) використовувалася для визначення візуального порогового значення сумарної кількості ультразвукових характеристик, які були значущими для злоякісного процесу в кожному вузлі. Статистичний аналіз проводили за допомогою пакета програм SPSS (версія 19.0, SPSS Inc., Chicago, IL) і MedCalc для ОС Windows (MedCalc, MedCalc версія програмного забезпечення 8.0.0.1; Mariakerke, Бельгія). Для всіх даних, р <0,05 вважалося статистично значущим.
3. Результати
3.1. Одновимірний аналіз
Не виявлено жодних істотних відмінностей за віком та статтю між пацієнтами зі злоякісними і доброякісними утвореннями. Максимальний діаметр вузла істотно не відрізнявся при злоякісному (13,5 ± 2,3 мм [середнє ± стандартне відхилення]) (р> 0,05) і доброякісному (13,2 ± 2,4 мм) процесі. У таблиці 1 представлені результати однофакторного аналізу УЗ характеристик, які спостерігалися у злоякісних і доброякісних вузлах 1-2 см в діаметрі.
Таблиця 1.
Одновимірний аналіз ультразвукових характеристик вузлових утворень щитоподібної залози розміром 1-2 см.
| Сонографічні характеристики | Злоякісні (n = 51) | Доброякісні (n = 72) |
Всього (n = 123) |
Значення р | Відношення шансів |
| Мікрокальцифікати A | 36 (70.6%) | 3 (4.2%) | 39 (31.7%) | <0.0001 | 55.2 (15.0–203.2 |
| Розмір більше в довжину, ніж в ширину A | 14 (27.5%) | 1 (1.4%) | 15 (12.2%) | <0.0001 | 26.8 (3.4–212.3) |
| Груба кальцифікація A | 11 (21.6%) | 1 (1.4%) | 12 (9.8%) | <0.0001 | 19.5 (2.4–156.8) |
| Виражена гіпоехогенність A | 16 (31.4%) | 2 (2.8%) | 18 (14.6%) | <0.0001 | 16 (3.5–73.5) |
| Загострений край A | 8 (15.7%) | 1 (1.4%) | 9 (7.3%) | 0.004 | 13.2 (1.6–109.3) |
| Неправильна форма A | 8 (15.7%) | 1 (1.4%) | 9 (7.3%) | 0.004 | 13.2 (1.6–109.3) |
| Гіпоехогенність A | 26 (50%) | 19 (26.8%) | 45 (36.6%) | 0.008 | 2.9 (1.4–6.2) |
| Ізоехогенність B | 9 (17.6%) | 48 (66.7%) | 57 (46.3%) | <0.0001 | 0.11 (0.05–0.26) |
| Комірчаста структура B | 0 | 11 (15.3%) | 11 (8.9%) | 0.003 | 0.000 |
| Гіпоехогенний обідок B | 4 (7.8%) | 22 (30.6%) | 26 (21.1%) | 0.003 | 0.19 (0.06–0.60) |
| Товщина гіпоехогенного обідка C | 0.75 ± 0.5 | 0.18 ± 0.4 | 7 (5.7%) | 0.092 | 3.8 (0.7–20.4) |
| Обідкова кальцифікація C | 5 (9.8%) | 2 (2.8%) | 3 (2.4%) | 0.125 | 0.0001 |
Числа в дужках – 95% ДІ.
A- діагностичні змінні для злоякісних вузлів щитоподібної залози.
B- діагностичні змінні для доброякісних вузлів щитоподібної залози.
C- діагностичні змінні були статистично незначущими.
Наявність мікрокальцифікатів, розмір більше в довжину, ніж в ширину, виражена гіпоехогенність, гіпоехогенність, груба кальцифікація, неправильна форма і загострений край – були значущими характеристиками для злоякісних вузлів (рис. 1, 3 і 4).
Рис. 3. Злоякісний гіпоехогенний вузол щитоподібної залози з у 58-річної пацієнтки. Поперечна сонограма показує 16,5 мм, гіпоехогенний вузол (стрілка). Жодна з інших УЗ характеристики не наводить на думку на злоякісність процесу. Після тиреоїдектомії було підтверджено наявність папілярного раку.
Рис. 4. Злоякісний вузол щитоподібної залози з грубою кальцификацією у 53-річного пацієнта чоловічої статі. Поперечна сонограма показує 13,1-мм, гіпоехогенний вузол з інтранодулярною грубою кальцифікацією (стрілки). Після тиреоїдектомії було підтверджено наявність папілярного раку.
Наявність мікрокальцифікатів показало найвище відношення шансів (55,2) при злоякісних пухлинах; потім – розмір більше в довжину, ніж в ширину (26,8), груба кальцифікація (19,5), виражена гіпоехогенність (16,0), загострений край (13,2), неправильна форма (13,2) і гіпоехогенність (2,9). Ізоехогенність, гіпоехогенний обідок і часточкова структура були суттєвими характеристиками для доброякісних вузлів (рис. 2 і 5). Обідкова кальцифікація (рис. 6), гіперехогенність і товщина гіпоехогенного обідка були статистично незначущими (р> 0,05).
Рис. 5. Типовий доброякісний вузол щитоподібної залози з ізоехогенністю і частковим гіпоехогенним обідком у 57-річної пацієнтки. Поздовжня сонограма показує 18,5-мм, ізоехогенний вузол з частково гіпоехогенним обідком. Ці ультразвукові характеристики можна було порівняти з доброякісним процесом. Цитологічне дослідження після FNA було негативним на наявність злоякісних клітин. Вузол не мав будь-яких ознак зміни розміру або форми через 17 місяців при повторному УЗ дослідженні.
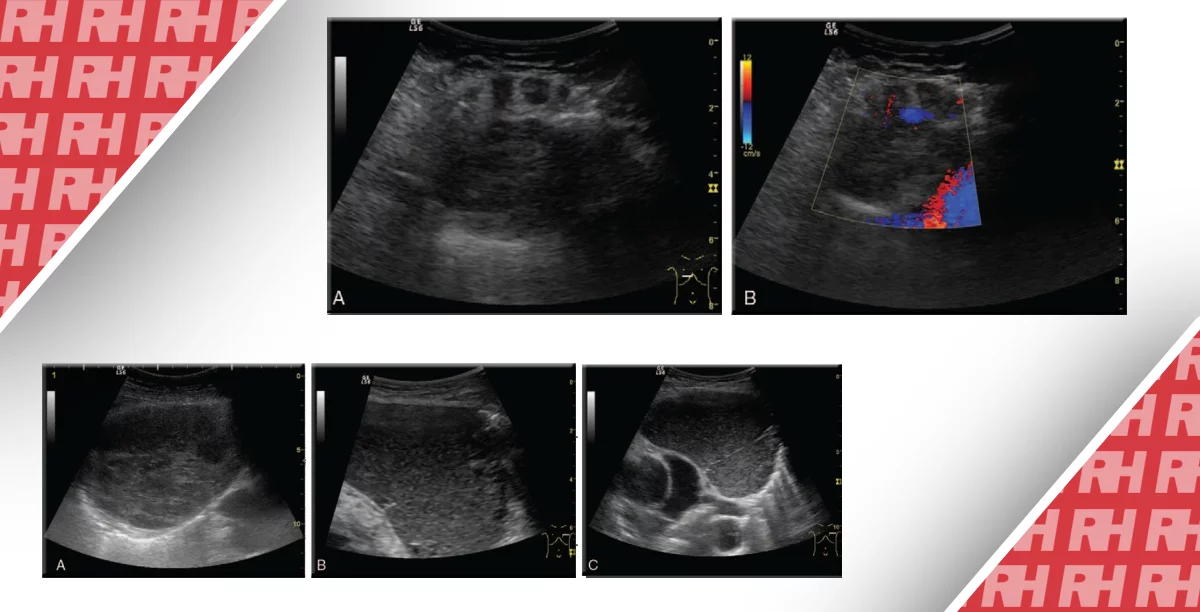
Рис. 6. Кальцифікація обідка. (А) Злоякісний вузол у 54-річної пацієнтки. Ультрасонограма показує 15-мм вузол з дугоподібною кальцифікацією (стрілка) і акустичною тінню в лівій частці. Вузлик має ізоехогенні ознаки, крім гіпоехогенної частини в зоні акустичної тіні. Він має розмір більше в довжину, ніж в ширину, що є однією з УЗ характеристик злоякісності. Після проведення FNA був запідозрений папілярний рак, що і було підтверджено після тиреоїдектомії в іншій лікарні. (В) Доброякісний вузол у 47-річної пацієнтки. Ультрасонограма показує 10,3-мм, вузол ЩЗ з обідковою кальцифікацією (вигнуті стрілки) в правій частці. Половина вузла прикрита акустичною тінню (пряма стрілка), а частина, що залишилася, майже ізоехогенна. Після проведення FNA виставлений діагноз аденоматозний зоб. Вузол не мав будь-яких ознак зміни розміру або форми через 12 місяців при повторному УЗ дослідженні.
У таблиці 2 наведені чутливість, специфічність, позитивна прогностична цінність (ППЦ) і негативна прогностична цінність (НПЦ) кожної із значущих УЗ характеристик. Наявність мікрокальцифікатів показала високу специфічність 85,8% і ППЦ – 92,1%. Ізоехогенність показала НПЦ – 85%. Розмір більше в довжину, ніж в ширину, виражена гіпоехогенність, груба кальцифікація, неправильна форма і загострений край показали високу специфічність і низьку чутливість. Комірчаста структура показала специфічність 100% і НПЦ – 100%, але низьку чутливість і ППЦ.
Таблиця 2
Діагностична ефективність для кожної із значущих ультразвукових характеристик вузлів щитоподібної залози розміром 1-2 см.
| Сонографічні характеристики | Чутливість (%) | Специфічність (%) | ППЦ (%) | НПЦ (%) |
| Мікрокальцифікати A | 70.6 (56.2–82.5) | 95.8 (88.3–99.1) | 92.3 | 82.1 |
| Розмір більше в довжину, ніж в ширину A | 27.5 (15.9–41.7) | 98.6 (92.5–99.8) | 93.3 | 64.7 |
| Груба кальцифікація A | 21.6 (11.3–35.3) | 98.6 (92.5–99.8) | 91.7 | 64.0 |
| Виражена гіпоехогенність A | 31.4 (19.1–45.9) | 97.2 (90.3–99.6) | 88.9 | 88.7 |
| Загострений край A | 15.4 (6.9–28.1) | 98.6 (92.4–99.8) | 88.9 | 61.4 |
| Неправильна форма A | 15.7 (7.0–28.6) | 98.6 (92.5–99.8) | 88.9 | 62.3 |
| Гіпоехогенність A | 50.9 (36.6–65.2) | 73.6 (61.9–83.3) | 57.8 | 67.9 |
| Ізоехогенність B | 82.5 (69.1–91.6) | 66.67 (54.6–77.3) | 66.7 | 85.0 |
| Комірчаста структура B | 15.3 (7.9–25.7) | 100.0 (93.0–100.0) | 45.5 | 100.0 |
| Гіпоехогенний обідок B | 30.6 (20.2–42.5) | 92.2 (81.1–97.8) | 48.5 | 84.6 |
Числа в дужках – 95% ДІ.
A- діагностичні змінні для злоякісних вузлів щитоподібної залози.
B- діагностичні змінні для доброякісних вузлів щитоподібної залози.
3.2. Ультразвукові критерії для визначення показань до FNA
Середнє число ультразвукових характеристик, важливих для злоякісних новоутворень у вузлі склала 2,1 ± 1,0 в групі злоякісних і 0,4 ± 0,7 в групі доброякісних новоутворень. Оптимальне граничне значення сумарного числа злоякісних УЗ ознак в вузлі було 2 або більше, які показували низьку чутливість – 78,5% і високу специфічність – 95.83%. Коли це порогове значення розглядалося як позитивне показання до проведення FNA (PFI-A) для виконання біопсії, 13 з 51 злоякісних вузлів були неправильно діагностовано як доброякісні, та виключені з показань для біопсії. Якщо граничне значення сумарного числа злоякісних УЗ ознак в вузлі встановлювалося як 1 або більше, для збільшення чутливості PFI-A, чутливість ставала набагато вище – 98,0%, специфічність ставала значно нижче – 70,8%. Коли це порогове значення розглядалося як позитивне показання до проведення FNA (PFI-B) для виконання біопсії, 51 з 72 справжніх доброякісних вузлів, і 1 з 51 справжніх злоякісних вузлів були виключені з показань для біопсії. Три доброякісні вузла, які показали комірчасту структуру, були помилково діагностовано як злоякісні новоутворення, оскільки ці вузли були гіпоехогенними. Для підвищення специфічності PFI-B, ознака – комірчаста структура була додана в якості одного з УЗ критеріїв для визначення показань до проведення FNA, з огляду на її специфічність, близьку до 100%. УЗ критерії для визначення відсутності показань для проведення FNA (NFI) (не виконувати біопсію) були згруповані наступним чином: (1) вузол має комірчасту структуру, або (2) вузол не має жодної з ультразвукових характеристик, характерних для злоякісних новоутворень. Якби застосовувалося NFI, 54 з 72 (75%) справжніх доброякісних вузлів і 1 з 51 (1.9%) справжніх злоякісних вузла (рис. 7) були б виключені з біопсії (рис. 8).
Рис. 7. Злоякісний вузол щитоподібної залози з УЗ характеристиками, що свідчать про доброякісному вузлі у 46-річної пацієнтки. Поздовжня сонограма показує 15-мм, ізоехогенний вузол з гіпоехогенним обідком (стрілка). УЗ характеристики узгоджуються з доброякісними вузлами. Після тиреоїдектомії було підтверджено наявність папілярного раку.
Рис. 8. Графік показує зменшення кількості FNA, коли застосовується NFI для виключення вузлів з біопсії. 54 з 72 (75%) справжніх доброякісних вузлів і 1 з 51 (1,9%) справжніх злоякісних вузлів виключені з біопсії.
Benign – доброякісні, Malignant – злоякісні.
Чутливість і специфічність NFI була 98,0% та 75,0%, відповідно. NFI показало найвище відношення шансів (150.0) серед 3-х УЗ критеріїв. У таблиці 3 наведена діагностична ефективність 3 УЗ критеріїв для визначення показань до виконання FNA.
Таблиця 3
Діагностична ефективність запропонованих ультразвукових критеріїв для визначення показань до FNA вузлів щитоподібної залози розміром 1-2 см.
| Сонографічні характеристики | Чутливість (%) | Специфічність (%) | ППЦ (%) | НПЦ (%) | Значення р | Відношення шансів |
| PFI-A | 74.5 | 95.8 | 92.7 | 84.1 | <0.0001 | 67.2 (18.0–250.7) |
| PFI-B | 98.0 | 70.8 | 70.4 | 98.1 | <0.0001 | 121.4 (15.7–937.3) |
| NFI | 98.0 | 75.0 | 73.5 | 98.2 | <0.0001 | 150.0 (19.3–1165.3) |
Числа в дужках 95% ДІ.
ППЦ: позитивна прогностична цінність. НПЦ: негативна прогностична цінність.
4. Обговорення
Це дослідження було зроблено з метою визначення ефективності використання УЗ характеристик вузлів щитоподібної залози, що не пальпуються, 1-2 см в діаметрі для відбору пацієнтів для біопсії і обмеження частоти виконання процедури FNA. Наявність мікрокальцифікатів, розмір більше в довжину, ніж в ширину, виражена гіпоехогенність, гіпоехогенність, груба кальцифікація, неправильна форма і загострений край були значущими характеристиками злоякісного процесу в цьому дослідженні. Наш результат, в цілому, подібний до попередніх досліджень, в яких були проаналізовані велика кількість даних з декількох установ. Проте, така УЗ характеристика, як неправильна форма вузла не була статистично значущою ознакою в попередньому дослідженні, що не узгоджується з нашим результатом. Наше попереднє дослідження показало, що гіпоехогенність є незначущою ознакою для злоякісних вузлів. Проте, дана ознака виявилася значущою для злоякісної пухлини в даному дослідженні. У нашому закладі FNA проводиться в вузлах розміром 1 см або менше, тільки якщо вони мають УЗ особливості, характерні для злоякісного процесу. У той же час, всі пацієнти з вузлами розміром більше 1 см, спрямовуються для проведення FNA, якщо вони не є повністю кістозними. У нашому попередньому дослідженні, гіпоехогенні вузли <1 см, які не мали ознак кальцифікації, розмір більше в довжину, ніж в ширину або загострений край, не були включені до досліджувану групу. Ця різниця показань до проведення FNA, в залежності від розміру вузлів, викликала зсув вибірки в попередньому дослідженні. Таким чином, можна припустити, що результат цього дослідження більш гомогенної групи є більш надійним. Груба кальцифікація відома як особливість доброякісних вузлів, особливо при великій тривалості захворювання. Проте недавні дослідження показали, що груба кальцифікація значно частіше зустрічається при злоякісних вузлах, що відповідає даним цього дослідження.
Ізоехогенність, гіпоехогенний обідок і комірчаста структура були значущими характеристиками для доброякісних вузлів. Результати добре узгоджуються з результатами попередніх даних, які показали, що більшість гіперпластичних або аденоматозних вузлів є ізоехогенними в порівнянні з нормальною тканиною щитоподібної залози. Комірчаста структура дуже специфічна для доброякісних вузлів, але ця ознака зустрічається рідше. Наше дослідження також показало, що тільки близько 15% доброякісних вузлів мали комірчасту структуру. Гіпоехогенний обідок, який з’являється при компресії нормальної тканини щитоподібної залози або капсули, з високою ймовірністю свідчить про доброякісну природу вузла. Раніше проведене дослідження показало аналогічний нашому аналізу результат, що говорить про те, що відсутність гіпоехогенного обідка пов’язана з ризиком злоякісного новоутворення. Гіперехогенність – відома ознака, яка характерна доброякісним вузлам. У нашому дослідженні, всі гіперехогенні вузли також були доброякісними. Що стосується обідкової кальцифікації, не отримано достатньої кількості даних для визначення, чи пов’язана ця ознака із злоякісною пухлиною. У дослідженні 65 ЩЗ, обідок кальцифікації значно частіше визначався при доброякісних вузлах (81,5%), ніж в злоякісних (18,5%). Проте, в нашому дослідженні, обідкова кальцифікація спостерігалася як в злоякісних, так і доброякісних вузлах, без будь-якої істотної відмінності. 5 з 7 вузлів з обідковою кальцифікацією були злоякісними і мали, принаймні, 1 злоякісну УЗ характеристику. Тому всі вони були правильно класифіковані, як злоякісний вузол по УЗ критеріям в NFI. При аналізі УЗ характеристик двох інших доброякісних вузлів з обідковою кальцифікацією, один з них мав злоякісні УЗ характеристики, а інший показав типові УЗ характеристики для доброякісного процесу. Сама кальцифікація обідка не впливає на діагностику злоякісних вузлів. Таким чином, передбачається, що вузли з обідковою кальцифікацією повинні бути проаналізовані на підставі УЗ характеристик твердої частини, уникаючи зони акустичного затінення.
У цьому дослідженню NFI значно скоротило число випадків виконання FNA, 75% в доброякісних вузлах, навіть незважаючи на те, що 2% злоякісних вузлів (1 випадок) було неправильно діагностовано. З огляду на помітно збільшену кількість виявлення вузлів щитоподібної залози, що не пальпуються,за допомогою ультразвукового дослідження і низькою смертністю від раку щитоподібної залози, діагностична ефективність NFI може бути прийнятним алгоритмом дій. PFI-A може бути недоречно в якості орієнтира для проведення FNA через низьку чутливість. PFI-В, через високу чутливість, є більш доречним, в якості орієнтира, для проведення FNA, ніж PFI-A. Проте, NFI показав кращу діагностичну ефективність. Показана більш висока специфічність, при тій же чутливості, в порівнянні з PFI-B. Підвищення специфічності було результатом включення характеристики комірчастої структури в якості одного з УЗ критеріїв для NFI. Ознака комірчастої структури показала 100% специфічність для доброякісних вузлів в нашому дослідженні, що було майже аналогічно результату попереднього дослідження. У дослідженні, в якому аналізується УЗ зразок вузлів щитоподібної залози, передбачається, що вузол з комірчастою структурою не вимагає біопсії. Таким чином, комірчаста структура, як вважають, є відмінним УЗ критерієм для відмови від біопсії.
В даному дослідженні були використані ультразвукові характеристики злоякісного процесу і чарункова структура для вибору вузлів для аспіраційної біопсії, які виявилися ефективними для зниження частоти проведення біопсії, при збереженні діагностичної ефективності. Був діагностований тільки один злоякісний вузол, який мав типові доброякісні УЗ характеристики: ізоехогенність і гіпоехогенний обідок, без будь-яких ознак злоякісності. Проте, було помітно, що гіпоехогенний обідок мав неоднорідну товщину. Якщо проаналізувати нерівномірність і товщину гіпоехогенного обідка в значній кількості вузлів, то можливо це допоможе в ефективності проведення відмінностей між злоякісними і доброякісними вузлами. У нашому дослідженні гіпоехогенний обідок злоякісних вузлів був товщий, ніж у доброякісних вузлів. Однак, кількість злоякісних вузлів, що мають гіпоехогенний обідок, була занадто мала для того, щоб бути статистично значущою. Гіперехогенність показала 100% чутливість і НПЦ для доброякісних вузлів в попередніх дослідженнях. У нашому дослідженні, кількість гіперехогенних вузлів була занадто мала, щоб бути статистично значущою, хоча всі вузли були доброякісними. У той же час, гіперехогенність може бути потенційним відмінним УЗ критерієм для відмови від біопсії, і, відповідно, зменшення числа FNA.
Фолікулярні і медулярні карциноми нерідко бувають ізоехогенними, і можуть бути діагностовані, як доброякісні вузли, в разі використання запропонованих нами УЗ критеріїв. Таким чином, діагностична точність УЗ критеріїв може бути трохи знижена, якщо пацієнти з цими двома типами раку були б включені в досліджувану групу.
Сцинтіграфія щитоподібної залози також є відмінним інструментом фільтрації доброякісних вузлів, так як вузли з гіперфункцією (“гарячі”) майже ніколи не є злоякісним процесом. Проте, роль сцинтіграфії обмежена в якості першого етапу оцінки вузлів щитоподібної залози в країнах з багатою на йод дієтою, де ультразвукове і гормональне дослідження щитоподібної залози дозволяє коректно діагностувати поодинокі вузли.
Більшість карцином щитоподібної залози є папілярного типу (75-80%), які ростуть дуже повільно і часто безсимптомно. Решта включають: фолікулярні (10-20%), медулярні (3-50%) і анапластичні (1-2%) типи. У нашому дослідженні, всі раки були папілярного типу. Відсутність різниці гістологічного спектру в даному дослідженні може бути пов’язана з вибором безсимптомних пацієнтів з програми скринінгу. Існують сумніви про користь діагностики злоякісних пухлин з низьким рівнем ризику, таких як малі папілярні карциноми. З даних літератури відомо, що сукупний ризик екстракапсулярної інвазії і метастазів в лімфатичних вузлах, пов’язаних зі збільшенням розміру вузлів, більш очевидний в вузлах папілярного типу, ніж при фолікулярному типі. Ризик віддалених метастазів збільшується після того, як розмір первинної пухлини стає 2 см. Дослідження припускає, що рання діагностика раку щитоподібної залози може зменшити ризик рецидиву і смертності.
Результати нашого дослідження можуть мати два обмеження. По-перше, це дослідження має ретроспективний дизайн. По-друге, радіологи аналізують УЗ зображення PACS не в режимі реального часу.
На закінчення, для вузлів щитоподібної залози, що не пальпуються, 1-2 см в діаметрі, УЗ характеристики можуть бути використані для диференціальної діагностики злоякісних і доброякісних вузлів. Злоякісні УЗ характеристики і комірчаста структура мають істотне значення при виборі вузлів для біопсії і зниження частоти процедури FNA. Для проведення досліджень рекомендуємо використовувати апарат від компании GE Voluson E8.

























14.10.2019
Вова