🤖 Короткий переказ від ШІ
Дослідження порівнює ефективність та безпеку черезшкірної біопсії печінки під контролем УЗД та ендоскопічної тонкоголкової аспірації під контролем ендоскопічного УЗД (EUS-FNA) для діагностики пухлин печінки. Основним висновком є те, що EUS-FNA демонструє вищу безпеку та діагностичну точність, особливо для пухлин, розташованих у важкодоступних місцях.
EUS-FNA показала 100% точність та значно нижчу частоту небажаних явищ (2%) порівняно з черезшкірною біопсією (17%), хоча остання забезпечувала довші зразки. Для повного розуміння технічних аспектів та вибору найкращого методу діагностики, особливо з урахуванням сучасних УЗД апаратів, важливо ознайомитися з усіма деталями дослідження.
✅ Ключові тези зі статті:
- Діагностика: EUS-FNA має вищу діагностичну точність (100%) порівняно з черезшкірною біопсією (96%).
- Лікування: Вибір методу біопсії залежить від локалізації та візуалізації пухлини, при цьому EUS-FNA є кращим для пухлин, що важко візуалізуються через УЗД.
- Переваги: EUS-FNA забезпечує вищу безпеку з меншою частотою небажаних явищ (2% проти 17%).
- Обмеження: Черезшкірна біопсія може бути складнішою для пухлин, розташованих поблизу шлунково-кишкового тракту або в лівій/хвостатій частках печінки.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: Yuichi Takano, Jun Noda, Masataka Yamawaki, Tetsushi Azami, Takahiro Kobayashi, Fumitaka Niiya, Naotaka Maruoka, Tomoko Norose, Nobuyuki Ohike, Tetsuji Wakabayashi, Kenichi Matsuo, Kuniya Tanaka, Masatsugu Nagahama
Зміст:
- Вступ
- Матеріали та методи
- Метод біопсії
- Визначення небажаних явищ (включаючи ступінь тяжкості)
- Результати
Вступ
В останні роки відбулися помітні успіхи у діагностичній візуалізації, і в результаті більшість пухлин печінки можна діагностувати без патологічного обстеження. Оскільки біопсія печінки пов’язана з ризиком кровотечі та посіву голкового тракту, гістологічне дослідження не є необхідним у випадках, які можна діагностувати за допомогою візуалізації або при підозрі на злоякісне новоутворення та призначення операції. Однак у деяких випадках все ще потрібна гістологічна оцінка, у тому числі при атипових результатах візуалізації, пухлинах, у яких важко розрізнити на доброякісні та злоякісні утворення, та метастатичних пухлинах печінки у випадках з множинними злоякісними новоутвореннями.
Черезшкірна біопсія під контролем УЗД часто виконується з високою діагностичною точністю. Однак поняття біопсії пухлини печінки за допомогою тонкоголкової аспірації під ендоскопічним ультразвуковим контролем (EUS-FNA) було вперше введено в 1999 р. EUS-FNA показана при невеликих пухлинах печінки або при утрудненні біопсії іншими методами. Однак жодне дослідження не порівнювало ці два методи біопсії, і в деяких випадках вибір методу біопсії може бути скрутним у клінічній практиці.
Матеріали та методи
Ретроспективне дослідження було проведено з використанням медичних карток пацієнтів, які перенесли біопсію пухлини печінки в нашій лікарні з 2012 по 2019 рік. Випадки були поділені на дві групи для порівняння: група черезшкірної біопсії під ультразвуковим контролем (черезшкірна група) та ендоскопічної тонкоголкової аспірації під ультразвуковим контролем (EUS-FNA група). Рішення про проведення черезшкірної біопсії або EUS-FNA приймалось лікарем.
Перед біопсією були виконані УЗД черевної порожнини та комп’ютерна томографія (КТ). Черезшкірна біопсія була виконана пацієнтам, у яких ураження можна було легко візуалізувати за допомогою УЗД черевної порожнини. Навпаки, EUS-FNA була обрана для випадків, коли було важко візуалізувати ураження за допомогою УЗД черевної порожнини, а також для пухлин, розташованих поблизу шлунково-кишкового тракту (шлунка або дванадцятипалої кишки).
Були вивчені клінічне тло, процедура біопсії, діагностичні можливості та побічні ефекти. Визначення злоякісного – це «випадок з гістологічно злоякісними ознаками», а доброякісними – випадки з «гістологічно доброякісними результатами та відсутністю росту пухлини навіть після одного року спостереження».
Дослідження проводилося з дозволу Комітету з етики Університету Сева.
Метод біопсії
Черезшкірна біопсія була виконана з використанням анальгетика (пентазоцин 15 мг) і пухлина печінки була візуалізована за допомогою УЗД черевної порожнини. На шкірі робили невеликий розріз скальпелем, і пухлина проколювалася 1-2 рази пункційною голкою 16-G tru-cut.
EUS-FNA проводилася шляхом введення аналгетиків та седативних засобів (петидину гідрохлорид 35 мг або пентазоцин 7,5-15 мг + мідазолам 2-5 мг). Використовувалися ендоскоп GF-UCT260 (Olympus Medical Systems, Токіо, Японія) та пристрій спостереження UE-ME1 або UE-ME2 (Olympus Medical Systems). Діаметр голки для пункції становив 19-25 G і вибирався на розсуд лікаря. Кількість ходів становила 10-20, а тиск всмоктування становив 10-20 см3 негативного тиску. Швидка оцінка цитології на місці не проводилася в жодній із груп. Черезшкірна біопсія печінки була виконана 4 лікарями, кожен з яких мав досвід більш ніж 30 випадків. EUS-FNA була проведена 3 ендоскопістами з досвідом роботи з більш ніж 50 випадками.
Визначення небажаних явищ (включаючи ступінь тяжкості)
Використовувалося визначення небажаних явищ, встановлених на семінарі Американського товариства гастроінтестинальної ендоскопії (ASGE). У цьому дослідженні біль був визначений як «біль, який вимагає застосування аналгетиків протягом 24 годин після процедури».
Статистичний аналіз
Статистичний аналіз проводився з використанням t-критерію Стьюдента та критерію chi-square для порівняння двох груп, і значення p<0,05 вважалися такими, що показують статистично значущу різницю.
Результати
Усього було включено 106 пацієнтів (47 у групі черезшкірної та 59 у групі EUS). Середній вік пацієнтів становив 68 (від 32 до 87) років, із них 60 були чоловіками, а 46 – жінками. Загалом 100 пацієнтам було поставлено остаточний діагноз злоякісного новоутворення, включаючи метастатичну пухлину печінки у 45 випадках та наступні первинні пухлини:
- рак підшлункової залози, 10 випадків;
- колоректальний рак – 9 випадків;
- рак легень – 7 випадків;
- рак грудей – 5 випадків;
- рак жовчного міхура – 3 випадки;
- рак стравоходу – 2 випадки;
- рак шлунка – 2 випадки;
- нейроендокринна пухлина підшлункової залози – 2 випадки;
- нейроендокринна карцинома підшлункової залози – 1 випадок;
- нирково-клітинний рак – 1 випадок;
- колоректальна нейроендокринна пухлина – 1 випадок;
- рак яєчників – 1 випадок;
- стромальна пухлина тонкої кишки – 1 випадок.
Крім того, було 32 випадки холангіоцелюлярної карциноми, 18 випадків гепатоцелюлярної карциноми, 4 випадки злоякісної лімфоми та 1 випадок лейоміосаркоми. Загалом 6 пацієнтам було поставлено остаточний діагноз доброякісної пухлини, включаючи два випадки абсцесу печінки, один випадок фокальної вузлової гіперплазії, один випадок запальної псевдопухлини, один випадок саркоїдозу печінки та один випадок некротичної тканини.
Порівняння процедури біопсії між двома групами
| Показник | Черезшкірна група (n = 47) | Група EUS (n = 59) |
| Голка | 16G во всех случаях | 19G: 5%, 22G: 61%, 25G: 34% |
| Діаметр ураження, середній діапазон | 62 мм (12-167) | 34 мм (6-170) |
| Ураження правої долі | 70% (33/47) | 28% (17/59) |
| Ураження лівої долі | 30% (14/47) | 64% (38/59) |
| Ураження хвостатої долі | 0% | 7% (4/59) |
| Імунофарбування | 74% (35/47) | 68% (40/59) |
| Довжина зразка, середній діапазон | 9,7 мм (3,1-14,4) | 3,3 мм (1,1-6,8) |
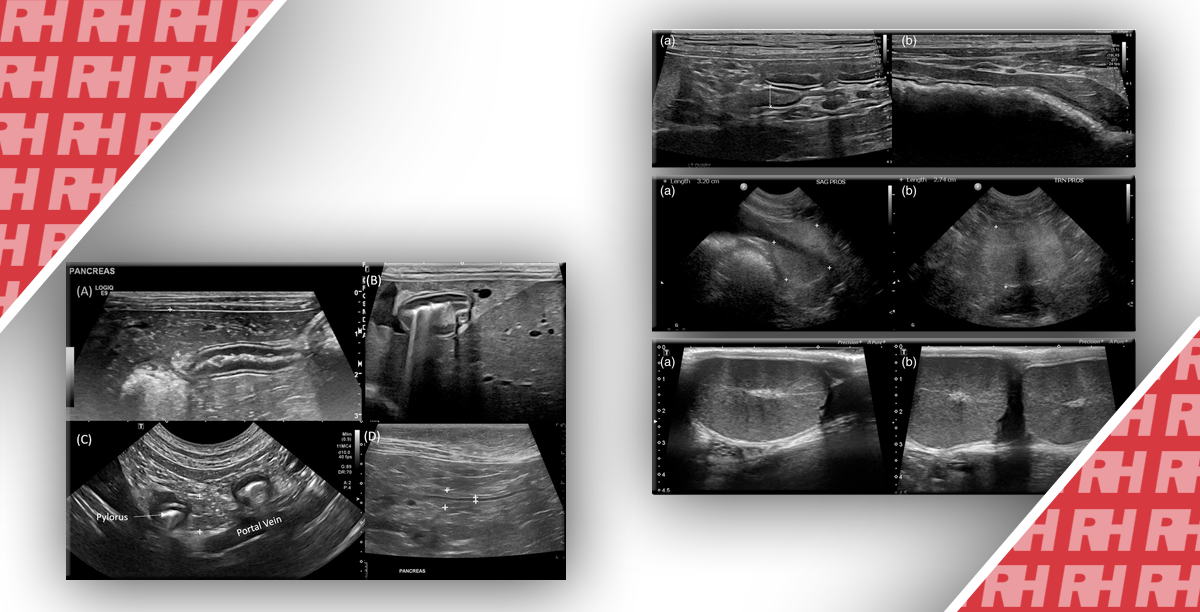
Зображення 1: a: КТ черевної порожнини з контрастним посиленням показала велику пухлину з кістозною дегенерацією у хвості підшлункової залози та невеликими метастазами в печінці у хвостатій частині (стрілка). Оскільки дисемінація та інфекція внаслідок біопсії пухлини підшлункової залози викликали побоювання, ми вирішили провести біопсію метастазів у печінці. b: УЗД черевної порожнини виявило неясну пухлину в хвостатій частині (стрілка). У цьому випадку черезшкірна біопсія була утруднена. c: Пухлина печінки в хвостатій частині легко візуалізувалася за допомогою EUS (стрілка), а EUS-FNA виконувалася за допомогою голки 22-G. d: Патологічним діагнозом була аденокарцинома, що відповідала метастазу раку підшлункової залози, і розпочато хіміотерапію. Ad: аденокарцинома, H: гепатоцит (фарбування гематоксиліном та еозином, × 400)
Зображення 2: а: Випадок із раком яєчників, раком щитовидної залози та колоректальним раком в анамнезі. Комп’ютерна томографія черевної порожнини виявила пухлину розміром 30 мм у 6 сегменті печінки. Потрібно було гістологічне дослідження для ідентифікації первинної пухлини, яка дала початок метастазам. b: Гіперехогенна пухлина чітко візуалізувалася при УЗД черевної порожнини. Виконана черезшкірна біопсія. c: Виявлено аденокарциному з веретеноподібними ядрами. Пацієнту встановлено діагноз: метастаз колоректального раку в печінку. Ad: аденокарцинома, H: гепатоцит (фарбування гематоксиліном та еозином, × 400)
Зображення 3: a: КТ черевної порожнини виявила пухлину неправильної форми розміром 30 мм у 8 сегменті печінки. Перед печінкою розташовувалась висхідна та поперечна ободова кишка (синдром Чилайдіті). Гістологічне дослідження знадобилося для хіміотерапії, бо пацієнтка відмовилася від операції. b: Було важко візуалізувати пухлину через наявність газів у шлунково-кишковому тракті (стрілка) на УЗД черевної порожнини. c: EUS змогла візуалізувати пухлину без впливу шлунково-кишкового газу. EUS-FNA виконували з цибулини дванадцятипалої кишки. d: У пацієнта діагностована внутрішньопечінкова холангіоцелюлярна карцинома. Ad: аденокарцинома, H: гепатоцит (фарбування гематоксиліном та еозином, × 400)
Пункційні голки, використані у групі черезшкірних втручань, були Tru-Cut типу 16-G у всіх випадках, а голки, використані у групі EUS, були голками 19-G у 5% (3 випадки), 22-G у 61% (36 випадків), і 25-G на 34% (20 випадків).
Середній діаметр ураження становив 62 (діапазон 12–167) мм у групі черезшкірного введення, але був значно меншим (34 мм; діапазон 6–170 мм) у групі EUS (p<0,01). У черезшкірній групі локалізація уражень склала 30% (14 випадків) у лівій частці та 70% (33 випадки) у правій частці. У групі EUS локалізація вогнищ склала 64% (38 випадків) у лівій частці, 28% у правій частці (17 випадків) та 7% (4 випадки) у хвостатій частці. У черезшкірній групі було більше пухлин правої частки, тоді як у групі EUS було більше пухлин лівої частки (p<0,01). EUS-FNA виконувалася як трансшлункова пункція у 72% випадків та як трансдуоденальна пункція у 28% випадків.
Імунофарбування було виконано у 74% (35/47) у групі черезшкірного введення та у 68% (40/59) у групі EUS, при цьому значних відмінностей не виявлено. Імунофарбування проводилося на розсуд патологоанатома. Таким чином, імунофарбування не проводилося у випадках, які можна було діагностувати лише за допомогою фарбування гематоксилін-еозином.
Середня довжина зразка становила 9,7 (діапазон 3,1-14,4) мм у групі черезшкірної біопсії та 3,3 (діапазон 1,1-6,8) мм у групі EUS; Таким чином, зразки були значно довшими у групі черезшкірної біопсії (p<0,05). Область ворітної вени не могла бути оцінена через велику кількість випадків злоякісних пухлин, так як іноді область ворітної вени заміщалася пухлинною тканиною.
Діагностична здатність та небажані явища
| Показник | Черезшкірна група (n = 47) | Група EUS (n = 59) |
| Чутливість | 95% (43/45) | 100% (55/55) |
| Специфічність | 100% (2/2) | 100% (4/4) |
| Точність | 96% (45/47) | 100% (59/59) |
| Небажані явища | 17% (8/47) | 2% (1/59) |
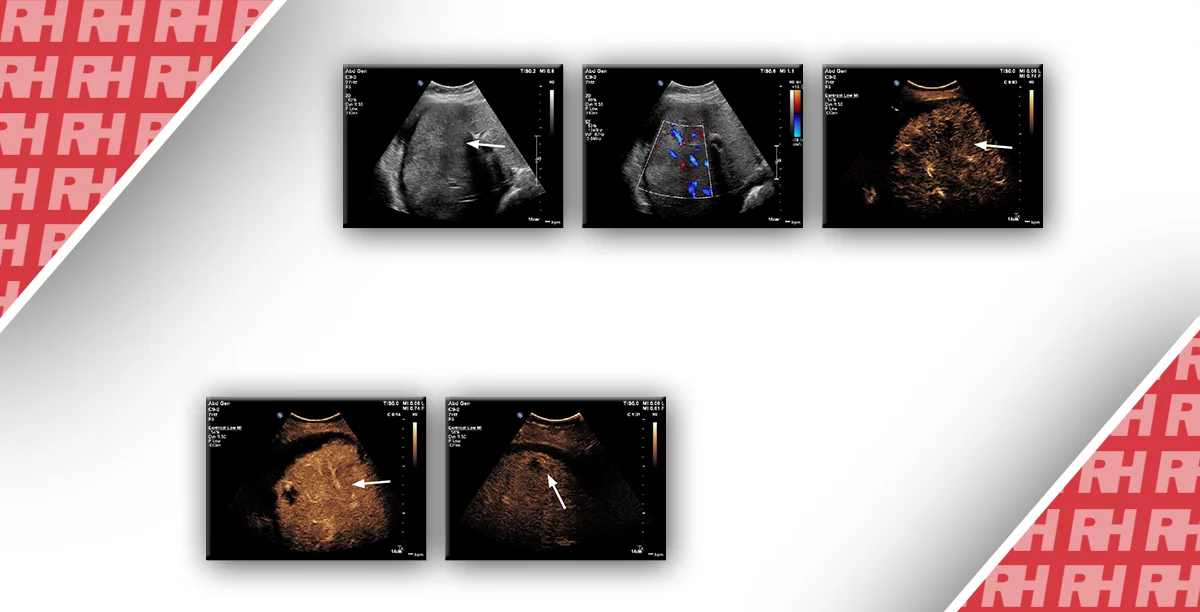
Зображення 4: а: УЗД черевної порожнини показує численні гіпоехогенні утворення печінки. При оцінці всього тіла не вдалося виявити будь-яких явних первинних уражень, і перед хіміотерапією було проведена черезшкірна біопсія печінки. У хворого діагностована внутрішньопечінкова холангіоцелюлярна карцинома. В цьому випадку антитромботичний препарат не приймався, кількість тромбоцити та коагуляційна здатність були в нормі. b: Наступного дня після біопсії пацієнт поскаржився на біль у животі, у нього було зниження артеріального тиску та тахікардія. Спостерігалося зниження гемоглобіну в крові (з 9,5 до 6,8 г/дл), було виконано переливання крові. Комп’ютерна томографія з контрастним посиленням показала екстравазацію поверхні печінки (стрілка). c: Ангіографія показала екстравазацію від периферії правої печінкової артерії (стрілка) і була виконана транскатетерна артеріальна емболізація.
Черезшкірна біопсія показала, що 43 випадки були злоякісними, а 4 випадки доброякісними. У двох із чотирьох доброякісних випадків пухлина зникла мимовільно, і діагноз не змінився; однак у двох випадках пухлина збільшилася в розмірах, і знову була проведена черезшкірна біопсія. В обох випадках була виявлена аденокарцинома, діагноз був змінений з доброякісного на злоякісний.
EUS-FNA діагностувала 55 випадків як злоякісні та 4 випадки як доброякісні. У чотирьох доброякісних випадках пухлини не спостерігалися навіть після одного року спостереження і діагноз не змінився.
Чутливість, специфічність та точність процедури становили 95%, 100% та 96% у групі черезшкірного введення та 100%, 100% та 100% у групі EUS, відповідно, не показуючи істотної різниці.
Небажані явища були зареєстровані у 17% випадків черезшкірної терапії [легкий біль у 6 випадках, помірна кровотеча у 1 випадку (проведено переливання крові та інтервенційна радіологія), легка інфекція у 1 випадку], при цьому значно менша частота була зареєстрована у групі EUS ( 2 %;слабкий біль у 1 випадку;p<0,01). Середній період спостереження становив 3,4 (діапазон 0,3-7) років у групі черезшкірного введення та 2,5 (діапазон 0,6-5) років у групі EUS; випадків дисемінації голкового тракту немає.
Поширені запитання та відповіді
Які два методи біопсії печінки порівнюються у дослідженні?
- У дослідженні порівнюються два методи біопсії печінки: черезшкірна біопсія під контролем ультразвуку (УЗД) та ендоскопічна тонкоголкова аспірація під контролем ендоскопічного ультразвуку (EUS-FNA).
Коли зазвичай потрібна гістологічна оцінка пухлин печінки?
- Гістологічна оцінка пухлин печінки потрібна у випадках атипових результатів візуалізації, коли важко розрізнити доброякісні та злоякісні утворення, а також при метастатичних пухлинах печінки у випадках з множинними злоякісними новоутвореннями.
Які основні відмінності у показаннях до застосування черезшкірної біопсії та EUS-FNA?
- Черезшкірна біопсія під контролем УЗД часто використовується, коли ураження легко візуалізується за допомогою УЗД черевної порожнини. EUS-FNA показана для невеликих пухлин печінки, коли важко візуалізувати ураження за допомогою УЗД черевної порожнини, або для пухлин, розташованих поблизу шлунково-кишкового тракту.
Які голки використовувалися для кожного методу біопсії?
- Для черезшкірної біопсії використовувалася пункційна голка типу Tru-Cut 16-G у всіх випадках. Для EUS-FNA використовувалися голки діаметром 19-G (5%), 22-G (61%) та 25-G (34%).
Яка була середня довжина зразка, отриманого під час біопсії?
- Середня довжина зразка у групі черезшкірної біопсії становила 9,7 мм, тоді як у групі EUS-FNA – 3,3 мм. Зразки були значно довшими у групі черезшкірної біопсії.
Яка була частота небажаних явищ при обох методах біопсії?
- Частота небажаних явищ була вищою у групі черезшкірної біопсії (17%), що включало легкий біль, помірну кровотечу та легку інфекцію. У групі EUS-FNA частота небажаних явищ була значно нижчою (2%), переважно у вигляді легкого болю.
Яка діагностична точність обох методів?
- Діагностична точність обох методів була високою: чутливість, специфічність та точність становили 95%, 100% та 96% для черезшкірної біопсії відповідно, та 100%, 100% та 100% для EUS-FNA відповідно. Істотної різниці не виявлено.