Автори: Marco Di Serafino, Valerio Vitale, Rosa Severino, Luigi Barbuto, Norberto Vezzali, Federica Ferro, Eugenio Rossi, Maria Grazia Caprio, Valeria Raia, Gianfranco Vallone
Вступ
Підшлункова залоза легко досліджується у дітей завдяки відносній відсутності жирової тканини і великій лівій долі печінки з оптимальним акустичним вікном.
Широкий спектр патологічних станів підшлункової залози можна ідентифікувати і контролювати за допомогою УЗД, хоча вони відносно рідко зустрічаються в дитинстві в порівнянні з дорослим віком. Знайомство з нормальним зовнішнім виглядом і захворюваннями, які зазвичай вражають цю залозу, важливо для точної і своєчасної діагностики у дітей.
В рамках цієї статті ми включаємо огляд анатомії, техніки УЗД і сонографычних аспектів підшлункової залози в педіатричному віці, а також короткий опис найбільш поширених вроджених, запальних, системних захворювань, пухлинних і травматичних пошкоджень, які в першу чергу впливають на підшлункову залозу.
Анатомія, техніка і сонографічні аспекти
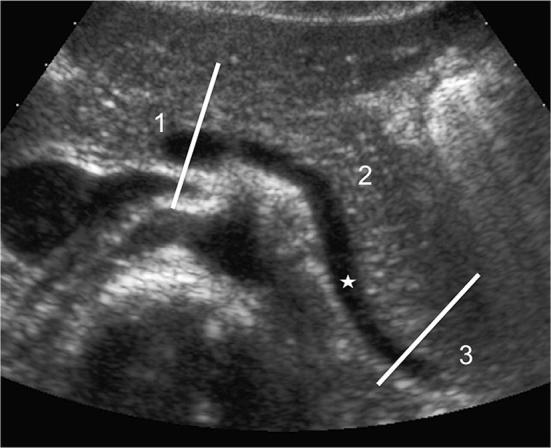
Підшлункова залоза розташована в передньому принирковому просторі, в заочеревинному просторі, і спрямована похило, а її головна частина розташована праворуч, на рівні нижче хвоста. Головка укладена в дуоденальній западині, а хвіст – між шлунком і селезінкою. Верхні черевні судини, поряд з верхніми судинами брижі і віссю селезінкової вени, являють собою важливий анатомічний орієнтир для підшлункової залози (зобр. 1).
Зображення 1: Схематичне зображення анатомічних орієнтирів підшлункової залози: вона розташована в заочеревинному просторі, попереду основних черевних судин і поперекового відділу хребта. Селезінкова вена – важливий анатомічний орієнтир (зірочка). Підшлункова залоза розділена на головку (1) справа, тіло (2) посередині і хвіст (3) зліва.
На УЗД залози краще візуалізуються у дітей, ніж у дорослих, через їх менший розміру і відносно велику ліву частку печінки, яка служить акустичним вікном, а також легко розпізнається через декілька важливих анатомічних орієнтирів, таких як аорта, нижня порожниста вена, селезінкова вена і мезентеріальні судини.
Обстеження підшлункової залози зазвичай починається з поперечного сканування, за яким слідують поздовжнє і похиле сканування з використанням лівої частки печінки в якості акустичного вікна для голівки і тіла (зобр. 2), селезінки для хвоста (зобр. 3) і, нарешті, вікна шлунка, наповненого водою для візуалізації тіла перешийка (зобр. 4).
Зображення 2: Поздовжнє ультразвукове сканування епігастрію від медіального до латерального напрямку. Головка і тіло підшлункової залози (зірочка) ідентифікуються через акустичне вікно лівої частки печінки (стрілка).
Зображення 3: Поздовжня (а) і поперечна (b) УЗД лівого підребер’я. Хвіст підшлункової залози ідентифікується через акустичне вікно селезінки.
Зображення 4: Поперечна епігастральна УЗД. Тіло перешийка підшлункової залози (зірочка) добре відображається, якщо вікно кишечника розширено водою. Зліва направо прогресивне наповнення шлунка.
Загальне співвідношення розміру залози до розміру тіла пацієнта з віком зменшується. Зазвичай у дітей головка підшлункової залози більш виражена, ніж тіло і хвіст, і це не слід приймати за патологічні процеси.
Підшлункова залоза в основному зростає протягом першого року життя, повільніше між 2-м і 18-м роком, збільшуючи свій передньо-задній діаметр (діаметр а – р) з часом (зобр. 5 і таблиця 1).
Зображення 5: Поперечна епігастральна УЗД підшлункової залози. Для оцінки діаметра залози вимірюють передньозадній діаметр підшлункової залози (штангенциркуль). Головка (a), тіло (b) і хвіст (c) атрофованої підшлункової залози.
Таблиця 1.
| Вік | Головка | Тіло | Хвіст |
| Новонароджені | 0.5–1.0 | 0.5–1.1 | 0.5–0.8 |
| 0-6 | 1.0–1.9 | 0.4–1.0 | 0.8–1.6 |
| 7-12 | 1.7–2.0 | 0.6–1.0 | 1.3–1.6 |
| 13-18 | 1.8–2.2 | 0.7–1.2 | 0.3–1.9 |
Зазвичай екоструктура підшлункової залози ізоехогенна або трохи більше ехогенна в порівнянні з печінкою, тому що паренхіма заміщена фіброзом і жиром, але менш виражена через її залозисту структури, яка викликає кілька кордонів розділу (зобр. 6); Вірсунгова протока також ідентифікується при УЗД як трубчаста безехова структура (зобр. 7). Середній діаметр протоки підшлункової залози у здорових дітей становить 1,65 ± 0,45 мм.
Зображення 6: Коса УЗД підшлункової залози в епігастрії з пацієнтом в положенні на правому боці. Підшлункова залоза орієнтована горизонтально і характеризується однорідною ехоструктурою, яка може виглядати як гіпоехогенною (а), так і гіперехогенною (b).
Зображення 7: Поперечна епігастральна УЗД підшлункової залози. У підшлунковій залозі, яка здається ізогіпоехогенною, є тонка анехогенна трубчаста структура, що представляє протоку Вірсунга (наконечники стріл).
Анатомічні варіанти
Анатомічні аномалії підшлункової залози класифікуються як аномалії злиття (pancreas divisum), міграція аномальної кільцеподібної підшлункової залози (ектопічна підшлункова залоза) або аномалія дуплікації (зміна кількості або форми).
Розподіл підшлункової залози виникає в результаті порушення злиття вентрального і дорсального зачатків. Вентральний (Вірсунгов) протока дренує тільки вентральний зачаток підшлункової залози, тоді як більша частина залози впадає в малий сосочок через дорсальний (Санторіні) проток.
За оцінками, захворюваність варіює приблизно від 5 до 10% населення. Його не часто ідентифікують за допомогою сонографії, хоча його можна легко розпізнати, коли протоки ектазійні, а також при перебігу панкреатиту (зобр. 8).
Зображення 8: Поперечна епігастральна УЗД підшлункової залози. Pancreas divisum: дорсальний проток підшлункової залози (стрілка) знаходиться в безпосередньому зв’язку з протокою Санторіні; вентральна протока Вірсунга (наконечник стрілки) впадає в просвіт кишки. Зверніть увагу на збільшену головку підшлункової залози (пунктирна двунаправленная стрілка) при гострому панкреатиті.
Кільцеподібна підшлункова залоза – рідкісна вроджена аномалія, що характеризується тим, що тканини підшлункової залози повністю або не повністю покривають спадну дванадцятипалу кишку. Поширеність становить приблизно 1 на 2000 осіб. Це часто пов’язано з іншими вродженими аномаліями, такими як атрезія стравоходу, неперфорований задній прохід, вроджені вади серця, мальротация середньої кишки і синдром Дауна.
Було запропоновано два типи: екстрамуральний підтип, коли вентральний проток підшлункової залози оточує дванадцятипалу кишку, щоб приєднатися до головного протоку підшлункової залози, і інтрамуральний підтип, де тканина підшлункової залози змішується з м’язовими волокнами стінки дванадцятипалої кишки, а численні невеликі протоки впадають безпосередньо в дванадцятипалу кишку . Він може мати широкий діапазон клінічного ступеня тяжкості і може вражати новонароджених і літніх людей, що ускладнює діагностику.
Приблизно у половини пацієнтів з дуоденальною непрохідністю в неонатальному віці може спостерігатися «подвійний міхур» на рентгенограмі черевної порожнини, якщо непрохідність повна. Цей стан важко підтвердити за допомогою УЗД, але округла голівка підшлункової залози і проксимальна частина дванадцятипалої кишки, що проходить через головку, повинні викликати підозру. Магнітно-резонансна томографія (МРТ) легко підтверджує діагноз; останній метод візуалізації кращий для оцінки як підшлункової залози, так і проток (зобр. 9).
Зображення 9: Поперечна епігастральна УЗД підшлункової залози. Кільцеподібна підшлункова залоза: головка підшлункової залози, що оточує дванадцятипалу кишку, з нормальною перистальтикою (верхня лінія a – c). Кільцева підшлункова залоза добре видна на МРТ (нижня рядок).
Клінічні показання
Основні захворювання підшлункової залози у дітей, при яких може знадобитися ультразвукове дослідження:
- Панкреатит.
- Панкреатична недостатність.
- Пухлини.
- Травми.
Панкреатит
Гострий панкреатит – це запальний процес підшлункової залози, вогнищевий або дифузний, який визначається у дітей як наявність принаймні двох з наступних трьох критеріїв:
- біль в животі, сумісна з панкреатичним походженням.
- амілаза і / або ліпаза, по крайній мірі, в три рази перевищують верхні межі норми.
- результати візуалізації, які передбачають і / або сумісні із запаленням підшлункової залози.
З точки зору візуалізації, гострий панкреатит може проявлятися як в незначній (інтерстиціальний набряк і некроз підшлункової залози), так і в важких формах (розширений некроз жирової тканини, некроз паренхіми і крововилив).
При УЗД підшлункова залоза може демонструвати різні моделі візуалізації. Незначні форми можуть мати або повністю нормальну залозу (50% випадків), або осередкове або дифузне збільшення об’єму зі зниженою ехогенністю, пов’язаною з набряком (зобр. 10, 11), і погане визначення ребер.
Також може бути присутнім розширення протоки підшлункової залози. Протоки підшлункової залози діаметром понад 1,5 мм у дітей у віці від 1 до 6 років, понад 1,9 мм у віці 7-12 років або більше 2,2 мм у віці 13-18 років часто пов’язані з наявністю гострого панкреатиту.
Перипанкреатична рідина – часта знахідка і найбільш часто виявляється в передньому принирковому просторі, малому мішечку, малому сальнику і поперечній ободовій кишці.
Більш важкі форми характеризуються різними патернами УЗД в залежності від часу обстеження, ступеня паренхиматозного некрозу, наявності крововиливу і ступеня екстрапанкреатичної дифузії запального процесу. Проте, важкий гострий некротичний панкреатит і пов’язані з ним ускладнення найкраще демонструються на зображеннях комп’ютерної томографії (КТ), а також на МРТ. Останні часто є додатковими до УЗД.
Зображення 10: Поперечне (а) і поздовжнє (b, c) сканування панкреатичного простору. Гострий панкреатит: спостерігається збільшення обсягу підшлункової залози, що також характеризується злегка гіпоехогенною ехоструктурою і розмитими краями через набряк (а, b, зірочка); крім того, є скупчення анехогенної рідини в заочеревинному принирковому просторі, поруч з правою ниркою (c, стрілки).
Зображення 11: Поперечне (а) і поздовжнє (b, c) сканування панкреатичного простору. Гострий панкреатит: спостерігається значне збільшення обсягу залози, особливо головки (b, жовті стрілки); крім того, є невелике скупчення приниркової рідини (а, біла стрілка).
Хронічний панкреатит в дитячому віці зустрічається вкрай рідко і пов’язаний зі спадковими і сімейними захворюваннями (спадковий панкреатит, амінокислотний хронічний панкреатит і хронічний геморагічний панкреатит).
При УЗД об’єм і ехоструктура підшлункової залози зберігаються в 70% випадків. У решти 30% ми можемо знайти деякі патогномонічні знахідки: розширення Вірсунгова протоки (30%) (зобр. 12), кальцифікати (10%) (зобр. 13), псевдокісти (10%) (зобр. 14). Останні розвиваються з гострою колекцією, і на їх формування може піти кілька тижнів. Більшість з них проходять спонтанно, але можуть виникнути такі ускладнення, як інфекція, кровотеча, непрохідність жовчних проток або навіть розрив.
Зображення 12: Приклад випадку у 17-річного хлопчика. Поперечна епігастральна УЗД підшлункової залози. Множинні гіперехогенні плями з загасанням в кінці через внутрішньопанкреатичні кальцифікати (зліва, стрілки); крім того, є розширений вірсунговий канал з ознаками гіперехогенних каменів всередині (справа).
Зображення 13: Поперечна епігастральна УЗД підшлункової залози. Хронічний панкреатит: невелике дифузне збільшення ехоструктури підшлункової залози з більш вираженими гіперехогенними плямами в головній частині через кальцифікати паренхіми.
Зображення 14: Поперечна епігастральна УЗД підшлункової залози. Хронічний панкреатит: у прогресивній розгортці (верхня лінія) від головки до хвоста підшлункової залози з множинними дифузними кальцифікація і двома скупченнями рідини псевдокіст (зірочка). МРТ (нижня лінія) з мультипланарною реконструкцією MRCP. Хронічний панкреатит у того ж пацієнта (див. Вище): аксіальні МРТ-зображення з Т1 після контрастування (в центрі і справа), підтвердили два вищевказаних скупчення рідини псевдокіст (зірочка) без зв’язку з протокою підшлункової залози на MRCP (зліва).
Аутоімунний панкреатит (АІП) стає все більш широко визнаним захворюванням, але дані про дітей обмежені.
AІП зустрічається в двох формах (типи 1 і 2). Тип 2, мабуть, частіше зустрічається у дітей і пов’язаний із запальними захворюваннями кишечника і іншими аутоімунними захворюваннями. У дорослих діагноз аутоімунного панкреатиту 1 типу заснований на підвищених рівнях імуноглобуліну G4 (IgG4). У дітей підвищення рівня IgG4 може бути відсутнім навіть при типовій гістології.
При УЗД можна було побачити дифузне або сегментарне збільшення підшлункової залози зі зниженою ехогенністю, пов’язане з флогозом, а також нерегулярне звуження протоки підшлункової залози, здавленого паренхімою залози.
Панкреатина недостатність
Муковісцидоз
Муковісцидоз (МВ) – рецесивне аутосомне спадкове захворювання, яке може не показувати будь-яких значущих результатів візуалізації на ранніх стадіях, але в кінцевому підсумку може призвести до зовнішньосекреторної недостатності підшлункової залози.
Паренхіма підшлункової залози заміщується фіброзом і жиром, тому на більш пізніх стадіях вона виглядає атрофічною, маленькою і гіперехогенною (зобр. 15). Жирова інфільтрація підшлункової залози при МВ пов’язана зі збільшенням м’якості при точковій еластографії зсувної хвилі (pSWE) (зобр. 16); цей параметр може використовуватися для моніторингу інволюції підшлункової залози при цьому прогресуючому захворюванні.
Крім того, можуть бути виявлені невеликі ретенційні кісти (цистоз підшлункової залози), зазвичай не більше 3 мм, і зони більш низької ехогенності через фіброз.
Зображення 15: Поперечна епігастральна УЗД підшлункової залози. Муковісцидоз: підшлункова залоза виглядає дифузно гіперехогенною в порівнянні з печінкою через жировуінфільтрацію.
Зображення 16: Поперечна епігастральна УЗД підшлункової залози. Вимірювання швидкості поперечної хвилі в голівці підшлункової залози у пацієнта з муковісцидозом.
Панкреатит – рідкісне ускладнення серед пацієнтів з МВ, яке слід враховувати при наявності передбачаючих клінічних ознак.
Нарешті, УЗД підшлункової залози у дітей, які страждають на муковісцидоз, завжди необхідно інтегрувати з оцінкою печінки, оскільки первинна патологія часто може співіснувати з біліарним цирозом (зобр.17).
Зображення 17: Поздовжні ультразвукові дослідження правої частки печінки. Муковісцидоз: дифузні ехоструктурні зміни печінки з чергуванням гіпоехогенних і гіперехогенних ділянок. Також проводиться вимірювання швидкостей поперечних хвиль.
Синдром Швахмана-Даймонда
Синдром Швахмана-Даймонда (СШД) – рідкісне аутосомно-рецесивне мультисистемні захворювання, що характеризується зовнішньосекреторною недостатністю підшлункової залози, порушенням кровотворення і схильністю до лейкемії.
Інші клінічні особливості включають скелетні, імунологічні, печінкові та серцеві захворювання. При УЗД дифузне підвищення ехогенності підшлункової залози, пов’язане з жировою інфільтрацією, типово для СШД (зобр. 18).
Зображення 18: Поперечна епігастральна УЗД підшлункової залози (а, b). Синдром Швахмана-Даймонда: підшлункова залоза дифузно гіперехогенна в порівнянні з прилеглою лівою часткою печінки через значну жирову інфільтрацію.
Пухлини
Примітивні новоутворення підшлункової залози в дитячому віці зустрічаються досить рідко. Ці пухлини можна розділити на три основні групи: екзокринні, ендокринні та кістозні ураження.
Найчастіше зустрічається вторинне ураження неходжкінської лімфоми, нейроектодермічних пухлин і заочеревинні новоутворення (нейробластома).
Панкреатобластома – найчастіша пухлина підшлункової залози у дітей раннього віку. Це карцинома підшлункової залози інфантильного типу з гістологічною подібністю з нормальною ембріональною підшлунковою залозою на 8-му тижні вагітності і демонструє підвищений рівень альфа-фетопротеїну в одній третині випадків.
При УЗД велика частина панкреатобластом є чітко окресленими гетерогенними утвореннями з твердими і кістозними компонентами. Кістозні утворення гіпоехогенні з гіперехогенними внутрішніми перегородками. Іноді виявляється гіпоехогенне тверде утворення. Описано вроджені випадки панкреатобластоми в поєднанні з синдромом Беквита – Відемана, і вони переважно кістозні.
Хоча панкреатобластома вважається найбільш поширеною злоякісною пухлиною у дітей, недавні дослідження показали, що солідне псевдопапілярне епітеліальне новоутворення (SPEN) є найбільш частою пухлиною підшлункової залози у дітей.
SPEN – це ураження з низьким потенціалом злоякісності, найчастіше вражає жінок репродуктивного віку. При УЗД пухлина зазвичай виглядає як чітко виражена велика маса з різними характеристиками в залежності від наявності кістозних і солідних компонентів, внутрішньопухлинного крововиливу і кальцифікатів. Фіброзна капсула може бути ідентифікована як ехогенний або, рідше, гіпоехогенний обідок.
Нейроендокринні пухлини виникають з острівцевих клітин підшлункової залози. При УЗД інсуліноми зазвичай круглі або яйцеподібні, гіпоехогенні з гіперехогенним обідком. Пухлини з більшими острівковими клітинами, зазвичай злоякісні інсуліноми, гастриноми (або інші нейроендокринні пухлини), можуть мати неоднорідний ультразвуковий вигляд залежно від наявності кістозних областей, крововиливів, некрозу і кальцифікатів.
Несідіобластома є аналогічним пухлинним захворюванням підшлункової залози, що характеризується новою диференціацією острівців Лангерганса від епітелію протоків підшлункової залози з наступною гіперпродукцією інсуліну. УЗД показує підвищену ехогенність і об’єм підшлункової залози. Несідіобластоз часто пов’язаний з гіпоглікемією і синдромом Беквита – Відерман.
Більш того, підшлункова залоза може бути залучена в неходжкінські лімфоми, особливо в великоклітинну лімфому і спорадичну лімфому Беркітта. На УЗД ці пухлини дуже гіпоехогенні і можуть по-різному проявлятися у вигляді одиничних або множинних уражень або дифузійної інфільтрації підшлункової залози.
Травма
Травми підшлункової залози зустрічаються рідко, їх частота становить 0,4% як у дорослих, так і у дітей.
Механізм травми пояснюється здавленням підшлункової залози жорстким хребтом або дискретними силами вторгнення. Маленькі діти з більш плоскими діафрагмами, більш тонкими черевними стінками і більш високим реберним краєм частіше, ніж дорослі, отримують травми підшлункової залози від ударів в живіт, особливо в дорожньо-транспортних пригодах з велосипедами (травма керма) або в результаті жорстокого поводження і травми автомобіля (травма ременя безпеки).
Оскільки підшлункова залоза є зачеревним органом, результати фізикального обстеження на предмет болю в животі або перитоніту не є надійними. Своєчасна діагностика травм підшлункової залози є складним завданням, особливо у пацієнтів з тупими травмами. Діагностика ґрунтувалася на рівнях амілази, УЗД, КТ і МРТ з різним рівнем успіху.
УЗД зазвичай використовується в якості початкового методу візуалізації у пацієнтів з тупою травмою, проте діагностична точність пошкоджень підшлункової залози за допомогою УЗД низька, і класифікація зазвичай заснована на зображеннях комп’ютерної томографії.
УЗД може показати збільшення підшлункової залози з неоднорідною текстурою, а також заочеревину гематому зі скупченням рідини, вторинним по відношенню до травм підшлункової залози.
Розрив і гематома розглядаються як область структурної неоднорідності з неправильними контурами, яка спочатку є ехогенною, а потім гіпоехогенною або анехогенною в залежності від часу виникнення травми (зобр. 19, 20).
Ця здатність УЗД важлива для діагностики та лікування травми підшлункової залози, але УЗД не може в достатній мірі відобразити локалізацію і тяжкість уражень підшлункової залози. Проте, CEUS (УЗД з контрастним посиленням), використовуваний не за прямим призначенням в педіатричній популяції, значно точний при ідентифікації посттравматичних уражень твердих органів черевної порожнини, а також підшлункової залози, досягаючи чутливості, що дорівнює чутливості КТ.
CEUS слід розглядати для початкового виявлення травми підшлункової залози. Однак його слід розглядати не як заміну КТ, а як вибіркову можливість підвищити роль УЗД в початковому скринінгу пацієнтів з травмою підшлункової залози.
Зображення 19: Ультразвукове сканування області підшлункової залози в B-режимі (а, b) і кольоровому доплерівском режимі (с). Посттравматичні пошкодження крючковидного відростка підшлункової залози: a Поперечне сканування показує нормальну ехоструктуру головки перешийка підшлункової залози зі звичайним вірсунговим протокою; b Поздовжнє сканування головки підшлункової залози показує гіпоехогенні ураження (штангенциркуль) в крючковидному відростку; c Поперечна УЗД підшлункової залози з використанням кольорового доплера показує видиме не васкуляризированне гіпоехогенне ураження в крючковидному відростку.
Зображення 20: Осьовий (а) і корональний (b) КТ знімки по верхній лінії. Осьове зображення T2 по нижній лінії (c) з мультипланарною реконструкцією MRCP (d). Посттравматичні пошкодження крючковидного відростка підшлункової залози у того ж пацієнта, наведеного вище: великий розрив крючковидного відростка.