Автори: Divya Singh, Ladbans Kaur
РЕЗЮМЕ:
Протягом багатьох років кесарів розтин зіграв ключову роль в зниженні материнської та перинатальної захворюваності та смертності. З ростом тенденції цієї операції, значній кількості вагітних жінок проводиться кесарів розтин. Рубець після операції може служити місцем розвитку серйозної патології при наступних вагітностях, а саме: вагітності в зоні кесарева рубця, патологічного прикріплення і прирощення плаценти і розходження країв рубця. Сонографічне дослідження стало надійним інструментом для діагностики цих потенційно небезпечних для життя станів. У цьому огляді висвітлюються ключові сонографічні особливості різних ускладнень, які можуть виникати на ділянці рубця після кесаревого розтину при наступних вагітностях.
КЛЮЧОВІ СЛОВА:
кесарів розтин; рубець; вагітність; ультразвук; патологічне прикріплення і прирощення плаценти
ВСТУП
Кесарів розтин є однією з найбільш часто виконуваних операцій у жінок. Ця процедура пройшла довгий шлях для скорочення як перинатальної, так і материнської захворюваності та смертності. Останнім часом спостерігається тенденція до зниження частоти кесаревого розтину. Частота повторного кесаревого розтину в Сполучених Штатах складає 91%. Як і будь-яка інша операція, у неї є певні безпосередні, відстрочені та віддалені ускладнення. Частота ускладнень вища після проведення екстрених процедур, ніж після планових. Рубець після кесаревого розтину може служити місцем розвитку патологічних станів при наступних вагітностях, а саме, вагітності кесарева рубця (ВКР), патологічного прикріплення плаценти (ППП) і розходження/розрив рубця. Ці патологічні процеси можуть викликати значну материнську і перинатальну захворюваність. Знання цих станів є обов’язковим, і їх слід виявляти якомога швидше для того, щоб провести своєчасне і ефективне втручання. Будучи безпечним і широко доступним, ультразвукове дослідження (УЗД) є методом вибору візуальної діагностики цих станів.
ВАГІТНІСТЬ В РУБЦІ ПІСЛЯ КЕСАРЕВОГО РОЗТИНУ
ВКР – це рідкісний тип позаматкової вагітності. Вона зустрічається в 1:1800-1:2226 всіх вагітностей. Однак спостерігається стійке зростання розвитку ВКР. Це можна пояснити збільшенням частоти кесаревого розтину, а також раннім виявленням при проведенні УЗД з високою роздільною здатністю.
ПАТОГЕНЕЗ
Точний патогенез ВКР невідомий. Передбачається, що ця патологія пов’язана з імплантацією бластоциста в сполучну тканину при клиноподібному дефекті міометрія в рубці в передньому нижньому сегменті матки (НСМ). Вважають, що цей дефект є наслідком неповного загоєння або надмірного фіброзу. Vial і ін. описали два типи ВКР. Перший тип виникає в результаті імплантації амніотичного мішку на ділянку рубця, що призводить до розвитку вагітності в шийно-перешийковому просторі і порожнині матки. Другий – наслідок глибокої імплантації в дефект кесаревого рубця з прогресуванням та розвитком кровотечі і розриву протягом першого триместру. Хоча рубець після вагітностей найчастіше спостерігають після кесаревого розтину, про його розвиток також повідомляється після таких процедур, як дилатація і кюретаж, міомектомія, метропластика, гістероскопія і ручне видалення плаценти. Більшість ВКР розвиваються у жінок, у яких було два або більше кесаревих розтинів. Множинні операції збільшують ризик розвитку фіброзу на місці рубців, що перешкоджає нормальному загоєнню, а також призводить до збільшення площі поверхні рубця, тим самим зростає ймовірність ВКР. Вважається, що ВКР є попередником ППП, так як обидва процеси мають однакову гістопатологічну будову. Якщо цей стан залишається недіагностованим, ВКР може викликати розрив матки і масивну кровотечу з катастрофічними наслідками. Тому важливо якомога раніше діагностувати ВКР для проведення відповідних лікувальних заходів.
УЛЬТРАЗВУКОВІ ОСОБЛИВОСТІ
Спочатку виконується трансабдомінальна сонографія з оптимально заповненим сечовим міхуром з метою загального огляду органів тазу і взаємин між маткою і сечовим міхуром. Однак вона має більш низьку роздільну здатність і тому виключно на це дослідження покладатися не можна. Трансвагінальна УЗД є методом вибору для виявлення ВКР. Були запропоновані різні ультразвукові критерії для діагностики ВКР в першому триместрі. До них відносяться: порожня порожнина матки з чітко окресленим ендометрієм; порожній шийковий канал; наявність гестаційного мішку (ГМ) на місці рубця, тобто в передній стінці НСМ, стоншений (<5 мм) або відсутній міометрій між ГМ і сечовим міхуром, і високошвидкісний (> 20 см/с) з низьким опором (індекс пульсативності <1) перитрофобластний потік навколо мішка на кольоровій доплерограмі. У недавньому дослідженні Timor-Tritsch і ін. використовували розташування центру ГМ між 5 і 10 тижнями вагітності, як ознаку, яка допомагала диференціювати ВКР від внутрішньоутробної вагітності з чутливістю і специфічністю 93% і 98,9% відповідно. Ця ідея була заснована на тому спостереженні, що більшість ВКР розташовані ближче до середньої осі матки, тоді як більшість нормальних внутрішньоутробних вагітностей розташовані більш дистально.
На малюнку 1 показаний випадок ВКР, при дослідженні за допомогою двовимірного і тривимірного ультразвукового дослідження. Додавання тривимірного УЗД дає панорамного вигляд взаємин ГМ з порожниною матки, міометрієм і стінкою сечового міхура. УЗД також ефективне для динамічного спостереження за пацієнтами, які лікуються консервативно.
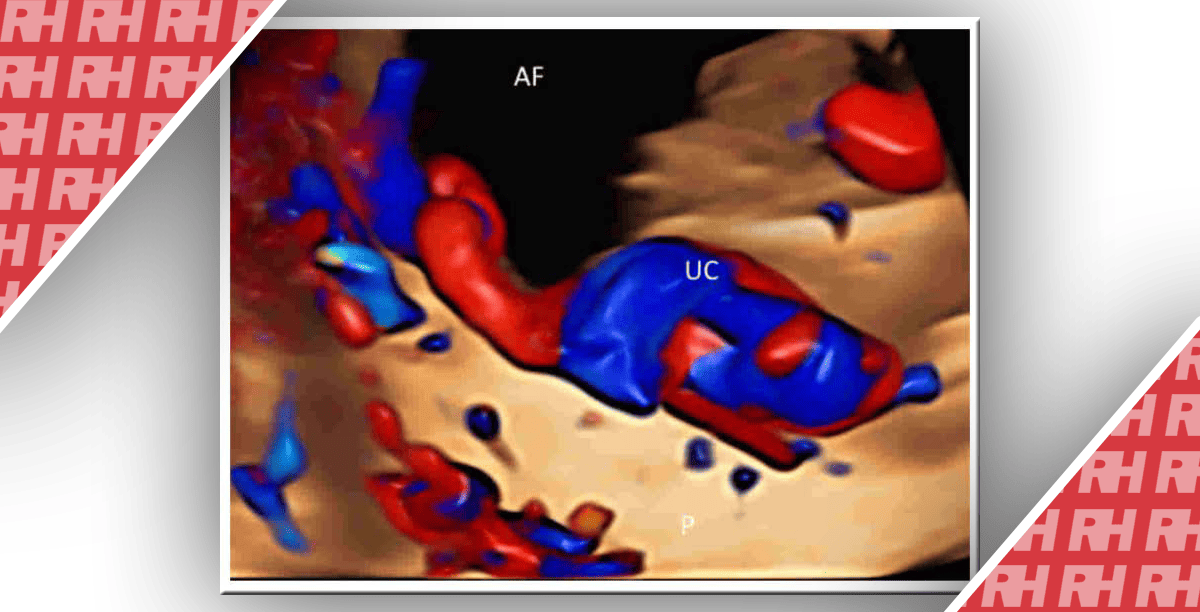
Рис. 1. Вагітність кесарева рубця на 7 тижні вагітності. (A) Трансабдомінальна поздовжня сонограма таза з сечовим міхуром (BL) (який забезпечує акустичне вікно) показує порожню порожнину матки (UT) з низько розташованим ГМ (стрілка), поблизу шийки (CX). (B) Трансвагінальна сагітальна сонограма показує низьку імплантацію ГМ поблизу шийки матки (CX) на місці рубця з майже непомітним гіпоехогенним міометрієм перед ехогенною трофобластичною тканиною (*). (C) Трансвагінальна сагітальна доплерограма показує перітрофобластну васкуляризацію. (D) Трансвагінальна поздовжня сонограма матки показує жовтковий мішок (біла стрілка) і фетальний полюс (червона стрілка) всередині ГМ. (E) Коронарне тривимірне об’ємне контрастне Omniview зображення показує взаємовідношення гестаційного мішка і порожньої порожнини матки (CAV) і шийки матки (CX). Зверніть увагу на нормальний гіпоехогенний міометрій (*). Трофобластична тканина «випирає» через стоншений міометрій на ділянці рубця після кесарева розтину.
Вимірювання об’єму ГМ і ступеня васкуляризації можна використовувати для оцінки відповіді на проведене лікування. Магнітно-резонансна томографія (МРТ) рідко необхідна для діагностики ВКР. Однак вона застосовується у випадках неоднозначних результатів досліджень.
ДИФЕРЕНЦІЙНА ДІАГНОСТИКА
Можливою діагностичної дилемою є диференціальна діагностика вагітності в рубці від мимовільного аборту або шийкової ектопічної вагітності. Першим етапом візуалізації, який дозволяє відрізнити шийкову ектопію від ВКР, є місце розташування ектопії в каналі шийки при нормальній товщині міометрію спереду. Класична ВКР розташована в НСМ зі стоншеним міометрієм спереду. При кольоровій доплерографії в разі самовільного аборту відсутній нормальний перитрофобластний потік. ГМ в шийці матки можна зміщувати шляхом ніжної компресії за допомогою ендовагінального датчика. Нарешті, в разі самовільного аборту під час динамічного ультразвукового спостереження можна виявити, що гестаційний мішок не фіксований в будь-якому місці і при цьому не збільшується в розмірі.
ЛІКУВАННЯ
Існують консервативні та хірургічні варіанти, які доступні для лікування ВКР. Однак не існує єдиної думки про оптимальний протокол лікування. Через розвиток серйозних наслідків рекомендується раннє переривання вагітності. План лікування повинен бути адаптований до кожного випадку з урахуванням гестаційного віку, життєздатності та плану майбутньої вагітності. Консервативне лікування включає місцеву інстиляцію ембріоцидних продуктів, таких як метотрексат, хлорид калію і гіпертонічна глюкоза. Ці препарати можуть вводитися в ГМ під ультразвуковим наведенням з трансабдомінального, або трансвагінального доступу. Трансвагінальний підхід має перевагу, оскільки він дозволяє краще візуалізувати голку, забезпечує більш коротку траєкторію голки і знижує ризик пошкодження сечового міхура. У недавньому огляді літератури Cheung і ін. зареєстрували частку успішних процедур при місцевому застосуванні метотрексату – 73,9%. Використовувалося також системне введення метотрексату. Для досягнення оптимальних результатів при системному застосуванні метотрексату рекомендується щоб рівень сироватки був менше 5000 мМО/мл β-субодиниці людського хоріонічного гонадотропіну (ß-ХГЛ). Іноді потрібно кілька доз через короткий період напіввиведення і повільну системну абсорбцію. В ході експертного огляду частота ускладнень при системному використанні метотрексату склала 62%. Це пояснюється повільною дією препарату і його сумнівною здатністю викликати зупинку серцеву діяльность і розширення плаценти. У деяких випадках очікування ефекту від препарату приводило до зростання ГМ, ембріона і плацентарної васкуляризації, що в результаті сприяло збільшенню ускладнень. Також було запропоновано поєднання місцевої та системної терапії. Timor-Tritsch і ін. повідомили про успішне лікування 19 випадків ВКР з використанням комбінованих внутрішньом’язового і внутрішньоматкового введень метотрексату. Також для лікування ВКР використовувалася емболізація маткових артерій в комбінації з метотрексатом.
Консервативне лікування допомагає уникнути операції зі збереженням фертильності. Воно підходить для нерозірваної ВКР у гемодинамічно стабільної пацієнтки з гестаційним віком менше 8 тижнів і тонким (<2 мм) переднім міометрієм між ГМ і сечовим міхуром. Ретельний моніторинг пацієнтки після проведення процедури має важливе значення, оскільки може виникати загрожуюча життю кровотеча. Виведення ß-ХГЛ може зайняти до 9 тижнів, в той час як очищення від ГМ може зайняти до 3 місяців після проведення консервативного лікування. Пацієнтці слід стежити щотижня за рівнем ß-ХГЛ в сироватці до тих пір, поки він не стане <5 мМО/мл. Деякі автори рекомендують проводити щомісячні трансвагінальні ультразвукові дослідження (ТВУЗД) для оцінки залишкових елементів вагітності. Цікавим спостереженням, яке було відзначено після проведення консервативного лікування, є тимчасове підвищення рівня сироваткового ß-ХГЛ, об’єму ГМ і його васкуляризації. Це явище пояснюється некрозом трофобластів, що призводить до вивільнення ß-ХГЛ. Трофобластичний некроз викликає перитрофобластну запальну реакцію, яка призводить до збільшення об’єму і васкуляризації мішка. Це тимчасове підвищення не повинно бути помилково сприйнято, як відсутність відповіді на проведене лікування. У подібному випадку рекомендується вичікувальна тактика. Поки рівень сироваткового β-ХГЛ знижується, ультразвукове дослідження показано тільки в тому випадку, якщо у пацієнтки з’являються нові симптоми.
Хірургічні варіанти лікування включають аспірацію ГМ або його видалення за допомогою гістероскопії, лапароскопії або лапаротомії. Відкрита хірургія може бути кращим методом лікуванням у пацієнток з більш пізнім гестаційним строком або після невдалих консервативних заходів. Проте, така операція пов’язана з ризиком тривалого періоду післяопераційного відновлення, погіршення фертильності і розвитку патологічного прикріплення і прирощення плаценти при наступній вагітності. Дилатація і вишкрібання не рекомендується, так як це може привести до пошкодження стінки матки і сечового міхура, що призводить до профузної кровотеча. Описана нова, мінімально інвазивна методика з використанням катетера з подвійним балоном для розширення шийки матки для лікування пацієнтів з ВКР і цервікальною вагітністю. Однак вона вимагає подальшого вивчення.
Не існує рекомендацій щодо необхідного часу спокою до наступної вагітності. Деякі автори пропонують уникати вагітності протягом 12-24 місяців. Дослідження показало хороші результати репродуктивності у жінок з ВКР, яким було проведено нехірургічне лікування в першому триместрі. Це підкреслює необхідність ранньої діагностики для своєчасного втручання.
ПАТОЛОГІЧНЕ ПРИКРІПЛЕННЯ ПЛАЦЕНТИ
ППП відноситься до аномальної імплантації плаценти до міометрію матки. Цей термін охоплює прирощення, вростання і пророщення плаценти. Ці варіанти характеризуються різним ступенем проникнення плацентарних трофобластичних ворсинок в міометрій матки. При прирощенні плаценти (placenta accreta) відзначається зв’язок ворсинок з міометрієм. При вростанні плаценти (placenta increta) вони розповсюджуються в міометрій, а при пророщенні плаценти (placenta percreta) вони проникають в міометрій, а також в серозний шар. З усіх ППП 75% – це прирощення плаценти, 18% – вростання, а 7% – пророщення плаценти.
Необхідно виявляти аномальну плацентацію якомога раніше, оскільки при цьому стані підвищується частота розвитку ускладнень і смертності. Це патологія була вперше описана в 1937 році. В даний час частота прирощення плаценти становить 3 на 1000 пологів. Збільшення її поширеності, ймовірно, пов’язано зі збільшенням числа виконуваних кесаревих розтинів.
ФАКТОРИ РИЗИКУ
Кесарів розтин в анамнезі і передлежання плаценти є двома найбільш важливими факторами розвитку ППП. Ризик прирощення плаценти при наявності передлежання плаценти у пацієнтки з трьома попередніми кесаревими розтинами досягає 40%, в порівнянні з менш ніж 1%, в разі відсутності передлежання плаценти. Отже, наявність передлежання плаценти у пацієнтки з наявністю кесарева рубця служить «червоним прапором» для можливого плацентарного прирощення. Іншими факторами ризику є: літній вік матері, багатоплідна вагітність, попередні хірургічні втручання на матці, абляція ендометрія, синдром Ашермана, лейоміоми матки, аномалії матки, гіпертонічна хвороба під час вагітності і куріння.
Точне патогенетичне обґрунтування ППП залишається загадкою. Вважається, що цей стан пов’язаний з патологічною децидуалізацією і надмірною трофобластичною проліферацією на місці рубця.
УЛЬТРАЗВУКОВІ ОСОБЛИВОСТІ
Ультразвукова візуалізація, яка включає як дослідження в відтінках сірого, так і кольорову доплерографію, є першою лінією діагностики у пацієнток з ризиком розвитку ППП. ТВУЗД – це метод вибору, оскільки він дозволяє отримувати зображення з високою роздільною здатністю плаценти і суміжних з нею структур. Кілька ультразвукових знахідок прирощення плаценти були описані в другому і третьому триместрі вагітності. До ознак, які характеризують даний стан, відносяться: наявність передлежання плаценти, аномальні лакуни плаценти, втрата нормальної гіпоехогенної ретроплацентарной чистої зони, товщина ретроплацентарного міометрію <1 мм, випинання плаценти за межі серозної оболонки матки, локальне екзофітне утворення, яке проходить через щілину в серозній оболонці матки, аномалії взаємного положення матки і сечового міхура. Характерними особливостями за даними кольорової доплерографії є: турбулентний потік в лакунах плаценти, наявність судинних мостиків і утеро-везікальна і субплацентарна гіперваскуляризація. Не так давно «Європейська робоча група по аномально інвазивній плаценті» запропонувала стандартизовані визначення ультразвукових дескрипторів ППП. Кожен дескриптор був пов’язаний з характерними зображеннями на сонограмі. Використання стандартизованої термінології дозволить забезпечити однаковість в описі аномальної плацентації, яка буде корисна для клінічних, освітніх і дослідницьких цілей.
Плацентарні лакуни є гіпоехогенні простори неправильної форми в тканині плаценти, які мають нечіткі краї і характеризуються турбулентним потоком. На відміну від них, плацентарні озера більш округлі і характеризуються ламінарним потоком. Множинні лакуни можуть надавати плаценті вигляд «швейцарського сиру» або «поїденого міллю». Наявність лакун має чутливість 80% -90% для діагностики прирощення плаценти в другому триместрі. Плацентарні лакуни були оцінені Finberg і Williams наступним чином: 0-й ступінь, коли лакуни не помітні; 1-й ступінь, коли є 1-3 невеликих лакуни; 2-й ступінь, якщо є 4-6 великих і більш аномальних лакун; 3-й ступінь, коли вздовж всієї плаценти визначаються окремі аномальні лакуни. Важливо відзначити, що діагностувалися випадки прирощення плаценти без наявності судинних лакун.
Нормальний ретроплацентарний простір визначається як гіпоехогенна зона між плацентою і маткою. Зникнення цього простору є маркером прирощенням плаценти з чутливістю – 52% і специфічністю – 57%. Візуалізація ретроплацентарного простору залежить від кута інсонації. Слід враховувати ймовірність артефактної не візуалізації простору в разі переднього розташування плаценти, що призводить до хибнопозитивної діагностики. Тому, зникнення ретроплацентарного простору не повинно інтерпретуватися ізольовано. На рис. 2 показаний випадок прирощення плаценти у пацієнтки з двома попередніми кесаревими розтинами і передлежанням плаценти у наявній вагітності.
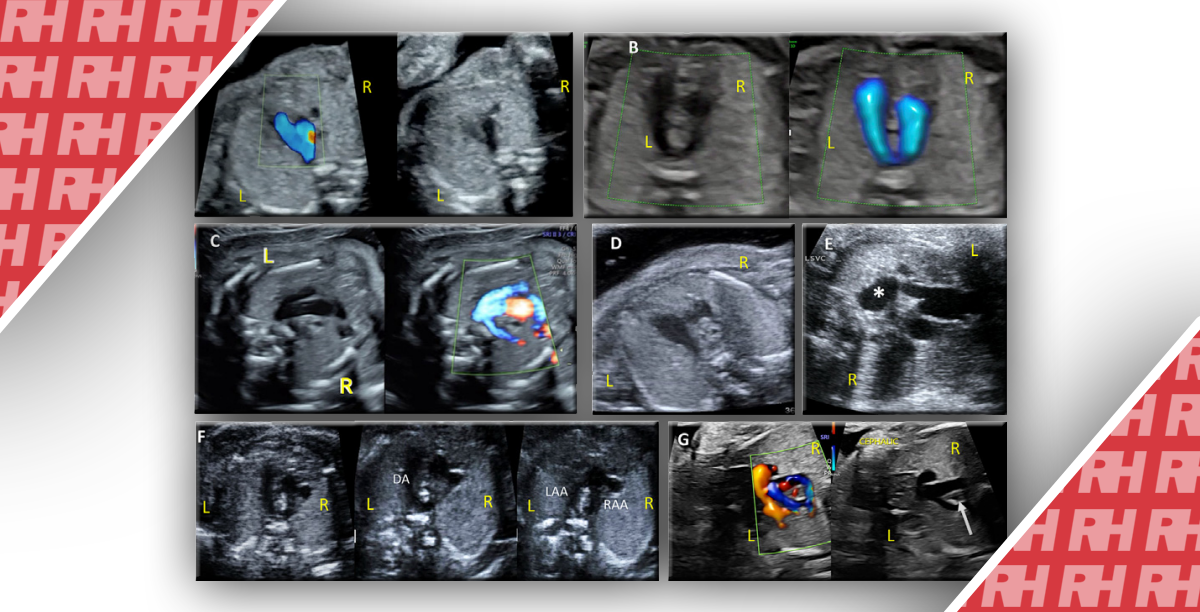
Рис. 2. Прирощення плаценти на 21 тижні вагітності. (A) Сагітальна трансвагінальна кольорова доплерограма показує плаценту, яка розташована спереду і прикриває внутрішній зів матки. Визначається підвищена субплацентарна васкуляризація. PL – плацента; BL – сечовий міхур; CX – шийка матки. (B) Трансвагінальна сонограма плаценти у відтінках сірого показує анехогенні лакуни (*). (C) Трансвагінальна сагітальная сонограма демонструє зникнення ретроплацентарного чистого простору (стрілки). PL – плацента; BL – сечовий міхур. (D) Тривимірна томографічна сонографічна візуалізація відображає ступінь аномальної васкуляризації. (E) Об’ємне тривимірне трансвагінальне доплерівське зображення демонструє інтенсивну васкуляризацію на межі матки і сечового міхура. PL – плацента; BL – сечовий міхур. (F) Об’ємна тривимірна сонограма демонструє картину плаценти у вигляді «швейцарського сиру» через численні лакуни. PL – плацента; BL – сечовий міхур.
Ретроплацентарна товщина міометрію вимірюється між ехогенною серозною оболонкою матки і ретроплацентарними судинами. Товщина менше 1 мм була ідентифікована як фактор ризику плацентарної інвазії з чутливістю – 100% і специфічністю – 72%.
Нормальна межа між серозної оболонкою матки і стінкою сечового міхура визначається як гладка, тонка ехогенна лінія без судинних сигналів. У разі плацентарної інвазії ця лінія утворює випинання неправильної форми, визначаються варикозно розширені вени і підвищена васкуляризація.
Проростання плаценти діагностується тоді, коли плацентарна тканина визначається в сечовому міхурі. Підвищена субплацентарна васкуляризація, утеро-везікальна васкуляризація і наявність аномальних судин, які простягаються від плаценти до сечового міхура і порушують звичну межу між маткою і сечовим міхуром, є ознаками приростання плаценти при кольоровій доплерографії. Тривимірне УЗД дає глобальну картину внутрішньоплацентарної гіперваскуляризації у випадках плацентарної інвазії.
У недавньому метааналізі D’Antonio і ін. повідомили про чутливість – 91% і специфічність – 97% для УЗД в діагностиці ППП. Вони відзначили, що серед різних ультразвукових ознак, наявність аномальної васкуляризації при кольоровій доплерографії було найбільш чутливим, в той же час аномалія границі матки і сечового міхура була найбільш специфічною ознакою. Наявність плацентарних лакун і зникнення ретроплацентарного чистого простору не відповідали ультразвуковим даним плацентарної інвазії. Дослідники запропонували бальну систему оцінки для прогнозування плацентарної інвазії, об’єднавши клінічні і ультразвукові параметри. Rac і ін. розробили «Індекс прирощення плаценти». Він заснований на кількості попередніх кесаревих розтинів, наявності плацентарних лакун 2-й і 3-го ступеня, найменшій товщині міометрію в сагітальній площині і наявності переднього передлежання плаценти і судинних мостиків. Отриманий таким чином індекс прирощення плаценти визначає ймовірність, чутливість, специфічність і прогностичну цінність плацентарної інвазії, які можуть визначати тактику лікування. Нещодавно Tovbin і ін. запропонували систему бальної оцінки для прогнозування ППП, використовуючи число попередніх кесаревих розтинів і кілька ультразвукових параметрів в сірій шкалі і кольоровій доплерографії. У своєму проспективному дослідженні система бальної оцінки була достатня прогностично точною для ППП.
В даний час основна увага приділяється ранньому виявленню прирощення плаценти, для забезпечення відповідної консультативної допомоги та планування напрямку подальших дій. Характерні ультразвукові прогностичні ознаки прирощення плаценти в першому триместрі включають: низька імплантація ГМ в порожнині матки поблизу післяопераційного рубця, множинні простори неправильної форми в плацентарному судинному ложі, тонка передня частина міометрію в сагітальній площині. Товщина міометрію <2 мм, який розташований над плацентою в першому триместрі, пов’язана з ППП при пологах.
МРТ не є першою лінією діагностики при прирощенні плаценти. Ця методика зарезервована для випадків, коли плацента має заднє розташування або у пацієнток з ожирінням, коли ультразвукове дослідження є субоптимальним. Palacios і ін. оцінювали ефективність МРТ у діагностиці прирощення плаценти і виявили, що МРТ не додавала діагностичної інформації до даних УЗД. Однак МРТ більш детально описувала ступінь плацентарної інвазії, що потенційно могло б допомогти в плануванні хірургічного лікування.
ЛІКУВАННЯ
ППП є потенційно небезпечним для життя станом. Його лікування вимагає зусиль узгодженої багатодисциплінарної команди. Серед ускладнень зустрічаються: масивні кровотечі, травми сечостатевої системи, емболії амніотичною рідиною, коагулопатія споживання, гемотрансфузійні ускладнення, гострий респіраторний дистрес-синдром, післяопераційна тромбоемболія, сепсис і поліорганна недостатність. Розродження виконується хірургічним методом. Однак оптимального хірургічного підходу на даний момент поки не встановлено. Зазвичай рекомендується уникати спроб відокремити плаценту, оскільки це може викликати масивну кровотечу. Тяжкість цього стану підкреслює значення точної пренатальної діагностики, оскільки вона має великий вплив на тактику і результати лікування пацієнток.
РОЗХОДЖЕННЯ І РОЗРИВ РУБЦЯ НА МАТЦІ
Утворений рубець в матці після кесаревого розтину схильний до розходження/розриву при наступних вагітностях. Це також може траплятися після інших операцій на матці, таких як: міомектомія, метропластика і септопластика. Розходження рубця визначається як порушення цілісності міометрію з інтактною серозної оболонкою. У разі розриву матки порушується цілісність як міометрію, так і серозної оболонки. Частота розривів рубця у жінок з пологами через природні родові шляхи після кесарева розтину становить від 0,2% до 1,5%. Ризик розходження рубців вище при класичному розрізі, ніж при поперечному. Розходження рубця може мати різноманітну клінічну картину. Цей стан може залишатися безсимптомним або характеризуватися болем внизу живота, відчуттям важкості або вагінальною кровотечею.
УЛЬТРАЗВУКОВІ ОСОБЛИВОСТІ
Ультразвукова оцінка НСМ використовується в якості предиктора ризику розриву матки під час спроби вагінальних пологів після попереднього кесаревого розтину (СВППКР) (індуковані пологи). Точне прогнозування ризику розходження рубця необхідно, так як це може збільшити безпеку проведення СВППКР. Рубець після кесаревого розтину описується як клиноподібна гіпоехогенна область в передній стінці нижнього сегмента невагітної матки. Кольорова доплерографія показує відносну аваскулярність на місці рубця. Чим довше час, що минув після операції, тим менше розмір клиноподібного дефекту. Слово «ніша» було введено Monteagudo і ін., щоб описати трикутну анехогенну область на передбачуваній ділянці хірургічного розрізу при соногістерографії під час інфузії сольового розчину. Naji і ін. запропонували стандартизований підхід для описання кесаревих рубців при ТВУЗД. Вони описали рубець як гіпоехогенні заглибини в передній стінці НСМ між матково-сечоміхуровою складкою і внутрішнім зівом. У сагітальній і поперечній площинах вимірюються три розміри рубця: довжина, ширина і глибина. Розміри кесарева рубця змінюються протягом всієї вагітності. Розрив рубця під час СВППКР безпосередньо пов’язаний з меншою залишковою товщиною міометрія (ЗТМ) під час вагітності. Дослідники вважають, що модель, що включає зміни ЗТМ від першого до другого триместру, може передбачати успішне проведення СВППКР у жінок з одним кесаревим розтином в анамнезі.
Кілька спроб були проведені для прогнозування ризику розриву рубця шляхом вимірювання товщини всього НСМ або тільки ЗТМ на місці рубця. Bujold і ін. вимірювали повну товщину НСМ і товщину міометрія при трансабдомінальному і трансвагінальному скануванні у вагітних жінок у віці від 35 до 38 тижнів. Вони відзначили, що товщина НСМ <2,5 мм була пов’язана з більш 10% частотою розриву матки з приблизною специфічністю 90%. Мартінс і ін. прийшли до висновку, що вимірювання м’язової товщини НСМ при трансвагінальній сонографії було більш надійним, ніж оцінка всієї товщини НСМ при трансабдомінальном доступі. У недавньому метааналізі Kok і ін. помітили, що граничне значення всієї товщини НСМ – 3,1-5,1 мм і граничне значення товщини міометрію – 2,1-4,0 мм мали сильне негативне прогностичне значення для розвитку дефекту під час СВППКР у жінок з кесаревим розтином в анамнезі. Граничне значення товщини міометрію між 0,6 і 2,0 мм мало сильне позитивне прогностичне значення для розвитку дефекту. Аналіз декількох досліджень для прогнозування ризику розриву рубця показує, що не існує стандартного протоколу з досить високою чутливістю і специфічністю. Також не існує консенсусу щодо ідеального доступу до проведення УЗД (трансабдомінального або трансвагінального), стандартизації методу вимірювання товщини НСМ або часу проведення дослідження. На рис. 3 показано розходження рубця у пацієнтки, яка потрапила на ультразвукове дослідження на 37 тижні гестації зі скаргами на біль внизу живота і відчуття тяжкості.
Рис. 3. Розходження рубця матки на 37-му тижні вагітності. Трансвагінальна сагітальна сонограма у пацієнтки з кесаревим розтином в анамнезі, скаргами на біль внизу живота і відчуття тяжкості, демонструє витончення нижнього сегменту матки з невиразним міометрієм на місці рубця. Ехогенна серозна оболонка (*) не пошкоджена. BL – сечовий міхур; CX – шийка матки; FH – головка плода.
Незважаючи на те, що МРТ не є першою лінією діагностики, вона допомагає візуалізувати ступінь розходження рубця в неоднозначних випадках і у пацієнтів з ожирінням, які не можуть бути адекватно оцінені за допомогою УЗД. Також ця методика здатна розрізняти супутні гематоми від скупчень рідини.
ЛІКУВАННЯ
Після постановки діагнозу розходження рубця, метод розродження є тільки хірургічним з усуненням дефекту або гістеректомією в залежності від клінічного стану пацієнтки і бажання подальшої фертильності.
ВИСНОВОК
Рубець від кесаревого розтину може сприяти розвитку патологічних станів при наступних вагітностях. Він може бути більш, ніж безневинним свідком таких станів, як вагітність кесарева рубця, патологічне прикріплення плаценти і розходження або розрив рубця. Ультразвукове дослідження є надійним інструментом для ранньої діагностики цих станів. Воно допомагає ініціювати своєчасні і ефективні дії, які сприяють зниженню материнської і перинатальної захворюваності і смертності.



















14.10.2019
елена