🤖 Короткий переказ від ШІ
Ультразвукова еластографія – це інноваційний метод візуалізації, що базується на оцінці твердості тканин, відмінно доповнюючи традиційне УЗД у діагностиці захворювань. Особливу ефективність цей метод демонструє у виявленні та моніторингу фіброзу печінки, а також у характеристиці інших патологічних процесів.
Ключовими перевагами еластографії є її неінвазивність та можливість кількісної оцінки. Вона дозволяє точно визначити стадію фіброзу печінки, що є критично важливим для вибору тактики лікування та прогнозу. Хоча метод має певні обмеження у диференціації злоякісних та доброякісних утворень, його потенціал у сучасній медицині залишається надзвичайно високим, особливо враховуючи доступність сучасних УЗД апаратів, таких як Siemens Acuson S2000.
✅ Ключові тези зі статті:
- Діагностика: Ультразвукова еластографія є точним неінвазивним методом для діагностики фіброзу печінки та оцінки портальної гіпертензії.
- Лікування: Метод допомагає у виборі тактики лікування хронічних захворювань печінки та контролі його ефективності.
- Переваги: Еластографія надає кількісну оцінку твердості тканин, що є корисним доповненням до традиційного УЗД, і потенційно зменшує потребу у біопсії.
- Обмеження: Метод обмежений у точній диференціації злоякісних та доброякісних утворень печінки через перекриття показників твердості.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Richard G. Barr, MD, PhD, FACR, FSRU
ОСНОВНІ ПОЛОЖЕННЯ
Існує 2 типи еластографії: компресійна еластографія – якісна, та зсувнохвильова еластографія – кількісна. Хоча локальні злоякісні ураження печінки є статистично жорсткішими, ніж доброякісні, все-таки існують значні подібності між показниками. Тому для будь-якого окремого ураження еластографія обмежена характеристикою пухлини доброякісної або злоякісної природи.
Зсувнохвильова еластографія є відмінним неінвазивним методом для оцінки фіброзу печінки.
Еластографія може оцінити характер рідини – серозний або муцинозний.
Виміри твердості печінки й селезінки можуть служити неінвазивним методом оцінки печінкового венозного тиску.
ВСТУП
Ультразвукова еластографія – це новий метод, який генерує зображення на основі твердості тканини на відміну від анатомічної будови. Багато захворювань органів мають різні показники твердості, які можуть бути виявлені за допомогою еластографії. Ультразвукова еластографія використовується для оцінки багатьох органів.
Існує 2 типи еластографії: компресійна еластографія (КЕ) – якісна, та зсувнохвильова еластографія (ЗХЕ) – кількісна.
Локальні утворення печінки мають змішану картину на еластографії, з великим накладенням у твердості при доброякісних і злоякісних ураженнях, що робить проблемним характеристику цих утворень у печінці. Проте, дифузні захворювання печінки, такі як фіброз, можуть бути досліджені, у тому числі в динаміці, за допомогою ЗХЕ. Зсув хвилі не поширюється в простій рідині. Початкові дослідження показують, що зображення зсуву хвилі може бути корисним у характеристиці кістозних уражень як серозної, так і муцинозної природи. Оцінка інших органів черевної порожнини – обмежена.
Дифузні захворювання печінки є одними із основних проблем здоров’я у світі. Гепатити являють собою групу уражень печінки, що характеризуються запаленням печінки й некрозом гепатоцитів. Гепатит може бути гострим або хронічним, якщо ці зміни зберігаються протягом принаймні 6 місяців. Віруси гепатиту С (HCV) і гепатиту В (HBV) є провідними причинами хронічних захворювань печінки. Вважається, що 180 і 350 мільйонів людей по всьому світу заражені гепатитом С і В відповідно. Річна смертність – від 500000 до 700000 при С і 350000 людей при В гепатитах відповідно.
У пацієнтів з HCV, нездатність до самостійної ерадикації вірусу – від 50% до 90% випадків, залежно від шляху передачі, присутності симптоматичного гепатиту й віку, в якому відбулося інфікування. У західних країнах гепатит С – основне показання для пересадження печінки.
Хронічне ураження печінки переходить у фіброз печінки, що характеризується збільшенням позаклітинного матриксного матеріалу, продукованого фібробластоподібними клітками в паренхімі печінки. Отже, печінка стає жорсткішою, ніж звичайно, і зміни її нормальної будови можуть привести до портальної гіпертензії. Фіброз є основною характеристикою, пов’язаною із прогресуванням хронічного гепатиту. Це може приводити до цирозу печінки, результатом чого може стати печінкова недостатність, підвищується ризик гепатоцелюлярної карциноми (ГЦК), і, в остаточному підсумку, смерті.
Гістологічна оцінка біопсії печінки здійснюється із застосуванням системи балів, які відбивають значення для різних категорій запалення (фаза) і фіброзу (стадія). Є кілька систем оцінок, однак усі мають подібні риси. При оцінці хронічного гепатиту С, найбільш відтворюваною системою балів є Metavir. У цій системі фіброз печінки оцінюється кількісно й стадіюється по 5-бальній шкалі від 0 до 4 (F0, відсутній; F1, фіброзне збільшення портального тракту; F2, перипортальний або початковий порто-портальний перегородковий фіброз із недоторканою архітектурою; F3, архітектурна перебудова, але без очевидних ознак цирозу; і F4, цироз).
Прогресування захворювання печінки відбувається протягом кількох десятиліть і прискорюється під впливом кофакторів, таких як споживання алкоголю, цукровий діабет, літній вік інфікування, вірус імунодефіциту (ВІЛ), комбінація з іншою інфекцією або вірусами. Залежно від впливу кофакторів, від 10% до 40% випадків у пацієнтів із хронічним вірусним гепатитом С розвивається цироз. Прогноз хронічного захворювання печінки сильно залежить від ступеня фіброзу печінки із загрозливими для життя ускладненнями, які можуть виникнути в пацієнтів із цирозом. Смерть, пов’язана з ускладненнями цирозу, становить приблизно 4% на рік, у той час як ГЦК у цій групі зустрічається від 1% до 5% на рік. Таким чином, точна оцінка ступеня печінкового фіброзу є основною для визначення виживаності, призначення лікування й прогнозу.
Циротична трансформація печінки пов’язана зі структурними й біологічними змінами, відповідальними за збільшення портального тиску. Хоча біопсія печінки залишається стандартом для встановлення діагнозу дифузійного захворювання печінки, цей метод – інвазивний, пов’язаний з дискомфортом для пацієнтів і, у рідких випадках, серйозними ускладненнями. Він обмежений значною варіабельністю при оцінці дослідниками й помилками при виборі матеріалу. Неінвазивні методи визначення фіброзу печінки дозволяють провести скринінг раннього фіброзу, що дозволяє почати лікування на етапі з найкращим ефектом. Крім того, це дозволяє неінвазивно моніторувати ефект лікування.
ПРИНЦИПИ ЕЛАСТОГРАФІЇ
Еластографія – новий метод у сонографії, який може забезпечити клінічно корисною інформацією, що раніше було недоступно. Еластографія є методом візуалізації на основі твердості тканини, а не анатомії. Пальпація використовується для оцінки злоякісної пухлини більше тисячі років. Ультразвукову еластографію можна розглядати як еквівалент зображення пальпації, при цьому даючи можливість кількісно оцінити твердість ураження, яку раніше оцінювали тільки суб’єктивно при фізикальному обстеженні. Є 2 типи еластографії: компресійна еластографія (КЕ) та зсувнохвильова еластографія (ЗХЕ). КЕ відтворює зображення на основі того, як тканини реагують на силу зсуву від зовнішнього джерела або самого пацієнта. Ця сила зсуву дозволяє провести якісну оцінку ураження. При ЗХЕ застосовується спеціальний сильний низькочастотний акустичний імпульс (поштовховий імпульс), який приводить до поширення поперечної хвилі, що може бути обчислено як швидкість зсуву. Оскільки швидкість зсуву хвилі через тканини залежить від твердості тканин, можуть бути отримані кількісні значення твердості.
КОМПРЕСІЙНА ЕЛАСТОГРАФІЯ
КЕ визначає відносну деформацію або еластичність тканини в межах контрольного об’єму/поля зору (ПЗ). Чим більше деформується об’єкт при докладанні зусиль, тим вищою є пружність та м’якшим вогнище ураження. Щоб визначити пружність тканини або ушкодження, необхідно оцінити як деформується ураження при застосуванні зовнішнього впливу. Наприклад, якщо мигдаль покласти в посудину з желатином і натиснути на желатин, то останній буде деформований. Це говорить про те, що він сам по собі м’який та має високу пружність. Проте мигдаль не деформується, тому що він твердий та має низьку пружність.
КЕ здійснюється на стандартному ультразвуковому устаткуванні з певним програмним забезпеченням, яке оцінює покадрові відмінності в деформації при дослідженні під зовнішнім впливом.
Сила може бути як від руху пацієнта, наприклад, подих, серцебиття, так і зовнішнього впливу з ритмічним притисненням ультразвукового перетворювача як джерела руху. Одержання оптимальних зображень залежить від системи. При КЕ абсолютне значення деформації не може бути розраховане, тому що сила натискання не може бути точно вимірена. У режимі реального часу зображення КЕ відображається зі шкалою, заснованою на відношенні натягу тканин у межах поля зору.
Результати можуть бути відображені в сірому масштабі або на різних кольорових дисплеях; перевага частіше визначається самим користувачем, залежно від зручності в інтерпретації. У сірому масштабі м’які тканини кодуються білим, у той час як тверді – чорним. Важливо пам’ятати, що при КЕ відображається відносна еластичність і її не слід плутати із зображенням ЗХЕ, де оцінюється абсолютна пружність і кодується в кольорі на попіксельній основі. Декілька факторів, що впливають на еластограму, важливі при виконанні КЕ, у тому числі: що за тканини включені в поле зору, кількість попереднього стиску та рух тканини.
ЕЛАСТОГРАФІЯ ПРИ ВИКОРИСТАННІ АКУСТИЧНОЇ ПРОМЕНЕВОЇ ІМПУЛЬСНОЇ ВІЗУАЛІЗАЦІЇ
Акустична променева імпульсна візуалізація (ARFI) (імпульсний поштовх) може бути використана у якості джерела зсуву тканини. Ця техніка називається ARFI. Цей поштовховий імпульс генерує як осьовий, так і поперечний зсув хвиль. Як з’являється зображення зсуву поперечних хвиль описано нижче. Техніка вимірювання осьового зсуву аналогічна КЕ та має назву Віртуальне Сенсорне Зображення (ВСЗ) (VTI; Siemens Ultrasound, Mountain View, CA, USA).
Існує кілька відмінностей між КЕ й ВСЗ. Однією із важливих відмінностей є те, що сила випромінювання при ARFI максимізується в точці у фокусі, тоді як при КЕ натяг тканин фіксується більш рівномірно в усі сторони, що грунтується на компресії датчиком та ступені зусилля, застосованого локально, що змінюється із глибиною. Таким чином, співвідношення натягу тканин для ВСЗ не повинні бути використані в якості нARFIкількісного методу. Кількісні значення твердості не можуть бути отримані за допомогою ВСЗ. Сила ARFI імпульсу обмежується шляхами входу енергії в тіло й, таким чином, може бути обмежена по глибині проникнення. Загалом, ARFI поштовховий імпульс обмежений у переміщенні не глибше ніж 8-9 см при абдомінальному застосуванні.
Якщо ARFI поштовховий імпульс використовується для генерації тканинного зсуву, то ручний зсув не повинен використовуватись. Датчик має бути зафіксованим, а пацієнт повинен затримати подих і залишатися нерухливим під час дослідження.
ЗСУВНОХВИЛЬОВА ЕЛАСТОГРАФІЯ SWE
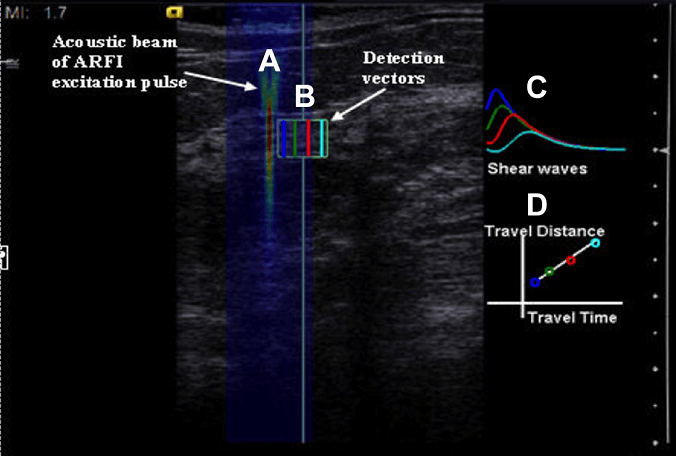
Другий метод для визначення властивостей пружності тканин – це ЗХЕ (SWE). При цій техніці початковий ARFI імпульс (імпульсний поштовх) застосовується до тканини, яка індукує поперечну хвилю, перпендикулярну ультразвуковому променю. Цей спосіб подібний кидку каменю (поштовховий імпульс) у ставок з водою, при цьому брижі відповідають поперечним хвилям. Звичайний B-Режим використовується для розрахунку швидкості зсуву хвилі, що проходить через тканини. Ця техніка показана на мал. 1. Швидкість зсуву хвилі пропорційна твердості. Жорсткість ураження може відображатися як швидкість зсуву хвилі (Vs) (метри /з [м/с]) через тканини, або модуль деформації (кПа [кПа]). При ЗХЕ кількісну оцінку твердості тканини одержують або в передбачуваній точці, або поле зору кодується в кольорі на попіксельній основі Vs ( 2-мірна [2D] – ЗХЕ). Три системи зсувнохвильової еластографії доступні для застосування в черевній порожнині. В апараті ACUSON S3000 ultrasound system (Siemens) може бути отриманий вимір у невеликій зоні (кількісне значення ступеня зсуву тканини), а також одне зображення з виміром швидкості зсуву хвилі в обраній області. Подібна техніка доступна на IU22 і EPIQ (Philips Ultrasound, Bothell, WA, USA), який називається Elastpq. В Aixplorer (Supersonic Imagine, ix-en-provence, France) ефект поштовхових імпульсів підсилюється посилкою серій імпульсів, сфокусованих на глибині, що збільшується, швидше, ніж швидкість зсуву хвилі, у такий спосіб генерується більший конус атаки. Висока частота кадрів зображення досягається шляхом передачі плоских хвиль, що відображає все поле зору (ПЗ) в одному дослідженні. У результаті швидкості зсуву хвилі можуть бути обчислені й відображені (м/с або кПа) у якості кількісного кольорового зображення, що накладається, із частотою кадрів близько 1 кадр в секунду.
Рис. 1. Високоенергетичні ARFI імпульси (А) є генераторами поперечних хвиль, тобто перпендикулярно поштовхового імпульсу. Звичайний ультразвук використовується для моніторингу зсуву хвилі в тканині (В). Зсуви хвиль мають більш високу інтенсивність сигналу ближче до поштовхового імпульсу, амплітуда піку зменшується з відстанню від поштовхового імпульсу (C). Вимірявши час до піка й відстань від поштовхового імпульсу (D), може бути обчислена швидкість зсуву хвилі. Це може бути виражено або у вигляді швидкості в м/с або модулі Юнга в кПа.
ЕЛАСТОГРАФІЯ ПРИ ВОГНИЩЕВИХ УРАЖЕННЯХ ПЕЧІНКИ
КЕ й ЗХЕ можуть бути використані для оцінки вогнищевих уражень печінки. Тому що КЕ є якісним методом, ураження може бути зрівняне з “нормальною” печінкою, тобто можна визначити, чи є ураження твердішим або м’якшим, ніж фонова тканина печінки. Проте цей метод обмежений тим, що фонова тканина печінки може мати змінну твердість, залежно від ступеня стеатозу або фіброзу. До того ж, доброякісні й злоякісні ураження печінки можуть бути і твердими, і м’якими порівняно з “нормальною” печінкою. При ЗХЕ ми одержуємо величину твердості, однак, у зв’язку із широкою варіабельністю патологічної твердості, проблематично відрізнити доброякісне ураження від злоякісного. Наприклад, у серії досліджень Yu and Wilson гемангіома мала діапазон Vs від 0,87 до 4,01 м/с, у середньому – 0,71 м/с, у той час як ГЦК мала діапазон від 0,77 до 4,34 м/с, у середньому – 1,01 м/с. У цілому, різниця в Vs у злоякісних 2,57 +-1,01 м/с і доброякісних новоутворень 1,73+- 0,8 була статистично значимою (P <0,01); Проте великий перехрест щільності між доброякісними й злоякісними утвореннями робить техніку ненадійною для масової оцінки утворень печінки в кожному конкретному випадку. На малюнку 2 показана еластограма зсуву хвилі пацієнта із множинним метастатичним ураженням при колоректальному раці, продемонстрована мінливість метастатичних уражень у того ж пацієнта.
В наш час використання еластографії не рекомендується для характеристики фокусних уражень печінки. Еластографія може бути використана для поліпшення візуалізації ураження для біопсії (мал. 3) і може бути корисна в оцінці ефекту лікування.
ДИФУЗНІ УРАЖЕННЯ ПЕЧІНКИ
Фіброз печінки – серйозна проблема в усьому світі. При його прогресуванні погіршується функція печінки й збільшується ризик раку печінки. Ці хронічні захворювання печінки характеризуються перерозподілом фіброзної тканини в печінці. Важливо визначити стадію фіброзу печінки для прогнозування виживаності й вибору варіантів лікування. На ранніх стадіях фіброз є оборотним, у той час як хвороби, які привели до цирозу, найбільш ймовірно – необоротні.
Рис. 2. 2D зсувнохвильова еластограма печінки в пацієнта з дифузною метастатичною колоректальною карциномою демонструє помітну відмінність твердості метастатичних уражень (білі кружки), один – із середнім значенням 32 кПа, а інший – зі значенням 81 кПа. Широкий діапазон твердості перекриває як доброякісні, так і злоякісні ураження, значно обмежуючи використання зсувнохвильової еластограми в характеристиці локальних уражень печінки.
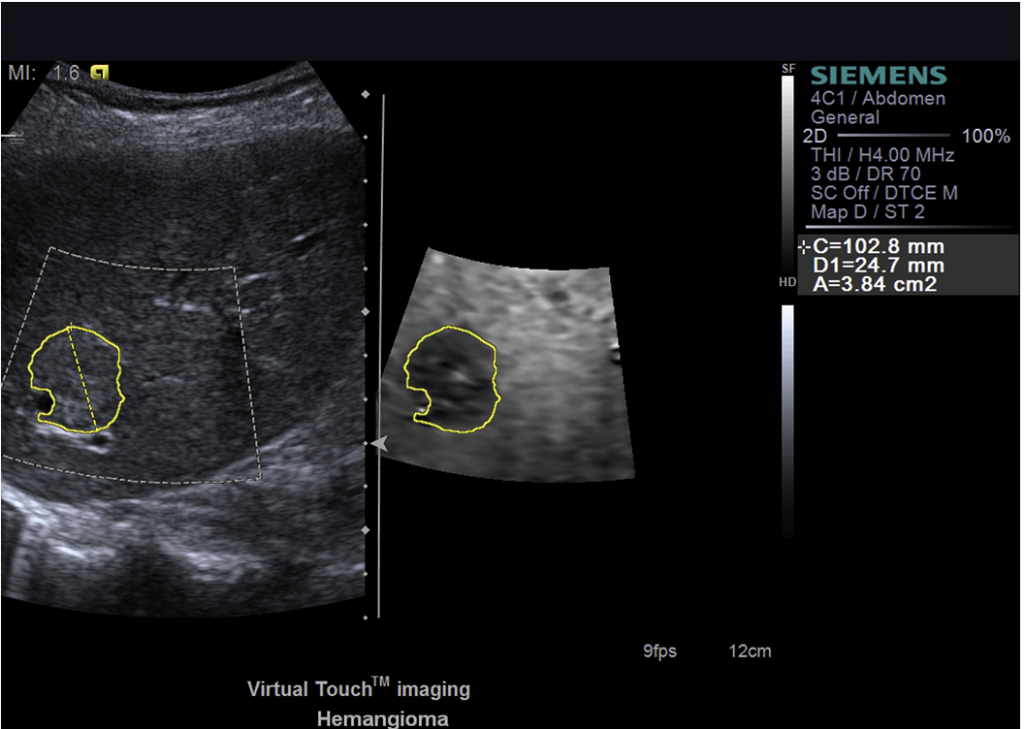
Рис. 3. Віртуальне сенсорне зображення гемангіоми печінки. Зображення ліворуч – в В-режимі. Гемангіома погано візуалізується в B-режимі. Зображення праворуч – Віртуальне сенсорне зображення. Ураження більш щільне, тому навколишня печінка відображається темніше (Надане Д. Clevert, MD, Мюнхен, Німеччина).
У наш час єдиним методом постановки діагнозу фіброзу є біопсія печінки. Біопсія печінки розглядається як золотий стандарт для оцінки фіброзу, його класифікації та визначення стадії, а також класифікації некротично-запальної активності. Але необхідно враховувати інвазивність методу із потенційними ускладненнями, які можуть бути важкими до 1% випадків. Біопсія печінки представляє приблизно 1/50000 об’єму печінки, що приводить до варіабельності результатів у різних дослідників при мікроскопічному дослідженні. Тому, неінвазивні методи оцінки фіброзу печінки завжди були в інтенсивному дослідженні, у тому числі еластографічні методи, що використовують ультразвук і магнітно-резонансну томографію.
Існують різні напрямки методів еластографії печінки для оцінки фіброзу, які не є еквівалентними, а це означає, що граничні величини є специфічними для певної системи й не можуть просто порівнюватись із іншими варіантами досліджень.
Існують спотворювальні фактори, які можуть вплинути на результати еластографії. Зокрема: пацієнт-залежні фактори, такі як застійна серцева недостатність, загострення гострого гепатиту, пов’язане з підвищенням трансаміназ, приймання їжі – усе це робить печінку жорсткішою. Індуковане підвищення твердості можна побачити при позапечінковому холестазі, при використанні бета-блокаторов, а також шляхом проведення проби Вальсальви. Вимірювання повинні проводитися під час затримки подиху в нейтральному дихальному положенні. Вимірювання, проведені в лівій частині печінки, часто ненадійні. Твердість печінки вище в районі від 1,5 см до 2,0 см від краю капсули печінки, тому у цьому місці не слід проводити вимірювання. Великі судини також не повинні бути включені в області дослідження.
ТРАНЗИТОРНА ЕЛАСТОГРАФІЯ
Транзиторна еластографія (ТЕ) впроваджена в 2003 році як перший ультразвуковий метод еластографії печінки й має найбільшу кількість публікацій. Це дослідження здійснюється за допомогою Fibroscan (Echosens, Париж, Франція). ТЕ виконується на спеціалізованому устаткуванні з певним датчиком через міжреберні проміжки. Датчик містить електродинамічний перетворювач, який використовується для генерації перехідних зсувів із частотою 50 Гц із 2-мм подвійною амплітудою (за допомогою М датчика). Одноелементний ультразвуковий перетворювач (3.5 Мгц із M датчиком) установлений на осі вібратора. Перетворювач використовується у звичайному приймачі для забезпечення А-режиму й M-режиму зображення для локалізації печінки для оператора в режимі реального часу. Під час вимірювання генерується надшвидкий імпульс із повторенням із частотою 6 кГц при поширенні контрольованих поперечних хвиль. Одержання даних триває 80 мс і натяг індукований в печінці шляхом поширення поперечних хвиль вимірюється за допомогою стандартного автокореляційного підходу між послідовними ультразвуковими лініями. Пацієнт лежить на спині, права рука знаходиться за головою. Рекомендується виконувати 10 повних вимірів, щоб мати завершене обстеження. При цьому медіана всіх повних вимірів використовується як остаточний показник жорсткості печінки (ЖП). Показники визначаються в кілопаскалях. Вимірювання печінки людини коливаються в діапазоні від 1,5 кПа до 75,0 кПа. Увесь обсяг паренхіми печінки, досліджуваний при ТЕ, як мінімум в 100 раз більше, ніж при біопсії печінки. Різні датчики доступні для пацієнтів з різною конституцією тіла. Відтворюваність вимірів ТЕ в одного або декількох операторів перебуває на високому рівні (внутрішньогруповий коефіцієнт кореляції [ВКК] дорівнює 0,98 в обох випадках) у пацієнтів без ожиріння. Значення ТЕ вище в чоловіків, ніж у жінок.
ТЕ не може бути виконана в пацієнтів з асцитом. Зображеня в В-режимі не можна одержати на Fibroscan. При 13369 дослідженнях ЖП, проведених стандартним датчиком, відсоток невдалих досліджень – 3,1%, а недостовірний результат – в 15,8%. Частота невдалих досліджень пов’язана з індексом маси тіла (ІВТ) більше, ніж 30 кг/м2, вік – страше 52 років і цукровий діабет 2 типу. В іншому дослідженні частота невдалих досліджень зі стандартним датчиком корелює з ІВТ. Частота невдалих досліджень – 7% для ІВТ більше або рівно 30 кг/м2, 19% – для ІВТ більше або рівно 35 кг/м2, 59% – для ІВТ більше або рівно 40 кг/м2. Однак частота невдалих досліджень значно знизилася в пацієнтів при використанні датчика XL.
У пацієнтів із хронічним гепатитом С ЖП мала була більше ніж 6,8 – 7,6 кПа, що означає високу ймовірність значимого фіброзу (F=2 і більше) при біопсії. Критичні значення для прогнозування цирозу (F=4) варіюють у діапазоні від 11,0 до 13,6 кпa. Хоча ТЕ і є менш точною в оцінці відмінності між стадіями фіброзу, але вона може відрізнити відсутність і легкий фіброз від значного фіброзу й цирозу. Мета-аналіз при рецидивуючому посттрансплантаційному гепатиті С показав 98% чутливість і 84% специфічність ТЕ для прогнозування цирозу. Використання ТЕ при хронічному гепатиті С було схвалено в рекомендаціях з лікування вірусного гепатиту Європейською асоціацією з вивчення печінки.
При хронічному гепатиті В, недавній мета-аналіз приводить середню площу під робочою кривою (СППРК) для діагностики значимого фіброзу (F2) і цирозу печінки (F4) від 0,859 до 0,929. При хронічному гепатиті В гостре запалення не є рідкістю й може впливати на вимір ЖП. Було висловлено припущення, що критичні значення повинні бути скоректовані залежно від рівня аланінамінотрансферази.
Дослідження, проведені в пацієнтів з неалкогольною жировою хворобою печінки (НАЖХП) і неалкогольним стеатогепатитом (НАСГ), виявили стеатоз, який, як виявилося, не впливає на вимір ЖП (45,51,52). Цей стеатоз не впливає на швидкість поперечних хвиль, але подовжує їх. Wong (53) порівнює ТЕ з біопсією печінки в 246 пацієнтів НАЖХП із 91% чутливістю й 75% специфічністю для прогнозування важкого фіброзу (F=>3), використовуючи граничне значення 7,9 кПа.
ТЕ використовувалася для оцінки багатьох інших дифузних захворювань печінки зі схожими хорошими результатами. ТЕ може використовуватися як скринінг для виявлення фіброзу в популяції. З 1190 хворих старше 45 років під час дослідження при медогляді 7.5% мали ЖП більше 8 кПа. Біохімія печінки була нормальною в цих пацієнтів, проте, причина хронічного ураження печінки була виявлена в 43%.
Вивчалося використання ТЕ для прогнозування ускладнень цирозу печінки, таких як портальна гіпертензія, а також смертності. СППРК для прогнозування клінічно значимої портальної гіпертензії (печінковий градієнт венозного тиску 12 мм рт.ст.) була від 0,94 до 0,99, для граничного значення – від 13,6 до 21 кпa (56,57). Також були оцінені виміри твердості селезінки, що показало кращу кореляцію з портальним тиском (г= 0,89), ніж значення ЖП у хворих із цирозом. Твердість селезінки мала більше значення СППРК (0,966) для ідентифікації хворих з портальною гіпертензією із градієнтом печінкового венозного тиску =>10 мм Hg. Граничні значення ТЕ від 19,8 до 47,5 кПа дозволяли передбачити варикозне розширення вен стравоходу класу 2 або 3 при СППРК від 0,72 до 0.78. Через значні відмінності у значеннях між дослідженнями, ТЕ не може замінити ендоскопію верхнього відділу шлунково-кишкового тракту для виявлення пацієнтів з варикозним розширенням вен стравоходу.
У великому проспективному дослідженні хворих із хронічним гепатитом С ТЕ була більш точною, ніж біопсія печінки при прогнозуванні. Пацієнти при показниках ТЕ більше 9,5 кПа мали, вірогідно, низьку 5-літню виживаність.
Два проспективних дослідження оцінюють ризик розвитку ГЦК, що розвивається в 3-х річний період в 866 хворих із хронічним гепатитом С и 1130 з гепатитом В. Ризик розвитку ГЦК пропорційний збільшенню ЖП, причому не тільки в пацієнтів розділених на тих у кого є цироз і ні, а й у групах пацієнтів з різним ризиком з уже встановленим цирозом. Європейська асоціація ультразвуку в медицині прийняла наступні рекомендації для клінічного використання ТЕ: ТЕ може бути використаний для оцінки важкості фіброзу печінки в пацієнтів із хронічним вірусним гепатитом за умови, що спотворювальні фактори беруться до уваги, і, особливо, для виявлення пацієнтів з нульовим і м’яким фіброзом, а також зі значним фіброзом і хворих із цирозом. ТЕ корисна для оцінки фіброзу печінки в пацієнтів з НАЖХП, у хворих з алкогольними захворюваннями печінки, з ВІЛ і гепатитом С. Інші типи хронічних захворювань печінки також можуть бути досліджені, але застосування методу обмежене.
ТЕ корисна для оцінки фіброзу печінки в пацієнтів з посттрансплантаційним рецидивом хронічного гепатиту С.
ТЕ має значення для прогнозування ускладнень цирозу печінки, портальної гіпертензії, ГЦК і печінко-асоційованої летальності, але не може замінити ендоскопію для виявлення пацієнтів з варикозним розширенням вен.
ОЦІНКА ШВИДКОСТІ ЗСУВУ ХВИЛІ
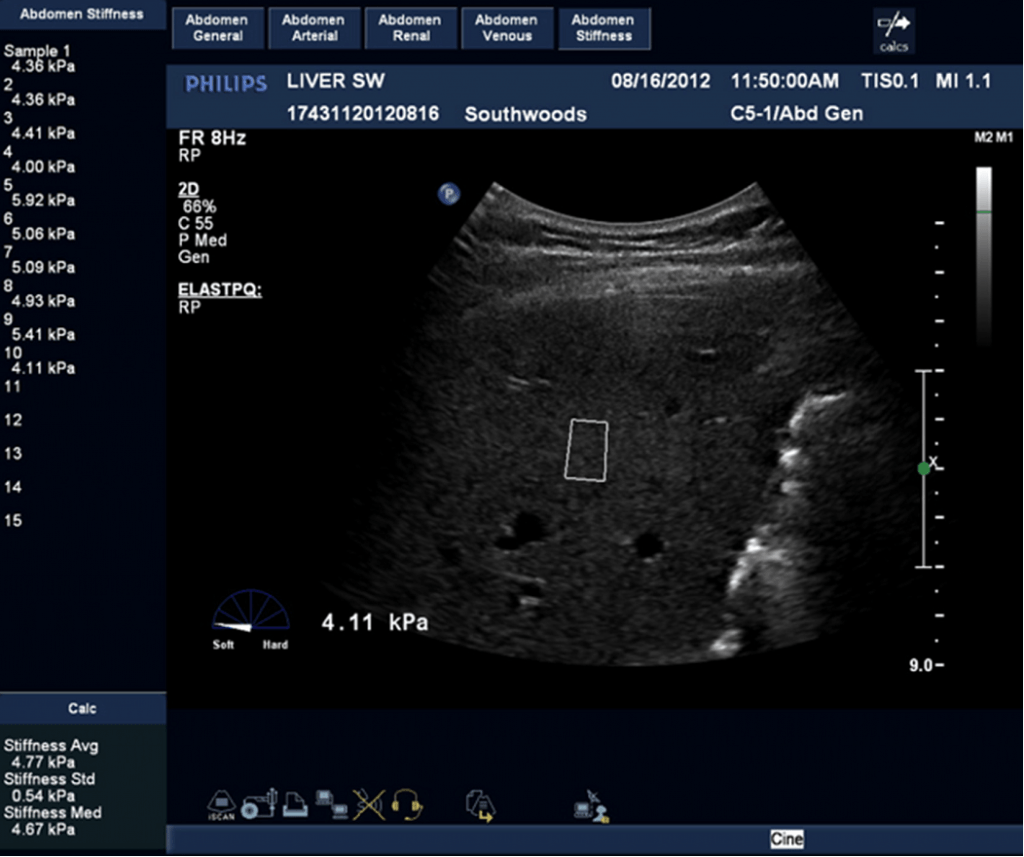
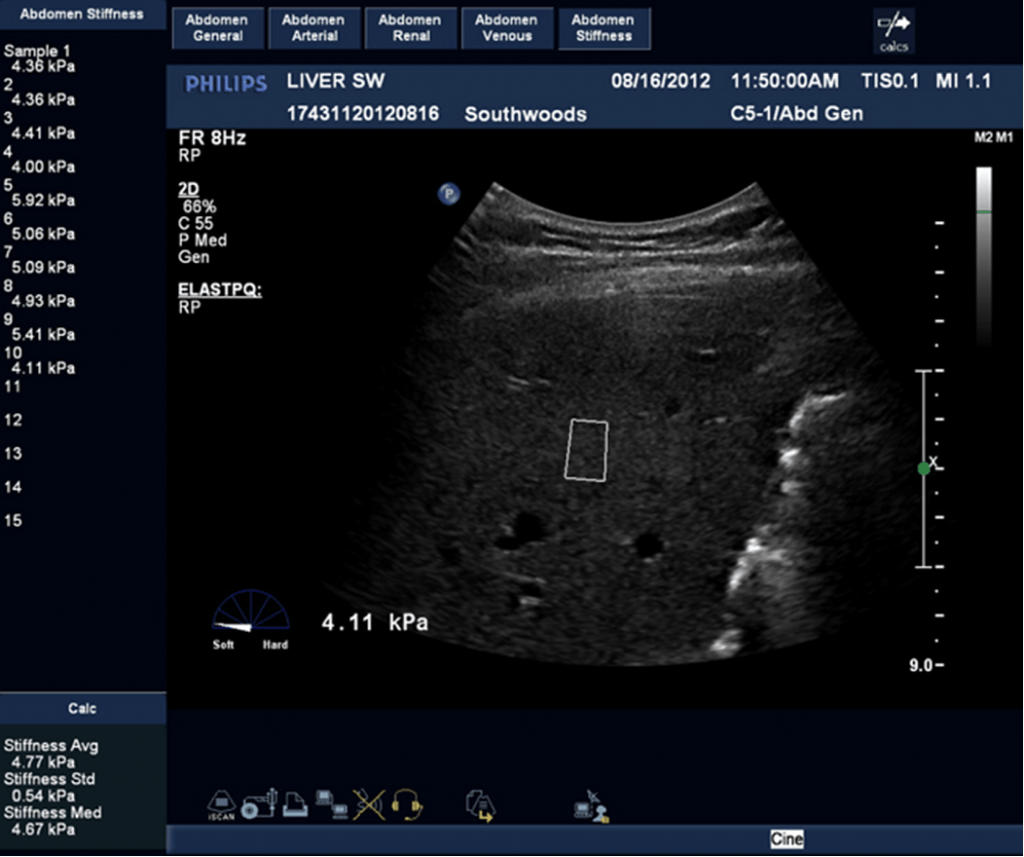
Зі збільшенням фіброзу, печінка стає щільніше, що можна визначити за допомогою ЗХЕ. При цій техніці, ПЗ поміщають в область печінки, яка не містить великих судин. Міжреберний доступ в 8-м сегменті печінки забезпечує більш точні результати. Серію вимірів проводять у той час, як пацієнт затримує подих. Середнє значення цих вимірів використовується для оцінки ступеня фіброзу печінки. На мал. 4 показані результати 27-літнього пацієнта із хронічним гепатитом С. Середня твердість 4,77 кПа узгоджується з результатами біопсії печінки пацієнта з м’яким фіброзом. Мал. 5 являє собою зображення пацієнта з вираженим цирозом, визначена підвищена твердість – 66 кПа.
Використання цієї нової технології в клінічній практиці тільки вивчається. Використання цього методу може зменшити кількість біопсій печінки, що виконуються для оцінки її хронічних захворювань. Потенційне застосування цієї техніки включає оцінку цирозу печінки, запідозреного, але не очевидного на УЗД в В-режимі, обстеження пацієнтів із хронічним гепатитом С, спостереження за пацієнтами для оцінки прогресування захворювання й необхідності початку лікування.
ЗХЕ може бути виконана в невеликому ПЗ (точкова ЗХЕ (тЗХЕ)), або в колірному кодуванні швидкості зсуву хвилі (у м/с або в кПа) у великому ПЗ.
Як і при КЕ, пацієнти повинні дотримувати дієти принаймні протягом 4 годин. Вимірювання ЗХЕ виконуються в міжреберних проміжках над правою часткою печінки з використанням традиційних вигнутих датчиків. Права рука перебуває за головою пацієнта. Датчик ставиться уздовж межребер’я, обмежуючись тінню ребер. ПЗ повинне перебувати, принаймні, на 1,5-2 см нижче капсули печінки, так, щоб не містити в собі великих судин. Рекомендована глибина між 3 і 7 см. Пацієнта просять затримати подих, але не на вдиху (проба Вальсальви). При тЗХЕ починається сканування й відображаються виміри швидкості зсуву хвилі. 2 D-ЗХЕ система дозволяє в режимі реального часу візуалізувати у кольоровому зображенні швидкості зсуву хвилі. Сканування від 3 до 4 секунд в одному місці необхідно для стабілізації показників швидкості зсуву хвилі. Якщо сигнал слабкий або нестабільний, може бути використаний пенетраційний режим.
Як і при ТЕ, підвищення рівня амінотрансферази пов’язані з більш високими значеннями ЖП при ЗХЕ. ЗХЕ дозволяє проводити виміри в різних точках. Порівняння правої і лівої долей показує тенденцію до більш високих значень у лівій долі; однак, результати, отримані в правій долі печінки, завжди більш точні в порівнянні з біопсією печінки.
Усі виробники рекомендують проводити серійні виміри й використовувати середнє значення для ухвалення клінічного рішення. Кількість рекомендованих вимірів варіюється в літературі від 5 до 10. Неточні виміри відкидаються. Неточні значення можуть бути пов’язані з рухом датчика або рухами пацієнта під час дослідження. Більшість систем мають систему оцінки якості адекватності виміру швидкості зсуву хвилі, але без показників для тЗХЕ або кольорового 2-D ЗХЕ. Рекомендовані якісні показники включають: межквартильний інтервал менше 30% і частку успішних досліджень більше 60% (69).
Була показана варіабельність у різних дослідників при тЗХЕ на достатньому рівні, МКК = 0.87. Відтворюваність між різними дослідниками також була достатня при використанні 2-D ЗХЕ (70).
Граничні значення від 1,21 до 1,34 м/с є достовірними для прогнозування вираженого фіброзу (F=>2) зі СППРК від 0,85 до 0.89 (71,72). Для діагностики цирозу печінки граничні значення ЗХЕ варіюються від 1,55 до 2.0 м/с зі СППРК 0,89 до 0.93. У недавно проведеному мета-аналізі 518 пацієнтів із хронічним захворюванням печінки (74) СППРК був 0,87 для прогнозування значимого фіброзу (F=>2), 0,91 для вираженого фіброзу (F=>3) і 0,93 для цирозу. Значення 2-DЗХЕ схожі на тЗХЕ зі СППРК від 0,95 до 0,98 для F =>2, 0,96 для F=>3 і від 0,97 до 0,98 для F=4 (75,76).
Точність ЗХЕ для оцінки фіброзу печінки відповідає КЕ. ЗХЕ дозволяє проводити виміри в пацієнтів з асцитом, у той час як ТЕ – ні. Попередні висновки використання ЗХЕ показали обнадійливі результати у хворих з НАЖХП і НАСГ, а також після трансплантації.
тЗХЕ й 2-DЗХЕ можуть бути рекомендовані для оцінки важкості фіброзу печінки в пацієнтів із хронічним вірусним гепатитом, особливо гепатиту С. Але граничні значення між різними методологіями оцінки зсуву хвилі й для різних марок сканерів, що використовують ту ж методологію, – різні.
Рис. 4. ЗХЕ 28-річного пацієнта із хронічним вірусним гепатитом С. Середня твердість 4,77 кПа узгоджується з результатом біопсії печінки пацієнта з помірним фіброзом. Білий прямокутник показує поле зору, де був отриманий вимір. Зверніть увагу, що було зроблено 10 вимірів. Система обчислює середню твердість, медіану твердості й стандартне відхилення.
КОМПРЕСІЙНА ЕЛАСТОГРАФІЯ
У більшість великих виробників КЕ доступна на всіх високопродуктивних системах як мінімум. КЕ не забезпечує розрахунки значення твердості. Тому було запропоновано декілька кількісних методів інтерпретації: німецький критерій еластичності, японський критерій еластичності та індекс фіброзу печінки (індекс ФП). Усі вони засновані на візуальній оцінці просторових характеристик зображення еластичності в рамках ПЗ. В індексі ФП використовується 9 характеристик, для того щоб обчислити значення твердості, у тому числі середнє й стандартне відхилення відносної величини деформації, складність і відношення синьої області в ПЗ, асиметрія, ексцес, ентропія, момент зворотної різниці й секундний кутовий момент. Опубліковано кілька досліджень використання КЕ. Однак застосування методу обмежене й не може рекомендуватися для клінічного використання. На мал. 6 показаний приклад еластограми при дифузійному захворюванні печінки.
Мал. 5. Еластограма 64-річного чоловіка з вираженим алкогольним цирозом, підтвердженим виміром твердості печінки на рівні 55,9 кПа. Білі кружки – поля зору місця виміру твердості. Виміри у бічній частині ПЗ не повинні використовуватися, оскільки точність виміру зменшується в бічних ділянках ПЗ.
ЕЛАСТОГРАФІЯ ПІДШЛУНКОВОЇ ЗАЛОЗИ
Новоутворення підшлункової залози можуть бути оцінені за допомогою еластографії, як ендоскопічно, так і трансабдомінально. Підшлункова залоза має рівномірно проміжну твердість, але з віком показники можуть стати неоднорідними.
При ендоскопічному підході використовується класифікація на основі колірної шкали КЕ (червоний – м’який, синій – твердий). Нормальна підшлункова залоза м’яка й однорідна, кодується зеленим. Доброякісне запалення підшлункової залози може виглядати як бджолині стільники, переважно синього кольору, або варіант у гетерогенному змішаному кольорі з переважним зеленим або як однорідний зелений варіант. Аденокарцинома має однорідний синій колір (твердість), а також буває гетерогенною з переважно синім кольором у вогнищі ураження. Однак, ця картина спостерігається й у половини хворих із хронічним панкреатитом, так що специфічність методу в діагностиці аденокарциноми становить близько 60%. Нейроендокринні пухлини підшлункової залози мають переважно синій варіант бджолиного стільника, а також однорідний синій варіант і варіант із зеленим центром, оточеним синьою тканиною або однорідний зелений варіант.
Попередні дослідження показують, що однорідний зелений варіант може бути використаний, щоб виключити малігнізацію. Однак, клінічна значимість цієї техніки в диференціації доброякісних від злоякісних утворень – обмежена. Запальні ураження підшлункової залози можуть бути твердими або м’якими залежно від стадії запалення. Неоплазма може мати некротичні області, які проявляються м’якими ділянками контрастними з життєздатною пухлиною, яка тверда. Itokawa виділяє коефіцієнт щільності (жорсткість ураження в порівнянні із щільністю нормальної підшлункової залози) – 23,7 +- 12,7 при розвитку індуративного панкреатиту й 39,1+- 20,5 для раку підшлункової.
У диференціації доброякісних і злоякісних пухлин підшлункової використовуються кількісні й кількісні методи еластографії, які відрізняються досить високою точністю. Два мета-аналізи ендоскопічної ультразвукової (ЕУЗ) еластографії показали високу чутливість, але низьку специфічність у диференціації локальних пухлин підшлункової. Комп’ютеравтоматизовані методи діагностики пропонуються для підвищення точності діфдіагностики утворень підшлункової залози.
Існує обмежена кількість публікацій по використанню ЗХЕ в оцінці кістозних утворень підшлункової залози. ЗХЕ з використанням методу точкового підрахунку може допомогти відрізнити злоякісне ураження із серозним компонентом від муцинозного. Серозні рідини мають низьку в’язкість і не поширюють поперечні хвилі. Значення XXX або 0 отримуються залежно від апарату, із вказівкою відсутності зсуву хвилі в рідині
Проте, муцинозні кістозні ураження мають високу в’язкість, і можуть поширювати поперечні хвилі. У кістах, які містять муцин, можна одержати швидкість зсуву хвилі (у м/с або кПа). У дослідженні D’onofrio et al. були вивчено 14 муцинозних цистоаденоми, 4 псевдокісти, 3 внутрішньопротокові папілярно-муцинозні пухлини й 2 серозні цистоаденоми. Отримані значення варіювали від ХХХХ /0 до 4,85 м/с у муцинозних цистоаденомах, від ХХХХ /0 до 3,11 м/с у псевдокістах, від XXXX / 0 до 4,57 м/с у внутрішньопротокових папілярно-муцинозних пухлинах. У серозних цистоаденомах усі обчислені значення були XXXX / 0 м/с. Діагностична точність при доброякісних та злоякісних панкреатичних кіст склала 78%.
Рис. 6. КЕ техніка в здорової людини (A) і в пацієнтів з компенсованим цирозом печінки (B). ПЗ кольорової еластографії накладається на звичайний B-режим зображення. Червоний колір означає, що тканина м’яка, а синій – тверда. Відображені еластограма та ЖП. (Надане Г. Ferraioli, MD, Італія.)
Рисунок 7 демонструє використання точкового підрахунку зсуву хвилі (А) і використання зображення пружності (В) у пацієнта із загостренням хронічного панкреатиту. Недавні дослідження показали, що діагноз гострий панкреатит може бути поставлений за допомогою ЗХЕ з високою чутливістю й специфічністю. При використанні граничного значення 1,63 м/с були отримані: чутливість 100% і специфічність 98% . ЗХЕ показала себе краще, ніж В-режим ультразвуку й КТ в діагностиці гострого панкреатиту.
У провідних європейських посібниках і рекомендаціях із клінічного використання ультразвукової еластографії відзначені наступні тези: (1) ЕУЗ еластографія рекомендована в якості додаткового методу для характеристики вогнищевих уражень підшлункової залози; (2) при серйозній клінічній підозрі на рак підшлункової залози, у випадку, коли біопсія не дає результатів або негативна, щільне вогнищеве ураження на еластографії й/або виявлене при ЕУЗ із контрастним посиленням (гіповаскулярне ураження), – слід керуватися клінічним ознаками, призначивши повторну ЕУЗ тонкогольну біопсію або скерувати хворого в хірургію; (3) ЕУЗ еластографія в цей час не може бути рекомендована для діфдіагностики хронічного панкреатиту й раку підшлункової залози у зв’язку з їхньою схожою щільністю тканини у великому відсотку випадків.
Рис. 7. У цього пацієнта, який мав скарги на біль у животі, на зображенні в В-режимі показана збільшена підшлункова залоза з нерівномірним контуром і ехогенністю, множинними петріфікатами, з помірним періпанкреатичним набряком. Підвищення швидкості зсуву хвилі 4,96 м/с (А), свідчить про гострий панкреатит. Відповідне КЕ зображення (B) показує підвищену жорсткість (колірна гама із червоним – тверді тканини) вздовж усього тіла підшлункової і її хвоста, що наводить на думку про гостре запалення (Надане A. Mateen, MD, Хайдарабад, Індія).
ЕЛАСТОГРАФІЯ ШЛУНКОВО-КИШКОВОГО ТРАКТУ
Еластографія може показати шарувату структуру кишкової стінки, але при цьому не завжди є відповідність шарам в В-режимі. Техніка називається strain rate imaging (SRI) і була запропонована для оцінки скоротливості стінок шлунково-кишкового тракту (ШКТ). КЕ може бути використана, щоб оцінити твердість вогнищевих уражень ШКТ (106). КЕ шлунково-кишкового тракту виконується лінійним перетворювачем і доступна на багатьох сканерах. SRI доступна тільки з певним програмним забезпеченням і тільки з одним сканером.
Тіні від газу кишечника і перистальтики є серйозною проблемою для еластографії шлунково-кишкового тракту, погіршуючи якість зображення, знижуючи точність напівкількісних еластографічних вимірів. Необхідне проведення додаткових досліджень, щоб установити роль еластографії в оцінці патологічних процесів і моторики.
Попередні роботи показують, що еластографія може бути корисна в оцінці стенозу при хворобі Крона, викликаного запальним або фіброзним процесом. Фіброзний стеноз виглядає щільним, у той час як запальний стеноз – м’яким. Пацієнти з активною хворобою Крона мають більш високий коефіцієнт натягу між запаленою та нормальною областю, ніж пацієнти в стадії ремісії.
Існує можливість оцінити відносну еластичність м’язового шару стінки шлунка й це дозволяє відображати розподіл натягу. Проведені дослідження показують можливість за допомогою SRI відрізнити скорочувальну активність поздовжніх м’язових шарів від кругових, які не можуть бути оцінені на B-режимі. SRI використовувалася як in vitrо, так і in vivo для моніторингу відповіді на введення препарату. Ahmed et al. змогли ідентифікувати підгрупи з диспепсією на основі вимірів еластичності стінки шлунка при SRI.
Провідні європейські (EFSUMB) посібники та рекомендації по клінічному використанню ультразвукової еластографії вказують, що еластографія показана:
Для характеристики уражень стінки кишківника та, можливо, розпізнаванні активної фази запалення від фіброзного стенозу за допомогою КЕ.
Для оцінки скоротливості шлунка й еластичності стінок ШКТ при SRI.
РЕЗЮМЕ
Ультразвукова еластографія може забезпечити додатковою інформацією в порівнянні з більш традиційним ультразвуком при виявленні та оцінці утворень черевної порожнини. Проте збіг значень твердості при доброякісних і злоякісних абдомінальних ураженнях, наприклад молочної залози і передміхурової залози, обмежує застосування цього методу. Необхідно провести додаткові дослідження для визначення корисності ультразвукової еластографії в оцінці пухлин черевної порожнини.
Попередні дослідження показують, що еластографія може бути корисна для діфдіагностики фіброзних і запальних стриктур при хворобі Крона.
Оцінка ЖП із використанням ультразвукової еластографії ретельно вивчена й при цьому показано, що вона є точним неінвазивним методом для постановки діагнозу фіброзу печінки. Кілька методів еластографії, включаючи КЕ й ЗХЕ, дозволяють досить точно поставити діагноз фіброзу печінки й діагностувати явища портальної гіпертензії. Можна очікувати, що більш широке використання ультразвукової еластографії дозволить зменшити кількість біопсій печінки, що виконуються для діагностики й постановки діагнозу фіброзу печінки. Використання еластографії дозволить поліпшити контроль ефективності лікування хронічних захворювань печінки.
УЗД апарат Siemens Acuson S2000 підтримує передову технологію еластографії зсувної хвилі. Кращі пропозиції від компанії RH.
Питання та відповіді (FAQ)
Що таке ультразвукова еластографія?
- Ультразвукова еластографія – це сучасний метод візуалізації, який створює зображення на основі твердості тканин, а не їх анатомічної структури. Багато захворювань органів мають різну твердість, яку можна виявити за допомогою цього методу.
Які типи еластографії існують?
- Існують два основних типи: компресійна еластографія (КЕ) – якісний метод, та зсувнохвильова еластографія (ЗХЕ) – кількісний метод.
Для чого використовується еластографія печінки?
- ЗХЕ є ефективним неінвазивним методом оцінки фіброзу печінки. Вона також може допомогти визначити характер рідини (серозний або муцинозний) та оцінити печінковий венозний тиск.
Чи може еластографія точно визначити доброякісні та злоякісні утворення в печінці?
- Еластографія обмежена у точному розрізненні доброякісних та злоякісних утворень печінки через перекриття показників твердості. Хоча статистично злоякісні утворення жорсткіші, існують значні подібності.
Як еластографія допомагає в діагностиці дифузних захворювань печінки?
- ЗХЕ особливо корисна для дослідження дифузних захворювань печінки, таких як фіброз, дозволяючи відстежувати їх динаміку.
Які обмеження еластографії при дослідженні органів черевної порожнини?
- Оцінка інших органів черевної порожнини, крім печінки, за допомогою еластографії обмежена.
Чим еластографія відрізняється від традиційної пальпації?
- Еластографію можна розглядати як візуальний еквівалент пальпації, але з можливістю кількісно оцінити твердість ураження, на відміну від суб’єктивної оцінки при фізикальному обстеженні.

















14.10.2019
Виктория