Автори: Elena Tatiana Cârțână, Dan Ionuț Gheonea, Adrian Săftoiu
ВСТУП
Ендоскопічне УЗД (ЕУЗД) являє собою цінний додаток до методів візуалізації при захворюваннях травної системи, сприяючи широкому спектру діагностичних і терапевтичних застосувань при захворюваннях шлунково-кишкового тракту (ШКТ) і підшлунково-жовчних шляхів.
Завдяки чудовому розширенню в порівнянні з іншими методами візуалізації поперечного перерізу і додатковій можливості виконання тонкоголкової аспірації для підтвердження патології, ЕУЗД може викликати зміни як в діагнозі пацієнта, так і в лікуванні, роблячи значний вплив на клінічне рішення.
Що стосується нижніх відділів шлунково-кишкового тракту, ЕУЗД зіграла значну роль у визначенні стадії раку прямої кишки, представляючи ключовий метод візуалізації для предтерапевтичної оцінки цих пацієнтів.
Мета цього огляду полягає в тому, щоб виділити останні дані про застосування ЕУЗД для оцінки колоректального раку (КРР).
ЕУЗД ДЛЯ ЗОБРАЖЕННЯ КОЛОРЕКТАЛЬНОГО РАКУ
ЕУЗД – це вже зарекомендував себе метод візуалізації, який використовується для первинної оцінки пацієнтів з раком прямої кишки, який вважається швидкою процедурою, яка добре переноситься, що дозволяє точно визначити його стадію.
Терапевтична стратегія визначається для кожного пацієнта на підставі точної оцінки локального поширення захворювання в стінці прямої кишки і оточуючих структурах (стадія Т), лімфатичних вузлах (стадія N), локалізації і можливому ураженні мезоректальної фасції.
ЕУЗД може оцінити глибину проникнення пухлини з точністю від 70% до 95%, найкраще підходить для діагностики ранніх уражень і знаходиться в руках досвідчених дослідників. Завдяки високій роздільній здатності, що забезпечує надійну демаркацію між гістологічними шарами стінки прямої кишки, ЕУЗД рекомендована як високоточний метод для вибору ранніх уражень прямої кишки, відповідний для ендоскопічної резекції або трансанальної ендоскопічної мікрохірургії, як альтернатива традиційної хірургії.
Одним з недоліків, зазначених ЕУЗД при оцінці пухлин прямої кишки, через обмежений обсяг глибокої візуалізації, була низька ступінь точності при оцінці залучення мезоректальної фасції, що є важливим чинником для прогнозування місцевого рецидиву і який краще оцінюється методом МРТ.
Результати недавнього дослідження показали, що для пухлин передньої стінки прямої кишки з низьким рівнем ураження ЕУЗД може прогнозувати залучення мезоректальної фасції з підвищеною точністю і високою негативною прогностичною цінністю, таким чином, виконуючи діагностику аналогічно МРТ.
Стадія за межами раку прямої кишки
При стадіюванні раку за межами прямої кишки широко використовується зображення поперечного перерізу за допомогою КТ, оскільки воно може надати надійну інформацію про дистальне поширення, хоча і не забезпечує ідеальної точності для локального визначення стадії.
У той час як хірургія раніше вважалася золотим стандартом лікування пацієнтів з КРР, в даний час адекватна терапія включає міждисциплінарний план, складений онкологами, гастроентерологами та хірургами. Отже, кількість резекцій первинної пухлини у пацієнтів з КРР знизилася, а показники виживаності покращилися з моменту введення нових хіміотерапевтичних режимів і біологічних агентів.
ЕУЗ-дослідження товстої кишки раніше робилося за допомогою ехоендоскопа з прямим косим оглядом, але його конструкція дозволяла отримувати зображення тільки сигмовидної кишки і лівої стінки товстої кишки. Міні-датчик також використовувався для пухлин товстої кишки, і завдяки його зменшеному діаметру, який дозволяє проходити через робочий канал звичайних колоноскопія, він може оцінювати ураження по всій товстій кишці. Хоча міні-датчик може точно визначити стадію більш ранніх пухлин, його ефективність утруднена через обмеження акустичного проникнення в глибину, що призводить до менш точного стадіювання більших і інвазивних видів раку.
Одним з поліпшень в технології ЕУЗД була розробка радіального ехоендоскопа з прямим оглядом, який був недавно протестований і довів свою придатність для визначення стадії раку за межами прямої кишки. Ехоендоскоп переднього огляду зміг безпечно досягти всіх уражень товстої кишки і в терміни, аналогічні стандартним процедурам колоноскопії. Хоча точність визначення стадії пухлини склала 81,0% і лише 52,4% для стадії лімфатичних вузлів, в цілому ЕУЗД було більш точним в порівнянні з КТ (81,0% проти 68,4%), і ці результати, безсумнівно, можуть бути поліпшені за допомогою подальших досліджень і постійно зростаючого досвіду.
У нашому інституті ми також виконали ЕУЗ-дослідження за допомогою ехоендоскопа з радіальними гратами переднього огляду для постановки діагнозу за межі прямої кишки, що виявилося дуже точним показником (зобр. 1).
Зображення 1: Ендоскопічне ультразвукове зображення раку сигмовидної кишки Т3, що показує гіпоехогенну інфільтрацію за межами власного м’язового шару (стрілки).
Методи поліпшення зображення ЕУЗД для оцінки колоректального раку
ЕУЗД з контрастним посиленням: використання внутрішньовенних ультразвукових контрастних речовин стало важливим кроком вперед в практиці ультразвукового дослідження, що дозволило краще охарактеризувати ураження на основі їх судинного посилення. Крім того, кількісна оцінка перфузії можлива за допомогою додаткових програмних додатків для постобробки, які дозволяють об’єктивно вимірювати кілька параметрів, що, таким чином, корисно для моніторингу ранніх змін васкуляризації після антиангіогенного лікування.
Отже, були проведені подальші клінічні дослідження, які доводять, що ультразвукове дослідження з контрастним посиленням (CE-US) може оцінити ранню відповідь кількох ділянок пухлини, включаючи гепатоцелюлярну карциному, колоректальні метастази і карциному нирок.
Однак щодо колоректальних захворювань є лише обмежена інформація про роль CE-US, і початкові опубліковані дані про КРР були результатом трансабдомінального обстеження.
Zhuang і інші запропонували можливість використання CE-US для кількісної оцінки ангіогенезу колоректальной пухлини на основі аналізу кривої залежності інтенсивності від часу (TIC). Один з обчислених параметрів, тобто AUC (площа під кривою), як непрямий показник об’єму крові, був значно вище в аденокарциномі в порівнянні з аденомами, а також позитивно корелював з MVD, що вказує на можливе прогностичне значення для колоректальних пухлин.
CE-EUS-дослідження пухлин прямої кишки проводилося з використанням жорсткого зонда, а аналіз TIC використовувався для визначення декількох параметрів перфузії при пошуку кореляцій з MVD і іншими клінічними і патологічними прогностичними факторами. Тільки слабка позитивна кореляція була підтверджена між параметром підвищеної інтенсивності та MVD (r = 0,295, P = 0,016). Той же самий параметр TIC зворотньо корелював зі ступенем гістологічної диференціювання (r = -0,264, P = 0,007). Однак це тільки початкові дослідження, які припускають можливість використання CE-US в якості безпечного і більш зручного методу візуалізації для динамічних вимірювань ангіогенезу пухлини при CRC, і, ймовірно, за ними підуть подальші валідаційні дослідження (зобр. 2).
Зображення 2: Ендоскопічна ультрасонографія з контрастним посиленням пухлини T3 ректо-сигмовидного переходу. A: до досягнення контрасту (тканинна гармоніка зображення з лівого боку, В-режим з правого боку); B: Максимальне посилення наповнення пухлини через 15 секунд після ін’єкції контрастної речовини з ділянками з підвищеною чутливістю, що чергуються з безсудинними (некротичними) ділянками.
Еластографія ЕУЗД: відображає відмінності між жорсткістю тканин шляхом додавання кольорового кодування для різних значень еластичності до звичайних зображень в градаціях сірого.
Деформація тканин вимірюється за допомогою інтегрованого програмного додатку, який аналізує відображені в зворотному напрямку ультразвукові сигнали, і, таким чином, можна оцінити еластичні властивості тканин, що дозволяє краще охарактеризувати і відрізнити доброякісні пухлини від злоякісних. Можлива також кількісна характеристика твердості тканин.
Аналіз гістограми відтінків має на увазі графічне представлення розподілу кольорів в області, що цікавить і встановлення середнього значення гістограми в якості міри твердості ураження. Розрахунок коефіцієнта деформації показує еластографічні властивості цільового ураження в обраній області з навколишніх нормальних структур. Для візуалізації ШКТ еластографія здається складнішою з технічної точки зору, особливо для нормального кишечника, оскільки вона порушена через його тонку стінку і перистальтичні рухи.
Тому дослідження були обмежені. Для колоректальних пухлин основним показанням до сих пір було диференціювання доброякісних утворень від злоякісних (зобр. 3). Трансректальна еластографія використовувалася при обстеженні 69 пацієнтів з пухлинами прямої кишки, що дозволило відрізнити аденокарциноми від аденом з високою точністю (0,94) на основі порогового значення коефіцієнта деформації (SR) 1,25.
Потім пішло валідаційне дослідження за участю 120 пацієнтів, яке продемонструвало таку ж високу точність при використанні спочатку запропонованого порогового значення SR для диференціації доброякісних пухлин від злоякісних. Крім того, розрахунок SR виявився точнішим порівняно з ЕУЗД і МРТ.
Зображення 3: Ендоскопічне ультразвукове зображення еластографії аденокарциноми прямої кишки з переважно синім малюнком, що вказує на низький ступінь деформації (зліва – режим соноеластографіі в реальному часі, справа – В-режим).
Тривимірна ЕУЗД: має збільшене розширення зображення для ЕУЗД, що дозволяє відображати анатомію прямої і периректальної анатомії в декількох площинах і, отже, має поліпшену точність стадіювання для оцінки T і N в порівнянні з традиційною ЕУЗД і КТ.
Нещодавно опубліковані дані показують відмінні результати для 3D-ЕУЗД, які змогли правильно класифікувати пухлини T1 в 97,1% випадків, T2 в 94,3%, T3 в 95,7% і T4 в 98,5% випадків, з післяопераційною морфологічною оцінкою, використаної в якості контролю.
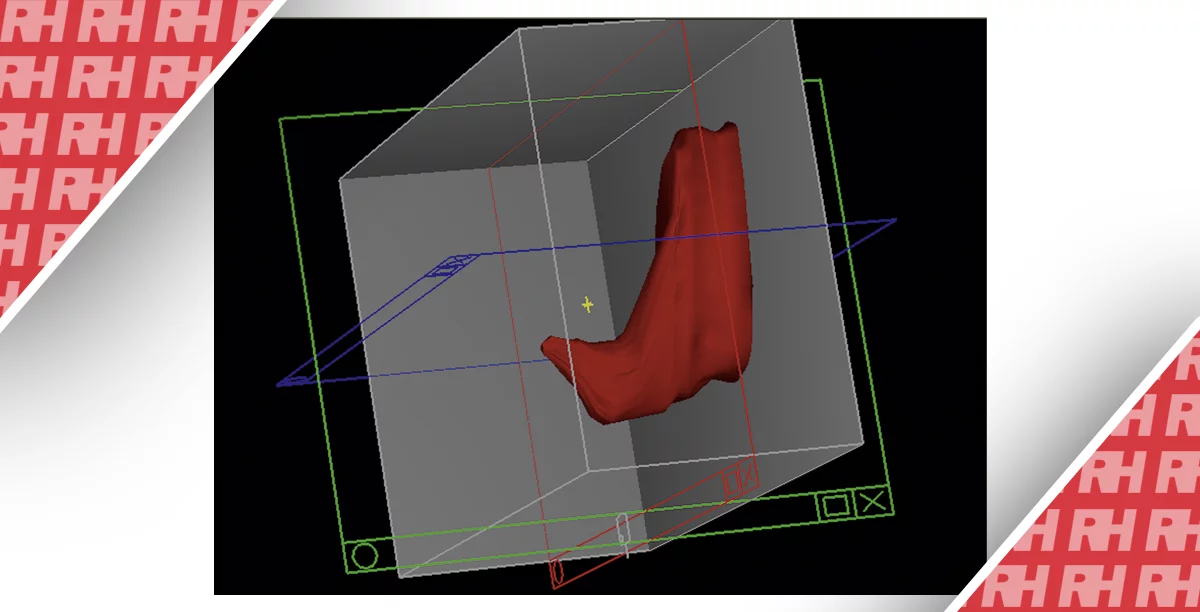
Сприятливі результати були також отримані при визначенні метастатичного ураження лімфатичних вузлів з діагностичною точністю 87,3%. Такі точні об’ємні вимірювання можна використовувати для оцінки відповіді пухлини після променевої та хіміотерапії і, можливо, для підвищення діагностичної ефективності ЕУЗД в цих умовах. Згодом слід додатково оцінити роль 3D-EUS для ведення пацієнтів з КРР, оскільки вона може компенсувати деякі обмеження, що накладаються традиційним ЕУЗД, і підвищити діагностичну точність (зобр. 4).
Зображення 4: Тривимірне ендоскопічне ультразвукове дослідження раку прямої кишки T3 з перітуморальними лімфатичними вузлами (червоні стрілки).
ЕУЗД ПРИ ЗАПАЛЬНИХ ЗАХВОРЮВАННЯХ КИШЕЧНИКА
У пацієнтів із запальним захворюванням кишечника основним показанням до ЕУЗД було визначення періанальних і параректальних ускладнень хвороби Крона.
У цих пацієнтів зазвичай складні свищі, з високою частотою рецидивів, тому точна анатомічна оцінка важлива при плануванні найбільш придатної хірургічної терапії з метою запобігання нетримання калу і погіршення якості життя пацієнтів. Для цього конкретного показання трансректальна ЕУЗД виявилася кращою за інші методи обстеження, включаючи КТ, фістулографію, і її можна порівняти з МРТ.
Недавній метааналіз, що порівнює ефективність МРТ і ендоанального УЗД для дослідження періанальних свищів, показав схожу чутливість (0,87), хоча і низьку специфічність для обох методів (0,69 для МРТ проти 0,43 для ендоанального УЗД).
Однак дослідження, включені в цей метааналіз, показали високу ступінь неоднорідності. На відміну від МРТ органів малого тазу, трансректальна ЕУЗД може також візуалізувати слизову прямої кишки і оцінити тяжкість запалення для прогнозування результату. 3D-ЕУЗД дає більш точну інформацію про свищевий тракт щодо аноректальної анатомії, вказуючи також повздовжню і сагітальну площини зображення.
ЕУЗД добре переноситься пацієнтами, безпечніша і дешевша в порівнянні з МРТ, тому її можна легко повторити і використовувати для контролю терапевтичної відповіді. У невеликому проспективному дослідженні за участю пацієнтів з хворобою Крона з періанальними свищами ЕУЗД, виконана під час комбінованого медикаментозного і хірургічного лікування, була пов’язана з кращими результатами, зменшуючи необхідність у додатковій операції.
Інші потенційні застосування включають диференціацію запальних і фіброзних стриктур і визначення запальних мас при хворобі Крона. Також перевірялася можливість використання деформаційної еластографії для відмінності активного запального стенозу від фіброзного.
Більш того, пілотне дослідження з використанням трансректального ЕУЗД також вивчало роль еластографії в класифікації фенотипів ЗЗК. У дослідження були включені 30 пацієнтів з хворобою Крона, 25 з виразковим колітом і 28 контрольних пацієнтів, і було виявлено значно вищий SR при хворобі Крона в порівнянні з пацієнтами з виразковим колітом і контрольною групою. Хоча товщина стінки прямої кишки була різною у пацієнтів з виразковим колітом і контрольної групи, не було різниці в розрахованому SR.
ЕУЗД при колоректальних субмукозних ураженнях
Субепітеліальні ураження, які можуть бути виявлені під час колоноскопії, охоплюють широкий спектр інтрамуральних уражень і зовнішніх стиснень. ЕУЗД являє собою ідеальний метод дослідження для забезпечення точної класифікації цих уражень по всій товстій кишці з використанням гнучких міні-датчиків або недавно представленого радіального ехоендоскопа прямого огляду, як описано раніше.
Ознаки, виявлені під час ЕУЗД, такі як вихідний шар стінки і ехоструктура, вказують на природу ураження, і цитологічне або гістологічне підтвердження може бути надано шляхом виконання біопсії. ЕУЗД також може використовуватися для безпечного проведення ендоскопічної резекції окремих нейроендокринних пухлин.
Особливо важливо розрізняти доброякісні та злоякісні новоутворення, особливо при пухлинах строми шлунково-кишкового тракту. Відбір проб під контролем ЕУЗД рекомендується тільки тоді, коли він може змінити лікування пацієнтів.
Недавні дослідження вивчали можливість використання CE-US для характеристики і диференціації підслизових пухлин. У той час як лейоміоми і гастроінтестинальні стромальні пухлини, що походять з одного і того ж шару, може бути важко диференціювати на основі одних тільки ознак ЕУЗД, недавнє дослідження повідомило про різні патерни в CE-EUS, при цьому ГІСП показує гіпернаповнення, на відміну від лейоміом, які були гіпонаповненними.
Крім того, CE-EUS може прогнозувати злоякісний потенціал ГІСП, спостерігаючи васкуляризацію пухлини. Гетерогенне посилення, по-видимому, вказує на наявність неоангіогенезу і являє собою особливість, що більш часто зустрічається в ГІСП середнього і високого ризику, як недавно було запропоновано. Хоча ці дослідження включали пухлини верхніх відділів шлунково-кишкового тракту, їх результати можуть бути переведені на колоректальні ураження в очікуванні подальшого дослідження, необхідного для підтвердження первинних результатів (зобр. 5).
Зображення 5: Ендоскопічне ультразвукове дослідження з контрастним посиленням при великій стромальній пухлині шлунково-кишкового тракту прямої кишки. A: До введення контрасту; B: Гетерогенне посилення після введення контрастної речовини.
ВИСНОВОК
ЕУЗД перетворилося не тільки в потужний діагностичний інструмент, якому сприяла розробка кількох методів поліпшення зображення і можливість відбору зразків тканин, але і як метод керівництва для менш інвазивних терапевтичних процедур з можливими показаннями як для злоякісних, так і для доброякісних колоректальних захворювань.
На додаток до вже встановлених показань, таким як визначення стадії раку прямої кишки, вивчаються нові можливості застосування, включаючи використання CE-EUS для діагностики та прогностичної оцінки як колоректальних пухлин, так і ЗЗК, або можливість виконання ЕУЗД-еластографії для поліпшення диференційного діагнозу уражень.
Однак для підтвердження цих початкових результатів необхідні більш всебічні дослідження. Терапевтичні процедури під контролем ЕУЗД включають дренування скупчень в черевній порожнині і тазу в якості менш інвазивної альтернативи звичайним хірургічним процедурам. Впровадження реперних маркерів під контролем ЕУЗД для проведення променевої терапії при раку прямої кишки і таргетна доставка ліків за допомогою мікропухирців є потенційними додатками, які можуть значно змінити лікування пацієнтів, хоча потрібні подальші дослідження, оскільки поточні дані обмежені лише звітами про випадки і доклінічними дослідженнями.















24.09.2020
Sadovnikov Sergii