🤖 Короткий переказ від ШІ
Ця стаття розглядає ендоскопічну діагностику раннього раку шлунка, зосереджуючись на системі класифікації “судина плюс поверхня” (VS) та простому алгоритмі діагностики MESDA-G. Аналізуються ключові ознаки, що спостерігаються за допомогою збільшувальної ендоскопії з вузькосмуговою візуалізацією (NBI).
Встановлено, що система VS та алгоритм MESDA-G є ефективними інструментами для диференціальної діагностики ракових і доброякісних уражень шлунка, хоча деякі знебарвлені плоскі недиференційовані ракові утворення можуть вимагати біопсії. Для повного розуміння контексту діагностики раннього раку шлунка, ознайомтеся з медичними ендоскопами.
✅ Ключові тези зі статті:
- Діагностика: Система класифікації VS та алгоритм MESDA-G дозволяють точно диференціювати ракові та доброякісні ураження шлунка за допомогою збільшувальної ендоскопії.
- Лікування: Точна ендоскопічна діагностика є ключовою для вибору оптимальної тактики лікування раннього раку шлунка.
- Переваги: Збільшувальна ендоскопія з NBI та аналіз патернів мікросудин (MV) і мікроповерхні (MS) підвищують точність діагностики.
- Обмеження: Деякі недиференційовані ракові утворення можуть бути складними для діагностики, що вимагає біопсії.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: Masaki Miyaoka, Kenshi Yao, Hiroshi Tanabe, Takao Kanemitsu, Kensei Otsu, Kentaro Imamura, Yoichiro Ono, Satoshi Ishikawa, Tatsuhisa Yasaka, Toshiharu Ueki, Atsuko Ota, Seiji Haraoka, Akinori Iwashita
Зміст:
- Вступ
- Діагностична система
- Система класифікації VS
- Діагностичні критерії
- MESDA-G З використанням системи класифікації VS
- Характерні дані слиЗової оболонки шлунка при ендоскопії Зі Збільшеною деталіЗацією
- WOS
- LBC
- Зовнішній вигляд білого глобуса (WGA)
- Судини всередині епітеліального кола (VEC)
Вступ
Ендоскопічна діагностика раннього раку шлунка в основному складається з двох етапів:
- виявлення раку
- диференціація ракових і незлоякісних уражень.
Корисність ендоскопічного спостереження з поліпшеним зображенням в скринінговій ендоскопії для виявлення раку шлунка на ранній стадії залишається неясною, але в даний час проводиться масштабне клінічне дослідження з цього питання. З іншого боку, вже встановлена корисність збільшувальної ендоскопії з поліпшеними зображеннями в диференціальній діагностиці раку шлунка.
Діагностична система
Система класифікації VS
Система класифікації “судина плюс поверхня” (VS) – це визнана діагностична система для диференціації ракових і доброякісних уражень з використанням ендоскопії зі збільшенням; ця система була запропонована Yao et al. в 2009 р. Корисність цієї системи для діагностики раку шлунка на ранніх стадіях підтверджена доказами високого рівня.
Найбільш корисними особливостями цієї діагностичної системи є наступні:
- вона дозволяє діагностувати дрібні ракові утворення розміром ≤5 мм і ранні злоякісні пухлини шлунка поверхневого плоского (0 – IIb) типу серед гастрітоподобних злоякісних пухлин (поверхневий тип) раннього раку шлунка 0 – II типів), який неможливо діагностувати за допомогою традиційної ендоскопії;
- дозволяє передопераційно визначити межі раннього раку шлунка.
Основним принципом системи класифікації VS є оцінка патернів мікросудин (MV) і мікроповерхностей (MS) з використанням анатомічних термінів для аналізу результатів ендоскопії шлунка зі збільшенням (зобр. 1).
Терміни, що використовуються для аналізу паттерна MV, включають наступне:
- субепітеліальна капілярна мережа (SEC)
- збираюча венула (CV)
- мікросудини (MV)
Терміни, що використовуються для аналізу паттерна MS, включають наступне:
- крайовий епітелій крипти (MCE)
- отвір крипти (CO)
- проміжна частина між криптами (IP)
- блакитний гребінь (LBC)
- біла знебарвлена речовина (WOS).
Зображення 1: Мікроанатомія, візуалізована за допомогою збільшувальної ендоскопії з вузькосмуговою візуалізацією (NBI) в шлунку. (A) Збільшувальне ендоскопічне зображення з NBI нормальної слизової оболонки фундальної залози шлунка. (B) Відповідність між ендоскопічним зображенням за допомогою NBI і гістологічними даними нормальної слизової оболонки фундальної залози шлунка. (C) Збільшувальне ендоскопічне зображення з NBI нормальної слизової оболонки воротаря шлунка. (D) Відповідність між ендоскопічним зображенням, отриманим за допомогою NBI, і гістологічними даними нормальної слизової оболонки воротаря шлунка. NBI, вузькосмугова візуалізація; SEC, субепітеліальний капіляр; MCE, крайовий епітелій крипти; СО, отвір крипти; CV, збиральна венула; IP, проміжна частина.
Відповідно до системи класифікації VS, характерні ендоскопічні дані раннього раку шлунка включають наявність чіткої демаркаційної лінії між злоякісними і незлоякісними слизовими оболонками і наявність нерегулярного паттерна MV і / або нерегулярного паттерна MS всередині демаркаційної лінії. Демаркаційна лінія визначається як межа, розпізнавана по різкій зміні патерну MV або MS між областями ураження і областями без пошкоджень. Патерни MV і MS оцінюються окремо в залежності від того, чи є вони регулярними, нерегулярними або відсутніми, і ураження, які відповідають наступним діагностичним критеріям, діагностуються як злоякісні, тоді як ті, які не відповідають, діагностуються як незлоякісні.
Діагностичні критерії
- Наявність нерегулярного малюнка MV з демаркаційною лінією;
- Наявність нерегулярного малюнка MS з демаркаційною лінією.
Ураження, які відповідають критерію (I) або (II) (або обом), діагностуються як ракові ураження, тоді як інші діагностуються як незлоякісні ураження.
Повідомляється, що 97% ранніх стадій раку шлунка теоретично відповідають цим діагностичним критеріям.
Як було показано раніше, патерни MV і MS можна розділити на три категорії: регулярні / нерегулярні / відсутні (зобр. 2). При регулярному патерні MV капіляри під кожним епітелієм мають морфологію замкнутої (багатокутної) або відкритої петлі, показуючи регулярне розташування симетрично розподілених однорідних форм. Тим часом, нерегулярний патерн MV характеризується замкнутою петлею (багатокутною), відкритою петлею, звивистою, гіллястою або нерегулярною морфологією.
MV мають неоднорідну форму, і вони розподілені асиметрично, показуючи неправильне розташування. Випадки, в яких немає спостережуваних субепітеліальних MV, оцінюються як відсутність паттерна MV. У таких випадках шаблон MS (показує такі функції, як MCE, WOS і LBC) замість шаблону MV використовується як індикатор для збільшення ендоскопічної діагностики.
Зображення 2: Класифікація VS з використанням збільшувальної ендоскопії з NBI. Мікросудинний візерунок (V) класифікується як регулярний / нерегулярний / відсутній, як і мікроповерхневий візерунок (S) (жовті стрілки позначають демаркаційну лінію). VS, судина плюс поверхня; NBI, вузькосмугова візуалізація.
Хоча MCE часто використовується для оцінки паттерна MS, інші результати, такі як CO, IP, LBC і WOS, також можуть використовуватися, якщо вони присутні. У звичайному патерні MS морфологія кожного MCE вигнута або овальна, показуючи однорідні форми, симетричний розподіл і правильне розташування. У нерегулярному патерні MS морфологія кожного MCE вигнута або овальна або в рідкісних випадках ворсинчатая, демонструючи неоднорідні форми, асиметричний розподіл і неправильне розташування. Коли не спостерігається ніякого патерну MS, включаючи MCE, випадок оцінюється як відсутній патерн MS. У таких випадках обов’язково добре візуалізується патерн MV; тому ознаки патерну MV замість патерну MS використовуються в якості індикаторів для збільшення ендоскопічної діагностики.
У багатоцентровому проспективному дослідженні також було показано, що деякі ураження важко спостерігати при збільшувальній ендоскопії з використанням даної системи класифікації. Такі ураження являють собою знебарвлені плоскі недиференційовані ракові утворення. Беручи до уваги клінічні обмеження, ми запропонували клінічну стратегію, як показано на зображенні 3.
Зображення 3: Стратегія збільшувальної ендоскопії з NBI при скринінговій гастроскопії. C-WLI, звичайна ендоскопія з візуалізацією в білому світлі; M-NBI, збільшувальна ендоскопія з вузькосмуговою візуалізацією; NBI, вузькосмугова візуалізація.
Зокрема, ми припустили, що біопсія необхідна при знебарвлений плоских ураженнях слизової оболонки, тоді як збільшувальна ендоскопія шлунка може використовуватися в якості оптичної біопсії у випадках інших уражень, якщо є надійний прогноз. Простий алгоритм діагностики раку шлунка (MESDA-G) при збільшувальній ендоскопії, описаний нижче, також повинен застосовуватися відповідно до цієї клінічної стратегії. На зображенні 4 показаний знебарвлений плоский недиференційований рак шлунка, який важко діагностувати за допомогою збільшувальної ендоскопії з використанням системи класифікації VS.
Зображення 4: Складний випадок збільшувальної ендоскопічної діагностики з використанням системи класифікації VS. Демаркаційна лінія відсутня, нерегулярний малюнок МV, відсутній, неправильний малюнок МS, відсутній. (A) Звичайне ендоскопічне зображення. На великій кривизні антрального відділу шлунка (жовта стрілка) присутнє добре відмежоване злегка стиснуте бліде ураження. (B) Збільшення ендоскопічного зображення з NBI [максимальне збільшення жовтого квадрата області (A)]. Було встановлено, що немає різких змін капілярів під епітелієм слизової оболонки або MCE в обох фонових слизових оболонках ураження. Відповідно, демаркаційна лінія відсутня. Форми окремих мікросудин однорідні, демонструють симетричне і правильне розташування. Таким чином, патерн був розцінений як звичайний патерн MV. Що стосується патерна МS, крайовий епітелій крипти має овальну форму, однорідну форму, симетричний розподіл і правильне розташування. Таким чином, шаблон був визнаний звичайним шаблоном MS. Отже, ураження мало звичайний патерн MV плюс звичайний патерн МS без демаркаційної лінії, і відповідно до системи класифікації VS був поставлений діагноз незлоякісного ураження. Однак гістопатологічно ураження було діагностовано як карцинома з перстневих клітин. Ці знебарвлені ракові утворення недиференційованого типу є складними випадками для діагностики за допомогою збільшувальної ендоскопії, що вимагає біопсії для встановлення остаточного діагнозу. VS, судина плюс поверхня; MV, мікросудина; MS, мікроповерхня; NBI, вузькосмугова візуалізація; MCE, крайовий епітелій крипти.
MESDA-G з використанням системи класифікації VS
Хоча в Японії і інших країнах були запропоновані численні діагностичні системи, спрямовані на посилення ендоскопічної діагностики раннього раку шлунка, консенсусу за встановленим і стандартизованим набором діагностичних критеріїв або діагностичної системі досягнуто не було.
На цьому тлі Підкомітет з рекомендаціями Японської гастроентерологічної асоціації провів систематичний огляд і вибрав терміни і діагностичну систему, які будуть використовуватися для збільшення точності ендоскопічної діагностики шлунка в доказовій медицині. Отже, система класифікації VS була прийнята в якості діагностичної системи разом з анатомічними термінами, використовуваними для цієї системи.
На цій основі було запропоновано MESDA-G. Цей алгоритм був схвалений Японською гастроентерологічною асоціацією, Японським товариством гастроентерологічної ендоскопії, Японською асоціацією раку шлунка і Всесвітньою ендоскопічною організацією, і був досягнутий консенсус щодо його статусу як стандартизованого алгоритму.
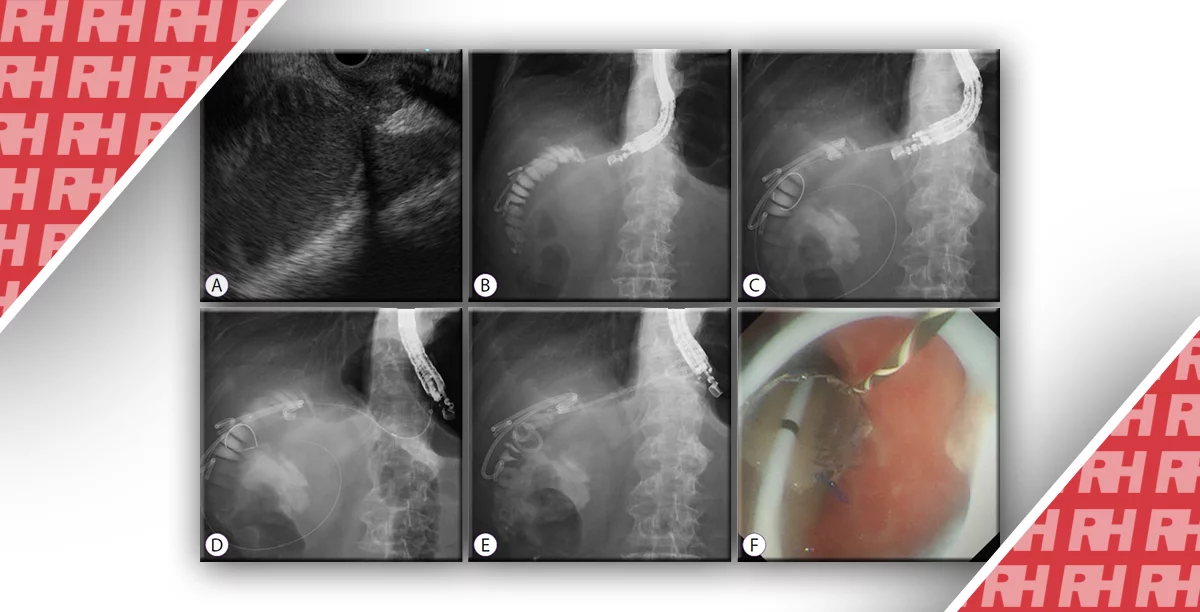
На зображенні 5 показано алгоритм. По-перше, ендоскопія зі збільшенням в білому світлі використовується для спостереження за внутрішньою частиною шлунка відповідно до протоколу систематичного скринінгу шлунка для виявлення будь-яких уражень, що вказують на ранній рак шлунка. Якщо виявлено таке підозріле ураження, слід провести збільшувальну ендоскопію, щоб відрізнити ракові і незлоякісні ураження. Більш конкретно, наявність / відсутність демаркаційної лінії слід визначати за допомогою збільшувальної ендоскопії (зобр. 5).
Якщо демаркаційна лінія не виявлена, ураження слід діагностувати як незлоякісне. Якщо є демаркаційна лінія, шаблони MV і MS всередині демаркаційної лінії повинні бути окремо досліджені на предмет того, чи є вони регулярними, нерегулярними або відсутніми. Якщо виявлено нерегулярний патерн MV і / або нерегулярний патерн MS, ураження діагностується як рак, тоді як, якщо ці патерни не ідентифіковано, ураження діагностується як незлоякісне. Це дійсно простий і зрозумілий алгоритм. На зображеннях 6-8 представлені фактичні ендоскопічні результати, що показують процедури, що виконуються для діагностики на основі MESDA-G.
Зображення 5: Простий алгоритм діагностики раку шлунка на ранніх стадіях (MESDA-G). VS, судина плюс поверхня; IMVP – неправильний мікроваскулярний патерн; IMSP, неправильний малюнок мікроповерхні.
Зображення 6: Приклад застосування MESDA-G (I). Демаркаційна лінія: відсутня. (A) Звичайне ендоскопічне зображення. На задній стінці антрального відділу шлунка є плоске червоне ураження слизової оболонки (жовта стрілка). (B) Збільшення ендоскопічного зображення з NBI. Субепітеліальні капіляри поступово розширюються від не червоних до червонуватих ділянок. Крім того, відбувається поступова зміна форми MCE. Більш конкретно, не існує ідентифікованої різкої зміни в прикордонній області між шаблонами MV і MS. Таким чином, демаркаційна лінія була визнана відсутньою. Діагноз доброякісного ураження поставлений згідно MESDA-G. MESDA-G, простий алгоритм діагностики раку шлунка за допомогою збільшувальної ендоскопії; NBI, вузькосмугова візуалізація; MCE, крайовий епітелій крипти; МВ, мікросудина; МС, мікроповерхня
Зображення 7: Приклад застосування MESDA-G (II). Демаркаційна лінія: присутня; нерегулярна картина МV: відсутня; нерегулярний патерн MS: відсутній. (A) Звичайне ендоскопічне зображення. На задній стінці тіла шлунка є регіональне злегка увігнуте червоне ураження (жовта стрілка). (B) Збільшення ендоскопічного зображення з NBI. Спостерігається різка зміна патернів MV і MS в місці, вказаному жовтими стрілками. А саме демаркаційна лінія присутня. В цьому випадку VS-класифікація патернів MV і MS всередині демаркаційної лінії була проведена відповідно до MESDA-G, щоб судити про наявність чи відсутність нерегулярного патерна MV і / або нерегулярного патерна MS. У патерні MV форми окремих мікросудин однорідні, показують симетричний розподіл і регулярне розташування. Отже, цей випадок був визнаний як маючий регулярний патерн MV. Що стосується патерна MS, то MCE має овальну морфологію, яка демонструвала б однорідні форми, симетричний розподіл і регулярне розташування. В отворах залоз є правильні світло-блакитні гребені, розташовані регулярно. Грунтуючись на цих висновках, було вирішено, що випадок мав звичайну картину розсіяного склерозу. Таким чином, відповідно до системи класифікації VS ураження було оцінене як маюче регулярний патерн МV плюс регулярний патерн MS, що призвело до діагнозу незлоякісного ураження. MESDA-G, простий алгоритм діагностики раку шлунка за допомогою збільшувальної ендоскопії; МV, мікросудина; MS, мікроповерхня; NBI, вузькосмугова візуалізація; VS, судина плюс поверхня; MCE, крайовий епітелій крипт.
Зображення 8: Приклад застосування MESDA-G (III). Демаркаційна лінія: присутня; нерегулярна картина MV: присутня; нерегулярний малюнок MS: присутній. (A) Звичайне ендоскопічне зображення. Є добре позначене стиснуте ураження, що супроводжується нерегулярним почервонінням малої кривизни антрального відділу шлунка (жовта стрілка). (B) Збільшувальне ендоскопічне зображення з NBI [жовтий квадрат в (A)]. У прикордонній зоні видно чітку демаркаційну лінію (жовті стрілки). Що стосується патерна MV всередині демаркаційної лінії, кожна мікросудина має неправильну морфологію петель. Мікросудини мають неоднорідну форму, асиметричний розподіл і неправильне розташування. Отже, патерн був розцінений як нерегулярний патерн MV. Що стосується петерну MS, є деякі області, позбавлені MCE, які, як вважається, мають відсутній петерн MS. В областях, де видно MCE, кожна має дугоподібну морфологію MCE, тобто форми MCE неоднорідні, з асиметричним розподілом і нерегулярним розташуванням. Було встановлено, що випадок мав відсутню / нерегулярну картину розсіяного склерозу. Грунтуючись на цих висновках, патерн був розцінений як нерегулярний патерн MV плюс відсутній / нерегулярний патерн MS відповідно до системи класифікації VS, і був поставлений діагноз раку. MESDA-G, простий алгоритм діагностики раку шлунка за допомогою збільшувальної ендоскопії; МV, мікросудина; MS, мікроповерхня; NBI, вузькосмугова візуалізація; MCE, крайовий епітелій крипти; VS, судина плюс поверхня.
Характерні дані слизової оболонки шлунка при ендоскопії зі збільшенням
WOS
WOS (біла знебарвлена речовина) являє собою білу речовину, яке приховує субепітеліальні MV, присутні в поверхневому шарі слизової оболонки, що чітко візуалізуються при збільшувальній ендоскопії з вузькосмуговою візуалізацією (NBI).
Про присутність WOS в слизовій оболонці шлунка вперше повідомили Yao et al. в 2008 р. Це відкриття часто спостерігається при кишковій метаплазії слизової оболонки при хронічному гастриті і епітеліальних пухлинах шлунка (аденома або рак) з кишковим фенотипом.
Природа WOS – це явище, яке визначається як біла речовина, що спостерігається за рахунок сильного розсіювання або відображення проектованого світла від ендоскопії на дрібні жирові краплі, накопичені в епітелії і під епітелієм. Коли присутня WOS, проекційне світло не може досягти субепітеліальних MV, що призводить до поганої видимості судин. Відмінності в морфологічних особливостях WOS служать корисними індикаторами при диференціальній діагностиці раку і аденоми.
Більш конкретно, ракові ураження мають нерегулярний WOS, тоді як аденоматозні ураження низького ступеня мають регулярний WOS. Крім того, повідомлялося, що WOS-позитивні епітеліальні пухлини шлунка мають слизовий характер певного кишкового фенотипу (кишкового типу або шлунково-кишкового фенотипу) і що WOS служить індикатором раку диференційованого типу, тому що WOS відсутня при недиференційованому раку. На зображеннях 9 і 10 показані фактичні результати ендоскопії.
Зображення 9: Аденома низького ступеня злоякісності зі звичайним WOS (без раку). (A) Звичайне ендоскопічне зображення (біле світло). На передній стінці нижньої частини тіла шлунка є знебарвлене плоске піднесення (жовта стрілка). (B) Збільшення ендоскопічного зображення з NBI [максимальне збільшення жовтого квадрата області (A)]. WOS всередині демаркаційної лінії дуже щільний і великий і локалізована в проміжній частині. WOS показує однорідні форми, симетричний розподіл і регулярне розташування, що дозволяє зробити висновок про регулярне петерні MS (звичайному WOS). Мікросудинні структури не видно через присутність WOS; отже, патерн був визнаний відсутнім патерном MV. Відповідно до системи класифікації VS результат був відсутнім патерном MV плюс регулярним патерном MS з демаркаційною лінією, і був поставлений діагноз незлоякісного ураження. Гістопатологічно ураження представляло собою канальцеву аденому низького ступеня злоякісності. WOS, біла знебарвлена речовина; NBI, вузькосмугова візуалізація; MS, мікроповерхня; МV, мікросудина; VS, судина плюс поверхня.
Зображення 10: Встановлено, що добре диференційована аденокарцинома (рак) має нерегулярний WOS. (A) Звичайне ендоскопічне зображення (біле світло). Знебарвлене підвищене ураження (жовта стрілка) присутнє в області малої кривизни в нижній частині тіла шлунка. (B) Збільшення ендоскопічного зображення за допомогою NBI [максимальне збільшення області жовтого квадрата, показане на (A)]. WOS всередині демаркаційної лінії показує неоднорідні форми, симетричний розподіл і нерегулярне розташування, що призводить до висновку про нерегулярний петерн MS (нерегулярну WOS). Мікросудинні структури не видно через присутність WOS, і патерн був визнаний відсутнім патерном MV. Відповідно до системи класифікації VS результатом був відсутній зразок MV плюс нерегулярний зразок MS з демаркаційною лінією, що призвело до діагнозу раку. Гістопатологічно ураження представляло собою дуже добре диференційовану тубулярну аденокарциному. WOS, біла знебарвлена речовина; NBI, вузькосмугова візуалізація; MS, мікроповерхня; МV, мікросудина; VS, судина плюс поверхня.
LBC
Було показано, що збільшувальна ендоскопія з NBI корисна для діагностики кишкової метаплазії. Порівняння збільшувальної ендоскопії з NBI і збільшувальної ендоскопією в білому світлі показало перевагу першої над другою для правильної діагностики кишкової метаплазії. Про ознаку LBC вперше повідомили Uedo et al. в 2006 р.
Згідно їх звіту, LBC (світло-блакитний гребінь) визначається як синьо-білі світлові лінії, які спостерігаються на краю MCE при збільшувальній ендоскопії з NBI (зобр. 11). Ознака LBC вважається явищем, яке виникає, коли щіткова облямівка абсорбуючої епітеліальної поверхні шістопатологічної CD10-позитивної кишкової метаплазії відображає вузькосмугове світло з центральною довжиною хвилі 415 нм.
Що стосується діагностичної здатності LBC для гістопатологічного кишкової метаплазії, заявлені чутливість і специфічність становлять 89% і 93% відповідно. Крім того, Канеміцу і ін. використовували комбінацію LBC і WOS для діагностики кишкової метаплазії і повідомили про чутливість і специфічність 87,5% і 93,8% відповідно. Більш того, метааналізи, включаючи дослідження, проведені за межами Японії, також підтвердили відмінну діагностичну спроможність LBC в діагностиці кишкової метаплазії. Патерн LBC також корисний для визначення межі пухлини; прикордонна лінія без LBC часто збігається з прикордонною лінією пухлини (зобр. 12).
Зображення 11: Слизова оболонка, позитивна на LBC. (A) Збільшувальне ендоскопічне зображення з NBI, що показує LBC на краю MCE. (B) Гістопатологічний зовнішній вигляд з фарбуванням гематоксиліном та еозином (H & E) (збільшення × 20), що показує келихоподібні клітини всередині епітелію крипти і щіткову облямівку, видиму на поверхні епітелію. (C) Гістопатологічний зовнішній вигляд з фарбуванням періодичною кислотою-Шиффом альціановим синім (збільшення × 20), що показує келихоподібні клітини і чітко видиму щіткову облямівку. (D) Імуногістохімічне забарвлення (CD10, збільшення × 20): щіткова облямівка (жовті стрілки) на поверхні абсорбуючого епітелію кишкової метаплазії стає CD10-позитивною. LBC, блакитний гребінь; NBI, вузькокополосна візуалізація; MCE, крайовий епітелій крипт.
Зображення 12: Аденома низького ступеня злоякісності (ракові), при якій LBC корисний для межі пухлини. (A) Звичайне ендоскопічне зображення (біле світло). Знебарвлене плоске підвищення (жовта стрілка) присутнє на малій кривизні тіла шлунка. (B) Збільшення ендоскопічного зображення за допомогою NBI [максимальне збільшення області жовтого квадрата, показане на (A)]. Навколо ураження є LBC-позитивна кишкова метаплазія, і лінія припинених LBC відповідає кордону пухлини (жовті стрілки). Пухлина була гістологічно тубулярною аденомою низького ступеня злоякісності. LBC, блакитний гребінь; NBI, вузькосмугова візуалізація.
Зовнішній вигляд білого глобуса (WGA)
WGA, якщо він присутній всередині демаркаційної лінії, являє собою високоспецифічний результат збільшувальної ендоскопії, який дозволяє проводити диференційну діагностику між злоякісними і незлоякісними ураженнями диференційованого типу.
WGA визначається як невелика (розміром ≤1 мм) біла глобулярна речовина безпосередньо під епітелієм, що виявляється при збільшувальній ендоскопії з NBI.
Вперше про WGA повідомили Doyama et al. в 2015 р. Він відповідає так званому внутрішньозалозистому некротичному залишку, який представляє собою помітно розширений проток пухлинної залози, що містить залишений еозинофільний некротичний матеріал, що спостерігається при ретельному гістологічному дослідженні.
WGA – високоспецифічний онкологічний маркер для збільшувальної ендоскопії. Іншими словами, наявність WGA дозволяє проводити диференційну діагностику між злоякісними і незлоякісними ураженнями диференційованого типу, такими як аденома низького ступеня злоякісності і гастрит, з високою специфічністю (зобр. 13).
Зображення 13: Кейс-презентація WGA. (A) Звичайне ендоскопічне зображення (біле світло). Почервоніле, регіональне, плоске ураження слизової оболонки присутнє на задній стінці малої кривизни у верхній частині тіла шлунка (жовта стрілка), а на крайових ділянках ураження видно білі плями. (B) Збільшення ендоскопічного зображення з NBI. Було підтверджено, що білі плями, які спостерігаються при звичайній ендоскопії (біле світло), являють собою WGA (білі стрілки). WGA зазвичай виявляється в слизовій оболонці, ураженій раком, дуже близько до демаркаційної лінії (жовті стрілки). WGA, зовнішній вигляд білого глобуса; NBI, вузькосмугова візуалізація.
Судини всередині епітеліального кола (VEC)
Повідомлялося, що патологічне дослідження показує більш високу біологічну злоякісність папілярної аденокарциноми, ніж тубулярної аденокарциноми. Однак за допомогою звичайної ендоскопії не вдалося діагностувати папілярну аденокарциному.
Канеміцу і ін. спостерігали ранній рак шлунка за допомогою збільшувальної ендоскопії та помітили конкретне відкриття, яке полягає в тому, що кровоносні судини були присутні під поверхневим епітелієм проміжної частини, оточеної кільцевим MCE. Вони назвали це «патерном судин всередині епітеліального кола (VEC)» і повідомили, що цей патерн характерний для раку диференційованого типу, що гістологічно демонструє сосочкову структуру (зобр. 14). Крім того, вони повідомили про співіснування недиференційованого раку і / або підслизової інвазії приблизно в одній чверті резектованих гістологічних зразків раннього раку шлунка з позитивним патерном VEC і припустили можливість того, що патерн VEC, спостережуваний при збільшувальній ендоскопії, може бути корисним маркером для прогнозування високого ступеня злоякісності до операції.
Зображення 14: Кейс-презентація патерна VEC. (A) Звичайні результати ендоскопії в білому світі раннього раку шлунка (тип 0-IIa). Поверхневе підвищення (жовта стрілка) присутнє на малій кривизні антрального відділу шлунка. (B) Збільшення ендоскопічного зображення з NBI. Усередині демаркаційної лінії (жовті стрілки) видно візерунок VEC. Нерівномірний мікроваскулярний візерунок спостерігається в круговій проміжній частині між криптами, що вистилана круглим крайовим епітелієм крипт. (C) Гістопатологічні дані. Забарвлення гематоксиліном і еозином (H & E) (збільшення × 40). Добре диференційована екзофітна карцинома з подовженими пальцеподібними відростками, покритими циліндричними або кубовидними клітинами, підтримуваними серцевиною з фіброваскулярною сполучною тканиною. NBI, вузькосмугова візуалізація; VEC, судини усередині епітеліального кола.
Таким чином, в цій статті описана діагностична система для збільшуючої ендоскопії з поліпшеним зображенням для діагностики раннього раку шлунка та інші характерні результати. Хоча подробиці тут не згадуються, слід підкреслити, що стандартний метод спостереження за слизовою шлунка при максимальному збільшенні необхідний для точної діагностики.
Поширені питання про діагностику раку шлунка на ранніх стадіях
Що таке система класифікації VS і як вона використовується в діагностиці раку шлунка?
- Система класифікації “судина плюс поверхня” (VS) – це діагностична система для розрізнення ракових і доброякісних уражень шлунка за допомогою ендоскопії зі збільшенням. Вона базується на оцінці патернів мікросудин (MV) і мікроповерхні (MS) слизової оболонки шлунка.
Які основні критерії використовуються в системі класифікації VS для діагностики раку шлунка?
- Основними критеріями є наявність чіткої демаркаційної лінії між злоякісними і незлоякісними ділянками, а також наявність нерегулярного патерну MV і/або MS всередині цієї лінії.
Що таке демаркаційна лінія і як вона визначається при ендоскопічному дослідженні?
- Демаркаційна лінія – це межа, яка візуалізується як різка зміна патерну MV або MS між ураженою і неураженою слизовою оболонкою шлунка.
Які особливості регулярного та нерегулярного патернів мікросудин (MV) і мікроповерхні (MS)?
- Регулярний патерн MV: Капіляри під епітелієм мають однорідну форму, симетричний розподіл і правильне розташування.
- Нерегулярний патерн MV: Мікросудини мають неоднорідну форму, асиметричний розподіл і неправильне розташування.
- Регулярний патерн MS: Крайовий епітелій крипти (MCE) має однорідні форми, симетричний розподіл і правильне розташування.
- Нерегулярний патерн MS: MCE має неоднорідні форми, асиметричний розподіл і неправильне розташування.
Що таке MESDA-G і як він використовується для діагностики раку шлунка?
- MESDA-G (Простий алгоритм діагностики раку шлунка) – це стандартизований алгоритм, розроблений для спрощення діагностики раку шлунка на ранніх стадіях за допомогою ендоскопії зі збільшенням. Він базується на системі класифікації VS і визначає наявність демаркаційної лінії та патернів MV і MS.
Які існують обмеження у використанні збільшувальної ендоскопії для діагностики раку шлунка?
- Знебарвлені плоскі недиференційовані ракові утворення можуть бути складними для діагностики за допомогою збільшувальної ендоскопії і вимагають проведення біопсії для встановлення остаточного діагнозу.
Які кроки передбачає алгоритм MESDA-G при діагностиці раку шлунка?
- Алгоритм MESDA-G передбачає наступні кроки: 1) Виявлення підозрілих уражень за допомогою ендоскопії в білому світлі. 2) Визначення наявності демаркаційної лінії за допомогою збільшувальної ендоскопії. 3) Оцінка патернів MV і MS всередині демаркаційної лінії на предмет регулярності або нерегулярності. 4) Постановка діагнозу на основі цих критеріїв.