Jonathan R. Dillman, Amer Heider, Jacob L. Bilhartz, Ethan A. Smith, Nahid Keshavarzi, Jonathan M. Rubin, M. James Lopez
Резюме
Только в небольшом количестве опубликованных исследований показана взаимосвязь между неинвазивным измерением скорости сдвига ультразвуковой волны (shear wave speed – SWS) и степенью фиброза печени по данным чрескожной биопсии у детей.
Цель исследования – оценить взаимосвязь между измерением скорости сдвига ультразвуковой волны в печени и фиброзом паренхимы у детей.
Материалы и методы.
Шестьдесят два ребенка (в возрасте от 0-18 лет) с известными или прогнозируемыми заболеваниями печени подверглись ультразвуковой сдвиговолновой эластографии (shear wave elastography – SWE) и клинически показанной чрескожной толстоигольной биопсии (все исследования выполнялись в один день). SWE выполнялась перед биопсией печени в зоне, которая отбиралась для проведения биопсии, с использованием системы Acuson S3000 с датчиком 9L4; при этом проводилось шесть измерений SWS с использованием режимов Virtual Touch Quantification (VTQ) and Virtual Touch IQ (VTIQ). Образцы биопсии изучали для гистологической оценки фиброза и воспаления. Двумерный анализ проводили с использованием корреляции Пирсона, в то время как множественная линейная регрессия была использована для выявления взаимосвязи между SWS и переменными предикторами. Кривые рабочей характеристики приемника (receiver operating characteristic – ROC) строили для оценки способности VTQ и VTIQ различать умеренный против выраженного фиброза печени (гистологический фиброз 0-2 баллов против 3-6 баллов).
Результаты.
Была выявлена значительная положительная корреляция между количеством баллов гистологического фиброза печени и средними значениями скорости сдвига волны при VTQ (n = 49) и VTIQ (n = 48) (r = 0,68 и r = 0,73; P-значения <0,0001). Также была выявлена значительная положительная корреляция между количеством баллов гистологического воспаления печени и средние значения скорости сдвига волны при VTQ и VTIQ (r = 0,47 и r = 0,44, а P = 0,0006 и р = 0,0016 соответственно). Для VTQ, количество баллов как для гистологического фиброза (Р <0,0001), так и для воспаления (Р = 0,04) были значимыми показателями-предикторами для скорости сдвига волны (скорректированная модель R2 = 0,49). Для VTIQ только количество баллов для гистологического фиброза (Р <0,0001) было значимым предиктором для скорости сдвига волны (скорректированная модель R2 = 0,56). ROC площади под кривой были 0,84 и 0,86 для VTQ и VTIQ, соответственно.
Выводы.
Показатели скорости сдвига ультразвуковой волны в печени увеличиваются с увеличением фиброза паренхимы у детей.
ВВЕДЕНИЕ
Существует много причин хронической патологии печени у детей. Со временем, регулярное повреждение гепатоцитов может привести к развитию фиброза паренхимы, или рубцеванию. Фиброз печени у детей – часто прогрессирующее заболевание, с увеличением степени фиброза (часто непредсказуемо) со временем, что иногда приводит к циррозу печени. Наиболее распространенные причины развития включают в себя билиарную атрезию (как без лечения, так и после портоэнтеростомии по Касаи), заболевания печени, связанные с полностью парентеральным питанием, кистозный фиброз, неалкогольная жировая болезнь печени (НЖБП), склерозирующий холангит, аутоиммунный гепатит, различные метаболические нарушения и криптогенный цирроз.
Несколькими методами визуализации, в том числе ультрасонография, МРТ и КТ, можно определить терминальную стадию фиброза печени или явный цирроза. Цирроз может быть заподозрен при анатомической визуализации на основе изменения морфологии печени (например, печень обычно выглядит сморщенной и имеет узловатую поверхность) или изменениях в интенсивности сигнала с использованием обычных методов МРТ. МР эластография недавно была изучена у детей и взрослых с хроническим заболеванием печени, в том числе у педиатрических больных с НАЖБП и после паллиативного лечения болезни Фонтана – врожденного заболевания сердца. При этом, документально подтверждено повышение жесткости печени при наличии фиброза. Однако, МР эластография имеет ограничения, в том числе: высокую стоимость (цена самого исследования и связанная с ним необходимая инфраструктура), ограниченная доступность, потребность в седации или общей анестезии у некоторых пациентов, и потеря МР сигнала в установке при избытке железа.
Не существует доступных в использовании устройств визуализации, которые могли бы обнаружить и точно количественно определить степень от легкого до умеренного фиброза печени, или оценить прогрессирование фиброза в течение долгого времени. Следовательно, биопсия печени, часто с использованием лапароскопической техники или чрескожного толстоигольного доступа под ультразвуковым контролем, обычно необходима для того, чтобы подтвердить наличие и измерить количественно фиброз печени у детей. Эта процедура имеет ограничения, такие как: отсутствие согласия на процедуру пациента и родителей, крайне ограниченные образцы печени, потребность в седации или общей анестезии, и различных процессуальные риски, в том числе опасный для жизни гемоперитонеум.
Недавно, количественные ультразвуковые методики, на основе сдвиговолновой эластографии (SWE), стали доступными в Соединенных Штатах, что позволило проводить неинвазивную оценку жесткости печени. Эти методы имеют многочисленные преимущества у детей, потому что они позволяют провести быструю оценку, не используют ионизирующее излучение, все больше и больше интегрируются в современные ультразвуковые системы, стоят меньше чем МР эластография, и не требуют седации или общей анестезии. Кроме того, ультразвуковая сдвиговолновая эластография представляет собой портативный метод, который позволяет получать изображения в отделе радиологии или клинике, а также у постели пациента. В настоящее время, проведено относительно небольшое число исследований по использованию ультразвуковой сдвиговолновой эластографии для обнаружения фиброз печени у детей. Акустическая лучевая импульсная визуализация (ARFI) – метод SWE, который использует ультразвуковой импульс для генерирования транзиторной деформации ткани, которая в естественных условиях приводит к сдвигу волны в органе мишени (например, печени). Скорость сдвига волны (shear wave speed – SWS) можно измерить (в м/с), используя тот же датчик, который обеспечивает оценку жесткости (твердости) ткани. SWS увеличивается с увеличением жесткости ткани и может быть напрямую связан с Модулем Юнга (кПа). КПа, свойство материала, которое описывает эластическую жесткость материала, и предоставляется некоторыми поставщиками, что приблизительно составляет 3 × (скорость сдвига волны в м/с)2.
Цель нашего исследования заключалась в перспективной оценке соотношения между показателями скорости сдвига ультразвуковой волны в печени и фиброзом паренхимы (на основе временной и анатомической связи с гистологической структурой) у детей для двух различных SWE методов. Кроме того, мы стремились смоделировать соотношение между SWS печени и различных предикторов, в том числе гистологический фиброз, гистологическое воспаление, возраст и пол.
МАТЕРИАЛЫ И МЕТОДЫ
Это исследование было одобрено институциональным контрольным органом и соответствует нормативам медицинского страхования.
Шестьдесят два ребенка (в возрасте 0-18 лет), которым была выполнена клинически показанная чрескожная пункционная толстоигольная биопсия печени для известного или вероятного (неопухолевого) заболевания печени, были включены в это проспективное исследование. Дети были включены между ноябрем 2012 и июлем 2014 года. Мы получили родительское/опекунское информированное согласие всех участников исследования; мы получили согласие самого субъекта для детей старше 10 лет. Некоторые данные 11 детей в этом исследовании были ранее представлены в предыдущем исследовании, в котором используется сдвиговолновая эластография, для дифференциальной диагностики билиарной атрезии от других причин неонатальной/младенческой желтухи.
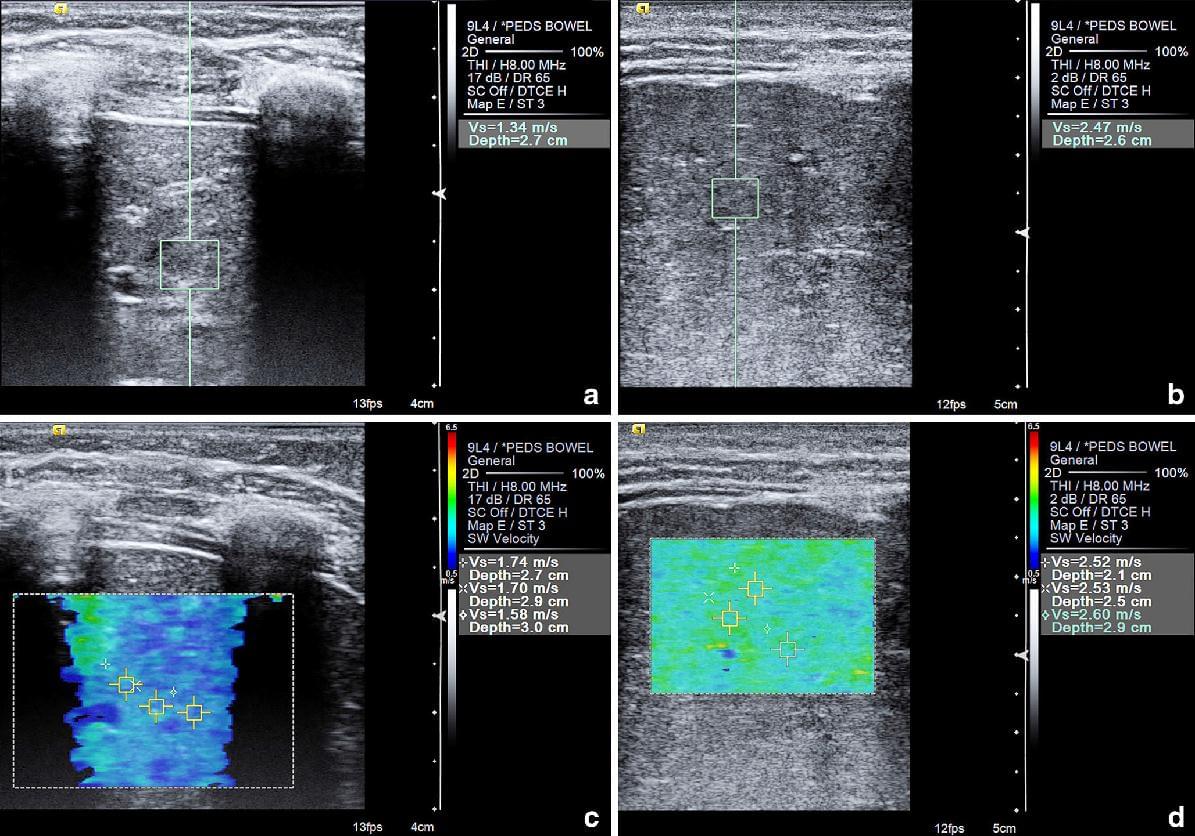
После инициации седации или индукции общей анестезии, ультразвуковая сдвиговолновая эластография выполнялась либо в палате интервенционной радиологии или прямо в операционной перед проведением чрескожной толстоигольной биопсии печени под ультразвуковым наведением. SWE проводили в зоне печени, которая определена для биопсии. Все ультразвуковые исследования проводились небольшой группой исследователей, которые специализировались на педиатрической ультразвуковой технике сдвиговолновой эластография под наблюдением руководителя исследования. Все исследования были проведены с использованием системы Acuson S3000 и датчика 9L4 (Siemens Medical Solutions USA, Malvern, PA). SWE выполнялась в положении ребенка лежа на спине при спонтанном дыхания, если ребенок был достаточно взрослый и в состоянии выполнить команду задержать дыхание. Мы использовали два метода: Virtual Touch Quantification (VTQ) and Virtual Touch IQ (VTIQ) (рис. 1).
Рис. 1. Сдвиговолновая эластография. Virtual Touch Quantification (VTQ) изображение у (а) 5-летнего мальчика и (b) 17-летней девочки. Режим изображения Virtual Touch IQ (VTIQ) сдвиговолновой эластографии (c) та же самая девочка и (d) тот же мальчик, как (а, b). Высокий показатель скорости сдвиговых волн (и неоднородность эластограммы на изображении VTIQ) коррелируют с увеличением фиброза паренхимы.
VTQ и VTIQ являются специфическими терминами от производителя для двух методов сдвиговолновой эластографии, также известные как акустическая лучевая импульсная визуализация (ARFI). Точный доступ для правильной визуализации (например, правая или левая доля, межреберье или подреберье) для данного ребенка, был определен гастроэнтерологом или интервенционным радиологом, который выполнял процедуру биопсии печени. Так как все процедуры биопсии проводились под седацией или общей анестезией, пациенты ничего не принимали перорально в течение SWE исследования в соответствии с принципами отделения анестезии.
Для VTQ сдвиговолновой эластографии используется устанавливаемый оператором режим 4.0 МГц ARFI или “толчковый импульс” для удаленного получения сдвиговых волн в пределах поля зрения, в то время как режим VTIQ использует несколько ARFI импульсов (4.0-5.7 МГц, которые возникают из различных точек вдоль поверхности датчика и сосредоточены на разных глубинах) для воспроизведения сдвиговых волн и создания цветного изображения (эластограммы) жесткости тканей. VTQ использует датчик 9L4, что позволяет разместить единое, фиксированного размера 5-мм2 поле зрения (region of interest – ROI) в полученном изображении для измерения скорости сдвига волны (м/с), в то время как VTIQ позволяет разместить несколько ROI фиксированного размера – 1,5 мм2 в полученном изображении для измерения скорости сдвига волны. Сдвиговолновая эластография выполнялась с использованием ультразвуковой системы с настройками по умолчанию; шкала VTIQ цветной эластограммы варьировала в диапазоне от 0,5 м/с (синий) до 6,5 м/с (красный).
При использовании режима VTQ, поле зрения было размещено в печени в зоне, которая была определена для биопсии, избегая видимых кровеносных сосудов и, по крайней мере, на 10 мм ниже поверхности печени. Шесть VTQ измерений скорости сдвига волны были получены у каждого ребенка, с повторным расположением датчика для каждой попытки. При использовании режима VTIQ, два изображения эластограммы печени были получены в зоне, которая была определена для биопсии. Шесть VTIQ измерений скорости сдвига волны также были получены у каждого ребенка (три измерения на эластограмме, с полем зрения, размещенным по усмотрению ультразвукового техника в зонах “полного заполнения цветом”). Все изображения SWE были получены с наименьшим давлением датчика, что необходимо для проведения диагностической визуализации.
Возраст, пол и индекс массы тела (ИМТ) были задокументированы для каждого ребенка. Мы изучили все электронные медицинские записи для того, чтобы получить клинические показания для проведения биопсии печени и получения гистологического диагноза.
ГИСТОЛОГИЧЕСКИЙ АНАЛИЗ ПЕЧЕНИ
Все дети в нашем исследовании подверглись клинически обоснованной процедуре толстоигольной биопсии печени под ультразвуковым контролем с использованием либо 16-го, либо 18-го калибра устройства для биопсии (одноразовая пункционная игла для биопсии Bard Monopty; Bard Biopsy Systems, Tempe, AZ).
Как минимум два образца тканей были получены от каждого ребенка. После обычной обработки ткани, образцы были помещены на предметные стекла и окрашены гематоксилином и эозином, а также и Массон трихромом. Образцы ткани были подвергнуты изучению для балльной оценки гистологического фиброза (система определения стадии фиброза Ishak, 0-6, где 0 указывает на отсутствие фиброза, а 6 показывает наличие цирроза) и воспаления (модифицированный индекс активности гепатита, 0-18, где 0 означает – нет воспаления, а 18 указывает на тяжелое воспаление и некроз); скоринг был проведен сертифицированным педиатрическим патологоанатомом (3,5 лет опыта), который не знал результатов ультразвуковой сдвиговолновой эластографии. Эти гистологические скоринговые системы были задействованы потому, что они используются и утверждены в многочисленных исследованиях у взрослых; при этом не существует похожих специальных педиатрических разработок для скоринга гистологического воспаления и фиброза.
СТАТИСТИЧЕСКИЙ АНАЛИЗ
Непрерывные данные были обобщены с помощью средних величин и стандартного отклонения, в то время как категориальные данные были обобщены с помощью графиков и процентов. Двухвариантные соотношения, в том числе VTQ и скорость сдвига волны VTIQ (индивидуальное для субъекта среднее, медиана и максимум) против количества баллов гистологического фиброза и воспаления были оценены с использованием корреляции Пирсона. Анализ дисперсии (ANOVA) был использован для сравнения VTQ и VTIQ средних значений скорости сдвига волны у детей с отсутствием или легким, против умеренного и против выраженного фиброза (гистологический фиброз 0-1 баллов, против 2-3 баллов, против 4-6 баллов). Эти средние также были сопоставлены попарным способом, используя многократное сравнение – тест Тьюки с соответствующей корректировкой значения Р.
Мы использовали множественный линейный регрессионный анализ для оценки соотношения между SWS и предикторами (количество баллов для гистологического фиброза и воспаления, а также возраст и пол) как для VTQ, так и VTIQ. Критерий информации Akaike был использован для окончательного выбора модели. Кривые рабочей характеристики приемника (ROC) были построены для оценки диагностической значимости VTQ и VTIQ для дифференциальной диагностики легкого (количество баллов гистологического фиброза 0-2) против выраженного (гистологический фиброз – 3-6 баллов) фиброза. Все статистические тесты проводились с помощью SAS версии 9.3 (SAS Institute, Cary, NC). Р-значение <0,05 считали значимым.
РЕЗУЛЬТАТЫ
Характеристики объектов исследования
Шестьдесят два ребенка были включены в наше исследование, 29 (47%) девочек и 33 (53%) мальчика. Средний возраст пациентов составил 8,0 ± 5,8 лет (диапазон, 4 недели-18 лет). Клинические показания для биопсии печени, а также гистологические диагнозы представлены в таблице 1.
Таблица 1. Клинические показания для биопсии печени и окончательные диагнозы у 62 детей.
|
Показания для биопсии |
n |
Окончательные диагнозы |
n |
|
Первичная ортотопическая трансплантация печени (OLT) |
24 |
OLT отторжение |
11 |
|
Повышенные печеночные пробы (родная печень) |
21 |
Неспецифическая аномалия развития печени |
10 |
|
Холестаз |
11 |
Нормальная печень |
9 |
|
Повышенные печеночные пробы (после процедуры Kasai) |
1 |
Билиарная атрезия / билиарная обструкция |
5 |
|
Известный аутоиммунный гепатит |
1 |
Аутоиммунный гепатит |
5 |
|
Известный криптогенный цирроз |
1 |
Склерозирующий холангит |
5 |
|
Известная болезнь накопления гликогена |
1 |
Лекарственный гепатит |
2 |
|
Известный дефицит пируваткиназы |
1 |
Болезнь накопления гликогена |
2 |
|
Известный склерозирующий холангит |
1 |
Неонатальный гепатит |
2 |
|
Неалкогольный стеатогепатит |
2 |
||
|
Недостаточность желчных протоков |
2 |
||
|
Криптогенный цирроз |
1 |
||
|
Врожденный фиброз печени |
1 |
||
|
Лейкемия |
1 |
||
|
Вирусный гепатит |
1 |
VTQ было успешным (это значит, что измерения скорости сдвига волны могут быть проведены) у 49 детей, в том числе 24 (49%) девочки и 25 (51%) мальчиков, при использовании датчика 9L4. Средний возраст был 7,2 ± 5,5 лет. Дети (5 девочек и 8 мальчиков) с недостоверными изображениями VTQ имели средний возраст -11,1 лет. Средний индекс массы тела (ИМТ) для детей с успешными изображениями VTQ составил 18,4 ± 4,7 кг/м2, против 30.4 ± 6.4 кг/м2 для детей с неудачными изображениями (Р <0,0001).
VTIQ было успешным (это означает, что более чем две трети эластограммы заполнены цветными данными на основе субъективной оценки) у 48 детей, в том числе 21 (44%) девочка и 27 (56%) мальчиков. Средний возраст детей был 6.7 ± 5.5 лет. Дети (8 девочек и 6 мальчиков) с недостоверными изображениями VTIQ имели средний возраст 12,4 лет. Средний ИМТ для детей с успешной визуализацией при VTIQ был 17,6 ± 4,1 кг/м2, против 27,8 ± 7,1 кг/м2 для детей с неудачным исследованием (Р = 0,0001).
Двумерный анализ
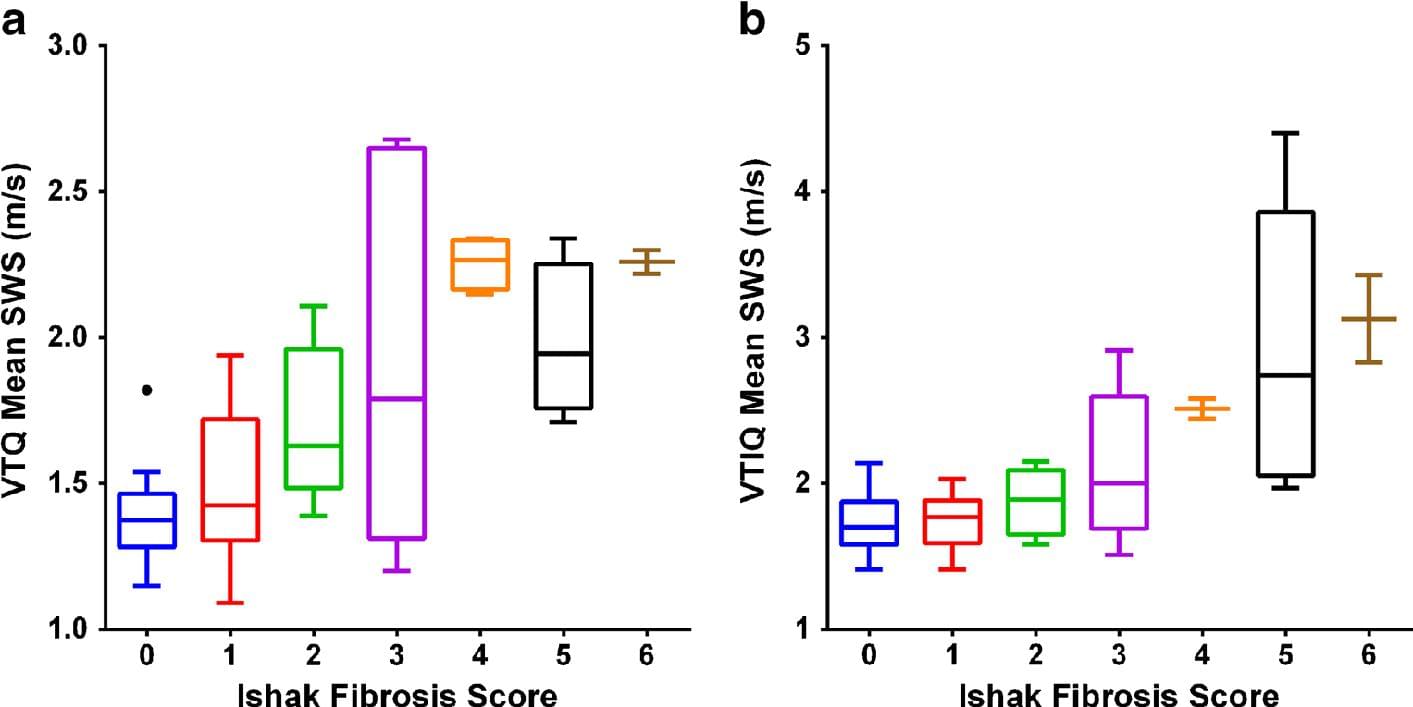
Выявлена значительная положительная корреляции между отдельными средними значениями для субъектов, медианой и максимумом VTQ измерений сдвиговолновой скорости и количеством баллов для гистологического фиброза и воспаления паренхимы (Таблица 2) (Рис. 2). Точно так же, существует значительная положительная корреляция между отдельными средними значениями для субъектов, медианой и максимумом VTIQ измерений сдвиговолновой скорости и количеством баллов для гистологического фиброза и воспаления паренхимы (Таблица 2), (Рис. 2).
Таблица 2. Корреляция Пирсона (R) между показателями скорости сдвига волны отдельных субъектов (в м/с, n = 6) и прогнозирующими переменными (предикторами), в том числе количеством баллов гистологического фиброза (0-6), гистологического воспаления (0-18) и возрастом.
|
r (P-значение) (n) |
VTQ – среднее SWS |
VTQ – медиана SWS |
VTQ – максимум SWS |
VTIQ – среднее SWS |
VTIQ – медиана SWS |
VTIQ – максимум SWS |
|
Баллы фиброза |
0.68 |
0.63 |
0.65 |
0.73 |
0.72 |
0.68 |
|
(<0.0001) |
(<0.0001) |
(<0.0001) |
(<0.0001) |
(<0.0001) |
(<0.0001) |
|
|
(49) |
(49) |
(49) |
(48) |
(48) |
(48) |
|
|
Баллы воспаления |
0.47 |
0.45 |
0.52 |
0.44 |
0.44 |
0.48 |
|
(0.0006) |
(0.001) |
(0.0001) |
(0.0016) |
(0.002) |
(0.0006) |
|
|
(49) |
(49) |
(49) |
(48) |
(48) |
(48) |
|
|
Возраст |
0.02 |
−0.02 |
0.07 |
−0.28 |
−0.27 |
−0.26 |
|
(0.87) |
(0.86) |
(0.63) |
(0.057) |
(0.06) |
(0.08) |
|
|
(49) |
(49) |
(49) |
(48) |
(48) |
(48) |
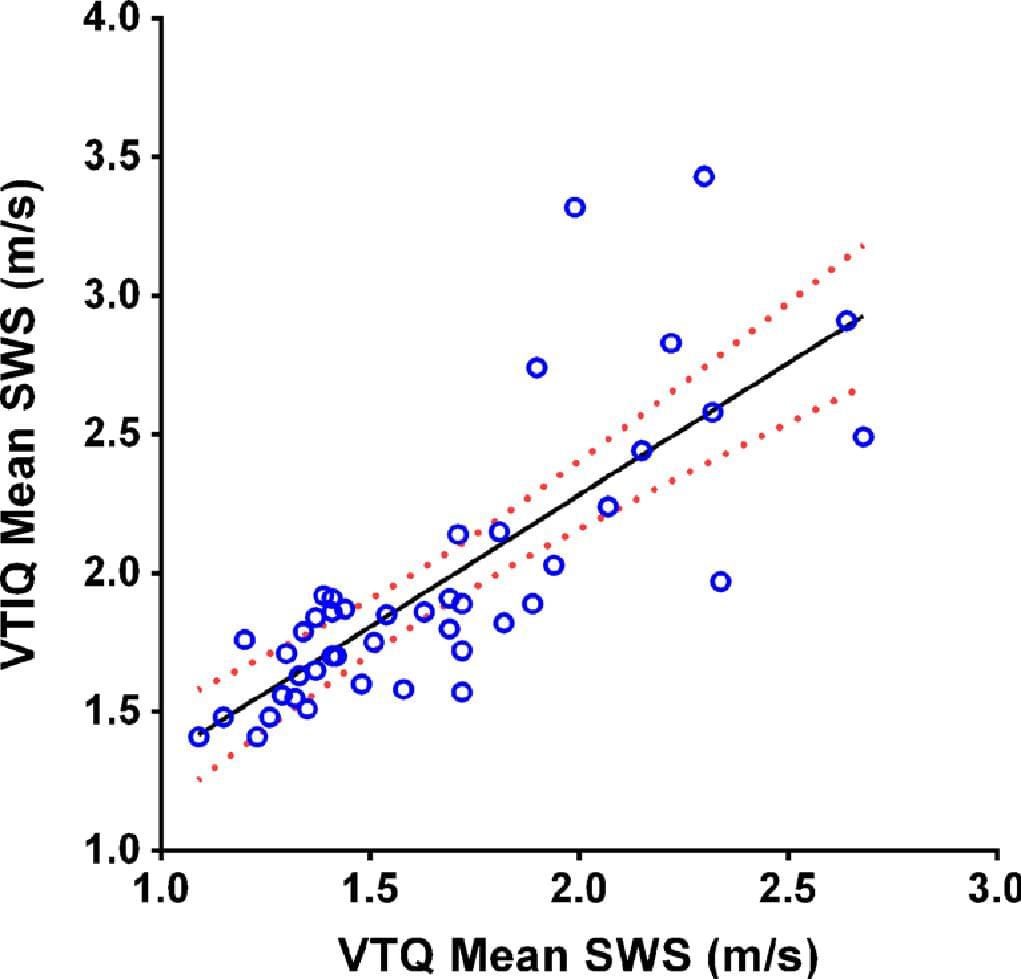
Средние показатели VTQ и VTIQ скорости сдвига волны имели также сильную положительную корреляцию, как и ожидалось (r = 0.79; Р <0,0001) (Рис. 3).
Рис. 2. Сравнение скорости сдвига волны (SWS) и фиброза. Бокс-графики показывают увеличение показателей SWS печени одновременно с увеличением фиброза паренхимы при (а) VTQ и (b) VTIQ режимах сдвиговолновой эластографии. VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification
Рис. 3. Корреляция между показателями скорости сдвига волны при Virtual Touch Quantification (VTQ) и Virtual Touch IQ (VTIQ). Диаграмма разброса (с усредненной кривой и 95% доверительным интервалом) показывает взаимосвязь между средними значениями скорости сдвига волны (SWS) при VTQ и VTIQ у 44 детей (r = 0,79; p <0,0001).
Не было выявлено значимой корреляции между измерениями SWS (среднее, медиана и максимум) и возрастом при VTQ. Выявлена незначительная негативная корреляция между измерениями SWS (среднее, медиана и максимум) и возрастом при VTIQ (P-значения = 0.057-0.08).
Дисперсионный анализ (ANOVA)
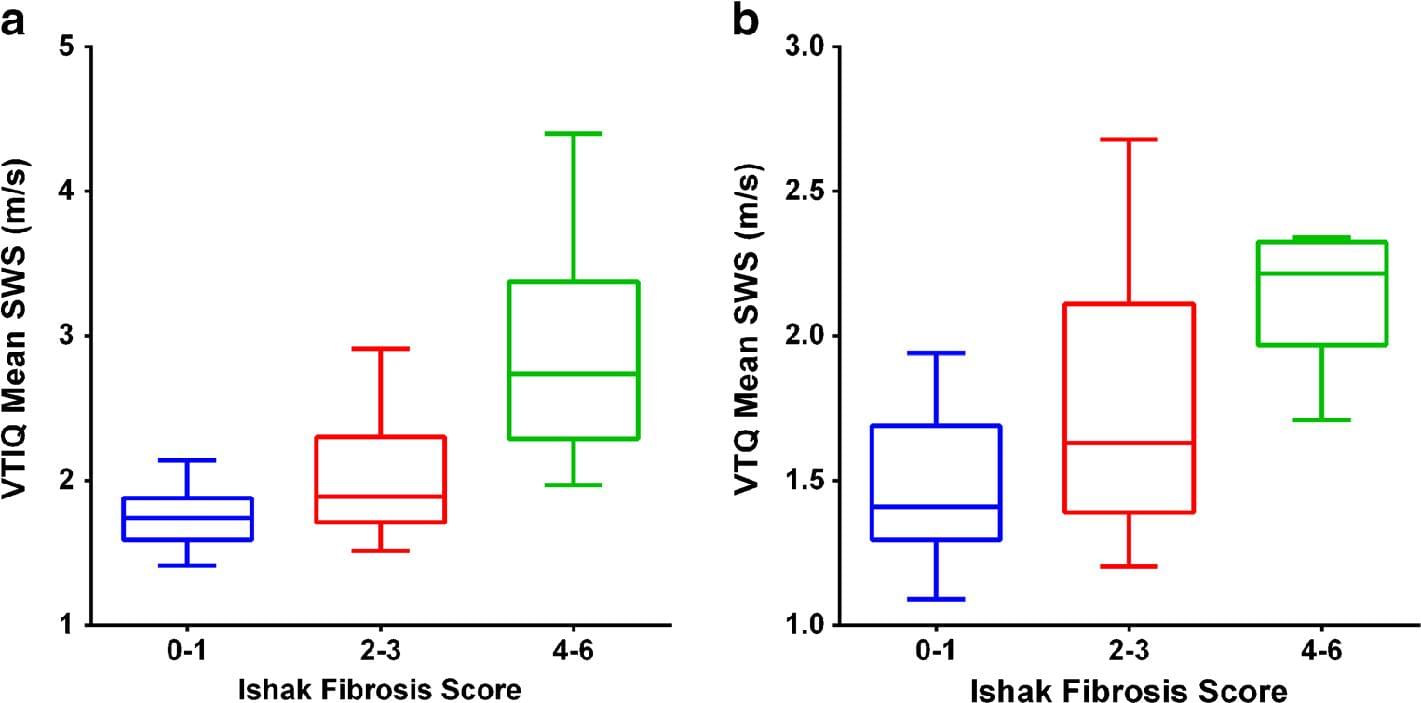
Выявлена значительная разница средних значений SWS среди детей с Ishak 0-1 (n = 28, 1,46 ± 0,23 м/с), 2-3 (n = 11, 1,82 ± 0,50 м/с) и 4-6 (n = 10, 2,15 ± 0,21 м/с) количеством баллов гистологического фиброза при VTQ (P <0,0001) (Рис. 4). Аналогично, существовала значительная разница средних значений SWS среди детей с Ishak 0-1 (n = 29, 1,74 ± 0,18 м/с), 2-3 (n = 10, 2,02 ± 0,44 м/с) и 4-6 (n = 9, 2,87 ± 0,75 м/с) и количеством баллов гистологического фиброза при VTIQ (P <0,0001) (рис. 4).
Рис. 4. Сравнение показателей скорости сдвига волны и количества баллов гистологического фиброза. Бокс-графики показывают среднее значение скорости сдвига волны (SWS) у детей с разной выраженностью фиброза печени, с использованием (а) VTIQ и (b) VTQ режимов. Оба режима изображения демонстрируют увеличение SWS с увеличением баллов гистологического фиброза (Р <0,0001 для обоих режимов VTQ и VTIQ). VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification.
Парное сравнительное тестирование среднего значения скорости сдвига волны среди групп с разным количеством баллов гистологического фиброза с Туки-коррекцией P-значений представлены в таблице 3.
Таблица 3. Парные сравнение значений средней скорости сдвига волны в печени у детей с легким, умеренным и выраженным гистологическим фиброзом.
|
Группы сравнения пациентов с гистологическим фиброзом |
Средние значения разницы SWS (мс) |
Значимость? |
Скорректированное значение Р* |
|
VTQ |
|||
|
0–1 vs. 2–3 |
0.36 |
Да |
0.006 |
|
0–1 vs. 4–6 |
0.69 |
Да |
<0.0001 |
|
2–3 vs. 4–6 |
0.33 |
Да |
0.045 |
|
VTIQ |
|||
|
0–1 vs. 2–3 |
0.27 |
Нет |
0.15 |
|
0–1 vs. 4–6 |
1.13 |
Да |
<0.0001 |
|
2–3 vs. 4–6 |
0.86 |
Да |
<0.0001 |
SWS – скорость сдвига волны, VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification
* P-значения, скорректированные с использованием метода Тьюки
Прогнозирование скорости сдвига волны в печени
Мы использовали множественную линейную регрессию для оценки соотношения между значением SWS печени (средним) и предикторами (количеством баллов гистологического фиброза печени и воспаления, а также возрастом и полом) как для VTQ, так и VTIQ.
VTQ
Для VTQ, количество баллов гистологического фиброза печени и воспаления были значимыми предикторами среднего значения скорости сдвига волны (P <0,0001 и P = 0,04 соответственно). Возраст и пол были не значимыми прогностическими факторами, и они привели к нежелательному увеличению информационного критерия Akaike.
Окончательная модель была следующей: SWS (м/с) = 1,32 + (0,13 × баллы гистологического фиброза) + (0,025 × баллы гистологического воспаления) (Р <0,0001; скорректированное R2 = 0,49).
VTIQ
Для VTIQ, баллы гистологического фиброза были единственным значимым предиктором средней скорости сдвига волны (Р <0,0001). Баллы гистологического воспаления (Р = 0,09) и возраст (Р = 0,10) были незначимыми прогностическими факторами и были включены в окончательную модель, потому что они привели к уменьшению информационного критерия Akaike. Пол не был значимым предиктором, что способствовало нежелательному увеличению информационного критерия Akaike. Окончательная модель была следующей: SWS (м/с) = 1,65 + (0,20 × баллы гистологического фиброза) + (0,028 × баллы гистологического воспаления) + (- 0,018 × возраст) (Р <0,0001; скорректированное R2 = 0,56).
Анализ кривой рабочей характеристики приемника (ROC)
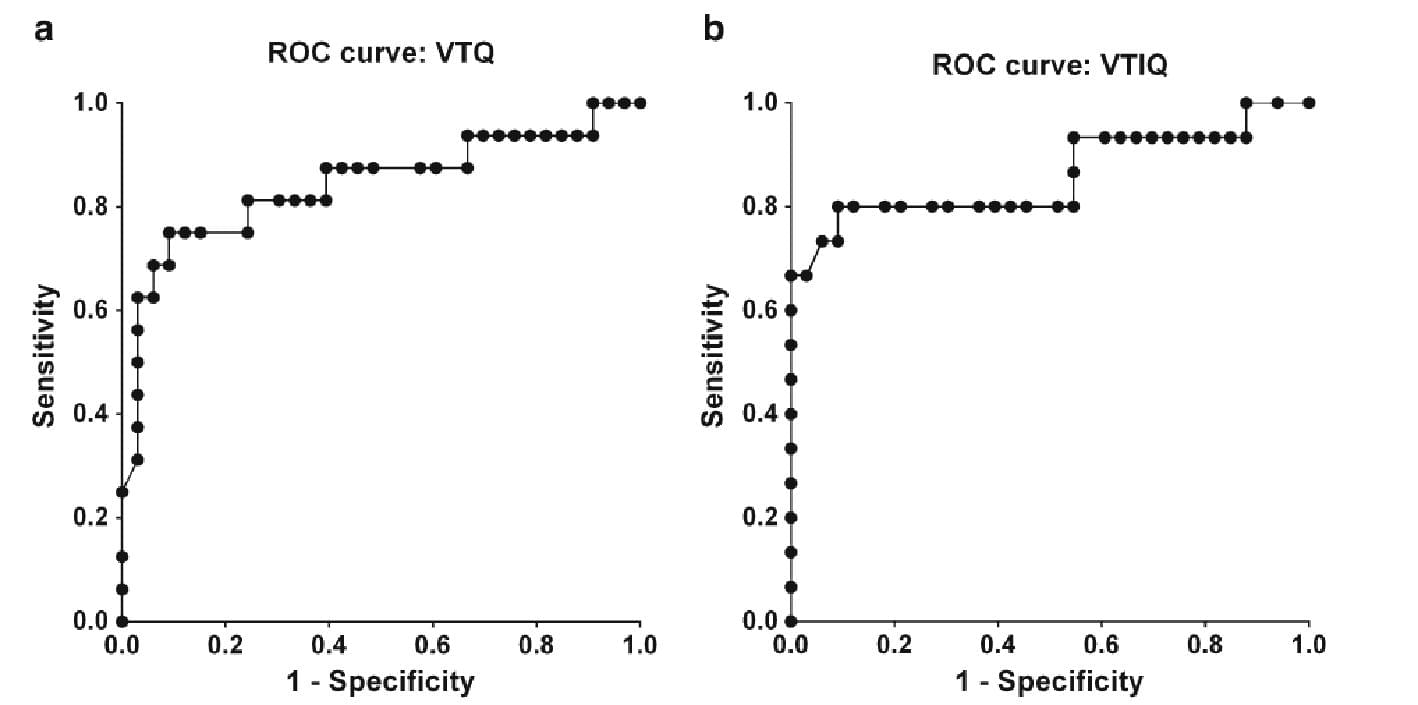
Анализ кривой рабочая характеристики приемника (ROC) провели с целью оценки возможностей использования показателей скорости сдвига волны для дифференциальной диагностики детей с незначительным гистологическим фиброзом печени и выраженного фиброза в баллах. Для VTQ, площадь под кривой была 0,84 (95% ДИ: 0.70-0.98; Р = 0,0001) (Рис. 5). Пороговое значение скорости сдвига волны 2,07 м/с способствовало отличному положительному значению вероятности (20,6) для обнаружения выраженного гистологического фиброза (в соответствии с баллами), с чувствительностью 63% и специфичностью 97%. Для VTIQ, площадь под кривой была 0,86 (95% ДИ: 0.72-1.0; Р <0,0001) (Рис. 5).
Рис. 5. Кривые рабочей характеристики приемника (ROC) для дифференциальной диагностики легкого (гистологический фиброз 0-2 балла) и выраженного (гистологический фиброз 3-6 баллов) фиброза печени с помощью показателя средней скорости сдвига волны. А. Площадь под кривой для VTQ составляет 0,84 (95% ДИ: 0.70-0.98). В. Площадь под кривой VTIQ составляет 0,86 (95% ДИ: 0.72-1.0). VTIQ – Virtual Touch IQ, VTQ – Virtual Touch Quantification.
Пороговое значение SWS 2,15 м/с способствовало получению отличного положительного значения вероятности (22,0) для обнаружения выраженного гистологического фиброза (в соответствии с баллами), с чувствительностью 67% и специфичность 97%.
ОБСУЖДЕНИЕ
Диагностические значения SWS могут быть получены у 49 из 62 (79%) детей с помощью VTQ и у 48 из 62 (77%) детей, при VTIQ. При анализе неудачных случаев (то есть детей, у которых не могли быть получены измерения скорости сдвига волны для VTQ – дисплей выводит сообщение об ошибке в этом случае, или в случае, когда меньше чем две трети эластограммы заполнены, цветными данными для VTIQ) было показано, что эти дети, как правило, были старше и имели большее телосложение, по сравнению с детьми с удачной диагностической визуализацией SWE. Интересно, что некоторые дети с неудачной визуализацией VTQ имели успешные VTIQ изображения, и наоборот, это явление – для которого мы не имеем определенного объяснения. Увеличение жировой ткани брюшной стенки может ослаблять звуковые волны и как результат уменьшать силу акустического импульса. Ухудшение сигнала приводит к неспособности диагностической оценки скорости сдвига волны. Небольшой процент недиагностических случаев, вероятно, был результатом выраженных дыхательных движений, которые, вероятно, препятствуют возможности регистрации сдвига волны. В случае неудачной ультразвуковой SWE печени, альтернативой является MR эластография, особенно у крупных педиатрических больных, таких, как дети с НАЖБП. Для исследования детей мы намеренно выбрали только 9L4 линейный датчик, чтобы минимизировать погрешность измерения, потому что изображения с более чем одним датчиком являются потенциальным источником вариабельности при попытках корреляции измерений SWS с гистологическими результатами, учитывая тот факт, что измерения скорости сдвига волны в какой-то степени зависят от датчика. Тем не менее, следует отметить, что VTQ SWE также может быть выполнено с помощью конвексного датчика 4C1, который имеет режим толчкового импульса низкого частоты и оптимизирован для визуализации печени у больших детей и взрослых. В настоящее время, только линейный датчик 9L4 совместим с SWE в режиме VTIQ.
Двумерный анализ показал значительную положительную корреляцию между измерениями SWS, как гистологического фиброза, так и воспаления для VTQ и VTIQ. Хотя соотношения между SWS и балльной оценкой гистологического фиброза были достаточно сильны для обоих режимов SWE, соотношения между SWS и балльной оценкой гистологического воспаления не были существенными. Наши многомерные регрессионные модели предполагают, что гистологическое воспаление влияет на SWS печени, когда учитывается количественная степень фиброза печени. Интересно, что, очень похожие сильные корреляции были обнаружены между средним значением отдельных субъектов, медианой и максимумом значений SWS и количеством балов гистологического фиброза и воспаления для обоих режимов VTQ и VTIQ.
Тестирование ANOVA также показало, что SWS печени увеличивается с увеличением фиброза печени. Тем не менее, бокс-график, построенный с использованием трех степеней фиброза печени (гистологический фиброз 0-1 баллов, 2-3 баллов и 4-6 баллов) показал некоторое перекрытие значений SWS для каждой гистологической категории. Таким образом, маловероятно, что SWE (или, по крайней мере, VTQ и VTIQ в их нынешнем виде) могут дифференцировать определенную степень гистологического фиброза с высокой долей достоверности (например, шкала фиброза Ishak: 1 против. 2, 2 против 3, или 3 против 4).
Анализы ROC кривой показывают, что определенные пороговые значения SWS могут давать разумную чувствительность и очень высокую специфичность для дифференциальной диагностики отсутствие/легкий фиброз от умеренный/тяжелый (выраженный) фиброз. ROC площади под кривой были схожи для VTQ и VTIQ (0,84 и 0,86, соответственно). Следует отметить, что пороговые значения SWS для дифференциальной диагностики гистологических степеней фиброза могут зависеть от конкретного производителя, что показано в какой-то степени на основе последних экспериментов получения данных на фантоме Альянсом количественной визуализации биомаркеров (Quantitative Imaging Biomarker Alliance). Это совместное групповое исследование показало, что «существует статистически значимая разница в значениях SWS среди [различных ультразвуковых] систем ». В конечном счете, SWE, вероятно, будет наиболее полезным маркером для определения наличия или отсутствия существенного фиброза печени и для мониторинга прогрессирования фиброза в течение долгого времени (в отличие от точного количественного определения фиброза).
Множественный линейный регрессионный анализ был использован для оценки соотношения между SWS печени и различных предикторов, в том числе количества баллов гистологического фиброза, гистологического воспаления, возраста и пола. Для VTQ, как гистологический фиброз, так и воспаление были значимыми предикторами; влияние гистологического воспаления является важным наблюдением и предполагает, что и другие факторы, кроме фиброза, могут воздействовать на изменения показателей скорости сдвига волны в печени. Если провести коррекцию по отношению к количеству баллов гистологического воспаления, то увеличение балла гистологического фиброза на 1 единицу (например, изменения по шкале фиброза Ishak от 3 до 4 баллов) вызывает увеличение средней SWS на 0,13-м/с. Для VTIQ, балльная оценка гистологического фиброза стала единственным значимым предиктором, хотя балльная оценка гистологического воспаления и возраст в целом улучшили качество модели. Если провести коррекцию по отношению к количеству баллов гистологического воспаления и возрасту, то увеличение балла гистологического фиброза на 1 единицу вызывает увеличение среднего значения SWS на 0,20м/с.
Для VTIQ, окончательная модель множественной линейной регрессии имело скорректированное R2-значение 0,56. Это означает, что примерно 56% значений средней SWS, зарегистрированных у детей в нашем исследовании, можно объяснить нашей моделью и ее предикторами; однако, 44% значений остаются необъяснимыми. Эта необъяснимая вариабельность, вероятно, является результатом нескольких факторов, в том числе вариабельность измерения, связанная с используемой техникой SWE, (например, вариабельность, присущая VTIQ), вариабельность выборки ткани и гистологического скоринга и индивидуальная биологическая вариабельность объекта. Кроме того, мы предположили линейную зависимость между SWS и количеством баллов гистологического фиброза и воспаления. При этом эти соотношения могут быть сложнее, чем мы их оценили, например, с нелинейным увеличением SWS увеличивается фиброз паренхимы или воспаление.
Одним из основных преимуществ нашего исследования является то, что оно является первым в своем роде, которое непосредственно сравнивает режимы VTQ и VTIQ SWE для исследования фиброза печени у детей. VTIQ, в отличие от VTQ, обеспечивает цветное изображение жесткости печени, что позволяет выявить самые жесткие области печени и оценить неоднородность паренхимы. Наши результаты показывают, что в среднем у детей, значения SWS при VTIQ немного выше, чем значения VTQ у того же ребёнка. Источник этой систематической разницы не достаточно изучен, хотя, вероятно, связан с техническими различиями между режимами VTQ и VTIQ. Забегая вперед, при клиническом применении SWE у детей и взрослых, будет важно учитывать различия в значениях SWS, которые получены с использованием различных режимов SWE и разных ультразвуковых систем для того, чтобы правильно интерпретировать результаты. В связи с тем, что в наше исследование включено почти 30 детей с отсутствием или очень минимальным фиброзом печени (гистологический фиброз 0-1 балл), наши результаты должны помочь установить характерное нормативное или околонормативное значения SWS для конкретной ультразвуковой системы, которую мы использовали в педиатрической популяции (примерно 1,46 м/с [95% ДИ: 1.37-1.55 м/с] для VTQ и 1,74 м/с [95% ДИ: 1.67-1,81 м/с] для VTIQ). Эти значения SWS немного выше, чем сообщалось в некоторых опубликованных исследованиях. Например, в недавнем исследовании Matos и др. с помощью VTQ и датчиком 4С1 определено нормальное значение SWS детской печени как 1.07 м/с, в среднем, в то время как исследование Fontanilla и др. с помощью датчика 9L4 находит, что нормальное значение SWS детской печени должно быть 1,15 м/с, в среднем. Еще одно недавнее исследование Tütar и др., с использованием другой ультразвуковой системы (SuperSonic Imagine, Aix-en-Provence, France), определило нормальное значение SWS детской печени как 1,56 м/с, что вполне похоже на наши результаты.
Наше исследование имеет несколько ограничений. Во-первых, около половины детей в нашем исследовании не имели, или имели очень минимальный фиброз печени, в то же время был минимальный процент детей с более высокими степенями фиброза (например, только восемь детей имели балл 5 или 6 по шкале фиброза Ishak). Несмотря на это, мы четко показали, что значения SWS печени возрастают с увеличением воспаления и фиброза. Большее число детей с умеренным и тяжелым фиброзом печени позволило бы нам еще точнее смоделировать соотношение между SWS и количеством баллов гистологического фиброза. Во-вторых, наши результаты могут иметь погрешности, так как в нашем исследовании был только один патологоанатом, который подсчитывал баллы гистологического воспаления и фиброза. Гистологическое определение стадии фиброза и воспаления – субъективно, несмотря на использование проверенных полуколичественных скоринговых систем, и потенциально подвержено систематическим и случайным ошибкам измерения. Наконец, хотя мы проводили SWE в области отбора проб ткани в момент биопсии, по-прежнему почти невозможно достичь идеальной корреляции 1: 1 – изображения к гистологии.
ВЫВОДЫ
Показатели SWS печени возрастают с увеличением фиброза печени у детей. Параметры скорости сдвига волны при VTQ и VTIQ имеют сильную корреляцию, и показатели SWS печени могут эффективно дифференцировать детей с отсутствием или слабым фиброзом печени, от детей с умеренным или тяжелым фиброзом печени. При использовании нескольких видов линейного регрессионного анализа, мы также показали, что и гистологический фиброз, и воспаление являются предикторами увеличения показателей SWS при ультразвуковом исследовании. Необходимы дополнительные исследования для улучшения диагностической точности ультразвукового метода SWE, а также понимания того, как показатели SWS меняются с течением времени у детей с хроническим заболеванием печени, как отек и запор влияют на измерения SWS печени, и как результаты ультразвуковой SWE соотносятся с таковыми, полученными при использовании МР эластографии. Для проведения исследований рекомендуем использовать аппарат от компании GE Voluson E8.




14.10.2019
Дядченко Святослав Андреевич