Sudheer Gokhale, MD, FICR, FICMU
Реноваскулярная гипертензия (РВГ) развивается тогда, когда артериальное давление повышается в результате почечной ишемии. Goldblatt, в его знаменитом эксперименте в 1934 году, показал, что окклюзия почечных артерий создает ишемию, которая инициирует высвобождение ренина и вызывает вторичную артериальную гипертензию. РВГ в результате стеноза почечной артерии – потенциально излечимая форма вторичной артериальной гипертензии. Почки одновременно являются и виновником, и жертвой; зачастую возникает порочный круг между реноваскулярной патологией, которая приводит к гипертензии, а та, в свою очередь, приводит к большему повреждению почек. Чем раньше есть возможность обнаружить эту ситуацию, тем меньше вероятность того, что разовьется перманентное и необратимое повреждение почек.
КЛИНИЧЕСКАЯ ИСТОРИЯ
Гипертония является первичным процессом у большинства пациентов, у которых не найдены ее причины, называется гипертонической болезнью и составляет от 95% до 99% пациентов. Вторичная гипертензия развивается у небольшой группы пациентов, и по оценкам составляет от 1% до 5% всех больных гипертонической болезнью. Гипертония, которая является вторичной по отношению к стенозу почечной артерии, затрагивает даже меньшую часть, и составляет от 1% до 2% пациентов в некоторых исследованиях, и от 2% до 5% пациентов по данным более современных исследований. Это частота изменчива по двум причинам: старение населения подвержено атеросклеротической болезни почек, и то, что развитие технологии диагностики улучшили уровень выявления стеноза почечной артерии.
РВГ определяется как хроническое повышение артериального давления в результате почечного артериального стеноза. Обычно процесс развивается в двух различных возрастных группах. В группе детей и молодых взрослых с гипертонией, которая развивается как следствие реноваскулярной патологии, проблема часто остается незамеченной и манифестирует в результате развитием осложнений, которые включают энцефалопатию, внутричерепное кровоизлияние или гипертоническую кардиомиопатию. Гипертония, которая развивается как следствие реноваскулярной патологии, является более распространенной в этой группе, чем у взрослых. Некоторые исследования показывают частоту встречаемости до 10% в случайной педиатрической популяции. Вторая группа, где гипертония является вторичной к реноваскулярной патологии, это группа пожилых людей, в которой существует высокая распространенность атеросклероза. Так как гипертоническая болезнь достаточно распространена в этой возрастной группе, подозрение на реноваскулярную причину часто основано на изменениях в поведении артериального давления или необъяснимой причине почечной недостаточности. Реноваскулярная патология и гипертоническая болезнь могут сосуществовать одновременно, и обнаружение поражения почечной артерии не всегда позволяет установить диагноз РВГ в этой группе пациентов. Это требует процедуры реваскуляризации; снижение артериального давления предполагает наличие причинно-следственной связи.
Невозможно провести визуальное обследование всех пациентов с гипертонией, частота обнаружения будет меньше, чем 1% и иррациональной в плане эффективности экономических затрат. В зависимости от того, каким образом пациенты с РВГ будут представлены, осуществляется выбор пациентов, которым необходима диагностическая визуализация. Это является оптимальным решением для обследования только тех пациентов, у которые предполагается высокий риск развития РВГ. С внедрением предварительного протокола обследования, процент выявления реноваскулярной патологии достигает 15% – 32%. Общепринятыми критериями отбора пациентов являются следующие:
-
Злокачественная гипертензия.
-
Гипертензия, которая не реагирует на оптимальное медикаментозное лечение.
-
Гипертоническая болезнь у молодых (возраст < 20 лет).
-
Известная гипертоническая болезнь с недавним и необъяснимым ухудшением функции почек.
-
Значительная разница размера почек у пациентов, у которых выявили недавно гипертонию.
-
Развитие почечной недостаточности у пациентов на фоне приема ингибиторов ангиотензин превращающего фермента (АПФ).
-
Рецидивирующий или молниеносный отек легких.
-
У больных с артериальной гипертензией с четким абдоминальным шумом (физиологичный шум является характерным для молодых лиц).
ПАТОФИЗИОЛОГИЯ
Ишемия почек вызывает увеличение секреции ренина из юкстагломерулярного аппарата почек. Выброс ренина ускоряет превращение ангиотензиногена – гормона, который вырабатывается печенью, в ангиотензин 1. Дальнейший процесс под контролем фермента АПФ, преобразует ангиотензин 1 в ангиотензин 2, который в свою очередь стимулирует выработку альдостерона. Ангиотензин 2 также вызывает сужение кровеносных сосудов в афферентных и эфферентных артериолах. Эффект на эфферентные артериолы гораздо более значительный, что приводит к снижению скорости клубочковой фильтрации (СКФ). Альдостерон в конечном итоге вызывает задержку воды и натрия. У здоровых любая резкая гипотензия вызывает ренин-ангиотензиновый каскад для стимуляции эфферентной вазоконстрикции, что приводит к увеличению клубочкового гидравлического давления для поддержания клубочковой фильтрации. В ишемизированной почке афферентный кровоток уменьшается. Клубочковая фильтрация затем поддерживается ангиотензин 2-опосредованным сужением эфферентных сосудов. У пациентов, которые получают ингибиторы АПФ, этот эфферентный вазоконстрикторный ответ не достаточный, что не позволяет поддерживать СКФ при уменьшении почечного кровотока в ишемической почке. Следовательно, у пациентов с двусторонним стенозом почечной артерии или у больных со стеноз почечной артерии единственной почки, ингибиторы АПФ могут вызвать ухудшение функции почек. Прекращение введения ингибиторов АПФ устраняет почечную дисфункцию у этих пациентов.
ДИАГНОСТИКА СТЕНОЗА ПОЧЕЧНОЙ АРТЕРИИ
Ангиография является общепринятым золотым стандартом для диагностической визуализации почечных артерий. Ангиография – инвазивная процедура и, в связи с этим, сопряжена с характерными осложнениями: разрыв стенки сосуда, эмболизация атеросклеротической бляшкой, кровоизлияния, инфекции и, при использовании препаратов, развитие нефротоксичности и аллергических реакций. Компьютерная томография (КТ) и магнитно-резонансная ангиография (МРА) являются альтернативными методами. Обе процедуры являются отличным методом визуализации анатомического стеноза, но не обеспечивают функциональной информацией о влиянии стеноза на физиологию сосудов. Контрастные вещества, которые используются во время КТ и MРТ имеют нефротоксичный эффект, что может быть опасно для функции почек у определенных пациентов, и это нельзя оставить без внимания. Цветная ультрасонография и спектральная допплерография являются неинвазивными и безопасными методами, которые обеспечивают как анатомической, так и физиологической информацией. Ультрасонография, однако, не всегда достаточна для оценки стеноза почечной артерии, частично из-за присущей сложности выполнения обследования, а также высокой степени зависимости от оператора.
Допплерография используется для скрининга пациентов с предположительно основной почечной причиной артериальной гипертензии на протяжении нескольких лет. В одном из ранних исследований с использованием ультрасонографии для оценки стеноза почечной артерии использовалась пиковая систолическая скорость (ПСС) артерии с пороговым значением 100 см/сек, с чувствительностью 89%, для определения наличия значительного стеноза почечных артерий. При дальнейшей оценке с помощью тех же критериев скорости сообщается о чувствительности – 91% и специфичности – 95% – для выявления наличия значительного стеноза почечной артерии. При использовании соотношения скоростей почечной артерии к аорте более чем 3,5 в диагностике более чем 60% случаев стеноза, Taylor и др. определили общую точность исследования – 93%. Другие исследования, ориентированные на ПСС основной почечной артерии, сообщили об успешном выполнении исследования артерий в 65%-80%, с чувствительностью от 79% до 91% и специфичностью от 73% до 93% для диагностики стеноза почечной артерии.
Визуализация основной почечной артерии была одной из главных проблем в этих ранних исследованиях и, к сожалению, без видимых значительных технических усовершенствований и сегодня. В попытке преодолеть ограничения метода прямой визуализации основной почечной артерии, Ханда и др. описали использование внутрипочечных допплеровских критериев для обнаружения постстенотических явлений, tardus-parvus (медленный и низкий) спектральный сигнал с точностью 95%. С тех пор несколько исследований с успехом использовали внутрипочечные допплеровские критерии для выявления стеноза почечной артерии. После этого начального периода энтузиазма была фаза, когда появилось чувство, что допплерография не является удачным методом скрининга в связи с техническими трудностями, так как проксимальный аспект почечных артерий остается невизуализированным у некоторых пациентов. Последующие исследования не подтвердили ранее полученные результаты и сообщили о плохой чувствительности и точности допплерографии в обнаружении стеноза почечной артерии, в основном за счет большого количества технически неадекватных результатов в этих исследованиях.
Совершенствование технологий ультразвукового оборудования и опыт операторов значительно продвинулись в течение последнего десятилетия. С эволюцией практики двойного доступа в визуализации интраренальных артерий вместе с основными почечными артериями, значительно снизилась частота неудачных исследований и значительно улучшилась в целом точность самой техники. По опыту автора, частота неудачных исследований составляет менее 5%. Другие авторы сообщают аналогичные показатели успешных процедур; Zeller и др. сообщили о 90% успешных исследований, а Radermacher и др. сообщили о показателе успеха процедуры равном 100%. Более того, в связи с высокой частотой успешного выполнения технических аспектов самой процедуры, значительно улучшилась общая точность допплерографии в качестве скринингового теста для стеноза почечной артерии. Zeller и др. сообщили о чувствительности – 90% и специфичности – 97%; Voiculescu и др. сообщили о чувствительности и специфичности – 96% и 89%, а Radermacher и др. сообщили о чувствительности – 96,8% и специфичности – 98%.
ТЕХНИКА
В связи новыми техническими достижениями как в датчиках, так и в приложениях обработки изображений, хорошее качество визуализации может быть достигнуто даже у пациентов с ожирением. Кишечные газы являются основным сдерживающим фактором для оптимального обследования и не могут быть преодолены с помощью новых технологий. Хотя пациенты должны голодать до исследования, небольшие объемы жидкости без газа допускаются. Ветрогонные и слабительные за день до исследования могут помочь, и даже показаны в день обследования. Исследование должно включать в себя осмотр почек и надпочечниковой области. Полное анатомическое обследование размеров почки и ее морфологии, для исключения патологии паренхимы, является частью реноваскулярного допплерографического исследования. Особое внимание должно быть уделено дифференциальной оценке любого изменения толщины в разных частях каждой почки, так как это может быть единственным доказательством сегментарного стеноза или окклюзии артерии. Обследование надпочечниковой области для выявления любой аномалии надпочечников оправдано и является важным с позиции выявления феохромоцитомы. Брюшная аорта, основная почечная артерия, внутрипочечные сегментарные и междолевые артерии, являются основными целями допплерографического исследования. Артерия доступна исследованию при переднем или переднебоковом доступе. Диаметр аорты должен быть измерен в верхней, средней и нижней частях. Аортальные стенки должны быть исследованы на наличие бляшек и любого сужения просвета. При переднем доступе аортальный кровоток почти перпендикулярен углу ультразвукового луча. Смещение датчика в каудальном и головном направлениях является полезным маневром для получения хорошего цветного сигнала, а также оптимального угла для допплерографии так, чтобы измерение пиковой систолической скорости было как можно более точным.
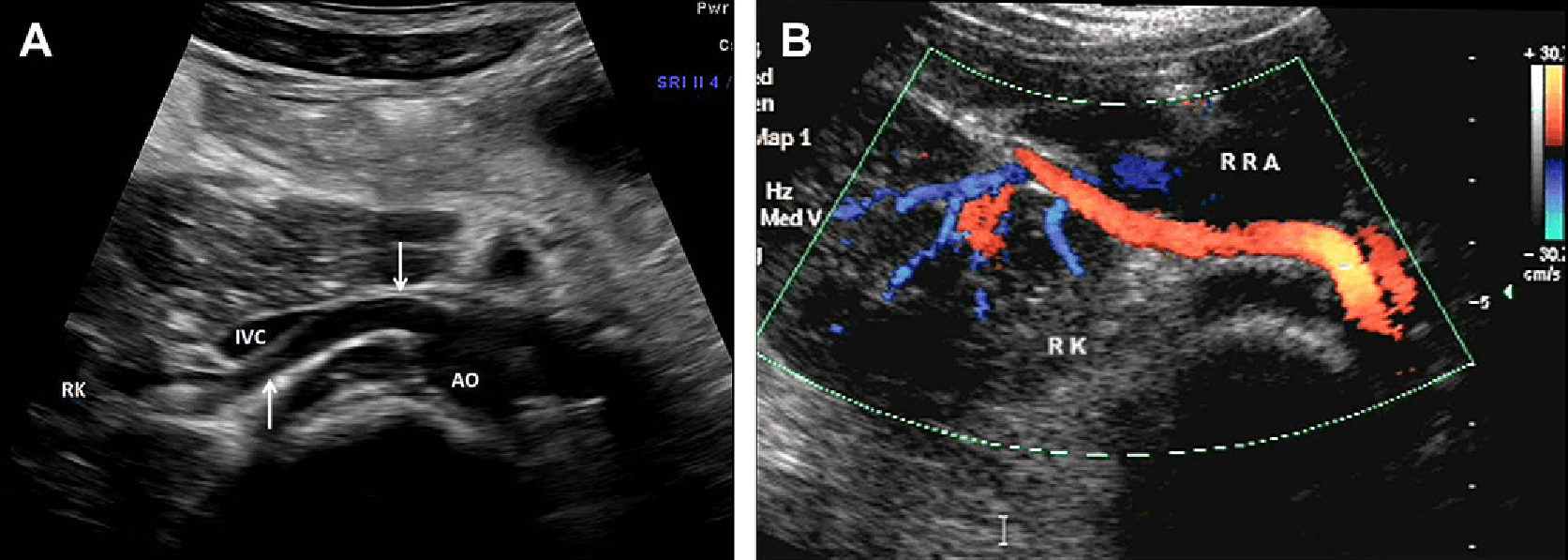
Правая почечная артерия (ППА) отходит от боковой или переднебоковой стенки брюшной аорты чуть дистальнее формирования верхней брыжеечной артерии. Затем она проходит сзади от нижней полой вены (НПВ). В большинстве случаев, ППА располагается перпендикулярно к ультразвуковому лучу, создавая сложную техническую задачу для создания хорошего допплеровского сигнала сосудистого потока. С другой стороны, это является преимуществом для изображения в оттенках серого и при этом артерия, как правило, хорошо видна. На практике иногда бывает трудно зарегистрировать хорошее цветное допплеровское изображение при переднем доступе. Существуют проблемы с определением границы ППА, так как цветной допплеровский поток в НПВ и ППА имеют одно направление и окрашиваются в один и тот же цвет. При этом лучше локализовать ППА путем применения импульсной спектральной допплерографии, без добавления цветного потока, по изображению в оттенках серого. Во время исследования артерии из переднего доступа, авторы считают полезным наклонить ультразвуковой датчик слегка в бок, в сторону исследования для получения лучшего угла атаки допплеровского измерения. Даже у пациентов с ожирением зачастую не трудно изучить дистальный аспект ППА из переднебокового доступа, используя печень в качестве акустического окна (рис. 1).
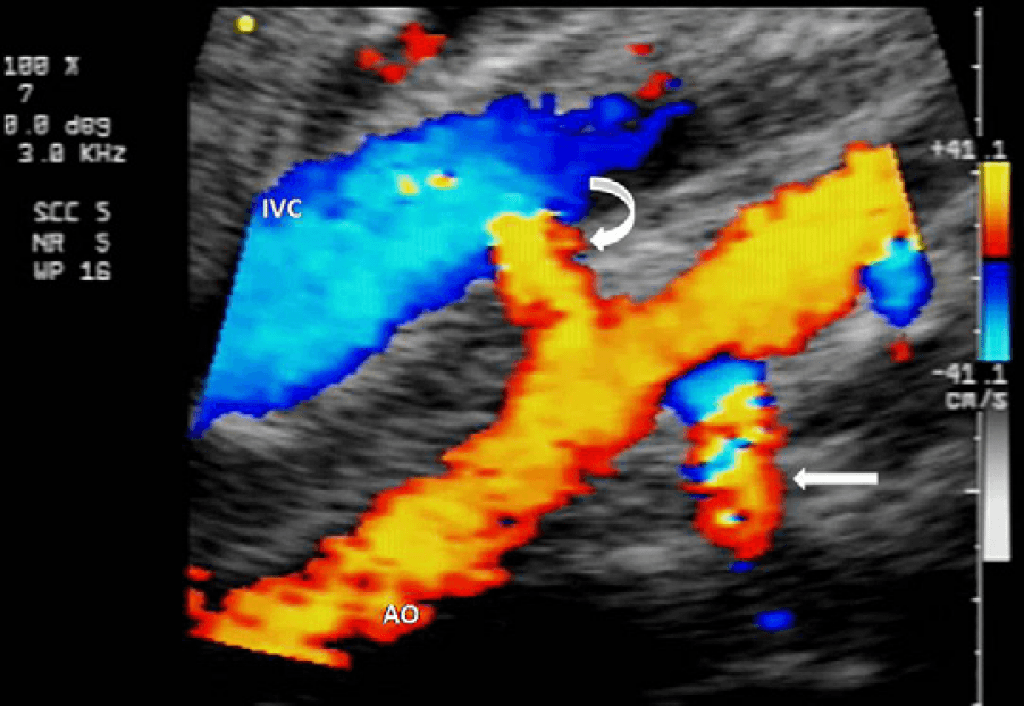
Рис. 1. Поперечные изображения правой почечной артерии (RRA). (А) Передней доступ, осевое изображение в оттенках серого RRA (стрелки), которая образуется от правой переднебоковой стенки аорты (АО). RRA проходит сзади от нижней полой вены (IVC) к правой почке (RK). (В) Поперечное цветное допплеровское изображения из переднебокового доступа отражает всю длину RRA.
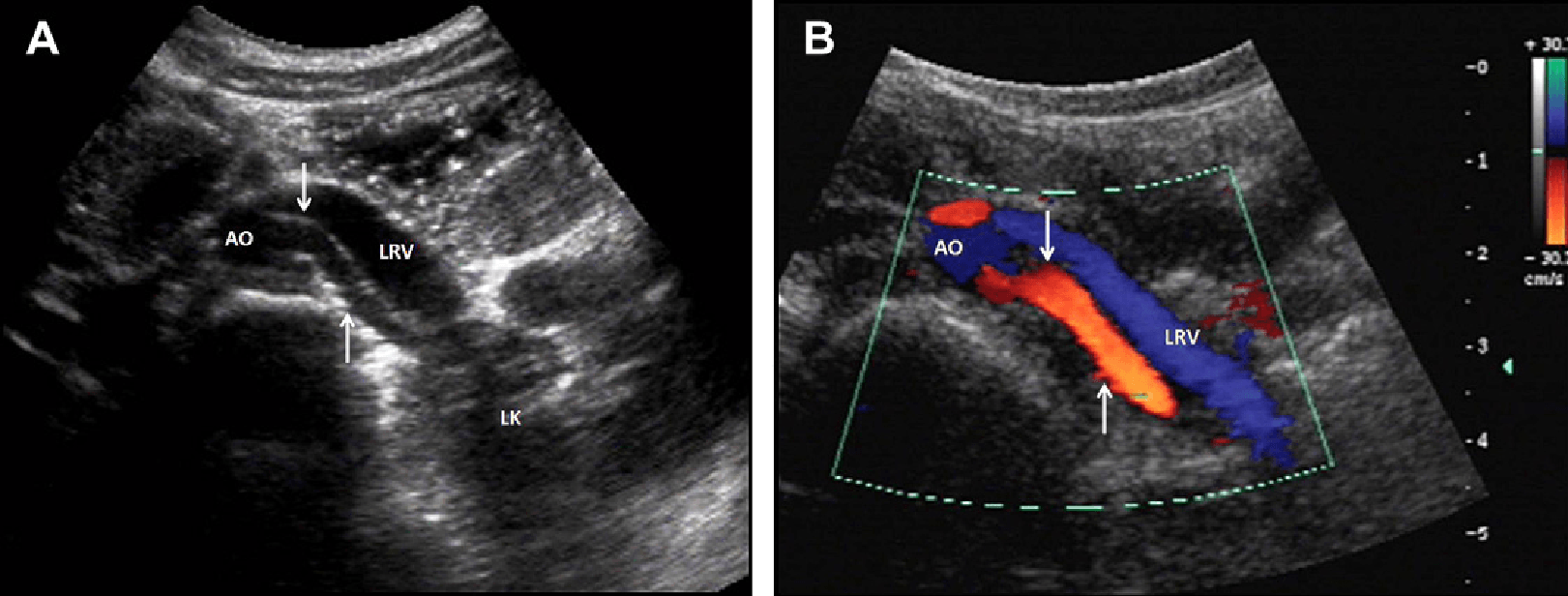
Левая почечная артерия (ЛПА) отходит от боковой или заднебоковой стенки брюшной аорты. Ее начало, как правило, находится выше начала ППА. ЛПА затем проходит латеральнее и сзади от левой почечной вены и впереди поясничной мышцы. Дистальная часть ЛПА более проблематична для визуализации и, как правило, может быть осмотрена со стороны левого фланка, используя левую почку в качестве акустического окна, путем размещения пациента в положении на правом боку (рис. 2).
Рис. 2. Поперечные изображения левой почечной артерии (LRA). (А) Поперечное изображение в оттенках серого LRA (стрелки), которая начинается от боковой поверхности аорты (AO). LRA проходит сзади и параллельно левой почечной вене (LRV), по направлению к воротам левой почки (ЛП). (В) Поперечное цветное допплеровское изображение LRA от уровня АО, сзади от LRV.
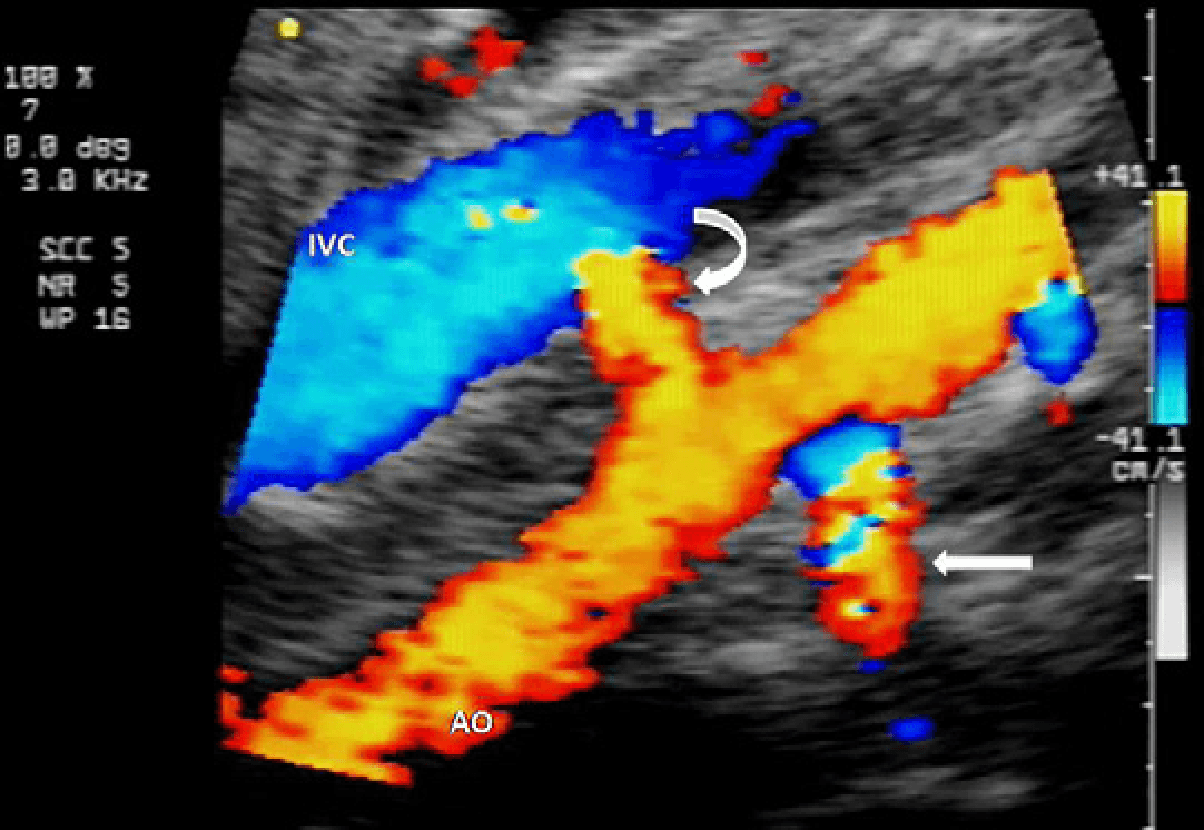
Иногда косой доступ в коронарной плоскости может быть необходим для того, чтобы определить место начала почечных артерий. Пациент помещается в частичное положение на левом боку и осмотр выполняется в косой фронтальной плоскости. С этой точки зрения обе почечные артерии, как правило, изгибаются проксимальнее и дистальнее по отношению к аорте. Этому маневру было дано название «вид банановой кожуры» (рис. 3).
Рис. 3. Косая коронарная проекция цветного допплеровского изображения аорты (АО) из правого переднего доступа. Правая почечная артерия (изогнутая стрелка) направлена к датчику и пересекает нижнюю полую вену (IVC) сзади. Левая почечная артерия (прямая стрелка) начинается позади аорты.
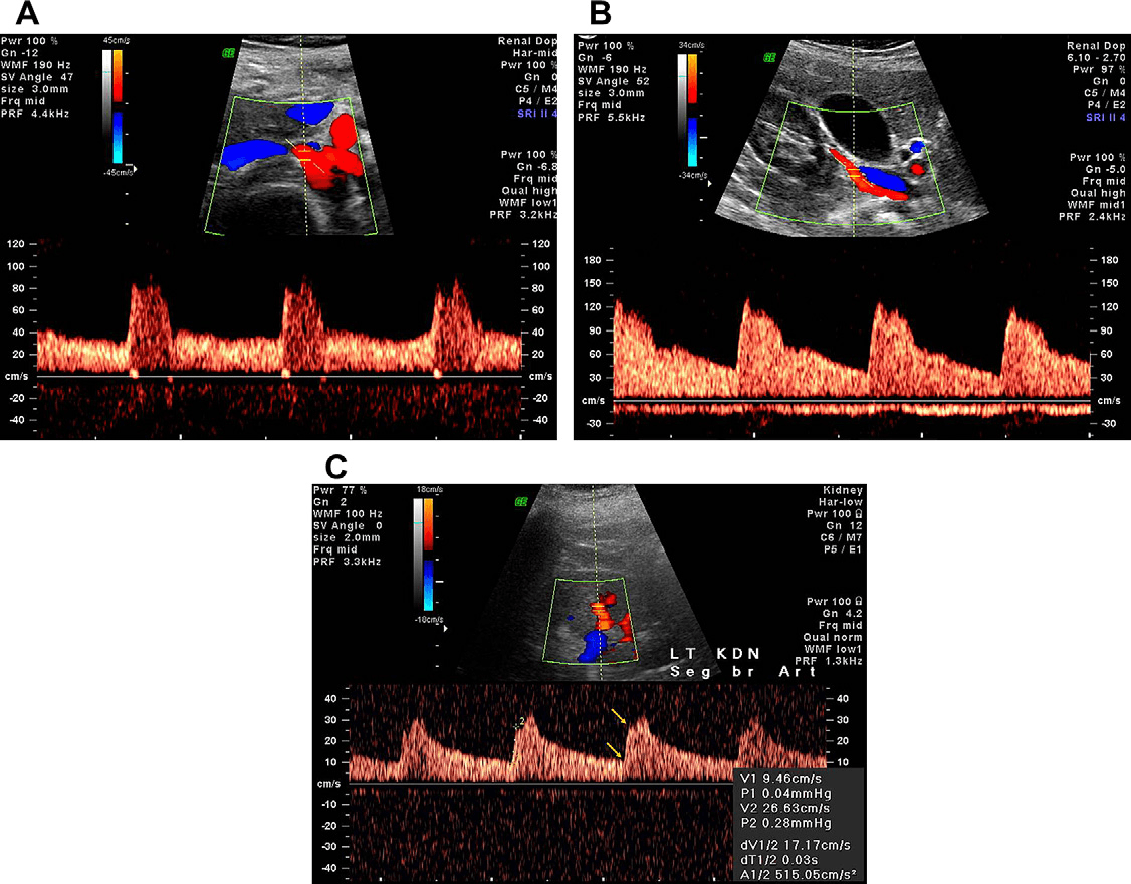
Цветное допплеровское изображение и спектральное допплеровское изображение являются основой исследования почечной артерии. Цветная допплерография обеспечивает визуализацию почечных артерий и кровотока в виде «птичьего глаза». Настройка усиления цвета должна быть установлена на высокие показатели – чуть ниже уровня, на котором появляется шум. Настройки частоты повторения импульсов (шкала) и фильтр должны быть отрегулированы в соответствии с скоростями потока в сосудах достаточно высоко, чтобы отрезать кровоток по венам, но достаточно низко, чтобы произвести наложение спектров на месте стеноза. Спектральный допплеровский анализ выполняется в главных почечных артериях, в идеале на каждом отрезке от 1 см до 2 см по длине артерии. Если это технически не осуществимо, то измерения должны быть выполнены, по крайней мере, в проксимальном, среднем и дистальном сегментах (рис. 4).
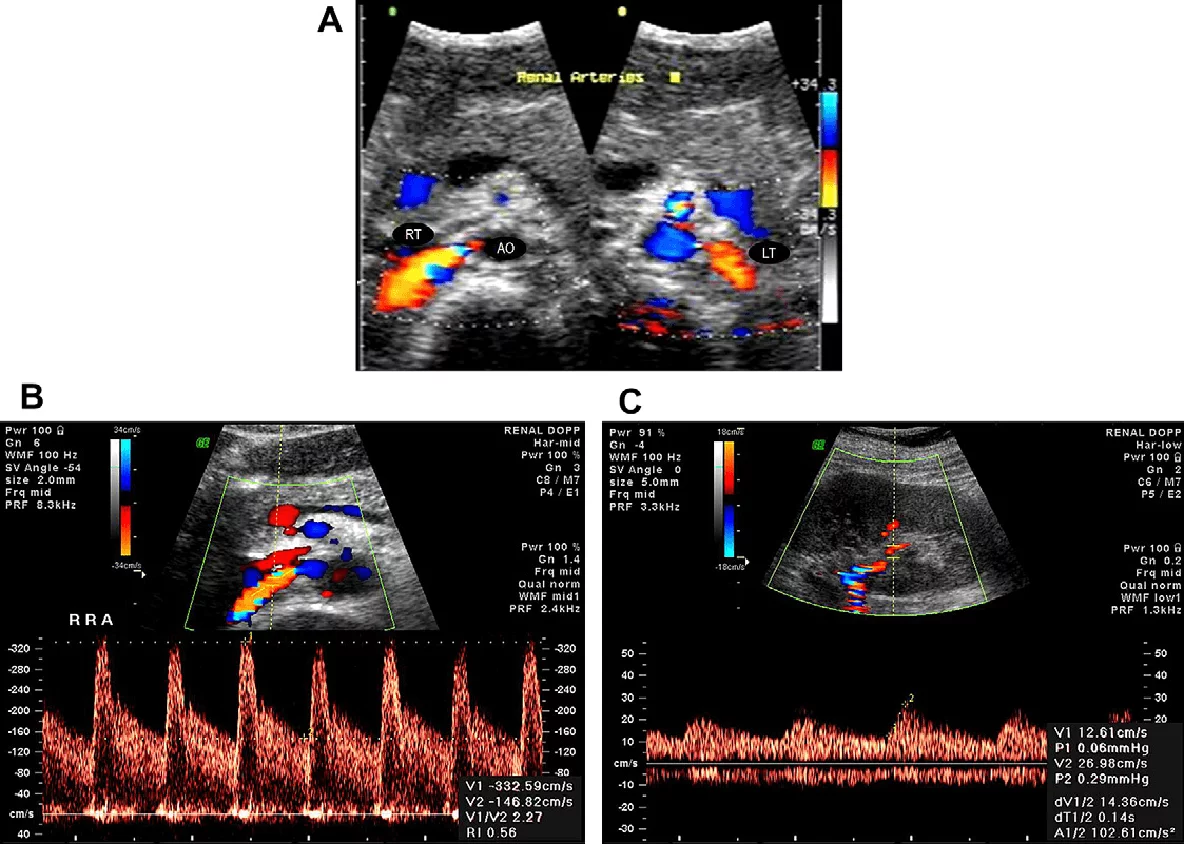
Рис. 4. Нормальные спектральные допплеровские сигналы в почечной артерии. (А) Спектральная допплерография у места образования правой почечной артерии. (В) Спектральная допплерография средней части почечной артерии. Нормальные формы волны показывают четкую систолу и хороший объем диастолического потока. (С) Исследование междолевой артерии. Измерение индекса ускорения и времени ускорения; измерения систолической кривой проводятся от начала кривой до вершины первого пика (стрелки).
Пиковая систолическая скорость записывается в почечной артерии и аорте, а затем рассчитывается почечно-аортальное соотношение (renaleaortic ratio – RAR). У пациентов с ожирением картографический цветной поток почечных артерий может не обеспечить адекватную визуализацию самих артерий, но диагностика стеноза почечной артерии основана исключительно на анализе спектральных данных, поэтому более важным является получение хорошего спектрального изображения, чем цветного допплеровского. Следовательно, большее внимание должно быть уделено на точное размещение акустических ворот и точную коррекцию допплеровского угла.
Интраренальные артерии легко достигаются со стороны фланков. Пациент может лежать на спине или, что предпочтительней, в положении на боку. Почечные артерии и вены проходят через почечные ворота в пространство почечного синуса. Артерии делятся на передние и задние ветви, которые, в свою очередь, делятся на сегментные, междолевые и аркуатные ветви. Как сегментные, так и междолевые артерии направлены непосредственно к датчику. Чувствительность допплеровского сигнала хорошая, что делает допплеровское исследование внутрипочечных судов относительно несложным. Однако, следует отметить, что качество цветного допплеровского сигнала зависит от угла атаки, интраренальные сосуды имеют противоположный цвет в ближнем и дистальном отделах почки. Спектральный анализ потока выполняется в сегментарных и междолевых артериях, последовательно в верхней, средней и нижней частях обеих почек. Индекс ускорения (Acceleration index – AI) и время ускорения (acceleration time – AT) систолической кривой должны быть зарегистрированы. Необходимо быть внимательным во время записи AI и AT, так как часто начало систолического пика не всегда соответствует максимальному систолическому пику. До систолического пика может быть выступ или ранняя систолическая впадина, и только первую наклонную кривую систолы следует измерять (см рис. 4).
Реноваскулярное допплеровское исследование является одним из самых сложных ультразвуковых исследований для выполнения, но при современном оборудовании, подготовке пациентов и тщательной техники исследования, можно добиться технически удовлетворительного результата в большинстве случаев, с частотой успешных исследований около 99% – по данным недавних исследований с использованием новой технологии.
ДИАГНОСТИКА СТЕНОЗА ПОЧЕЧНОЙ АРТЕРИИ
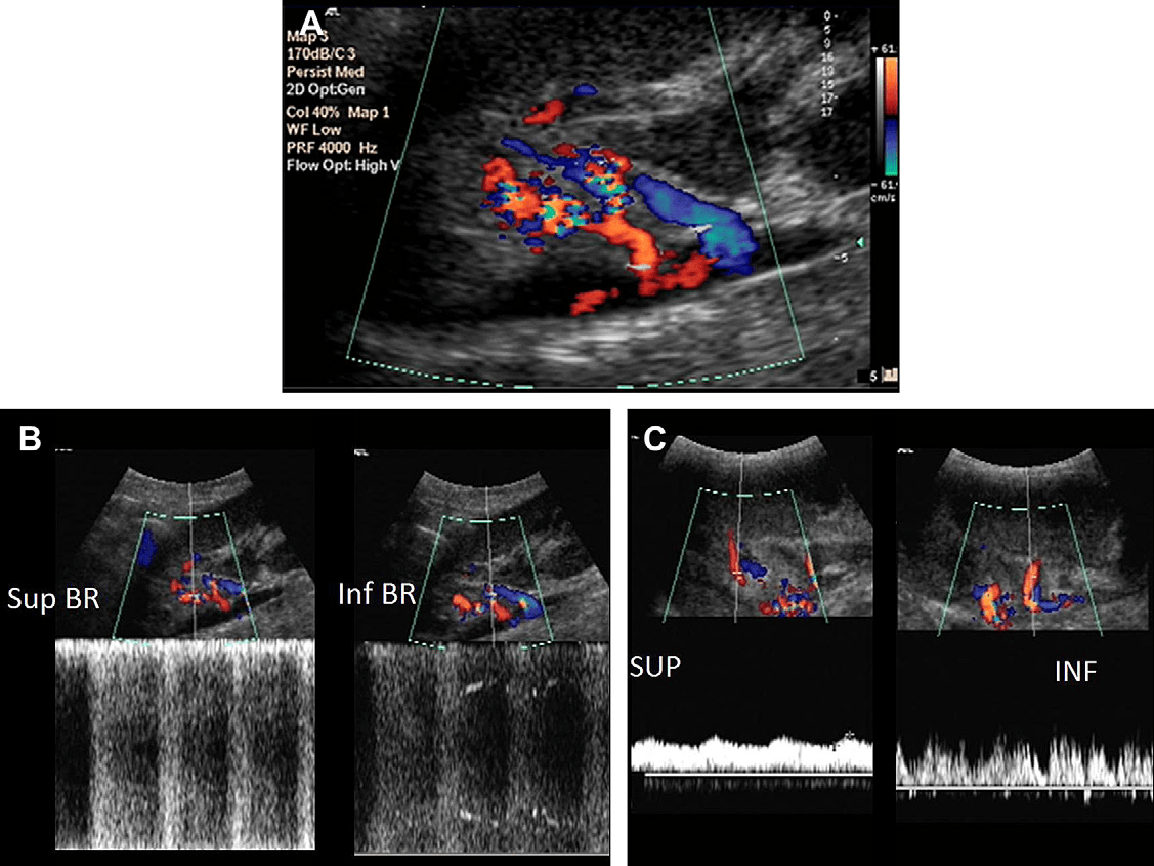
Скорость кровотока значительно увеличивается в узком сегменте, а объемный поток должен оставаться неизменным в стенозированном сегменте. Увеличение скорости пропорциональна степени сужения просвета. Цель допплерографии заключается в обнаружении фокального высокоскоростного турбулентного потока в главных почечных артериях, что указывает на стеноз. Это проявляется в виде фокальной области наложения при цветном картировании потока. Спектральная допплерография показывает высокую ПСС и расширение допплеровского спектра из-за турбулентности, которая создается в этом месте. Значимый стеноз имеет декомпрессионное влияние на артериальный поток и ослабленный поток с tardus-parvus сигналом видно за пределами стеноза. Интраренальные сегментарные артерии также необходимо исследовать для обнаружения этого постстенотического явления. В настоящее время существует консенсус об использовании двойного доступа в диагностике стеноза почечной артерии. Прямое доказательство места стеноза в главных почечных артериях и косвенные данные из интраренальных артерий способствуют повышению точности допплеровского исследования (рис. 5).
Рис. 5. Допплеровские признаки при стенозе почечной артерии. (А) Поперечное изображение цветного кровотока в почечных артериях в месте их отхождения от аорты (АО). Сужение просвета в начале и очень яркие оттенки цвета и наложение указывают на высокую скорость и турбулентный поток в обоих почечных артериях. (В) Импульсная допплерография в суженной артерии показывает высокую пиковую систолическую скорость (3,3 м/с). (С) Импульсная допплерография в сегментарной ветке суженной почечной артерии показывает tardus-parvus сигнал с аномальными параметрами (AI – 1.02 м/с и AT – 140 мс).
Большинство исследователей признают показатели от 1.8 до 2.0 м/с, как пороговые значения для ПСС – для основной почечной артерии и 3,5 как пороговое значение для RAR ( соотношении ПСС в почечных артериях к ПСС в аорте) – для диагностики значимого стеноза почечной артерии. Снижение RAR до 3.0 значительно повышает чувствительность, не затрагивая специфику исследования. Интраренальные параметры, которые наиболее часто используются: медленное нарастание систолического ускорения, AI менее 3,0, и увеличение AT более 70 миллисекунд.
Некоторые наблюдатели, однако, признают, что визуальный контроль допплеровского сигнала и выявление tardus-parvus волн достаточно для того, чтобы диагностировать постстенотическое нарушение потока и, что измерения интраренальных параметров излишни. Расчет AI зависит от угла атаки. Некоторые из этих исследований показали, что показатель AT является предподчительным из этих двух внутрипочечных параметров для оценки постстенотического замедления. Существует ряд доказательств для того, чтобы предположить, что назначение ингибиторов АПФ перед допплерографией может улучшить выявление постстенотических изменений, в частности изменения раннего систолического пика.
Расчет индекса резистентности (resistance index – RI) используется в качестве другого косвенного показателя для оценки постстенотического потока в почках. Снижение RI в обе стороны более чем на 5% принимается в качестве дискриминационного показателя для значимого стеноза почечной артерии, с высокой специфичностью от 90% до 99%, но с низкой чувствительностью от 30% до 77%. Необходимо помнить, что двусторонний стеноз, стеноз единственной почки, аритмия, недостаточность аортального клапана являются условиями, которые изменяют интраренальные параметры и они становятся ненадежными для диагностики стеноза почечной артерии. Почечно-сегментарное соотношение также предлагается в качестве превосходного параметра для диагностики значительного стеноза почечной артерии, а почечное междолевое соотношение предложено, как лучший параметр для диагностики стеноза почечной артерии (СПА) в более чем 50% . Эти авторы выяснили, что пороговое значение соотношения почечной междолевой систолической пиковой скорости более 5 и междолевая ПСС менее чем 15 см/с, являются лучшими внутрипочечными критериями диагностики для выявления стеноза почечной артерии. Утверждение заключается в том, что в некоторых случаях струйный поток из дистального стеноза может все равно влиять на параметры ПСС сегментарных артерий, но не достигает междолевых артерий, тем самым увеличивая вероятность регистрации пониженной постстенотической ПСС. Использование дистального соотношения вместо RAR вполне логично. С увеличением степени стеноза, ПСС в зоне стеноза по сравнению с ПСС в постстенотическом сегменте имеет противоположное направление. Таким образом, соотношение становится гораздо более значительным, даже с небольшим повышением степени сужения (рис. 6).
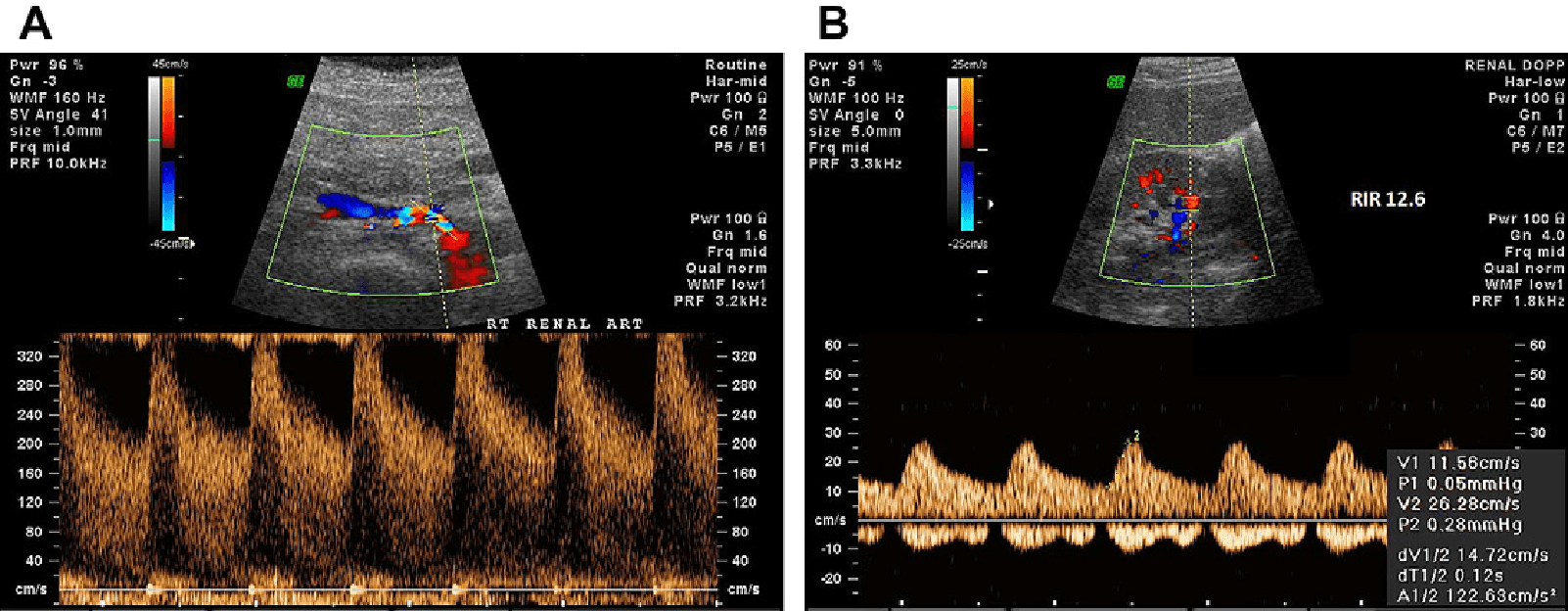
Рис. 6. Аномальное почечное междолевое соотношение (RIR) при стенозе почечной артерии. (А) Спектральный допплеровский сигнал пиковой систолической скорости при стенозе в месте формирования почечной артерии (330 см/с). (В) Спектральный допплеровский сигнал потока в междолевой артерии с пиковой систолической скоростью 26 см/с дает аномальную RIR 12,6.
Использование различных критериев может ввести в заблуждение врача. Большинство авторов согласны с использованием двойного доступа для выявления основных почечных артерий и интраренальных сосудов. Не существует единственного параметра, который подходит для каждого пациента. Основные почечные артерии трудно визуализировать, но специфичность и положительная прогностическая ценность допплеровского исследования для основной почечной артерии отличные. Кровоток во внутрипочечных сосудах, с другой стороны, относительно несложно оценить по сравнению с основными почечными артериями. Тем не менее, на него влияют другие факторы, такие как податливость стенки сосуда, частота сердечных сокращений, и сердечный выброс, и он не чувствительный у пожилых пациентов с известным атеросклерозом (Таблица 1).
Таблица 1.
Допплеровские критерии для диагностики стеноза почечной артерии
|
Допплеровские критерии |
Основная почечная артерия |
Внутрипочечные артерии |
|
Прямые |
ПСС> 1,8 м/с, RAR> 3.0 |
|
|
Косвенные |
AI <3.0, AT> 70 мс |
|
|
В сочетании |
RIR > 5, ПСС в междолевых артериях <15 см/с |
|
Включение прямых критериев является предпочтительным, и диагноз не должен быть основан исключительно на косвенных критериях.
Сокращения: AI – индекс ускорения; АТ – время ускорения; ПСС – пиковая систолическая скорость; RAR – почечно-аортальное соотношение; RIR – почечное междолевое соотношение.
ДОБАВОЧНАЯ ПОЧЕЧНАЯ АРТЕРИЯ
Значительный изолированный стеноз добавочной почечной артерии или ветви основной почечной артерии может быть связан с региональным уменьшением толщины паренхимы почек, которое определяется на изображениях в оттенках серого. При визуализации основных артерий, исследование выполняется в поперечной плоскости выше и ниже главных почечных артерий с целью выявления наличия любых добавочных артерий. Если определяется добавочная артерия, необходимо исследовать кровоток вдоль ее длины, как и для главной почечной артерии. Изучение внутрипочечного кровотока во всех трех сегментах обеих почек проводится для покрытия всей области, в которой могут быть выявлены любые дополнительные почечные артерии. Значимое различие в сигналах между тремя сегментами почки указывает на наличие добавочной артерии или стеноза ветви артерии (рис. 7).
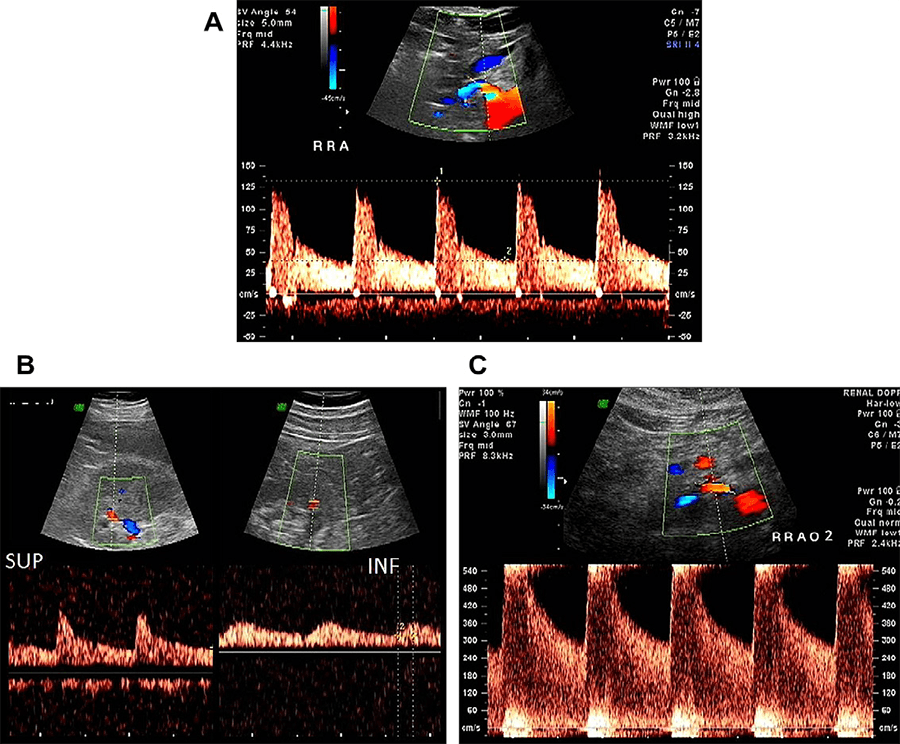
Рис. 7. Различные спектральные допплеровские сигналы в разных частях одной почки помогают определить стеноз добавочной почечной артерии. (А) Спектральный допплеровский сигнал при визуализации правой почечной артерии показывает нормальную пиковую систолическую скорость 130 см/сек. (В) Спектральный допплеровский сигнал во внутрипочечной артерии в верхней части почки (SUP) показывает нормальный сигнал с резким систолическим пиком, индекс ускорения (AI) – 4.2 и время ускорения (АТ) – 20 мс. Спектральный допплеровский сигнал во внутрипочечной артерии нижней части почки (INF), демонстрирует parvus-tardus (слабый и медленный) сигнал, АI – 1.8 и АТ – 170 мс. (С) Добавочная вторая почечная артерия с высокой скоростью турбулентного потока через зону стеноза в месте начала артерии.
Тем не менее, существует общее мнение, что при допплерографии можно пропустить стеноз добавочной почечной артерии, которая может быть ответственной за развитие гипертонии. Эта точка зрения была специально рассмотрена в нескольких недавних исследованиях, которые пришли к выводу, что стеноз добавочной почечной артерии не связан с повышенным риском развития гипертензии. В исследовании 68 стенотических почечных артерий по данным ангиографии, Bude и др. нашли изолированный стеноз добавочной почечной артерии только у одного пациента (1,5%) и пришли к выводу, что невозможность обнаружения добавочных почечных артерий не должна чрезмерно влиять на эффективность неинвазивного теста для обнаружения РВГ.
БОЛЕЗНИ, ЛЕЖАЩИЕ В ОСНОВЕ РЕНОВАСКУЛЯРНОЙ ПАТОЛОГИИ
АТЕРОСКЛЕРОЗ
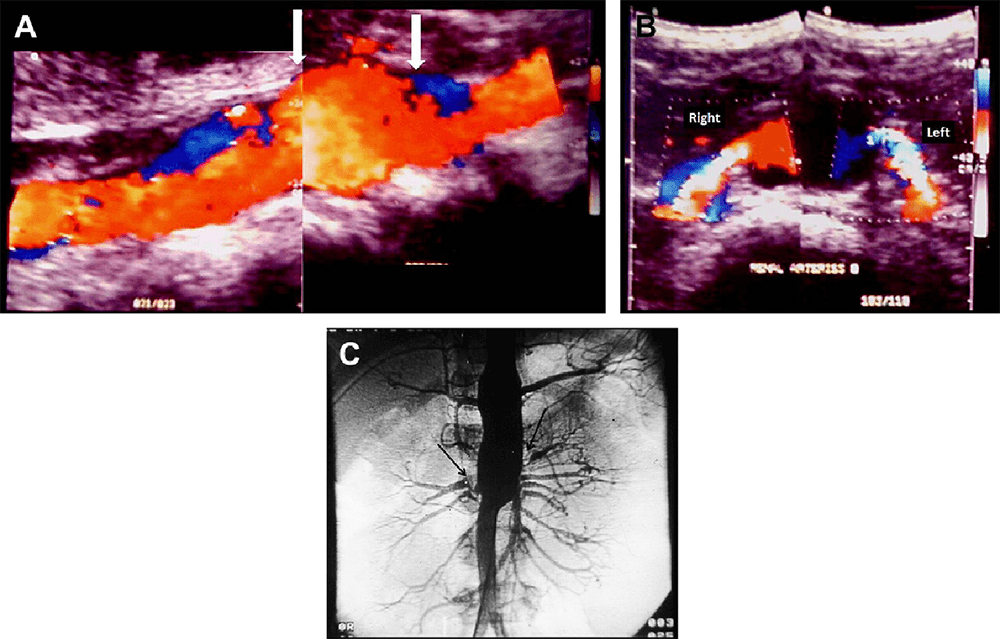
Атероматозные бляшки, вызывающие сужение артериального просвета являются наиболее распространенными причинами реноваскулярной гипертонии у пожилых людей. Стеноз развивается часто с двух сторон и наиболее часто производит к фокальному сужению артерии в месте ее начала. Поражение развивается медленно, но манифестация или изменение в поведении клинического заболевания может быть внезапным. В серии аутопсии, стеноз почечной артерии (стеноз ≥50%) был обнаружен у 27% пациентов старше 50 лет; эта частота увеличилась до 53% у пациентов с анамнезом диастолической гипертензии. Атеросклеротическое сужение просвета может прогрессировать в течение долгого времени и часто связано с уменьшением размера и функции почек. Было выявлено уменьшение длины почек на 1 см в год примерно у 19% пациентов со значительной РВГ. Исследования естественного прогрессирования заболевания у пациентов, которые находятся на лечении по поводу РВГ, показали, что прогрессирования артериальной окклюзии происходит от 9% до 16% всех пациентов. Атероматозное реноваскулярное сужение является одной из основных причин терминальной стадии почечной патологии (рис. 8).
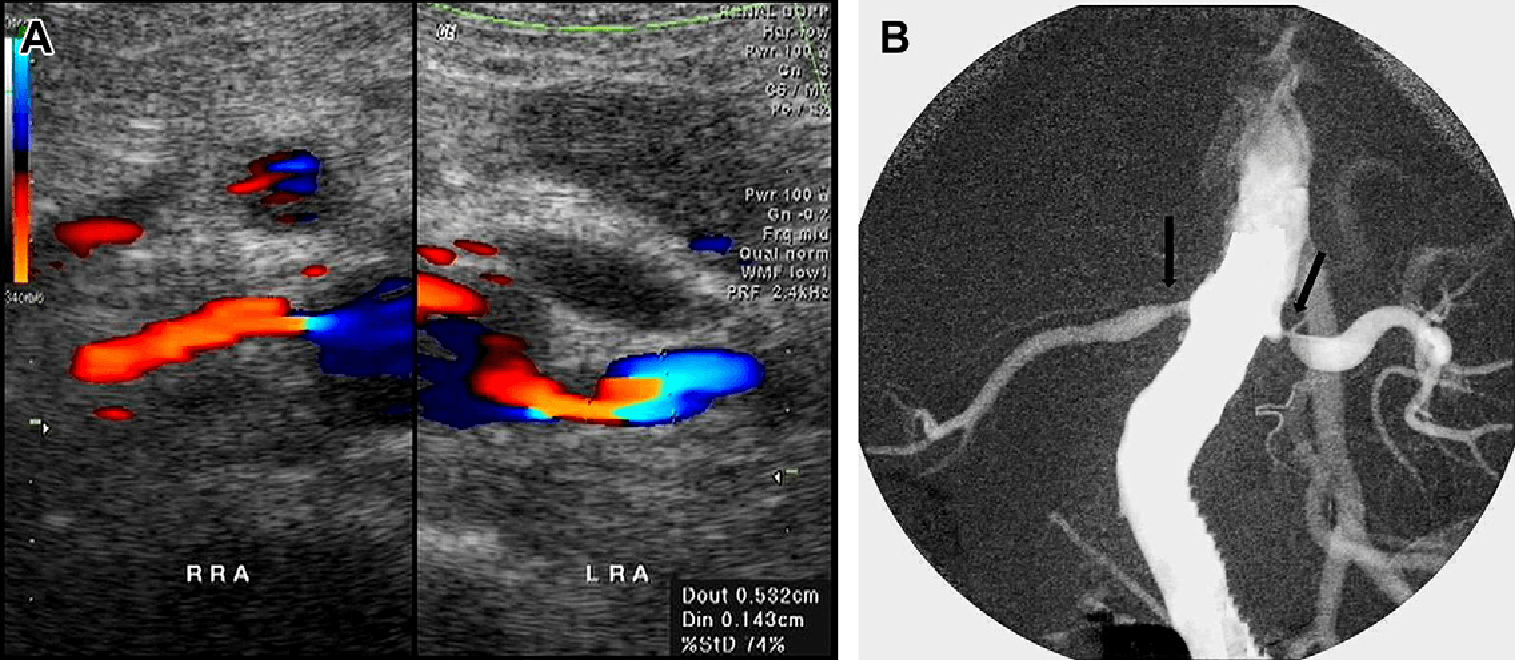
Рис. 8. Двусторонний стеноз почечной артерии у 57-летнего мужчины с прогрессирующей гипертензией, которая не контролируется с помощью трех препаратов. (А) Поперечная цветная допплерограмма демонстрирует стеноз у начала обеих почечных артерий. Цветовое наложение обозначает очень высокую скорость кровотока. Отмечается постстенотическое расширение в левой почечной артерии. (В) Аортограмма того же пациента демонстрирует стеноз в месте начала обеих почечных артерий (стрелки), а также постстенотическую дилатацию левой почечной артерии.
ФИБРОМУСКУЛЯРНАЯ ДИСПЛАЗИЯ/ФИБРОПЛАЗИЯ МЕДИИ
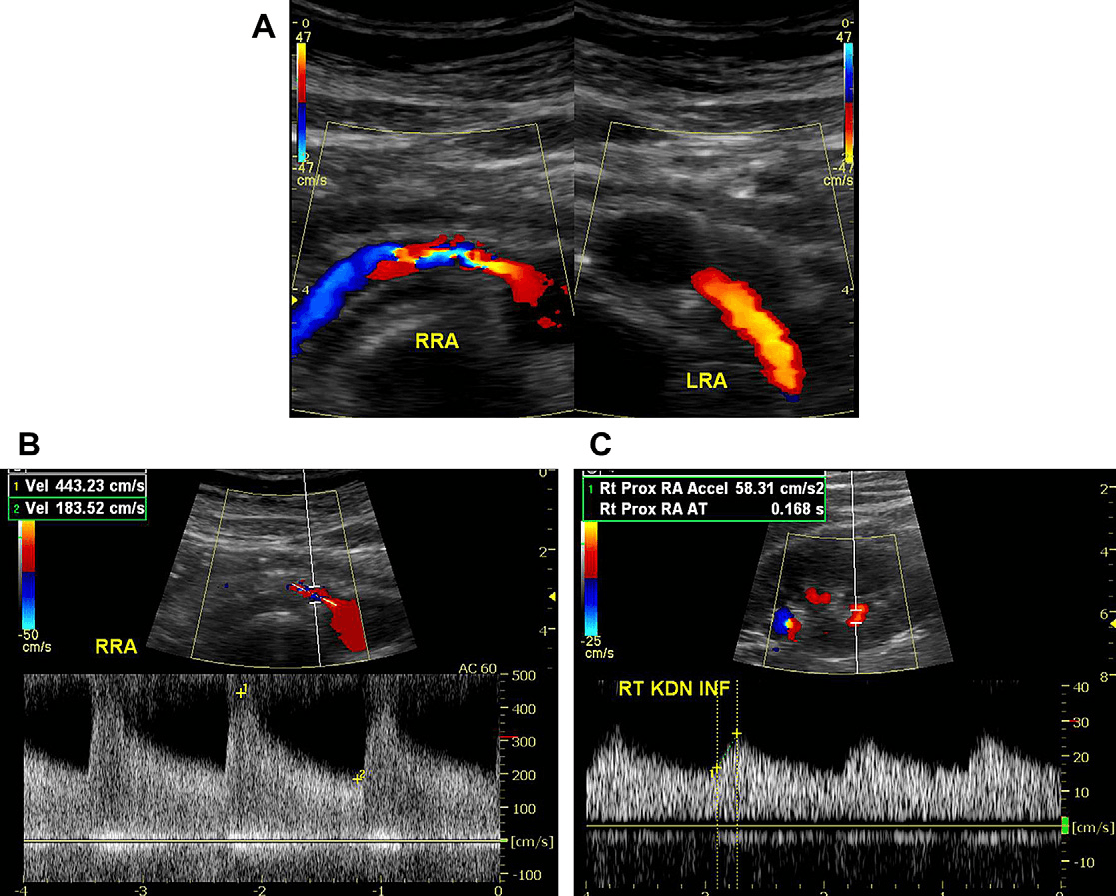
Артериальная дисплазия является второй наиболее распространенной причиной стеноза почечной артерии и ответственна за 10%-30% пациентов со стенозом почечной артерии. Фибромускулярная дисплазия (ФМД) более характерна для молодых и женщин. ФМД описывается как причина стеноза почечной артерии от 30% до 60% детей с РВГ. ФМД приводит к характерным изменениям сосудистой стенки. Как правило, внешний вид «нитки с бисером» описывается при ангиографии. Обычно средний или дистальный сегмент артерии имеет утолщенную стенку. Высокая скорость турбулентного потока выявляется при цветном допплеровском ультразвуковом исследовании. Зачастую цветное картирование потока помогает выявить неровные края пораженного сегмента почечных артерий. Скорость потока зачастую остается нормальной в проксимальном сегменте, который остается нетронутым (рис. 9).
Рис. 9. 30-летняя женщина перенесла инсульт и у нее обнаружили тяжелую гипертоническую болезнь. (А) Поперечная цветная допплерограмма показывает сужение просвета и наложения в средней части правой почечной артерии. Сегментарное поражение средней части артерии является общим признаком фиброзно-мышечной дисплазии. (В) Сигнал при спектральной допплерографии при стенозе показывает высокоскоростной турбулентный поток с пиковой систолической скоростью (PSV) – 443 см/с и EDV – 183 см/с. (С) Сигнал при спектральной допплерографии в внутрипочечной артерии пораженной области показывает типичный parvus-tardus сигнал (индекс ускорения [AI] 0,58 и время ускорение [AT] 168 мс).
АОРТОАРТЕРИИТ (НЕСПЕЦИФИЧЕСКИЙ АРТЕРИИТ, АРТЕРИИТ ТАКАЯСУ)
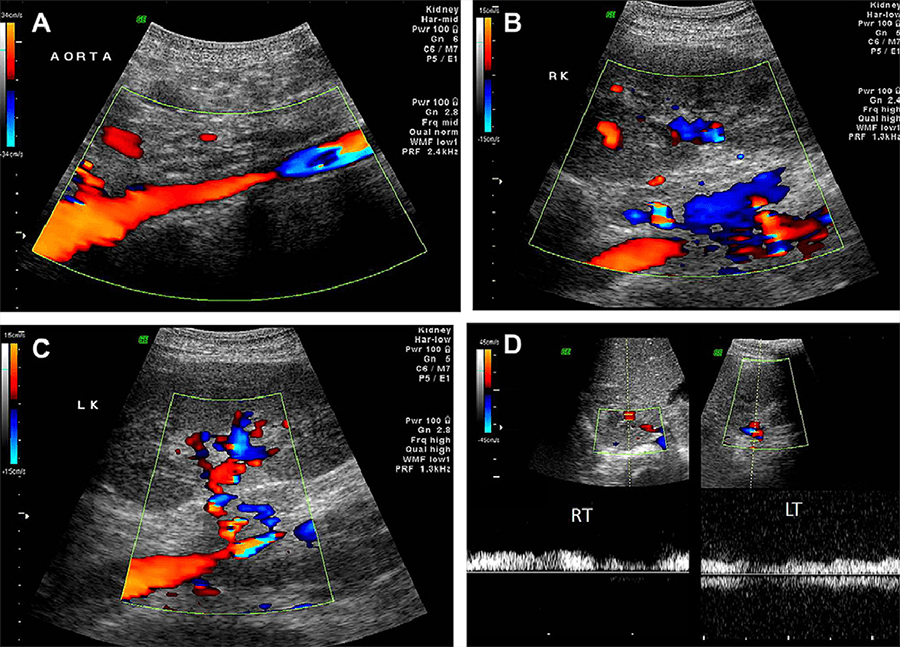
Большинство западных исследований отмечают низкую частоту артериита, как причину стеноза почечной артерии (в диапазоне от 10% до 20%), но в развивающихся странах, это заболевание составляет значительную часть. Неопубликованные данные 2008 года из центра, где работает автор, говорят о том, что артериит составляет более чем одну треть РВГ в педиатрической популяции. Сообщается, что это аортоартериит является основной причиной реноваскулярной патологии в группе детей, у которых диагностирована злокачественная гипертензия. Артериит встречается чаще у детей и молодых взрослых. На начальном этапе острое воспаление может приводить к утолщению стенок и локальному расширению аорты, но на поздних стадиях, фиброзное уплотнение приводит к локальному стенозу, который обычно включает в себя аорту и область формирования почечных артерий. Последствия заболевания с резидуальным фиброзным стенозом могут быть неотличимы от остиального сужения аорты или почечной артерии, которое вызвано заболеваниями аномалий развития. Артериит очень часто вызывает двустороннюю РВГ. Хотя туберкулез был выявлен в качестве этиологического фактора в некоторых случаях, в значительной части, причина воспаления не является очевидной. Неспецифический артериит – патология, которая часто самостоятельно ограничивается, и прогрессирование поражения стабилизируется на некотором этапе. Отсюда следует, что метод простой баллонной ангиопластики может быть эффективным в этих случаях, и установка стентов считается излишней (рис. 10 и 11).
Рис. 10. 8-летний мальчик, поступил с болью в животе с 6 месяцев. Недавно у него развилась тяжелая гипертония. (А) Среднесагиттальное цветное допплеровское сканирование выявило локальную дилатацию брюшной аорты (стрелки). (В) Поперечное цветное допплеровское сканирование показывает остиальный стеноз обеих почечных артерий. Высокая скорость турбулентного потока обозначена наложением и мозаичной картиной в обеих почечных артериях. Импульсная допплерография правой и левой почечных артерий показывает ПСС более чем 300 см/сек, RAR – 4.0. (С) Аортограмма подтверждает веретеновидную сегментарную дилатацию аорты и остиальный стеноз обеих почечных артерий (стрелки), что характерно для ранних стадий аорто-артериита.
Рис. 11. 15-летняя девочка с аортоартериитом, который вызывает тяжелую артериальную гипертензию. Правая почка – 7.6 см и левая почка – 8,2 см. Диагностировано увеличение эхогенности паренхимы 1 степени. (А) Выявлено утолщение стенки аорты со значительным аортальным стенозом. Цветная допплерография демонстрирует высокую скорость наложения сразу за зоной стеноза. Соотношение A/B в аорте – 4,0, что указывает на 70% – 80% стеноз. (B, C) Цветные допплеровские изображения в коронарной плоскости через почки выявляют полную облитерацию почечных артерий и наличие коллатеральных артерий, которые кровоснабжают обе почки. (D) Спектральный допплеровский сигнал во внутрипочечных артериях обеих почек выявляет непульсирующий, значительно ослабленный кровоток от коллатералей.
НЕЙРОФИБРОМАТОЗ И MIDAORTIC СИНДРОМ
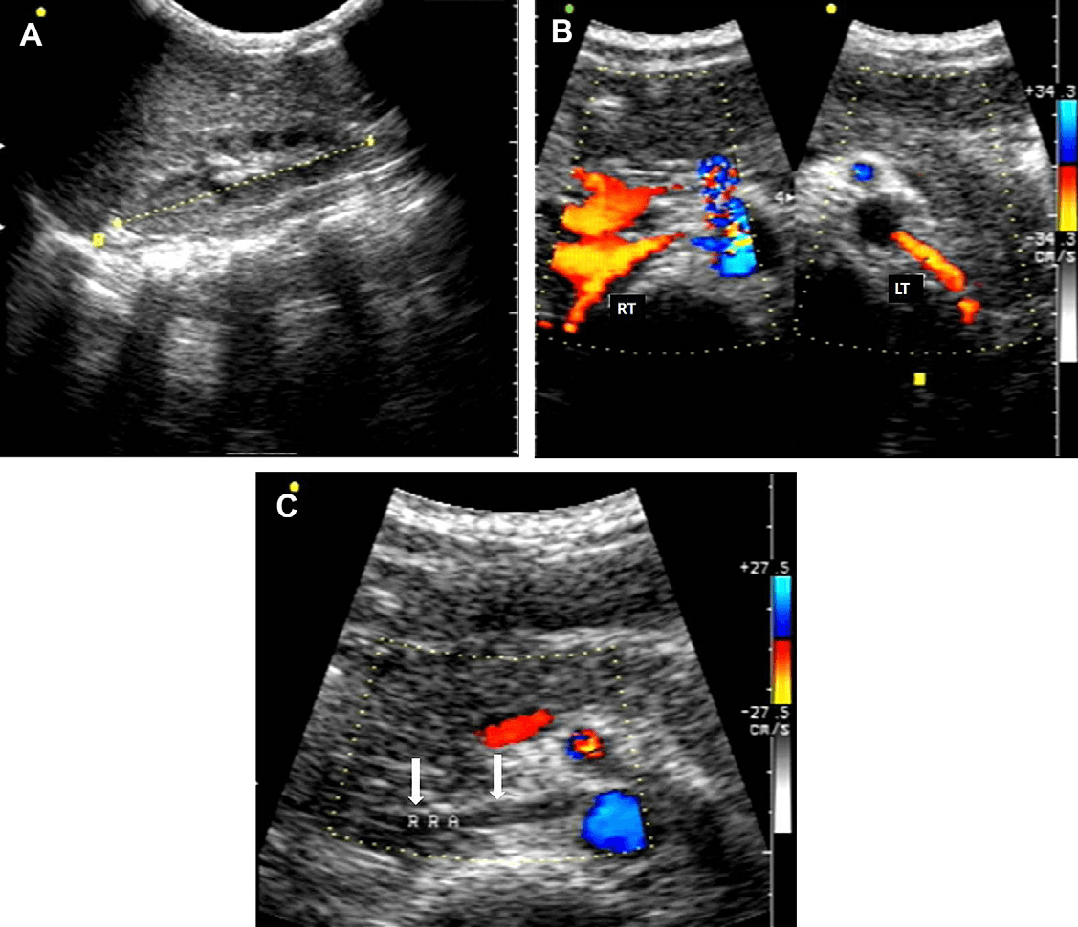
Развитие стеноза почечной артерии является сложным патологическим процессом, который поражает среднюю оболочку артерии со вторичной фиброплазией интимы. Артериальное сужение часто неотличимы от стеноза, который вызван другими заболеваниями. Половина пациентов имеет утолщение стенки аорты, что приводит к остиальному стенозу почечных артерий. В серии из 162 операций по поводу реноваскулярной патологии, патология аномалий развития была описана Stanley и его коллегами в 80% (рис. 12). Коарктация аорты, синдром Уильяма и радиационное поражение аорты и почечных артерий являются другими редкими причинами, которые вызывают вазоренальную гипертензию.
Рис. 12. 12-летний мальчик с нейрофиброматозом и тяжелой артериальной гипертензией. (А) В правой почке продемонстрировано диффузное истончение паренхимы в ее нижней половине. (B) Одна правая почечная артерия имеет нормальный диаметр и нормальный кровоток. Спектральный допплеровский сигнал во внутрипочечной артерии в нижней части правой почки выявляет parvus-tardus сигнала (индекс ускорения [AI] – 2.2 и время ускорение [AT] – 97 мс). (С) Тщательный поиск, ниже визуализированной правой почечной артерии, показал окклюзию второй почечной артерии (стрелки).
ИССЛЕДОВАНИЯ ДЛЯ ВЫБОРА ЛЕЧЕНИЯ
Хирургическая реваскуляризация несет значительные риски. Не так давно развитие техники и широкая доступность оборудования сделали баллонную ангиопластику и установку стентов безопасными вариантами. Хотя частота технически успешных результатов при баллонной ангиопластике и стентировании является отличной и соответствует 95% – 98%, не все пациенты имеют в результате полное излечение гипертонии. Наиболее распространенной причиной неудач в улучшении показателей кровяного давления является завышение уровня стеноза до ангиопластики. Вполне возможно, что у некоторых пациентов с гипертонической болезнью, атероматозные бляшки, которые вызывают стеноз, развиваются позже в течение всей жизни. Поэтому наличие стеноза почечных артерий не обязательно является причиной гипертонии у пациента. Идеальным был бы тест, с помощью которого можно было бы оценить эффективность процедуры реваскуляризации для каждого пациента.
ИР отражает реакцию судов, следовательно, он может отражать характер необратимого патологического процесса. ИР более чем 0,80 прогнозировал неблагоприятный исход реваскуляризации у пациентов с РВГ в одном из исследований. Наоборот, когда ИР был меньше, чем 0,80, результаты лечение после ангиопластики или стентирования были превосходными. Эти прогностические результаты не повторялись в более поздних исследованиях, так как не было найдено никакого существенного различия в исходной группе пациентов с ИР более или менее чем 0.80.
Совсем недавно при ультразвуковой допплерографии и оценке соотношения ренина, пороговое значение ИР 0,80 не было эффективным при прогнозировании исхода реваскуляризации, но было установлено, что тяжелая РВГ с ИР менее 0,55 отвечает лучше, чем умеренная РВГ с высоким постстенотическим ИР. Таким образом, логичным есть тот факт, что пациенты с тяжелым стенозом, который приводит к почечной ишемии, но без обширного гломерулосклероза, будут лучше реагировать на реваскуляризацию, чем пациенты с умеренной ишемией, но длительным гломерулосклерозом. Это также объясняет, почему результаты процедуры реваскуляризации у детей и молодежи лучше, чем у пожилых людей.
КОНТРАСТНАЯ УЛЬТРАЗВУКОВАЯ ДОППЛЕРОГРАФИЯ
В настоящее время доступны данные об использовании ультразвуковых контрастных веществ при допплеровском исследовании почечных артерий. Усиление сигнала, которое вызывают контрастные вещества, повышает чувствительность и специфичность допплерографии в обнаружении стеноза почечных артерий. Сообщается об увеличении на 25% выявленного числа стенозов почечных артерий с использованием контрастных веществ, наряду со снижением времени исследования.
СТЕНОЗ ТРАНСПЛАНТАТА ПОЧЕЧНОЙ АРТЕРИИ
Стеноз почечной артерии трансплантата, как известно, вызывает тяжелую гипертензию и дисфункцию трансплантата. Если это остается незамеченными и не лечится, то в конечном счете приводит к потере трансплантата. Раннее выявление и своевременное вмешательство значительно повышает частоту сохранения трансплантата. Стеноз почечной артерии развивается в трансплантированной почке чаще от 3 месяцев до 2 лет после трансплантации. Различные сроки появления и расположения стеноза могут зависеть от основной причины. Ранний стеноз развивается в зоне анастомоза и, как правило, вторичный в результате травмы донорского органа или артерии реципиента во время операции. Позднее развитие стеноза вдали от анастомоза может быть вторичным, в результате атеросклеротического процесса.
Так как пересаженная почка и связанные с ней артерии размещены поверхностно, то они более легко поддаются ультразвуковому исследованию. Цветное допплерографическое обследование у пациентов после трансплантации выполняется сразу, без необходимости какой-либо подготовки. Обычно кровоток подвздошной и почечной артерии оценивается с помощью цветной и спектральной допплерографии, а ПСС измеряется в подвздошной артерии сразу проксимальнее зоны анастомоза, а в почечной артерии сразу за анастомозом. Точное измерение ПСС в трансплантате почечной артерии иногда вызывает технические трудности, особенно, когда существует артериальный перегиб. Это требует от оператора маневрирования датчиком для оптимального размещения, чтобы достичь хороший угол атаки, а вместе с ним точный угол при допплерографии для правильного измерения скорости. Эта проблема является основной причиной диапазона нормальных ПСС для почечной артерии трансплантата. Нормальная ПСС в проксимальном отделе почечной артерии трансплантата колеблется между 80 и 180 см/с. Интраренальные артерии исследуются для оценки структуры кровотока при постстенотических изменениях, таких как волны по типу тardus-parvus. AI и AT также измеряются стандартно.
Диагноз стеноза почечной артерии трансплантата ставится путем использования аналогичных допплеровских параметров, как и для нативных почечных артерий. Различные критерии использовались различными исследователями для диагностики стеноза. Baxter и др. использовали ПСС – 250 см/с; Loubeyre и др. предложил ПСС – 180 см/сек, а в последнее время de Morais и др. пришли к выводу, что ПСС почечной артерии трансплантата более чем 200 см/с, является наиболее точным значением (рис. 13).
Рис.13. 18-летний реципиент с трансплантатом с тяжелой артериальной гипертензией через 3 месяца после пересадки. (Цветное допплеровское сканирование показало очень короткую основную почечную артерию с ранней бифуркацией). Цветовое наложение и цветная мозаичность в двух ветвях указывают на значительный стеноз в бифуркации. (В) Спектральный допплеровский сигнал в двух основных ветвях показали очень высокую скорость (пиковая систолическая скорость [PSV]> 280 см/с) турбулентного потока. (С) Спектральный допплеровский сигнал в сегментарных ветвях в верхней и нижней части пересаженной почки показал заметное снижение сигналов кровотока.
СЛУЧАЙНО ОБНАРУЖЕННЫЙ СТЕНОЗ ПОЧЕЧНОЙ АРТЕРИИ
Не редкость для кардиологов и радиологов – найти стеноз почечной артерии при выполнении коронарной или периферической ангиографии. Так как атеросклероз является медленно прогрессирующим заболеванием, при документальном подтверждении поражения существует реальная вероятность прогрессирования поражения со временем. Атеросклеротический стеноз почечной артерии, как сообщается, прогрессирует где-то на 7% в год с учетом того, что это может в итоге привести к терминальной почечной патологии. В большом исследовании было выявлено 33% случаев значимых случайно выявленных стенозов почечной артерии у пациентов при ангиографии по поводу хронической ишемии при патологии периферических артерий. Ни у одного из этих пациентов, однако, не развилась терминальная стадия почечной патологии при наблюдении в течение 10 лет, что ставит вопрос над необходимостью агрессивного интервенционного лечения при обнаружении стеноза почечной артерии. При ретроспективном анализе пациентов, которым случайно был выявлен стеноз почечной артерии во время коронарной ангиографии, и которые подверглись стентированию почечных артерий, не было выявлено ни пользы, ни вреда от процедуры. Доказательства, имеющиеся в настоящее время – не в пользу агрессивной тактики стентирования каждого стеноза почечной артерии, обнаруженного случайно во время периферической или коронарной ангиографии. Аналогичная ситуация имеет место и с распространением спиральной КТ и магнитно-резонансной томографии (МРТ), при которых легкие или умеренные стенотические поражения почечной артерии выявляются случайно. Необходимо проявлять некоторую сдержанность и действовать рассудительно, для того, чтобы полностью оценить каждый случай индивидуально, прежде чем подвергать все эти изменения ангиографии и стентированию.
МОНИТОРИНГ ПОСЛЕДУЮЩЕЙ РЕВАСКУЛЯРИЗАЦИИ
Допплерография является отличным методом визуализации для мониторинга пациентов после баллонной ангиопластики, размещения стентов или сосудистой хирургии. Скоростной турбулентный поток в зоне стеноза исчезает после восстановления нормального диаметра просвета, а пиковая систолическая скорость возвращается в пределы нормального диапазона. Аналогичным образом tardus-parvus сигнал во внутрипочечных артериях возвращается к нормальному резкому систолическому ускорению после успешного устранения стеноза. Новое появление высокой скорости, турбулентного потока в главной почечной артерии или внутрипочечный tardus-parvus сигнал указывает на рестеноз.
РЕЗЮМЕ
Цветная допплерография является отличным скрининговым методом для диагностики РВГ. Эта методика является одним из самых сложных методов ультразвуковых исследований. Тем не менее, с опытом и мастерством можно выполнять обследование у большинства пациентов на достаточном техническом уровне. Технология ультразвукового оборудования и опыт оператора постоянно улучшаются последние десятилетия. С развитием методики двойного доступа для визуализации интраренальных артерий вместе с основными почечными артериями, значительно снизилось количество неудачных исследований и улучшилась общая точность исследования. Преимущество допплерографии по сравнению с другими методами визуализации заключается в том, что этот метод неинвазивный, недорогой, легкодоступный и обеспечивает как физиологической, так и анатомической информацией. Идеальные допплеровские параметры для диагностики значимого стеноза почечной артерии являются: ПСС – более чем 1,8-2,0 м/с в основной почечной артерии и почечно-аортальное соотношение более 3,0. Интраренальные параметры АI – менее 3,0 и АТ – более 70 миллисекунд. Соотношение ПСС почечной артерии к междолевой артерии более чем 5 и ПСС междолевой артерии менее 15 см/с являются дополнительными интраренальными допплеровскими критериями. В будущем наличие ультразвуковых контрастных веществ обещает улучшить чувствительность и специфичность допплеровского ультразвукового исследования в выявлении стеноза почечных артерий. Тем не менее, необходимо иметь ввиду, что визуализация стенотического поражения не всегда означает, что он является единственной причиной гипертонии у пациента. У некоторых пациентов стеноз и вторичная гипертензия протекают легко и стабильно. Эта ситуация легко контролируется медикаментозным лечением. У других пациентов даже использование трансстенотического измерения градиента давления и определения ренина при заборе крови из почечной вены не гарантирует полностью благоприятный результат. Диагностику и варианты лечения всегда следует оценивать с точки зрения клинического поведения болезни. Для проведения исследований рекомендуем использовать аппарат от компании GE Voluson E8.