Авторы: Yuichi Takano, Jun Noda, Masataka Yamawaki, Tetsushi Azami, Takahiro Kobayashi, Fumitaka Niiya, Naotaka Maruoka, Tomoko Norose, Nobuyuki Ohike, Tetsuji Wakabayashi, Kenichi Matsuo, Kuniya Tanaka, Masatsugu Nagahama
Содержание:
- Введение
- Материалы и методы
- Метод биопсии
- Определение нежелательных явлений (включая степень тяжести)
- Результаты
Введение
В последние годы произошли заметные успехи в диагностической визуализации, и в результате большинство опухолей печени можно диагностировать без патологического обследования. Поскольку биопсия печени сопряжена с риском кровотечения и посева игольного тракта, гистологическое исследование не является необходимым в случаях, которые можно диагностировать с помощью визуализации или при подозрении на злокачественное новообразование и назначении операции. Однако в некоторых случаях все еще требуется гистологическая оценка, в том числе при атипичных результатах визуализации, опухолях, в которых трудно различить доброкачественные и злокачественные образования, и метастатических опухолях печени в случаях с множественными злокачественными новообразованиями.
Чрескожная биопсия под контролем УЗИ часто выполняется с высокой диагностической точностью. Однако понятие биопсии опухоли печени с помощью тонкоигольной аспирации под эндоскопическим ультразвуковым контролем (EUS-FNA) было впервые введено в 1999 г.. EUS-FNA показана при небольших опухолях печени или при затруднении биопсии другими методами. Однако ни одно исследование не сравнивало эти два метода биопсии, и в некоторых случаях выбор метода биопсии может быть затруднительным в клинической практике.
Материалы и методы
Ретроспективное исследование было проведено с использованием медицинских карт пациентов, перенесших биопсию опухоли печени в нашей больнице с 2012 по 2019 год. Случаи были разделены на две группы для сравнения: группа чрескожной биопсии под ультразвуковым контролем (чрескожная группа) и эндоскопической тонкоигольной аспирации под ультразвуковым контролем (EUS-FNA группа). Решение о проведении чрескожной биопсии или EUS-FNA принималось врачом.
Перед биопсией были выполнены УЗИ брюшной полости и компьютерная томография (КТ). Чрескожная биопсия была выполнена пациентам, у которых поражения можно было легко визуализировать с помощью УЗИ брюшной полости. Напротив, EUS-FNA была выбрана для случаев, когда было трудно визуализировать поражения с помощью УЗИ брюшной полости, а также для опухолей, расположенных вблизи желудочно-кишечного тракта (желудка или двенадцатиперстной кишки).
Были изучены клинический фон, процедура биопсии, диагностические возможности и побочные эффекты. Определение злокачественного – это «случай с гистологически злокачественными признаками», а доброкачественными – случаи с «гистологически доброкачественными результатами и отсутствием роста опухоли даже после одного года наблюдения».
Исследование проводилось с разрешения Комитета по этике Университета Сева.
Метод биопсии
Чрескожная биопсия была выполнена с использованием анальгетика (пентазоцин 15 мг), и опухоль печени была визуализирована с помощью УЗИ брюшной полости. На коже делали небольшой разрез скальпелем, и опухоль прокалывалась 1-2 раза пункционной иглой 16-G tru-cut.
EUS-FNA проводилась путем введения анальгетиков и седативных средств (петидина гидрохлорид 35 мг или пентазоцин 7,5-15 мг + мидазолам 2-5 мг). Использовались эндоскоп GF-UCT260 (Olympus Medical Systems, Токио, Япония) и устройство наблюдения UE-ME1 или UE-ME2 (Olympus Medical Systems). Диаметр иглы для пункции составлял 19-25 G и выбирался на усмотрение врача. Количество ходов составляло 10-20, а давление всасывания составляло 10-20 см3 отрицательного давления. Быстрая оценка цитологии на месте не проводилась ни в одной из групп. Чрескожная биопсия печени была выполнена 4 врачами, каждый из которых имел опыт более чем 30 случаев. EUS-FNA была проведена 3 эндоскопистами с опытом работы с более чем 50 случаями.
Определение нежелательных явлений (включая степень тяжести)
Использовалось определение нежелательных явлений, установленное на семинаре Американского общества гастроинтестинальной эндоскопии (ASGE). В этом исследовании боль была определена как «боль, требующая применения анальгетиков в течение 24 часов после процедуры».
Статистический анализ
Статистический анализ проводился с использованием t-критерия Стьюдента и критерия chi-square для сравнения двух групп, и значения p <0,05 считались показывающими статистически значимую разницу.
Результаты
Всего было включено 106 пациентов (47 в группе чрескожной и 59 в группе EUS). Средний возраст пациентов составлял 68 (от 32 до 87) лет, из них 60 были мужчинами, а 46 – женщинами. В общей сложности 100 пациентам был поставлен окончательный диагноз злокачественного новообразования, включая метастатическую опухоль печени в 45 случаях и следующие первичные опухоли:
- рак поджелудочной железы, 10 случаев;
- колоректальный рак – 9 случаев;
- рак легких – 7 случаев;
- рак груди – 5 случаев;
- рак желчного пузыря – 3 случая;
- рак пищевода – 2 случая;
- рак желудка – 2 случая;
- нейроэндокринная опухоль поджелудочной железы – 2 случая;
- нейроэндокринная карцинома поджелудочной железы – 1 случай;
- почечно-клеточный рак – 1 случай;
- колоректальная нейроэндокринная опухоль – 1 случай;
- рак яичников – 1 случай;
- стромальная опухоль тонкой кишки – 1 случай.
Кроме того, было 32 случая холангиоцеллюлярной карциномы, 18 случаев гепатоцеллюлярной карциномы, 4 случая злокачественной лимфомы и 1 случай лейомиосаркомы. В общей сложности 6 пациентам был поставлен окончательный диагноз доброкачественной опухоли, включая два случая абсцесса печени, один случай фокальной узловой гиперплазии, один случай воспалительной псевдоопухоли, один случай саркоидоза печени и один случай некротической ткани.
Сравнение процедуры биопсии между двумя группами
| Показатель | Чрескожная группа (n = 47) | Группа EUS (n = 59) |
| Игла | 16G во всех случаях | 19G: 5%, 22G: 61%, 25G: 34% |
| Диаметр поражения, средний диапазон | 62 мм (12-167) | 34 мм (6-170) |
| Поражения правой доли | 70% (33/47) | 28% (17/59) |
| Поражения левой доли | 30% (14/47) | 64% (38/59) |
| Поражения хвостатой доли | 0% | 7% (4/59) |
| Иммуноокрашивание | 74% (35/47) | 68% (40/59) |
| Длина образца, средний диапазон | 9,7 мм (3,1-14,4) | 3,3 мм (1,1-6,8) |
Рисунок 1: a: КТ брюшной полости с контрастным усилением показала большую опухоль с кистозной дегенерацией в хвосте поджелудочной железы и небольшими метастазами в печени в хвостатой доле (стрелка). Поскольку диссеминация и инфекция в результате биопсии опухоли поджелудочной железы вызывали опасения, мы решили провести биопсию метастазов в печени. b: УЗИ брюшной полости выявило неясную опухоль в хвостатой доле (стрелка). В этом случае чрескожная биопсия была затруднена. c: Опухоль печени в хвостатой доле легко визуализировалась с помощью EUS (стрелка), а EUS-FNA выполнялась с помощью иглы 22-G. d: Патологическим диагнозом была аденокарцинома, соответствующая метастазу рака поджелудочной железы, и была начата химиотерапия. Ad: аденокарцинома, H: гепатоцит (окрашивание гематоксилином и эозином, × 400)
Рисунок 2: а: Случай с раком яичников, раком щитовидной железы и колоректальным раком в анамнезе. Компьютерная томография брюшной полости выявила опухоль размером 30 мм в 6 сегменте печени. Требовалось гистологическое исследование для идентификации первичной опухоли, которая дала начало метастазам. b: Гиперэхогенная опухоль четко визуализировалась при УЗИ брюшной полости. Выполнена чрескожная биопсия. c: Обнаружена аденокарцинома с веретеновидными ядрами. Пациенту поставлен диагноз: метастаз колоректального рака в печень. Ad: аденокарцинома, H: гепатоцит (окрашивание гематоксилином и эозином, × 400)
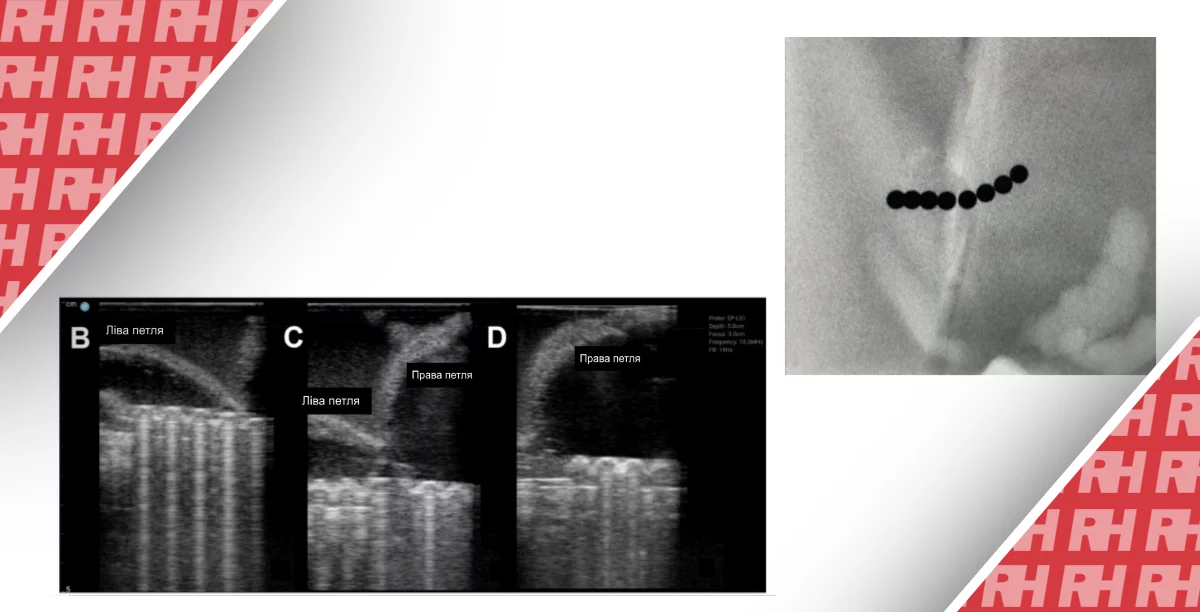
Рисунок 3: a: КТ брюшной полости выявила опухоль неправильной формы размером 30 мм в 8 сегменте печени. Перед печенью располагалась восходящая и поперечная ободочная кишка (синдром Чилайдити). Гистологическое исследование потребовалось для химиотерапии, потому что пациентка отказалась от операции. b: Было трудно визуализировать опухоль из-за наличия газов в желудочно-кишечном тракте (стрелка) на УЗИ брюшной полости. c: EUS смогла визуализировать опухоль (стрелка) без воздействия желудочно-кишечного газа. EUS-FNA выполняли из луковицы двенадцатиперстной кишки. d: У пациента диагностирована внутрипеченочная холангиоцеллюлярная карцинома. Ad: аденокарцинома, H: гепатоцит (окрашивание гематоксилином и эозином, × 400)
Пункционные иглы, использованные в группе чрескожных вмешательств, были Tru-Cut типа 16-G во всех случаях, а иглы, использованные в группе EUS, были иглами 19-G в 5% (3 случая), 22-G в 61% (36 случаев), и 25-G в 34% (20 случаев).
Средний диаметр поражения составлял 62 (диапазон 12–167) мм в группе чрескожного введения, но был значительно меньше (34 мм; диапазон 6–170 мм) в группе EUS (p <0,01). В чрескожной группе локализация поражений составила 30% (14 случаев) в левой доле и 70% (33 случая) в правой доле. В группе EUS локализация очагов составила 64% (38 случаев) в левой доле, 28% в правой доле (17 случаев) и 7% (4 случая) в хвостатой доле. В чрескожной группе было больше опухолей правой доли, в то время как в группе EUS было больше опухолей левой доли (p <0,01). EUS-FNA выполнялась как трансжелудочная пункция в 72% случаев и как трансдуоденальная пункция в 28% случаев.
Иммуноокрашивание было выполнено в 74% (35/47) в группе чрескожного введения и в 68% (40/59) в группе EUS, при этом значительных различий не выявлено. Иммуноокрашивание проводилось по усмотрению патологоанатома. Таким образом, иммуноокрашивание не проводилось в случаях, которые можно было диагностировать только с помощью окрашивания гематоксилин-эозином.
Средняя длина образца составляла 9,7 (диапазон 3,1–14,4) мм в группе чрескожной биопсии и 3,3 (диапазон 1,1–6,8) мм в группе EUS; Таким образом, образцы были значительно длиннее в группе чрескожной биопсии (p <0,05). Область воротной вены не могла быть оценена из-за большого количества случаев злокачественных опухолей, так как иногда область воротной вены замещалась опухолевой тканью.
Диагностическая способность и нежелательные явления
| Показатель | Чрескожная группа (n = 47) | Группа EUS (n = 59) |
| Чувствительность | 95% (43/45) | 100% (55/55) |
| Специфичность | 100% (2/2) | 100% (4/4) |
| Точность | 96% (45/47) | 100% (59/59) |
| Нежелательные явления | 17% (8/47) | 2% (1/59) |
Рисунок 4: а: УЗИ брюшной полости показывает многочисленные гипоэхогенные образования в печени. При оценке всего тела не удалось выявить каких-либо явных первичных поражений, и перед химиотерапией была проведена чрескожная биопсия печени. У больного диагностирована внутрипеченочная холангиоцеллюлярная карцинома. В этом случае антитромботический препарат не принимался, количество тромбоцитов и коагуляционная способность были в норме. b: На следующий день после биопсии пациент пожаловался на боль в животе, у него было снижение артериального давления и тахикардия. Наблюдалось снижение гемоглобина в крови (с 9,5 до 6,8 г / дл), было выполнено переливание крови. Компьютерная томография с контрастным усилением показала экстравазацию на поверхности печени (стрелка). c: Ангиография показала экстравазацию от периферии правой печеночной артерии (стрелка), и была выполнена транскатетерная артериальная эмболизация.
Чрескожная биопсия показала, что 43 случая были злокачественными, а 4 случая доброкачественными. В двух из четырех доброкачественных случаев опухоль исчезла самопроизвольно, и диагноз не изменился; однако в оставшихся двух случаях опухоль увеличилась в размерах, и снова была проведена чрескожная биопсия. В обоих случаях была выявлена аденокарцинома, диагноз был изменен с доброкачественного на злокачественный.
EUS-FNA диагностировала 55 случаев как злокачественные и 4 случая как доброкачественные. В четырех доброкачественных случаях опухоли не наблюдались даже после одного года наблюдения, и диагноз не изменился.
Чувствительность, специфичность и точность процедуры составляли 95%, 100% и 96% в группе чрескожного введения и 100%, 100% и 100% в группе EUS, соответственно, не показывая существенной разницы.
Нежелательные явления были зарегистрированы в 17% случаев чрескожной терапии [легкая боль в 6 случаях, умеренное кровотечение в 1 случае (проведено переливание крови и интервенционная радиология), легкая инфекция в 1 случае], при этом значительно меньшая частота была зарегистрирована в группе EUS ( 2%; слабая боль в 1 случае; p <0,01). Средний период наблюдения составил 3,4 (диапазон 0,3-7) лет в группе чрескожного введения и 2,5 (диапазон 0,6-5) лет в группе EUS; случаев диссеминации игольного тракта не наблюдалось.