🤖 Краткий пересказ от ИИ
Неалкогольная жировая болезнь печени (НАЖБП) требует эффективных методов ранней диагностики для предотвращения прогрессирования цирроза. В данном исследовании предложен и протестирован новый диагностический метод, основанный на акустическом количественном анализе структуры (ASQ) и параметре «соотношение фокального искажения» (FD-ratio) с использованием УЗИ.
Исследование показало, что FD-ratio демонстрирует значительную отрицательную корреляцию с площадью и размером жировых включений в печени, что подтверждает его потенциал как количественного биомаркера стеатоза. Этот метод может дополнить диагностические возможности УЗИ аппаратов, таких как Toshiba Aplio XG.
✅ Ключевые тезисы из статьи:
- Диагностика: Метод ASQ с FD-ratio может использоваться для количественной оценки стеатоза печени.
- Лечение: Ранняя диагностика НАЖБП важна для своевременного вмешательства и предотвращения цирроза.
- Преимущества: УЗИ, в отличие от КТ и МРТ, является неинвазивным, недорогим и безопасным для многократного использования.
- Ограничения: Диагностическая точность традиционного УЗИ зависит от оператора, что указывает на потребность в более объективных количественных методах.
Последнее обновление: 22 июля 2025 р.
Экспертная проверка: Материал проверен и отредактирован экспертами RH.ua
Примечание об ИИ: Этот блок создан с помощью генеративного ИИ для быстрого ознакомления с основными идеями статьи. Для полного понимания темы рекомендуем прочесть полный текст.
⚠️ Не заменяет медицинскую консультацию
Hidekatsu Kuroda, Keisuke Kakisaka, Naohisa Kamiyama, Takayoshi Oikawa,
Mio Onodera, Kei Sawara, Kanta Oikawa, Ryujin Endo, Yasuhiro Takikawa, Kazuyuki Suzuki
Резюме
Цель. Протестировать на дефицитных по лептину мышах с ожирением (ob/ob) и разными степенями стеатоза печени новый диагностический метод, используя акустический количественный анализ структуры (ASQ) и ассоциированный с ним аналитический параметр «соотношение фокального искажения» (FD-ratio, focal disturbance ratio).
Методы. Девять мышей с ожирением (ob/ob) на 5, 8 и 12 неделях жизни (n=3 в каждой возрастной группе) использовали для моделирования стеатоза печени. Эхо-сигналы полученные при УЗИ анализировались с помощью ASQ, который делает статистический анализ эхо-амплитуд для оценки негомогенности в исследуемой области. Предметом данной работы было вычисление FD-ratio. FD-ratio, области жировых включений и их размеры сравнивались между групами.
Результаты. В группах не наблюдалось фиброза и воспаления. Области жировых включений значительно (P<0.01) увеличивались с возрастом: 1,25% ± 0,28% в 5 недель, 31,07% ± 0,48% в 8 недель, 51,69% ± 3,19% в 12 недель. Среднее значение размера жировых включений также значительно (P<0.01) увеличивалось с возрастом: 1,33 (0,55-10,52) мкм в 5 недель, 2,82 (0,61-44,13) мкм в 8 недель и 6,34 (0,66-81,83) мкм в 12 недель. Среднестатистическое значение FD-ratio составляло 0,42 ± 0,11 в 5 недель, 0,11 ± 0,05 в 8 недель и 0,03 ± 0,02 в 12 недель. Наблюдалась значительная негативная корреляция между FD-ratio и либо площадью жирового включения (r = -0.7211, P = 0.0017) или его размером (r = -0.9811, P = 0.0052).
Вывод. Этот инструмент для статистического анализа сигналов при УЗИ, что использует FD-ratio, может применяться для точного определения количества жира in vivo в животной модели стеатоза печени, и может служить как количественный биомаркер стеатоза печени.
ВВЕДЕНИЕ
Неалкогольная жировая болезнь печени (НАЖБП) – это клинически важное заболевание, которое возникает у людей с такими предрасполагающими заболеваниями как ожирение или инсулинорезистентность, и часто сопровождается метаболическим синдромом, который включает диабет, гиперлипидемию и/или гипертензию. Неалкогольный стеатогепатит (НАСГ) самая тяжелая форма НАЖБП, и считается основной причиной цирроза печени неизвестного происхождения. Методы ранней диагностики и оценки НАЖБП, путем количественного измерения стеатоза, необходимы для более раннего вмешательства, и для предотвращения прогрессирования цирроза.
Золотым стандартом для количественной оценки стеатоза считается гистологический анализ печени (биопсия). Однако, биопсия печени имеет различные недостатки, такие как потенциальные ошибки при заборе биоптатов, трудности повторной процедуры из-за этических проблем и осложнений (кровотечение). Поэтому, необходимо разрабатывать альтернативные неинвазивные методы диагностики.
Недавно стали широко использоваться для количественного анализа стеатоза несколько неинвазивных методов, таких как УЗИ, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). Однако, повторное обследование пациентов с НАЖБП проводить тяжело потому, что при КТ пациент получает дозу облучения, а МРТ дорого стоит. Исходя из этого, УЗИ является отличным методом диагностики, поскольку обладает минимальной инвазивностью, недорого стоит, а повторное его использование не вредит здоровью пациента. Более того, УЗИ высокочувствительное в определении жировых накоплений в печени. Однако, диагностическая способность УЗИ зависит от умений оператора, а качественные методы диагностирования липогенеза в печени еще не открыты.
За последние годы, Yamaguchi et al. сообщили, что диффузные патологические изменения в ткани печени можно оценить качественно на основании статистического отклонения ультразвуковых сигналов по сравнению со здоровой печенью. В основном, ультрасонографические изображения паренхиматозных органов, таких как печень имеют картину «спекл-структуры» (speckle pattern), которая состоит из множества маленьких эхо крапинок. Спекл картина образуется ультразвуковой интерференцией рассеянных ультразвуковых волн, которые вызваны бесчисленным количеством отражающих объектов. Анализ изображений спекл картин может применяться для идентификации характеристик тканей печени, при хронических заболеваниях потому, что картина меняется, зависимо от структурных характеристик среды. Один из таких методов – функция плотности вероятности (probability density function – PDF) эхо-амплитуд спекл картины, которая, как описано в литературе, аппроксимируется функцией распределение Рэлея (Rayleigh distribution). Toyoda et al. предложили акустический количественный анализ структуры (ASQ), и сообщили о возможности квантификации диффузных заболеваний печени или мониторинга регрессии/прогрессирования фиброза во время лечения. Однако, еще не публиковали работ, в которых бы описали возможность оценки стеатоза печени у пациентов с НАЖБП используя этот инструмент для статистического анализа ультразвуковых сигналов.
Данная работа нацелена подтвердить возможности метода количественной визуализации, который применяется для определения и измерения стеатоза со статистической информацией от эхо-сигналов с «соотношением фокального искажения» (FD-ratio). Как истинную модель НАЖБП мы испольовали дефицитных по лептину мышей с ожирением (ob/ob).
МАТЕРИАЛЫ И МЕТОДЫ
Это исследование – совместный труд Медицинского Университета Ивате и Toshiba Medical Systems. Но, прямой финансовой поддержки от Toshiba Medical Systems небыло.
Животные
Протоколы исследований на животных были одобрены центром исследований на животных нашего учреждения. Девять самцов мышей (ob/ob) пяти недельного возраста (в начале исследования) были куплены в Charles River Laboratories (Yokohama, Japan). Во время эксперимента их держали на обычной диете. Мышей поделили на три группы (n=3 в каждой), и каждая из них прошла эксперимент, которий описан ниже, на 5, 8 и 12 неделях жизни, соответственно.
В общий наркоз мышей вводили путем внутрипариетального введения 40-50 мг/кг пентобарбитала натрия (Ovation Pharmaceutical, Deerfield, IL). Далее, провели интраоперационное УЗИ до того, как удалить печень для гистологического исследования.
Ультразвуковое исследование
Для ультразвукового исследование в этой работе использовали УЗ аппарат Aplio XG (Toshiba Medical Systems, Otawara, Japan) вместе с линейным датчиком 12 МГц (PLT-1204BT). Режим сканирования – В-режим (T: 6.0/R: 12.0 МГц). Глубина и фокус изображения были постоянными: 15 мм и 7,5 мм. Поперечные срезы паренхимы печени фиксировались в цифровом виде с сырыми данными, которые состояли из линейных амплитуд без косметической обработки изображений. Сырые данные загрузили на компьютер в DICOM формате. FD-ratio вычисляли с помощью программного обеспечения ASQ (подробно расписанное в следующем разделе). Исследуемую область (ИО) установили на одной глубине – 2,5 мм от поверхности печени (Рис. 1). FD-ratio измеряли 10 раз подряд, и среднестатистическое число (после исключения резко отклоняющихся чисел) использовали как конечный результат. Параллельно, среднестатистическое число интенсивности эхо паренхимы печени измерялось программным обеспечением Image-J (NIH, USA).
Аналитический метод
Принципы метода ASQ заключаются в следующем. Когда эхо-сигналы генерируются от маленьких концентрированных разбросов, которые находятся за пределами пространственного разрешения, ультразвуковое изображение строится с интерференции звуковых волн (спекл шум). В таком случае, PDF эхо-амплитуд можно приблизительно вычислить за распределением Рэлея. В нормальной паренхиме печени, такие статистические результаты нельзя описать распределением Рэлея потому, что есть наличие таких структур, как сосудистые стенки. Результаты еще больше отдаляються от распределения Рэлея при наличие узлов, фиброза, т.е. цирроза. Мы подали гипотезу, что при прогрессивном увеличении жировых включений, эти разбросы будут генерировать интерференцию волн или будут маскировать оригинальные маленькие структуры, что приблизит PDF к распределению Рэлея.
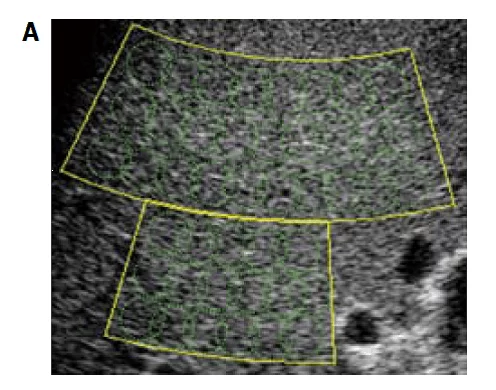
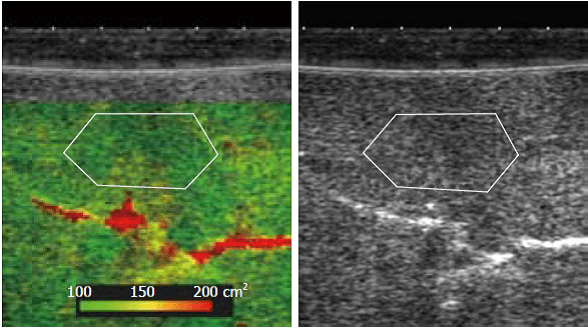
Рис. 1. ASQ. При параметрической визуализации, интенсивность распределения можно отображать на разделенном экране цветовой кодировкой. Большая исследуемая область находилась на фиксированной глубине 2,5 мм от поверхности печени.
Как только оператор выбирает всеобъемлющую ИО (далее большая-ИО) на изображении, несколько сотен маленьких ИО (далее маленькие-ИО) автоматически выставляются для того, чтобы вычислить PDF (Рис. 2А). Необходимый параметр Сm2 , в анализе обозначается этим уравнением:
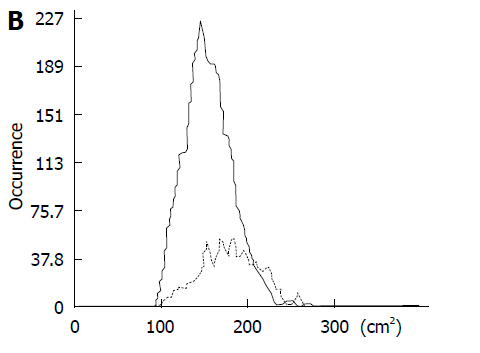
где µ и δ2 – среднестатистическое число и дисперсия эхо-амплитуд в маленькой-ИО, соответственно. δ2R(µ) является вариантом, когда распределение Рэлея вычисляется от среднестатистического числа. Результаты для маленьких‑ИО в большой-ИО выведены на гистограмме вхождения С2 (вещественная ось Рис. 2В). Если образцы состоят из спекл шума, С2 гистограмма сходится к 100 с узкой дисперсией, а структурная информация сделает среднестатистическое число больше, а дисперсию шире.
FD–ratio вычисляется следующим образом. Сначала, Сm2 обозначается как:
где δm дисперсия, вычисленая с образцов меньше µ+4δ. Если соотношение С2/Сm2 больше, чем предельное значение α, результат Сm2 исключается с гистограммы (вещественная ось), но добавляется к альтернативной гистограмме (пунктирная линия). FD–ratio– это соотношение площади ограниченной кривой (AUC) для этих двух гистограмм:
RFD =[AUC (real)]/[AUC (dotted)]
Рис. 2. Схематическое изображение исследуемых областей использованных для статистического анализа радиочастотного сигнала с помощью акустического количественного метода, и Сm2-гистограмма.
А: установленная большая ИО на самом деле состоит из нескольких сотен маленьких-ИО, которые используются для вычисления множества Сm2 (интенсивность или амплитуда) значений; В: результаты показаны как вхождение на Сm2 гистограмме.
Здесь, предельное значение α было 1,2, поэтому RFD= 0 когда образцы показывали распределение Рэлея для PDF, и имеет положительное значение в присутствие малейших структурных изменениях.
Программное обеспечение ASQ также имеет функцию визуализации, которая реконструирует двухмерное цветное изображение С2, измеренное для каждой позиции (параметрическое изображение).
Гистопатологический анализ
Гистопатологическое исследование проводил опытный патолог, сертифицированный Японским Сообществом Патологии. Снимки с биопсии печени записывались в JPEG формат. Используя Image–Jsoftware, процент жирных включений вычислялся за соотношением между общей площадью жировой ткани и общей площадью образца, а среднестатистическое число обозначало площадь жировых включений. Снова, используя Image–Jsoftware измеряли максимальный диаметр жировых включений в 8 и 12 недельных мышей, срединные числа использовались для обозначения размера включений. Таким образом полученые площадь и размер жировых включений, сравнивались с FD–ratio.
Статистический анализ
Значения выведены как среднестатистическое число ± стандартное отклонение, или медиана по распределению значений. Для статистического анализа использовалось StatViewsoftware (version 5.0$ SASInstitute, Cary, NC, USA). Тест ранговой корреляции Спирмена использовался для оценки корреляций между двумя переменными величинами, со значительной корреляцией Р<0.05, и коэффициентом корреляции r≥0.40. Критерий Туки-Крамера использовали для многократных сравнительных тестов, и значения Р<0.05 считались показателем значительной разницы.
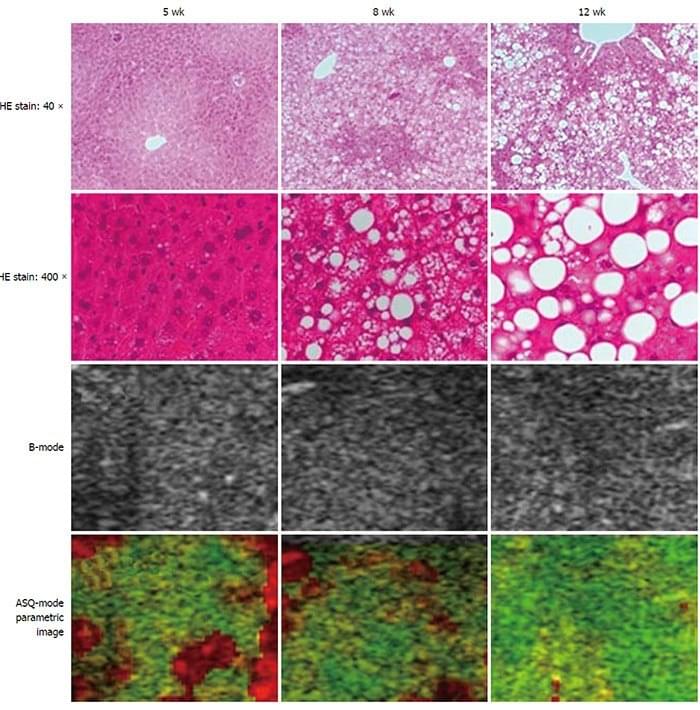
Рис. 3. Гистологические образцы, снимки акустическим количественным методом в В-режиме для каждой группы. Во всех исследуемых групах отсутствует фиброз и воспалительный процесс. Большие жировые включения в основном наблюдались в 12 недельных мышей. На параметрической визуализации, красный и зеленый цвета наблюдали вместе в мышей 5 недельного возраста. Далее, к 12 неделям, количество красного цвета уменьшилось, а зеленый стал доминировать.
РЕЗУЛЬТАТЫ
Сравнение гистологических данных и эхогенности печени
Во всех исследуемых групах не наблюдался фиброз и воспалительный процесс. В основном, большие жировые включения наблюдались у 12 недельных мышей (Рис. 3). Области жировых включений значительно (P<0.01) увеличивались с возрастом: 1,25% ± 0,28% в 5 недель, 31,07% ± 0,48% в 8 недель, 51,69% ± 3,19% в 12 недель. Срединное значение размера жирового включения также значительно (P<0.01) увеличивалось с возрастом: 1,33 (0,55-10,52) мкм в 5 недель, 2,82 (0,61-44,13) мкм в 8 недель и 6,34 (0,66-81,83) мкм в 12 недель. Среднестатистическое значение серых пикселей составляло 65,31 ± 22,52 в 5 недель, 65,95 ± 19,41 в 8 недель и 91,32 ± 21,83 в 12 недель (Рис. 5). Не наблюдалось значительной разницы между группами 5 и 8 недель, но среднестатистическое значение серых пикселей значительно возросло в 12 недельной группе, с увеличением яркости паренхимы печени.
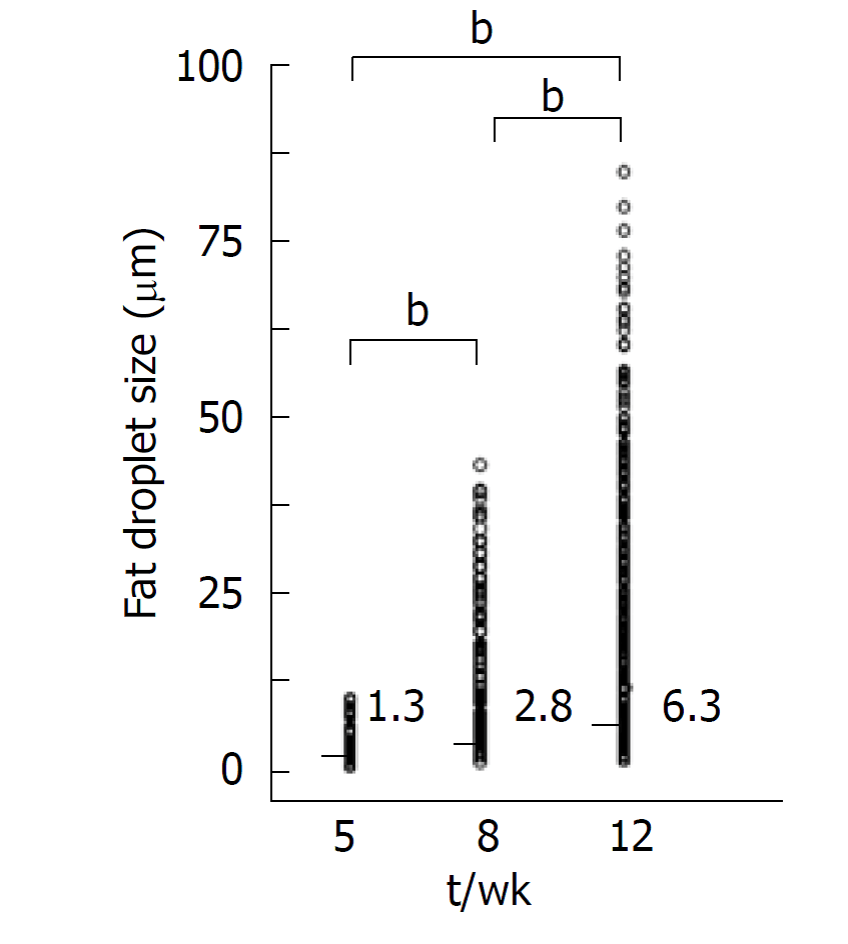
Рис. 4. Сравнение размеров жировых включений. Срединное значение размеров жировых включений значительно увеличивалось (bP<0.01) с возрастом:1,33 мкм (диапазон: 0,55-10,52 мкм) на 5 неделе, 2,82 мкм (диапазон: 0,61-44,13 мкм) на 8 неделе и 6,34 мкм (диапазон: 0,66-81,83 мкм) на 12 неделе.
Рис. 5. Сравнение эхогенности печени. Среднестатистическое значение серого в каждой группе составляло 65,31±22,52 в 5 недель, 65,95±19,41 в 8 недель и 91,32±21,83 в 12 недель. Не наблюдалось значительной разницы между группами 5 и 8 недель, но среднестатистическое значение серых пикселей значительно возросло в 12 недельной группе, с увеличением яркости паренхимы печени. bP<0.01 NS: не значительное.
Взаимоотношение FD–ratio и площади/размера жировых включений
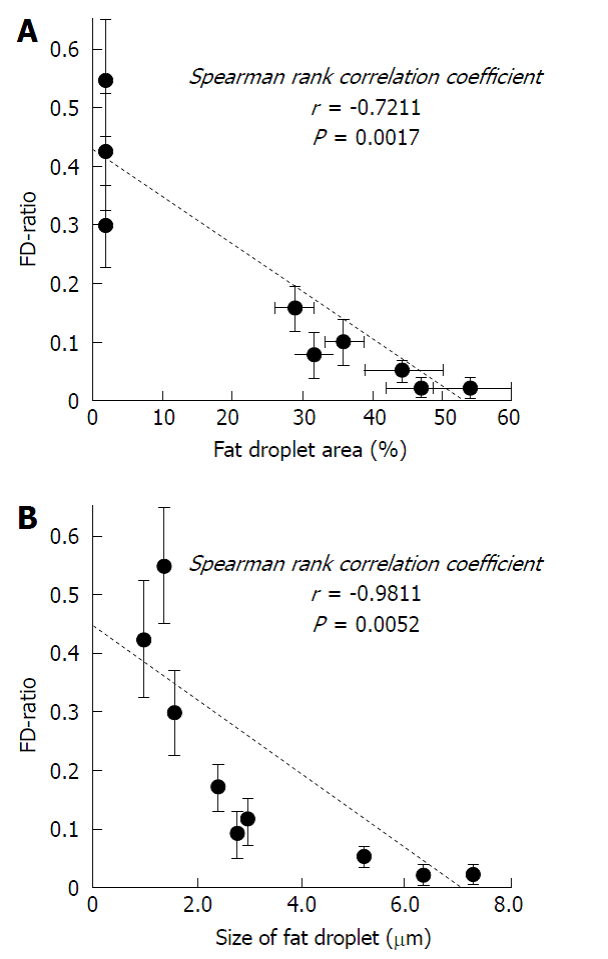
Среднестатистическое число FD–ratioсоставляло 0,42±0,11 в 5 недель, 0,11±0,05 в 8 недель и 0,03±0,02 в 12 недель. FD–ratio было значительно ниже в 12 недель, чем в 5 или 8 недель (P<0.01 для каждой). В параметрической визуализации красный и зеленый цвета были в примерно равном количестве в 5 недель, а в 12 недель стал доминировать зеленый цвет (Рис. 3). Значительная негативная корреляция наблюдалась между FD–ratio и площадью жирового включения (r = -0.7211, P = 0.0017) (Рис. 6А) или размером жирового включения (r = -0.9811, P = 0.0052) (Рис. 6В).
ОБСУЖДЕНИЕ
Результаты исследования продемонстрировали близкую корреляцию между FD–ratio и степенью жирового накопления в печени (гистологическая оценка). Эти данные показывают, что ASQ анализ УЗИ печени и его представительный параметр, FD–ratio, может выступать, как новый надежный клинический метод для оценки стеатоза печени.
Что касается УЗИ жировых болезней печени, Josephetal поддерживают яркую картину печени, и, следовательно, предлагают квантифицировать гепатоспленический или гепаторенальный контраст.
Рис. 6. Взаимоотношение между «соотношением фокального искажения» и площадью/размером жирового включения. А: значительные негативные корреляции наблюдались между соотношением фокального искажения (FD–ratio) и либо площадью жирового включения (r= -0.7211, P=0.0017), либо (В) размером жирового включения (r= -0.9811, P=0.0052).
Несмотря на то, что яркая картина печени и гепаторенальный контраст широко признаны, как чувствительные, достоверные методы для определения жировой болезни печени, не существует количественного метода для оценки степени жирового накопления в печени. Трудности в УЗ диагностике могут происходить потому, что у графической информации, полученной путем обычного УЗИ, не хватает объективной или количественной природы, в отличие от поглощения рентгеновских лучей при КТ. ASQ анализ способен давать объективную информацию и количественную оценку гистологии печени по отношению к накоплению жировой ткани. Беря во внимание неинвазивность и небольшую стоимость УЗИ, ASQ анализ может стать основным методом для диагностики жировой болезни печени, оценки ее степени и призначения курса лечения. В дополнение, эти исследования характеристик тканей с помощью ASQ анализа, могут далее развивать методы количественной диагностики других диффузных заболеваний печени, включая фиброз или воспалительный процесс, таким образом, уменьшая потребность в биопсии.
Что касается метода ASQ, существует ряд процедур, которые проводят анализ радиочастотных сигналов большого количества маленьких-ИО в большой-ИО, в целях улучшения аналитической точности. Мы предположили, что в маленьких-ИО с высокой степенью искажения от распределения Рэлея, силы сигналов были бы негомогенными. Мы также предположили, что существует два вида негомогенных образцов: диффузная негомогенность и фокальная негомогенность. Исходя из этого, и фокусируя наше внимание на маленьких-ИО с высокой степенью искажения от распределения Рэлея, как результат фокальной негомогенности структуры, мы установили FD-ratio как параметр.
С другой стороны, при стеатозе печени наблюдаются яркая картина и васкулярная размытость, из-за отражения и рассеивания ультразвуковых волн, а также физического давления на мелкие кровеносные сосуды набухшими гепатоцитами (вызвано жировыми включениями). Мы прогнозируем, что из-за плотного размещения жировых включений (таким образом обвертывают такие структуры как мелкие кровеносные сосуды и желчные протоки), яркость паренхимы печени увеличивается, а венозные стенки печени стают размытыми, что таким образом приводит к гомогенизации силы сигнала в каждой маленькой-ИО и уменьшению количества фокально негомогенных маленьких-ИО. Поэтому, мы считаем, что если площадь и диаметр жировых включений увеличиваются, FD-ratio уменьшается. Интересно заметить, что не было значительной разницы в яркости паренхимы печени между 5 и 8 недельными мышами, а FD-ratio было самое низкое у 8 недельных мышей. Выходя из этого, можно сделать вывод, что статистический анализ ультразвуковых сигналов может обнаружить, малейшие изменения спекл картины, вызванные стеатозом.
В заключение, новый инструмент для статистического анализа ультразвуковых сигналов, используя FD-ratio как параметр, может быть полезным для количественной оценки стеатоза печени. Следовательно, FD-ratio можно применять, как неинвазивный биологический маркер для раннего обнаружения и количественной оценки стеатоза печени.
УЗИ аппарат Toshiba Aplio XG – многофункциональный диагностический комплекс экспертного класса по специальной цене от компании RH.
Вопросы и Ответы
Что такое неалкогольная жировая болезнь печени (НАЖБП) и почему важна ее ранняя диагностика?
- Неалкогольная жировая болезнь печени (НАЖБП) – это заболевание, связанное с ожирением и инсулинорезистентностью.
- Ранняя диагностика и оценка НАЖБП необходимы для своевременного вмешательства и предотвращения прогрессирования заболевания до цирроза.
Какие традиционные методы диагностики стеатоза печени существуют и каковы их недостатки?
- Золотым стандартом считается гистологический анализ печени (биопсия), но он имеет недостатки: возможные ошибки при заборе образца, трудности повторения процедуры из-за этических соображений и риска осложнений (например, кровотечения).
- Другие неинвазивные методы, такие как компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), также имеют ограничения: КТ связана с дозой облучения, а МРТ – высокая стоимость.
Почему ультразвуковое исследование (УЗИ) считается перспективным методом для диагностики стеатоза печени?
- УЗИ является минимально инвазивным, недорогим и безопасным для многократного повторения.
- УЗИ обладает высокой чувствительностью в выявлении жировых накоплений в печени.
- Однако, диагностическая способность УЗИ зависит от навыков оператора, и требуются более точные количественные методы.
Что такое акустический количественный анализ структуры (ASQ) и параметр «соотношение фокального искажения» (FD-ratio)?
- ASQ – это метод, который использует статистический анализ ультразвуковых эхо-амплитуд для оценки негомогенности тканей печени.
- FD-ratio – это аналитический параметр, вычисляемый в рамках ASQ, который отражает соотношение между различными характеристиками эхо-сигналов и используется для количественной оценки структурных изменений, в данном случае – жировых включений.
Каковы были основные результаты исследования по применению ASQ и FD-ratio для определения степени стеатоза печени на мышиной модели?
- Исследование показало значительное увеличение областей и размеров жировых включений в печени с возрастом мышей (с 5 до 12 недель).
- Была обнаружена значительная отрицательная корреляция между FD-ratio и площадью, а также размером жировых включений.
- Это свидетельствует о том, что FD-ratio может быть надежным количественным биомаркером стеатоза печени.
Может ли метод ASQ с использованием FD-ratio быть использован для диагностики стеатоза печени у людей?
- Результаты исследования на животной модели показали высокую корреляцию между FD-ratio и степенью жирового накопления в печени.
- Это позволяет предположить, что ASQ анализ УЗИ с параметром FD-ratio может стать новым надежным клиническим методом для оценки стеатоза печени у пациентов.


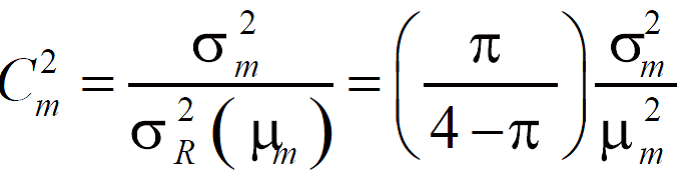
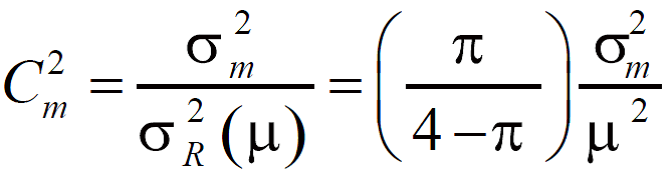
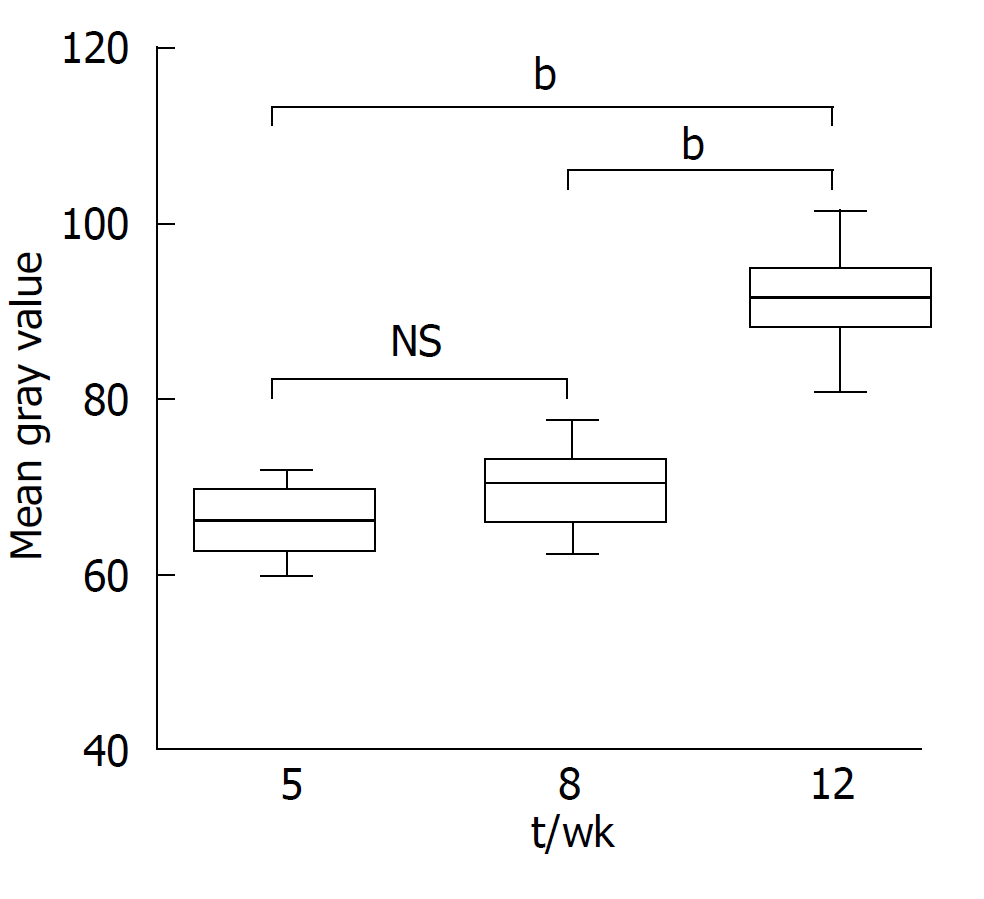











14.10.2019
Лина Павловна