🤖 Краткий пересказ от ИИ
Проблема заключается в точном определении количества метастазов в подмышечных лимфатических узлах (ПЛУ) у пациенток с ранними стадиями HR+/Her2- рака молочной железы, особенно когда диссекция ПЛУ (ДПЛУ) не проводится после выявления 1-2 положительных сторожевых лимфатических узлов (СЛУ). В данном исследовании была разработана прогностическая номограмма для выявления таких пациенток с высоким риском.
Номограмма показала высокую эффективность (AUC 0,777; С-индекс 0,802) в прогнозировании наличия ≥4 положительных ПЛУ, используя данные УЗИ аппараты подмышечных узлов, маммографические кальцинаты, T-стадию и количество положительных СЛУ. Этот инструмент помогает онкологам идентифицировать пациентов, которым показана терапия абемациклибом для усиления системного лечения без необходимости проведения ДПЛУ.
✅ Ключевые тезисы из статьи:
- Диагностика: Номограмма использует данные УЗИ-ПЛУ, маммографических кальцинатов, Т-стадии и числа положительных СЛУ для прогнозирования риска ≥4 метастазов в ПЛУ.
- Лечение: Инструмент помогает определить пациентов с HR+/Her2- раком молочной железы, которым, несмотря на пропущенную ДПЛУ, показана адъювантная терапия абемациклибом.
- Преимущества: Номограмма обеспечивает точное прогнозирование риска, способствуя персонализированному лечению, которое сочетает деэскалацию хирургии с усиленной системной терапией.
- Ограничения: Исследование было одноцентровым ретроспективным, и разработанной номограмме требуется внешняя валидация в проспективных многоцентровых исследованиях.
Последнее обновление: 21 июля 2025 р.
Экспертная проверка: Материал проверен и отредактирован экспертами RH.ua
Примечание об ИИ: Этот блок создан с помощью генеративного ИИ для быстрого ознакомления с основными идеями статьи. Для полного понимания темы рекомендуем прочесть полный текст.
⚠️ Не заменяет медицинскую консультацию
Резюме
ПРЕДУСЛОВИЯ: Эффективность абемациклиба у пациенток высокого риска с ранними стадиями HR+/Her2- рака молочной железы была подтверждена исследованием MonarchE. Однако точное определение количества метастазов в подмышечных лимфатических узлах (ПЛУ) остается сложной задачей. Исследование Z0011 изменило стратегию лечения подмышечных лимфатических узлов, устранив потребность в диссекции подмышечных лимфатических узлов (ДПЛУ) у пациентов с 1-2 метастазами в сторожевых лимфатических узлах (СЛУ). Поэтому необходимы дальнейшие исследования для выявления пациентов, которые могут получить пользу от терапии абемациклибом.
МАТЕРИАЛЫ И МЕТОДЫ: Ретроспективное исследование включало пациентов с CT1-2N0M0 HR+/Her2- с 1-2 положительными СЛУ, которым была проведена ДПЛУ. Были собраны клинико-патологические данные, и с помощью логистического регрессионного анализа были определены независимые предикторы для ≥4 положительных ПЛУ. Разработана прогностическая номограмма, оценена дискриминация и калибровка с помощью С-индекса и калибровочной кривой. Клиническую эффективность оценивали с помощью кривой анализа принятия решений (КАР).
РЕЗУЛЬТАТЫ: Мы включили 444 пациентки, из которых 77 (17,3%) имели ≥4 положительных ПЛУ. Независимыми предикторами ≥4 положительных ПЛУ были аномальные ПЛУ на УЗИ, маммографические кальцинаты, Т-стадия и количество положительных СЛУ. Номограмма продемонстрировала AUC 0,777 (95% ДИ: 0,735-0,815, P<0,001), а внутренняя валидация показала хорошую калибровку и дискриминацию (С-индекс 0,802; 95% ДИ: 0,779-0,824). КАР выявил положительную чистую пользу для уровней риска от 5% до 54%.
ЗАКЛЮЧЕНИЯ:Эта номограмма является удобным и надежным инструментом для прогнозирования риска ≥4 положительных ПЛУ у HR+/Her2- пациентов. Она помогает в выборе протокола, определяя СЛУ-положительных пациентов, которые могут получить пользу от терапии абемациклибом без ДПЛУ.
КЛЮЧЕВЫЕ СЛОВА: Абемациклиб, Новообразования в молочной железе, номограммы
Предусловия
Рак молочной железы является самой частой злокачественной опухолью у женщин, а диссекция подмышечных лимфатических узлов (ПЛУ) была стандартным методом лечения положительных ПЛУ у пациенток. Исследование ACOSOG Z0011 [1] и AMAROS [2] доказали, что ДПЛУ не улучшает общую выживаемость у пациентов cT1-2 с клинически отрицательными подмышечными и 1-2 метастазами в СЛУ. Что касается рецидивирования локорегиональных лимфатических узлов, то исследование Z0011 показало, что в группе биопсии сторожевых лимфатических узлов (БСЛУ) кумулятивная частота рецидивирования подмышечной области составляла 1,5% по сравнению с 0,5% в группе ДПЛУ. Аналогично, у пациентов, получавших ДПЛУ, 5-летняя частота подмышечных рецидивов составляла 0,43% по сравнению с 1,19% у пациентов, получавших лучевую терапию в подмышечной области. Приведенные выше данные продемонстрировали, что ДПЛУ не имеет преимуществ в увеличении общей выживаемости и контроле локальных рецидивов. Таким образом, большинство пациенток на ранних стадиях рака молочной железы с отрицательными лимфатическими узлами избегают ДПЛУ. HR+/Her2- рак молочной железы является самым распространенным подтипом среди пациенток на ранних стадиях [3], на который приходится около 60% всех случаев рака молочной железы. Несмотря на более благоприятный прогноз, чем при Her2 и трижды негативном раке молочной железы, пациентки все еще имеют 40% риск развития отдаленных рецидивов, и этот риск возрастает вместе с повышенным анатомическим риском [4]. Пациентки с высоким риском рецидива должны получать лечение как можно раньше, чтобы предотвратить рецидив и метастазирование. MonarchE [5] – это глобальное, рандомизированное, III-этапное исследование, которое доказало, что стандартное эндокринное лечение + абемациклиб (ингибитор циклинзависимых киназ 4 и 6) может улучшить терапевтические результаты у пациенток на ранних стадиях рака молочной железы с высоким риском HR + / Her2-. Абсолютная 4-летняя выживаемость без инвазивных заболеваний (ВБИЗ) составила 6,4% (группа Абемациклиба (85,8% [95% ДИ 84,2-87,3] против 79,4% в группе стандартного эндокринного лечения [95% ДИ 77,5-81,1]). Риск возникновения события ВБИЗ был снижен на 33,6%. Пациентки, включенные в исследование MonarchE, имели положительные ПЛУ ≥4 или имели 1-3 положительные ПЛУ и по крайней мере 1 клинический признак высокого риска: опухоль ≥5 см или гистологический класс 3 или Ki-67 ≥20%. Начиная с исследования Z0011, отказ от ДПЛУ широко применяется у пациенток, сохраняющих молочную железу, с 1-2 положительными СЛУ. Это приводит к новой проблеме: как решить, нуждается ли пациентка в терапии абемациклибом при 1-2 положительных СЛУ без клинических признаков высокого риска? Является ли ДПЛУ необходимым для подтверждения метастатической нагрузки подмышечных узлов? Было показано, что 13,0-18,4% пациентов, которые соответствовали критериям Z0011, имели более 4 положительных ПЛУ [1,2,6]. Таким образом, мы должны определить риск метастазов ПЛУ ≥4 у пациенток с HR+/Her2- раком молочной железы с 1-2 положительными СЛУ и пропущенным ДПЛУ без признаков опухоли высокого риска. Эти пациентки, вероятно, могут получить пользу от терапии абемациклибом для усиления системной терапии и деэскалации местного хирургического лечения. Целью данного исследования было проанализировать ретроспективные данные одноцентрового исследования с помощью одномерного и многомерного регрессионного анализа и построить номограмму для отбора пациентов, которые подходят для терапии абемациклибом.
Материалы и методы
СТАТИСТИЧЕСКИЙ АНАЛИЗ:
Были собраны клинические данные пациенток, включая возраст, ИМТ, менопаузальный статус, унифокальные/мультифокальные опухоли, ультразвук ПЛУ (УЗИ-ПЛУ), маммографические кальцинаты, хирургический метод, патологический тип, гистологический класс, размер опухоли, лимфоваскулярную инвазию (ЛВИ), положительное и отрицательное число СЛУ, N классификацию, уровень экспрессии рецепторов прогестерона и Her2. Клинико-патологические факторы были проанализированы как категориальные переменные для изучения их корреляции с положительным числом ПЛУ ≥4. Категориальные переменные анализировали с помощью одномерного логистического регрессионного анализа, из которого полученные значимые переменные анализировали в многомерном логистическом регрессионном анализе для подтверждения независимых предикторов положительных ПЛУ ≥4. Номограмма была построена с помощью пакета “rms” программного обеспечения R. Для оценки эффективности номограммы использовали дискриминацию и калибровку. Внутренняя валидация была выполнена с помощью метода повторной выборки 1000 бутстрапов, с вычислением С-индекса и построением калибровочной кривой. Дискриминационную способность оценивали по площади под ROC-кривой и С-индексом. Для оценки клинической эффективности и чистой пользы номограммы использовали кривую анализа принятия решений (КАР). Все статистические анализы были проведены с использованием SPSS 25.0 (IBM Corporation, Армонк, Нью-Йорк, США) и R 4.1.1 (The R Foundation for Statistical Computing, Австрия, Вена). P<0,05 интерпретировался как статистически значимый.
Результаты
Мы набрали 444 пациентки с раком молочной железы, которые соответствовали критериям включения, с января 2015 года по июнь 2022 года. Исходные характеристики пациентов приведены в Таблице 1. Средний возраст составлял 50 лет. У 274 пациенток (61,7%) были опухоли cT1, у 318 пациенток (71,6%) – 1 положительный СЛУ и у 126 пациенток (28,4%) – 2 положительных СЛУ. Среди пациентов с 1 положительным СЛУ 9,43% имели положительные не-СЛУ ≥3, а среди пациентов с 2 положительными СЛУ 36,5% имели положительные не-СЛУ ≥2. В целом 367 (82,7%) пациентов имели 1-3 положительные СЛУ (pN1), а 77 (17,3%) пациентов имели положительные СЛУ ≥4 (pN2-3) (Табл. 2). Для выявления факторов положительного значения ПЛУ ≥4 был проведен одномерный и многомерный логистический регрессионный анализ. Факторы с P<0,05 в одномерном анализе были проанализированы в многомерном анализе. Независимыми предикторами положительных ПЛУ ≥4 были УЗИ-ПЛУ (ОШ= 2,289, 95% ДИ: 1,327-3,948, P = 0,003), маммографические кальцинаты (ОШ = 2,452, 95% ДИ: 1. 297-4,638, P = 0,006), Т-стадия (ОШ = 2,426, 95% ДИ: 1,414-4,161, P = 0,001) и положительное число СЛУ (ОШ = 5,175, 95% ДИ: 3,007-8,904, P <0,001). На основе данных многомерного логистического регрессионного анализа была построена номограмма для прогнозирования положительных ПЛУ ≥4 среди пациентов с cT1-2N0M0 HR+/Her2- с 1-2 положительными СЛУ (Рис. 1). Вероятность положительных СЛУ ≥4 рассчитывали путем сложения баллов по 4 факторам и отношением к общей сумме баллов и шкале минимального риска. Калибровочная кривая и ROC-кривая были использованы для оценки калибровки и дискриминации номограммы. Калибровочная кривая показала хорошее соответствие между прогнозируемыми и наблюдаемыми результатами для номограммы (Рис. 2А). ROC-кривая номограммы показана на Рис. 2B. Чувствительность составила 75,32%, специфичность – 73,30%, а AUC – 0,777 (95% ДИ: 0,735-0,815, P<0,001), что свидетельствует о том, что номограмма имеет хорошие прогностические характеристики. Номограмма продемонстрировала хорошую дискриминацию со значением С-индекса 0,802 (95% ДИ: 0,779-0,824). Анализ кривых принятия решений был использован для определения клинической применимости принятия решений на основе прогностической модели по сравнению со стандартной стратегией. По сравнению с лечением всех пациентов (наклонная линия) или не лечением ни одного пациента (горизонтальная линия), модель продемонстрировала высокие чистые преимущества. КАР (Рис. 3) продемонстрировала, что в диапазоне порогового риска от 5% до 54% решения о вмешательстве на основе номограммы были однозначно полезными.
Обсуждение
В этом исследовании была построена номограмма с использованием клинико-патологических факторов для оценки риска положительных ПЛУ ≥4 среди пациентов с cT1-2N0M0 HR+/Her2- с 1-2 положительными СЛУ. Номограмма включала УЗИ-ПЛУ, маммографические кальцинаты, Т-стадию и количество положительных СЛУ. Внутренняя валидация показала, что номограмма имеет хорошую дискриминацию, калибровку и клиническую эффективность.
Сейчас основными тенденциями в лечении рака молочной железы являются деэскалационная химиотерапия для пациенток с низким риском и интенсивная системная терапия для пациенток с высоким риском. Для разработки протоколов адъювантной химиотерапии больных раком молочной железы на ранних стадиях с HR+/Her2- (например, Oncotype DX [9,10] и MammaPrint [11]) были разработаны многочисленные методы выявления генов, ориентированные на рак молочной железы с HR+ и отрицательными лимфатическими узлами или 1-3 положительными лимфатическими узлами. Пациентки с клинико-патологическими характеристиками высокого риска (например, участницы исследования MonarchE) имели показатели смертности, подобные показателям смертности пациенток с тройным негативным раком груди (ТНРГ) [12]. Исследование MonarchE [5] показало, что 2-летнее применение абемациклиба может улучшить клинические результаты. Сейчас у большинства пациентов, которые соответствовали критериям Z0011, не выявлено ДПЛУ, что делает невозможным получение полных данных о метастазировании ПЛУ, поэтому частично пациенты не имеют оснований для интенсивного лечения. Индекс Ki-67 может отражать степень пролиферации клеток, и пациенты с высоким уровнем Ki-67 имели худшие прогнозы [13]. Пациентам, включенным в исследование MonarchE, было разрешено лечение абемациклибом при Ki-67 ≥20%, если были метастазы в лимфатические узлы, за исключением только ≥4 метастазов в лимфатические узлы, когда Ki-67 был <20%. Поэтому пациенты с Ki-67 ≥20% были исключены из этого исследования. В группе намерений на лечение и в первой когорте клинического опыта MonarchE отмечено, что лечение абемациклибом значительно улучшило ВБИЗ у пациентов с опухолями с высоким уровнем экспрессии Ki-67. В когорте 1 преимущество абемациклиба постоянно наблюдалось независимо от экспрессии Ki-67, что указывает на то, что Ki-67 не может предсказать терапевтическую пользу абемациклиба. Примечательно, что пациенты с высоким уровнем экспрессии Ki-67 имели более высокие показатели рецидивов, чем пациенты с низким уровнем экспрессии Ki-67. Таким образом, экспрессия Ki-67 является прогностическим показателем рецидива, но не может предсказать терапевтические преимущества абемациклиба [14]. Предварительное исследование показало, что 13,0-18,4% пациентов, которые соответствовали критериям Z0011, имели более 4 положительных ПЛУ [1,2,6]. Наше исследование показало, что вероятность положительных ПЛУ ≥4 среди пациентов cT1-2N0 HR+/Her2- с 1-2 положительными СЛУ составляла 17,1%, 9,43% для 1 положительного СЛУ и 38,1% для 2 положительных СЛУ.
Большинство прогностических исследований были сосредоточены на наличии метастазов не в СЛУ, тогда как исследований относительно точного количества метастазов в лимфатические узлы (например, положительные лимфатические узлы ≥4) немного. Кроме того, переменными, включенными в эти исследования, были прежде всего размер метастатического очага СЛУ, экстрамембранозная инфильтрация лимфатических узлов и ЛВИ [15], которые базировались на послеоперационных патогистологических исследованиях. Gilles и соавт.[16] создали предоперационную клиническую модель и послеоперационную патологическую модель для прогнозирования риска метастазов ПЛУ на основе 12572 случаев рака молочной железы на ранних стадиях, показав, что послеоперационная модель имеет лучшую дискриминацию (AUC=0,780), чем предоперационная модель (AUC=0,717). Интраоперационных моделей мало. Shimazu и соавт. [17] построили интраоперационную модель прогнозирования метастазирования не-СЛУ с помощью метода одношаговой амплификации нуклеиновых кислот. Модель включала общую опухолевую нагрузку и размер опухоли, с AUC 0,70. AUC модели в этом исследовании составляла 0,777, и она была такой же эффективной, как и приведенная выше послеоперационная модель. Считается, что размер опухоли, гистологический класс, ЛВИ, возраст на момент постановки диагноза, положительное СЛУ-число, экспрессия гормональных рецепторов, статус Her-2 и молекулярный подтип являются значимыми факторами риска метастазирования не-СЛУ [18]. Это исследование показало, что УЗИ-ПЛУ, маммографические кальцинаты, Т-стадия и положительное число СЛУ являются независимыми предикторами положительных ПЛУ ≥4.
В исследовании Z0011 [1], исследовании BCSG 23-01 [19] и исследовании AMAROS [2] клинически отрицательные лимфатические узлы определялись как отсутствие увеличенных лимфатических узлов при физикальном обследовании. Тем не менее, оценка статуса ПЛУ с помощью клинического обследования является неточной, а ультразвуковое исследование способствует выявлению пациентов с высокой нагрузкой на подмышечные лимфатические узлы [20,21]. В этом исследовании 146 пациентов имели аномалии ПЛУ на УЗИ, из них 39 пациентов (26,7%) имели ≥4 положительных лимфоузлов, 260 пациентов имели нормальное состояние ПЛУ на УЗИ, и 38 (14,6%) из них имели положительные лимфоузлы ≥4. Было показано, что пациенты с аномальными ПЛУ на УЗИ имели большую подмышечную нагрузку (ОШ=2,289, 95% ДИ: 1,327-3,948, P=0,003) по сравнению с пациентами с нормальными результатами УЗИ, что согласуется с исследованием Muneer и соавт. [21]. Lim и соавт. [22] сообщили, что ≥3 патологических лимфатических узлов на УЗИ является критическим предиктором высокой нагрузки на подмышечные лимфатические узлы у пациентов, которые соответствуют критериям Z0011. Кроме того, было показано, что предоперационная МРТ может точно выявить метастазы ПЛУ для оценки опухолевой нагрузки на подмышечные лимфатические узлы [23,24]. Радиоимические переменные могут быть включены в будущие прогностические модели для дальнейшего улучшения прогностической эффективности модели.
Связь между визуализационными проявлениями первичной опухоли и метастазами ПЛУ недостаточно изучена, особенно с помощью маммографии. Zheng и соавт. [25] обнаружили значительную связь между метастазированием ПЛУ и маммографическими кальцификатами среди 7317 пациенток. Yan и соавт. [26] сообщили, что маммографические кальцинаты существенно связаны с высокой нагрузкой метастазирования ПЛУ как независимый прогностический фактор для пациенток с раком молочной железы. Визуализационные проявления первичного локуса не были включены в исследования, подобные исследованию Z0011. Однако мы продемонстрировали значительную корреляцию между маммографическими кальцификатами и положительными ПЛУ ≥4 (ОШ=2,452, 95% ДИ: 1,297-4,638, P=0,006).
ЛВИ является независимым предиктором метастазирования в лимфатические узлы и неблагоприятных результатов [27,28]. Он требует рутинной окраски послеоперационных срезов гематоксилином и эозином (ГЭ), что не подходит для интраоперационных моделей. ЛВИ в значительной степени коррелирует с возрастом, Т-стадией, гистологическим классом и экспрессией гормональных рецепторов [29]. В этом исследовании было обнаружено, что ЛВИ не имеет отношения к метастазированию ПЛУ (P=0,420), что может быть связано с тем, что включенные пациенты имели положительные гормональные рецепторы, исключая вовлечение продвинутой стадии T/N и гистологической степени опухоли 3.
Экспрессия Her2 существенно коррелирует с метастатическим потенциалом клеток рака молочной железы. Ahmed и соавт. [30] сообщили, что экспрессия Her2 является независимым предиктором метастазирования ПЛУ. В настоящее время считается, что низкая экспрессия Her2 может быть новым молекулярным подтипом. Francesco [31] обнаружил, что пациенты с HR-положительными заболеваниями (65,4%) имели более высокую долю низкой экспрессии Her2, чем пациенты с ТНРГ (36,6%). Низкий уровень экспрессии Her2 не имел отношения к общей выживаемости пациенток с HR-положительным раком молочной железы. Немного исследований изучали взаимосвязь между экспрессией Her2 и метастазированием ПЛУ. Наше исследование показало, что доля низкой экспрессии Her2 (85,6%) была выше, чем Her2 0 (14,4%) среди HR + / Her2- пациентов, что согласуется с данными в исследовании Francesco. Однако не было выявлено достоверной корреляции между низкой экспрессией Her2 и статусом HER2 0 и количеством метастазов в лимфатических узлах (P = 0,151).
Номограмма в этом исследовании показала С-индекс 0,802 (95% ДИ: 0,779-0,824), что свидетельствует о хорошей дискриминации. Что касается оценки калибровки, то калибровочная кривая продемонстрировала сильное соответствие между кривой распределения прогнозируемых значений модели и кривой распределения, полученной после коррекции переобучения с помощью повторной выборки. Она тесно совпадала с оптимальной кривой (стандартной кривой), что свидетельствует о хорошей калибровке модели. Для оценки клинической эффективности была применена кривая анализа принятия решений (КАР) для расчета чистой пользы и построения КАР. КАР проиллюстрировала, что кривая принятия решения модели отклонилась от 2 крайних кривых сценариев, что свидетельствует о хорошей клинической эффективности.
Это исследование имеет определенные ограничения. Во-первых, это было одноцентровое ретроспективное исследование с потенциальными предубеждениями. Во-вторых, номограмма не прошла внешнюю валидацию. Таким образом, для оценки и валидации результатов необходимы проспективные многоцентровые исследования.
Заключения
Мы создали интраоперационную прогностическую номограмму для прогнозирования вероятности положительных ПЛУ ≥4 среди HR+/Her2- пациентов с положительными СЛУ и пропущенными ДПЛУ, чтобы помочь в принятии клинических решений. Прогностическая модель является точной и может помочь онкологам идентифицировать пациентов, нуждающихся в терапии абемациклибом. Таким образом, пациентам могут быть предложены лучшие стратегии лечения, включая деэскалационную хирургию и системную эскалационную терапию в эпоху БСЛУ и точной медицины.
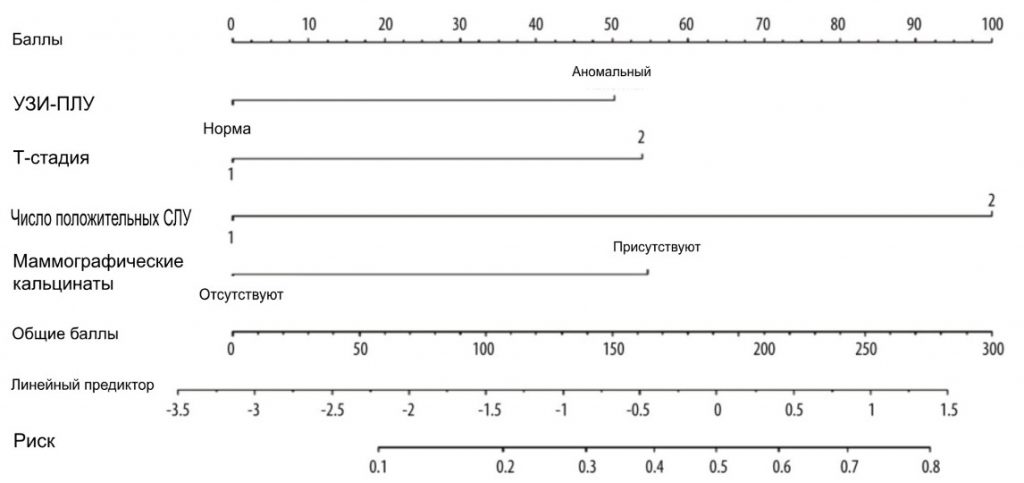
Рисунок 1. Номограмма для прогнозирования пациентов с ≥4 положительными суммарными ПЛУ в популяции HR+/HER2- с 1-2 положительными СЛУ. Баллы по 4 факторам суммировались для расчета вероятности ≥4 положительных суммарных ПЛУ, а общие баллы и нижняя шкала риска были отнесены к шкале риска. Программное обеспечение R 4.1.1 (The R Foundation for Statistical Computing, Австрия, Вена).
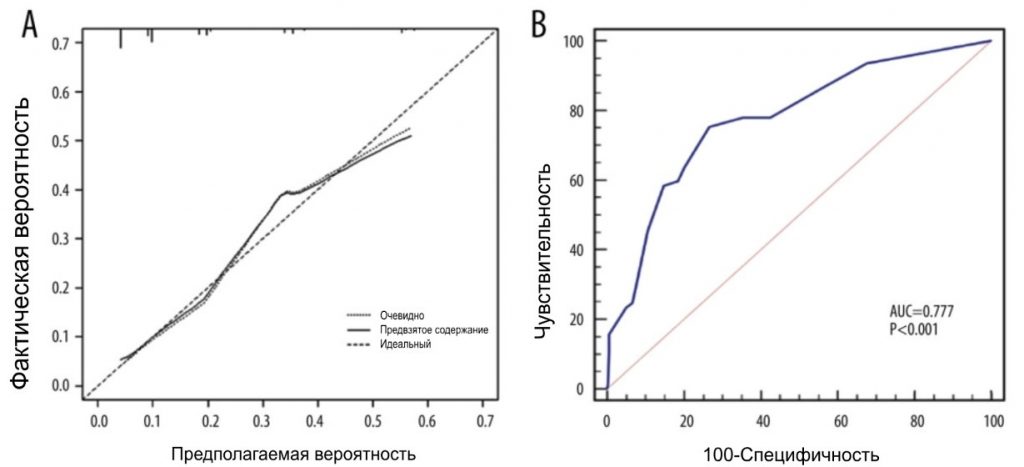
Рисунок 2. (А) Калибровочная кривая показала удовлетворительное соответствие между прогнозом и фактическим наблюдением. (B) ROC-кривая номограммы. Программное обеспечение R 4.1.1 (The R Foundation for Statistical Computing, Австрия, Вена).
Рисунок 3. КАР демонстрирует клиническую эффективность номограммы. Красная линия – это номограмма, которая прогнозирует риск появления ≥4 положительных узлов у пациентов. Серая линия обозначает всех пациентов с ≥4 положительными узлами, тогда как черная линия не обозначает ни одного пациента с ≥4 положительными узлами. Эта КАР может обеспечить большую чистую выгоду в диапазоне от 5% до 54%. КАР – кривая анализа принятия решений. Программное обеспечение R 4.1.1 (The R Foundation for Statistical Computing, Австрия, Вена).
Таблицы
Таблица 1. Характеристика HR+/HER2- пациенток.
| Характеристики | Пациенты(n=444) |
| Возраст, медиана (мин, макс), годы | 50 (26-80) |
| 215 (48.4%) | |
| ≥50, нет. (%) | 229 (51.6%) |
| ИМТ | 244 (22.3-26.1) |
| Менопаузальный статус, количество- (%) | |
| Предменопаузальный период | 254 (57.2%) |
| Постменопаузальный период | 190 (42.8%) |
| Мультифокальность, количество (%) | |
| Отсутствие | 394 (88.7%) |
| Присутствие | 50 (11.3%) |
| Клиническая стадия опухоли, количество (%) | |
| 1 | 274 (61.7%) |
| 2 | 170 (38.3%) |
| Размер опухоли, медиана (мин, макс), см | 1.9 (0.2-5.0) |
| УЗИ-ПЛУ, количество (%) | |
| Норма | 298 (67.1%) |
| Аномальный | 146 (32.9%) |
| Маммографические кальцинаты, количество (%) | |
| Отсутствуют | 365 (82.2%) |
| Присутствуют | 79 (17.8%) |
| Хирургическое вмешательство, количество (%) | |
| Мастэктомия | 350 (78.8%) |
| Сохранение груди | 94 (21.2%) |
| Тип опухоли, количество (%) | |
| Проточный | 425 (95.7%) |
| Дольковый | 15 (3.4%) |
| Другие | 4 (0.9%) |
| Гистологическая степень, количество (%) | |
| I | 7 (1.6%) |
| II | 397 (89.4%) |
| Отсутствует | 40 (9.0%) |
| Удалено 1 положительный СЛУ, всего, количество (%) | 318 (71.6%) |
| 0 положительных не-СЛУ, нет | 166 |
| 1 положительных не-СЛУ, нет | 95 |
| 2 положительных не-СЛУ, нет | 27 |
| ≥3 положительных не-СЛУ, нет | 30 |
| Удалено 2 положительных СЛУ, всего, количество (%) | 126 (28.4%) |
| 0 положительных не-СЛУ, нет | 62 |
| 1 положительных не-СЛУ, нет | 18 |
| 2 положительных не-СЛУ, нет | 22 |
| ≥3 положительных не-СЛУ, нет | 24 |
| Стадия pN, количество (%) | |
| 1 | 367 (82.7%) |
| 2-3 | 77 (17.3%) |
| ЛВИ, количество (%) | |
| Отсутствует | 348 (78.4%) |
| Присутствует | 96 (21.6%) |
| Рецептор прогестерона, количество (%) | |
| Негативный | 33 (7.4%) |
| Положительный | 411 (92.6%) |
| Экспрессия HER2, количество (%) | |
| 0 | 64 (14.4%) |
| 1+ | 137 (30.9%) |
| 2+ | 243 (54.7%) |
ИМТ – индекс массы тела; УЗИ-ПЛУ – ультразвуковое исследование подмышечного лимфатического узла; СЛУ – сторожевой лимфатический узел; ЛВИ – лимфоваскулярная инвазия.
Таблица 2. Одномерный и многомерный анализ среди пациенток с HR+/HER2-.
| Характеристики | pN1 (n=367) | pN2-3 (n=77) | Неизменная P | Многомерная P |
| Возраст, количество (%) | 0.747 | |||
| 179 (48.8) | 36 (46.8) | |||
| ≥50, нет. (%) | 188 (51.2) | 41 (53.2) | ||
| Менопаузальный статус, количество (%) | 0.990 | |||
| Отсутствует | 210 (57.2) | 44 (57.1) | ||
| Присутствует | 157 (42.8) | 33 (42.9) | ||
| Мультифокальность, количество (%) | 0.356 | |||
| Отсутствует | 328 (89.4) | 66 (85.7) | ||
| Присутствует | 39 (10.6) | 11 (14.3) | ||
| Клиническая стадия опухоли, количество (%) | 0.001 | |||
| 1 | 241 (65.7) | 33 (42.9) | ||
| 2 | 126 (34.3) | 44 (57.1) | ||
| УЗИ-ПЛУ, количество (%) | 0.003 | |||
| Норма | 260 (70.8) | 38 (49.4) | ||
| Аномальный | 107 (29.2) | 39 (50.6) | ||
| Маммографические кальцинаты | 0.017 | 0.006 | ||
| Отсутствуют | 309 (84.2) | 56 (72.7) | ||
| Присутствуют | 58 (15.8) | 21 (27.3) | ||
| Хирургическое вмешательство, количество (%) | 0.602 | |||
| Мастэктомия | 291 (79.3) | 59 (76.6) | ||
| Сохранение груди | 76 (20.7) | 18 (23.4) | ||
| Тип опухоли, количество (%) | 0.571 | |||
| Проточный | 353 (96.1) | 72 (93.5) | ||
| Дольковый | 11 (3.0) | 4 (5.2) | ||
| Другие | 3 (0.9) | 1 (1.3) | ||
| Гистологическая степень, количество (%) | 0.880 | |||
| I | 6 (1.6) | 1 (1.3) | ||
| II | 329 (89.6) | 68 (88.3) | ||
| Отсутствует | 32 (8.8) | 8 (10.4 | ||
| Количество удаленных положительных СЛУ | ||||
| 1 | 287 (78.2) | 31 (40.2) | ||
| 2 | 80 (21.8) | 46 (59.8) | ||
| Количество удаленных негативных СЛУ | 0.004 | |||
| 0 | 18 (4.9) | 10 (13.0) | ||
| 1 | 66 (18.0) | 18 (23.4) | ||
| 2 | 79 (21.5) | 9 (11.7) | ||
| 3 | 65 (17.7) | 20 (26.0) | ||
| ≥4 | 139 (37.9) | 20 (26.0) | ||
| ЛВИ, количество (%) | 0.420 | |||
| Отсутствует | 285 (77.7) | 63 (81.8) | ||
| Присутствует | 82 (22.3) | 14 (18.2) | ||
| Рецептор прогестерона, количество (%) | 0.895 | |||
| Негативный | 27 (7.4) | 6 (7.8) | ||
| Положительный | 340 (92.6) | 71 (92.2) | ||
| Экспрессия HER2, количество (%) | 0.151 | |||
| 0 | 48 (13.1) | 16 (20.8) | ||
| 1 | 112 (30.5) | 25 (32.5) | ||
| 2 | 207 (56.4) | 36 (46.7) |
УЗИ-ПЛУ – ультразвуковое исследование подмышечного лимфатического узла; СЛУ – сторожевой лимфатический узел; ЛВИ – лимфоваскулярная инвазия.
Ссылки на источники
- Giuliano AE, Ballman KV, McCall L, Effect of axillary dissection vs no axillary dissection on 10-year overall survival among women with invasive breast cancer and sentinel node metastasis: The ACOSOG Z0011 (Alliance) randomized clinical trial: JAMA, 2017; 318(10); 918
- Donker M, van Tienhoven G, Straver ME, Radiotherapy or surgery of the axilla after a positive sentinel node in breast cancer (EORTC 10981-22023 AMAROS): a randomised, multicentre, open-label, phase 3 non-inferiority trial: Lancet Oncol, 2014; 15(12); 1303-10
- Howlader N, Altekruse SF, Li CI, US incidence of breast cancer subtypes defined by joint hormone receptor and HER2 status: J Natl Cancer Inst, 2014; 106(5); dju055
- Pan H, Gray R, Braybrooke J, 20-year risks of breast-cancer recurrence after stopping endocrine therapy at 5 years: N Engl J Med, 2017; 377(19); 1836-46
- Johnston SRD, Toi M, O’Shaughnessy J, Abemaciclib plus endocrine therapy for hormone receptor-positive, HER2-negative, node-positive, high-risk early breast cancer (monarchE): Results from a preplanned interim analysis of a randomised, open-label, phase 3 trial: Lancet Oncol, 2022; 24(1); 77-90
- Katz A, Smith BL, Golshan M, Nomogram for the prediction of having four or more involved nodes for sentinel lymph node-positive breast cancer: J Clin Oncol, 2008; 26(13); 2093-98
- Wolff AC, Hammond MEH, Allison KH, Human epidermal growth factor receptor 2 testing in breast cancer: American Society of Clinical Oncology/College of American Pathologists clinical practice guideline focused update: Arch Pathol Lab Med, 2018; 142(11); 1364-82
- Hammond MEH, Hayes DF, Dowsett M, American Society of Clinical Oncology/College of American Pathologists Guideline Recommendations for Immunohistochemical Testing of Estrogen and Progesterone Receptors in Breast Cancer (Unabridged Version): Arch Pathol Lab Med, 2010; 134; 25
- Sparano JA, Gray RJ, Makower DF, Adjuvant chemotherapy guided by a 21-gene expression assay in breast cancer: N Engl J Med, 2018; 379(2); 111-21
- Kalinsky K, Barlow WE, Gralow JR, 21-gene assay to inform chemotherapy benefit in node-positive breast cancer: N Engl J Med, 2021; 385(25); 2336-47
- Cardoso F, van’t Veer LJ, Bogaerts J, 70-gene signature as an aid to treatment decisions in early-stage breast cancer: N Engl J Med, 2016; 375(8); 717-29
- Nelson DR, Brown J, Morikawa A, Method M, Breast cancer-specific mortality in early breast cancer as defined by high-risk clinical and pathologic characteristics: PLoS One, 2022; 17(2); e0264637
- Yerushalmi R, Woods R, Ravdin PM, Ki67 in breast cancer: Prognostic and predictive potential: Lancet Oncol, 2010; 11(2); 174-83
- Harbeck N, Rastogi P, Martin M, Adjuvant abemaciclib combined with endocrine therapy for high-risk early breast cancer: Updated efficacy and Ki-67 analysis from the monarchE study: Ann Oncol, 2021; 32(12); 1571-81
- Kim I, Ryu JM, Kim JM, Development of a nomogram to predict N2 or N3 stage in T1-2 invasive breast cancer patients with no palpable lymphadenopathy: J Breast Cancer, 2017; 20(3); 270
- Houvenaeghel G, Lambaudie E, Classe JM, Lymph node positivity in different early breast carcinoma phenotypes: A predictive model: BMC Cancer, 2019; 19(1); 45
- Shimazu K, Sato N, Ogiya A, Intraoperative nomograms, based on one-step nucleic acid amplification, for prediction of non-sentinel node metastasis and four or more axillary node metastases in breast cancer patients with sentinel node metastasis: Ann Surg Oncol, 2018; 25(9); 2603-11
- van la Parra RFD, Peer PGM, Ernst MF, Bosscha K, Meta-analysis of predictive factors for non-sentinel lymph node metastases in breast cancer patients with a positive SLN: Eur J Surg Oncol, 2011; 37(4); 290-99
- Galimberti V, Cole BF, Zurrida S, Axillary dissection versus no axillary dissection in patients with sentinel-node micrometastases (IBCSG 23–01): A phase 3 randomised controlled trial: Lancet Oncol, 2013; 14(4); 297-305
- Farrell TPJ, Adams NC, Stenson M, The Z0011 Trial: Is this the end of axillary ultrasound in the pre-operative assessment of breast cancer patients?: Eur Radiol, 2015; 25(9); 2682-87
- Ahmed M, Jozsa F, Baker R, Meta-analysis of tumour burden in pre-operative axillary ultrasound positive and negative breast cancer patients: Breast Cancer Res Treat, 2017; 166(2); 329-36
- Lim GH, Upadhyaya VS, Acosta HA, Preoperative predictors of high and low axillary nodal burden in Z0011 eligible breast cancer patients with a positive lymph node needle biopsy result: Eur J Surg Oncol, 2018; 44(7); 945-50
- Kuijs VJL, Moossdorff M, Schipper RJ, The role of MRI in axillary lymph node imaging in breast cancer patients: A systematic review: Insights Imaging, 2015; 6(2); 203-15
- Schacht DV, Drukker K, Pak I, Using quantitative image analysis to classify axillary lymph nodes on breast MRI: A new application for the Z 0011 Era: Eur J Radiol, 2015; 84(3); 392-97
- Zheng K, Tan JX, Li F, Relationship between mammographic calcifications and the clinicopathologic characteristics of breast cancer in Western China: A retrospective multi-center study of 7317 female patients: Breast Cancer Res Treat, 2017; 166(2); 569-82
- Li Y, Cao J, Zhou Y, Mammographic casting-type calcification is an independent prognostic factor in invasive breast cancer: Sci Rep, 2019; 9(1); 10544
- Houvenaeghel G, Lymphovascular invasion has a significant prognostic impact in patients with early breast cancer, results from a large, national, multicenter, retrospective cohort study: ESMO Open, 2021; 6(6); 10
- Rakha EA, Martin S, Lee AH, The prognostic significance of lymphovascular invasion in invasive breast carcinoma: Cancer, 2012; 118(15); 3670-80
- Aleskandarany MA, Sonbul SN, Mukherjee A, Rakha EA, Molecular mechanisms underlying lymphovascular invasion in invasive breast cancer: Pathobiology, 2015; 82(3–4); 113-23
- Ahmed ARH, HER2 expression is a strong independent predictor of nodal metastasis in breast cancer: J Egypt Natl Cancer Inst, 2016; 28(4); 219-27
- Schettini F, Chic N, Brasó-Maristany F, Clinical, pathological, and PAM50 gene expression features of HER2-low breast cancer: NPJ Breast Cancer, 2021; 7(1); 1
Вопросы и ответы
Что такое номограмма, разработанная в исследовании?
- Номограмма — это прогностический инструмент, разработанный для определения вероятности наличия 4 и более положительных подмышечных лимфатических узлов (ПЛУ) у пациенток с HR+/Her2- раком молочной железы, имеющих 1-2 положительных сторожевых лимфатических узла (СЛУ) и которым не проводилась диссекция подмышечных лимфатических узлов (ДПЛУ).
Какие факторы включены в разработанную номограмму?
- Номограмма учитывает следующие факторы:
- Аномальные результаты УЗИ подмышечных лимфатических узлов (УЗИ-ПЛУ).
- Наличие маммографических кальцинатов.
- T-стадия опухоли (размер опухоли).
- Количество положительных сторожевых лимфатических узлов (СЛУ).
Какова эффективность разработанной номограммы?
- Номограмма показала хорошую дискриминацию и калибровку. Площадь под ROC-кривой (AUC) составила 0,777 (95% ДИ: 0,735-0,815, P<0,001), а С-индекс — 0,802 (95% ДИ: 0,779-0,824). Кривая анализа принятия решений (КАР) показала, что номограмма имеет клиническую пользу при пороговом риске от 5% до 54%.
Для каких пациенток предназначена терапия абемациклибом?
- Терапия абемациклибом предназначена для пациенток с ранними стадиями HR+/Her2- рака молочной железы высокого риска, которые могут получить пользу от усиленной системной терапии для предотвращения рецидивов и метастазирования. Исследование MonarchE подтвердило эффективность абемациклиба в этой группе пациентов.
Почему важно определять количество метастазов в подмышечных лимфатических узлах?
- Определение точного количества метастазов в подмышечных лимфатических узлах (ПЛУ) важно, так как это влияет на оценку риска рецидива и необходимость более интенсивного лечения. Исследования, такие как Z0011 и AMAROS, показали, что диссекция подмышечных лимфатических узлов (ДПЛУ) не всегда улучшает общую выживаемость у пациенток с 1-2 положительными СЛУ. Номограмма помогает выявить пациенток, которым, несмотря на отсутствие ДПЛУ, может потребоваться более агрессивная терапия, включая абемациклиб, при наличии высокого риска метастазирования в ПЛУ (≥4 положительных ПЛУ).
Какова связь между результатами данного исследования и терапией абемациклибом?
- Разработанная номограмма помогает идентифицировать пациенток с HR+/Her2- раком молочной железы и 1-2 положительными СЛУ, которые имеют высокий риск (≥4 положительных ПЛУ), но которым не была проведена ДПЛУ. Эти пациентки могут получить наибольшую пользу от терапии абемациклибом, что способствует деэскалации местного хирургического лечения при одновременном усилении системной терапии.
Каковы независимые предикторы ≥4 положительных ПЛУ, выявленные в исследовании?
- Независимыми предикторами ≥4 положительных ПЛУ у пациенток с HR+/Her2- раком молочной железы с 1-2 положительными СЛУ были:
- Аномальные результаты УЗИ подмышечных лимфатических узлов.
- Наличие маммографических кальцинатов.
- Более высокая T-стадия опухоли.
- Большее количество положительных сторожевых лимфатических узлов.