🤖 Короткий переказ від ШІ
Стаття розглядає сучасні методи візуалізації перфузії головного мозку у новонароджених, зокрема ультразвук з контрастним посиленням (CEUS) та надшвидку ультразвукову візуалізацію (UUI), комп’ютерну томографію (КТ) та спектроскопію в ближньому інфрачервоному діапазоні (NIRS), а також ядерну візуалізацію (ПЕТ та ОФЕКТ).
Аналізуються переваги, обмеження та технічні аспекти кожного методу, підкреслюючи, що ультразвук та МРТ є найбільш підходящими для неонатальної візуалізації через їх безпеку та здійсненність, незважаючи на те, що методи, пов’язані з іонізуючим випромінюванням, мають свої переваги в отриманні детальних даних. Ось посилання: УЗД апарати
✅ Ключові тези зі статті:
- Діагностика: Різноманітність методів візуалізації дозволяє оцінювати перфузію мозку у новонароджених, кожен з яких має свої сильні сторони.
- Лікування: Вибір методу візуалізації залежить від балансу між необхідною діагностичною інформацією та ризиками для новонароджених, зокрема від впливу іонізуючого випромінювання.
- Переваги: Ультразвук та МРТ визнаються як найбільш безпечні та практичні методи для новонароджених, тоді як CEUS та UUI пропонують покращення візуалізації кровотоку.
- Обмеження: КТ та ядерна візуалізація обмежуються ризиками, пов’язаними з іонізуючим випромінюванням, а NIRS має обмежене просторове розділення та проникнення.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: Jérôme Baranger, Olivier Villemain, Matthias Wagner, Mariella Vargas-Gutierrez, Mike Seed, Olivier Baud, Birgit Ertl-Wagner, Julien Aguetg
3.2.3. Ультразвук з контрастним посиленням (CEUS)
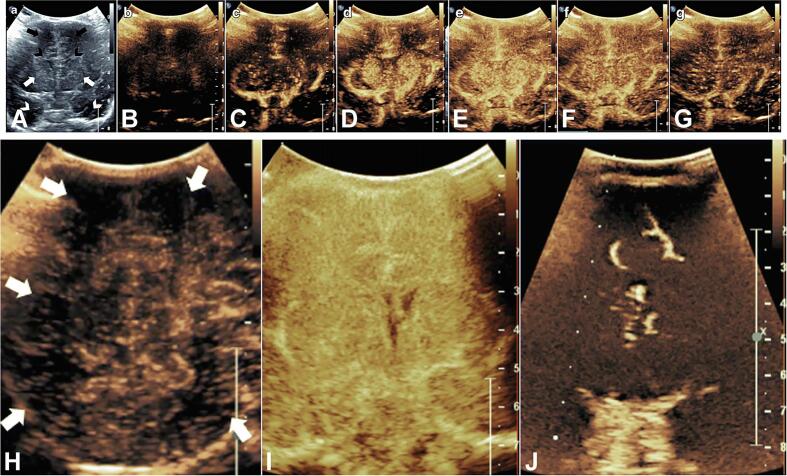
CEUS спрямований на підвищення внутрішньосудинної ехогенності шляхом введення контрастної речовини для ультразвуку: газових мікропухирців, укладених в фосфоліпідну мембрану, які стискаються і розширюються нелінійним чином під впливом ультразвукового променя. Результуючий посилений ехо-сигнал створює внутрішньосудинний контраст, в принципі схожий на зображення поперечного перерізу з використанням внутрішньосудинних контрастних агентів (зобр. 7).
Зображення 7: Ультразвук з контрастним посиленням (CEUS). A: Середньо-корональне зображення в b-режимі, що показує двосторонні лобові частки (чорні стрілки), лобові роги бокових шлуночків (чорні шеврони), базальні ганглії (білі стрілки) і скроневі частки (білі шеврони). B-G: Статичні зображення динамічного вливання мікропухирців на средньокорональних зображеннях здорового новонародженого. H: Задній тім’яно-потиличний вид новонародженого з гіпоксично-ішемічним пошкодженням, що показує дифузну гіпоперфузію з безліччю ділянок з малою кількістю мікропухирців (білі стрілки), що відображають порушення перфузії. I: корональний вид через базальні ганглії у новонародженого з дифузним гіпоксично-ішемічним пошкодженням в період відразу після травми, що демонструє дифузну гіперперфузію. J: Корональне зображення базальних гангліїв у немовляти після тривалої зупинки серця, яке демонструє дифузну гіпоперфузію. Зображення адаптовано і використано з дозволу Hwang.
Використання CEUS у новонароджених було обмежено. Хоча до 2016 року це вважалося протипоказанням для пацієнтів з серцевим шунтом, контрастні речовини для ультразвукових досліджень за минулі роки довели свою безпеку і ефективність (Appis et al., 2015). Використання контрастних агентів для УЗД як і раніше не рекомендовано для ультразвукового дослідження головного мозку і вимагає згоди батьків. CEUS може бути краще МРТ з точки зору необхідної інфраструктури, доставки контрастної речовини і витрат. Однак в даний час є мало даних, що підтверджують рутинне використання ультразвукового контрасту для візуалізації головного мозку новонароджених (Hwang, 2019).
3.2.4. Надшвидка ультразвукова візуалізація (UUI)
За останні два десятиліття в ультразвуковій візуалізації стався великий прорив з появою нових технологій, таких як UUI. Хоча лежача в основі акустична фізика така ж, як і в звичайному ультразвуку, раніше описаному в цій роботі, прогрес в електроніці та обчислювальній техніці дозволив використовувати плоскі або розбіжні хвилі.
Ці несфокусовані хвилі дозволяють реконструювати зображення за допомогою одного випромінювання. Отже, модальність може досягати частоти кадрів до 10 000 зображень в секунду. За рахунок об’єднання декількох хвиль різної орієнтації просторова роздільна здатність еквівалентна звичайному ультразвуку (до 50 мкм) (Tanter and Fink, 2014 року).
Поєднання цієї високої частоти кадрів і високого просторово-часового дозволу дозволяє використовувати передові стратегії обробки сигналів для зображення потоків крові у великих артеріях, а також більш повільних потоків в мікросудинах (зі швидкістю до 1 мм / с), що призводить до надшвидкого доплерівського сканування.
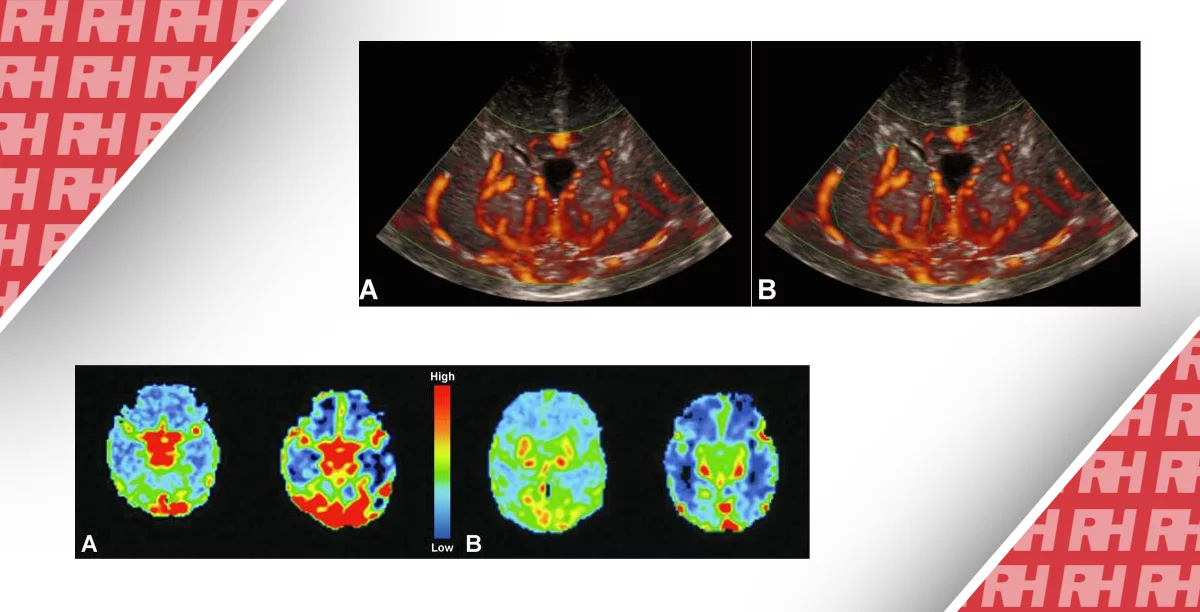
Цей метод особливо добре підходить для новонароджених, так як ультразвук може проникати глибоко в мозок (до 8 см) через тім’ячко і проводитися біля ліжка хворого. Як і у випадку зі звичайним ультразвуком, UUI не інвазивний і не вимагає іонізуючого випромінювання. За допомогою усереднення надшвидких зображень Power Doppler протягом одного серцевого циклу, карти васкуляризації мозку з високою роздільною здатністю були отримані Демени і ін. З використанням лінійного датчика (зобр. 8, A, B, C). Секторні зображення були отримані з використанням датчика з фазованою решіткою деякими авторами цієї роботи (JB, OV, JA) в лікарні для хворих дітей, Торонто, Канада (рис. 8D).
Зображення 8: Надшвидка ультразвукова візуалізація (UUI). Трансфонтанелярні надшвидкі доплерівські зображення мозку новонародженого в різних ракурсах. A: Зліва направо, коронарний, похилий парасагітальний і парасагітальний види. Колірна шкала відображає CBV з використанням функції ультразвукового доплера. B: зліва направо, сагітальний, парасагітальний і трансскроневий осьові види. Зображення Power-Doppler включають інформацію про направлення (червоний: потік до датчика, синій: потік від датчика). Видимі структури включають периклозальну артерію, вени нижче шлуночків головного мозку, коркові проникаючі артеріоли і венули, а також вілізієве коло. C: Судинні зони інтересу, відображені в сагітальній, аксіальній і парасагітальній проекціях. (A, B і C). D: Секторне надшвидке доплерівське зображення, отримане в корональній проекції.
В рамках одного і того ж збору даних також можна кількісно оцінити кровотік в будь-який цікавлячих областях з точки зору CBV і швидкості потоку. Як і в звичайному доплерівському режимі, вимірювання CBV виражаються у відносних одиницях. Таким чином, надшвидкий доплер об’єднує традиційний кольоровий доплер і імпульсно-хвильовий доплер в єдину модальність.
Аналізуючи зміни потоку під час серцевого циклу, можна оцінити і нанести на карту судинний опір кожної судини (зобр. 8C). Перші клінічні застосування виявили потенціал цього методу в вивченні перфузії головного мозку новонароджених під час гіпотермії у новонароджених. Аналіз змін кровотоку під час серцевого циклу також дозволяє диференціювати артеріальний і венозний кровотік на основі їх різного опору.
Надшвидка доплерографія – багатообіцяючий метод приліжкового моніторингу. При повторному отриманні зображень перфузії головного мозку також можна спостерігати нервово-судинний зв’язок. Перше застосування цього так званого функціонального ультразвукового методу дозволило по-новому поглянути на складну підкіркову і коркову гемодинаміку під час епілептиформних нападів.
Спостережувані спонтанні коливання CBV також виявляються різними в таламічній і корковій областях у недоношених і новонароджених у контрольній групі новонароджених.
3.3. Комп’ютерна томографія (КТ)
КТ-перфузія – це динамічне отримання послідовних КТ-зрізів після внутрішньовенного введення болюса йодованої контрастної речовини (Proisy et al., 2016).
Режим безперервного сканування (режим кіно) використовується для відстеження проходження болюса контрасту через судинну мережу головного мозку, в той час як посилення контрасту тканини зображується кривою загасання з тимчасовим дозволом. КТ-перфузія може забезпечити точну оцінку регіонального мозкового кровотоку (CBF), об’єму (CBV) і середнього часу проходження (Krishnan et al. 2017). Карти CBF, CBV і середнього часу проходження інтерпретуються за допомогою програмного забезпечення для постобробки для візуальної оцінки і кількісного аналізу.
У новонароджених менший розмір мозку і більш висока швидкість кровотоку є біологічними перешкодами, які перешкоджають здійсненню перфузії КТ в цій віковій групі. Крім того, перфузія при КТ у дітей утруднена через більш високу частоту артефактів руху, використання невеликих внутрішньовенних катетерів, які обмежують швидкість ін’єкції і збільшують час ін’єкції, і, що найбільш важливо, через іонізуючого випромінювання, яке зазвичай вимагає додаткових 1, 57 – 2,96 мЗв для комп’ютерно томографічної перфузії. Аналіз ризику і користі іонізуючого випромінювання при КТ-перфузії передбачає, що його застосування у дітей дуже обмежене (Raybaud and Barkovich, 2012).
Далеко не всі КТ-дослідження перфузії включали новонароджених. Wintermark et al. оцінили використання перфузії КТ в умовах невідкладної допомоги (Wintermark et al., 2005) і визначили вікові варіації кількісних значень перфузії при КТ у 77 дітей у віці від 7 днів до 18 років, включаючи 10 пацієнтів молодше 12 місяців (рис. 9). Значення перфузії при КТ відповідали іншим методам візуалізації і показали вікові варіації з піком перфузії у віці близько 3 років.
Зображення 9: Комп’ютерна томографія (КТ) перфузії. Розміщення областей інтересу (ROI) для аналізу регіонального об’єму церебральної крові і кровотоку в сірому (чорні області інтересу) і білому (білі області інтересу) речовинах.
3.4. Спектроскопія в ближньому інфрачервоному діапазоні (NIRS)
NIRS – це неінвазивний метод візуалізації, який використовує різні властивості оптичного поглинання біологічних структур. Біологічна тканину відносно прозора для ближнього інфрачервоного світла в так званому оптичному вікні з довжинами хвиль від 650 до 1350 нм (Smith et al., 2009). У цьому ж вікні всмоктування крові сильно залежить від концентрації оксігемоглобіну і дезоксігемоглобіну (Mohammadi-Nejad et al., 2018).
При випромінюванні ближнього інфрачервоного світла в тканини головного мозку через непошкоджений череп фотони можуть проникати в тканини на відстань кількох сантиметрів. Через багаторазове розсіювання частина цього світла досягає шкіри голови в віддаленій від випромінювача точці, де її можна знайти (зобр. 10). Дотримуючись закону Бера-Ламберта, динамічні зміни абсорбції можуть бути пов’язані зі змінами оксігемоглобіну і дезоксігемоглобіну. На основі цих концентрацій NIRS забезпечує аналіз локальних змін об’єму крові, а також споживання кисню.
Клінічно NIRS використовувався в реанімації для безперервного неінвазивного моніторингу регіональної мозкової сатурації оксигенації, що дозволяє приймати діагностичні та терапевтичні рішення (Claessens et al., 2019, Garvey and Dempsey, 2018). Однією з переваг використання NIRS є його простота і портативність, яка полягає в розміщенні оптичних датчиків або «оптодів» на шкірі новонародженого біля ліжка хворого, що можливо з урахуванням тонкої кістки черепа і відносної відсутності волосся.
Зображення 10: A – Принципи ближньої інфрачервоної спектроскопії (NIRS). Оптод пропускає інфрачервоне світло через шкіру голови і череп, тканини, які мають обмежене поглинання на цих довжинах хвиль. Приймальний оптод збирає розсіяне світло. Адаптовано з дозволу Mohammadi-Nejad et al. (Mohammadi-Nejad et al., 2018). B – Динамічні зміни абсорбції можуть бути пов’язані з концентрацією оксі- і дезоксігемоглобіну [HbO] і [HbR], що володіють різними характеристиками абсорбції, з яких потім визначаються зміна об’єму церебральної крові і оксиметрія. [HbT] – загальна концентрація гемоглобіну.
Поєднання моніторингу церебральної оксигенації з артеріальним тиском – це неінвазивний метод, який безперервно оцінює церебральну ауторегуляцію і дає можливість підтримувати стабільну церебральну перфузію і оксигенацію під час коливань артеріального тиску (Claessens et al., 2019).
Недоношені новонароджені, немовлята, які перенесли кардіохірургічні операції з приводу критичного вродженого пороку серця, а також діти, яким потрібна екстракорпоральна мембранна оксигенація, схильні до ризику придбаного пошкодження головного мозку через змінену гемодинаміки, кровотеч і / або емболічних явищ. Безперервний нейромоніторинг змін гемодинамічного статусу надзвичайно важливий для цих новонароджених в спробі виявити тих, хто схильний до більш високого ризику травми головного мозку на ранній стадії.
Було показано, що NIRS є цінним інструментом для безперервного моніторингу церебральної оксигенації, особливо для недоношених дітей (Hyttel-Sorensen et al., 2015) і для новонароджених, які перенесли кардіохірургічні операції (Hirsch et al., 2009).
Його тимчасовий дозвіл величезний (≈ 10 мс) в порівнянні з МРТ або нуклеарною візуалізацією. Він також вивчається як багатообіцяючий метод моніторингу епілепсії (Wallois et al., 2010). Крім того, функціональний NIRS – це метод нейровізуалізації, що розвивається, і здатний оцінити нервово-судинний зв’язок. Подальші поліпшення включають розробку матриць оптодів високої щільності (HD) для поліпшення просторового дозволу, що призвело до появи дифузійної оптичної томографії HD (Singh et al., 2014 року).
Головний недолік – погане просторовий дозвіл, оскільки шлях світла через тканину по суті невідомий. Дослідження глибоких структур також представляє проблему для NIRS через обмежене проникнення.
3.5. Ядерна візуалізація
Підходи ядерної медицини з використанням або однофотонної емісійної томографії (ОФЕКТ), або позитронно-емісійної томографії (ПЕТ) були розроблені для візуалізації різних фізіологічних і біохімічних процесів в мозку, який розвивається.
У ПЕТ-сканування використовуються радіоактивно мічені індикатори з короткоживучими ізотопами, що випускають позитрони, які реагують з електронами, виділяючи високоенергетичні гамма-промені, які виявляються ПЕТ-камерою. Швидкість місцевого метаболізму глюкози в головному мозку оцінюється in vivo з використанням 2-дезоксі-2 [18F] -фтор-D-глюкози (FDG) (Huang et al., 1980). На відміну від цього, в ОФЕКТ використовуються сполуки, що випромінюють гамма-випромінювання, при цьому виявлення одиночного гамма-випромінювання обмежує його просторову роздільну здатність (5-7 мм для ОФЕКТ в порівнянні з 3-4 мм для ПЕТ). Індикатори ОФЕКТ можна використовувати для оцінки церебрального кровотоку.
У той час як ПЕТ і ОФЕКТ використовувалися для вимірювання біохімічних процесів у дітей з порушеннями розвитку, ПЕТ також застосовувалася у новонароджених. Новонароджених з різними типами черепно-мозкових травм, включаючи перинатальну гіпоксію-ішемію і внутрішньошлуночкові крововиливи, оцінювали за допомогою ПЕТ (Doyle et al., 1983), і було показано, що низький метаболізм глюкози пов’язаний або зі зниженням кровотоку, або із затримкою розвитку ( Suhonen-Polvi). і ін., 1993).
Було виявлено, що результати ПЕТ протягом перших трьох тижнів життя корелюють з інтегрованою за амплітудою ЕЕГ і дозволяють прогнозувати результат розвитку нервової системи після перинатальної асфіксії (Thorngren-Jerneck et al., 2001) (зобр. 11).
Зображення 11: Позитронно-емісійна томографія (ПЕТ). Швидкість церебрального метаболізму глюкози вимірюється в підгострому періоді (10-11 днів) після перинатальної асфіксії у трьох дітей (по одному на стовпець) з різним ступенем гіпоксично-ішемічної енцефалопатії і відображається на рівні мозочка (верхній ряд), таламуса. (Середній ряд) і сенсомоторної кори (нижній ряд). У новонародженого справа розвинувся церебральний параліч з ускладненими припадками. Новонароджений зліва був здоровим при дворічному спостереженні. Адаптовано з дозволу Thorngren-Jerneck et al.
Як правило, роль ядерної візуалізації, включаючи ПЕТ і ОФЕКТ, у новонароджених дуже обмежена, враховуючи природний вплив іонізуючого випромінювання. Незважаючи на те, що вона все ще вважається відносно низькою, розрахунковий еквівалент ефективної дози на все тіло в дослідженнях, проведених Thorngren-Jerneck et al. склав 0,16-0,17 мЗв / МБк. Якщо прийняти стандартну вагу новонародженого 3,5 кг (IRCP, 2002) і слідувати керівним принципам введення радіофармпрепаратів на основі ваги (Treves et al., 2016), розрахункова введена активність складе 14 МБк, що призведе до ефективної дози приблизно 2,4 мЗв.
Поточні обмеження і перспективи неонатальної візуалізації головного мозку
Існує кілька методів візуалізації для оцінки перфузії мозку. Однак при візуалізації новонародженого безпеку і здійсненність обмежують доступні варіанти. Як описано в цьому огляді, комп’ютерна томографія і ядерна візуалізація мають технічні переваги, але властиві їм ризики, пов’язані з впливом іонізуючого випромінювання, обмежують їх використання у новонароджених. З іншого боку, NIRS вважається безпечним і легко вживаним у ліжку пацієнта, однак має обмежене застосування, враховуючи його місцеву і недосконалу оцінку перфузії мозку. У світлі цього, ультразвук і МРТ в даний час здаються найбільш підходящими методами візуалізації для відповідності обмеженням і особливостям новонароджених
Поширені запитання про візуалізацію перфузії головного мозку у новонароджених
Що таке ультразвук з контрастним посиленням (CEUS) і як він працює?
- CEUS – це метод, який використовує мікропухирці газу, укладені у фосфоліпідну мембрану, для підвищення ехогенності крові. Ці мікропухирці реагують на ультразвуковий промінь, створюючи внутрішньосудинний контраст, що дозволяє краще візуалізувати перфузію головного мозку.
Чому використання CEUS у новонароджених було обмежено?
- До 2016 року CEUS вважався протипоказаним для пацієнтів з серцевим шунтом. Хоча дослідження довели безпеку та ефективність контрастних речовин для ультразвукових досліджень, їх використання для ультразвукового дослідження головного мозку все ще вимагає згоди батьків.
Що таке надшвидка ультразвукова візуалізація (UUI) і які її переваги?
- UUI – це сучасна технологія ультразвукової візуалізації, яка дозволяє отримувати зображення з дуже високою частотою кадрів (до 10 000 зображень в секунду). Це дозволяє візуалізувати кровотік у великих артеріях і мікросудинах, є неінвазивним методом та не потребує іонізуючого випромінювання.
Що таке КТ-перфузія і які обмеження її використання у новонароджених?
- КТ-перфузія – це метод, який використовує комп’ютерну томографію для оцінки регіонального мозкового кровотоку. У новонароджених застосування КТ-перфузії обмежене через менший розмір мозку, більш високу швидкість кровотоку, артефакти руху та, головне, через вплив іонізуючого випромінювання.
Що таке спектроскопія в ближньому інфрачервоному діапазоні (NIRS) і як вона працює?
- NIRS – це неінвазивний метод візуалізації, який використовує ближнє інфрачервоне світло для аналізу змін об’єму крові, а також споживання кисню в тканинах головного мозку. Він дозволяє безперервно моніторити регіональну мозкову сатурацію оксигенації.
Які переваги та недоліки NIRS у новонароджених?
Переваги:
-
- простота, портативність, можливість безперервного моніторингу церебральної оксигенації.
Недоліки:
- погане просторовий дозвіл, обмежене проникнення для дослідження глибоких структур.
Яку роль відіграє ядерна візуалізація (ПЕТ та ОФЕКТ) у новонароджених?
- Ядерна візуалізація, включаючи ПЕТ і ОФЕКТ, використовується для візуалізації різних фізіологічних і біохімічних процесів у мозку. Однак її використання у новонароджених обмежене через вплив іонізуючого випромінювання. ПЕТ може застосовуватися для оцінки метаболізму глюкози в головному мозку.