РІШЕННЯ КОНСЕНСУСУ АМЕРИКАНСЬКОГО ЕХОКАРДІОГРАФИЧНОГО ТОВАРИСТВА ТА ЄВРОПЕЙСЬКОЇ АСОЦІАЦІЇ ЕХОКАРДІОГРАФІЇ ПРО МЕТОДОЛОГІЮ ТА ПОКАЗАННЯ. СХВАЛЕНО ЯПОНСЬКИМ ТОВАРИСТВОМ ЕХОКАРДІОГРАФІЇ
Victor Mor-Avi, PhD, FASE, Roberto M. Lang, MD, FASE, Luigi P. Badano, MD, FESC, Marek Belohlavek, MD, PhD, FESC, Nuno Miguel Cardim, MD, PhD, FESC, Genevieve Derumeaux, MD, PhD, FESC, Maurizio Galderisi, MD, FESC, Thomas Marwick, MBBS, PhD, Sherif F. Nagueh, MD, FASE, Partho P Sengupta, MBBS, FASE, Rosa Sicari, MD, PhD, FESC, Otto A. Smiseth , MD, PhD, FESC, Beverly Smulevitz, BS, RDCS, Masaaki Takeuchi, MD, PhD, FASE, James D. Thomas, MD, FASE, Mani Vannan, MBBS, Jens-Uwe Voigt, MD, FESC, and Jose Luis Zamorano , MD, FESC
|
Скорочення |
|
CRT = Серцева ресинхронізуюча терапія DTI = Тканинна доплерографія EAE = Європейська асоціація ехокардіографістов EF = Фракція викиду IBS = Integrated backscatter (інтегроване зворотне розсіювання) IVPG = Внутрішньошлуночковий градієнт тиску LV = Лівий шлуночок RV = Правий шлуночок SR = Швидкість деформації STE = Speckle-tracking ехокардіографія 3D = Тривимірна 2D = Двовимірна |
РЕЗЮМЕ
Ехокардіографічне дослідження ідеально підходить для оцінки серцевої механіки у зв’язку із її динамічною природою. Протягом багатьох десятиліть ехокардіографія була єдиним методом динамічної візуалізації серця, тому цілком природньо, що нові, більш автоматизовані техніки складного аналізу серцевої механіки були розроблені дослідниками і виробниками ультразвукового устаткування. Кілька таких методів виникли протягом останніх десятиліть для вирішення питання про роль досвіду дослідника і міждослідницької варіабельності при інтерпретації. Деякі з них були широко впроваджені ехокардіографістами по всьому світу і стали частиною повсякденної клінічної практики, в той час як інші залишилися предметом досліджень і вивчення нових клінічних додатків. Два таких методи дослідження являються домінантними на арені ехокардіографії: (1) доплерографічне вимірювання швидкості тканини, що часто називається тканинною доплерографією або міокардіальною доплерографією, а також (2) speckle tracking на основі вимірів зсуву. Обидва типи таких вимірювань надають інформацію про велику кількість параметрів функції міокарда. Мета цього документа полягає в тому, щоб зосередити увагу читача на наявних в даний час методах, що дозволяють отримати кількісну оцінку функції міокарда за допомогою візуального аналізу локальної динаміки міокарда, в тому числі тканинної доплерографії і speckle tracking ехокардіографії, а також комплексного аналізу зворотного розсіювання. Цей документ описує існуюче і потенційне клінічне застосування цих методів, їх сильні і слабкі сторони, надає короткий огляд відповідної літератури, висвітлюючи нормальні і патологічні результати дослідження в контексті різної серцево-судинної патології, а також узагальнює проблему невирішених питань, майбутні пріоритети наукових досліджень і рекомендовані показання для клінічного застосування.
1. ТЕРМІНИ І ВИЗНАЧЕННЯ: ОСНОВНІ ПАРАМЕТРИ ФУНКЦІЇ МІОКАРДА
Зсув (Displacement, d) є параметром, який визначає відстань, на яку певна ознака, такий як спекл або серцеві структури, зміщуються між двома послідовними кадрами. Зсув вимірюється в сантиметрах.
Швидкість (Velocity, v) відображає зміщення в одиницю часу, тобто, як швидко змінюється положення певної ознаки, і вимірюється в сантиметрах на секунду.
Деформація (Strain, e) описує деформації міокарда, тобто, відносну зміну довжини сегмента міокарда. Деформація є безрозмірною величиною і, як правило, виражається у відсотках. Деформація може мати позитивні або негативні значення, які відображають вкорочення або подовження, відповідно. У своєму найпростішому одновимірному прояві, 10 см струна, натягнута до 12 см, буде мати 20% позитивну деформацію.
Швидкості деформації (Strain rate, SR) є швидкістю зміни деформації і зазвичай виражається як 1/сек або сек-1.
Зсув і швидкість є векторами; тобто, на додаток до величини, вони мають і напрямок. Таким чином, можна вивчити їх різні просторові компоненти уздовж напрямків х, у і z, або, альтернативно, по анатомічних координатах камер серця, поздовжній, радіальний і циркулярний компоненти, які особливо актуальні для характеристики механіки міокарда.
Аналогічна логіка застосовна і до деформації, і SR, які забезпечують локальною інформацією про деформації міокарда. Важливою перевагою деформації і SR над зміщенням в тому, що вони відображають локальну функцію незалежно від поступального руху. Проте, по зображеннях деформації неможливо відрізнити активну від пасивної деформації. Термін ”головна деформація/principal strain” описує локальну величину і напрямок вкорочення або подовження міокарда. Термін ”глобальна деформація/global strain” або, точніше, ”глобальна поздовжня деформація” або ”глобальна циркулярна деформація”, як правило, відноситься до середньої поздовжньої або циркулярної складової деформації всього міокарда, що може бути апроксимована усередненими сегментарними компонентами деформації в окремих сегментах стінки міокарда. Значення деформації може бути виражене для кожного сегмента (”сегментарна деформація”), в якості середнього значення для всіх сегментів (”глобальна деформація”, що зазначено вище), або для кожного з теоретичних судинних областей розподілу (”територіальна деформація”).
Термін ротація лівого шлуночка (LV) відноситься до обертання міокарда навколо поздовжньої осі лівого шлуночка. Цей є зсув обертання і виражається в градусах. Як правило, основа і верхівка шлуночка обертаються в протилежних напрямках. Абсолютною різницею «верхівка до основи» при обертанні LV називають кінцевий кут повороту LV (також виражений в градусах). Термін скручування відноситься до градієнту «основа до верхівки» кута повороту вздовж довгої осі лівого шлуночка, яке виражене в градусах на сантиметр.
2. МЕТОДИ, ЩО ВИКОРИСТОВУЮТЬСЯ ДЛЯ ОЦІНКИ ЛОКАЛЬНОЇ ДИНАМІКИ СЕРЦЕВОЇ СТІНКИ
2.1. Тканинна доплерографія (Doppler Tissue Imaging (DTI))
З початку спроб реалізації концепції трекінгу руху тканини за допомогою ультразвукової доплерографії та подальший розвиток DTI за останні два десятиліття, цей метод візуалізації використовувався багатьма дослідниками для більш глибокого розуміння серцевої патофізіології та тестування ряду потенційних нових методів діагностики, про що свідчить велика кількість літератури. Хоча багато з цих методів залишаються обмеженими на дослідному терені, деякі з них отримали широке визнання і стали основним інструментом в арсеналі клінічної ехокардіографії.
Хоча безперервно-хвильовий доплерографічний аналізує зсув частоти ехо-сигналу, що повертається, в порівнянні з вихідною частотою ультразвукового променя (рис 1А), і імпульсно-хвильова, і кольорова доплерографія використовують фазовий зсув між послідовним ехо для розрахунку швидкості. У режимі імпульсно-хвильової доплерографії ультразвукові імпульси генеруються неодноразово на певній частоті повторення уздовж однієї лінії сканування, а ехо, що повертається, реєструється в заданий час після генерування кожного імпульсу, що дозволяє визначити відстань між мішенню і датчиком. Амплітуда зареєстрованих ехо-сигналів в плині часу перетворюється в спектр швидкості з використанням швидкого перетворення Фур’є (рис.1В).
Рис. 1. (А) Безперервно-хвильова доплерографія, постійна ультразвукова хвиля з частотою f0 повертається з частотою f0 + Δf, коли відбивається від рухомого об’єкта. Форма змішаного переданого і прийнятого сигналу має частоту, яка дорівнює частоті зсуву Δf. На противагу цьому, імпульсно-хвильова і кольорова доплерографія аналізують фазовий зсув між послідовними ультразвуковими імпульсами, в той час як частотний зсув ехосигналу нехтується. (В) При імпульсно-хвильовій доплерографії цей зсув фази аналізується шляхом оцінки всіх ехосигналів в одній і тій же точці часу після емісії. Вибіркові амплітуди сформують сигнал в часі, який перетворюється в спектр швидкостей за допомогою швидкого перетворення Фур’є. (С) При кольоровій доплерографії, фазовий зсув між послідовними імпульсами трансформується за допомогою автокореляції в параметри швидкості, які відображаються кодуванням у вигляді кольорових нашарувань.
У режимі кольорової доплерографії реєструється ехо уздовж всієї лінії сканування і розділяється на кілька діапазонів. Щоб визначити фазовий зсув між імпульсами у всіх діапазонах, використовується алгоритм автокореляції для перетворення фазових зрушень в значення швидкості, які відображаються, як кольорові нашарування на зображенні (рис. 1С). Хоча імпульсно-хвильова доплерографія має перевагу, оскільки надає пряме відображення кривої під час дослідження, але тільки кольорова доплерографія дозволяє проводити постобробку, в тому числі трекінг всього об’єму мішені, а також розрахунок похідних параметрів (наприклад, зсуву або SR).
Тканинна доплерографія базується на основі тих же принципів, що і імпульсно-хвильова і кольорова доплерівська ехокардіографія для кровотоку. Щоб відрізнити сигнали, що виходять при зміщенні тканини і кровотоку використовується так званий фільтр стінки, який є фільтром високих частот і застосовується для зображення швидкостей крові, або фільтр низьких частот, який використовується для відображення швидкості зсуву тканини. Оскільки інтенсивність сигналів, які генеруються міокардом вище, ніж від кровотоку, швидкості кровотоку зазвичай перевищують швидкість зсуву міокарда.
Техніка проведення DTI
Спектральна доплерографія вимагає установки контрольного об’єму, його розміру і положення так, щоб він залишався в межах міокарда протягом усього серцевого циклу. Шкала і базова лінія повинні бути відрегульовані таким чином, щоб сигнал заповнював більшу частину дисплею. Швидкість розгортки повинні бути відрегульовані згідно з додатком для вимірювання відхилень і тимчасових інтервалів: висока швидкість розгортки для вимірювання відхилень протягом декількох ударів серця і низька швидкість розгортки для вимірювання пікових значень при серії ударів серця. Деякі системи візуалізації дозволяють провести ретроспективне коригування швидкості розгортки в збережених даних без втрати якості. Посилення (Gain) має бути встановлено в значенні, яке виробляє майже чорний фон, лише з деякими слабкими включеннями шуму, щоб переконатися, що не буде втрачена важлива інформація. З іншого боку, слід бути обережним для того, щоб уникнути надмірного посилення, так як це призводить до розширення спектру і може призвести до завищення значень пікової швидкості. Хоча рухи серця є тривимірними і складними, методи доплерографії можуть виміряти тільки один компонент локального вектора швидкості уздовж лінії сканування. Тому слід бути уважним для того, щоб бути впевненим, що ультразвуковий промінь суміщений з напрямком руху, для правильного проведення дослідження (рис.2). Кут атаки не повинен перевищувати 15градусів, тим самим запобігаючи недооцінці швидкості до <4%.
Рис. 2. Доплерівські методи вимірювання швидкості в одному вимірі. (А) Вирівнювання доплерівського променя відносно стінки, що дуже важливо. (Ліворуч) Обмірювані швидкості (жовтий) занижені, якщо ультразвуковий промінь добре невирівняний з рухом під час дослідження (червоний). (Праворуч) Вузький одностінний сектор дослідження допомагає звести до мінімуму цю проблему. (В) Рух і компоненти деформації, які можуть бути оцінені з використанням доплерівських методів.
Тільки деякі напрямки руху можуть бути досліджені за допомогою доплерівських методів (рис. 2В). В апікальній проекції LV, параметри швидкості зазвичай отримують на рівні кілець і на базальному кінці базальних і середніх рівнів, і рідше в апікальних сегментах різних стінок.
Техніка проведення DTI
Кольорова доплерографія вимагає високу частоту кадрів, переважно >100 кадр/сек, а в ідеалі >140 кадрів/сек. Це може бути досягнуто за рахунок зменшення глибини і ширини сектора (в ідеалі, як в режимі градацій сірого, так і доплерівського сектора) і вибором параметрів з переважним тимчасовим, ніж просторовим дозволом. Як правило, зображення оптимізується в режимі відтінків сірого перед перемиканням в кольоровий режим дослідження. Слід проявляти обережність, щоб уникнути артефактів реверберації шляхом зміни кута атаки і положення датчика, оскільки такі артефакти можуть вплинути на значення SR на великій площі (рис. 3).
Рис. 3. Артефакти реверберації краще відображаються в напівтоновому зображенні (А) і можуть бути пропущені при кольоровій доплерографії (B). Вони стають знову очевидними на дисплеї в кольоровому кодуванні SR як паралельні жовті і сині лінії високої інтенсивності (C). Якщо взяти до уваги тільки реконструйовану криву часу такої області (D), то можуть з’являтися помилкові артефакти патологічних кривих, що імітують ”систолічне подовження” або ”постсистолічне вкорочення” (червоні стрілки).
Шкала швидкості повинна бути встановлена в діапазоні, який дозволяє уникнути накладення спектрів в будь-якій області міокарда. Повільна прокрутка зображення перед збереженням дозволяє розпізнати можливі артефакти накладення. Як і при спектральній доплерографії, напрямок руху при дослідженні повинен бути поєднаним з ультразвуковим променем. При необхідності, проводяться окремі дослідження для кожної стінки з декількох різних позицій датчика. Дані повинні бути отримані щонайменше за період трьох ударів серця, тобто за такий, що охоплює, щонайменше чотири QRS комплекси, і зберігаються в необробленому форматі даних. Старі системи візуалізації, які зберігають тільки значення кольору в зображенні, не повинні використовуватися, якщо не планується післяобробка. Оцінка доплерівських спектрів кровотоку впускних і випускних клапанів шлуночка серця дає корисну інформацію про час відкривання і закривання клапанів, і, таким чином, гемодинамічне вимірювання часу даних, отриманих з тимчасових кривих різних параметрів. Для адекватного зіставлення даних у період часу, всі дослідження повинні проводитися з однаковою частотою серцевих скорочень і кривою на ЕКГ.
Техніка проведення DTI
Дані спектральної доплерографії не можуть бути додатково оброблені. Пікові швидкості, відхилення і тимчасові інтервали вимірюються безпосередньо на спектральному дисплеї. Рис. 4 показує нормальні криві швидкості і часу, які отримані на рівні базального відділу перегородки LV і бічної стінки.
Рис. 4. Нормальні спектри тканинної доплерографії отримані біля основи перегородки (ліворуч) та основи бічної стінки (праворуч). Зверніть увагу на відмінність амплітуди і форми кривих.
Аналіз зображень DTI.
Дані кольорової доплерографії можуть бути по-різному відображені і піддані післяобробці. Різні функціональні параметри можуть бути отримані з попередньо заданої області дослідження в рамках того ж набору даних кольорової доплерографії, в тому числі: швидкість, зсув, SR і деформація (рис. 5).
Рис. 5. Функціональні параметри отримані з одного поля зору (жовта крапка) в тому ж наборі даних кольорової доплерографії: (А) швидкість, (В) зміщення, (С) SR, і (D) деформація. (Зверху) Кольорове кодування зображення. (Нижче) Відповідні криві часу. (Внизу) Електрокардіограма. Артефакти відкриття і закриття дозволяють точно визначити кардіальні інтервали часу. Відзначимо, що в цьому випадку базова лінія встановлюється довільно відповідно значення кривої (червоні стрілки), яка розпізнається автоматично на початку комплексу QRS (червона відкрита дужка). AVC – закриття аортального клапана; AVO – відкриття аортального клапана; MVC – закриття мітрального клапана; МВО – відкриття мітрального клапана.
Використовуються дві концепції відображення: кольорове кодування з або без прямого або викривленого М-режиму, і реконструйовані криві локальної функції. Колір-кодовані дані інтерпретуються найкращим чином в стоп кадрах, зокрема, на екрані в M-режимі. Таким чином, ми отримуємо легкий візуальний доступ до локального і тимчасового розподілу конкретного параметру в стінці. У подальшому можна виконати реконструкції кривої з будь-якої точки в наборі даних, що зберігаються (рис. 5). Це дозволяє відображати точний хід часу локальних швидкостей і інших параметрів. Перевагою обробки кольорової доплерографії над імпульсно-хвильовою доплерографією є те, що під час постобробки обсяг мішені може регулюватися для підстроювання під рух міокарда, таким чином залишаючись у тій же зоні протягом усього серцевого циклу. Ще однією перевагою є те, що оцінка вибірки з різних зон міокарда можлива в один і той же час.
Кольорова доплерографія для оцінки функції міокарда
У зв’язку з тим, що доплерографія генерує інформацію про швидкість, параметри швидкості – v, можуть бути отримані, в будь-якій точці і в будь-який час безпосередньо з даних кольорової доплерографії. Зсув – d, може бути отримано шляхом обчислення часового інтеграла швидкості тканини, v:
Через природу доплерівського зображення, d описує тільки компонент руху в найближенні або віддаленні від датчика зразку тканини, в той час як компоненти, перпендикулярні пучку, залишаються невідомими. Таким чином, крива руху мітрального кільця, отримана з даних кольорової доплерографії повинна мати ту ж форму і величину, що і зображення мітрального кільця в M-режимі, яке отримано в тому ж місці.
SR є тимчасовою похідною деформації. Аналітично вона ідентична просторовому градієнту швидкості тканини і, таким чином, може бути отримана з даних кольорової доплерографії як різниця між швидкостями, виміряними в двох зразках тканини 1 і 2, поділена на відстань між цими двома зразками:
Деформація може бути обчислена, як інтеграл часу SR з відповідними математичними коригуваннями:
Криві часу можуть бути отримані з даних кольорової доплерографії для кожного просторового компонента (тобто поздовжнього, радіального і циркулярного) з кожного з цих чотирьох параметрів серцевої функції (рис. 6).
Рис. 6. Сегментні SR криві поздовжніх, кругових і радіальних напрямків. Крім інверсії радіальної кривої, загальні закономірності аналогічні.
Динаміка кривої швидкості при спектральній доплерографії аналогічна отриманій при кольоровій доплерографії. Тим не менше, їх абсолютні значення відрізняються, оскільки спектральна крива зазвичай вимірюється на зовнішньому краї спектра, в той час як дані кольорової доплерографії характеризують середню швидкість локальної зони, таким чином, пікова швидкість при імпульсній доплерографії, як правило, є на 20-30 % вище, ніж виміряна при кольоровій доплерографії. Відповідно, рекомендується, щоб модальна швидкість (найбільш яскрава або темна лінія на спектральному дисплеї, залежно від дисплея) була використана для вимірювань при імпульсній доплерографії.
Потенційні «пастки» при DTI
Параметри швидкості при тканинній доплерографії можуть залежати від глобального руху серця (зсуву, кручення і обертання), зміщення суміжних структур і кровотоку. Ці ефекти не можна повністю усунути, але вони можуть бути зведені до мінімуму, шляхом використання меншого розміру мішені (що, однак, може привести до збільшення шуму на кривих) і ретельного трекінгу необхідного сегмента. Щоб звести до мінімуму вплив дихальних рухів, пацієнт повинен затримати дихання протягом декількох серцевих циклів.
Сигнал при тканинній доплерографії може бути оптимізований шляхом формування ширини ультразвукового пучка якомога більш вузьким. Хоча часова роздільна здатність має відмінний показник в М-режимі і при спектральній тканинній доплерографії, цей параметр не такий точний при кольоровій тканинній доплерографії через низьку частоту кадрів.
Апікальні проекції найбільше підходить для вимірювання більшості параметрів LV, правого шлуночка (RV) і передсердних сегментів при дослідженні паралельно руху, хоча можуть бути деякі зони з недостатньою просторовою роздільною здатністю, наприклад, поблизу верхівки, через поширенні артефакти і проблеми з проксимальною роздільною здатністю. У парастернальній проекції поздовжньої і поперечної осі, проведення тканинної доплерографії неможливо в багатьох сегментах (наприклад, в нижній частині міжшлуночкової перегородки і бічної стінки), тому що ультразвуковий промінь не може бути встановлений паралельно напрямку руху стінки. При цьому повинні бути використані модифіковані проекції, для того, щоб досягти оптимального кута зображення.
Зсув і деформація міокарда є циклічними процесами з невизначеним початком і кінцем. Таким чином, позиція базової лінії (нульової лінії) є довільною. Більшість аналітичних програмних пакетів визначають нуль автоматично, як значення на початку QRS комплексу (червоні стрілки на малюнках 5B і 5D) і відображають фактичний стан або довжину зміни по відношенню до цього значення. Хоча це і зручно для деяких ситуацій, цей підхід може не працювати в певних умовах (блокада пучків, неправильний комплекс QRS на електрокардіограмі, фібриляція передсердь і т.д.). Необхідно дотримуватися обережності в таких випадках і чітко визначити і відзначити час початку аналізу параметрів деформації або позначити (можливо, за допомогою ручного редагування) базову лінію (нульову лінію), так щоб аналогічні параметри використовувалися при повторних дослідженнях.
Крім того, інтеграція, яка використовується для обчислення зсуву і деформації часто призводить до помилкового зрушення базової лінії. Більшість комп’ютерних програм автоматично застосовують лінійну корекцію, яка застосовується в якості компенсації зсуву (рис. 7).
Рис. 7. Інтеграція даних швидкості або SR часто призводить до значних зрушень базової лінії в результаті руху або деформації (ліворуч) кривих. Більшість комп’ютерних програм дозволяють провести лінійну корекцію (праворуч). Слід зазначити, що як систоличні, так і діастолічні значення перебувають під впливом цієї корекції.
Сильні і слабкі сторони DTI
Головна сила DTI в тому, що цей метод легко доступний і дозволяє провести об’єктивну кількісну оцінку локальної динаміки міокарда. За останнє десятиліття, ця можливість стимулювала проведення великих досліджень при різних патологічних станах, які вражають функцію міокарда, на глобальному або локальному рівні, що відображено у великій кількості літератури за участю цієї методології. Також встановлено, що пікові швидкості тканини досить відтворювані, що має вирішальне значення для проведення послідовних досліджень. Крім того, спектральний імпульсний DTI має перевагу проведення онлайн виміру швидкостей і тимчасових інтервалів з відмінною часовою роздільною здатністю, що необхідно для оцінки ішемії (див. Розділ 3.6) та діастолічної функції (див. Розділ 3.5). Головним недоліком методу DTI є його кутова залежність. Як і будь-яка методика, заснована на ефекті Доплера, вона може за визначенням тільки вимірювати швидкості уздовж ультразвукового променя, в той час як компоненти швидкості, які розташовані перпендикулярно до променя залишаються непоміченими. До того ж, параметри деформації при кольоровій доплерографії і параметри SR мають багато шуму, і, як наслідок, для правильної їх інтерпретації, а також розпізнавання артефактів, необхідні підготовка і досвід.
2.2. Двовимірна (2D) Speckle-Tracking Ехокардіографія (STE)
STE відносно нова техніка для оцінки функції міокарда, зі значно меншою кутовою залежністю. Спекли, видимі у відтінках сірого на В-режимі, є результатом конструктивної і деструктивної інтерференції розсіяного ультразвуку від структур менших, ніж сама довжина хвилі ультразвуку. За допомогою цієї технології, випадковий шум фільтрується, зберігаючи при цьому невеликі, тимчасово стабільні і специфічні особливості міокарда, які називаються спеклами. Блоки або самі ядра спеклів можуть бути зареєстровані покадрово (одночасно в декількох зонах в межах площини зображення) за допомогою блоку узгодження, і дають інформацію про локальні зміщенні, з яких можуть бути отримані параметри міокардіальної функції, такі як: швидкість, деформація і SR (рис . 8).
Рис. 8. Сегментні криві деформації (D, E), виміряні 2D STE в апікальній двокамерній проекції (A, C). Контрастне магнітно-резонансне зображення того ж самого пацієнта показує білі області затримки посилення при інфаркті міокарда (B). (A) Сегменти міокарда, відповідні кривим сегментарної деформації (С). Зелені і фіолетові криві деформації отримані з трансмуральних міокардіальних сегментів, червоні і сині криві представляють субендокардіальні сегменти інфаркту, а жовті та блакитні криві – сегменти без інфаркту. (С) Кольорові кола відповідають кривим деформації (Е) в межах одного сегмента (апікального нижнього), який в основному складається з трансмурального інфаркту. Жовта крива відповідає прикордонній зоні інфаркту, а червона знаходиться в межах трансмуральної частини.
Крім того, можуть бути обчислені миттєві вектори швидкості та накладені на динамічні зображення (рис. 9). На відміну від DTI, аналіз цих векторів швидкості дозволяє оцінити кількісно деформацію і SR в будь-якому напрямку в площині зображення. Залежно від просторової роздільної здатності, може бути також проведений селективний аналіз епікардіальної, міокардіальної і ендокардіальної функції. Для методики STE була підтверджена ефективність для проведення оцінки деформації міокарда в порівнянні з ультразвуковою мікрометрією, а клінічно в порівнянні з DTI.
Рис. 9. Вектори радіальної швидкості в апікальній проекції короткої осі здорової людини (ліворуч) і пацієнта з блокадою лівої ніжки пучка Гіса (БЛНПГ) (праворуч). У здорової людини, на початку / середині систоли (А) і в пізній / кінцевій фазі систоли (B), радіальні вектори мають однакову величину і напрямок. На противагу цьому, у пацієнта з БЛНПГ, на початку / середині систоли (C) вектори перегородки мають більш високі величини, ніж бічні радіальні швидкості, в пізній систолі (D) вектори перегородки досягають свого піку, в той час як вектори бічної стінки направлені в протилежному напрямку (дисинхронія).
Техніка виконання 2D STE
Speckle tracking – це офлайн методика, який використовує раніше отримані 2D-зображення. Використання низької частоти зміни кадрів може призвести до втрати спеклів (плям), що на послідовних кадрах проявляється виходом за межі досліджуваної площині або за межі поля зору. Але з іншого боку, висока частота кадрів може бути досягнута шляхом зменшення кількості ультразвукових променів в кожному кадрі, що тим самим знижує просторову роздільну здатність і якість зображення. Тому, хоча частота кадрів 40-80 кадрів/сек і використовується в різних додатках, пов’язаних з нормальною частотою серцевих скорочень, бажано застосування більшої частоти кадрів для того, щоб уникнути недооцінки даних при тахікардії.
Фокус має бути встановлений на проміжній глибині, щоб оптимізувати зображення для режиму 2D STE, а сектор глибини і ширини повинні бути скоректовані так, щоб включати в себе якомога менше тканини за межами області дослідження. Будь-який артефакт, схожий за структурою зі спеклами, впливатиме на якість speckle tracking і це слід враховувати, щоб уникнути спотворення результатів. Для пакетів програмного забезпечення, які обробляють окремі біти, отримання даних повинне початися з ≥100 мс до піку R хвилі першого QRS комплексу і закінчуватися 200 мс після останнього QRS, щоб правильно визначати комплекс QRS, інакше це може привести до помилкової компенсації відхилення. Верхівковий ракурс серйозно впливає на результати 2D STE, і тому повинен бути зведений до мінімуму. Аналогічним чином, проекції короткої осі лівого шлуночка повинні бути круглої форми для оцінки деформації в анатомічно правильних циркулярних і радіальних напрямках.
2D STE аналіз міокардіальной механіки
Двовимірна STE дозволяє вимірювати вищезгадані чотири параметри міокардіальної механіки шляхом реєстрації груп інтраміокардіальних спеклів (в або v) або деформацію міокарда (е або SR) в площині зображення. Ефективність вимірювання цих параметрів, отриманих при STE, була підтверджена в порівнянні з ультразвуковою мікрометрією і магнітно-резонансною томографією.
Оцінка 2D деформації за допомогою STE – напівавтоматичний метод, який вимагає мануального визначення міокарда. Крім того, поле зору необхідно відрегулювати так, щоб більша частина стінки була включена в аналіз, уникаючи попадання перикарда. При автоматизованому трекінгу, при невідповідності візуальному образу руху стінки серця, поле зору необхідно відрегулювати вручну до досягнення оптимального процесу трекінгу. Для лівого шлуночка кінець систоли може бути визначений як закриття аортального клапана, що визначається в апікальній площині довгої осі серця і ця площина повинна бути проаналізована в першу чергу. Якщо закриття клапана проблематично точно розпізнати (наприклад, через склероз аорти), може бути корисно проведення спектральної доплерографії, яка відображає відтік з LV.
Оцінка 2D деформації при STE може застосовуватися для обох шлуночків і передсердь. Тим не менш, через тонкі стінки передсердь і правого шлуночка, якість сигналу може бути неоптимальною. Навпаки, всі сегменти LV можна успішно проаналізувати у більшості пацієнтів. Найкраща доступність для дослідження спостерігається для поздовжньої й циркулярної деформації, і більш проблематична для радіальної.
Час, протягом якого вимірюється пікова деформація, не є однорідним, згідно з публікаціями. Пікова деформація може бути виміряна як пікова систолічна деформація (позитивна чи негативна), як пікова деформація в кінці систоли (на момент закриття аортального клапана), або пікова деформація, незалежно від часу (в систолу або на початку діастоли). Момент часу, який використовується для вимірювання пікової деформації для оцінки систолічної функції, залежить від конкретного питання на яке потрібно відповісти.
Потенційні проблеми проведення 2D STE
Субоптимальний трекінг ендокардіальної межі може бути проблемою при виконанні STE. Іншим важливим обмеженням методу є його чутливість до акустичної тіні або реверберації, що може призвести до недооцінки істинної деформації. Тому, коли дані про деформацію з’являються у відсутності фізіологічних варіантів, якість сигналу або неоптимальний трекінг слід розглядати в якості потенційних причин. Алгоритми трекінгу використовують просторове згладжування і апріорні дані ”звичайної” функції LV, які можуть помилково вказувати на регіональну дисфункцію або вплинути на сусідні сегментні значення деформації.
При використанні STE для вимірювання скручування LV якість зображення в базальної площини короткої осі LV може бути обмеженням. Це частково пов’язано з акустичними проблемами: глибиною розташування базальної частини шлуночка і необхідністю широкого кута сектора огляду для візуалізації всієї основи LV.
Крім того, вимірювання ускладнюється через рух за межі площини дослідження, коли основа опускається до вершини в систолу. Через те, що обертання LV збільшується до вершини, дуже важливо стандартизувати зображення в апікальній площині по короткій осі. Частіше найлегше знайти правильну циркулярну апікальну проекцію вздовж короткої осі, нахиляючи датчик з апікальної чотирьохкамерної площини, а не переміщаючи його в апікальному напрямку вздовж парастернальної лінії вздовж короткої осі серця. Це також збільшує шанс захоплення циркулярної апікальної проекції по короткій осі, коли ендокард майже змикається в кінці систоли.
Дані про глобальну деформацію можуть бути неточними, якщо занадто багато значень сегментної деформації відкидаються через неоптимальність трекінгу. Це особливо вірно при локальних захворюваннях міокарда, коли значення деформації розподілені нерівномірно.
Сильні і слабкі сторони 2D STE
Обидва методи, і DTI, і STE вимірюють рух проти фіксованої зовнішньої точки в просторі (тобто датчика). Тим не менш, STE має ту перевагу, що може вимірювати цей рух в будь-якому напрямку в площині зображення, в той час як DTI обмежується визначенням компонентів швидкості з напрямком вектора до або від датчика. Ця властивість дозволяє STE проводити вимірювання циркулярних і радіальних компонентів, незалежно від напрямку пучка. Зауважимо, однак, що STE неповністю залежить від кута атаки, тому що ультразвукові зображення зазвичай мають більш високу роздільну здатність уздовж ультразвукового променя, порівняно з перпендикулярним напрямком. Таким чином, в принципі, speckle tracking працює краще для вимірювання руху і деформації в напрямку вздовж ультразвукового променя, ніж в інших напрямках. Як і при інших 2D методах візуалізації, STE покладається на хорошу якість зображення, а також можливість покадрової реєстрації морфологічних деталей зображення (тобто так, щоб вони могли бути ідентифіковані в послідовних кадрах), що не може бути виконано, коли рух об’єкта виходить з досліджуваної площини. У зв’язку з тим, що speckle tracking спирається на досить високу часову роздільну здатність, DTI може мати перевагу при оцінці пацієнтів з більш високою частотою серцевих скорочень (наприклад, при стрес-ехокардіографії) або якщо повинні бути оцінені короткочасні дані (ізоволюмічна фаза діастоли, і т.п.).
Істотним недоліком поточного використання 2D STE є різниця в апаратах різних виробників, що призводить до того, що аналіз STE здійснюється на даних, що зберігаються у власному лінійному (полярному) форматі сканування, який не може бути проаналізований за допомогою програмного забезпечення інших виробників. Існує кілька варіантів аналізу, які засновані на даних, що зберігаються в растровому (декартовому) цифровому зображення і у форматі DICOM, але на сьогоднішній день існує тільки обмежений досвід перехресного порівняння різних зображень від різних виробників. Це питання потребує подальшого дослідження, перш ніж STE може стати основним методом дослідження. В даний час на вирішення цієї проблеми спрямовані спільні зусилля Американського товариства ехокардіографії (ASE), Європейської асоціації ехокардіографії (EAE) та ультразвукової промислової індустрії.
2.3. Тривимірна (3D) STE
Хоча 2D STE є ефективним методом дослідження, він має внутрішні обмеження, характерні для 2D-зображень: використання укорочених проекцій, що впливає на точність кількісної оцінки окремих компонентів міокардіального руху. Крім того, припущення, що спекли залишаються в 2D площині дослідження і можуть бути адекватно зареєстровані протягом серцевого циклу, не завжди може бути дійсним, внаслідок комплексного 3D руху камер серця. Нездатність 2D STE методики провести вимірювання одного з трьох компонентів зміщення локального вектора є важливим обмеженням, яке впливає на точність отриманих значень локальної динаміки.
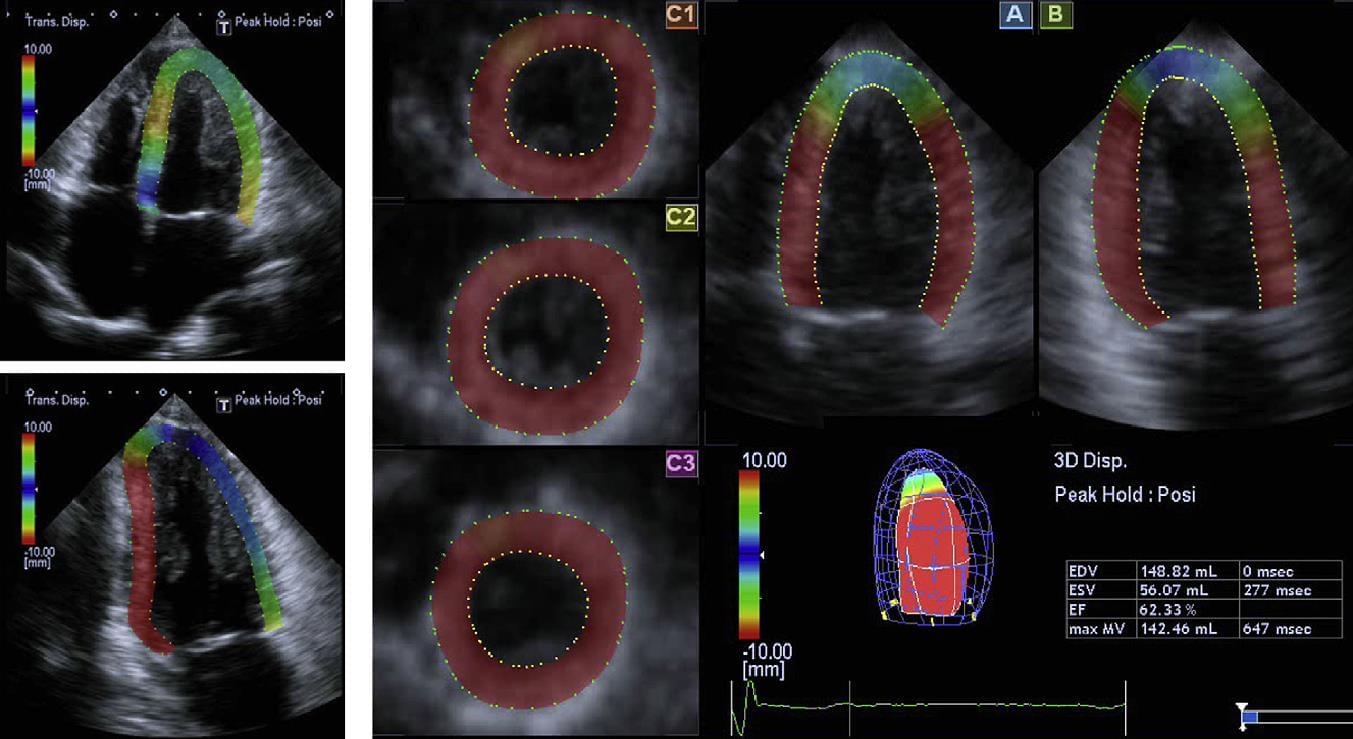
На відміну від методики 2D STE, яка не може реєструвати рух за межами площини дослідження, нещодавно розроблений метод 3D STE може реєструвати рух спеклів незалежно від їх напрямку, до тих пір, поки вони залишаються в межах обраного об’єму сканування. Кілька недавніх досліджень показали, що в окремих пацієнтів 3D STE, у порівнянні з 2D STE, призводить до більш однорідного просторового розподілу виміряних параметрів в здорових шлуночках. Цей висновок узгоджується з нормальним прикладом функції LV і тим фактом, що за допомогою 3D STE можна виміряти всі три просторові компоненти вектора зміщення міокарда (рис. 10).
Рис. 10. Приклад зображення, отриманого в кінці систоли у пацієнта з нормальною функцією LV і концентричною гіпертрофією: 2D STE (зліва зверху, апікальна чотирикамерна [A4C] проекція; внизу ліворуч, апікальна двокамерна [A2C] проекція) і 3D STE отримана з набору пірамідальних даних 3D ехокардіографії в реальному часі (праворуч, [А] і [B]: проекції A4C і A2С; [С1-С3]: проекції від верхівки до основи по короткій осі). Кольорові моделі в 2D проекціях показали значні відмінності у вимірюваному регіональному зміщенні, і це відображено в різних кольорах, незважаючи на нормальну функцію LV, що відображає рух спеклів поза площиною. На противагу цьому, 3D зрізи показали більш рівномірні кольорові моделі, відповідно з нормальними рухами стінки LV в проекціях по короткій осі, а також у апікальних проекціях, в яких можна також оцінити поступове зниження ендокардіального зсуву до вершини LV.
Дослідження 3D STE, засновані на вимірі об’ємів LV, мали гарну кореляцію з еталонними значеннями магнітно-резонансного дослідження, а рівні кореляції були вищими, ніж для вимірювань 2D STE, отриманих в одних і тих же пацієнтів, що відбивається в більш високих коефіцієнтах кореляції, меншими відхиленнями і жорсткими межами узгодження.
Хоча 3D STE генерує > 3000 векторів в об’ємі і його часова роздільна здатність така ж, як частота кадрів 3D набору даних в режимі реального часу (зазвичай 20-30 об’ємів/сек), було встановлено, що при цьому значно скорочується час дослідження (на одну третину, у порівнянні з 2D STE). Крім того, за допомогою 3D STE може бути проаналізовано значно більше число сегментів міокарда. Ця перевага 3D STE пов’язана з тим, що весь лівий шлуночок може бути проаналізований в одному об’ємі даних, отриманому в апікальній позиції датчика. Ці початкові клінічні результати показують, що 3D STE має серйозні переваги в порівнянні з 2D STE, що дозволяє провести більш швидкий і потенційно більш повний і точний аналіз функції міокарда, незважаючи на відносно низьку часову роздільну здатність.
Проведення 3D STE дослідження
Тривимірна STE може бути використана із зображеннями при 3D ехокардіографії, отриманими за допомогою матричного датчика в апікальній площині і ширококутному форматі в режимі ”повного об’єму”. У цьому режимі велику кількість клиноподібних підоб’ємів отримують протягом послідовних серцевих циклів протягом одного періоду затримки дихання і з’єднуються разом, для створення одного зразка пірамідального об’єму. Цілком імовірно, що 3D STE буде застосовний і для 3D набору даних, отриманих в режимі одного серцевого циклу, коли цей режим дозволяє візуалізувати об’єкт при досить високій частоті кадрів. Особливу увагу слід приділити включенню всієї порожнини LV в пірамідальний об’єм, інакше це може чинити негативний вплив на часову роздільну здатність.
3D STE аналіз міокардіальної деформації
Набори пірамідальних даних аналізуються за допомогою спеціалізованого програмного забезпечення – напівавтоматична 3D STE. Визначаються анатомічно правильні, нескорочені верхівкові проекції в кінці діастоли та ініціалізуються ендокардіальні і епікардіальні межі LV, 3D ендокардіальні і епікардіальні поверхні визначаються автоматично, при необхідності з ручним коригуванням. Потім ці межі визначаються в 3D-просторі автоматично протягом серцевого циклу. Для отримання інформації про локальний рух LV і деформації, шлуночок розділяється на 3D сегменти. Радіальне і поздовжнє зміщення і ротація, а також радіальна, поздовжня і циркулярна деформація, автоматично розраховуються для кожного сегмента за період часу. Крім того, розраховується зміщення у 3D просторі. Пікові значення і часовий інтервал до піку також можуть бути отримані для кожного значення, аналогічно 2D STE.
Потенційні проблеми 3D-STE
Головною проблемою методу 3D STE є його залежність від якості зображення. Випадковий шум і відносно низька часова і просторова роздільна здатність впливає на визначення межі ендокарда і епікарда. Ці проблеми в основному впливають на зв’язок локальних особливостей на зображенні від кадру до кадру, що призводить до субоптимального трекінгу міокарда. Як і з 2D STE, якість трекінгу має бути ретельно перевірено і скориговано при необхідності.
Сильні і слабкі сторони 3D STE
З теоретичної точки зору ми отримуємо перевагу, шляхом додавання третього компоненту вектора руху, який ”невидимий” і при DTI, і при 2D STE. STE 3D – багатообіцяючий метод точної оцінки регіональної динаміки шлуночків. Тим не менш, він як і раніше вимагає суворої перевірки та тестування. Зворотний бік медалі – набагато менша частота кадрів 3DE порівнянні з 2D STE може обмежувати аналіз швидких подій, таких як ізоволюмічне скорочення і релаксація. Майбутні дослідження повинні оцінити вплив щодо низької частоти кадрів.
Ще одним обмеженням є те, що ефективність цієї методики була підтверджена на основі ультразвукової мікрометрії у тварин, проте неінвазивного методу – “золотого стандарту”, який міг би бути використаний на людях для оцінки ефективності регіональної функції шлуночків у трьох вимірах, не існує. В результаті, більшість літератури по цій темі, опублікованій досі, представляє можливість проведення дослідження та потенційні переваги 3D STE, але при цьому не визначає точність методу. Клінічне значення цієї нової технології – у великій різноманітності клінічних ситуацій, таких як: вимірювання об’єму камери серця, оцінка глобальних і регіональних аномалій руху стінки міокарда, (рис. 11) і оцінка дисинхронії LV у пацієнтів з серцевою недостатністю, що залишається для визначення в майбутніх дослідженнях.
Рис. 11. На відміну від зображень на рис. 10, 3D speckle-tracking ехокардіографічні зрізи, отримані в кінці систоли у цього пацієнта, показують зменшення 3D зміщення в боковій стінці (зелені відтінки), що узгоджується з хронічним нижньобоковим інфарктом міокарда.
3D STE, навіть більше ніж 2D STE, в даний час розвивається по шляху індивідуальної специфікації для окремих виробників. Хоча ця методика і знаходиться на початковій стадії розвитку, дуже важливо рухатися в бік взаємозамінності між виробниками.
2.4. Integrated backscatter (IBS) (інтегроване зворотне розсіювання) аналіз
Аналіз IBS можна вважати першим методом, використовуваним для візуалізації міокарда, який спочатку описувався як метод, який розвивався паралельно з розвитком 2D техніки, більш ніж три десятиліття тому. IBS аналіз описує спосіб кількісної акустичної характеризації структури міокарда. При цьому аналізі потужність відбитого сигналу в кожному рядку розгортки підраховується перш ніж радіочастотний сигнал демодулюється для побудови зображення в реальному часі. Сигнал IBS відображає взаємодію між додатковими ультразвуковими хвилями і структурною неоднорідністю в міокарді, і може бути проаналізований або в часі, або в частотній області.
Реєстрація IBS сигналу
Сигнал IBS виходить зі стандартного динамічного 2D зображення, як правило, в парастернальній площині довгої осі. Однак, зображення повинні бути збережені у вихідному форматі даних для того, щоб провести IBS аналіз перед обробкою зображень.
IBS аналіз міокардіальної динаміки
Цей аналіз виконується за допомогою спеціального програмного забезпечення, яке може бути використане для двох основних цілей. Зміни зворотного розсіювання протягом серцевого циклу, як вважається, відбивають взаємодію актину та міозину в межах міофибрилярних структур. Цей процес призводить до зміни відбивної здатності, а отримані в результаті циклічні зміни, як було показано, корелюють з міокардіальною деформацією. Проблема полягає в тому, що через міокардіальну анізотропію (спрямована неоднорідність міофібрил), структура цього варіанту відрізняється від стінки до стінки і від площини до площини, і таким чином конкретні нормальні діапазони вимірювань повинні бути задокументовані для кожної стінки і для кожної проекції. Тим не менш, цей сигнал може бути використаний як неінвазивний маркер скоротливості, наприклад, при оцінці життєздатності міокарда. Другий варіант вимірювання відноситься до порівняння міокарда з іншими тканинами, для того, щоб задокументувати відбивну здатність міокарда (рис. 12).
Рис. 12. Аналіз IBS. Стардантизована backscatter обчислюється по різниці між сигналом міокарда (жовтий) і, або перикарда (червоний), або порожнини LV (синій). Циклічні зміни backscatter вимірюються зміною інтенсивності сигналу протягом систоли.
При відсутності системи відліку, цей параметр буде залежати від налаштувань при дослідженні та стану пацієнта, таким чином, цей варіант дослідження вимагає калібрування власної системи відліку (стандартизована IBS), наприклад перикард (який яскравіше міокарда) або депо крові (яке є більш темним).
Результати клінічних досліджень були детально описані в попередніх оглядах. Нормальний діапазон циклічної зміни при IBS в перетинці і задній стінці варіює від 4,5 до 6,0 дБ. Дилятаційна кардіоміопатія пов’язана з обструкцією циклічних змін відповідних областей зі зниженням функції. Точно так само, зменшення циклічних змін було зафіксовано в умовах гострого інфаркту міокарда. У життєздатному міокарді залишкові (резидуальні) циклічні зміни визначаються, навіть якщо тканина виглядає акінетичною. Циклічні зміни при IBS також знижуються при ранньому розвитку патології міокарда, наприклад при діабеті або гіпотиреозі. Точно так само, стандартизована IBS використовується в якості маркера фіброзу при різних кардіальних станах, у тому числі гіпертонічної хвороби серця і гіпертрофічної кардіоміопатії. Для оцінки наявності фіброзної тканини в цих випадках, було проведено біопсію тканин, що підтверджують дані. Крім того, IBS може визначити збільшення передсердної дегенерації, що може прогнозувати виникнення фібриляції передсердь до розширення LA.
Потенційні пастки IBS аналізу
При налашуванні зображення необхідно ретельно регулювати налаштування вихідної потужності для того, щоб бути впевненим, що сигнал не є насиченим. Це особливо проблематично при використанні відеосигналу замість радіочастотного сигналу, тому що відносини між інтенсивністю сигналу і яскравістю є нелінійними по верхньому і нижньому екстремуму інтенсивності сигналу. Ультразвуковий промінь повинен бути перпендикулярним до досліджуваної стінки, а вимірювання повинні бути виконані в межах міокарда, виключаючи ендокард, оскільки інтерфейс кров-тканина набагато яскравіший, ніж інтраміокардіальний сигнал, а це може призвести до переоцінки сигналу IBS.
Сильні і слабкі сторони IBS аналізу
Привабливою стороною цього додатку є те, що міокардіальні текстури можуть бути проаналізовані на стандартних зображеннях в градаціях сірого. Потенційно, цей метод може бути використаний для кількісної характеристики тканини незалежно від звичайних параметрів форми і функції LV. Тим не менш, існує безліч слабких місць. Методика чутлива до поганої якості зображення і шуму сигналу. Виміри, як правило, обмежується передньосептальними і задніми сегментами в парастернальній площині. Хоча й інші сегменти і проекції можуть бути досліджені, користувач повинен бути в курсі того, що нормальні значення можуть визначатися не чітко, а варіабельність сигналу вище, що пов’язано з проблемою ангуляції.
Довга історія застосування цієї техніки в порівнянні з її рідкісним клінічним використанням говорить про труднощі її виконання. Ця процедура технічно складна, наявність артефактів пов’язана з появою додаткових міокардіальних відображень ультразвуку; методика вимагає налаштування зображення і точного визначення місцезнаходження досліджуваного об’єму тканин. В епоху вимірювань деформації, існує небагато свідчень для того, щоб рекомендувати вимір циклічних змін в якості маркера скоротливості міокарда. Стандартизована IBS як і раніше має значення в якості маркера фіброзу, але, мабуть, є найбільш ефективним при складнішій патології. Таким чином, ця методика залишається більше інструментом дослідження, ніж клінічним методом.
3. ФІЗІОЛОГІЧНІ ВИМІРЮВАННЯ ФУНКЦІЇ ЛІВОГО ШЛУНОЧКА
3.1. Архітектура та вектори міокардіальної деформації LV
Знання кардіальної мікро- і макро-архітектури є корисним в розумінні відносного значення різних шарів серця у 3D деформації компонентів міокарда. Ця інформація важлива для оптимізації аналізу руху при використанні DTI і STE.
Кілька проведених досліджень вивчили 3D деформацію шлуночкової тканини, описуючи будову міоцитів, як продовження двох спіральних геометрій волокон. Субендокардіальна область показує правобічну спіральну геометрію м’язового волокна, яка поступово змінюється на лівосторонню спіральну геометрію м’язового волокна у субепікардіальній зоні. Таким чином, поздовжня вісь міокардіального шару безперервно обертається. У субендокардіальній зоні, практично всі волокна орієнтовані в поздовжньому напрямку, з кутом близько 80 град по відношенню до циркулярного напрямку. Кут зменшується до середньої стінки, де волокна орієнтовані в циркулярному напрямку (0 град), і опускаються далі до нахиленої орієнтації близько -60 град в субепікардіальній зоні (рис. 13А).
Рис. 13. Зв’язок між трансмуральними змінами напрямків міокардіальних волокон (А) і спекл зразки, що генеруються при ехокардіографії (B). Зміни напрямку волокон від правої (R) спіралі в субендокарді, в ліву (L) спіраль в субепікарді. Напрямок м’язових волокон переважно циркулярний в середній стінці. Ультразвукове зображення в апікальній чотирикамерній площині (A) (стрілки) від ортогональної до циркулярної орієнтації волокон в середній стінці. Область стінки LV, де волокна ортогональні до площини ультразвукового променя, продукує яскраві спекли і можуть бути легко ідентифіковані в перегородці і боковій стінці лівого шлуночка (B) (стрілки). LA – ліве передсердя; RA – праве передсердя; RV – правий шлуночок.
Ця структурна анізотропія стінки LV впливає на поширення та відображення ультразвукових хвиль і появу серцевої тканини на ехокардіографічних зображеннях. Велике відображення і більш яскраві спекли видно тоді, коли м’язові волокна і ультразвуковий промінь перпендикулярні один одному, а не паралельні.
Наприклад, в апікальній чотирикамерній проекції, яскраві спекли в середині міжшлуночкової перегородки являють розташування середнього шару циркулярно орієнтованих волокон, які перпендикулярні ультразвуковому променю (рис. 13В). У проекціях уздовж короткої осі, яскраві спекли видно в передніх і задніх сегментах, де міофібрильний шар перпендикулярний пучку, в той час, як значне ослаблення відбувається в перегородці і боковій стінці, де міофібрильні шари розташовані паралельно лініям сканування (рис. 14).
Рис. 14. Малюнок, що показує локальні кути зони дослідження між ультразвуковим променем і переважаючою орієнтацією м’язового волокна в проекції короткої осі. Проекція короткої осі лівого і правого шлуночка, що показує анатомію м’язового волокна з боку апікального кінця лівого шлуночка (A). Поперечний перетин лівого шлуночка показує паралельні і перпендикулярні промені по відношенню до орієнтації м’язових волокон (B). Це призводить до помітного ослаблення і зниження спеклів (стрілки) в перегородці і сегментах бічних стінок проекції короткої осі лівого шлуночка (C).
Вищевказана міокардіальна структура, в цілому, визначає компоненти деформації міокарда. У субендокардіальній області здійснюється переважно поздовжня механіка лівого шлуночка, в той час як у середній стінці і субепікардіальній зоні – переважно обертальний рух.
Поздовжна і циркулярна механіка
У перебігу пресистоли, перебудова геометрії LV призводить до одночасного вкорочення та розтягування зон, що збуджуються рано і пізно відповідно. Таким чином, вкорочення волокон субендокардіальної зони супроводжується одночасним розтягуванням субепікардіальних волокон. Сегментарні розтягнення можуть також відбуватися в регіонах субендокардіальної зони, які активуються в кінці, особливо поруч з базальною постеролатеральною зоною, яка активується останньою в шлуночку. Таким чином, початок поздовжнього і циркулярного вкорочення показує істотну трансмуральну неоднорідність, а також неоднорідність від верхівки до основи.
Скорочення субендокардіального і субепікардіального шару відбувається одночасно під час серцевого викиду. Величина циркулярної деформації під час серцевого викиду перевищує поздовжню деформацію. Крім того, поздовжня і циркулярна деформація під час викиду демонструють невеликий градієнт від верхівки до основи, наприклад, послідовна деформація вкорочення вище в апікальних і середніх сегментах в порівнянні з основою LV.
Постсистолічний період також показує значну неоднорідність на початку релаксації м’язового волокна. Подовження субепікардіальних волокон супроводжується скороченням шару субендокардіальних волокон. Ця транзиторна неоднорідність становить фізіологічне поздовжнє постсистолічне вкорочення сегментів міокарда, характерне для здорової людини.
Радіальна механіка
Продовжуючи говорити про механіку, логічно припустити, що скорочення в подовжньому і циркулярному напрямку може призвести до потовщення в радіальному напрямку для збереження об’єму тканини. Тим не менш, потовщення стінки LV не є результатом простого скорочення окремих міоцитів, а ефектом зміщення груп міоцитів відносно один одного. Одне з головних завдань міокардіальной деформації зсуву полягає в трансформації 15% скорочених міоцитів в> 40% радіальне потовщення стінки LV, що в свою чергу призводить до> 60% зміни фракції викиду LV (EF) нормального серця. У зв’язку з тим, що ступінь зсуву збільшується до субендокардіальної зони, більша деформація і потовщення виявляється в субендокардіальній зоні в порівнянні з субепікардіальною зоною. Ця різниця не відображає відмінність в скоротливій функції між шарами міокардіальної стінки, а є наслідком геометрії та нестислості тканини. Трансмуральна неоднорідність при оцінці механіки потовщення стінок серця також визначається протягом пресистолічної та постсистолічної фаз серцевого циклу.
Механіка скручування
Гвинтовий характер серцевого м’яза визначає характер його руху протягом серцевого циклу, з обертанням проти годинникової стрілки верхівки і обертанням за годинниковою стрілкою основи навколо довгої осі LV, якщо дивитися з боку верхівки.
У нормальному серці, початок вкорочення м’язового волокна відбувається спочатку в ендокарді, а потім в епікарді. Під час пресистоли субендокардіальне скорочення і субепікардіальне розтягнення сприяють короткому обертанню за годинниковою стрілкою верхівки LV. Під час викиду, активація та скорочення субепікардіальної області з великим радіусом плеча виробляють більш високий крутний момент для того, щоб визначити домінуючий напрямок обертання, в результаті чого відбувається глобальне обертання проти годинникової стрілки LV поблизу верхівки і обертання по годинниковій стрілці основи LV. Скручування і зсув субендокардіальних волокон деформують матрицю, що призводить до накопичення потенційної енергії.
Подальше відновлення після скручування, або розкручування, яке пов’язане з вивільненням накопиченої енергії сприяє діастолічному всмоктуванню, що полегшує ранню фазу наповнення LV. Наступ релаксації м’язового волокна відбувається раніше в епікарді, ніж в ендокарді. Таким чином, на початку діастоли, і субепікардіальне подовження, і субендокардіальне вкорочення полегшують розкручування в напрямку за годинниковою стрілкою. Майже від 50% до 70% розкручування LV відбувається в період ізоволюмічної релаксації, а решта завершується протягом фази раннього діастолічного наповнення. Одним з проявів цього є те, що під час систоли скручування відбувається одночасно уздовж довгої осі з радіальним скороченням, в той час як під час діастоли, розкручуванню чітко передує подовження і розширення, явище, яке ще більш помітно при фізичному навантаженні. Це призводить до лінійної залежності між скручуванням і об’ємом LV під час систоли, при цьому в діастолу крива залежності нелінійна.
Компоненти міокардіальної деформації і трансмуральної патології
Загалом, поздовжня механіка LV, яка переважно регулюється субендокардіальним шаром, найбільш вразлива і чутлива до розвитку патології міокарда. При відсутності ураження, міокардіальна і епікардіальна функція може мати нормальні або майже нормальні циркулярну механіку і параметри скручування з відносно збереженою насосною функцією LV і EF. Тим не менш, при порушені ранньої діастолічної поздовжньої механіки і редукції та / або затримці розкручування LV, може підвищуватися тиск наповнення LV і розвиватися діастолічна дисфункція. З іншого боку, гостре трансмуральне ураження чи прогресування захворювання, яке призводить до супутньої міокардіальної і субепікардіальної дисфункції, веде до редукції циркулярної механіки і скручування LV і зниження EF. Таким чином, розуміння впливу різних шарів серця на компоненти серцевої деформації допомагає правильно оцінити трансмуральну патологію міокарда та сприяє розумінню патофізіологічних механізмів дисфункції LV.
3.2. Клінічне використання зсуву, швидкості, деформації та SR лівого шлуночка
Існує велика кількість літератури з використання показників зміщення і деформації міокардіальної динаміки при безлічі патологічних станів. Нижче наведено короткий опис існуючих узагальнюючих даних.
Нормальні значення
Нормальні значення параметрів міокардіальної механіки LV варіюються залежно від специфічності стінки LV і конкретного 3D компонента кожного параметра. Для обох досліджень і DTI, і STE, поздовжні вимірювання є більш надійними, ніж радіальні. Це пов’язано з тим, що апікальне вікно дозволяє досліджувати всі сегменти міокарда LV і найбільш доступні клінічні дані відносяться до поздовжньої деформації. Поздовжні швидкості в боковій стінці вищі, ніж в перетинці. Існує також градієнт основа-верхівка, з більш високими швидкостями біля основи, ніж у верхівки LV.
Незначні відмінності визначаються між сегментами LV для значень деформації і SR, отриманих при DTI. Вимірювання, отримані при STE зазвичай показують більш високі значення у верхівкових сегментах, ніж при DTI. В межах сегмента, більш високі швидкості і деформація, як правило, реєструються в субендокардіальній зоні, ніж в субепікардіальній зоні. Швидкості і параметри деформації також залежать від віку та умов навантаження. У недавньому дослідженні у великій європейській популяції, нижні межі нормального діапазону при доплерографії були встановлені на рівні 18,5% і 44,5% для поздовжньої та радіальної деформації, і 1.00 і 2.45 сек-1 для поздовжнього й радіального параметру SR. Нормальні значення деформації змінюються від публікації до публікації і, головне, залежать від марки виробника обладнання, що використовують різні алгоритми для обробки даних вимірювань. Крім того, умови навантаження і частота серцевих скорочень повинні бути прийняті до уваги при інтерпретації всіх функціональних даних.
Опубліковані висновки. Оцінка тиску наповнення лівого шлуночка
Параметри тиску наповнення лівого шлуночка, отримані при катетеризації серця мають хорошу кореляцію з співвідношенням швидкості мітрального припливу Е до значення хвилі мітрального кільця, виміряної при DTI – (Е / е ‘) (латеральне) ≥ 12 і Е / е’ (перегородкове) ≥ 15 – корелює з підвищенням раннього діастолічного тиску LV; і Е / е ‘ (латеральне-перегородкове або середне) <8 – корелює з нормальним тиском ранньої діастоли LV.
Субклінічна патологія
Аналіз деформації і SR збільшують чутливість визначення субклінічного залучення серця в такі стани, як: амілоїдоз, цукровий діабет і гіпертонічна хвороба серця, а також зміни функції LV після лікування раку, тому що параметри е ‘ швидкості зменшуються у пацієнтів при всіх цих станах.
Констриктивна в порівнянні з рестриктивною фізіологією
У відсутності міокардіальної патології, параметри е ‘ швидкості, як правило, залишаються нормальними у пацієнтів з конструктивним перикардитом (зазвичай > 8 см / сек). На відміну від цього, внутрішні характеристики порушень міокарда при рестриктивній кардіоміопатії призводять до порушення релаксації і зниження е’ швидкості.
Серце спортсмена в порівнянні з гіпертрофічною кардіоміопатією
Існує збільшення е ‘ швидкості в серцях спортсменів, на відміну від зменшення е’ швидкості у людей з гіпертрофічною кардіоміопатією.
Рухи мітрального і тристулкового кільця
Мітральне і трикуспідальне кільця – анатомічні структури, які чітко візуалізуються при 2D ехокардіографії майже у всіх хворих, незалежно від візуалізації ендокарда. В результаті, поздовжнє зміщення кільця може бути точно оцінено у більшості пацієнтів.
Міокардіальна деформація і SR
При патологічних станах, моделі міокардіальної деформації можуть або залишатися порівнянними з нормальною картиною, але при цьому мати нижчі пікові значення, або відображати значні зміни, при прогресуванні хвороби.
Ішемічна хвороба серця
Зміни деформації не тільки сприяють діагностиці ішемізованого міокарда під час стрес-ехокардіографії (рис. 15), але також надають прогностичну інформацію.
Рис. 15. Приклад ішемічної (апікальний сегмент) і неішемічної (базальний сегмент) реакції на стрес у кривих деформації і SR. Зверніть увагу на зменшення систолічного вкорочення і вираженого післясистолічного вкорочення (ЕPS) при стрес-індукованій ішемії. AVC – закриття клапана аорти; AVO – відкриття аортального клапана; MVC – закриття мітрального клапана; MVO – відкриття мітрального клапана.
Крім того, оцінка серцевої деформації допомагає у визначенні поширеності трансмурального інфаркту міокарда та наявності життєздатного міокарда.
Кардіоміопатія
Серцева деформація і SR можуть бути знижені при кардіоміопатіях і потенційно можуть бути використані для моніторингу прогресування захворювання та впливу терапевтичного лікування. DTI і speckle-tracking ехокардіографічні вимірювання є корисними інструментами в кількісній оцінці диссинхронії LV. Тим не менш, у даний час відсутній консенсус про те, як слід вимірювати індекси диссинхронії LV в клінічній практиці.
Вроджені захворювання серця
Нещодавно проведено кілька досліджень з використанням DTI і STE для оцінки деформації міокарда у дітей, як з нормальним серцем, так і з вродженими аномаліями. Однак на сьогоднішній день дуже мало відомо про клінічну ефективність цих методів в контексті діагностики вроджених вад серця.
Невирішені проблеми та пріоритети наукових досліджень
Зростаюча кількість даних свідчить про те, що оцінка деформації LV при доплерографії або speckle-tracking методи забезпечують необхідною інформацією для клінічних досліджень. Області, які найбільш перспективні для потенційного застосування, включають в себе: оцінку ішемії міокарда та його життєздатності (див нижче), виявлення субклінічного захворювання серця, і серійна оцінка різних кардіоміопатій. Однією з основних проблем є швидкий темп технологічного зростання, що призводить до появи різних пакетів програм та алгоритмів. Майбутні клінічні випробування повинні включати: стандартизацію номенклатури, кроки в оптимізації отримання даних та оптимізацію підготовки спеціалістів для того, щоб зменшити варіабельність даних.
Резюме та рекомендовані показання
Клінічне застосування DTI або STE для вивчення параметрів міокардіального зсуву, швидкості, деформації та SR поступово стає стандартним інструментом для оцінки діастолічної функції, але як і раніше вимагає подальшого уточнення. Результати швидкості мітрального кільця, отримані при DTI за допомогою імпульсної доплерографії рекомендуються для рутинної клінічної оцінки діастолічної функції LV, як детально описано нижче в розділі 3.5. Параметри деформації, отримані як при STE, так і DTI порівнянні, але STE має переваги щодо легкості його застосування та аналізу, а також відтворюваності даних. Для обох методів, точність вимірювань залежить від якості зображення і точності трекінгу. У досвідчених руках, параметри деформації і SR можуть поліпшити точність і прогностичне значення стрес-ехокардіографії. Необхідна додаткова технічна розробка і стандартизація методології, перш ніж може бути рекомендовано додаткове клінічне застосування.
3.3. Обертання лівого шлуночка
Обертання LV або рух скручування відіграє важливу роль у систолічної та діастолічної функції. Незважаючи на те, що ротаційна деформація LV може бути визначена кількісно за допомогою кольорової DTI з високою часовим роздільною здатністю, цей метод технічно складний і не отримав широкого розповсюдження. На противагу цьому, безліч недавніх досліджень показали, що 2D STE являє собою клінічно реальну альтернативу кольоровій DTI в оцінці обертання міокарда і механіки скручування у більшості пацієнтів.
Нормальні значення
Нормальні значення для обертання LV і кута повороту мають варіабельність залежно від методу, що використовується для вимірювання, розташування області дослідження в субендокардіальній або субепікардіальній зоні, віку суб’єкта і гемодинамічного навантаження шлуночка. Недавнє дослідження великої групи здорових добровольців повідомили, що середнє значення піку кута повороту LV становить 7,7 ± 3.5º. Піковий кут повороту LV був значно більшим у суб’єктів у віці> 60 років (10.8 ± 4.9 º) в порівнянні з людьми, у віці <40 років (6.7 ± 2,9 º) і навіть у віці від 40 до 60 років (8, 0 ± 3,0 º). Збільшення кута повороту лівого шлуночка можна пояснити меншим опозиційним верхівковим обертанням, в результаті поступового зниження субендокардіальної функції з віком. Погіршення діастолічного розслаблення і зниження раннього діастолічного всмоктування пов’язано зі зниженням частоти і амплітуди розкручування. У дослідженні пацієнтів з дитинства до середнього віку, було відзначено, що скручування збільшується від 5,8 ± 1.3º в дитинстві, до 6,8 ± 2,3º в початковій школі, 8.8 ± 2.6º в підліткові роки і 13,8 ± 3, 3º в середньому віці. Верхівкове обертання є досить постійним в дитинстві, з базальним обертанням проти годинникової стрілки в дитинстві з переходом до обертання за годинниковою стрілкою у дорослих, в результаті чого параметри скручування більше в дитинстві. Згодом, скручування збільшується, в основному, через поступове збільшення апікального обертання з віком.
Опубліковані висновки
Через те, що на верхівкове обертання припадає велика частина скручування LV, порушення руху апікальної стінки значно погіршують пікові параметри скручування LV. Це може проявлятися в (1) зменшенні початкового скручування за годинниковою стрілкою в період ранньої систоли, (2) збільшенні піку скручування проти годинникової стрілки і (3) скороченні розкручування LV в ранню діастолу (рис. 16).
Рис. 16. Базальне і апікальне обертання (зелені й сині криві, відповідно) і поворот LV (червоний) протягом одного серцевого циклу у здорової людини (А) і у хворого з цукровим діабетом без гіпертрофії LV (B). Вісь часу була нормалізована до 100% тривалості систоли (з кроком 10%), з подальшою 100% тривалістю діастоли (з кроком 5%). Зверніть увагу на менш помітний початковий поворот за годинниковою стрілкою, більш високий піковий поворот і нижчє розкручування на початку діастоли у пацієнта з діабетом у порівнянні зі здоровою людиною. ES – кінець систоли.
Основні висновки, що містяться в опублікованих дослідженнях, описані нижче і узагальнені в таблиці 1.
Таблиця 1 Динаміка скручування LV при різній патології
|
Скручування LV |
Розкручування |
Час до піку розкручування |
|
|
Серцева недостатність |
|||
|
Зі збереженою LV EF |
˃ або ˄ |
˃ або ˄ |
Затримка |
|
Зі зниженої LV EF |
˅ |
˅ |
Затримка |
|
Патологія коронарних артерій |
|||
|
Субендокардіальний MI |
˃ |
˃ |
Затримка |
|
Трансмуральний MI |
˅ |
˅ |
Затримка |
|
Аортальний стеноз |
˅ |
˃ або ˄ |
Затримка |
|
Гіпертрофія LV |
|||
|
Гіпертензія |
˃ або ˄ |
˅ |
Затримка |
|
HCM |
Варіабельно |
Варіабельно |
Затримка |
|
Дилятаційна кардіоміопатія |
˅ |
˅ |
Затримка |
|
Перикардіальна патологія |
˅ |
˅ |
Затримка |
HCM – гіпертрофічна кардіоміопатія; MI – інфаркт міокарда; ˅ – знижено, підвищено; ˃ – без змін.
Синдром серцевої недостатності
На ранніх стадіях серцевої недостатності діастолічна дисфункція пов’язана з відносно збереженим або навіть високим кутом повороту LV при нормальній EF. Початок розкручування і пік розкручування на початку діастоли, тим не менш, значно затримується і можуть бути додатково виявлені під час фізичного навантаження. Пацієнти з серцевою недостатністю і зниженим EF мають прогресуюче зниження кута повороту LV і швидкості розкручування. Тим не менш, у пацієнтів з серцевою недостатністю та збереженою систолічною функцією, пік розкручування, як правило, нормальний, але може бути з затримкою у деяких пацієнтів.
Ішемічна хвороба серця
Хоча поздовжня деформація LV послаблюється в присутності субендокардіального дефіциту перфузії, циркулярна деформація LV і скручування можуть залишатися незмінними у ішемізованому міокарді. Так само, пацієнти з субендокардіальними інфарктами та збереженою EF мають знижену радіальну і подовжню деформацію, хоча циркулярна деформація LV і механіка скручування залишаються відносно збереженими. На противагу цьому, великі трансмуральні інфаркти пов’язані зі зниженням систолічного кута повороту LV і швидкості діастолічного розкручування, що корелює зі зниженою EF.
Патологія аортального клапана
Кут повороту LV значно збільшується при стенозі аортального клапана, хоча діастолічне верхівкове розкручування пролонгується в порівнянні з нормальними суб’єктами. Після заміни аортального клапана, кут повороту LV нормалізується.
Патологія мітрального клапана
Зміни в кутах повороту LV також було вивчено у хворих з мітральною регургітацією. Хронічна мітральна регургітація пов’язана з комплексною адаптивною перебудовою LV та ексцентричною гіпертрофією. Вплив хронічної мітральної регургітації на скручування, ймовірно, залежить від ступеня субклінічої систолічної дисфункції. Пікова швидкість розкручування мітрального клапана залишається нормальною, але негативно корелює з параметром кінцевого систолічного об’єму і об’ємом регургітації, припускаючи, що пікова швидкість розкручування, як і пікове систолічне скручування, залежить від стадії захворювання. Це підтверджує важливий вплив кінцевого систолічного об’єму LV на розкручування LV, тому що кінцевий систолічний об’єм LV є важливим чинником, що визначає пікову швидкість розкручування, незалежно від EF.
Кардіоміопатія
При дилятаційній кардіоміопатії, амплітуда пікового систолічного кута повороту LV змінюється пропорційно глобальної LV функція. Це зменшення кута повороту LV пов’язано з ослабленням апікального обертання LV, в той час, як базальне обертання може бути збережено. У деяких випадках, обертання верхівки може бути різко перервано, і таким чином велику частину систоли, основа і верхівка LV обертаються разом за годинниковою стрілкою в одному і тому ж напрямку. У пацієнтів, які перенесли ресинхронізуючу терапію resynchronization therapy (CRT), настає негайне поліпшення кута повороту LV і, як повідомляється, прогнозується зворотне ремоделювання LV при 6-місячному спостереженні.
Дилятаційна в порівнянні з гіпертрофічною кардіоміопатією
На відміну від ділатаційної кардіоміопатії, пацієнти з гіпертрофічною кардіоміопатією мають варіабельність у ступені закручування і розкручування LV, залежно від ступеня і розподілу гіпертрофії і обструкції. Пацієнти з гіпертрофією LV через системну гіпертензію, мають відносно збережену механіку скручування LV, хоча швидкості розкручування LV, особливо під час ізоволюмічного розслаблення, обидва параметри знижені і мають затримку. Виражена дисфункція ендокарда з відносно збереженою епікардіальною функцією призводить до аномальної поздовжньої механіки, з відносно збереженою циркулярною механікою і скручуванням при рестриктивній кардіоміопатії.
Патологія перикарда
Як і констриктивний перикардит, інша патологія перикарда має ознаки переважного порушення циркулярної механіки і скручування, з відносно збереженою субендокардіальною поздовжньою механікою.
Діастолічна функція
Під час систоли, значна кількість енергії пружності накопичується в міоцитах і інтерстиції у вигляді кручення. Ранній прояв механічної діастоли – різке розкручування, яке практично завершується до відкриття мітрального клапана. Це розкручування допомагає створити градієнт основа-верхівка внутрішньошлуночкового тиску (intraventricular pressure gradient (IVPG)), або діастолічне всмоктування на початку діастоли, що сприяє наповненню серця при низькому тиску. Дослідження здорових суб’єктів і пацієнтів з гіпертрофічною кардіоміопатією вивчили взаємозв’язок між швидкістю розкручування і IVPG у спокої і при низькому рівні (частота серцевих скорочень близько 100 уд / хв) фізичного навантаження. Було отримано дані IVPG допомогою застосування рівняння Ейлера для кольорового М-режиму трансмитрального поширення кровотоку у собак і людей. І у здорових суб’єктів, і пацієнтів з гіпертрофічною кардіоміопатією був відзначений лінійний зв’язок між швидкістю шлуночкового розкручування і піковим градієнтом діастолічного всмоктування (R = 0,72). Це відображає інше дослідження з фізичним навантаженням, яке показало, що кращим критерієм, що визначає максимальне споживання кисню міокардом у здорових суб’єктів і пацієнтів з серцевою недостатністю, була здатність збільшувати діастолічне всмоктування при фізичному навантаженні, в той же час дослідження на тваринах підтвердили, що розкручування безпосередньо пов’язане з IVPG і має зворотний зв’язок з часом шлуночкової релаксації – константою t.
Невирішені проблеми та пріоритети наукових досліджень
Відсутність стандартизації проекцій зображень і різні алгоритми speckle-tracking дослідження серед виробників призвело до неможливості порівнювати або встановлювати нормальні значення для скручування LV з високим рівнем достовірності. Проведення багатоцентрового дослідження з великою кількістю здорових суб’єктів на різних ультразвукових машинах необхідно для вирішення цієї проблеми. Крім того, розвиток 3D STE швидше за все, дозволить стандартизувати проекції LV для оцінки вимірювань торсіонних скручувань. Потім, пацієнти з популяції, що представляють захворювання, що впливають на функцію серця, повинні бути вивчені для визначення діагностичного та аномального діапазонів значень скручування LV.
Інше питання, яке потрібно уточнити, відноситься до визначень ” ротація ”, ” поворот ” і ” кручення ”. Іноді можна знайти в сучасній літературі, що ці терміни взаємозамінні. Оскільки математичні визначення необхідно чітко диференціювати між цими трьома параметрами, дуже важливо, щоб вони використовувалися правильно, як визначено в розділі 1.1.
Резюме та рекомендовані показання
Незважаючи на зростаючу кількість доказів на підтримку клінічного застосування вимірювань скручування LV за допомогою 2D STE, рутинне клінічне застосування цієї методики не рекомендується в даний час.
3.4. Диссинхронії лівого шлуночка
Ехокардіографічні підходи до візуалізації диссинхронії включають кілька методів, в тому числі М-режим, 2D, DTI (рис. 17 і 18), STE і 3D ехокардіографію.
Рис. 17. Запис швидкості при кольоровій DTI базальних, септальних і бічних сегментів стінки. Здоровий пацієнт (зверху) і пацієнт зі значною затримкою скорочення бічної стінки (внизу). Червоні стрілки вказують на різницю в часі піку септальних і бічних швидкостей.
Рис. 18. Поздовжні криві деформації ясно показують асинхронне вкорочення різних стінок LV. (А) CRT «off»: зверніть увагу на офф-фазу вкорочення в перегородці і боковій стінці, що нагадує типовий зразок блокади лівої ніжки пучка Гіса (В) CRT «on»: в основному синхронне вкорочення обох стінок під час викиду (ET), що вказує на більш ефективну функцію LV при CRT.
На сьогоднішній день, декілька досліджень вивчили можливості використання цих методів для прогнозування відповіді на CRT. Поточні керівництва визначають показання до CRT тільки на підставі клінічних даних (і симптомів серцевої недостатності за класифікацією Нью-Йоркської Асоціації серця), функції LV (EF) і електокардіографічних даних (ширина комплексу QRS). Тим не менш, приблизно третина пацієнтів з CRT не реагують на це лікування поліпшенням функції LV, що свідчить про клінічну необхідність більш чіткого відбору пацієнтів і засобів для оптимізації терапії.
Внутрішньошлуночкова диссинхронія зазвичай спостерігається у хворих із серцевою недостатністю, яка, як вважають, вказує на більш тяжке захворювання міокарда і поганий прогноз. Раніше, блокада лівої ніжки пучка Гіса була запропонована в якості основної ознаки систолічної диссинхронії. При блокаді лівої ніжки пучка Гіса або RV ритмі, відбувається активація спочатку перегородки, що призводить до перерозтягуванню ще нерухомої бічної стінки, скороченню діастолічної функції і зниженню ізоволюмічного скорочення за рахунок зменшення пікової швидкості збільшення тиску (dP / dtmax). Потім, із затримкою, бокова стінка генерує енергію скорочення, яка частково розсіюється за рахунок повторного розтягування раніше розслаблених септальних зон, знижуючи тим самим чистий серцевий викид. Дискординована активація папілярних м’язів може ще більше послабити загальну продуктивність LV за рахунок збільшення ступеня тяжкості мітральної регургітації. Диссинхронія при релаксації подовжує ізоволюмічний час релаксації і зменшує наповнення надалі.
Кілька досліджень показали примарну залежність між тривалістю QRS і механічною діссінхронією. Перетворення електричної в механічну диссинхронію модулюється обміном кальцію, взаємодією кальцію міофіламентів, регіональним навантаженням, фіброзом та іншими факторами. Тому, незважаючи на відмінності в часі регіональної механічної функції, вона може не бути строго пов’язана з електричною затримкою збудження.
Нормальні значення
У таблицях 2, 3 і 4 резюмовані параметри, отримані на основі DTI і STE, які використовуються для оцінки внутришньошлуночкової диссинхронії з опублікованими пороговими значеннями, які найбільш часто застосовуються для прогнозування зворотнього ремоделювання після CRT.
Таблиця 2. Параметри на основі DTI, які використовуються для оцінки внутрішньошлуночкової диссинхронії з опублікованими пороговими значеннями для прогнозування відповіді на CRT
|
Параметри |
Порогове значення для прогнозування відповіді на CRT |
|
Час до пікової систолічної швидкості в чотирьох базальних сегментах |
Дисперсія > 65 мс |
|
Час до пікової систолічної швидкості в шести базальних сегментах |
Дисперсія > 110 мс |
|
Час до пікової систолічної швидкості в шести базальних сегментах і шести серединних сегментах |
Стандартне відхилення> 33 мс |
|
Початок базальної руху в трьох сегментах (перегородці, бічному і задньому) |
Дисперсія> 60 мс |
Таблиця 3. Параметри на основі STE оцінки інтравентрикулярної диссинхронії з опублікованими пороговими значеннями для прогнозування відповіді на CRT
|
Параметри |
Порогове значення для прогнозування відповіді на CRT |
|
Час до пікової радіальної деформації в 2 базальних сегментах (септальний і задній) |
Дисперсія ˃ 130 msec |
|
Час до пікової поздовжньої деформації в 12 базальних і серединних сегментах |
Стандартне відхилення ˃ 60 msec |
|
Час післясистолічний скорочення швидкості в 12 базальних і серединних сегментах |
Сумарний час вкорочення ˃ 760 msec |
Таблиця 4. Параметри на основі STE і DTI, які найбільш часто використовуються для прогнозування зворотного ремоделювання після CRT.
|
Параметри |
Нормальні |
Порогове значення для прогнозування зворотнього ремоделювання |
|
Затримка піку систолічної швидкості протилежної стінки при кольоровій DTI |
˂ 60 msec |
≥ 60 msec |
|
Yu індекс (12-сегментна модель) |
˂ 30 msec |
≥ 33 msec |
|
Затримка радіальної деформації перегородка-задня стінка при STE |
˂ 40 msec |
≥ 130 msec |
|
Міжшлуночкова затримка |
˂ 20 msec |
≥ 40 msec |
|
Індекс затримки радіальної деформації при STE |
˂ 20 % |
≥ 25 % |
Опубліковані висновки
Значення міжшлуночкової диссинхронії також недавно було досліджено для прогнозування відповіді на CRT. Це дослідження показало, що в доповненні з доплерівським виміром кровоносних потоків в RV і LV, методика DTI може бути використана для порівняння початку систолічного руху базальної вільної стінки RV з базальними сегментами LV з найбільшою затримкою, використовуючи значення затримки> 56 мс, як наявність диссинхронії. Тим не менш, загальноприйнято, що внутрішньошлуночкова диссинхронія – це важливий параметр оцінки пацієнтів з серцевою недостатністю. ”Апікальний підйом”, який візуалізується на 2D ехокардіографічних знімках також нещодавно запропонований, як потенційний предиктор відповіді на CRT.
Недавній консенсус виступає за використання параметра затримки протилежної стінки при кольоровому DTI і затримку між передньосептальною радіальною деформацією і задньою (або нижньо-бічною) радіальною деформацією при STE. Також рекомендується застосування стандартного відхилення часу піку систолічної швидкості 12 сегментів або Yu індекс. З моменту публікації цього документа, додаткові дослідження показали, що вимірювання поздовжньої деформації також можуть бути корисними. Зокрема, вимірювання як радіальної, так і поздовжньої диссинхронії, має набагато більш високу точність у прогнозуванні відповіді на CRT, ніж кожен параметр окремо. Стає очевидним, що повинні бути прийняті до уваги ряд факторів, крім механічної диссинхронії, при спробі передбачити реакцію на CRT. Вони включають в себе тривалість комплексу QRS, міжшлуночкову механічну затримку і кількість рубцевої тканини та її відношення до імплантованого водія ритму LV, на додаток до імплантації водія ритму LV в безпосередній близькості до місця останньої механічної активації.
Обсерваційне багатоцентрове дослідження (предиктори відповіді на CRT) свідчить про обмежену роль вимірювань швидкості диссинхронії при кольоровий DTI в прогнозуванні відповіді на CRT. Тим не менш, це дослідження мало кілька важливих обмежень, у тому числі реєстрацію пацієнтів, які не відповідали критеріям для CRT (20% пацієнтів з EF> 35%), загальна низька доступність і відтворюваність вимірювань DTI, використання ультразвукових систем і програмного забезпечення різних виробників , у тому числі систем, які мали більш низький тимчасовий дозвіл, ніж інтервали часу, які вимірювалися.
В даний час для пацієнтів з тривалістю QRS <120 мс, існуючі дані не підтримують використання DTI або М-режиму вимірювання для відбору пацієнтів на CRT. З іншого боку, недавнє дослідження показало, що радіальна діссінхронія по STE може мати значення в прогнозуванні змін в об’ємах LV і EF після CRT у пацієнтів з тривалістю QRS від 100 до 130 мс. Було також повідомлено, що індекс диссинхронії, отриманий при вимірюванні деформації, дозволяє диференціювати пацієнтів з блокадою лівої ніжки пучка Гіса або зниженням EF LV від пацієнтів з нормальною систолічною функцією і нормальною тривалістю QRS з мінімальним перекриттям і більш ефективно виявляти пацієнтів з внутрішньошлуночкової диссинхронії, ніж при використанні параметрів DTI. Ще одне недавнє дослідження показало, що поєднання часу і величини поздовжньої деформації може прогнозувати відповідь на повторну ресинхронізацію.
Невирішені проблеми та пріоритети наукових досліджень
Оцінка механічної диссинхронії у пацієнтів з проведеною або плануванням CRT – це нова концепція, яка виникла з клінічної необхідності для більш ефективного відбору пацієнтів і способів оптимізації терапії. Хоча концепція в основному прийнята серед фахівців, незважаючи на наявні проблеми, клінічне значення цього підходу має бути більш чітко визначено. Очевидна необхідність додаткових багатоцентрових досліджень результатів у пацієнтів з хронічною серцевою недостатністю. Однак, щоб уникнути колишніх помилок і зробити різні дослідження співставними, ми спочатку повинні провести стандартизацію технічних характеристик систем візуалізації, що використовуються для оцінки диссинхронії, визначення кінцевих точок дослідження (тобто визначення пацієнтів, що реагують на CRT), даних для характеристики пацієнтів і на початку, і в ході спостереження (кількісна оцінка рубцевої тканини міокарда, кількісна оцінка об’єму LV, потреба в оптимізації пристрою і т.д.), характеристик імплантатів (тобто їх розташування по відношенню до рубця і сегменту LV з найбільшою затримкою). Крім того, варіабельність різних методів вимірювання синхронності скорочення шлуночка повинна бути оцінена в багатоцентрових дослідженнях.
Резюме та рекомендовані показання
В даний час, незважаючи на дослідження «Прогнозування відповіді на CRT» і досліджень клініки Мейо, які підтримують дані в клінічних посібниках, не визначена певна роль для ехокардіографічного вимірювання механічної диссинхронії в необхідності CRT у пацієнтів з серцевою недостатністю. Доведено потенційна роль візуалізації диссинхронії у пацієнтів з межовою тривалістю QRS, коли ця додаткова інформація може бути корисною, а також ця методологія ефективна у визначенні місця останньої механічної активації, що може бути прийняте до уваги при CRT імплантації.
3.5. Діастолічна функція
Клінічна ефективність вимірювань швидкості міокарда для оцінки діастолічної функції широко прийняті і були задокументовані раніше. Міокардіальна деформація і SR, також чутливі параметри для кількісної оцінки діастолічної функції. Діастолічні SR сигнали можуть бути записані під час ізоволюмічної релаксації (SRIVR), у початковій фазі наповнення (SRE) і в кінці діастоли (SRA). І DTI, і STE можуть бути використані для отримання сигналів діастолічної деформації.
Нормальні значення
Нормальні значення були раніше опубліковані для DTI швидкостей мітрального кільця в декількох популяціях. У дорослих, е ‘швидкість зменшується з віком; відповідно, нормальні значення в залежності від віку повинні використовуватися при складанні висновків про діастолічної функції. Тим не менш, в цілому, септальна е ‘≥ 8 см / с і латеральна е’ ≥ 10 см / с, як правило, спостерігаються у здорових людей, і знижені у пацієнтів з порушенням релаксації LV і підвищеним тиском наповнення LV (рис. 19 ). Нормальні значення деформації і SR поки ще не встановлені.
Рис. 19. DTI швидкості, виміряні у пацієнта з порушенням релаксації LV і підвищеним тиском наповнення LV: мітральний приплив (вгорі) і швидкості мітрального кільця, отримані при DTI в септальних (внизу зліва) і бічних (внизу праворуч) частинах кільця. Зверніть увагу на зниження е ‘швидкості і підвищеня співвідношення E /е’.
Опубліковані висновки
Діастолічні значення SR надають важливу інформацію про діастолічну функцію LV. Воно включає в себе оцінку післясистолічної міокардіальної деформації, яка розвивається в умовах ішемії, електричної і механічної диссинхронії. Також встановлено тісний зв’язок з затримкою регіональної релаксації в умовах ішемії і диссинхронії. Гемодинамічні детермінанти SRЕ включають: релаксацію LV, регіональну діастолічну жорсткість, систолічну функцію, напругу стінки в кінці систоли і тиск наповнення. Крім того, SRЕ може оцінити інтерстиціальний фіброз, а також може бути використаний для ідентифікації життєздатного міокарда після забиття та інфаркту.
Кілька досліджень показали значну кореляцію між сегментарною SRE і постійним часом релаксації LV. Тим не менше, існують проблеми з екстраполяцією висновків регіональної SRE на глобальну діастолічну функцію. Це обмеження можна обійти, використовуючи дані з усіх сегментів міокарда. У зв’язку з цим, були опубліковані два дослідження, присвячені глобальній SRIVR і SRE за даними STE. Обидва дослідження показали, що ці виміри доступні і легко відтворювані і пов’язані з константою часу релаксації LV. Тим не менш, в дослідженні, в якому виконано порівняння «обличчям до обличчя» між SRIVR і SRE, SRIVR має велику кореляцію з константою часу релаксації LV. Відношення E до SRIVR було ефективно в прогнозуванні тиску наповнення LV у хворих, у яких співвідношення E / e’ було неінформативним і було більш точним, ніж E / e’ у пацієнтів з нормальним значенням EF і з регіональною дисфункцією. Зовсім недавно було показано, що SRIVR, має інкрементне прогностичне значення у хворих з інфарктом міокарда з підйомом ST-сегмента.
Існують і інші показники діастолічної функції, в тому числі деформація лівого передсердя (LA) під час систоли LV і розкручування LV, включаючи можливість вимірювання параметрів на початку і в кінці-діастоли, як відповідних маркерів релаксації і піддатливості міокарда. До того ж, в даний час існує можливість ефективного визначення мінімального систолічного порушення поздовжньої функції LV у пацієнтів з серцевою недостатністю та збереженою систолічною функцією, що підтверджує той факт, що систолічна і діастолічна функції LV неподільні. Це було продемонстровано шляхом вимірювань деформації і розкручування.
Невирішені питання
Хоча наведені вище показники діастолічної функції є перспективними, вони мають обмеження, які включають в себе: необхідність високого співвідношення сигнал-шум, задовільну міокардіальну візуалізацію верхівкових проекцій, досвід проведення дослідження і роботи з алгоритмами аналізу, тривалий час автономного аналізу деформації в порівнянні з вимірами швидкості і більш низька частота кадрів для сигналів, отриманих за допомогою STE.
Резюме та рекомендовані показання
DTI вимірювання швидкостей мітрального кільця при імпульсно-хвильової доплерографії рекомендуються для рутинної клінічної оцінки діастолічної функції LV. Вимірювання діастолічної деформації і SR може бути корисно для дослідницьких цілей, але в даний час не рекомендується для рутинного клінічного використання.
3.6. Ішемія міокарда
Звичайна ехокардіографічна оцінка регіональної функції міокарда заснована на вимірі потовщення стінки і не надає інформацію, що стосується трансмурального розподілу скорочення волокон. Аналіз потовщення волокна між різними шарами стінки міокарда є важливим в диференційній діагностиці різних моделей скорочувальних порушень, які можуть виникати під час гострої або хронічної (гібернація) ішемії міокарда. Ішемічний міокард характеризується зниженням або відсутністю регіонального систолічного поздовжнього і циркулярного вкорочення і радіального потовщення. Постсистолічне вкорочення після закриття аортального клапана – часта знахідка при гострій ішемії.
Нормальні значення
Існує значна доказова база в літературі про те, що глобальна пікова систолічна деформація варіює в діапазоні від -16% до -20% і глобальне пікове систолічне значення SR <-0,9 сек-1 – вельми чутливі і специфічні для виявлення хворих на ранній стадії інфаркту міокарда.
Опубліковані дані
Метод DTI використовується для кількісної оцінки впливу ішемії міокарда на його функцію. Експериментально індукована міокардіальна ішемія у свиней приводила до значного швидкого зниження систолічних швидкостей, помітного збільшення швидкості ізоволюмічної релаксації (що визначає післясистолічний рух) і раннього зменшення співвідношення ранніх і кінцевих діастолічних швидкостей в межах 5 сек ішемічної оклюзії. Хоча зниження систолічної швидкості значно корелює з систолічним вкороченням і регіональним міокардіальним кровотоком під час зменшення кровотоку по коронарних артеріях, систолічні швидкості злегка переоцінюють ступінь регіональних аномалій руху стінки і не диференціюють ішемію від реперфузійно-індукованої скорочувальної дисфункції. У хворих з хронічною обструкцією коронарної артерії, аномалії поздовжнього скорочення спостерігалися за допомогою DTI. Функціональні порушення, індуковані інфарктом міокарда та ішемією, відображаються зниженням піку систолічної швидкості у залученому міокарді, зокрема, у відповідних частинах мітрального кільця, в той же час і віддалені сегменти також можуть бути порушені. Тим не менш, виявити відмінності між регіональними і глобальними змінами скоротливої функції не можливо.
На додаток до фізіологічної оцінки поздовжньої функції LV, перевага DTI у візуальному відображенні і кількісній оцінці функції міокарда. Експериментальні результати показали, що DTI дозволяє оцінити регіональну функцію міокарда протягом серцевого циклу і є чутливим методом, як до інотропної стимуляції, так і ішемічної. Клінічні дослідження показали можливість застосування DTI при стрес-ехокардіографії, але відтворюваність методу не була оптимальною, а точність не кращою, ніж при візуальній інтерпретації експертом. Крім того, регіональна оцінка складна в середньошлуночкових сегментах і практично неможлива на верхівці, оскільки поздовжній систолічний рух стінки у верхівки є мінімальним, і, отже, швидкості міокарда є занадто низькими і варіабельними для точної діагностики аномалій верхівкових рухів стінки. Хоча пікові систолічні швидкості, отримані при DTI, як правило, знижуються під час ішемії, кілька експериментальних досліджень продемонстрували обмежену здатність методики розрізняти різні стадії ішемічної дисфункції і диференціювати ішемічну від післяішемічної дисфункції.
Експериментальні дослідження показали, що значення SR, отримані при DTI, можуть бути корисними у виявленні та кількісній оцінці порушень при ішемії міокарда та виявленні життєздатного міокарда, коли значення SR нормалізувалися в уражених областях після інотропної проби з добутаміном або діпірідамолом. Клінічні дослідження показали здатність значень деформації, отриманих при доплерографії, допомагати у виявленні ішемії міокарда після інотропної проби з добутаміном під час стрес-ехокардіографії і додаткову прогностичну цінність вимірювань пікового систолічного значення SR.
Ефективність значень деформації, отриманих при двовимірній STE була підтверджена експериментально, показуючи хорошу відтворюваність значень поздовжньої і циркулярної деформації. Чутливість і специфічність STE значень радіальної і циркулярної деформації для діагностики сегментарної дисфункції шлуночка є достатніми для диференціальної діагностики нормокінетичних від гипокинетичних або акінетічних сегментів, в порівнянні з серцевою магнітно-резонансною томографією. Глобальна поздовжня деформація, отримана з апікальної проекції, використовується в якості індексу серцевої функції, як додаткові прогностичні значення до клінічних параметрів і EF LV.
STE значення деформації є корисними параметрами для виявлення міокардіальної ішемії в умовах стрес-тестування і мають добру відтворюваність через їх, здебільшого, автоматизовану природу, що є особливо важливою перевагою для недосвідчених дослідників. Поздовжня і циркулярна деформація при STE були оцінені під час інфузії добутаміну у свиней під наркозом з різним ступенем коронарної оклюзії. Вплив оклюзії коронарної артерії на різні компоненти деформації було більш виразним при інфузії добутаміну (рис. 20). Перші дослідження на людях показали високий рівень можливості виконання цього дослідження при тесті з фізичним навантаженням і інфузії добутаміну з аналогічною точністю DTI значень деформації в оцінці циркуляції передньої стінки, проте низьку точність для задньої стінки.
Рис. 20. Двовимірне speckle-tracking ехокардіографічне зображення верхівки, отриманого у свині під час коронарної оклюзії у спокої (А) і на піку дози добутаміну (B), показує зниження глобальної поздовжньої деформації (GS). Кількісна оцінка швидкості та напрямки векторів по глобальній деформації допомагають описати рух у комплексній і кількісній моделях.
Невирішені проблеми та пріоритети наукових досліджень
Не всі клінічні дослідження одностайно підтвердили переваги даних експериментальних досліджень, порівнянність значень SR і візуалізації швидкості тканини для діагностики ішемічної хвороби серця та зіставну точність у порівнянні з візуальною інтерпретацією експертом. Здатність STE значень деформації виявляти ранні фази ішемічної відповіді у пацієнтів з болем у грудній клітці повинна бути ще перевірена. Пікові амплітуди швидкості при DTI і значення деформації залежать від кута падіння променя на стінку міокарда та якості зображення, цю методику дуже часто важко використовувати в апікальних сегментах. Для значень деформації як на основі STE, так і на основі DTI, необхідний значний досвід для досягнення достатньої точності і відтворюваності дослідження.
Резюме та рекомендовані показання
Пряме спостереження систолічної дисфункції, що розвивається, в поєднанні з післясистолічним вкороченням, свідчить про гостру ішемію міокарда. Проте, відсутність клінічних випробувань не дозволяє рекомендувати конкретні параметри для диференціальної діагностики різних станів гострої і хронічної ішемії, коли вихідні дані не доступні.
3.7. Фіброз і життєздатність міокарда
Виявлення фіброзу міокарда та життєздатності залежить від оцінки як характеристик тканини міокарда, так і зміни форми міокарда протягом серцевого циклу. Фіброзні тканини можуть розташовуватися або фокально (як це відбувається у хворих, які перенесли інфаркт міокарда), або дифузно (як це відбувається у відповідь на збільшення післянавантаження або метаболічні порушення). Фіброз найбільш легко ідентифікувати за допомогою пізнього міокардіального посилення кардіальної магнітно-резонансної томографії, але також може бути виявлений при використанні різних методів ехокардіографії, в тому числі зображень деформації. Дифузний фіброз важко виміряти. Його вплив на підвищену відбивну здатність тканини може бути виміряний за допомогою стандартизованого аналізу Integrated backscatter (інтегроване зворотне розсіювання) (див. Розділ 2.4). При цьому можуть бути виявлені тканинноспецифічні особливості, які іноді згадуються як ознака ” подвійний пік “, який характеризується зразком, що складається з нерегулярного раннього систолічного піку з наступним швидким падінням SR близько до нуля, а другий пік – у фазі ізоволюмічної релаксації.
Зміни у формі міокарда можуть бути оцінені з використанням стандартного зображення, DTI або STE. Відмінності між цими підходами були описані вище. Для оцінки життєздатності міокарда, привабливість доплерографії полягає в її високій часовій роздільній здатності, що дозволяє точно охарактеризувати короткі тимчасові явища, такі як післясистолічне потовщення і ізоволюмічне скорочення. З іншого боку привабливість методики STE полягає в її здатності проводити вимірювання в будь-якій площині, незалежно від напрямку ультразвукового променя, його відносна стійкість до шуму сигналу (зокрема уникнення накладення) і вимір деформації у всіх площинах (поздовжньої, радіальної і циркулярної) з можливістю вимірювання зсуву деформації між шарами міокарда.
Основні показання для цих методів були: визначення та кількісна оцінка глобального фіброзного процесу, існуючих порушень руху стінки і оцінка життєздатності міокарда. Дифузний фіброз міокарда сприяє порушенню наповнення шлуночків, особливо зниженню податливості LV і може бути присутнім в умовах перевантаження тиском, таких як стеноз аорти, а також при патологічних станах порушенні обміну, таких як діабет і ожиріння. Хоча ідентифікація компонентів дисфункції міокарда (наприклад, фіброз) є важливим кроком у плануванні таргетної терапії для такого багатофакторного процесу, як діастолічна дисфункція, терапевтичні застосування цих специфічних даних залишаються невизначеними.
Визначення аномалій руху стінки у спокої, пов’язаних з вогнищевим фіброзом, вважається одним з найскладніших аспектів ехокардіографічної інтерпретації і є дослідженням, яке вимагає хорошої підготовки і досвіду.
Нормальні значення
Нормальна поздовжня систолічна деформація становить ≥ 18%, зі стандартним відхиленням від 2% до 3%. Вимірювання ≤ 12%, безумовно, являє собою ненормальне значення. Є істотні відмінності навіть між нормальними сегментами, а визначення нормального діапазону визначається індувідуальною мінливістю кожної зони (таблиця 5), між здоровими людьми за віком, а також в залежності від гемодинамічних станів.
Опубліковані висновки
Клінічні дослідження підтвердили надійність кількісного підходу в порівнянні з експертними аналізами дослідників і, зокрема, підкреслили, зменшення варіацій вимірювання деформації для визначення регіонального порушення руху стінки в порівнянні з візуальною оцінкою.
Життєздатність міокарда може бути оцінена як у спокої, так і у відповідь на інотропну стимуляцію. Акінетичний або строго гіпокінетичний міокард, який показує залишкову подовжню деформацію, може бути визнаний як життєздатний. У цих ситуаціях, часто виникає проблема невеликого зниження субендокардіальної функції у спокої, з функціональним резервом, що виходить зі скорочення середніх і епікардіальних компонентів стінки. Трансміокардіальний розподіл потовщення може бути документовано шляхом диференціації між різними компонентами деформації міокарда.
Таблиця 5. Нормальні параметри поздовжньої систолічної деформації, які отримані при різних техніках і опубліковані в літературі
|
Дослідження |
Методика |
n |
Вік (р) |
Средня деформація (%) |
Септальна (%) |
Латеральна (%) |
Нижня (%) |
Передня (%) |
|
Moore та ін.. |
МРТ |
31 |
37 ± 2 |
16 ± 3 |
||||
|
Базальна |
14±3 |
15±3 |
15±3 |
15 ± 3 |
||||
|
Середньовентрикулярна |
15±3 |
14±4 |
15±3 |
15 ± 3 |
||||
|
Апікальна |
18±4 |
19±3 |
18±4 |
19 ± 3 |
||||
|
Edvardsen та ін.. |
МРТ |
11 |
41 ± 13 |
18 ± 4 |
||||
|
Базальна |
17±3 |
18±4 |
18±4 |
17±3 |
||||
|
Апікальна |
19±5 |
17±4 |
19±3 |
18±4 |
||||
|
Edvardsen та ін.. |
DTI |
33 |
41 ± 13 |
19± 4 |
||||
|
Базальна |
17±3 |
18±4 |
5±5 |
19±4 |
||||
|
Апікальна |
19±4 |
17±3 |
6±5 |
18±5 |
||||
|
Kowalski та ін… |
DTI |
40 |
29 ± 5 |
17± 5 |
||||
|
Базальна |
21±5 |
13±4 |
15±5 |
17±6 |
||||
|
Середньовентрикулярна |
21±5 |
14±4 |
16±5 |
17±6 |
||||
|
Апікальна |
23±4 |
15±5 |
18±5 |
18±6 |
||||
|
Sun та ін.. |
DTI |
100 |
43 ± 15 |
18 ± 5 |
||||
|
Базальна |
18±5 |
18±7 |
15±6 |
22±8 |
||||
|
Середньовентрикулярна |
18±1 |
19±5 |
14±5 |
18±6 |
||||
|
Апікальна |
19±6 |
18±6 |
24±5 |
13±6 |
||||
|
Marwick та ін.. |
2D STE |
242 |
51 ± 12 |
19 ± 5 |
||||
|
Базальна |
14±4 |
18±5 |
17±4 |
20±4 |
||||
|
Середньовентрикулярна |
19±3 |
18±3 |
20±4 |
19±3 |
||||
|
Апікальна |
22±5 |
19±5 |
23±5 |
19±5 |
Поздовжня деформація піддається порушенню на порівняно ранньому етапі розвитку ішемічної хвороби та ключовими моментами наявності субендокардіального інфаркту міокарда або ішемії можуть бути розбіжності між значеннями поздовжньої і радіальної деформації. Ступінь зниження радіальної деформації була використана в якості маркера збільшення протяжності трансміокардіального рубця, а також у визначенні нетрансмурального інфаркту міокарда. Недавнє дослідження показало, що пряме вимірювання трансміокардіального градієнта деформації при STE може надати аналогічну інформацію. Тим не менш, цей підхід може забезпечити інформативними результатами, якщо роздільна здатність зображення в напрямку дослідження достатня.
Початкова перевірка адекватності відповіді міокарда на інотропний стимул, такий як добутамін, в якості маркера життєздатності, проводилася майже десять років тому, в порівнянні з позитрон емісійною томографією. Це дослідження показало, що сегменти з невідповідністю перфузійного метаболізму мали регіональний скоротливий резерв, що було відображено збільшенням SR у відповідь на добутамін. Подальші дослідження документально підтвердили, що збільшення SR у відповідь на добутамін було пов’язано з подальшим функціональним відновленням сегментів, а також були визначені порогові значення для деформації і SR, або змін цих параметрів, які відповідали наступному функціональному відновленню. Подальші роботи в цій області підтвердили ці порогові значення.
Найбільш надійною ехокардіографічною ознакою того, що міокард, швидше за все, почав відновлюватися після реваскуляризації, є двофазна відповідь, коли знижена базова функція поліпшується при ізотропній стимуляції (як правило, з тестом з добутаміном), але погіршується при достатньому навантаженні, що перевищує резерв перфузії і провокує ішемію. Малюнки 21, 22 і 23 показують приклади досліджень передбачуваної ішемії та життєздатності міокарда.
Рис. 21. Застосування зображень SR полегшує діагностику життєздатного міокарда. У спокої, обидва перегородкових сегмента показують знижене значення SR, а апікальний також демонструє затримку. У відповідь на низькі дози добутаміну, обидва перегородкових сегмента показують збільшення SR, яке стає більш синхронним. Бічна стінка (червоний) використовується в якості нормального опорного сегмента.
Рис. 22. Застосування зображень деформації, отриманих на основі швидкості тканини, для розпізнавання двухфазної відповіді. При низькій дозі добутаміна, обидва перегородкових сегмента показують нормальну деформацію, з синхронією. При піковій дозі добутаміна, базальний перегородковий сегмент (жовтий) показує збільшення деформації, а середньоапікальний сегмент (синій) показує незначне зниження і затримку.
Рис. 23. Застосування зображень деформації, отриманих на основі швидкості тканини, для розпізнавання монофазної відповіді. У спокої, обидва нижніх сегмента показують зменшення деформації. При низькій дозі добутаміна починається збільшення деформації. При пікової дозі добутаміна, у середньонижнього сегмента (синій) деформація не збільшується, а у базального сегмента (жовтий) продовжує збільшуватися і надалі.
Експерименти на тваринах показали, що найбільш надійним маркером скоротливості у відповідь на стрес (навантаження) є SR, ніж деформація. Нормальна реакція SR на збільшення дози добутаміну – продовження збільшення значення, в той час як нормальна відповідь значення деформації на добутамін проявляється початковим ростом, а потім плато або незначне зниження зі збільшенням серцевого ритму і падінням ударного об’єму. Післясистолічне вкорочення може бути корисним маркером життєздатного міокарда, особливо якщо воно нормалізується у відповідь на добутамін.
Невирішені проблеми та пріоритети наукових досліджень
Хоча виявлення фіброзу міокарда та оцінки життєздатності міокарда довели ефективність програмного забезпечення візуалізації деформації, інтерпретація мінімальних змін потовщення міокарда та відповіді на добутамін досить ускладнена, залежить від підготовки і досвіду і показує значну варіабельність між дослідниками, навіть при використанні стандартних критеріїв оцінки. Необхідні додаткові дослідження в цій області.
Резюме та рекомендовані показання
Місце аналізу деформації у визначенні та оцінці фіброзу та життєздатності міокарда є основним питанням проведеного розслідування. В даний час переконливий доказ для оцінки життєздатності міокарда стосується комбінації деформації і низьких доз добутаміну. Незважаючи на те, що були отримані обнадійливі результати використання аналізу деформації для розпізнавання фіброзу і визначення відмінностей нетрансмурального рубця в умовах аномалій руху стінок у фазі релаксації, клінічне застосування цієї методики не рекомендується в даний час.
4. ФІЗІОЛОГІЧНІ ВИМІРЮВАННЯ ПРАВОГО ШЛУНОЧКА І ФУНКЦІЇ ЛІВОГО І ПРАВОГО ПЕРЕДСЕРДЯ
4.1. Правий шлуночок
Стінки RV тонші, ніж міокард LV, а самі шлуночки мають різні форми. Це пов’язано з низьким тиском в легеневому колі кровообігу. Тонкостінний і податливий правий шлуночок має швидку адаптацію при змінах переднавантаження. Збільшення післянавантаження RV призводить до збільшення деформації його стінки, до тих пір, поки товщина стінок камери не збільшується або внутрішній радіус камери зменшується. Нормальне скорочення RV відбувається в послідовному порядку, а перистальтична хвиля спрямована від зони припливу до воронки. Поздовжнє вкорочення – основний компонент загальної функції RV з рівноцінною участю вільної стінки RV і міжшлуночкової перегородки. Оцінка функції RV за допомогою звичайної 2D-ехокардіографії є складним завданням через складну геометрію RV і сильно трабекулярного внутрішнього контуру стінки. Залежність більшості звичайних ехокардіографічних параметрів від навантаження, додає ще одну проблему для функціональної оцінки RV.
Простий кількісний підхід до оцінки поздовжньої функції RV – це вимірювання систолічної екскурсії в проекції тристулкового кільця, яке оцінює рівень систолічної екскурсії кільця бічного трикуспідального клапана у напрямку до верхівки в чотирикамерній проекції серця. Вимірювання систолічної екскурсії в проекції тристулкового кільця продемонструвало відмінну кореляцію зі значенням EF RV (фракціх викиду ПШ), отримане при радіоізотопної вентрикулографії і виявилося сильним предиктором прогнозу при серцевій недостатності. Тим не менш, це дослідження може бути кут залежним, якщо зображення збільшеного правого шлуночка виходить за вісь дослідження, а також може залежати від поступального руху.
DTI і STE надають показники функції RV. DTI дозволяє проводити кількісну оцінку систолічного і діастолічного поздовжнього руху RV за допомогою вимірювання швидкостей міокарда в апікальній чотирикамерній проекції. Двовимірна кольорова DTI дозволяє досліджувати декількох сегментів одночасно. Імпульсно-хвильова DTI вивчає функцію RV шляхом запису швидкостей тристулкового кільця, які корелюють з функцією RV, оскільки поздовжнє зміщення основи RV становить більшу частину зміни загального об’єму RV в порівнянні з радіальним вкороченням нормальних шлуночків.
Систолічна функція RV може бути оцінена шляхом вимірювання систолічних швидкостей при DTI і ізоволюмічного міокардіального прискорення, яке розраховується шляхом поділення максимальної ізоволюмічної міокардіальної швидкості на час до пікової швидкості і має ту перевагу, що воно менш схильне до впливу форми RV і умов навантаження, ніж систолічні швидкості. Експериментальне дослідження виявили, що ізоволюмічне прискорення міокарда є найбільш надійним показником скоротливості серед різних швидкісних параметрів у порівнянні з систолічною еластичністю. На додаток до систолічних швидкостей, імпульсно-хвильова DTI також може бути використана для вимірювання піку швидкість на початку і в кінці діастоли, дозволяючи провести оцінку діастолічної функції RV і тиску правого передсерді (RA) з використанням співвідношення між ранньою діастолічною трикуспідальною швидкістю (за допомогою звичайної імпульсно-хвильової доплерографії) до піку швидкості в ранній діастолі при DTI бічного строни трикуспідального кільця.
Крім оцінки швидкості, DTI дозволяє вимірювати часові інтервали. На відміну від лівого шлуночка, час ізоволюмічної релаксації практично відсутній в здоровому правому шлуночку (рис. 24А), і збільшення правобічної тривалості ізоволюмічної релаксації передбачає погіршення функції RV, що пов’язано з первинною дисфункцією RV або збільшенням післянавантаження RV. Індекс Tei правого шлуночка може бути обчислений за даними імпульсно-хвильової DTI і має перевагу одночасної реєстрації систолічної та діастолічної швидкості, в порівнянні із звичайною доплерографією (рис. 24В). DTI допомагає також визначати диссинхронію RV шляхом вимірювання затримки перегородка-вільна стінка RV.
Рис. 24. (A) Швидкості трикуспідального кільця оцінювали за допомогою імпульсного DTI в здорової людини. (B) Вимірювання індексу Tei RV ([час ізоволюмічного скорочення + час ізоволюмічної релаксації]) / час викиду).
Для DTI була підтверджена здатність кількісної оцінки деформації міокарда RV. Хоча оцінка поздовжньої деформації в апікальній проекції і здійсненна в клінічній практиці, аналіз радіальної деформації RV в парастернальному акустичному вікні дуже проблематичний. Ці перешкоди пов’язані з близько розташованими артефактами, які утворюються в безпосередній близькості від датчика і тонкої стінки RV, що вимагає проведення вкрай малих обчислень відстані <5 мм для SR вимірювань. Вимірювання SR добре корелюють з вимірами довжини сегмента при ультразвуковій мікрометрії і можуть бути використані для кількісної оцінки функції RV при різних умовах навантаження на експериментальній моделі. Різке збільшення післянавантаження RV може призвести до збільшення значення SR міокарда RV і до зниження систолічного піку деформації, що вказує на зменшення ударного об’єму RV. Крім того, профіль деформації після звуження легеневої артерії, демонструє зсув міокардіального вкорочення від ранньої середини до кінця систоли, або навіть ранньої діастоли (післясистолічне вкорочення).
STE також має великі перспективи в оцінці регіональної та глобальної деформації RV в різних напрямках з точки зору амплітуди і часу, маючи перевагу в тому, що STE менш схильна до впливу руху серця.
Нормальні значення
На рівні трикуспідального кільця, нормальна систолічна швидкість вільної стінки RV при імпульсним DTI -> 12 см / сек, хоча вона може залежати від віку, подібно нормальним швидкостям міокарда LV. Пікова систолічна швидкість – <10 см / сек повинна викликати підозру аномальної функції RV, особливо у молодих дорослих людей. Пікова систолічна швидкість – <11,5 см / сек може свідчити про присутність дисфункції RV або легеневої гіпертензії з чутливістю і специфічністю 90% і 85%, відповідно (рис. 24А). Крім того, порогове значення <9.5 см / сек було визначено в якості прогностичного фактора ризику для прогнозування несприятливих результатів при різних захворюваннях, у тому числі хронічної серцевої недостатності.
Пікові значення S-хвиль при імпульсній DTI і на кольоровій DTI не можуть бути використані як взаємозамінні, тому що перша методика вимірює пікові швидкості міокарда, в той час, як друга вимірює середні швидкості міокарда, які на 20% нижче (рис. 25).
Рис. 25. Міокардіальний профіль швидкості трикуспідального кільця оцінювали за допомогою кольорової DTI (A) і імпульсного DTI (B) у здорового пацієнта. Зверніть увагу на більш низькі швидкості, отримані при кольоровому DTI в порівнянні з імпульсним DTI.
Опубліковані висновки
Стандартні профілі швидкості міокарда були встановлені у великій когорті здорових суб’єктів у широкому діапазоні віку, при цьому систолічні швидкості вільної стінки міокарда RV не залежать від віку, в той час як діастолічні швидкості змінювалися, з поступовим зменшенням ранньої діастолічної швидкості. Ця інформація важлива для інтерпретації значень у хворих в широкому діапазоні вікових груп.
У здорових осіб, поздовжні швидкості RV відображають типовий градієнт основа-до-верхівки з більш високими швидкостями на основі (рис. 26А). Крім того, швидкості RV постійно вищі в порівнянні з лівим шлуночком. Це може бути пояснено відмінностями в умовах навантаження і піддатливості стінки при більш низькому після навантаженню в правому шлуночку і домінуванням поздовжніх і косих волокон міокарда у вільній стінці RV. При дисфункції RV, поздовжні швидкості RV зменшуються, а градієнт основа-до-верхівки має тенденцію до зникнення (рис. 27).
Рис. 26. Швидкості вільної бічної стінки RV (A) і поздовжньої деформації (B), отримані за допомогою кольорової DTI у здорової людини. Зверніть увагу на градієнт основа-верхівка по швидкості і градієнт верхівка-основа по поздовжній деформації. Жовтий = базальний; синій = середній; червоний = верхівковий.
Рис. 27. Міокардіальні швидкості (угорі) і поздовжня деформація (внизу) бічної вільної стінки RV, оцінені за допомогою кольорової DTI у здорової людини (ліворуч) і у пацієнта з легеневою гіпертензією (праворуч). Хоча верхівковий (червоний), середній (синій) і базальний (жовтий) сегменти мають подібний профіль швидкості без будь-якого градієнта основа-верхівка, апікальні і середні сегменти демонструють різке зниження систолічної деформації в порівнянні з базальним сегментом у пацієнта з легеневою гіпертензією.
Значення систолічної швидкості трикуспідального кільця було вивчено в широкому діапазоні патологічних станів, таких як: легенева гіпертензія, хронічна серцева недостатність, хронічна і гостра легенева емболія, системний склероз, захворювання коронарних артерій, вроджені захворювання серця і різні види кардіоміопатій (рис. 28).
Рис. 28. Міокардіальний профіль швидкості трикуспідального кільця оцінювали за допомогою імпульсного DTI у пацієнта з системним склерозом без легеневої гіпертензії (A) і пізніше утворена легенева гіпертензія (B). Зверніть увагу на збільшення тривалості ізоволюмічної релаксації.
При цих патологічних станах, систолічна швидкість тристулкового бічного кільця і рання діастолічна швидкість значно менша порівняно зі здоровими людьми. У пацієнтів з серцевою недостатністю, зниження систолічної швидкості тристулкового кільця пов’язано з тяжкістю дисфункції RV і є сильним предиктором клінічного результату. При системному склерозі і гіпертрофічної кардіоміопатії, субклінічні зміни правого шлуночка проявляються також зниженням пікової систолічної та початкової діастолічної швидкостей тристулкового кільця і змінами значення співвідношення тристулкового кільця – E ‘/ a’.
Деформація міокарда
На відміну від більш рівномірного розподілу деформаційних властивостей в лівому шлуночку, SR і значення деформації не так рівномірно розподілені в правому шлуночку і мають зворотний градієнт основа-до-верхівки, досягаючи найвищого значення у верхівкових сегментах і вивідному тракті (рис. 26В). Ця особливість може бути пояснена складною геометрією тонкостінного, у формі півмісяця, правого шлуночка і менш однорідним розподілом регіонального навантаження на стінку, в порівнянні з товстостінним і, що нагадує форму кулі, лівим шлуночком.
Дані деформації і SR, отримані при DTI і STE можуть бути використані для оцінки динаміки RV і, як виявилося, є легко відтворюваними і досить порівнянними. Деформація і SR добре корелюють з радіонуклідними дослідженнями EF RV. Граничні значення систолічної деформації і SR в базальному відділі вільної стінки RV – 25% і -4 sec-1, з чутливістю 81% і 85% і специфічністю 82% і 88%, відповідно, з можливістю прогнозування EF RV> 50%.
У пацієнтів з патологією або дисфункцією RV, пікова систолічна деформація і SR значно знижені і мають затримку, порівняно з пацієнтами з нормальною функцією RV (Рис. 26B, 27 і 29).
Рис. 29. Подовжню деформацію правого шлуночка оцінювали за допомогою STE в апікальній чотирикамерній проекції у здорового пацієнта (А) і у хворого з порушеною функцією RV (B). GS, глобальна деформація.
Аномалії деформації і SR правого шлуночка можуть бути виявлені при легеневій гіпертензії, а також при амілоїдозі, вродженій серцевій патології і аритмогенній кардіоміопатії RV. Значення деформації і SR, отримані при доплерографії, можуть сприяти визначенню невеликих змін у відповідь на судинорозширювальне лікування і виявленню ранніх ознак залучення RV в патологічний процес, пов’язаний з гіпертензією легеневої артерії (рис. 27). Крім того, доведена достатня чутливість для того, щоб виявляти ранні зміни функції RV у пацієнтів з системним склерозом і нормальним легеневим тиском. Вимірювання деформації може бути корисним для ранньої діагностики дисфункції RV. Наприклад, у безсимптомних дітей з оперованою тетрадою Фало, деформація RV зменшується, якщо наростає легенева недостатність. Крім того, в умовах периопераційного динамічного спостереження за функцією RV, параметри деформації мають переваги перед М-режимом або параметрами, заснованими на вимірах швидкості, тому що деформація не залежить від можливих змін у загальній структурі руху серця після перикардектомії.
Недавнє дослідження у пацієнтів з легеневою гіпертензією підтвердило зворотний зв’язок між тиском в RV і значеннями поздовжньої деформації вільної стінки RV. Крім того, було виявлена значна кореляція між тиском в RV і поздовжньою деформацією перегородки, але не з деформацією бічної стінки, це передбачає, що поздовжні волокна не можуть поширювати вплив тиску RV в глибину лівого шлуночка. На противагу цьому, циркулярна деформація як в перегородці, так і бічній стінці LV, мала прямий зв’язок з тиском в RV, що свідчить про те, що циркулярні волокна можуть поширювати фактори впливу RV через лівий шлуночок.
Невирішені проблеми та пріоритети наукових досліджень
Наявний досвід щодо застосування STE для оцінки функції RV обмежується невеликими одноцентровим дослідженнями. Техніка представляється доцільною для проведення кількісної оцінки функції RV і допомагає поліпшити розуміння патофізіології різних захворювань. Однак її клінічне значення для обстеження пацієнтів залишається доведеним.
Резюме та рекомендовані показання
Параметри швидкості і деформації, отримані при DTI, як було продемонстровано, можуть бути надійними і корисними даними, особливо для виявлення невиражених аномалій і для оцінки прогнозу. Вони були недавно запропоновані в якості параметрів, необхідних для динамічного спостереження за хворими з легеневою гіпертензією. Міокардіальні швидкості, записані на рівні трикуспідального кільця, є корисними для кількісного визначення поздовжнього руху RV. Вони забезпечують корисною інформацією з точки зору кількісного раннього виявлення невиражених порушень міокарда та прогнозу.
4.2. Ліве передсердя
Ліве передсердя виконує чотири основні механічні функції: фаза 1, резервуарна (накопичення легеневої венозної крові під час систоли LV); фаза 2, провідна (проходження крові в лівий шлуночок під час ранньої діастоли); фаза 3, активна скорочувальна насосна (15% -30% наповнення LV в кінці діастоли); і фаза 4, всмоктування (передсердя наповнюється кров’ю спочатку систоли). За допомогою цих функцій, ліве передсердя модулює наповнення LV. Розширення лівого передсердя відбувається у відповідь на порушення наповнення LV і, як наслідок патології мітрального клапана та / або фібриляції передсердь.
Функція LA може бути розділена на приблизно експоненціальне співвідношення «тиск-об’єм» під час резервуарної і провідної фаз і цикл «тиск-об’єм» проти годинникової стрілки під час скорочення передсердя і фази всмоктування. Комплексна оцінка функції LA вимагає точного визначення тиску LA, яке може бути побічно оцінено тільки за допомогою ехокардіографії. Ускладнює ситуацію ще й той факт, що (1) на відміну від лівого шлуночка, не існує ніякої істинної ізоволюмічної фази LA (бо отвори легеневих вен завжди відкриті), і (2) резервуарна функція визначається більшою мірою функцією LV (опущенням мітрального кільця під час систоли), ніж первинними властивостями LA. Пасивні та активні властивості LA можуть бути охарактеризовані шляхом об’єднання 3D ехокардіографічних об’ємів з інвазивними методами виміру тиску, в поєднанні зі змінами умов навантаження.
За допомогою цього методу, визначається зниження систолічного циклу LA під час циркулярної перев’язки (яка індукує ішемію LA) артерії, але не включаючи ліву передню низхідну коронарну артерію (яка впливає тільки на лівий шлуночок). На регіональному рівні, функція LA може бути принципово описана з точки зору відносин напруження-деформація. Хоча визначення деформації і стало більш доступним за допомогою ехокардіографії, не існує навіть інвазивного способу оцінки напруження стінки. На щастя, через те, що ліве передсердя тонкостінне, можна обґрунтовано прирівнювати тиск LA до напруження стінки.
Глобальна та регіональна функція лівого передсердя
Функція LA в даний час оцінюється за допомогою вимірювання 2D об’ємів у LA, доплерівського аналізу трансмітрального потоку (пік і час швидкісного інтеграла швидкості, фракція наповнення передсердя) і потоку легеневої вени (пік і тривалість зворотньої швидкості передсердя). Оскільки 2D ехокардіографія обмежена використанням геометричних моделей і можливих помилок через ракурси, вона може недооцінювати об’єм LA в порівнянні з кардіальним магнітно-резонансним дослідженням, в той час як доплерівська оцінка функції LA та / або використання сили викиду LA, являються непрямими параметрами. Тривимірні методики вимірювання об’єму LA, які не вимагають геометричних моделей, можуть точно оцінити глобальну функцію LA. Акустична кількісна оцінка, з автоматизованою методикою виявлення межі, забезпечує онлайн картину безперервної області LA або його об’єм протягом часу, але отримані дані сильно залежать від настройки посилення, що призводить до великої варіабельності між дослідниками і тест-ретест варіабельності.
Обидва дослідження і DTI, і 2D STE дозволяють провести неінвазивну оцінку глобальної функції LA і регіональних значень деформації стінок LA. Двовимірна STE також надає криві об’єму LA протягом одного серцевого циклу, з яких можуть бути отримані різні механічні показники LA, що дозволяє провести пряму оцінку ендокардіальної скорочувальної фукції LA і пасивної деформації. Дві різних модальності запропоновані для кількісного визначення деформації передсердя при STE (рис. 30).
Рис. 30. Дві різних модальності пропонуються для кількісного визначення регіональної та глобальної передсердної деформації при 2D STE: (A) використання початку QRS в якості точки відліку і вимірювання позитивного піку поздовжньої деформації лівого передсердя (LA) і (B) використання Р-хвилі в якості вихідної точки і вимір першого негативного піку поздовжньої деформації LA (систола LA), другого позитивного піку деформації LA (функції проведення LA), і їх сума.
Перший (в цілому 12 рівновіддалених зон, шість в апікальній чотирикамерній площині і шість в апікальній двокамерній площині) приймає в якості точки відліку початок QRS комплексу і вимірює позитивний пік поздовжньої деформації передсердь (відповідно до порожнини передсердя). Другий (в цілому 15 рівновіддалених зон, шість в апікальній чотирикамерній площині і шість в апікальній двокамерній площині і три в проекції задньонижньої стінки по довгій осі) використовує P хвилю в якості точки відліку, що дозволяє провести вимірювання першого негативного піку поздовжньої деформації передсердь (відповідають систолі передсердь), другого позитивного піку деформації передсердь (відповідає провідній фазі LA) і обчислити їх суму.
Нормальні значення
Нормальні значення деформації LA при двовимірній speckle-tracking ехокардіографії були опубліковані нещодавно. При використанні 12-сегментної моделі і в якості точки відліку початок комплексу QRS, середня пікова поздовжня деформація передсердь у 60 суб’єктів була 42.2 ± 6.1% (з 5 і 95 процентильним діапазоном 32,2% -53,2%). Середні значення позитивного і негативного піку деформації були 23.2 ± 6.7% і 14.6 ± 3.5%, відповідно в 15-сегментній моделі, яка використовує Р-хвилю в якості точки відліку (64 здорових суб’єкта).
Опубліковані висновки
Деформація і SR і рання діастолічна глобальна деформація знижується в 12 передсердних сегментах у пацієнтів з атріосептальним окклюдером в порівнянні з контрольною групою. У хворих з синусовим ритмом, які піддавалися або кардіоверсії, або катетерній абляції у зв’язку з фібриляцією передсердь, параметри швидкостей і деформацій при кольоровій DTI були нижчі в порівнянні зі здоровою групою контролю, але в групі після абляції, була більш виражена регіональна та глобальна дисфункція LA. З іншого боку, деформація LA була збільшена у пацієнтів з мітральної регургітацією. Також показники деформації і SR були використані для обстеження пацієнтів з фібриляцією передсердь для оцінки ризику повторної фібриляції передсердь після кардіоверсії. Тривимірна 3D кольорова DTI, яка має перевагу одночасної реєстрації SR в трьох проекціях для зведення до мінімуму варіацій ритму, була використана для того, щоб продемонструвати значно нижчий пік SR у пацієнтів з артеріальною гіпертензією у порівнянні зі здорової групою контролю і спортсменами. Подібно DTI, STE аналіз глобального руху LA після черезшкірного відновлення міжпередсердного дефекту показав очікуваний результат відсутності деформації, яка вимірювалася в місці імплантації пристрою. Зниження негативного LA SR є також незалежним предиктором епізодів пароксизмальної фібриляції передсердь у пацієнтів з синусовим ритмом.
Регіональна неоднорідність деформації і SR значень LA відзначена у здорових суб’єктів, з найбільшим значенням в нижній стінці, в порівнянні з серединою і верхніми сегментами LA. Ця неоднорідність підтверджується тим фактом, що значення SR нижньої стінки LA, отримані при DTI дослідженні, є одним з кращих предикторів збереження синусового ритму після кардіоверсії фібриляції передсердь, і що показник деформації LA поліпшується більшою мірою на боковій стінці у пацієнтів, що реагують на CRT.
Головна перевага дослідження деформації LA є його легка можливість виконання, яка досить висока як при кольоровій DTI, так і при STE (94% у 84 здорових суб’єктів). Крім того, STE має важливе патофізіологічне значення, тому що пікова глобальна позитивна деформація LA має сильну кореляцію (зворотна залежність) з інвазивним виміром кінцевого діастолічного тиску LV, з доплерографічними показниками трансмітрального потоку, швидкостями легеневих вен, об’ємами DTI та об’ємами LA.
Невирішені проблеми та пріоритети наукових досліджень
Основна слабкість вимірювань регіональної деформації ЛА – це анатомічне розташування отвору легеневої вени, яке може перешкоджати точній оцінці базальних відділів LA, зокрема, коли легеневі вени розширені. Подібний спотворюючий ефект можна спостерігати в апікальній двокамерній проекції вушка LA, зокрема, коли воно надзвичайно велике.
Хоча регіональна оцінка функції LA може забезпечувати більш детальною інформацією про механіку LA, її значення у дослідженні глобальної функціональної оцінки LA ще не визначені, і необхідні додаткові дослідження для того, щоб з’ясувати це питання. Крім того, нормальні референтні значення для деформації LA, які були опубліковані, були отримані у відносно невеликих групах пацієнтів і, таким чином, повинні бути підтверджені на великих популяціях.
Резюме та рекомендовані показання
Показання для 2D STE лівого передсердя включають регіональну оцінку LA у пацієнтів з діастолічною дисфункцією, оцінку властивостей LA після фібриляції передсердь для прогнозування збереження синусового ритму, і оцінку стану після черезшкірного відновлення міжпередсердних дефектів. Крім того, регіональна деформація LA, очевидно, потенційно ефективна для ідентифікації пацієнтів з ризиком недостатності лівого передсердя або аритмії, а також оцінки характеристик LA у пацієнтів з розширенням LA невстановленого генезу. Тим не менш, у даний час, методика 2D STE лівого передсердя не готова для клінічного застосування.
4.3. Праве передсердя
Якщо правий шлуночок є «забутим шлуночком», то праве передсердя перебуває в істинній невідомості. Практично не існує ехокардіографічних досліджень, які зосереджені на оцінці власне механічної функції RA, оскільки більшість досліджень направлено на оцінку середнього тиску RA. Подібно лівому передсердю, праве передсердя має три окремих фази: резервуарну (заповнення правого передсердя під час систоли шлуночків), проведення (проходження крові в правий шлуночок під час діастоли до Р-хвилі) і активного скорочення (систола передсердь). Таким чином, можна сказати, що праве передсердя має пасивну функціональну фазу RA (резервуарна плюс фаза проведення) і активну фазу скорочення.
Опубліковані висновки
Правому передсердю приділено дуже обмежену увагу з використанням нових методик тканинної доплерографії та дослідження 2D деформації. Реалізація цих нових методик проблематична через малу товщини стінки RA. В одному недавньому дослідженні використовувалася STE для оцінки деформації вільної стінки RA у пацієнтів після CRT. Пацієнти, які відповіли на CRT (що відбивається у зменшенні > 15% кінцевого систолічного об’єму LV) мали менші розміри RA (13.2 ± 4.4 проти 19.7 ± 5,5 см2 / м2, Р <0,001) і більш високі значення деформації RA (40.2 ± 8.9% проти 24.3 ± 10.2%, Р <0,001).
Резюме та рекомендовані показання
Очевидно, що необхідно провести велику кількість дослідницької роботи, перш ніж можна буде використовувати вимірювання деформації RA для рутинного клінічного використання.
5. ВИСНОВКИ
Цей документ відображає консенсус групи авторів, зібраних спільно ASE і EAE, присвячений доступним методам обстеження в даний час для оцінки механіки міокарда. Консенсус полягає в тому, що методи, описані в даному документі, значною мірою сприяють вкрай необхідному процесу трансформації ехокардіографії із суб’єктивного мистецтва інтерпретації зображень в набір об’єктивних діагностичних інструментів. Хоча опубліковані результати досліджень і забезпечують доказову базу для потенційних клінічних застосувань цих методів при різних клінічних ситуаціях, група авторів вважає, що в більшості областей, ця методика ще не готова до рутинної клінічній практиці. Консенсус ухвалив: що (1) необхідно додаткове тестування різних режимів для поліпшення якості діагностичної точності різних параметрів і їх відтворюваності при різних патологічних станах; (2) необхідна стандартизація параметрів, які вимірюються, і методики самого вимірювання; (3) стандартизація серед виробників обладнання має важливе значення, тому що лікар повинен мати можливість інтерпретувати дані, отримані за допомогою різних пристроїв, незалежно від постачальника. Після того, як ці умови будуть виконані і велика ехокардіографічна спільнота отримає необхідний досвід роботи з цими методами, вони стануть невід’ємною частиною «панелі інструментів» клінічної ехокардіографії. Для проведення досліджень рекомендуємо використовувати узд апарати для кардіології.



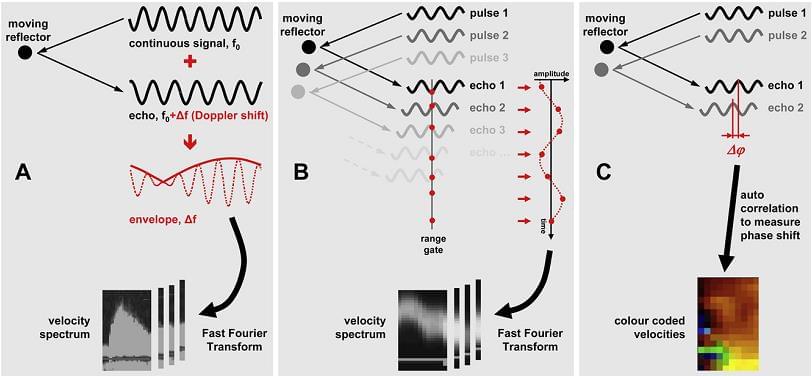
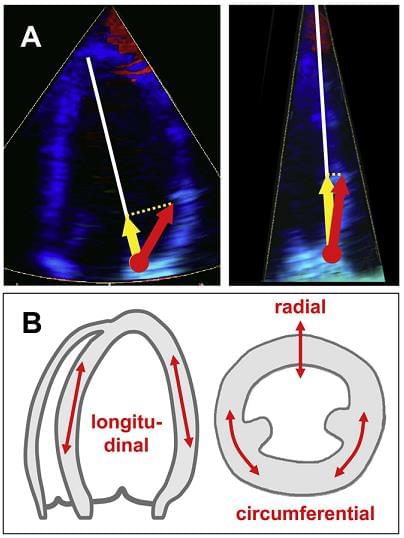
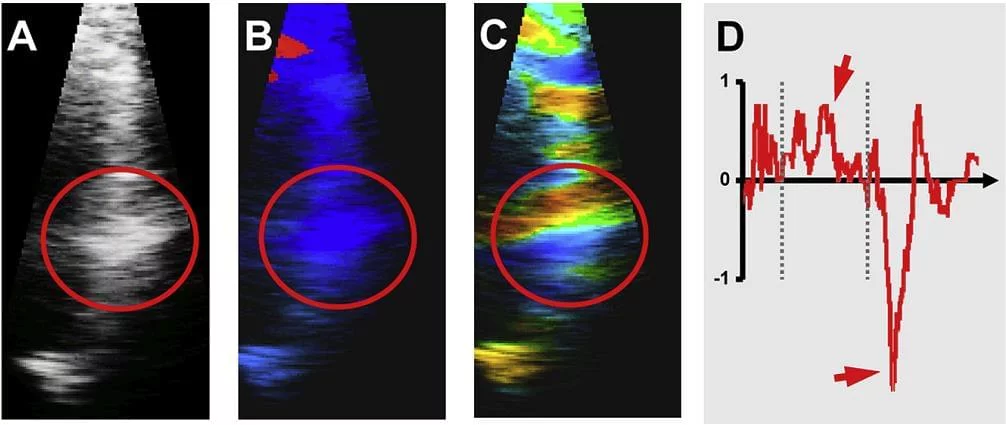
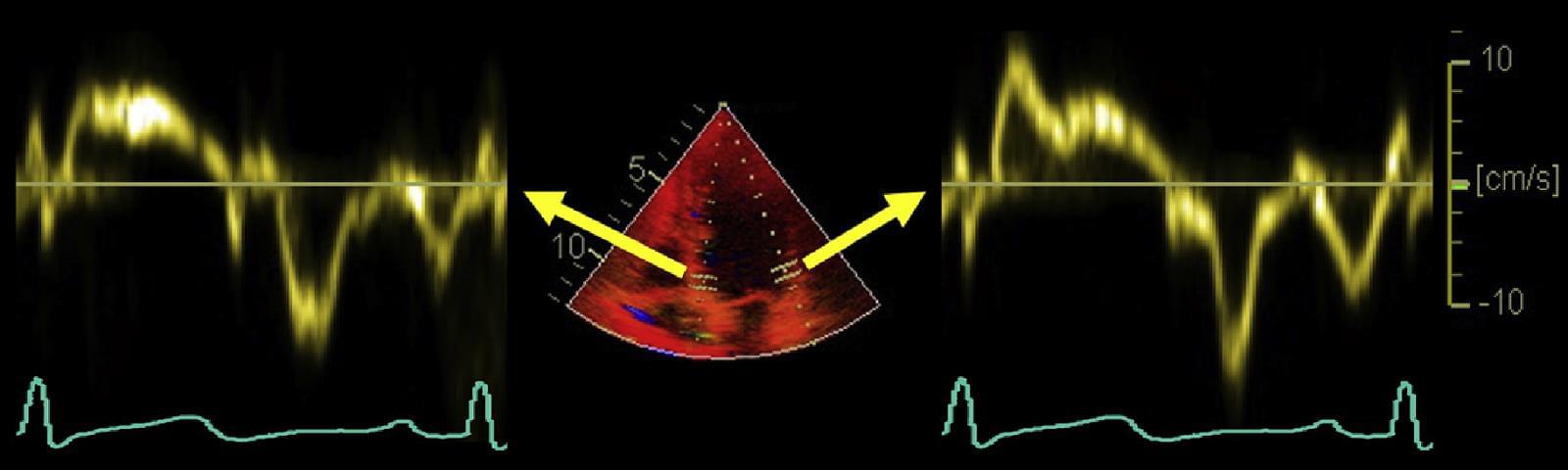
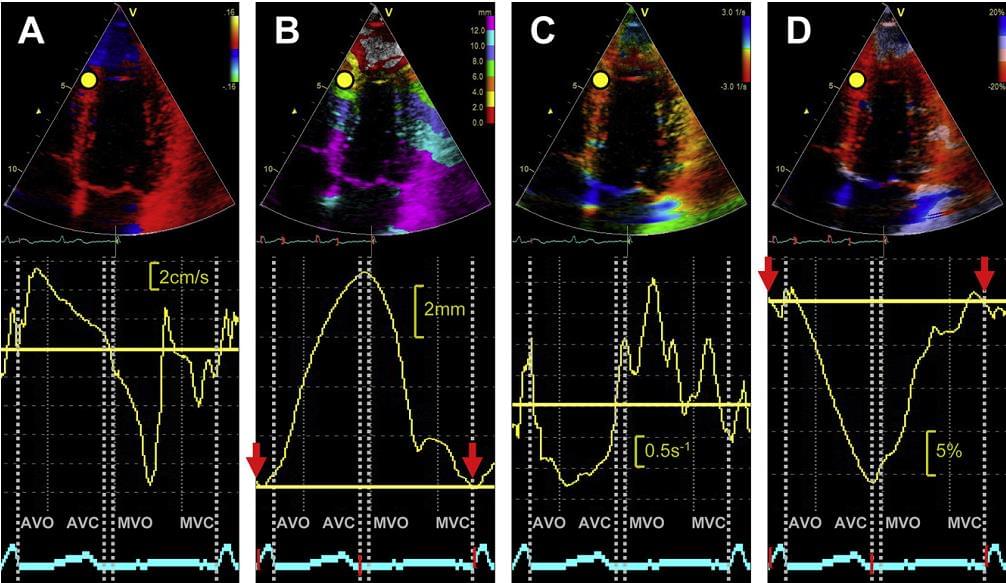



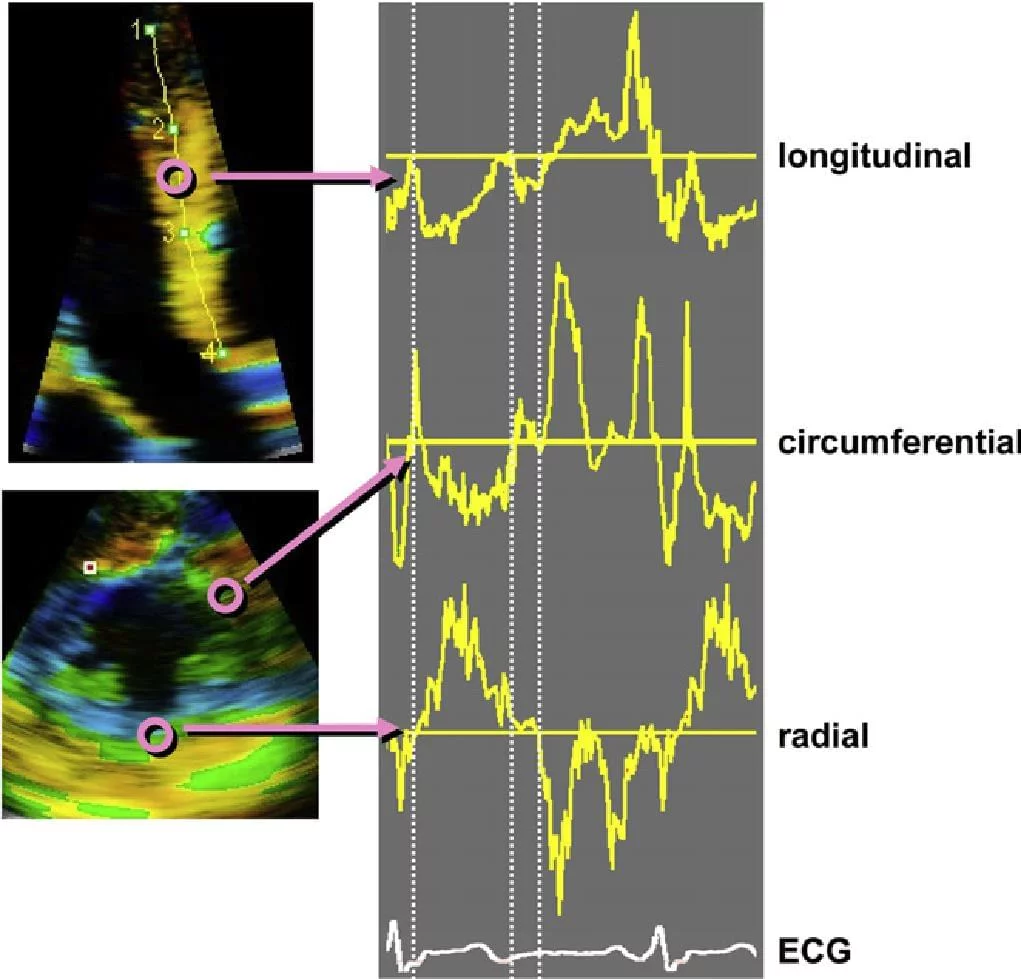
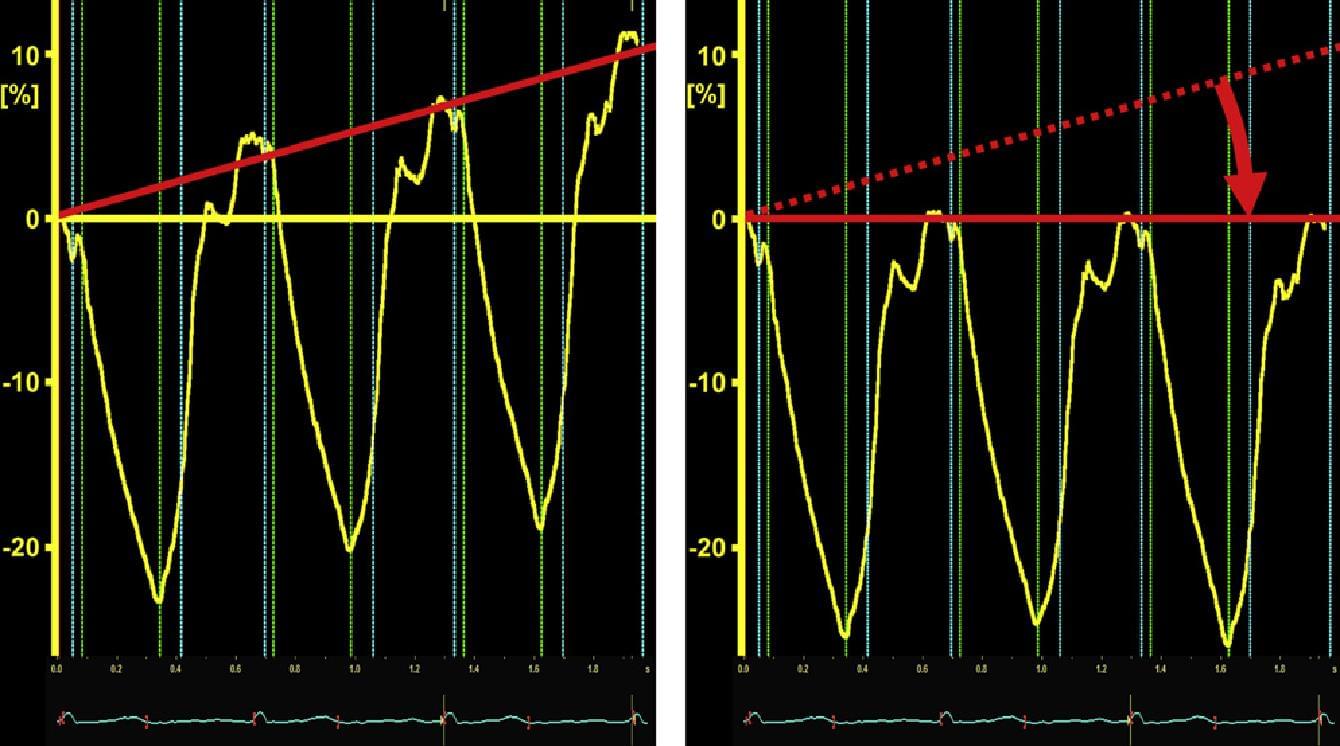
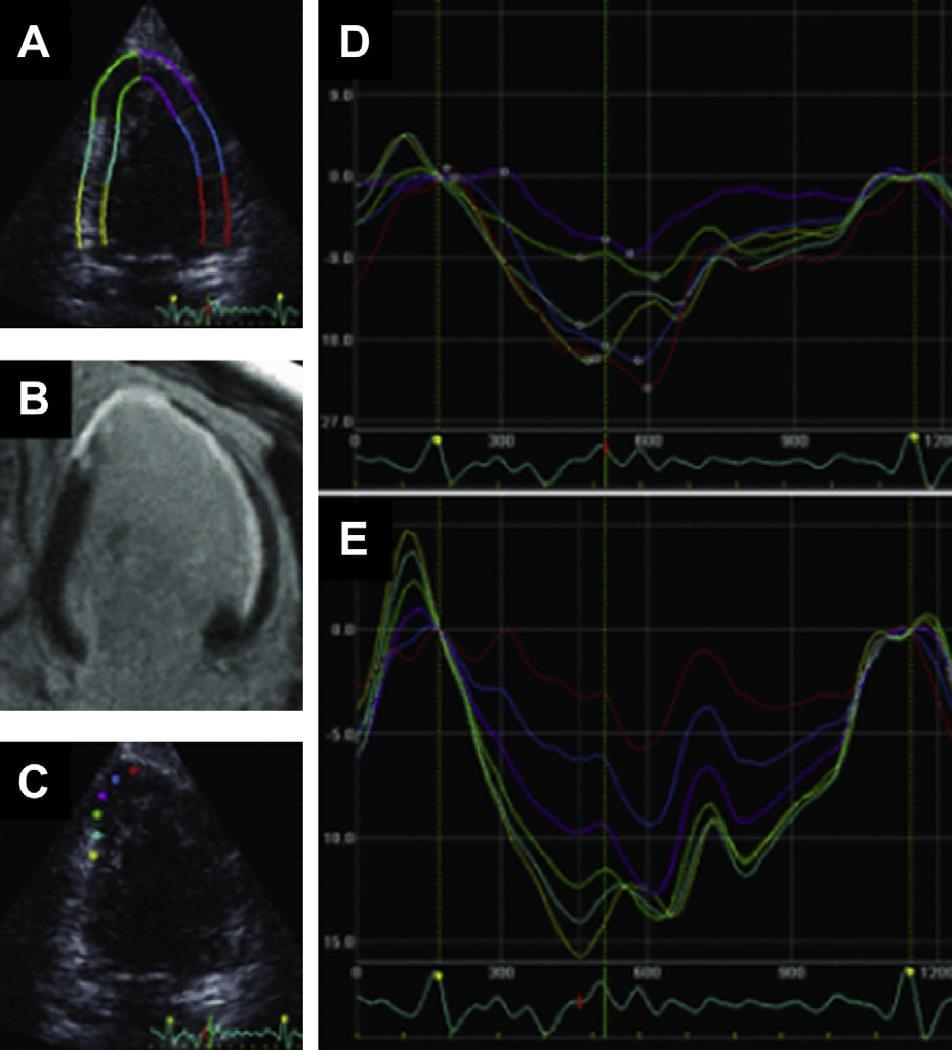
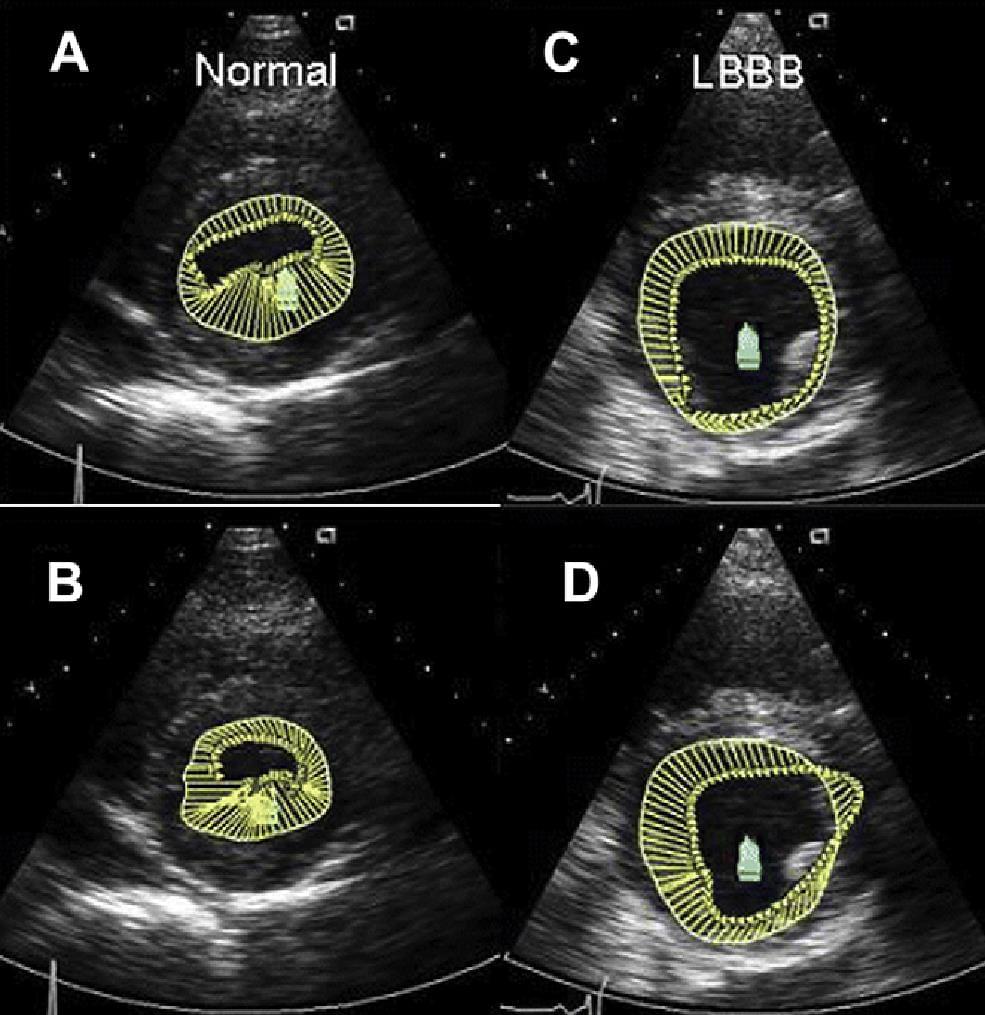
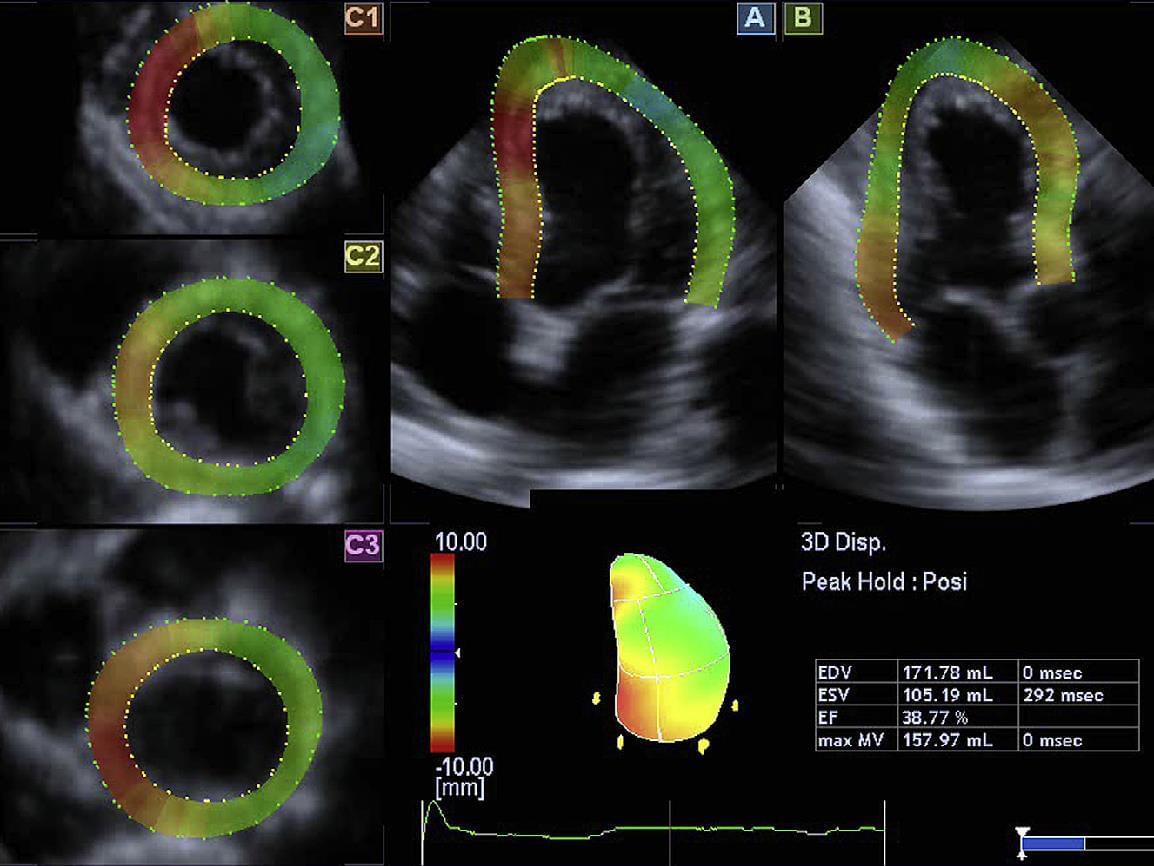
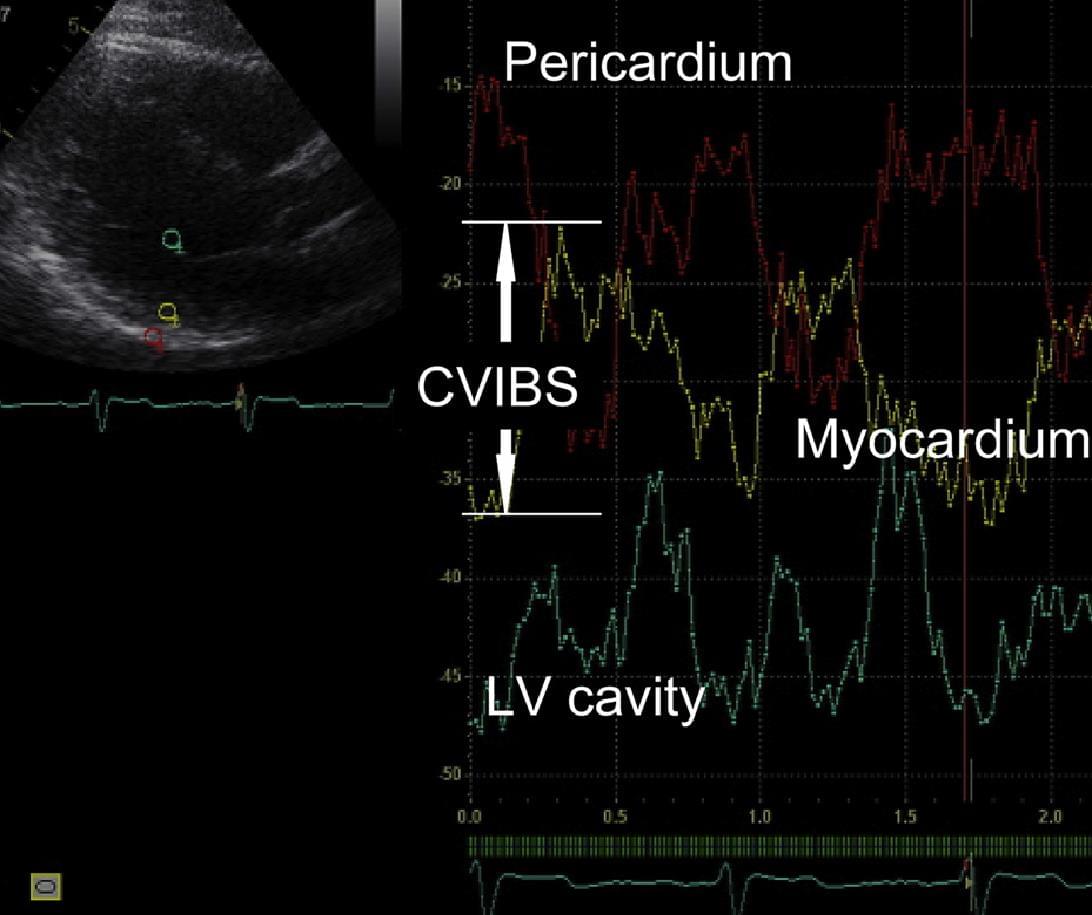
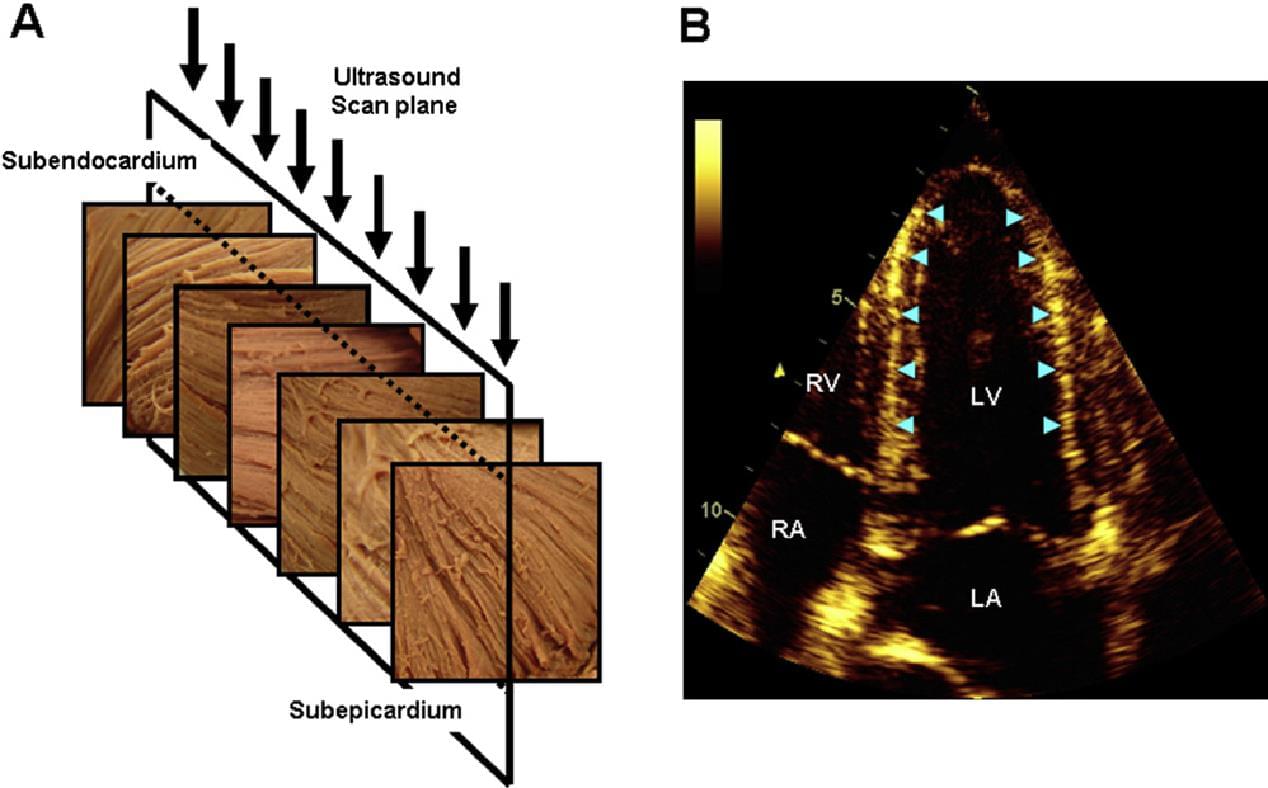
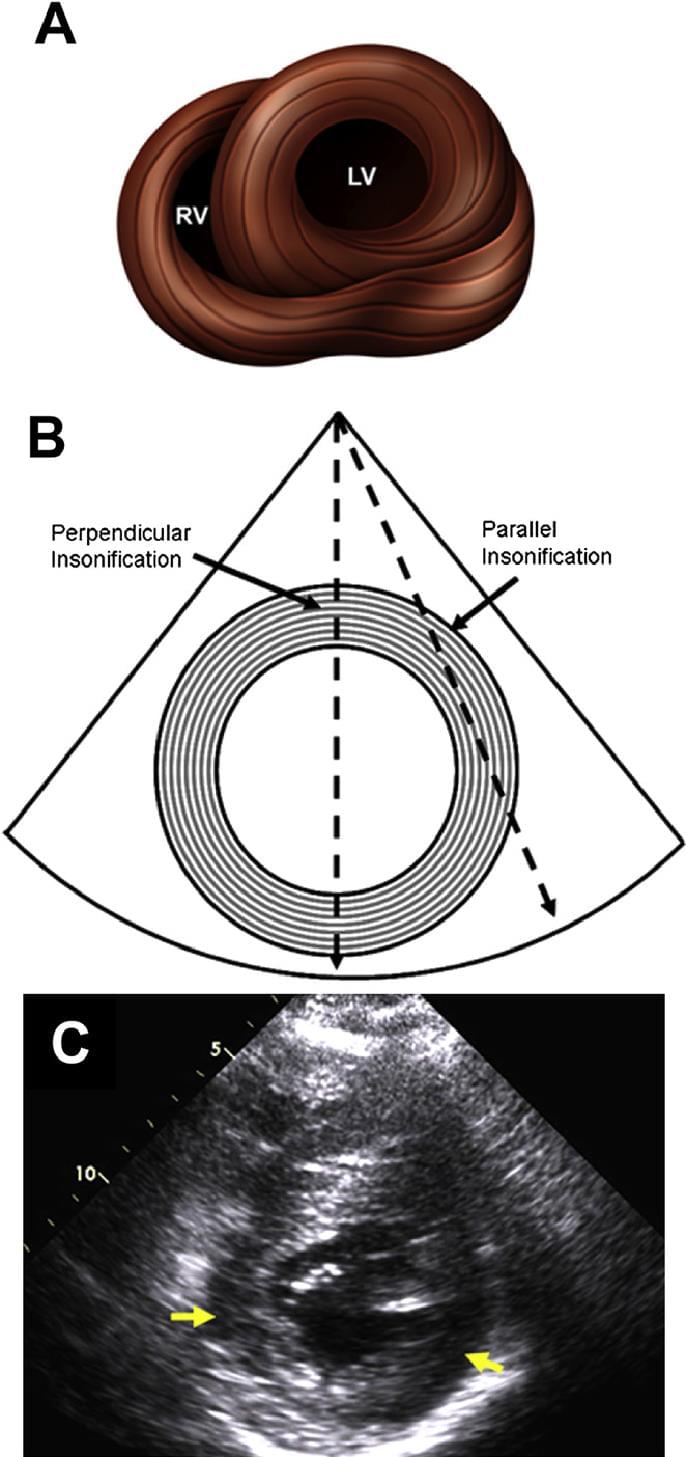
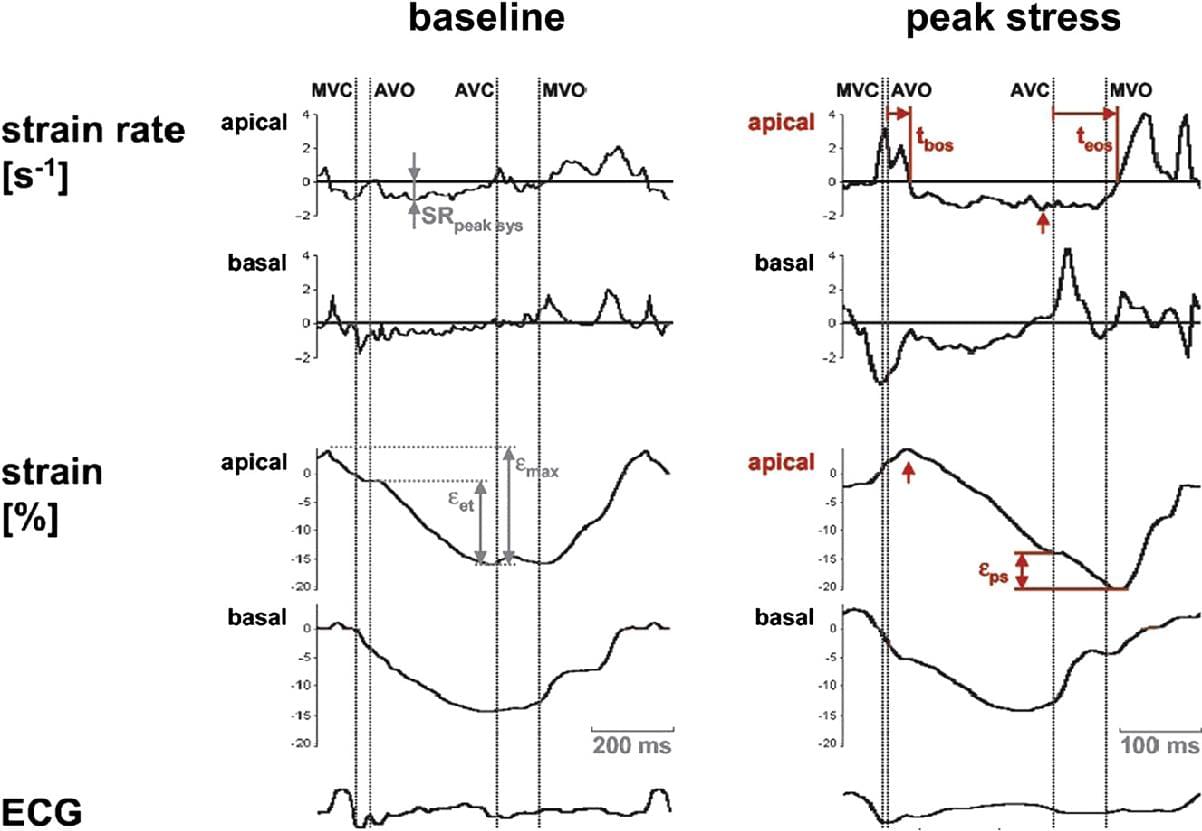
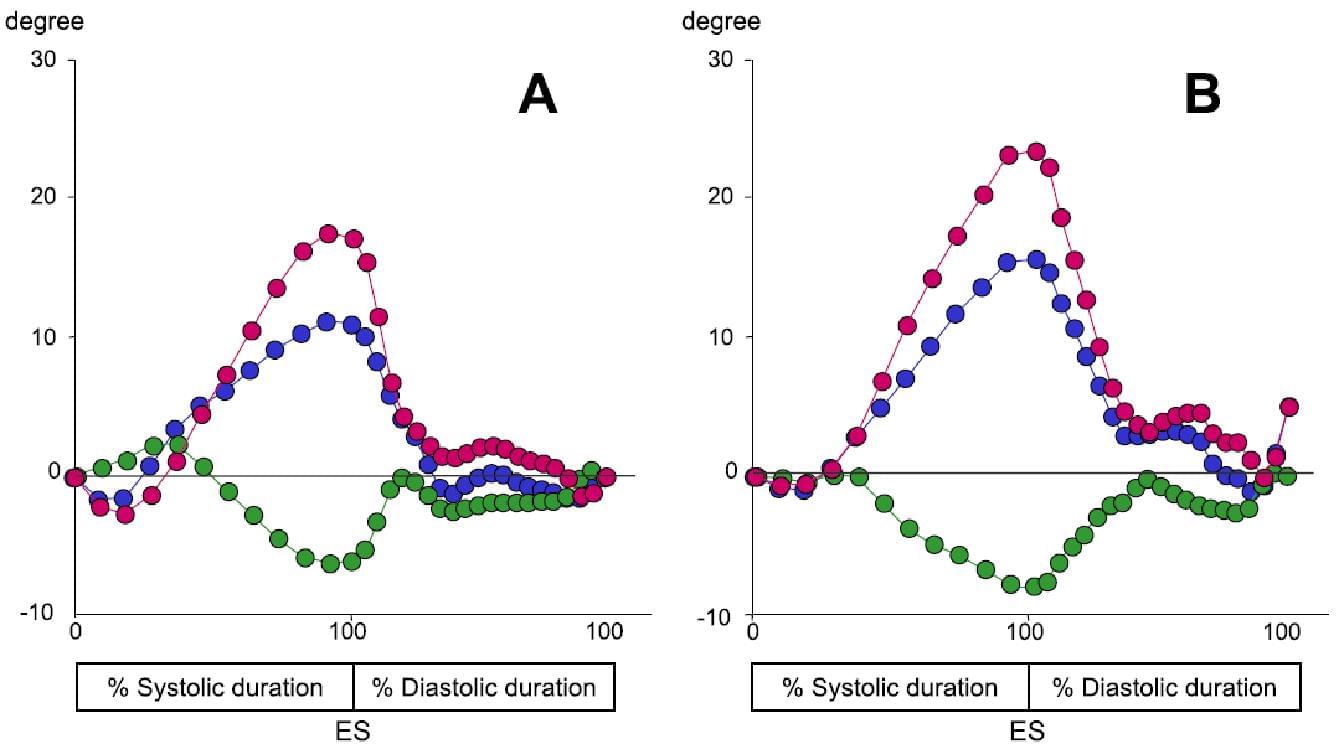
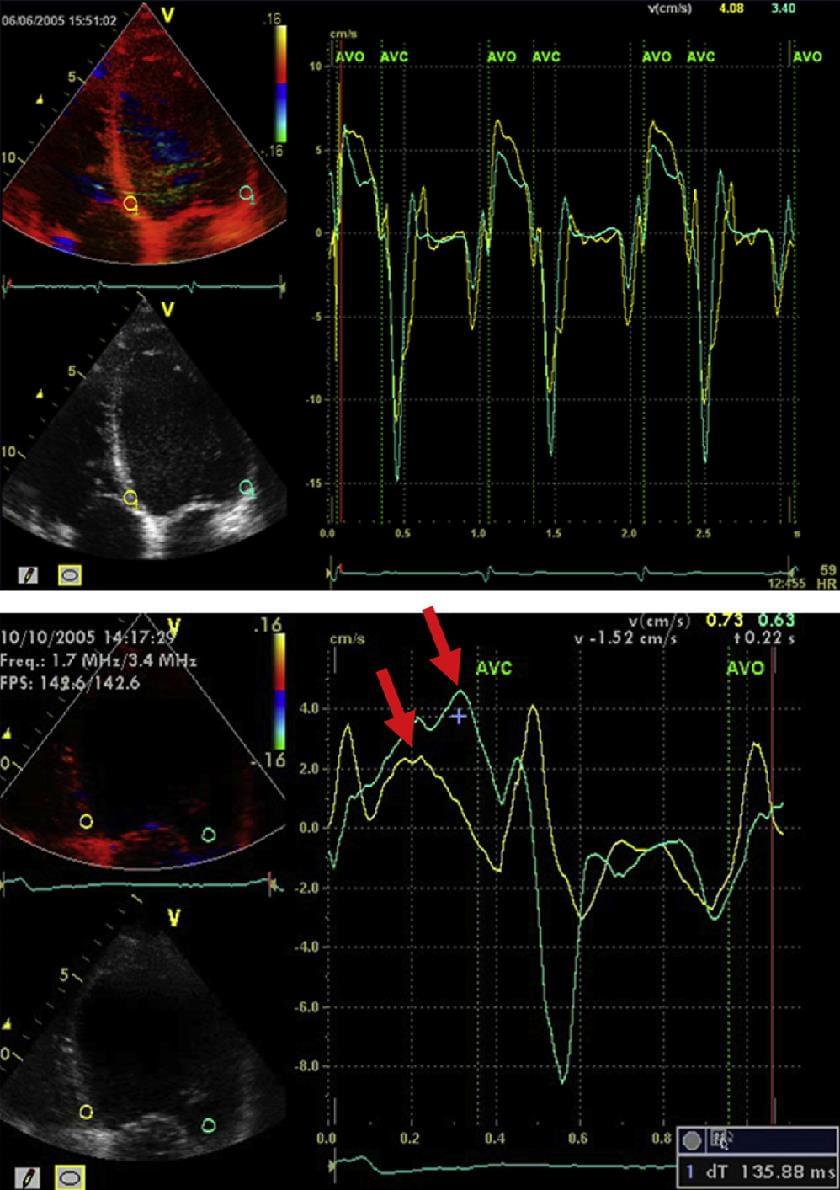
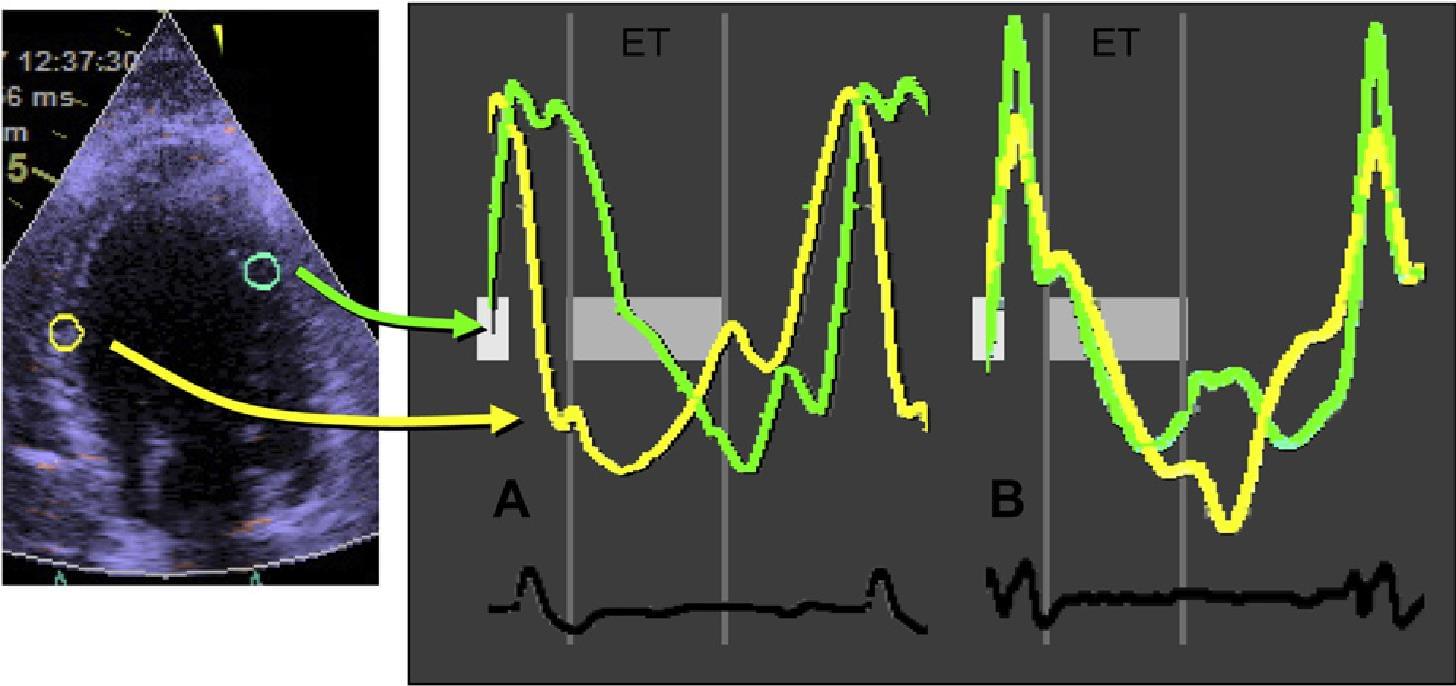
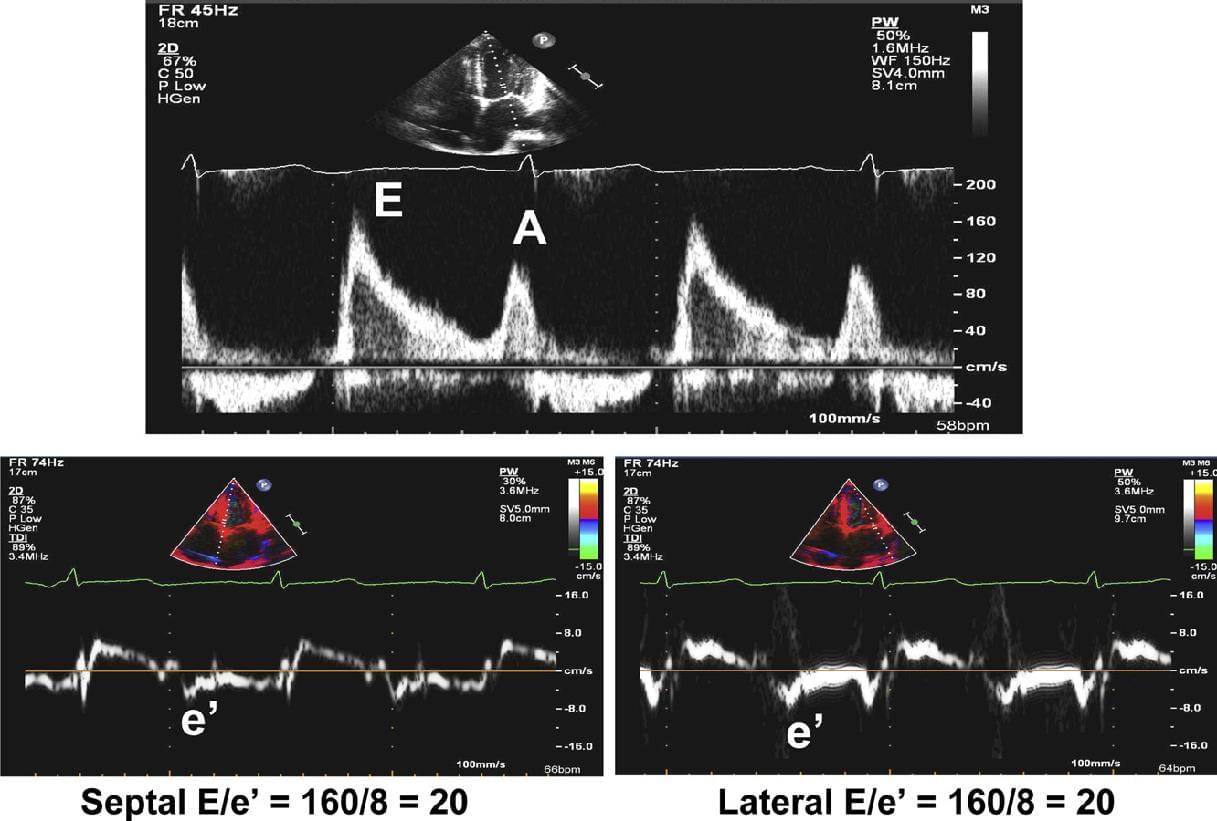
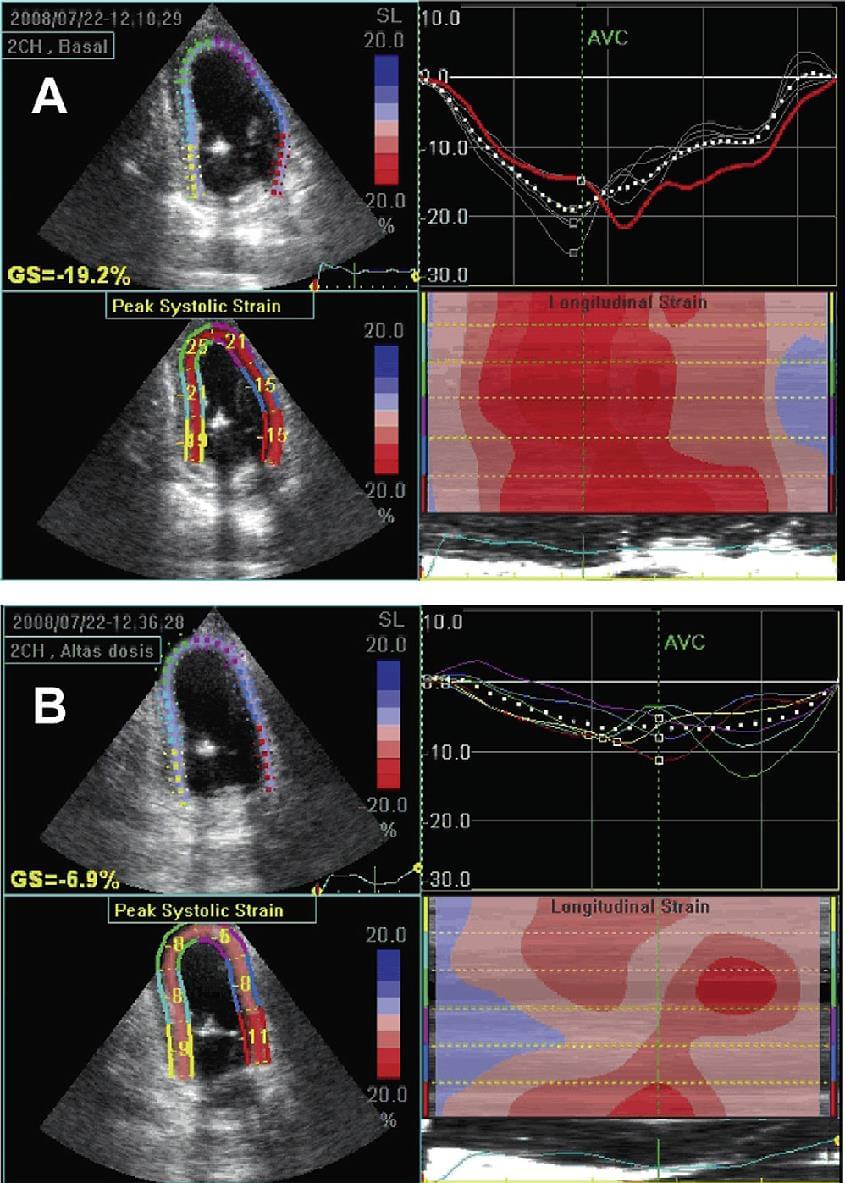
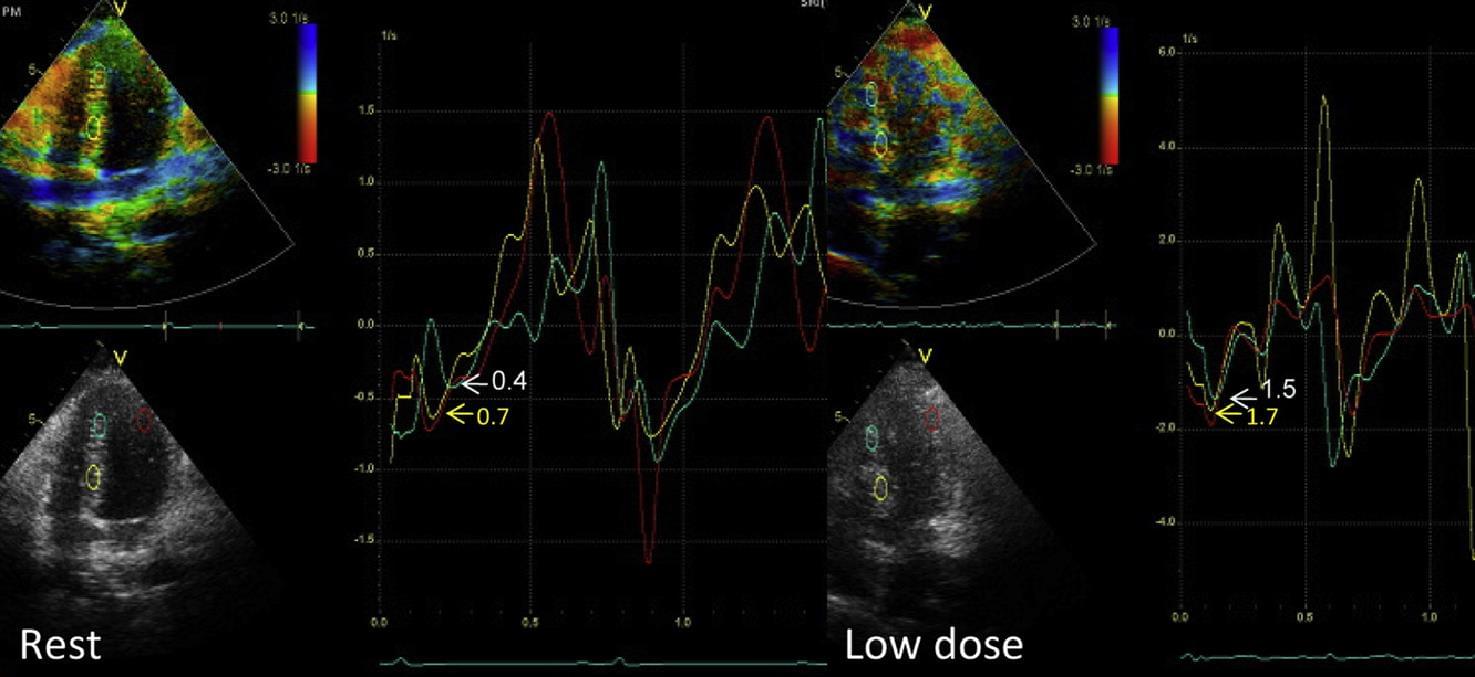
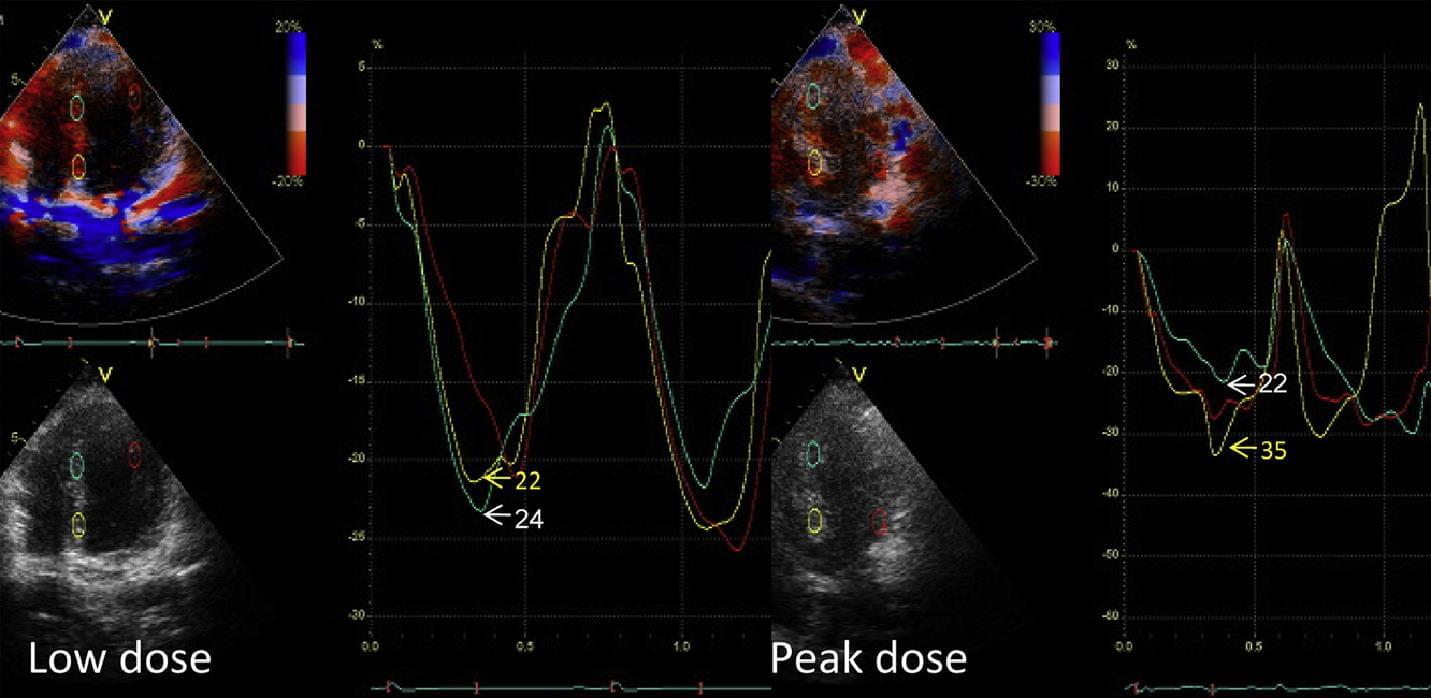
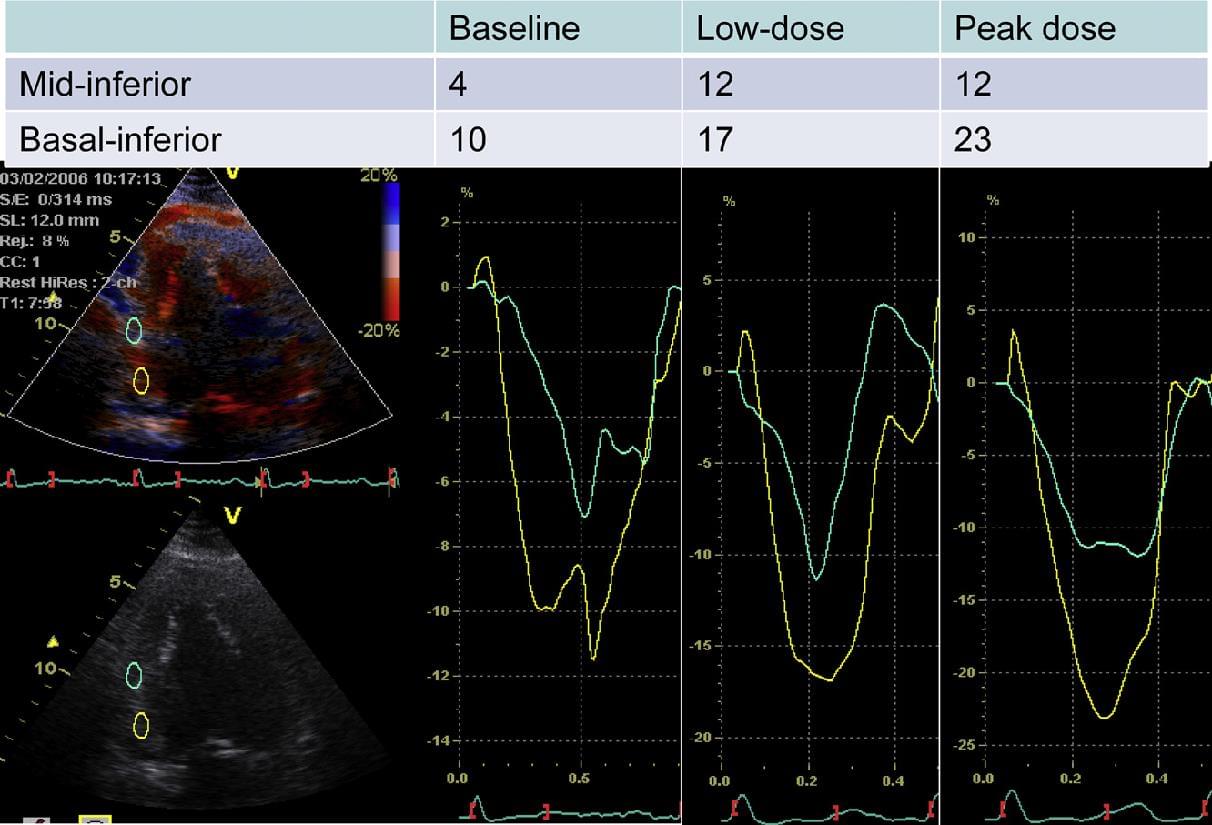
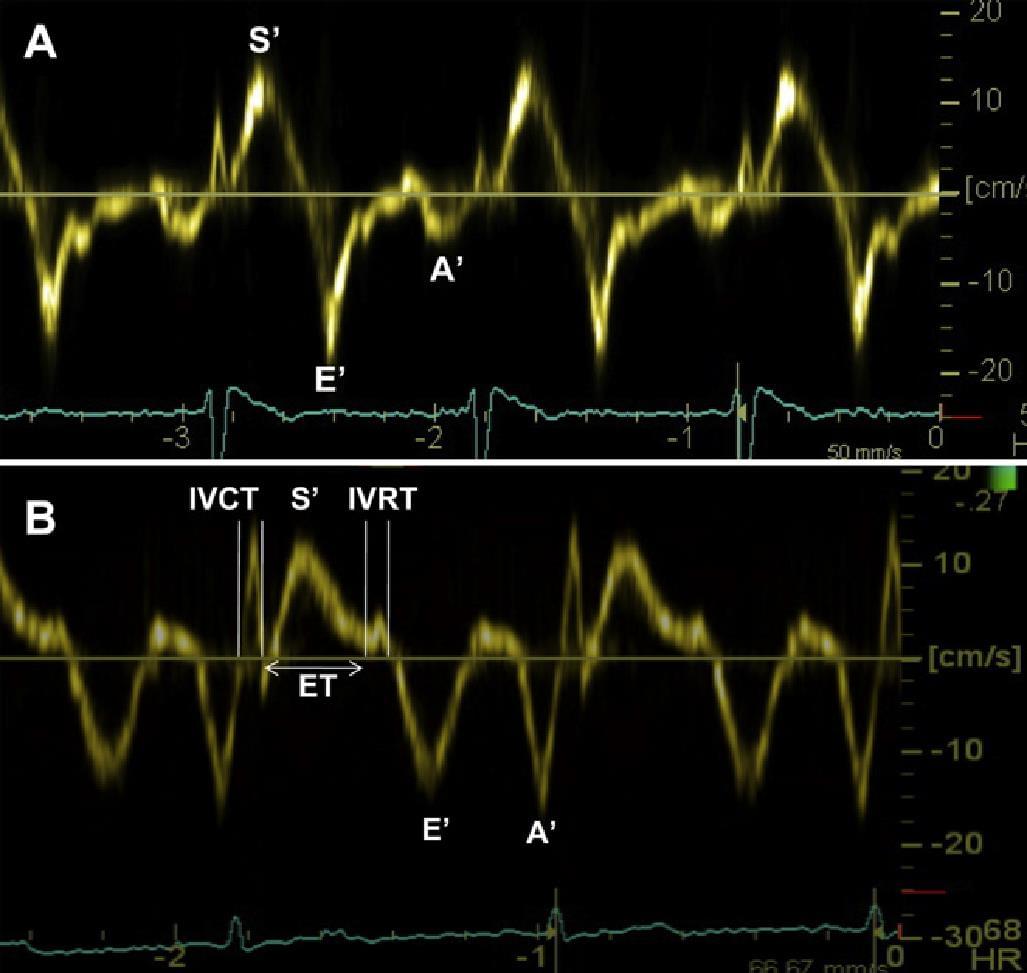
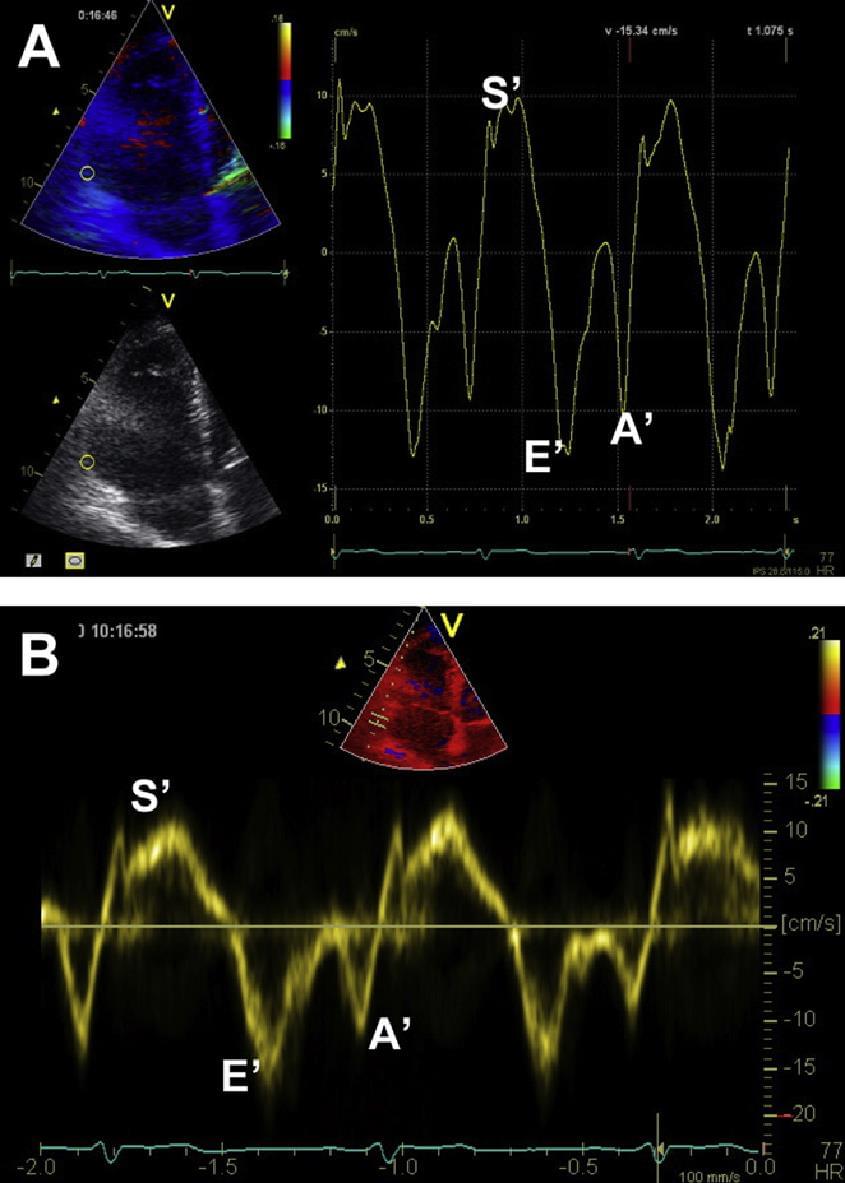
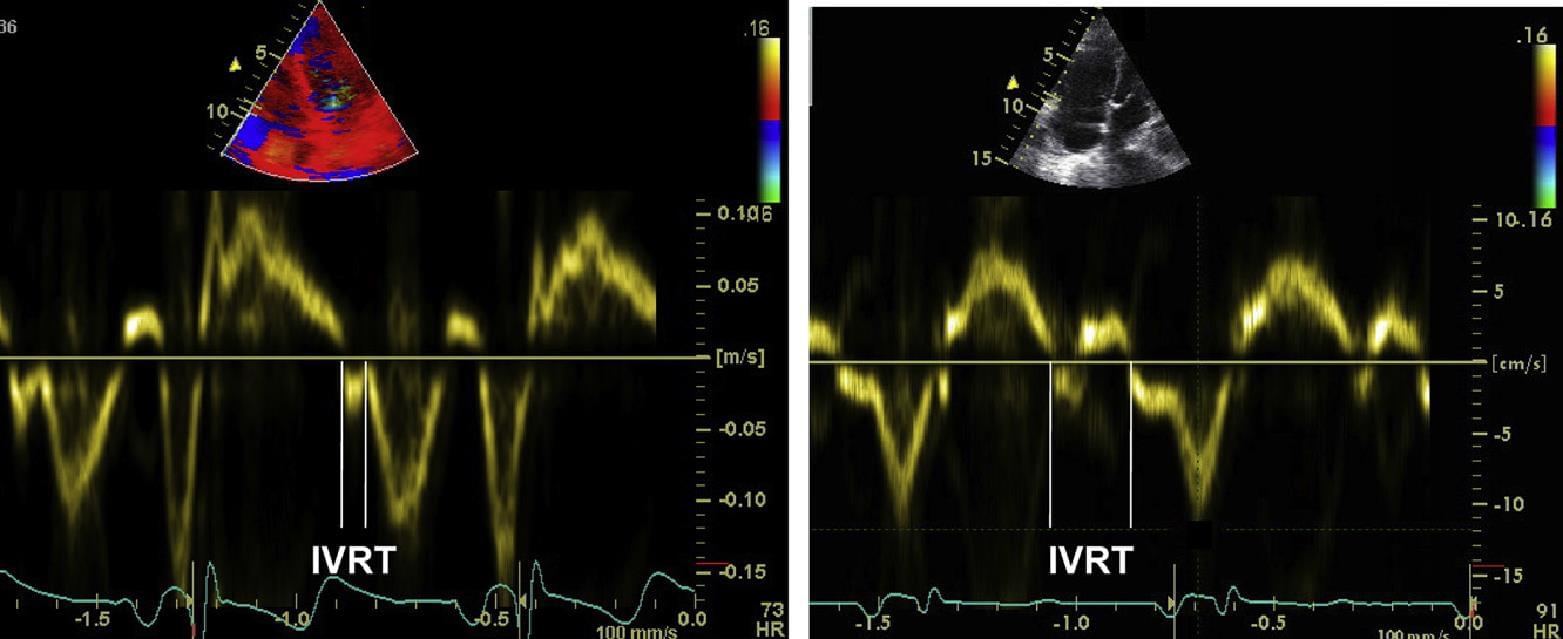
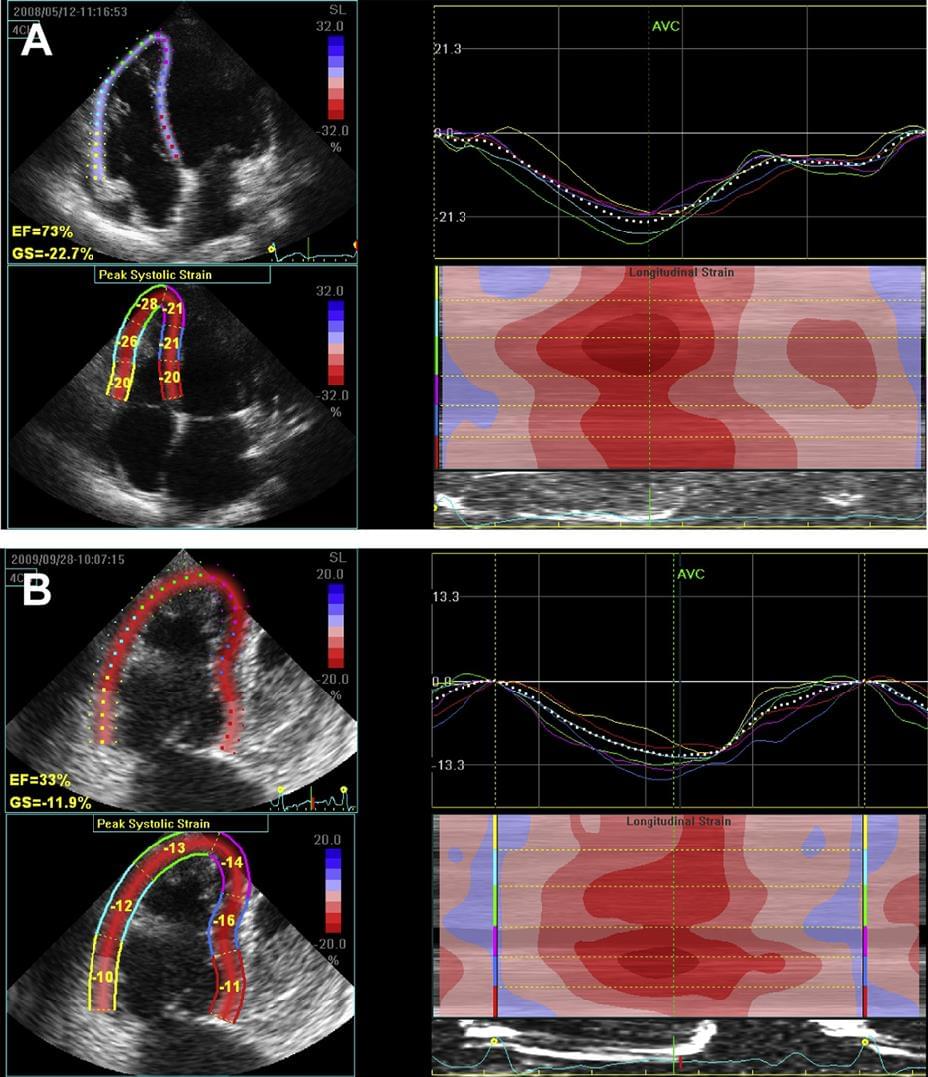
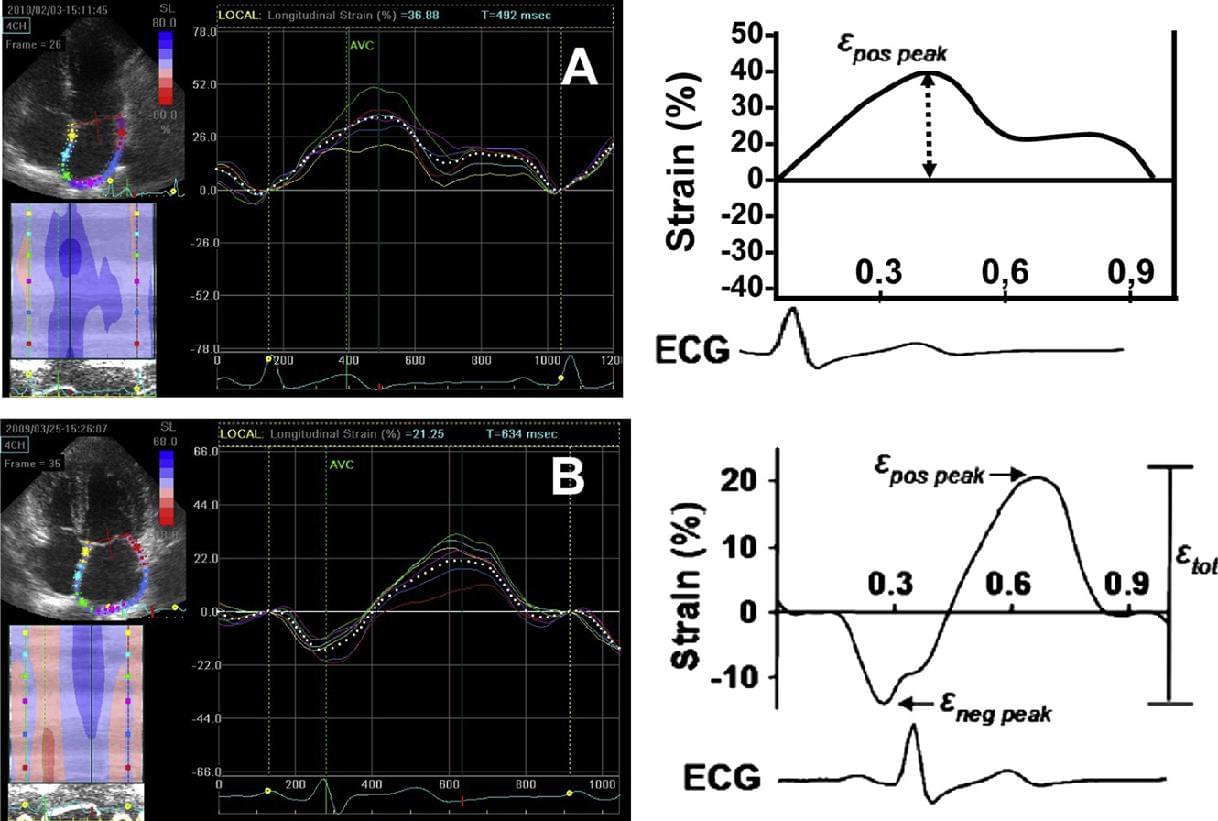










14.10.2019
Зубенко Виктор Петрович