Зміст
Резюме
Синдром внутрішньосудинної абсорбції при оперативній гістероскопії (OHIA) – це рідкісне і потенційно небезпечне для життя ускладнення, пов’язане з системною абсорбцією іригаційної рідини під час гістероскопії. Це може призвести до тяжких електролітних порушень, набряку головного мозку та легень, дизритмії та коагулопатії. Наводимо випадок 30-річної жінки, яка перенесла гістероскопічну міомектомію. Після введення 2,5 л фізіологічного розчину у неї виникла гемодинамічна нестабільність, дихальний дистрес і важкий метаболічний ацидоз, спочатку помилково сприйнятий як анафілактичний або геморагічний шок. Недостатній моніторинг дефіциту рідини та тиску іригаційної рідини спричинив погіршення стану. Цей випадок підкреслює важливість розпізнавання синдрому OHIA та його факторів ризику для своєчасного втручання і запобігання несприятливим наслідкам. Ретельний моніторинг балансу рідини є життєво важливим під час гістероскопічних операцій, щоб зменшити ризик розвитку синдрому OHIA.
Ключові слова
Гістероскопія, набряк легенів, перевантаження рідиною, ятрогенез
Ключові моменти
- Синдром OHIA виникає через системну абсорбцію іригаційної рідини, що використовується під час гістероскопічних процедур.
- Симптоматика різноманітна: енцефалопатія, набряк легенів, дизритмії, порушення електролітного балансу та коагулопатія.
- Під час гістероскопічних процедур слід контролювати баланс рідини та тиск іригаційної рідини, щоб зменшити ризик розвитку синдрому OHIA.
Вступ
Гістероскопія зазвичай використовується для внутрішньоматкових операцій, таких як міомектомія та поліпектомія. Дослідження повідомляють про низьку частоту небажаних явищ (0,2-0,4%), при цьому повідомлялося про випадки, пов’язані з перфорацією матки, масивною кровотечею та перевантаженням рідиною. Синдром внутрішньосудинної абсорбції при оперативній гістероскопії (OHIA) відноситься до ускладнень перевантаження рідиною, пов’язаних з іригаційним розчином і тиском, що застосовуються під час процедури. Можуть виникати тяжкі ускладнення, такі як серйозні електролітні порушення, набряк головного мозку та легенів, дизритмії та коагулопатія[1][2].
Опис випадку
Ми повідомляємо про випадок 30-річної жінки з добре контрольованою астмою в анамнезі та відсутністю алергії на лікарські препарати. Їй була виконана планова трансвагінальна міомектомія матки за допомогою гістероскопічного резектоскопа у зв’язку з підслизовою міомою матки. Операція проводилася під спінальною анестезією бупівакаїном, а також седоаналгезією мідазоламом і фентанілом. Для антибіотикопрофілактики вводили цефазолін. Як середовище для розтягнення матки використовували фізіологічний розчин (ФР).
Через сімдесят хвилин після операції стан пацієнтки раптово погіршився. У неї розвинулася гемодинамічна нестабільність (артеріальний тиск 76/42 мм рт.ст.), синусова брадикардія (35 уд./хв), зниження свідомості та десатурація (насичення периферичного кисню 85% без додаткового кисню). Спостерігався набряк обличчя та шийки матки, а також розсіяні двосторонні хрипи при аускультації легень. Розглядався анафілактичний шок, і пацієнтка отримала внутрішньом’язово адреналін та внутрішньовенно (в/в) клемастин і гідрокортизон. Через стійку брадикардію та змінену свідомість було запідозрено побічні ефекти, пов’язані з препаратами для індукції анестезії. Атропін і флумазеніл були введені без клінічного покращення. Тому було встановлено комбіновану загальну анестезію з севофлураном, пропофолом і рокуронієм та забезпечено оротрахеальну інтубацію. Був очевидний глотковий набряк.
Аналіз газів артеріальної крові показав змішану тяжку гіперхлоремічну метаболічну та респіраторну ацидемію (FiO2 100% – рН 7,03, PCO2 52 мм рт.ст., PO2 140 мм рт.ст., HCO3 13,7 мекв/л, лактат 0,6 ммоль/л) та гіпокаліємію. Розпочато заміщення електролітів та інтенсивну внутрішньовенну збалансовану кристалоїдну терапію. Через триваючу гіпотензію розпочали амінергічну підтримку норадреналіном через центральний венозний катетер. Підозрювали перфорацію матки, але лапароскопія виявила дифузний набряк кишкових петель, а з черевної порожнини аспірували приблизно 400-500 мл негеморагічної вільної рідини. Травматичних ушкоджень не виявлено.
Пацієнтка була госпіталізована у відділення інтенсивної терапії (ВІТ) для надання невідкладної післяопераційної допомоги.
Аналіз крові виявив анемію, лейкоцитоз з нейтрофілією, але без еозинофілії. Електролітна панель показала гіпернатріємію (146 ммоль/л) і гіперхлоремію (113 ммоль/л). Рівень триптази в сироватці крові був у межах норми. Рентгенограма грудної клітки показала застійні явища в легенях (Зображення 1А), а комп’ютерна томографія (КТ) – обширні двосторонні паренхіматозні ущільнення легень, особливо в залежних ділянках, а також двосторонній плевральний випіт і вільну внутрішньоочеревинну рідину (Зображення 2).
КТ голови виключила внутрішньочерепний набряк або крововилив, а трансторакальна ехокардіограма показала нормальну систолічну та діастолічну функцію без регіональних порушень руху стінок.
Аналіз операційного протоколу виявив позитивний баланс рідини від 1,5 до 2 л під час процедури, що спонукало до розгляду синдрому OHIA. Було застосовано низьку дозу петльового діуретика, і через 48 годин було досягнуто негативного балансу 2,5 л з клінічним покращенням (Зображення 1B). Вазопресорну підтримку припинили через шість годин після госпіталізації, а екстубацію успішно виконали впродовж перших 24 годин. Через вісім годин після госпіталізації у відділення інтенсивної терапії кислотно-лужні порушення були усунені. Пацієнтка була виписана зі стаціонару на 6-й день госпіталізації.
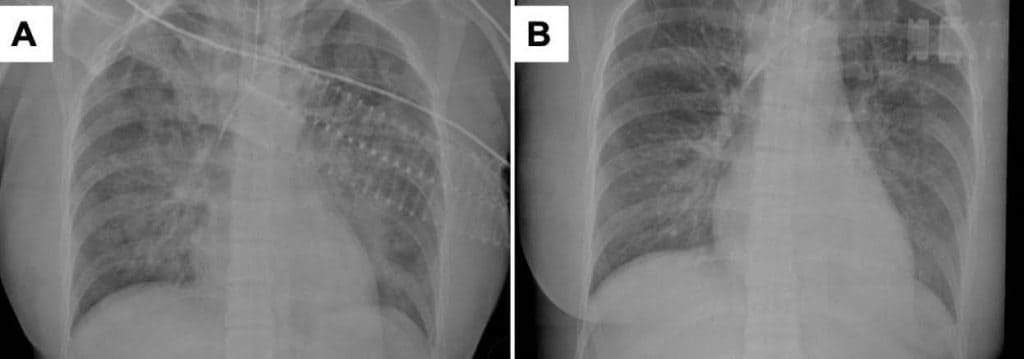
Зображення 1. Рентгенограма грудної клітки при надходженні у відділення інтенсивної терапії (А): набряк легеневих альвеол та просвітлення легеневих вен верхньої частки. Повторний огляд через 8 годин (В) зі значним покращенням.
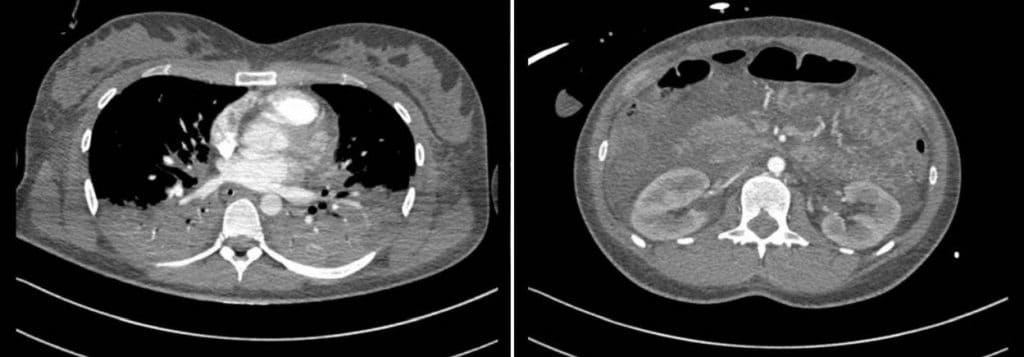
Зображення 2. КТ грудної клітки, черевної порожнини і тазу при надходженні у відділення інтенсивної терапії показує двосторонні паренхіматозні ущільнення в легенях, а також двосторонній плевральний випіт і вільну внутрішньоочеревинну рідину.
Обговорення
Синдром OHIA був вперше описаний у 1993 році, і на сьогоднішній день у світі зареєстровано менше 30 випадків, причому в Португалії не було жодного повідомлення. Він виникає внаслідок системної абсорбції іригаційної рідини, що використовується під час гістероскопії, шляхом ретроградного проходження через маткові труби, ендометрій та відкрите судинне русло, якому сприяють гідростатичний тиск та градієнт онкотичного тиску.
Жінки в пременопаузі більш схильні до підвищеного пасажу рідини в порожнину очеревини, що підвищує ймовірність розвитку гіпонатріємічної енцефалопатії та постійних неврологічних наслідків. Це пояснюється впливом естрогену, який інгібує аденозинтрифосфатні насоси та збільшує міжклітинний осмотичний градієнт, що призводить до більшої затримки рідини та набряку. На сьогоднішній день резектоскопи з біполярним струмом дозволяють використовувати ізотонічні розчини електролітів з кращим профілем безпеки, мінімізуючи ризик гіпонатріємії через гіпотонічні розчини, що не містять електролітів. Підвищена абсорбція рідини залежить від таких факторів, як глибина проникнення в міометрій (міомектомії та резекції перегородок матки становлять вищий ризик), обсяг операції на судинному руслі, тривалість операційного часу та хірургічний досвід. Вищий тиск іригаційної рідини (40-60 мм рт. ст.) і температура призводять до швидкого поглинання іригаційної рідини.
Регіонарній анестезії надають перевагу, оскільки вона дозволяє виявити ознаки та симптоми синдрому на ранніх стадіях і пов’язана з меншою абсорбцією рідини при гіпотонічній хворобі. Якщо необхідна загальна анестезія, перевага надається пропофолу, а не інгаляційному севофлурану, оскільки він пов’язаний з меншою абсорбцією рідини. Кількість введеної внутрішньовенно рідини також корелює з розвитком синдрому OHIA.
Синдром OHIA може проявлятися енцефалопатією, артеріальною гіпотензією, набряком легенів, аритмією та коагулопатією. У нашому випадку жінка в пременопаузі перенесла гістероскопічну міомектомію з використанням ФР як іригаційного середовища, і у неї розвинувся набряк дихальних шляхів і легенів. У неї також була гіпокаліємія і тяжка метаболічна та респіраторна ацидемія, що, можливо, сприяло виникненню брадиаритмії.
Початкові діагностичні гіпотези включали анафілаксію, побічні ефекти анестезуючих препаратів або перфорацію матки, що призвело до непотрібних процедур. Баланс рідини та тиск іригаційної рідини не контролювалися ефективно. Згідно з рекомендаціями BSGE/ESGE, баланс рідини слід вимірювати щонайменше кожні десять хвилин, а при використанні ФР у здорової жінки слід встановити максимальний баланс рідини 2 500 мл; при досягненні цієї межі операція повинна бути негайно припинена. Підхід до лікування залежить від симптомів і тяжкості стану. Якщо у пацієнтки спостерігається перевантаження об’ємом, основна увага при лікуванні буде зосереджена на оптимізації респіраторного статусу за допомогою таких заходів, як додаткова подача кисню, неінвазивна вентиляція з позитивним тиском або інтубація, за необхідності. Крім того,
Висновок
Цей випадок висвітлює недостатньо розпізнаний і потенційно небезпечний для життя стан, підкреслюючи важливість пильного моніторингу балансу рідини та врахування факторів ризику для запобігання розвитку синдрому OHIA при гістероскопічних операціях.
Посилання на джерела
- Munro MG, Christianson LA. Complications of hysteroscopic and uterine resectoscopic surgery. Clin Obstet Gynecol 2015;58:765–797.
- Lee EB, Park J, Lim HK, Kim Y Il, Jin Y, Lee KH. Complications of fluid overload during hysteroscopic surgery: cardiomyopathy and epistaxis – a case report. Anesth Pain Med (Seoul) 2020;15:61–65.
- Jackson S, Lampe G. Operative hysteroscopy intravascular absorption syndrome. West J Med 1995;162:53–54.
- Wang MT, Chang CC, Hsieh MH, Chang CW, Fan Chiang YH, Tsai HC. Operative hysteroscopy intravascular absorption syndrome is more than just the gynecological transurethral resection of the prostate syndrome: a case series and literature review. Taiwan J Obstet Gynecol 2020;59:748–753.
- Elegante M, Hamera J, Xiao J, Berger D. Operative hysteroscopy intravascular absorption syndrome causing hyponatremia with associated cerebral and pulmonary edema. Clin Pract Cases Emerg Med 2019;3:252–255.
- Umranikar S, Clark TJ, Saridogan E, Miligkos D, Arambage K, Torbe E, et al. BSGE/ESGE guideline on management of fluid distension media in operative hysteroscopy. Gynecol Surg 2016;13:289–303.
- Palancsai Siftar J, Sobocan M, Takac I. The passage of fluid into the peritoneal cavity during hysteroscopy in pre-menopausal and postmenopausal patients. J Obstet Gynaecol (Lahore) 2018;38:956–960.
- Yoo SW, Ki MJ, Oh YJ, Kim T, Nam S, Lee J. Rapid correction of severe hyponatremia and control of subsequent overcorrection in operative hysteroscopy intravascular absorption syndrome: a case report. Medicine (Baltimore) 2022;101:e31351.
- Singh S, Kumar N, Paul D, Sasidharan S. A case of operative hysteroscopy intravascular absorption syndrome: gynaecological TURP syndrome. Indian J Anaesth 2021;65:167–169.
- de Freitas Fonseca M, Andrade CM, de Mello MJE, Crispi CP. Effect of temperature on fluidity of irrigation fluids. Br J Anaesth 2011;106:51– 56.
- Bergeron ME, Ouellet P, Bujold E, Cote M, Rhéaume C, Lapointe D, et al. The impact of anesthesia on glycine absorption in operative hysteroscopy: a randomized controlled trial. Anesth Analg 2011;113:723–728.
- Munmany M, Gracia M, Nonell R, Cardona M, Pons M, Martin M, et al. The use of inhaled sevoflurane during operative hysteroscopy is associated with increased glycine absorption compared to intravenous propofol for maintenance of anesthesia. J Clin Anesth 2016;31:202–207.
- Smith CC, Brown JPR. A case of cardiac arrhythmia from absorption of normal saline during hysteroscopic myomectomy. J Minim Invasive Gynecol 2019;26:770–773.