Автори: Johannes Rübenthaler, Maximilian Reiser, Dirk-André Clevert
Вступ
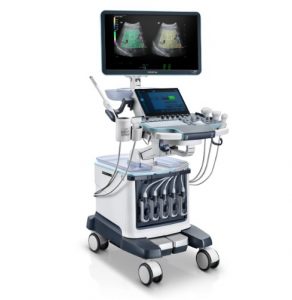
Первісна діагностика пацієнтів з підозрою на захворювання сонної артерії полягає в дуплексному УЗД судин (Зобр. 1). Дуплексна ультрасонографія також є найкращим методом візуалізації для спостереження пацієнтів після імплантації стента або ендартеректоміі.
Кількісне визначення стенозу внутрішньої сонної артерії (ВСА) має важливе значення для клінічного ведення пацієнтів з симптомами вираженого стенозу (70% -90%) ВСА, а також у пацієнтів без симптомів з високим рівнем стенозу.
При УЗД черевної порожнини аневризми черевної аорти (АЧА) виявляються у 2-8% чоловіків у віці старше 65 років, причому частота зустрічальності у жінок нижче в 4 рази. Всі АЧА визначаються як збільшення черевної аорти більше 3,0 см або більше 50% від нормального розміру. Приблизно 85% всіх АЧА виявлені нижче відходження ниркових судин. Хірургічне втручання рекомендується при будь-якому діаметрі більше 5,5 см у чоловіків або 5,0 см у жінок.
Розрив AЧA показує рівень смертності від 85% до 90%. Клінічне ведення включає в себе консервативне лікування з подальшим УЗД для безсимптомних АЧА діаметром менше 5,5 см, так як існує більш високий ризик ускладнень після втручання, ніж розриву і хірургічного відновлення. Дуплексна ультрасонографія також є методом вибору візуалізації для виявлення ускладнень після пункції стегнової артерії, так як вони зустрічаються в 0,1% -9% випадків з аневризмами, причому артеріовенозні свищі, розшарування і гематоми є найбільш поширеними ускладненнями.
УЗД с контрастним посиленням
Сучасні режими контрастування використовують режим з низьким механічним індексом, який обробляє нелінійні сигнали, що випускаються мікробульбашками контрастної речовини, і розділяє сигнали тканини і контрастної речовини. SonoVue (Бракко, Мілан, Італія), найбільш часто використовуваний серед сучасних контрастних агентів УЗД, складається з фосфоліпідних оболонок, які стабілізують мікропухирці, і їх серцевини, що містять газ гексафторид сірки (SF6). Фосфоліпіди метаболізуються ендогенно, а газ SF6 виділяється через легені протягом періоду часу до 8 хвилин.
Захворювання сонної артерії
Стеноз
Близько 10% -15% всіх інсультів і транзиторних нападів ішемічного походження є наслідком атеросклеротичного стенозу ВСА, особливо в проксимальній частині. Найбільш важливою при початковій обробці стенозу ВСА є диференціація між повною оклюзією ВСА або преокклюзивним стенозом, який характеризується як стеноз не менше 90%. Прекклюзивний симптоматичний стеноз можна лікувати хірургічним втручанням або іншими інтервенційними заходами, щоб запобігти загрозливий геміпарез. З чутливістю від 86% до 98% і специфічністю від 87% до 100%, УЗД судинної системи ВСА має високу діагностичну точність в характеристиці стенозу ВСА і диференціації оклюзії ВСА в залежності від досвіду дослідника і налаштувань параметрів. За допомогою CEUS навіть можливо поліпшити візуалізацію захворювань сонної артерії, виявляючи кровотік через стеноз навіть в подовжених судинах, без браку в залежності від кута або накладення артефактів кровотоку (Зобр. 2).
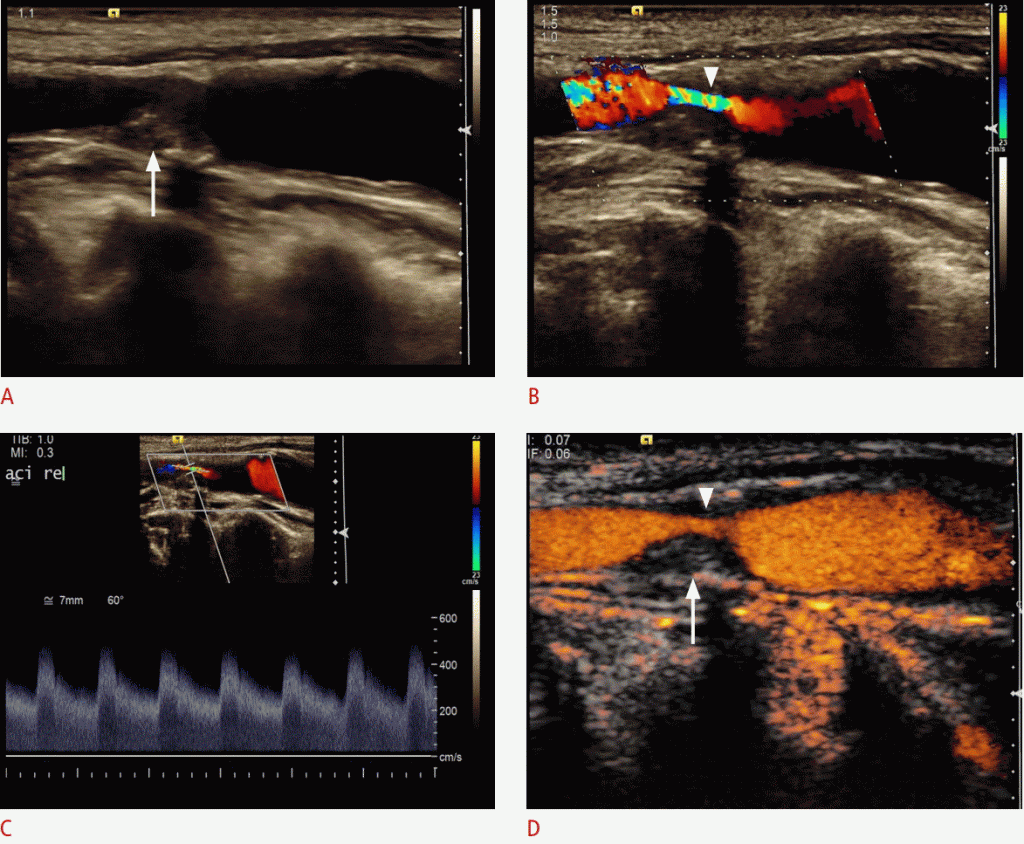
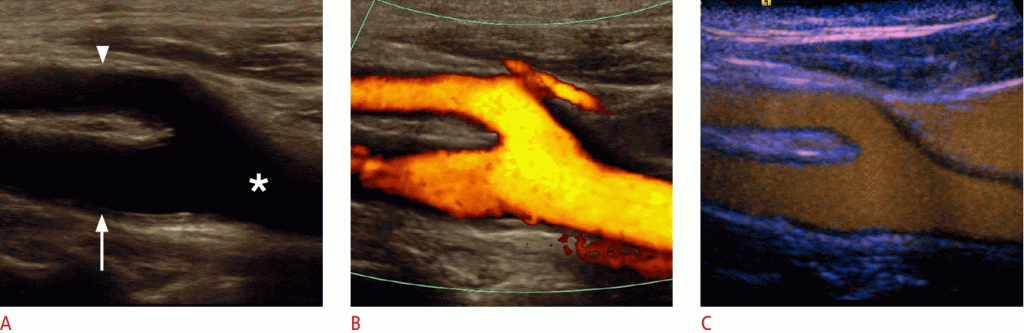
Зображення 2: УЗД 67-річної жінки з недавніми ішемічними неврологічними симптомами.
B-режим показує стеноз внутрішньої сонної артерії (ICA) високого ступеня з м’якими бляшками (стрілка). B, C. Дуплексная ультрасонографія показує стеноз ВСА високого ступеня (наконечник стрілки) з максимальною систолічною швидкістю потоку близько 500 см / сек. D. Ультрасонографія з контрастним посиленням (CEUS) виявляє внутрішньостенотичний потік (наконечник стрілки) і виявляє повний залишковий просвіт і довжину стенозу. Крім того, CEUS підтверджує відсутність неоваскуляризации всередині сплетення (стрілка).
Постінтерваційне спостереження
Традиційним методом вибору для лікування симптоматичних і безсимптомних пацієнтів зі стенозом ВСА є каротидна ендартеректомія. Стентування сонної артерії (CСА) є альтернативою каротидної ендартеректомії, особливо у пацієнтів з високим ризиком ускладнень після операції, наприклад, у пацієнтів із значним серцево-легеневим захворюванням. Використання КЕЕ несе ризик рестенозу близько 25%, тоді як ризик рестенозу після ССА нижче 5% в більшості випадків в перші 5 років після стентування. Дуплексна ультрасонографія і CEUS представляють собою методи візуалізації, вибрані для постінтерваціонного спостереження за рестенозом після CСА і для характеристики рестеноза в стенті після стентування (Зобр. 3)
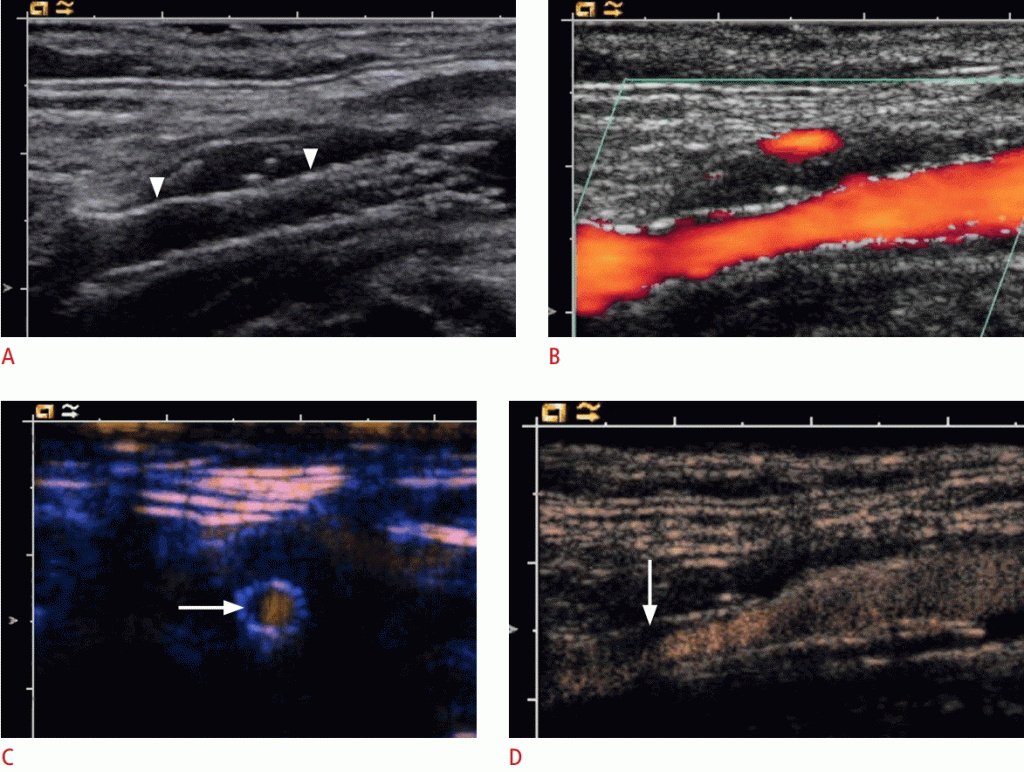
Зображення 3: УЗД після установки стента внутрішньої сонної артерії (ВСА).
B-режим показує стент (стрілки). B. Ультразвукова доплерографія не може показати будь-якого стенозу в стенті. C. На зображенні стента, отриманому за допомогою контрастного ультразвукового дослідження (CEUS) з поперечним перерізом, показана напівкругла м’яка бляшка (стрілка) і перфузуючий просвіт стента. Відповідно до критеріїв стенозу області ступінь стенозу в стенті становитиме приблизно 40-50%. D. CEUS показує деякі м’які бляшки (стрілка) на передній стінці стента.
Ускладнення після втручання
З частотою близько 2% -10%, прокол сонної артерії є найбільш поширеним ускладненням після катетеризації внутрішньої яремної вени. Це втручання в основному виконується у відділенні інтенсивної терапії або для інтервенційних радіологічних процедур. Найбільш важливим ускладненням є артеріо-венозний свищ, який іноді клінічно можна розглядати як набряк шиї, іноді пульсуючий. (Зобр. 4)
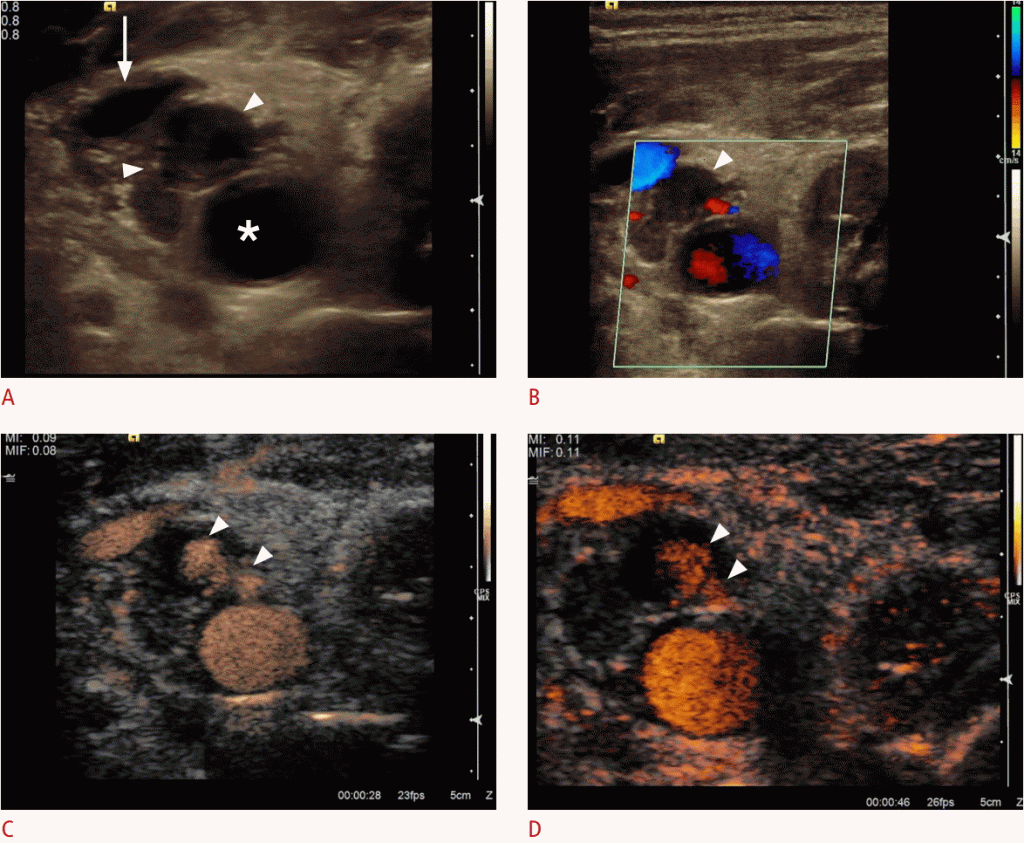
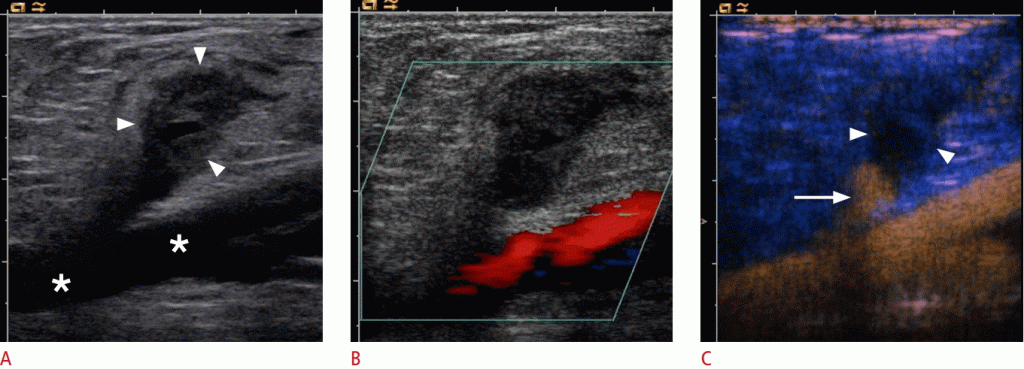
Зображення 4: A. Поперечний перетин B-режиму ідентифікує гіпоехогенну структуру, яка передбачає гематому (стрілки) без зв’язку між загальною сонною артерією (зірочка) і внутрішньої яремної веною (стрілка). B. Гематома не вказує перфузії (стрілки) на кольоровому Доплера. C, D. Сонограми з підвищеною контрастністю загальної сонної артерії демонструють поглинання контрасту всередині гематоми (наконечники стріл) як наявність псевдоаневризма.
Характеристика бляшок
Вважається, що виразкові бляшки є фактором етіології інсультів при захворюваннях сонних артерій. Використання CEUS є методом візуалізації для виявлення виразкових бляшок, які можуть бути викликані запальними процесами і неоваскуляризією всередині бляшки (Зобр. 5)
Зображення 5: УЗД атероматозної бляшки в сонної артерії.
B-режим показує значний стеноз атероматозних бляшок (стрілки). B. Ультрасонографія з контрастуванням показує неоваскуляризації всередині бляшки (наконечник стрілки) як ознаку вразливості бляшки.
Аневризма черевної аорти
Аневризма черевної аорти
АЧА визначаються як збільшення черевної аорти більше 3,0 см або більше 50% від нормального розміру. Розрив AЧA показує рівень смертності від 85% до 90% і є 10-й найбільш поширеною причиною смерті серед чоловіків старше 55 років. Негайне лікування розірваної АЧА має важливе значення, так як нелікована розірвана АЧА, швидше за все, призведе до смерті. Приблизно 85% всіх AЧA виявлених нижче виходу ниркових судин.
Хірургічне втручання рекомендується при будь-якому діаметрі більше 5,5 см у чоловіків або 5,0 см у жінок. Основним ризиком є розрив, з ризиком менше 1% для аневризм діаметром менше 5,5 см, 10% для аневризм діаметром від 5,5 до 7,0 см і 33% для аневризм діаметром більше 7,0 см. З чутливістю 95% – 98%, дуплексна ультрасонографія є вихідним методом візуалізації для діагностики АЧА. Використання CEUS може допомогти візуалізувати прямі ознаки розриву (Зобр. 6).
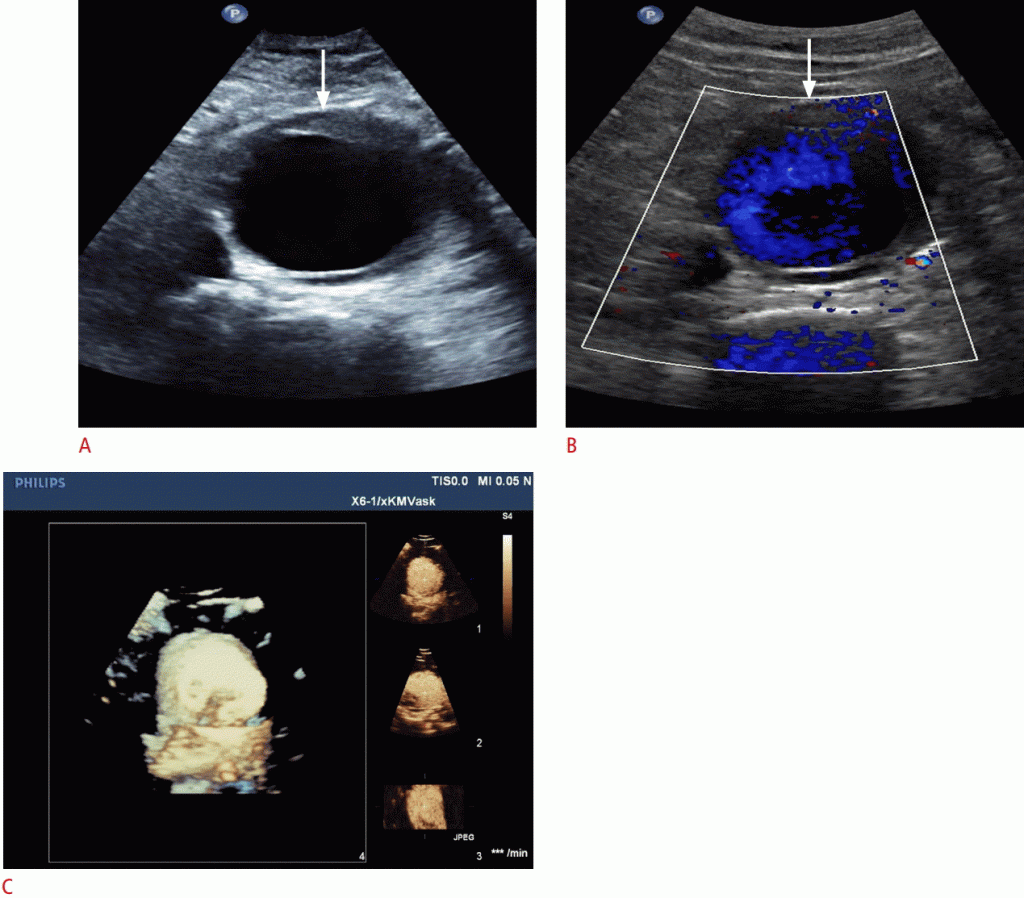
Зображення 6: УЗД аневризми аорти. Сонограми A, B. B-режим (A) і кольорова доплерографія (B) демонструють інфрааортальну аневризму (стрілки). C. Ультрасонографія з чотириразовим контрастуванням з дозволом в реальному часі показує ту ж аневризму інфраренального відділу аорти в площині x (справа вгорі), площини y (праворуч у центрі) і площині z (справа внизу) з об’ємним зображенням (зліва).
Ускладнення після трансфеморальної пункції
Псевдоаневризми
Помилкові аневризми або псевдоаневризма після трансфеморальної пункції зустрічаються в 0,05% -9% всіх випадків. Вони характеризуються як розрив в шарі стінки артерії, яка не закупорюється після пункції. Протікаюча кров викликає пульсуючу гематому, яка утворює заповнену кров’ю порожнину, яка подається через з’єднання між порожниною і проколеної артерією. Зі збільшенням розміру збільшується ризик розриву, що робить необхідним швидкий діагноз (Зобр. 7)
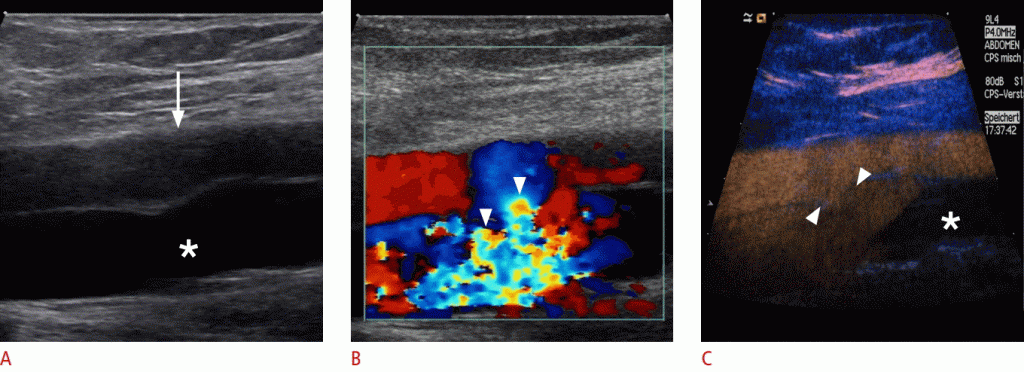
Зображення 7: УЗД стегнової артерії після катетерного втручання.
A, B. Знімки поперечного перерізу B-режиму (A) і кольорового доплера (B) стегнової артерії (зірочки) визначають псевдоаневризму (наконечники стріл) без будь-якого помітного сигналу потоку. C. Ультрасонографія з контрастуванням показує часткову перфузію (стрілка) псевдоаневризма, в той час як в дистальній частині перфузия відсутня (стрілки).
Артеріовенозний свищ
Артеріовенозні свищі виникають в 0,1% -3,6% усіх випадків після трансфеморальним пункції. Вони описані як ятрогенно аномально пов’язані артерії та вени. Якщо фістула досить велика, вони можуть бути гемодинамічно значущими, викликаючи зниження периферичного опору.
Артеріовенозні свищі мають тенденцію до збільшення в розмірах, що робить хірургічне лікування кращим втручанням у багатьох випадках. У деяких випадках артеріовенозна фістула виникає мимовільно або може бути здавлена ультразвуком. (Зобр. 8)
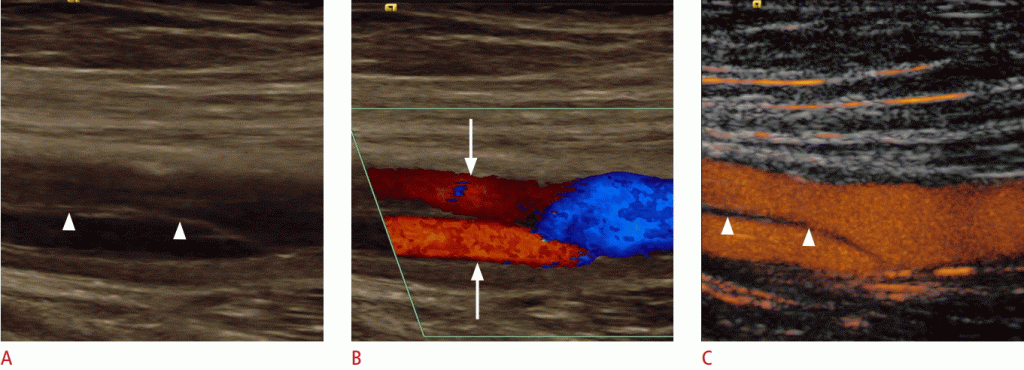
Зображення 8: УЗД стегнової артерії після катетерного втручання.
A, B. На поперечних зрізах B-режиму (A) і кольорового доплера (B) артеріовенозна фістула з турбулентним кровотоком в артеріовенозній фістулі (наконечники стріл) показана між загальною стегновою артерією (стрілка) і веною (зірочка)). Повна довжина свищової доріжки обумовлена розмежуванням аліасів. C. Ультрасонографія загальної стегнової артерії та вени з посиленням контрасту дозволила виявити повну протяжність артеріовенозного свищуватого шляху (наконечники стріл) і підтвердити наявність артеріовенозної комунікації. Дистальна частина загальної стегнової вени (зірочка) не вказує жодного контрастного поглинання через артеріального сканування.
Диссекція
Розсічення відбувається в 0,3% -3,6% усіх випадків після трансфеморальної пункції. Подібно до того, як це було описано раніше для розтину сонних артерій, судинна ультрасонографія є методом візуалізації вибору для виявлення і характеристики розшарування, показуючи фрескову гематому, а також помилковий і істинний просвіт, і додатково візуалізуючи будь-яке зменшення об’ємного потоку крові в хибному просвіті, що призводить до збільшення ризику тромбозу, емболізації або навіть часткової або повної оклюзії артерії. Як обговорювалося раніше, сучасні ультразвукові зонди можуть ідентифікувати невеликі розсічення з дуже тонкими мембранами менше 1 мм. CEUS може підвищити точність діагностики в складних випадках (Зобр. 9, 10).
Гематома
Гематоми виникають в 0,4% -11% всіх випадків після трансфеморальним пункції і є досить поширеним ускладненням в цьому випадку. Зазвичай гематоми локально обмежені і резорбуються протягом короткого періоду часу. Їх можна легко зобразити за допомогою дуплексного УЗД.
Зображення 9: УЗД диссекции загальної стегнової артерії.
На сонограмах A, B. B-режиму (A) і кольорового доплера (B) показана загальна стегнова артерія з розшаруванням інтими (стрілки). Обидва просвіти перфузуються в кольоровому доплеровському режимі (стрілки). C. Завдяки своєму чудовому просторовому розширекнню, що розсікає мембрану (наконечники стріл) обидва перфузованих просвіти чітко зображені на УЗД з контрастним підсиленням.
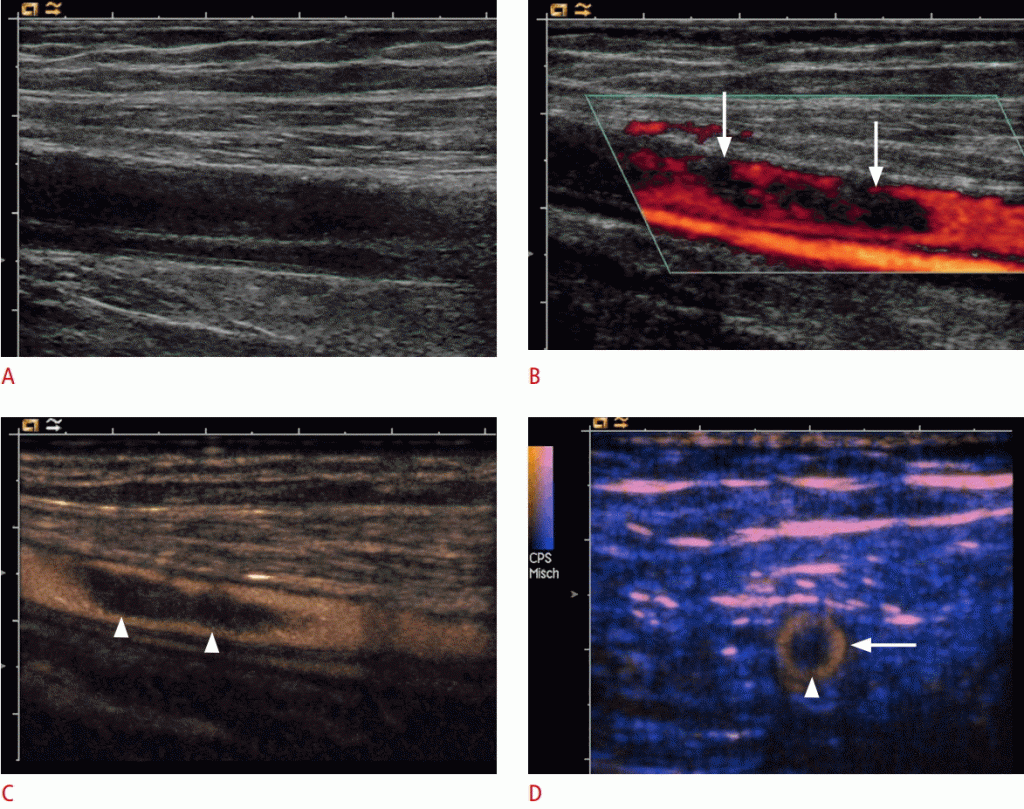
Зображення 10: УЗД загальної стегнової артерії з підозрілим розшаруванням.
На сонограмах A, B. B-режиму (A) і кольорового доплера (B) показана неповна перфузія просвіту судини (стрілки). C, D. Поздовжні (C) і поперечні (D) контрастні зображення демонструють плаваючу емболію (наконечники стріл) в центрі загальної стегнової артерії (стрілка).
Висновок
Для виявлення, характеризації та спостереження судинних патологій першим вибором є дуплексна ультрасонографія. Тим не менш, дуплексна УЗД має технічні обмеження в діагностичному використанні, наприклад, через накладення артефактів, які можуть ускладнити діагностику. Застосування CEUS може підвищити діагностичну ефективнысть.
Обстеження з використанням CEUS сонної артерії і периферичних судин покращують розмежування судинних розладів у окремих випадках. Це швидка, не йонізуюча, економічно ефективна візуальна модальність практично без протипоказань. Застосування ультразвукового контрастного агента підвищує чутливість ультразвукового дослідження при судинних захворюваннях і долає деякі обмеження у виявленні кровотоку в судинних структурах.
В нашому каталозі вам доступні апарати з підтримкою досліджень з контрастними речовинами. Якщо у вас залишились питання, звяжіться з нашим менеджером і він відповість на них.