🤖 Короткий переказ від ШІ
Ультразвукове контрастне дослідження (УКД) є ефективним методом для виявлення та характеристики фокальних уражень печінки, надаючи детальнішу інформацію про кровопостачання порівняно з традиційною сонографією. Попри обмеження, цей метод значно підвищує точність діагностики раку печінки.
Стаття детально розглядає технічні аспекти, застосування УКД у діагностиці доброякісних та злоякісних уражень, а також його роль в абляційній терапії. Для ефективної діагностики та моніторингу рекомендується використання сучасних УЗД апаратів, таких як GE Voluson E8.
✅ Ключові тези зі статті:
- Діагностика: УКД забезпечує високу точність (92-95%) у виявленні та характеристиці фокальних уражень печінки.
- Лікування: УКД допомагає при плануванні та моніторингу абляційної терапії, покращуючи результати лікування.
- Переваги: Метод безпечний, неіонізуючий, має високу часову роздільну здатність та покращену візуалізацію порівняно зі стандартним УЗД.
- Обмеження: До обмежень відносяться погане проникнення на великій глибині та артефакти, а також можливе перекриття шаблонів посилення різних уражень.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
АВТОРИ: Mark Abel, MBBS, Wey Chyi Teoh, MBBS, Edward Leen, MD
ОСНОВНІ ПОЛОЖЕННЯ
• Ультразвукове контрастне дослідження (УКД) є дуже ефективним у виявленні та характеристиці фокальних уражень печінки (ФУП), а також для моніторингу абляційної терапії.
• Ультразвукові контрастні речовини (УКР) є чистими внутрішньосудинними індикаторами з відмінним профілем безпеки, які ідеально підходять для оцінки змін перфузії.
• Обмеження включають в себе погане проникнення і нелінійне поширення артефактів.
ВВЕДЕННЯ
За оцінками, щорічно у 782.000 пацієнтів діагностується первинний рак печінки і 746.000 смертельних випадків від нього. Печінка також є другим найбільш поширеним місцем для метастазування, і значно більше пацієнтів страждають від метастазів у печінку, ніж від первинного раку.
Ультразвук є найбільш часто використовуваним методом візуалізації печінки. Це недорогий, портативний, неіонізуючий метод, який має відмінний профіль безпеки. Традиційна сонографія у відтінках сірого і кольорова доплерографія все ж таки мають характерні обмеження. По-перше – це те, що виявлення ФУП ускладнюється наявністю аналогічної ехогенності вогнища ураження і навколишньої паренхіми печінки. По-друге, точна характеристика ФУП є проблематичною при різних патологічних ураженнях, які мають особливості накладення або недискретність картини при сірошкальному відображенні. І по-третє, хоча кольорова і спектральна доплерографія дозволяє візуалізувати основні динамічні характеристики кровотоку, вона не може визначати мікросудинні ураження або якісні показники посилення.
Поява УКР поліпшило характеристику новоутворень печінки шляхом порівняння зміни динаміки накопичення препарату вогнищем ураження з сусідньою паренхімою печінки. Крім того, здатність провести оцінку ФУП в реальному часі у всіх судинних фазах наділяє УКД часовою роздільною здатністю, яка перевершує більшість інших методів візуалізації. УКД є дуже корисним методом диференціальної діагностики ФУП, з точності від 92% до 95%, за даними літератури. Його використання зменшило частоту проведення подальшого дослідження або біопсії.
У 2012 році Всесвітня федерація з ультразвуку в медицині і біології (WFUMB) і Європейська федерація товариства з ультразвуку в медицині та біології (EFSUMB) спільно з Азіатською федерацією товариства з ультразвуку в медицині та біології, Американським інститутом ультразвуку в медицині, Австралоазіатським товариством ультразвуку в медицині і Міжнародним товариством контрастного ультразвуку опублікувало ряд керівних принципів для того, щоб стандартизувати використання УКД при діагностичних дослідженнях печінки.
Ця оглядова стаття охоплює всі технічні особливості проведення УКД, УКР при оцінці характерних новоутворень печінки та їх використання при абляційній терапії, обмеження техніки, підводні камені та перспективи на майбутнє.
ЧАСТИНА 1: ТЕХНІЧНІ АСПЕКТИ
УЛЬТРАЗВУКОВІ КОНТРАСТНІ РЕЧОВИНИ
Фізичні властивості
УКР містять газові бульбашки, які називаються мікробульбашками. Велика частина УКР, які використовуються в клінічній практиці в даний час, відносяться до другого покоління. Типове друге покоління мікробульбашок має стабільну зовнішню оболонку з тонкого (10-200 нм) біосумісного матеріалу (наприклад, фосфоліпіди) і внутрішнє ядро гідрофобного газу (наприклад, перфторвуглероди, гексафторид сірки або азот), який має високомолекулярну вагу, знижує розчинність і здатність до дифузії . Ці властивості підвищують стійкість до артеріального тиску, що запобігає розчинення мікробульбашок в кровотоці.
Мікропухирці мають розмір приблизно від 3 до 5 мкм в діаметрі, що трохи менше, ніж клітини червоної крові людини, але набагато більше, ніж молекули контрастних речовин для КТ і магнітно-резонансної томографії (МРТ). Вони залишаються в кровоносному басейні, тому що не можуть проникати через судинний ендотелій в інтерстицій. При цьому вони залишаються досить маленькими для того, щоб переходити в мікроциркуляторне русло легеневих капілярів для безпечної екскреції. Газова складова УКР експірується легенями через, приблизно, 10- 15 хвилин, в той час як оболонка або руйнується в печінці або екскретується нирками.
Більшість УКР поступово виводиться з кровоносного басейну після п’ятої хвилини. Винятком є Sonazoid (Daiichi Sankyo, GE Токіо, Токіо, Японія), який залишається в печінці людини протягом декількох годин. Це пояснюється тим, що мікропухирці Sonazoid фагоцитуються купферівськими клітинами, після того, він очищається з пулу крові. Sonazoid, таким чином, порівнюється з суперпарамагнітними речовинами на основі оксиду заліза, які використовуються для МРТ візуалізації печінки. Це єдиний комерційно доступний УКР з ефективною післяваскулярною фазою.
Взаємодія мікробульбашок з ультразвуком
Незважаючи на те, що мікропухирці збільшують зворотне розсіювання ультразвукових променів і викликають високоехогенний сигнал, для ефективного контрастного зображення потрібно коливні мікросфери.
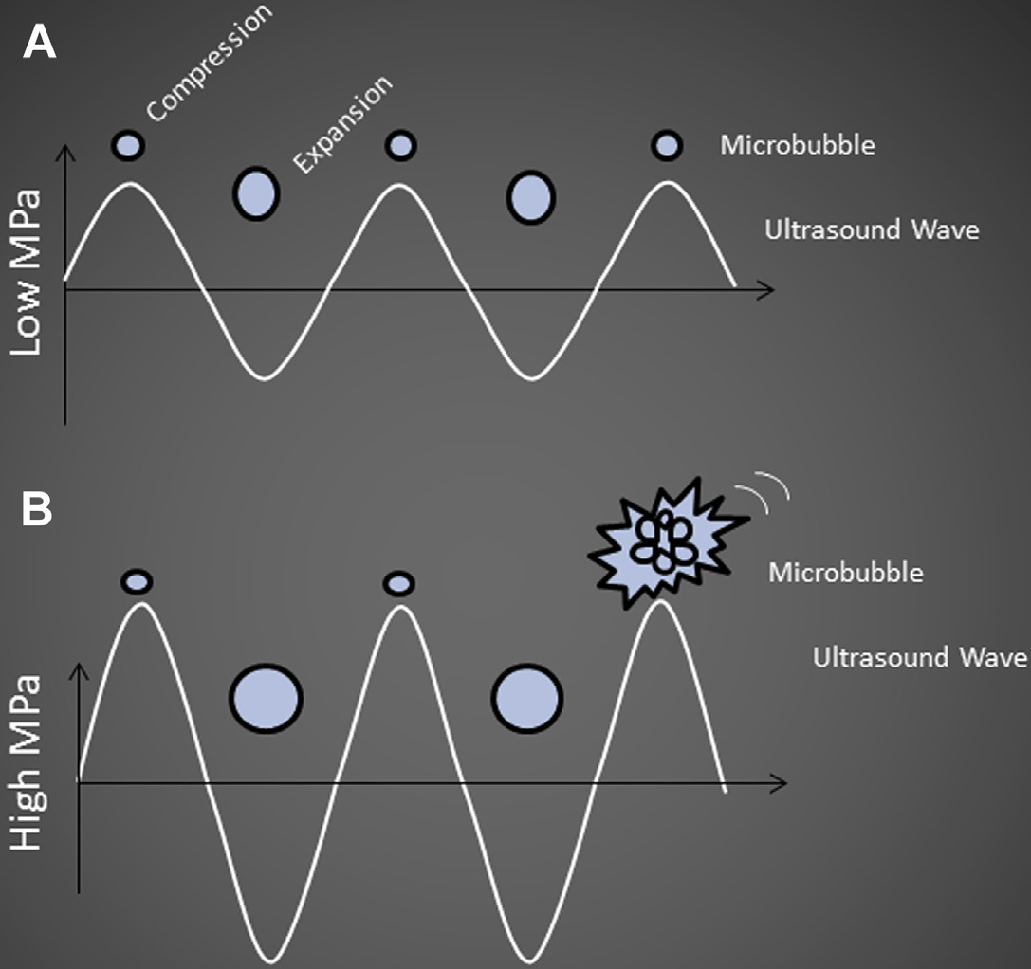
Природні резонансні частоти мікробульбашок (при яких вони виробляють максимальні коливання) знаходяться між 3 і 5 МГц. Це співпадає з частотами, які ми використовуємо для візуалізації органів черевної порожнини. При впливі ультразвукової хвилі з низьким акустичним тиском, мікропухирці об’ємно розширюються і стискаються контрольованим чином, і таким чином піддаються стабільній кавітації. При високому акустичному тиску, мікропухирці досягають нестабільного розміру і руйнуються, піддаючись інерціальній кавітації (рис. 1).
Коливні мікропухирці виробляють асиметричні, нелінійні сигнали. Тканини людини відбивають в значній мірі лінійні сигнали з мінімальною кількістю нелінійних сигналів з низьким акустичним тиском. Гармоніки, що виникають із нелінійних сигналів від коливних мікробульбашок, обробляються спеціалізованим програмним забезпеченням для контрастної ультрасонографії, для отримання зображення, яке відображає виключно ехосигнал мікробульбашок.
Рис. 1. Коливання мікробульбашок. (А) Стабільна кавітація при низькому акустичному тиску. (B) Інерційна кавітація при високому акустичному тиску.
|
Комерційно дозволені УКР • SonoVue (Бракко SpA, Мілан, Італія) складається з газу гексафториду сірки, який міститься в межах фосфоліпідної оболонки. Це УКР в даний час схвалено для використання в Європі, Китаї, Кореї, Гонконгу, Сінгапурі, Індії, Нової Зеландії, та Бразилії. • Sonazoid складається з перфторбутана в фосфоліпід ній оболонці. Це УКР ліцензовано для використання в Японії і Південній Кореї. • Definity/Luminity (Lantheus Medical, Billerica, Массачусетс) складається з перфлутрена в ліпідній оболонці. Воно ліцензоване в Канаді, Мексиці, Ізраїлі, Новій Зеландії, Індії, Австралії, Кореї, Сінгапурі й Об’єднаних Арабських Еміратах. • Optison (GE Healthcare, Прінстон, Нью-Джерсі) складається з сироваткового альбуміну людини з перфлутреновим ядром. В даний час проходить випробування для візуалізації печінки. • Levovist (Bayer AG, Schering AG, Берлін, Німеччина) складається з галактози, пальмітинової кислоти і повітря. Це перше покоління УКР, яке було схвалено для візуалізації печінки. Це УКР в даний час не доступно, хоча його виробництво відновила Японія. • На сьогоднішній день, не існує УКР, які були б схвалені комісією з нагляду за харчовими продуктами і медикаментами США (FDA) для оцінки патології черевної порожнини. Optison і Definity були схвалені FDA тільки для візуалізації серця і можуть бути використані юридично не за прямими показаннями для візуалізації органів черевної порожнини. |
Фази посилення
Нормальна печінка має подвійне кровопостачання, і приблизно одна третина крові йде від печінкової артерії і дві третини від портальної вени. Судинні фази при УКД печінки схожі з КТ і МРТ, прогресуючи від артеріальної до портовенозної фази, і закінчуються пізньою (відстроченою) фазою. Посилення малюнка ФУП протягом всієї судинної фази має вирішальне значення для їх ідентифікації.
Артеріальна фаза починається з потрапляння УКР в печінкову артерію. Залежно від циркуляторного статусу, це, як правило, відбувається від 10 до 20 секунди після ін’єкції УКР. Портовенозна фаза починається тоді, коли УКР потрапляє в основну портальну вену, і це відбувається приблизно від 30 до 45 секунди. Артеріальна і портовенозна фази перекриваються, тому що остання триває до 45 секунд. Пізня фаза починається після 120 секунд і триває до зникнення мікробульбашок з циркуляторного русла, приблизно від 4 до 6 хвилин. Додаткова постваскулярна фаза описується для препарату Sonazoid, яка починається через 10 хвилин після ін’єкції і триває до години або довше (Таблиця 1).
Таблиця 1.
Показано початок судинних фаз та їх тривалість.
|
Судинна фаза |
Початок |
Кінець |
|
Артеріальна фаза |
10-20 сек |
30-45 сек |
|
Портовенозна фаза |
30-45 сек |
120 сек |
|
Пізня фаза |
> 120 сек |
4-6 хв |
|
Постваскулярна/Купферовська фаза |
10 хв |
> 1 год |
Побічні ефекти і протипоказання
УКР мають значно кращий профіль безпеки в порівнянні з контрастними речовинами для КТ або МРТ, з набагато меншою частотою алергічних і анафілактичних реакцій. Вони не мають нефротоксичності або гепатотоксичності. Найбільш поширені побічні ефекти включають: запаморочення, нудоту/блювоту, свербіж, які зазвичай є незначними і минущими. Деякі пацієнти можуть мати помірну гіпотензію, хоча це, швидше за все, вазовагальна відповідь. Єдиним протипоказанням для Sonazoid є алергія на яйця. Іншими протипоказаннями, крім відомої гіперчутливості до гексафториду сірки (SonoVue) і перфлутрену (Definity), також є погіршення застійної серцевої недостатності у пацієнтів, гострий коронарний синдром, важка легенева гіпертензія, гострий респіраторний дистрес синдром і пацієнти з серцевими шунтами. Серйозні некритичні побічні реакції на УКР у пацієнтів з серцевими шунтами рідкісні і зустрічаються приблизно в 0,01% до 0,03% пацієнтів, більшість з яких анафілактоїдні по природі. Не існує зв’язку між використанням УКР і збільшенням ризику смерті серед пацієнтів.
При введенні УКР, має бути доступне реанімаційне обладнання і навчений персонал для ліквідації несприятливих ускладнень, у тому числі гострої анафілаксії. Після ін’єкції УКР, пацієнти повинні спостерігатися протягом, як мінімум, 30 хвилин перед випискою.
УКР не ліцензовані для використання у педіатричних хворих, хоча вони широко призначаються за прямими показаннями у дітей. Повідомляється про поодинокі побічні ефекти, без серйозних ускладнень або смертельних результатів. Існують дані про використання УКР протягом вагітності або під час годування грудьми.
ОБЛАДНАННЯ
Зображення з низьким механічним індексом
Механічний індекс (МІ) ультразвукової системи є наближеним відображенням акустичного тиску переданого ультразвукового пучка. Щоб звести до мінімуму руйнування мікробульбашок і продовжити їх присутність в крові, необхідно низький МІ зображення. Низький МІ також зменшує кількість нелінійних гармонійних сигналів, які виникають в м’яких тканинах.
Хоча недостатня акустична потужність і дає слабкий зворотний сигнал, технологічні досягнення дозволяють одержувати зображення гарної якості при низькому МІ. Це досягається за рахунок використання короткої послідовності імпульсів, які модулюються по амплітуді, фазі, або комбінації обох. Налаштування МІ менше або дорівнює 0,3, як правило, рекомендуються для візуалізації при УКД. Оптимальні параметри візуалізації різняться між виробниками пристроїв і можуть бути набагато нижче.
Режим візуалізації
Зображення УКД розглядаються за допомогою режимів side-by-side або накладення ультразвукових зображень в контрастному режимі. Автор використовує вид подвійного екрану, який розділяє дисплей на налаштований контрастний режим і зображення в B-режимі з низьким МІ. На останнє зображення в контрастному режимі накладається картина в B-режимі.
В-режим зображення має важливе значення для анатомічного визначення структур. Крім того, лінійне відбиття від біопсійної голки або абляційного зонда, які використовуються при інвазивних процедурах, не можуть бути відображені тільки в контрастному режимі, що робить паралельну візуалізацію необхідною для інструментального наведення.
Програми для аналізу і кількісного підрахунку
Розроблено спеціальні програми для кількісного визначення перфузійних параметрів і з метою об’єктивної ідентифікації ФУП, шляхом синхронного аналізу зображень при скануванні або при післяпроцедурній оцінці. Більшість сучасних продуктів програмного забезпечення дозволяють отримати кінопетлю хорошої якості шляхом включення компенсації руху та/або дихання. Приклади комерційно доступних продуктів включають: SonoLiver (Tomtec Imaging Systems, Унтершлайсхайм, Німеччина), VueBox (Bracco Suisse SA-Software Applications, Женева Швейцарія) і QLAB (Philips, Ботелл, Вашингтон).
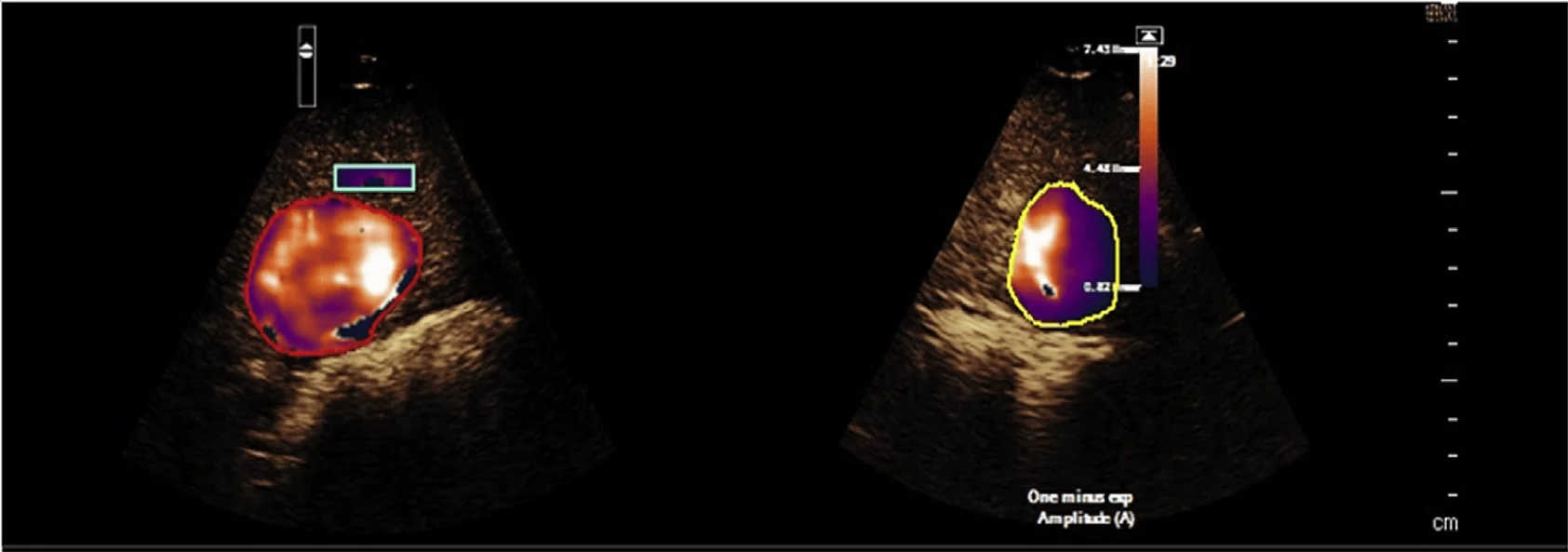
При використанні таких програм, картини посилення можуть бути кількісно оцінені у вигляді тимчасових кривих інтенсивності, шляхом вибору поля зору в межах ураження, що дозволяє проводити порівняння з сусідньою паренхімою печінки та інтервальний моніторинг спостереження за змінами перфузії. При включенні параметричного аналізу зображень, картина динамічного посилення ураження може бути об’єктивно візуалізована, що збільшує точність діагностики (Рис. 2).
Рис. 2. Параметрична візуалізація УКД. Динамічний судинний малюнок в межах ураження відображається в кольорі і може бути порівняний з доданою колірною шкалою.
ПОРЯДОК ДОСЛІДЖЕННЯ
Введення ультразвукових контрастних речовин
Мікропухирці повинні бути приготовлені відповідно до методичних рекомендацій виробника. УКР можуть бути введені в якості болюсної ін’єкції або безперервної інфузії.
Болюсне введення
Метод болюсного введення сприяє швидкому розподіленню мікробульбашок в судинному руслі печінки. Контрастні ін’єкції повинні бути виконані через запірний клапан і 20 калібру (або більше) канюлю в ліктьову вену, без додаткової трубки. УКР дається у вигляді болюса з наступним швидким введенням 0,9% фізіологічного розчину. Дозу слід розраховувати відповідно до керівництва виробників, щоб забезпечити рівномірний розподіл УКР і уникнути артефактів від надмірної кількості мікробульбашок. Болюсні ін’єкції можуть повторюватися, якщо це потрібно, як тільки раніше введені мікропухирці зникають. Це може бути досягнуто швидким тимчасовим збільшенням МІ, щоб сприяти руйнуванню мікробульбашок.
Інфузійні ін’єкції
До проведення інфузії, УКР, в першу чергу, готують перед розведенням фізіологічним розчином в шприці. Суспензія повинна бути ретельно збовтана для того, щоб забезпечити постійну форму мікробульбашок і їх рівномірний розподіл. Потім УКР вводять з постійною швидкістю через інфузомат. Як тільки досягається стійкий потік мікробульбашок (2-3 хвилини), можна визначати динамічні характеристики потоку за допомогою флеш візуалізації – техніка, при якій коротка серія із збільшеним акустичним тиском перекриває бульбашки в площині візуалізації. Мікропухирці потім накопичуються повторно, що дозволяє спостерігати за характеристиками посилення. Можуть знадобитися повторні серії для збільшення діагностичної точності. Необхідність в додатковому обладнанні і складна підготовка робить цей спосіб введення менш привабливим.
Візуалізація
До ін’єкції контрасту, повинна здійснюватися візуалізація з використанням звичайної сірошкальної і доплерографічної ультрасонографії для ідентифікації цільового ураження і оптимального позиціонування зображення.
Для подальшої візуалізації в контрастному режимі, до ін’єкції контрасту повинні бути скоректовані динамічний діапазон, глибина зображення, глибина вогнища, і локальний розмір зони. Секундомір використовується для відображення тривалості фаз посилення. Запис кінопетлі під час дослідження дозволяє провести ретроспективний покадровий огляд, оскільки зміни в посиленні в артеріальній фазі можуть протікати швидко.
У перші 2 хвилини дослідження (артеріальна і портовенозна фази), захоплення зображення повинно здійснюватися без перерви в одній площині. У пізній фазі виконується часте переривчасте сканування до тих пір, поки не зникнуть мікропухирці. Судинна фаза дослідження за допомогою УКР повинна тривати не менше 5-6 хвилин. При використанні Sonazoid, пізня фаза дослідження вважається менш важливою і, як правило, замінюється післяваскулярною фазою зображень, яка починається через 10 хвилин.
|
Поради для візуалізації
|
ЧАСТИНА 2
ОЦІНКА УЛЬТРАЗВУКОВИХ КОНТРАСТНИХ ЗАСОБІВ ДЛЯ НОВОУТВОРЕНЬ ПЕЧІНКИ
Характеристика ФУП
Точна характеристика уражень печінки може бути проблематичною. Один метод візуалізації часто призводить до непереконливих або сумнівних результатів, що вимагає подальшого дослідження за допомогою альтернативних технік. Характеристика ФУП є найпоширенішим застосуванням для УКД. Цей метод сприяє впевненій діагностиці, коли виявляються патогномонічні характеристики посилення. У Японії, УКД визнаний дослідженням першої лінії для діагностики гепатоцелюлярної карциноми (ГЦК).
До виконання УКД дослідження, повинні бути встановлені медичний анамнез пацієнта і фактори ризику злоякісної пухлини печінки. Будь які попередні дослідження печінки повинні бути розглянуті і проведено їх порівняння.
|
Номенклатура посилення Посилення вказує на перфузію і відсутність посилення означає аваскулярний статус. Інтенсивність посилення ФУП описується в порівнянні з інтенсивністю прилеглої тканини. |
|
ХАРАКТЕРНІ ДОБРОЯКІСНІ УРАЖЕННЯ
Гемангіома
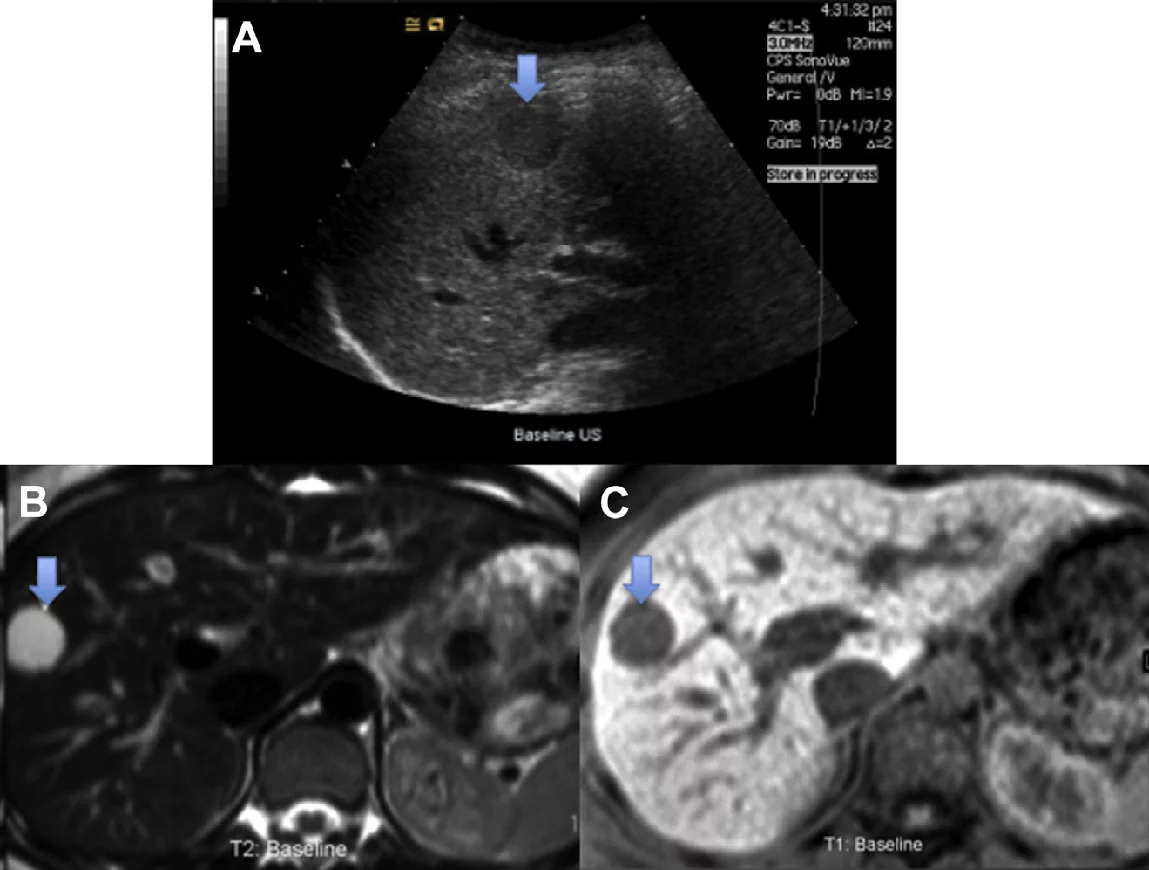
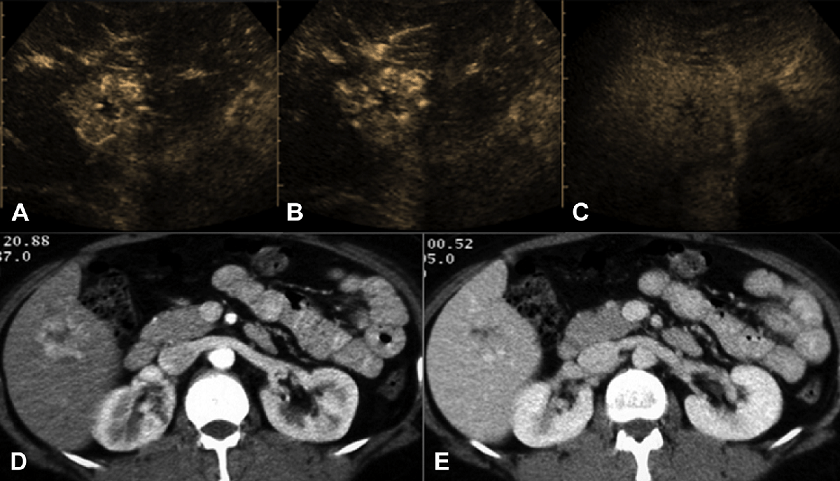
Гемангіоми є найбільш поширеними доброякісними новоутвореннями печінки. Вони є розростанням судинних ендотеліальних клітин і мають мезенхімальне походження. Як правило, гемангіома має периферійне вузлоподібне посилення в артеріальній фазі. Вона заповнюється повністю або частково в портовенозній фазі і показує ізопосилення по відношенню до паренхіми печінки в пізній стадії (рис. 3).
Рис. 3. Неуточнене тверде вузлове утворення в печінці (сині стрілки): (А) Ультрасонографія в В-режимі показує чітко окреслений, гіпоехогенний вузлик у 8-му сегменті; (B, C) Відповідне МРТ зображення одного і того ж ураження, Т2 гіперінтенсивне і T1 гіпоінтенсивне. УКД та МРТ з контрастним посиленням оцінка неуточненого вузлика: (D-F) УКД показує картину периферичного вузлового посилення в артеріальній фазі, з поступовим доцентровим наповненням у портовенозній фазі. Пізня фаза відображає постійне посилення; (G-I) МРТ з контрастним посиленням, показує аналогічні зміни у відповідних фазах. Дані результати на УКД та МРТ з контрастним посиленням характерні для гемангіом печінки.
Правильний діагноз досягається до 95%, коли візуалізуються типові особливості. Наповнення може бути швидким при невеликих ураженнях, і зображення в режимі реального часу дозволяє виявити блискавичне наповнення гемангіоми, яке може бути пропущено при КТ та MРТ.
Слід дотримуватися обережності, невелике і швидке посилення кровотоку при гемангіомі можуть бути помилково прийняті за високодиференційовану ГЦК, у той час, як не посилені тромбовані частини гемангіоми можуть бути помилково прийняті за вимивання.
|
Типова схема посилення
Увага
|
Фокальна вузлова гіперплазія
Фокальна вузлова гіперплазія (ФУГ) – доброякісне гіперпластичне ураження, яке розвивається у відповідь на існуючі артеріовенозні вади розвитку. Характерні особливості включають: судинний малюнок за типом «спиць колеса», живляча судина, наявність центрального рубця. Упевнений діагноз іноді може бути поставлений на основі доплерографії. Одна з трьох характерних особливостей може визначатися в 75% уражень, розміром більше, ніж 3 см, зменшення розміру ураження зменшує частоту до 30%.
Після ін’єкції УКР, ФУГ зазвичай мають картину швидкого посилення по типу «спиць колеса», до відцентрового і однорідного заповнення протягом артеріальної фази. Нерівномірне заповнення ураження визначається в 30% ФУГ. У портовенозній та пізній фазах ураження може залишатися з гіперпосиленням або стати ізопосиленим. У випадку, коли присутній центральний рубець, він не посилений або з гіпопосиленням (Рис. 4).
Рис. 4. ФУГ з центральним рубцем. (А-С) УКД показує артеріальне посилення ураження з центральним рубцем. Ураження стає ізопосиленим по відношенню до печінки в пізній фазі. Рубець залишається посиленим. (D, E) Ураження має схожі характеристики на КТ з контрастним підсиленням, з не посиленим центральним рубцем.
Зрідка, ФУГ ураження можуть повністю вимиватися, у більшість випадків після 75 секунд. У таких випадках, може бути поставлений помилковий діагноз злоякісного ураження, якщо відсутні характерні ознаки.
|
Типова схема посилення • Швидке артеріальне посилення по типу «спиць колеса» і відцентрове наповнення. • Залишається в стані гіпер- або ізопосилення в портовенозній та пізній фазах. • Центральний рубець (якщо він присутній) не посилений або з гіпопосиленням Увага • 30% ФУГ мають картину нерівномірного наповнення. • ФУГ рідко вимиваються. |
Гепатоцелюлярна аденома
Гепатоцелюлярні аденоми – рідкісні доброякісні ураження, пов’язані з надмірним рівнем естрогену. Вони розвиваються в основному у жінок дітородного віку і тісно пов’язані з оральним використанням таблетованих контрацептивів і анаболічних/андрогенних стероїдів. Їх розрив або злоякісне переродження можливі, тому хірургічне лікування рекомендується для гепатоцелюлярної аденоми розміром більше ніж 3 см. Артеріальна фаза дослідження демонструє периферичне гіперпосилення з наступним швидким доцентровим наповненням. Вони стають ізопосиленими в портовенозній і в пізній фазах. Іноді вони показують картину невеликого вимивання, що може привести до некоректної постановки діагнозу ГЦК. Хоча типові характеристики посилення гепатоцелюлярної аденоми не є патогномонічними, сімейний анамнез і історія хвороби пацієнта може допомогти для її ідентифікації.
|
Типова схема посилення • Швидке периферичне артеріальне посилення й доцентрове наповнення. • Ізопосилення в портовенозній і в пізній фазах. Увага
|
Кістозні ураження
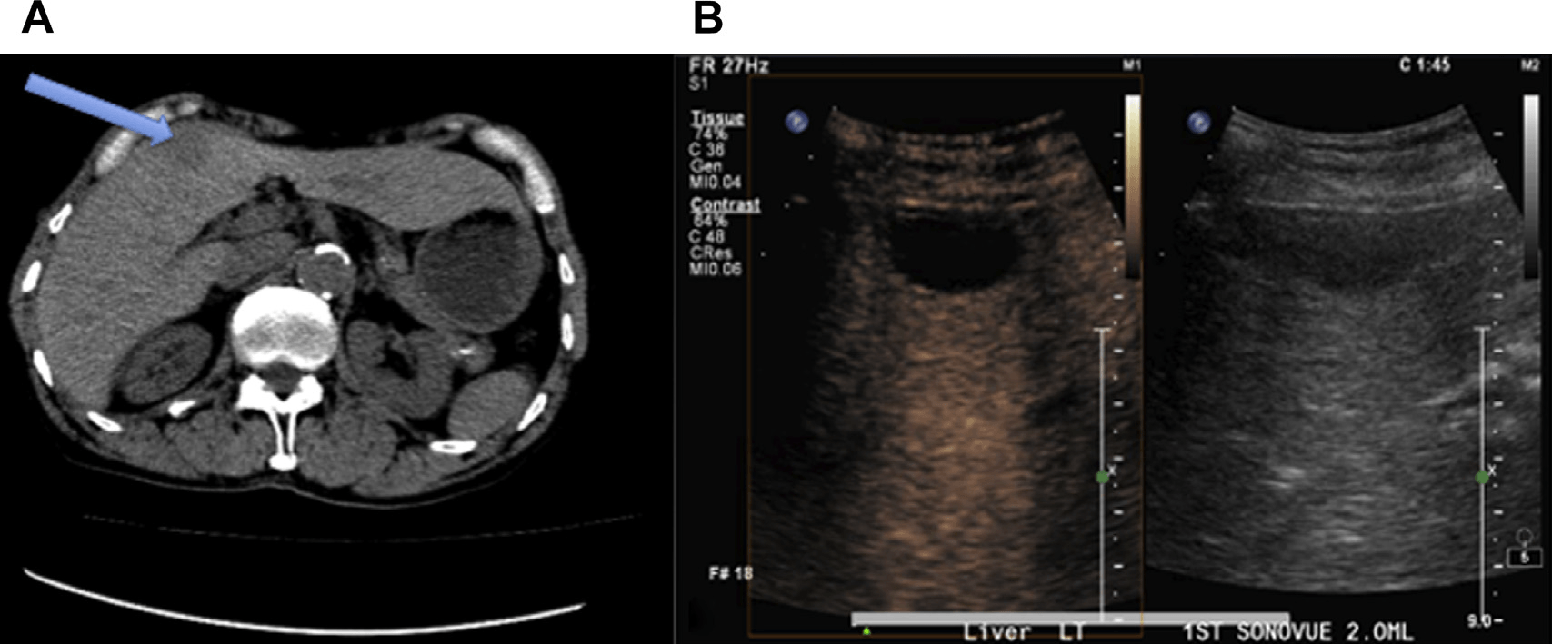
Прості кісти часто можуть бути ефективно діагностовані за допомогою звичайного ультразвукового дослідження, де вони проявляються як тонкостінні, чітко окреслені анехогенні пошкодження з дистальним акустичним посиленням. Клітинний дебріс або геморагічний компонент всередині кісти значно ускладнює диференціальну діагностику від твердого вузлика. УКД ефективна для оцінки складних кіст у зв’язку з відсутністю інтракістозного щільного посилення або посилення обідка вузла, що виключає злоякісне захворювання (рис. 5).
Рис. 5. Випадково виявлене субкапсулярне утворення низької щільності на КТ (синя стрілка). (А) Утворення низької щільності розташоване в сегменті 4, 50 одиниць виміру Хаунсфілда. Це наводить на думку про тверде ураження. Подальша оцінка не може бути проведена без додаткового контрастного КТ дослідження. (В) УКД виявляє кістозне ураження без посилення внутрікістозного папілярного компонента. Злегка посилений ехосигнал всередині ураження (визначається на паралельному зображенні в B-режимі) відноситься до клітинного дебрісу або білкововмісних компонентів.
Інфекція/запалення
Абсцеси печінки можуть мати ознаки артеріального посилення в межах їх стінок і перегородок, в результаті чого вони мають картину бджолиних сот. Якщо ознаки гіперпосилення очевидні, то, як правило, реєструється раннє вимивання протягом 30 секунд після ін’єкції контрасту. Відсутність посилення рідинних ділянок є найбільш характерною особливістю. Рідкісні запальні псевдопухлини мають варіабельну картину посилення на всіх етапах, без істотних відмітних особливостей при УКД.
Фокальні жирові зміни
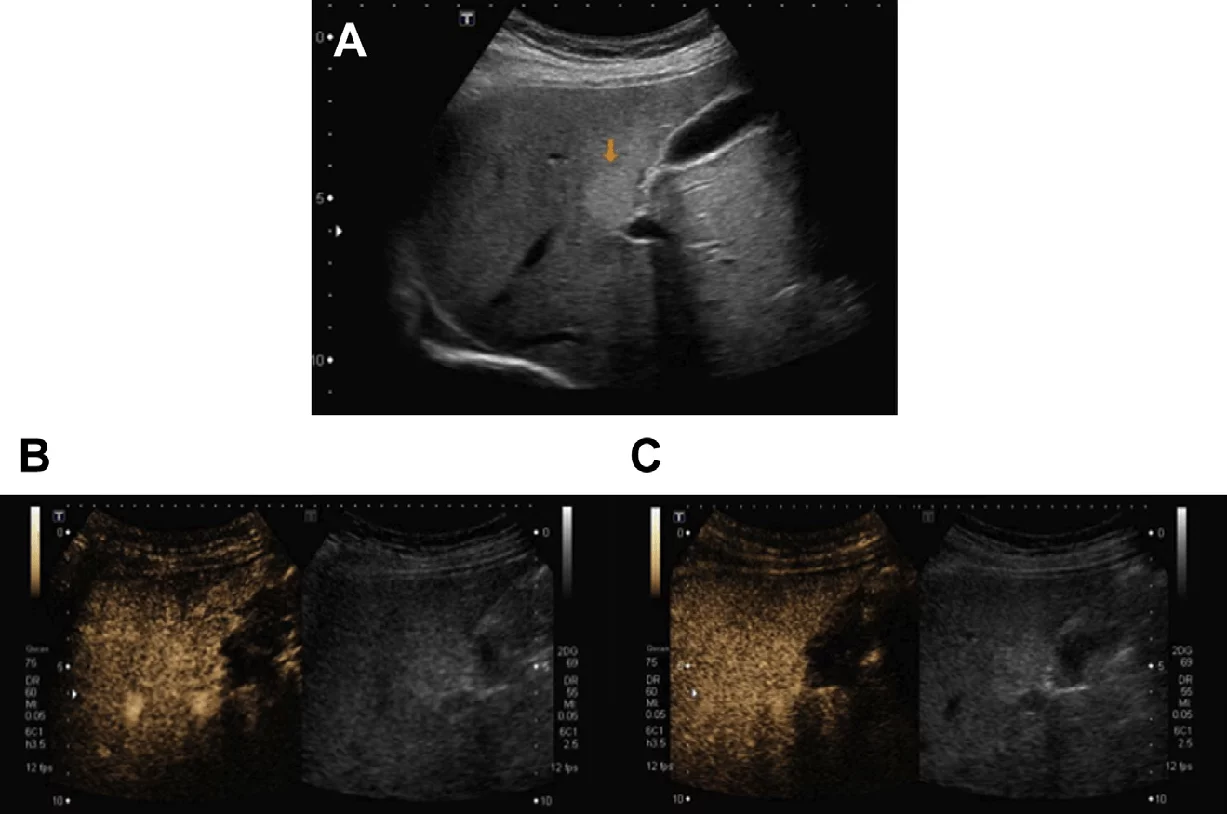
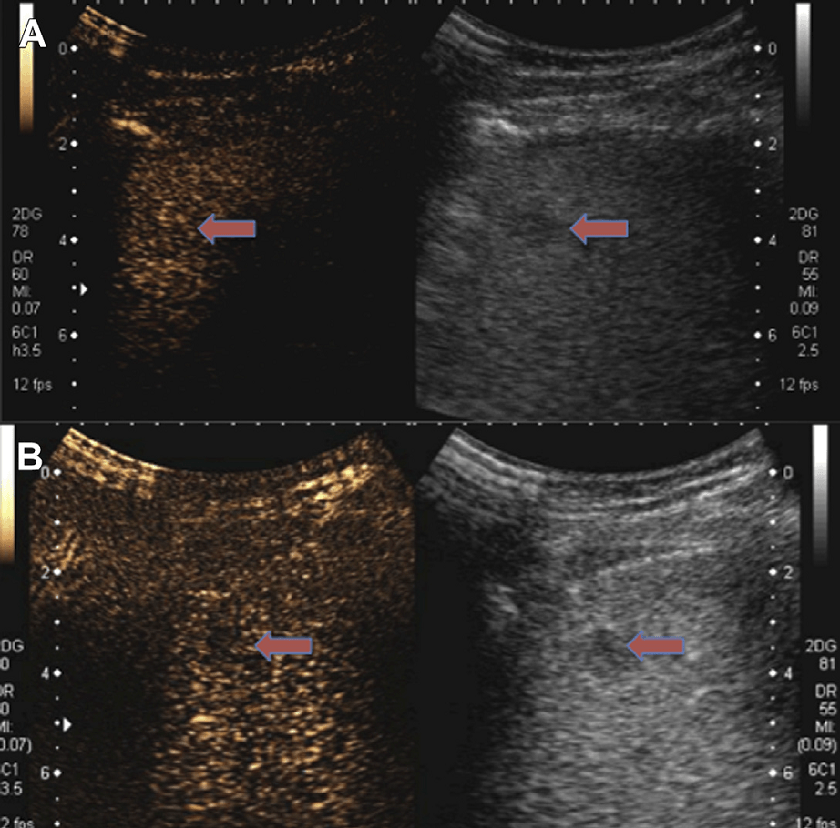
Фокальна жирова інфільтрація (ехогенна) і фокальне жирове переродження (гіпоехогенне), як правило, розвиваються навколо круглої зв’язки, поруч з ямкою жовчного міхура та прилеглих воріт печінки. Атипова локалізація може ускладнювати постановку діагнозу. Дуже важливим є диференціальна діагностика із злоякісними ураженнями у пацієнтів з високим ризиком. Зображення УКД відображають фокальні жирові зміни, як області з ізопосиленням, у порівнянні з навколишньою паренхімою печінки, у всіх судинних фазах (рис. 6).
Рис. 6. Фокальна жирова інфільтрація. (А) Зображення у В-режимі показує нечітку гіперехогенну область попереду від основної портальної вени (помаранчева стрілка). (B, C) Гіперехогенні області залишаються в стані ізопосилення по відношенню до печінки наприкінці артеріальної і портовенозної фаз при УКД.
ХАРАКТЕРНІ ЗЛОЯКІСНІ УРАЖЕННЯ
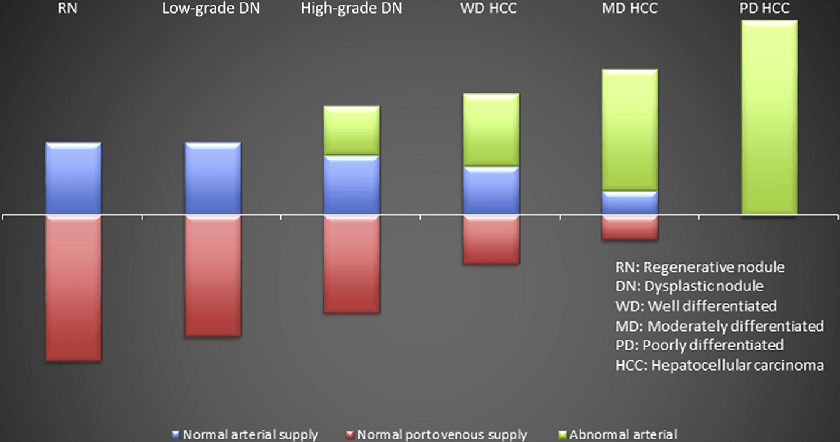
Цироз печінки є фактором розвитку ГЦК, при цьому 90% ГЦК мають поступове прогресування. Регенеративні вузлики, які формуються під час спроби печінки відновити циротичну тканину, мають подвійне кровопостачання, схоже на нормальну паренхіму печінки. Прогресування дисплазії вузлика призводить до втрати нормального артеріального і портовенозного кровопостачання. При подальшому розвитку ГЦК, вогнище ураження кровопостачаеться з аномальних непарних артерій, що призводить до чистої артеріалізаціі пухлини. Цей ангіогенез збільшується пропорційно прогресуванню пухлини до низькодиференційованої ГЦК (рис. 7).
Рис. 7. Патогенез ГЦК. Зміни в кровопостачанні при прогресуванні ураження від регенеративного вузлика до низькодиференційованої ГЦК. RN – регенеративний вузлик, DN – диспластичний вузлик, WD – добре диференційована, PD – погано диференційована, HCC – гепатоцелюлярна карцинома. Синій колір – нормальне артеріальне кровопостачання, червоний колір – нормальне портовенозне кровопостачання, зелений – ненормальне артеріальне кровопостачання.
Хоча ГЦК зазвичай розвивається на фоні цирозу печінки, вона також може розвиватися і в нормальній печінці. Деякі стани, такі як неалкогольна жирова патологія печінки, як відомо, сприяють канцерогенезу в печінці при відсутності цирозу.
Регенеративний вузлик
Типовий регенеративний вузлик, що показує ізопосилення у всіх фазах.
Диспластичний вузлик
Диспластичний вузлик – скупчення гепатоцитів, які містять диспластичні характеристики, але не відповідають гістологічним критеріям злоякісного процесу. Зі збільшенням дисплазії, інтранодулярні портальні тракти зникають і замінюються непарними артеріями залежно від ступеня дисплазії. Диспластичний вузлик може проявлятися гіпопосиленням, ізопосиленням або гіперпосиленням в артеріальній фазі, і переходить в стан ізопосилення або мінімального гіпопосилення, під час портовенозної та пізньої фаз. Диспластичні вузлики високого ступеня (ДВВС) можуть мати характеристики посилення, подібні до високодиференційованій ГЦК. У зв’язку з тим, що ДВВС вважаються передраковими захворюваннями, деякі центри виступають за їх резекцію або абляцію, ніж за динамічне спостереження.
|
Типова схема посилення • Регенераторні вузли мають посилення у всіх фазах. • Дегенеративні вузлики низького ступеня маю ізо- або гіпопосилення в артеріальній фазі і ізопосилення в порто венозній та пізній фазах. • Диспластичні вузлики високого ступеня можуть мати гіперпосилення в артеріальній фазі і невелике вимивання в пізній фазі. Увага
|
Гепатоцелюлярна карцинома
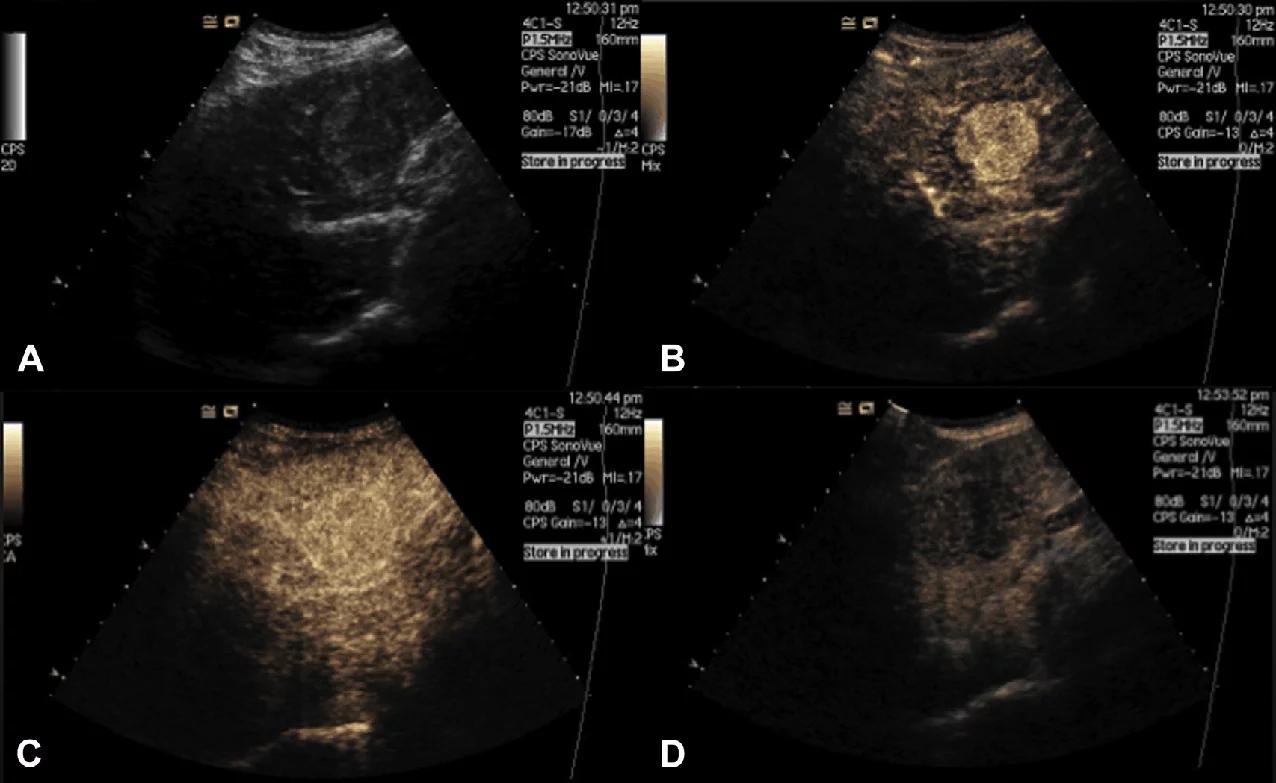
ГЦК має найбільш варіабельний шаблон посилення серед усіх злоякісних уражень. Класична картина посилення для ГЦК – артеріальне гіперпосилення з подальшим вимиванням в пізній фазі (рис. 8 і 9).
Рис. 8. Типовий зразок посилення ГЦК при УКД. (А) Практично ізоехогенне новоутворення на ультрасонограмі у В-режимі. (В) Новоутворення має однорідне гіперпосилення в артеріальній фазі. (С) Новоутворення показує практично ізопосилення по відношенню до печінки в портовенозній фазі. (D) Новоутворення характеризується вимиванням і гіпопосиленням по відношенню до печінки в пізній фазі.
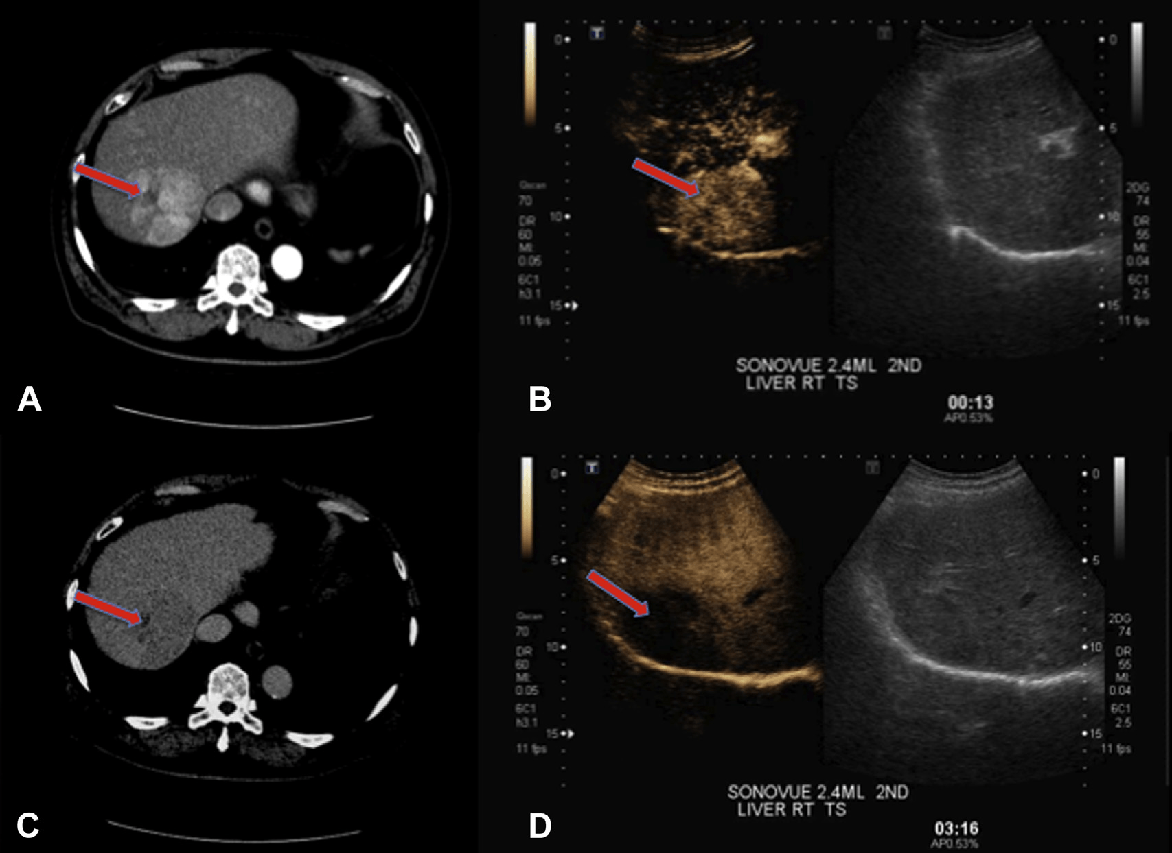
Рис. 9. Відповідні КТ і УКД зображення ГЦК (червоні стрілки). (A, B) КТ і УКД зображення новоутворення з артеріальним посиленням в 7-8 сегменті. (C, D) КТ і УКД зображення одного і того ж ураження, показують вимивання у відстроченій (пізній) фазі.
Практичні лікарі повинні знати, що ГЦК можуть мати ізопосилення або навіть гіпопосилення протягом артеріальної фази. ГЦК, як правило, має дисморфну, корзиноподібну картину артеріального кровопостачання з доцентровим наповненням. Живильна артерія і S-образні судини іноді чітко визначаються в межах або поблизу пухлини під час артеріальної фази. Гетерогенне посилення більш характерно для пухлин більшого розміру.
Тривалість вимивання ГЦК є змінною, хоча це відбувається зазвичай повільніше, порівняно з іншими злоякісними пухлинами. Розширена візуалізація необхідна до зникнення УКР в судинній фазі (5-6 хв) для того, щоб не упустити з виду ГЦК (рис. 10).
Рис. 10. Варіабельність пухлинного посилення ГЦК (червоні стрілки). (А) Пухлина, яка помірно гіпоехогенна на ультрасонограмі у В-режимі, має ізопосилення в артеріальній фазі. (B) Пухлина показує певне вимивання тільки з 3-4 хв, що свідчить про необхідність подовженого спостереження, принаймні, 5 хв.
Чим більш недиференційована пухлина, тим швидше вона вимивається. Sonazoid показує такі пошкодження, як посилені дефекти в післяваскулярній фазі.
Іноді ГЦК має артеріальне гіперпосилення без вимивання. Це можна побачити в високодиференційованих ГЦК, в яких залишилася значна кількість портальних трактів, при цьому вони і можуть бути помилково прийняті за доброякісну патологію. Індекс настороженості при артеріальному посиленні ураження, отже, повинен залишатися високим, особливо у пацієнтів на тлі цирозу печінки.
Портальний тромбоз, який не є рідкістю при цирозі печінки, підвищує рівень посилення в артеріальній фазі і зменшує посилення паренхіми печінки в портовенозній фазі. Це може зменшити невідповідність між дуже артеріалізованою ГЦК та прилеглою тканиною печінки, що ускладнює характеристику уражень.
|
Типова схема посилення
Увага
|
Холангіокарцинома
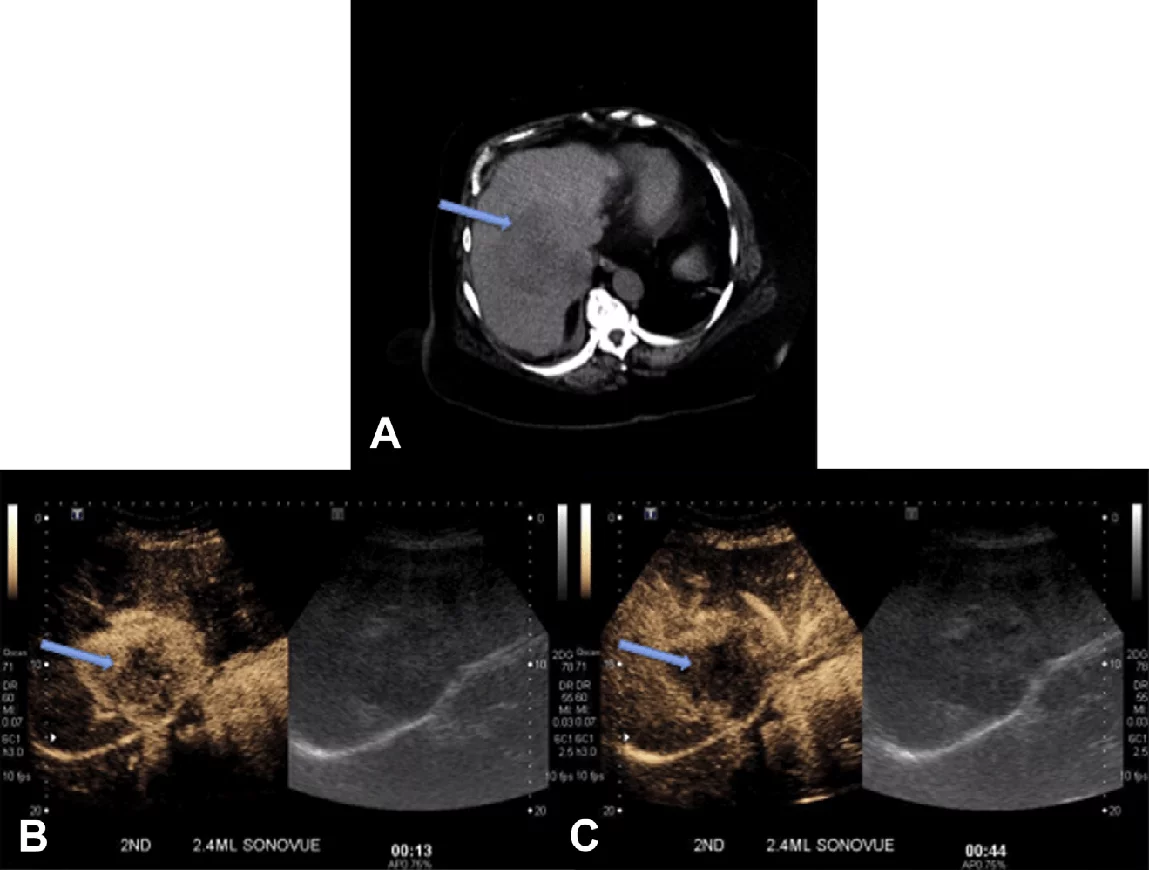
Більшість холангіокарціном в артеріальній фазі мають гіперпосилення через неоангіогенез. Існує чотири різних шаблони артеріального підсилення: периферійне посилення обідка, гетерогенне гіперпосилення, однорідне гіперпосилення і гетерогенне гіпопосилення. Пухлини з високою концентрацією ракових клітин виявляють підвищене артеріальне гіперпосилення, в той час як ураження з пропорційно великим вмістом фіброзної тканини посилюються менше. Картина периферичного посилення обідка частіше визначається в печінці без супутньої патології, у той час як гетерогенне гіперпосилення є більш характерним для хворих з цирозом печінки або хронічним гепатитом. Перідуктальна інфільтруюча внутрішньопечінкова холангіокарцинома, найчастіше, має гетерогенне посилення, яке зумовлене збільшенням кількості фіброзної тканини. Холангіокарціноми вимиваються в пізній фазі при УКД (рис. 11), але можуть характеризуватися уповільненням посилення при КТ з контрастуванням або МРТ з контрастуванням. Втягування поверхні печінки в пухлину, як наслідок фіброзної проліферації, є корисною радіологічною ознакою, яка повинна викликати підозру про наявність холангіокарціноми. Це легко визначити в В-режимі зображення. Холангіокарціноми також рано вимиваються, на відміну від низькодиференційованих ГЦК або метастазів.
Рис. 11. Неуточнене новоутворення печінки (сині стрілки). (А) КТ черевної порожнини без контрасту показує нечітке гетерогенне новоутворення у 8 сегменті. (В) УКД показує артеріальне посилення гетерогенного новоутворення. (C) Ураження швидко вимивається на початку портовенозної фази. Біопсія ураження показує холангіокарциному.
|
Типова схема посилення
Увага
|
Метастази
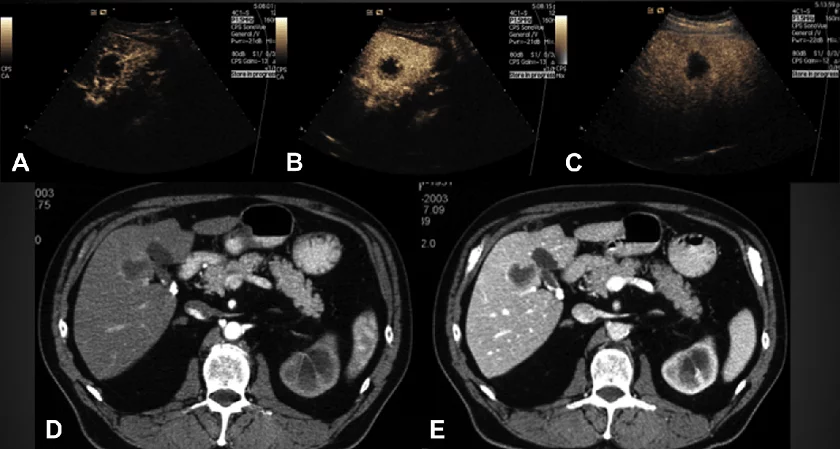
Метастази зазвичай відображаються при УКД з артеріальним гіперпосиленням, тому що пухлина містить більше артеріальних судин, ніж навколишня паренхіма печінки. Швидкий ріст метастазів найчастіше характеризується кільцеподібним посиленням або у вигляді ореолу, що пов’язано з наявністю периферичних артеріальних судин і некротичного ядра зі зменшеним судинним потоком (рис. 12). Метастатичні ураження вимиваються досить рано і залишаються з гіпопосиленням, починаючи з кінця артеріальної або з початку портовенозної фази. Деякі метастази проявляються гіпопосиленням протягом всієї судинної фази, і це частіше зустрічається при первинному раку ободової і прямої кишки і бронхогенному раку.
Рис. 12. Посилення обідка метастазів печінки. (А-С) УКД метастазів печінки показує посилення обідка в артеріальній фазі, з вимиванням в порто венозній і пізній фазах. Центральна частина, яка складається з некротичної тканини, що не посилена. (D, E) Відповідна КТ з контрастуванням тих же метастазів печінки в артеріальній і портовенозній фазах.
Метастази можуть імітувати низькодиференційовану ГЦК або холангіокарціному при УКД. Ключові моменти, які допомагають диференціювати метастази включають: історію хвороби пацієнта, наявність цирозу (підвищена ймовірність ГЦК) і множинні ураження (підвищена ймовірність метастазів).
|
Типова схема посилення
Увага
|
Лімфома
Первинна лімфома печінки зустрічається досить рідко. Більшість випадків розвиваються у пацієнтів з ослабленим імунітетом, особливо, у чоловіків в 50 років. Існує невелика кількість опублікованих даних про моделі посилення печінкової лімфоми. Як повідомляється, характеристики посилення є типовими для злоякісних уражень, з гіперпосиленням протягом артеріальної фази і вимиванням в пізній фазі.
Виявлення уражень
УКД допомагає збільшити чутливість у виявленні уражень печінки, оскільки воно здатне виявляти малі пухлини до 3 мм. УКД виявлення малих метастазів печінки також перевершує динамічну КТ при правильно виконаному дослідженні. Таким чином, керуючі принципи організацій WFUMB-ESFUMB рекомендують використання УКД в якості тесту, що виключає малі метастази і абсцеси.
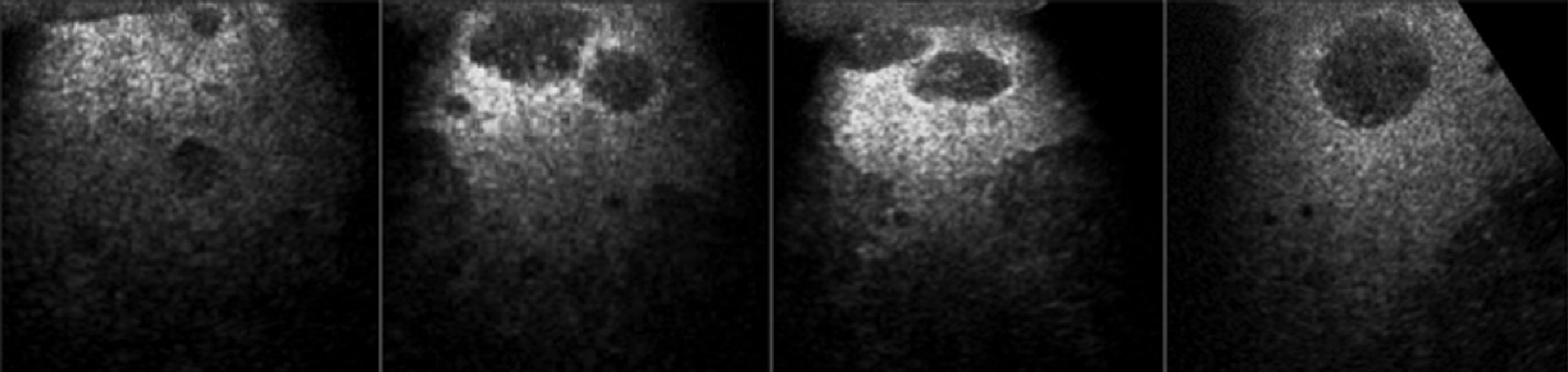
Речовини з післяваскулярною фазою (Sonazoid), особливо корисні для цієї мети, враховуючи те, що злоякісні ураження, як правило, позбавлені купферівских клітин (рис. 13).
Рис. 13. Виявлення метастазів у печінці. Контраст Sonazoid в післяваскулярній фазі. Метастази печінки краще візуалізуються у вигляді дефектів посилення.
До половини всіх високодиференційованих ГЦК мають ознаки вимивання, однак, і безсудинні ураження (наприклад, кісти) можуть бути помилково прийняті за дефекти посилення. Таким чином, додаткові ін’єкції болюса Sonazoid показані для повторної візуалізації в артеріальній фазі всіх виявлених уражень.
Інтраопераційна контрастна ультрасонографія
Інтраопераційна ультразвукова сонографія (ІО-УЗ) використовується для того, щоб допомогти хірургу прийняти рішення під час резекції печінки шляхом виявлення ФУП. Додавання УКР (ІО-УКД), як було показано, є більш чутливим методом, ніж КТ з контрастуванням, МРТ з контрастуванням і ІО-УЗ, для виявлення та характеристики уражень. ІО-УКД може змінити обсяг хірургічного втручання від 25% до 30% випадків. Це призводить до більш високої частоти ефективних лікувальних процедур, меншій частоті резидуальних пухлинних країв і збільшенню частоти органозберігаючих операцій. Для виконання ІО-УКД рекомендується застосування спеціальних високочастотних інтраопераційних датчиків. Тривалість контрастного підсилення коротше при ІО-УКД, бо мікропухирці руйнуються швидше, через близькість датчика до печінки.
УКД при абляційній терапії
УКД покращує можливість адекватного розміщення датчика, більш чітко зображуючи пухлини меншого розміру і підвищуючи контрастну роздільну здатність між периферичною зоною ураження і навколишніми тканинами. Дослідження показали, що додавання УКР для ультразвукового наведення при проведенні втручань, призводить до поліпшення результатів аблятивних процедур в порівнянні з ультрасонографією без контрастування. УКД особливо ефективно тоді, коли КТ з контрастуванням, МРТ з контрастуванням або стандартна сонографія не можуть чітко візуалізувати зону ураження.
Періпроцедурне УКД показало співставні результати в порівнянні з КТ з контрастуванням, при виявленні протягом 24 годин резидуальної пухлинної тканини і визначення успіху лікування. Залишкові ураження, які визначаються відразу після абляційного лікування, можуть бути негайно усунені, виключаючи необхідність повторного знеболювання і збільшення термінів перебування в лікарні. УКД повинно бути виконано приблизно через 5 хвилин після абляції, для забезпечення відводу газу, який утворюється під час процедури (рис. 14).
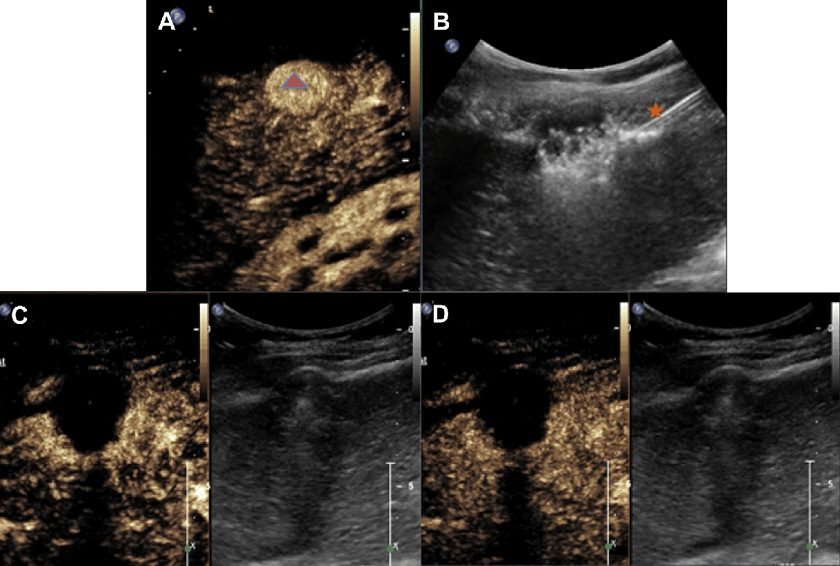
Рис. 14. УКД при абляційній терапії. (А) Преабляційна УКД підтверджує присутність артеріального посилення ГЦК (помаранчевий трикутник). (В) Зображення ураження у В-режимі, отримане в ході радіочастотної абляції. Зверніть увагу на наявність абляційної голки (помаранчева зірка). Наявність газу (артефактів «кільце, звернене вниз» з тінню) ускладнює оцінку цього ураження відразу після терапії. (С, D) Післяабляційне УКД показує гладкий, злегка гіперемований обідок. Це не повинно бути помилково прийнято за залишкову пухлину. Післяабляційна зона не посилюється в портовенозній пізній фазі.
Післяабляційний моніторинг за допомогою УКД також корисний для виявлення локальних рецидивів. Рентгенолог повинен мати на увазі збереження посилення гіперваскуляризованого обідка, який часто визначається протягом місяця після лікування, і це не повинно бути помилково прийнято за рецидив пухлини.
Обмеження
УКД страждає від тих же обмежень, як і стандартна ультрасонографія, тому погана якість сканування без контрастування навряд чи забезпечить гарну якість УКД зображення. Піддіафрагмальні ураження можуть бути складними для виявлення і їх характеристики. Крім того, проблематичним є зображення глибоких уражень, особливо у пацієнтів, які страждають ожирінням або які мають серйозну жирову дистрофію печінки або цироз. Практикуючі лікарі повинні знати, що ультразвукові хвилі послаблюються мікробульбашками, і це явище відоме як самозатінення. Це є важливим тому, що надмірно висока доза мікробульбашок обмежує проникнення. Крім того, коли ультразвукові хвилі поширюються через мікропухирці, вони змінюються і вносять свій внесок у формування нелінійного ехосигналу (нелінійне поширення), що призводить до появи артефактів у дальньому полі.
Хоча найменше ураження, що визначається при УКД – від 3 до 5 мм, діагностичний довірчий інтервал збільшується при розмірі ураження більше 1 см. Це не є несподіваним, тому що чим менше ураженння, тим важче оцінити його шаблон посилення.
Підводні камені
Важливо пам’ятати про можливе перекриття шаблонів посилення доброякісних і злоякісних уражень. Bhayana та ін. повідомляють про 97% ракових пухлин, у яких визначалося вимивання і цей факт має позитивну прогностичну цінність в 72%. Хоча вимивання контрасту є ключовим елементом для диференціальної діагностики доброякісних і злоякісних уражень, приблизно 30% доброякісних уражень мають ознаку вимивання, в той час як деякі ГЦК його не мають.
Можливість диференціювати пухлини значно складніший процес, зі специфічністю тільки 64%. Класичне артеріальне гіперпосилення з подальшим вимиванням визначається не тільки при ГЦК, але також і при холангіокарціномі, лімфомі і метастазах.
ГЦК на сьогоднішній день є найбільш поширеною злоякісною пухлиною, яка в більшості випадків характеризується повільним вимиванням. У сумнівних випадках рекомендується додаткове проведення КТ з контрастуванням або МРТ з контрастуванням. Для гістологічної кореляції рекомендується біопсія, у разі якщо діагноз залишається сумнівним.
ЧАСТИНА 3:
ПЕРСПЕКТИВИ
Кількісне визначення перфузії пухлини
Вивчення критеріїв реакції солідних пухлин є сучасним стандартом, використовуваним для оцінки відповіді на лікування раку печінки. Однак, вони призначені для вимірювання зменшення об’ємів пухлин після цитостатичної терапії, обмежуючи їх ефективність оцінкою реакції на цитостатичні препарати. Як чисто внутрішньосудинні речовини, мікропухирці ідеально підходять для кількісного виміру перфузії. Динамічне УКД є потенційним біомаркером для оцінки відповіді на лікування, особливо для антиангіогенних речовин.
3-D і 4-D дослідження з мікробульбашками
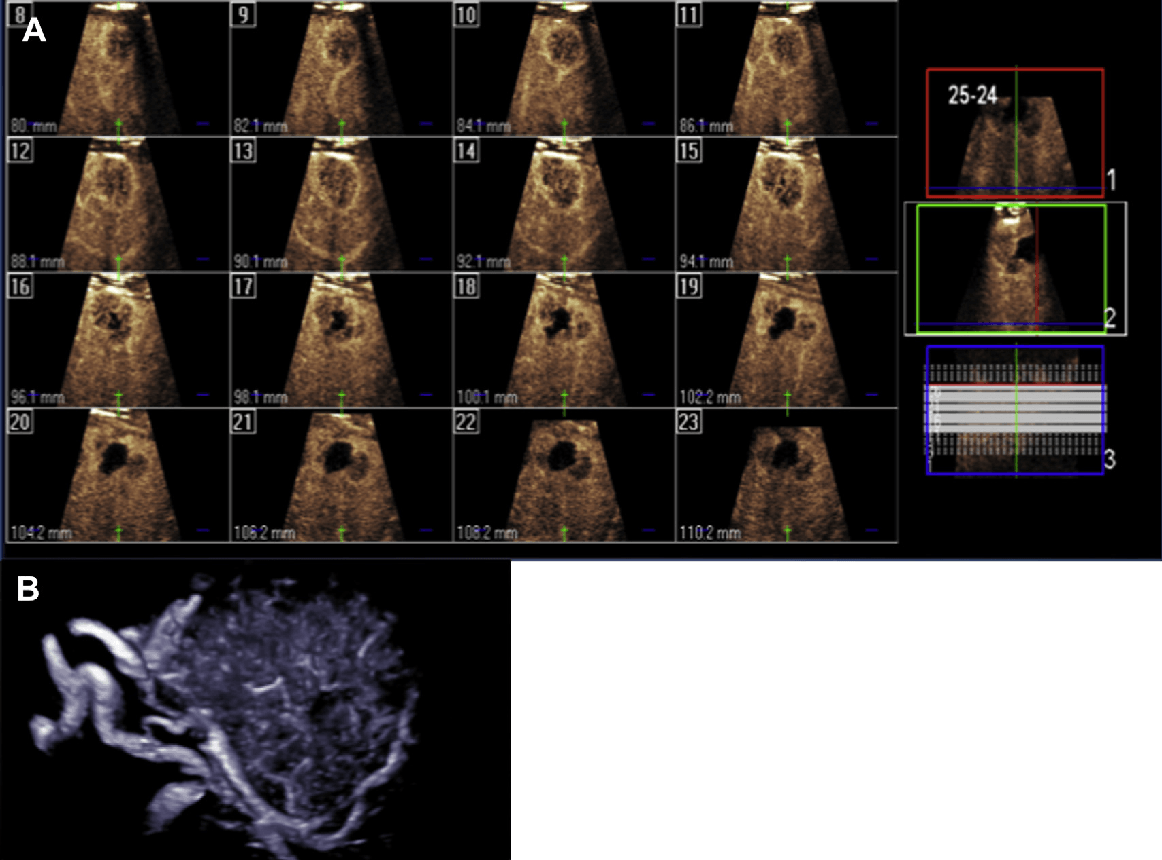
3-D візуалізація дозволяє провести більш якісну оцінку морфології та об’єму всієї пухлини, тоді як 4-D візуалізація дозволяє оцінити 3-D зображення в режимі реального часу. Одночасне використання багатозрізового пакету програмного забезпечення, який відображає отриману 3-D картину у вигляді послідовних зображень, що дозволяє ефективно виявляти невеликі ураження (Рис. 15).
Рис. 15. 3D ультрасонографія. (А) Формування 3D зображення накладенням мультизрізів при дослідженні всієї післяабляційної зони. При цьому об’єм (щільної) рецидивної пухлини може бути оцінений краще. (B) 3-D візуалізація ФУГ показує її центральну артерію і відгалуження гілок.
3-D візуалізація в режимі реального часу може також поліпшити визначення характеристик васкуляризації ФУП.
Таргетна (прицільна) візуалізація
Мікропухирці, покриті поверхневими антигенами, націлені на конкретні клітинні рецептори, перебувають у стадії розробки. Їх цілі включають: фактор росту ендотелію судин 2 і avb3 інтегрин. Ці розробки можуть виявитися цінним у виявленні уражень і їх диференціальної діагностики. Це також може допомогти полегшити планування лікування шляхом виявлення клітинних поверхневих мутацій, які сприйнятливі або непроникні для певних режимів лікування.
РЕЗЮМЕ
УКД – цінний діагностичний інструмент, який є економічно ефективним, безпечним і не володіє іонізуючим випромінюванням. Його застосування в режимі реального часу і використання чисто внутрішньосудинних контрастних речовин – унікальні особливості, яких немає в інших методів візуалізації. Безперервні технологічні досягнення і поліпшення методів контрастування необхідні для того, щоб твердо встановити роль УКД при візуалізації печінки. Для проведення досліджень рекомендуємо використовувати апарат від компании GE Voluson E8.
Часті питання та відповіді (FAQ)
Що таке контрастне ультразвукове дослідження (УКД) печінки?
- Контрастне ультразвукове дослідження (УКД) – це метод візуалізації, який використовує ультразвукові хвилі та спеціальну контрастну речовину для покращення візуалізації фокальних уражень печінки (ФУП), таких як пухлини.
Які переваги УКД перед традиційною ультрасонографією?
- УКД дозволяє краще диференціювати ФУП від навколишньої тканини печінки завдяки контрастуванню.
- УКД надає детальнішу інформацію про кровопостачання ураження.
- УКД підвищує точність діагностики та зменшує потребу в додаткових дослідженнях.
Які фази посилення спостерігаються під час УКД печінки?
- Артеріальна фаза (10-20 сек після ін’єкції).
- Портовенозна фаза (30-45 сек).
- Пізня фаза (>120 сек).
- Постваскулярна фаза (для Sonazoid, через 10 хв).
Які існують типи ультразвукових контрастних речовин (УКР)?
- SonoVue, Sonazoid, Definity/Luminity, Optison, Levovist (деякі з них мають обмежену доступність).
Чи є побічні ефекти від використання УКР?
- Побічні ефекти зазвичай незначні та тимчасові (запаморочення, нудота, свербіж).
- Протипоказання включають алергію на компоненти УКР та деякі серцево-судинні захворювання.
Як готуватися до контрастного ультразвукового дослідження печінки?
- Необхідно проконсультуватися з лікарем щодо можливих протипоказань та підготовки до процедури.
Яка точність діагностики за допомогою УКД?
- Точність УКД при диференціальній діагностиці ФУП становить від 92% до 95% за даними літератури.