🤖 Короткий переказ від ШІ
УЗД з контрастуванням (CEUS) за допомогою SonoVue стає все більш важливим методом для діагностики вогнищевих уражень печінки (ВУП), особливо враховуючи зростання випадково виявлених уражень завдяки поширеності УЗД. Цей метод пропонує безпечну, неінвазивну та економічно ефективну альтернативу традиційним методам візуалізації.
CEUS дозволяє точно диференціювати доброякісні та злоякісні ураження, оцінювати ефективність аблятивного лікування та моніторити рецидиви. Його переваги включають динамічну візуалізацію мікроциркуляції, можливість застосування у пацієнтів з нирковою недостатністю та порівнянну з КТ/МРТ точність. Завдяки цим властивостям, CEUS може значно покращити діагностичний процес та зменшити витрати на дослідження, а також доступний широкий вибір УЗД апаратів для його проведення.
✅ Ключові тези зі статті:
- Діагностика: CEUS з SonoVue ефективно характеризує вогнищеві ураження печінки, відрізняючи доброякісні від злоякісних за типом посилення та вимивання контрасту.
- Лікування: Метод застосовується для моніторингу після аблятивного лікування, дозволяючи оцінити ефективність та виявити залишковий життєздатний матеріал.
- Переваги: SonoVue безпечний, неінвазивний, економічно вигідний, не використовує іонізуючого випромінювання та може використовуватися при протипоказаннях до КТ/МРТ.
- Обмеження: Обмежене поле зору та залежність від досвіду оператора є основними недоліками CEUS.
Останнє оновлення: 22 липня 2025 р.
Експертна перевірка: Матеріал перевірено та відредаговано експертами RH.ua
Примітка про ШІ: Цей блок створено за допомогою генеративного ШІ для швидкого ознайомлення з основними ідеями статті. Для повного розуміння теми рекомендуємо прочитати повний текст.
⚠️ Не замінює медичну консультацію
Автори: Giovanna Ferraioli, Maria Franca Meloni
Вступ
Завдяки широкому використанню УЗД як методу візуалізації, завдяки його неінвазивності і відносно низькій вартості, частота випадково виявлених вогнищевих уражень печінки збільшилася. У здорових людей без факторів ризику і пацієнтів з безсимптомним перебігом хвороб ці ураження зазвичай доброякісні; отже, вкрай важливо прийти до точного діагнозу таким чином, щоб уникнути більш дорогих досліджень, які не вільні від ризиків.
Проте, раннє виявлення та характеристика первинного і метастатичного раку печінки можуть дозволити більш ефективне лікування, тим самим покращуючи виживання пацієнтів.
Трохи ультразвукових контрастних агентів є на ринку для проведення досліджень CEUS. В Європі використовується SonoVue (Bracco Imaging, Мілан, Італія). На відміну від контрастного середовища комп’ютерної томографії (КТ) або магнітно-резонансної (МРТ), SonoVue є чисто внутрішньосудинним агентом, без міжсудинної фази, що дозволяє динамічно визначати мікроциркуляцію.
SonoVue складається з мікропухирців (2-10 мкм) з оболонкою з фосфоліпідів, заповнених газом гексафториду сірки. Контрастний агент, який утримується в судинах після ін’єкції, має високу відбивну здатність і низьким механічним індексом і дозволяє візуалізувати крихітні судини в капілярному шарі, тим самим забезпечуючи динамічне виявлення капілярної мікроваскулярізаціі.
Контрастна речовина не виводиться нирками, і тому його можна застосовувати у пацієнтів з порушеною функцією нирок, яким протипоказано посилене контрастування КТ або посилене контрастування MРТ. Безпека SonoVue була ретроспективно оцінена в серії з 23 188 досліджень, проведених на дорослих суб’єктах: ніяких летальних випадків не було, а загальна частота серйозних небажаних явищ склала 0,0086%.
Печінка має подвійне кровопостачання з воротної вени і печінкової артерії, що призводить до появи трьох контрастних судинних фаз при УЗД: артеріальна фаза, яка починається через 20 секунд після ін’єкції і триває протягом 30-45 секунд, після чого слідує портальна венозна фаза, яка закінчується через 120 секунд, а потім пізня фаза, яка триває до виведення контрастної речовини з кровообігу (зазвичай 6 хвилин).
Спеціальне програмне забезпечення для перфузії також дозволяє вимірювати параметри, засновані на обсязі крові, і параметри, засновані на швидкості потоку.
Діагностика вогнищевих уражень печінки
SonoVue – це вид ультразвукового контрасту, який широко використовується в Європі і деяких частинах Азії для характеристики вогнищевих уражень печінки (ВУП) протягом майже 15 років, і його ефективність оцінювалася в численних дослідженнях.
Стале посилення в портальній венозній і пізній фазах без ознак вимивання, як правило, спостерігається майже у всіх твердих доброякісних ураженнях печінки, тоді як гіпопосилення в пізніх фазах, сопутніх вимиванню, є ключовим виявленням злоякісних новоутворень (Зобр. 1, 2).
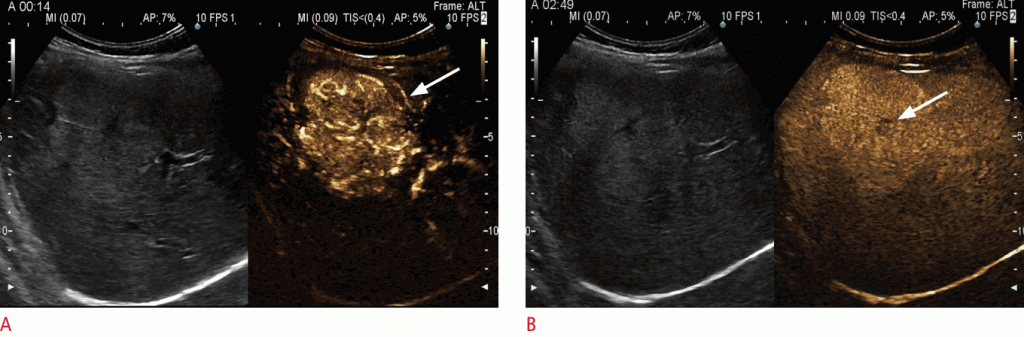
A. Випадкове осередкове ураження печінки розміром 4,8 × 5,1 см в сегменті 5 показує вид спицевого колеса (стрілка) після ін’єкції SonoVue. На ранній артеріальній фазі спостерігалося посилення відцентрової сили. B. В пізній фазі ураження демонструє стійке посилення за винятком центрального рубця (стрілка).
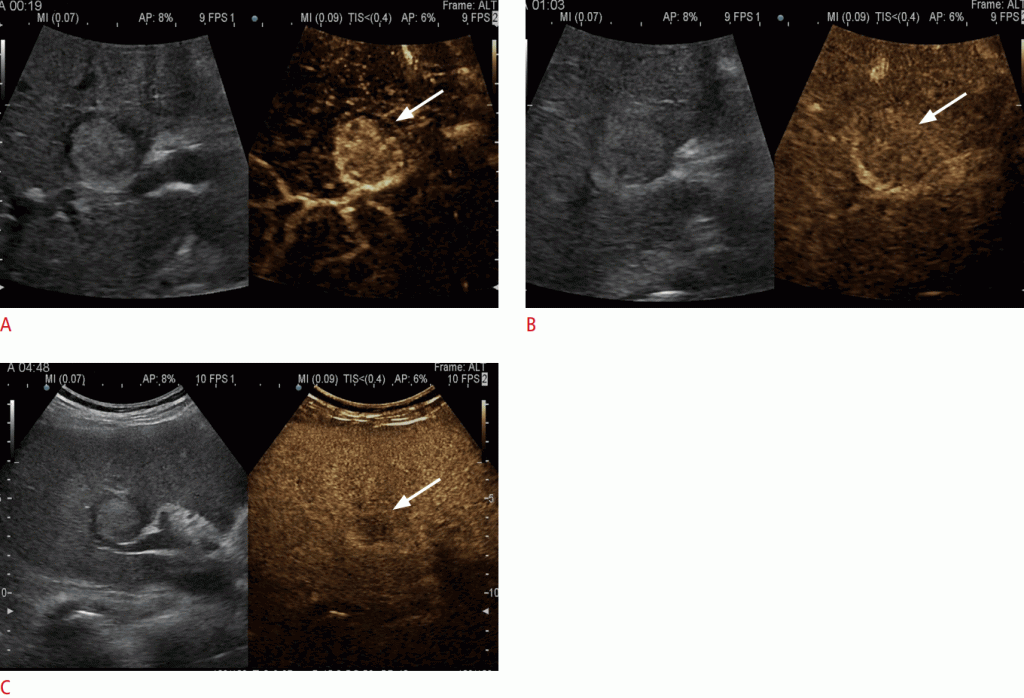
A. Під час спостереження в 5-м сегменті був виявлений вузлик розміром 2,5 см. У ранній артеріальній фазі ураження стає гіперпосиленним (стрілка) по відношенню до навколишньої паренхіми печінки. Вузлик ізопосиленний (стрілка) в портальній венозній фазі. C. Вузлики показали повільне і м’яке вимивання і стають гіпоехогенними (стрілка) в пізній фазі.
Багатоцентрові випробування показали, що ефективність CEUS для характеристики ВУП аналогічна кКТ або кМРТ. Мета-аналіз, що включає 8 147 тварин, показав, що загальна чутливість і специфічність CEUS для діагностики злоякісних уражень печінки склали 93% (95% довірчий інтервал [ДІ], 91-95) і 90% (95% ДІ, 88-92) відповідно. Мета-аналіз включав 45 досліджень, 35 (77,8%) були виконані з SonoVue, а решта 10 з іншими контрастними речовинами.
Вествуд і співавтори провели дослідження на замовлення міністра охорони здоров’я Великобританії, порівнюючи клінічну ефективність і економічну ефективність CEUS з використанням SonoVue з результатами кКТ і кМРТ для оцінки дорослих з ВУП, у яких попередні дослідження печінки були непереконливими. Автори повідомили, що CEUS може забезпечити діагностичну ефективність, аналогічну іншим методам візуалізації. Економічний аналіз показав, що CEUS є економічно ефективною заміною кКТ і кМРТ при характеристиці вузлів, виявлених під час епіднагляду за пацієнтами з цирозом, і для характеристики випадково виявлених ВУП, з аналогічними витратами і ефектами для виявлення метастазів в печінці при колоректальному раку.
Дослідження, в якому брали участь три центри та 485 суб’єктів з 575 випадково виявленими ВУП, повідомило, що CEUS правильно диференціював (доброякісні та злоякісні) 559 з 575 уражень (97,2%), з чутливістю 98,1% і специфічністю 95,7% , і заощадив 175,39 євро на пацієнта.
CEUS – це метод динамічної візуалізації в реальному часі, який можна використовувати, коли кКТ і кМРТ не показані або протипоказані. Фактично, цей безперервний спосіб візуалізації в реальному часі може дозволити виявити тимчасове посилення ураження, яке може бути пропущено іншими способами візуалізації.
У ретроспективному дослідженні, проведеному на 282 пацієнтах з цирозом і 34 доброякісними і 248 гістологічно підтвердженими злоякісними ВУП, час вимивання> 55 секунд виявило пацієнтів з ГЦК з найвищим рівнем точності (92,7%), тоді як час вимивання ≤55 секунд правильно ідентифікувало переважну більшість злоякісних новоутворень без ГЦК (чутливість 100%, специфічність 98,2%, діагностична точність 98,3%).
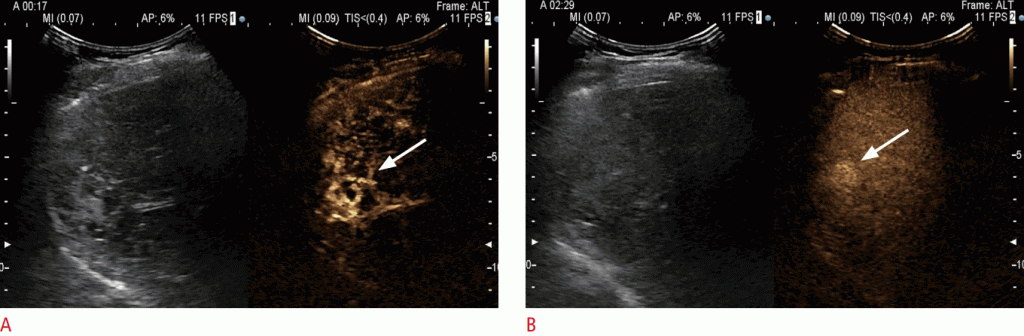
А. При УЗД з контрастним посиленням вузлик показує глобулярне посилення (стрілка) в артеріальній фазі. Ця особливість була типовою для гемангіоми. B. В пізній фазі весь вузлик є гіпер-посиленим (стрілка) по відношенню до сусідньої паренхімі печінки. Він був класифікований як LR-1 (безумовно доброякісне ураження).
Зображення 4: 64-річний чоловік з хронічним гепатитом С.
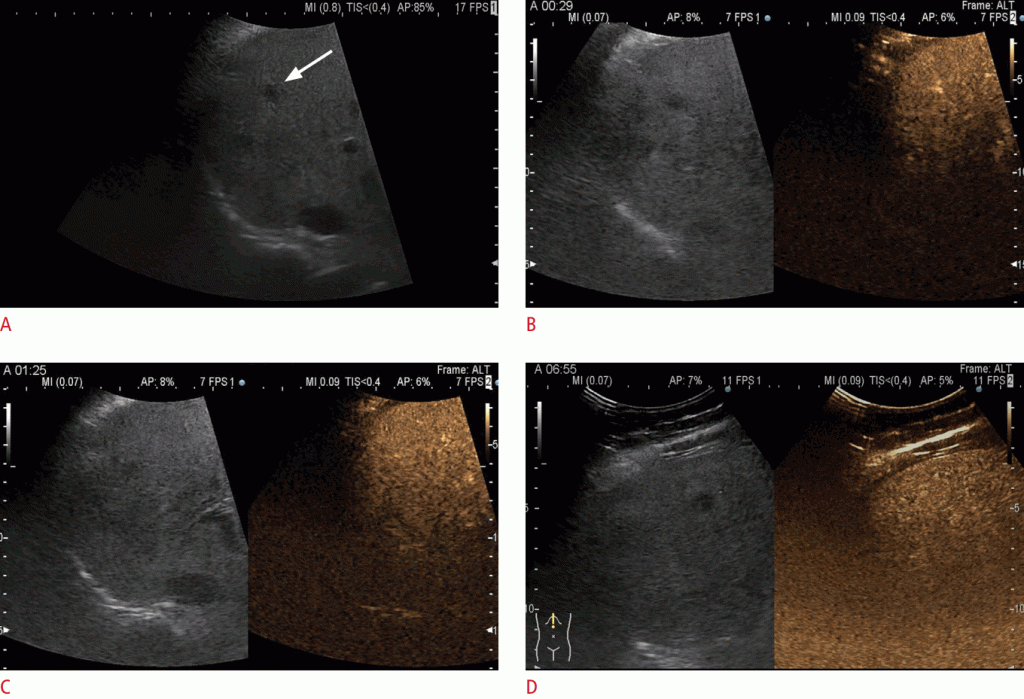
A. Гіпоехогенний вузлик 9 мм (стрілка) видно в 5 сегменті печінки. B. У артеріальної фазі вузлик показує посилення, схоже на навколишню паренхіму печінки. C. У портальній венозній фазі немає вимивання контрастної речовини, відмінного від фонової паренхіми. D. На пізній стадії вузлик виглядає ізопосиленним. Він був класифікований як LR-2 (ймовірно, доброякісний).
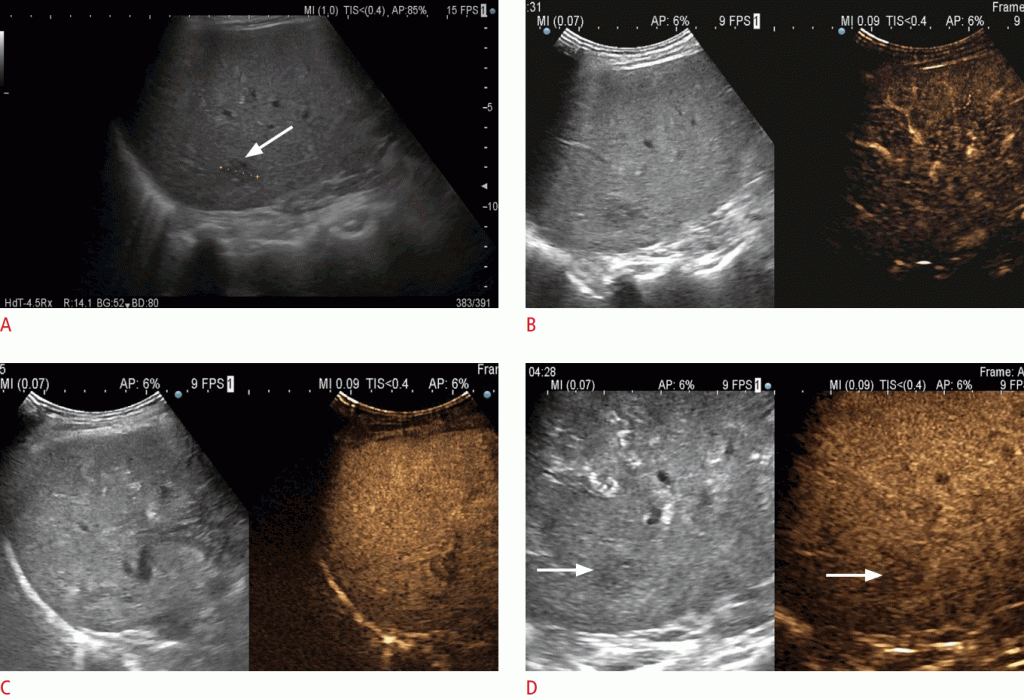
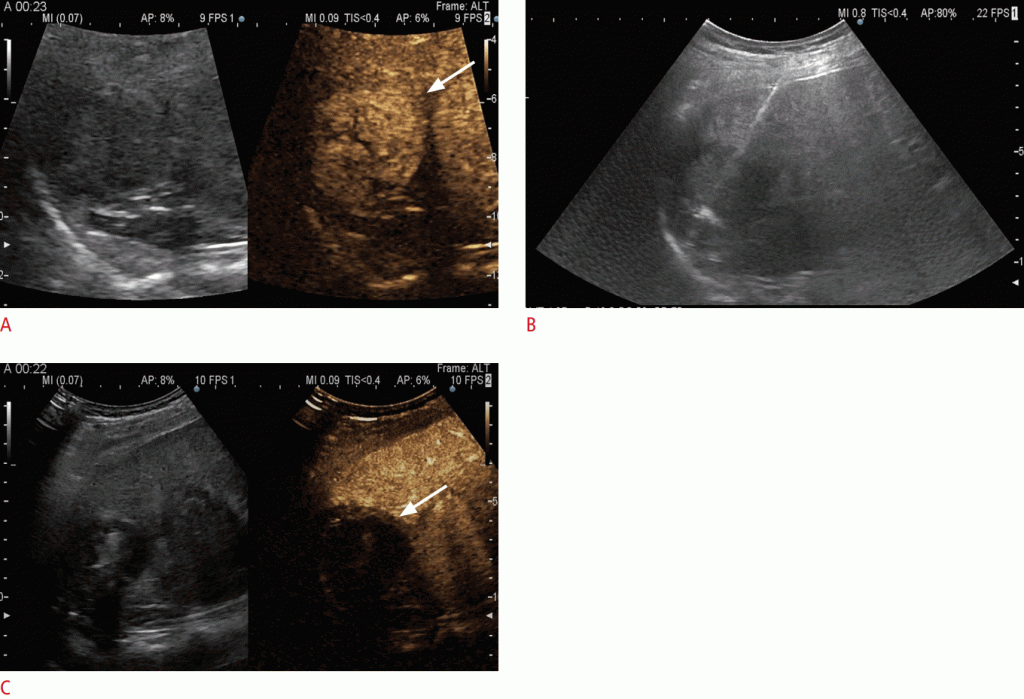
A. Під час спостереження в сегменті 7 видно вузликовий вогнище діаметром 19 мм (стрілка). B. Вузлик ізопосиленний по відношенню до навколишньої паренхіми печінки в артеріальній фазі. C. На пізній стадії, через 3 хвилини 45 секунд після введення ультразвукового контрасту, вузлик як і раніше виглядає ізопосиленним. Через 4 хвилини 28 секунд виявляється легке змивання (стрілки). Вузлик був класифікований як LR-3 (проміжна ймовірність гепатоцелюлярної карциноми). Біопсія вузла під контролем УЗД підтвердила наявність дисплазії з високим ступенем вираженості.
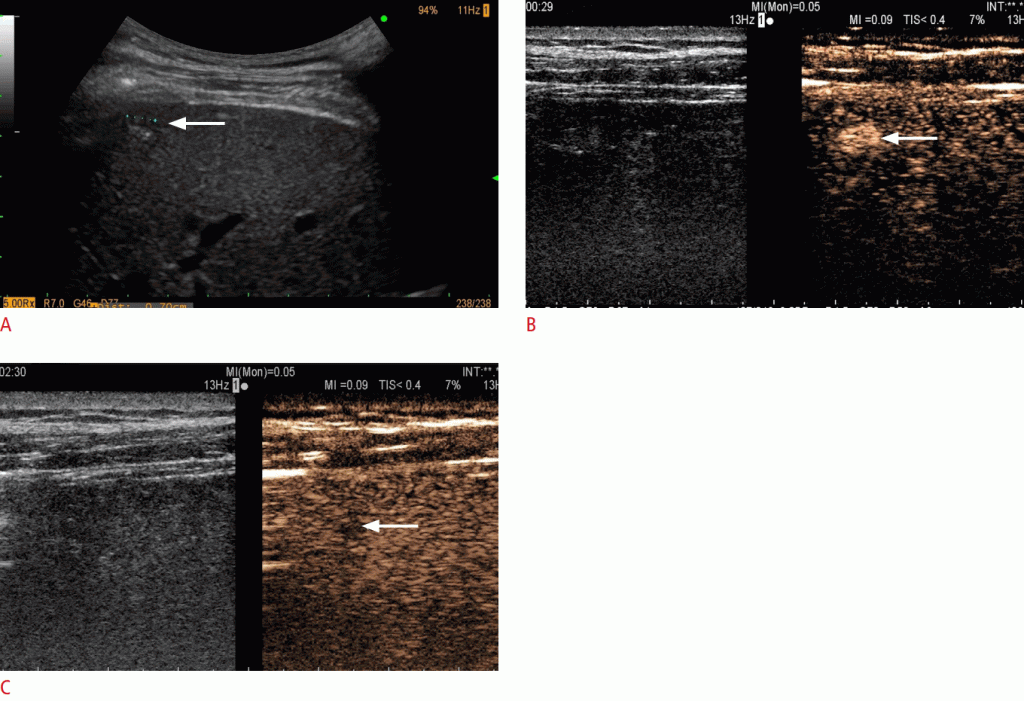
A. 7-мм субкапсулярний вузлик (стрілка) видно під час УЗД. B. Весь вузлик є гіперпосиленним (стрілка) в артеріальній фазі. C. Вузлик показує легке і пізнє вимивання (стрілка) в пізній фазі, через 2 хвилини 30 секунд після введення контрастної речовини. Через розміри менше 10 мм він був класифікований як LR-4 (вузлик з високою ймовірністю гепатоцелюлярної карциноми). Біопсія вузла під контролем УЗД підтвердила добре диференційовану гепатоцеллюлярную карциному.
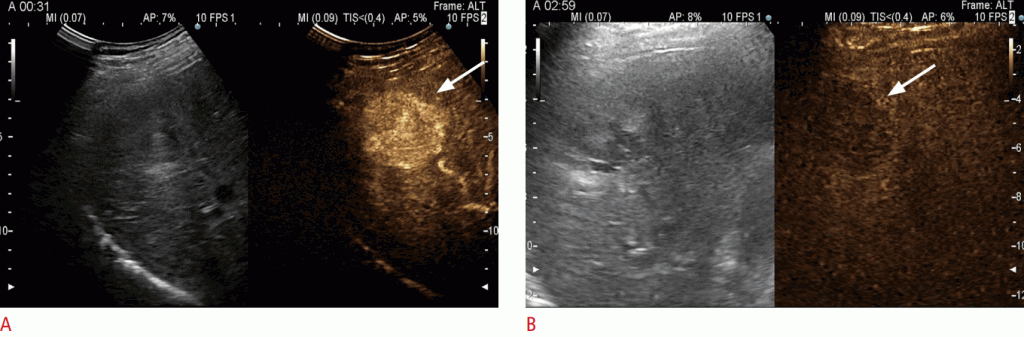
A. Вузлик гіпер-посилений (стрілка) в артеріальній фазі. B. Вузлик показує легке і пізнє вимивання (стрілка), що типово для гепатоцелюлярної карциноми. Він був класифікований як LR-5 (безумовно гепатоцелюлярна карцинома).
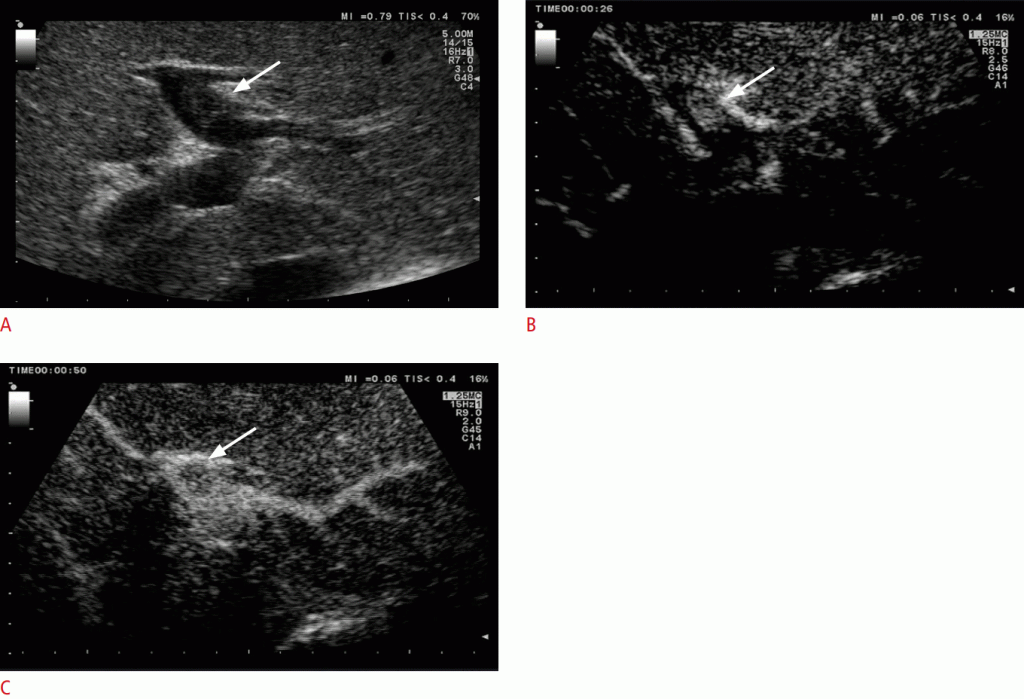
А. Ультразвукове дослідження показує тромб (стрілка) в лівій гілці воротної вени. B. Тромб показує посилення (стрілка) в артеріальній фазі. C. На пізній фазі відбувається вимивання контрасту (стрілка), що дозволяє діагностувати пухлинний тромб (Пухлина в вені) після УЗД з посиленою контрастністю і класифікується LR-5V.
Через відсутність панорамного огляду, CEUS не рекомендується для постановки злоякісних новоутворень печінки; проте методика дуже точна в характеристиці ВУП. У дослідженнях CEUS метастази в печінці показують дуже швидке і помітне вимивання, що означає, що помітність і виявлення збільшується в пізній фазі (Зобр. 9), що дозволяє оцінити всю печінку. В умовах колоректального раку після хіміотерапії рекомендується замінити не посилену УЗД на CEUS при спостереженні пацієнтів з метастазами в печінці.
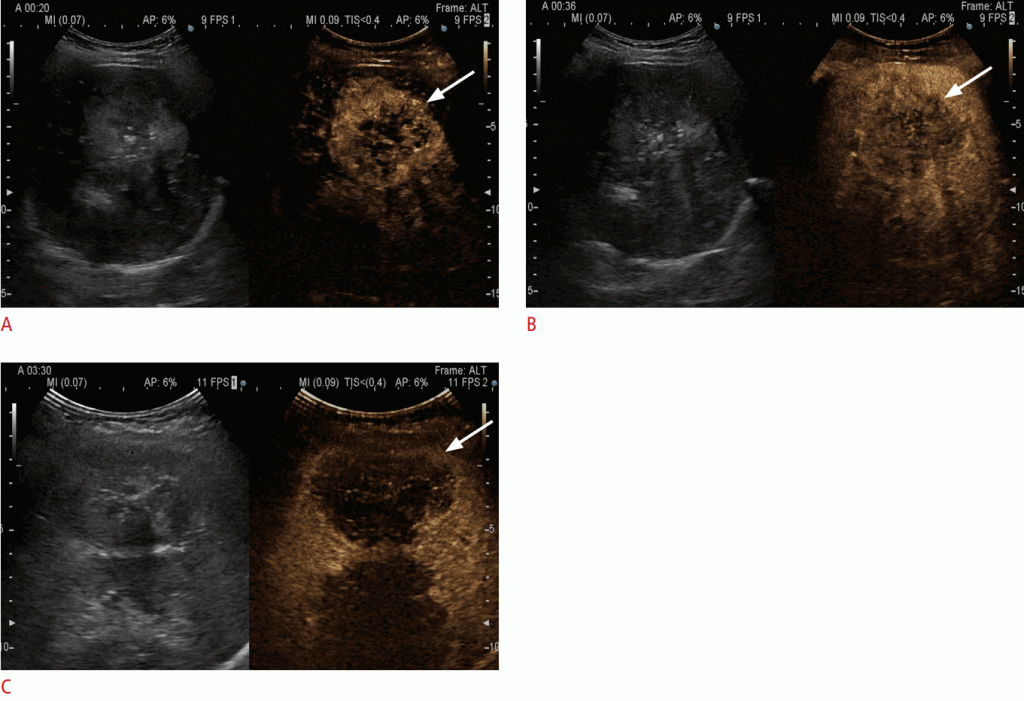
A. Показує раннє посилення (стрілка) в артеріальній фазі, через 20 секунд після введення контрасту. B. У артеріальній фазі відбувається дуже швидке вимивання (стрілка) через 36 секунд після введення контрастної речовини. C. В пізній фазі контраст виглядає повністю розмитим (стрілка).
CEUS з SonoVue отримав схвалення на використання в педіатрії при дослідженнях печінки в Сполучених Штатах, де він доступний під назвою Lumason, але ще не в Європі, де він все ще використовується не за призначенням. EFSUMB опублікував заяву про роль CEUS в педіатричній практиці, підкресливши, що література довела здійсненність, безпеку і високу діагностичну точність CEUS щодо характеристики ВУП, аналогічно з кКТ і кМРТ.
Аблятивне лікування і подальше спостереження пухлин печінки
CEUS з SonoVue ефективно використовувався для черезшкірне лікування злоякісних пухлин печінки, які невидимі або погано візуалізуються в традиційних сірих шкалах УЗД. У серії з 60 злоякісних новоутворень печінки введення радіочастотних електродів проводилося CEUS при всіх ураженнях, і відразу після абляції первинна ефективність становила 100%, за остаточною оцінкою за допомогою кМРТ.
Ураження, яке було успішно видалено, не виказує посилення після введення контрастної речовини, тоді як залишкові життєздатні ГЦК або метастази показують типову схему посилення з наступним вимиванням (Зобр. 10). Проте, протягом першого тижня після абляції можна спостерігати посилення крайової зони в зв’язку з запальною реакцією, яка починається незабаром після лікування. Цей гіперпідсиленний ореол, як правило, регулярний, товщиною близько 1,0 см, і не проявляє вимивання в пізній фазі.
Зображення 10: Гепатоцеллюлярная карцинома у чоловіка 72 років з хронічним гепатитом С і цирозом печінки.
А. На малюнку показане гіперпосилення (стрілка) маси в артеріальній фазі. Б. Черезшкурна мікрохвильова абляція гепатоцелюлярної карциноми проводиться при потужності 100 Вт, що подається антеною протягом 10 хвилин. На малюнку показана мікрохвильова антена, правильно розташована в масі. C. Через двадцять чотири години після обробки ультразвукове дослідження з контрастуванням не показало збільшення (стрілка) маси, що вказує на те, що ураження було ефективно видалено.
Ретроспективне дослідження, в якому взяли участь 92 пацієнта з 94 пухлинами, показало, що діагностична точність постпроцедурного CEUS при ранній оцінці пухлин печінки після термічної абляції була порівнянна з CEUS і кКТ, виконаними через 24 години. Таким чином, передбачається, що постпроцедурний CEUS може бути використаний для виявлення і ретриту залишкової життєздатної тканини в одному і тому ж абляційному сеансі.
Аналіз економічної ефективності, виконаний в серії з 93 пацієнтів з 148 ГЦК, показав, що використання внутрішньопроцедурного CEUS в порівнянні зі стандартним лікуванням зменшило витрати на 21,9%, оскільки використання контрастності дозволило виявити неповну абляцию, тобто що додаткове лікування може бути виконано у час того ж сеансу.
При спостереженні за віддаленими пухлинами кКТ і кМРТ є золотим стандартом для оцінки терапевтичної ефективності завдяки їх високій діагностичній точності і можливості ретельної оцінки потенційних метастатичних ділянок. Проте, CEUS може використовуватися, коли кКТ або кМРТ не переконливі або протипоказані.
У серії з 588 пацієнтів з повністю видаленими пухлинами, які спостерігалися послідовно з використанням CEUS і ККТ почергово, кожні 3 місяці протягом 2 років, рецидиви розвинулися в одному і тому ж сегменті віддаленого ураження в 72% випадків.
Таким чином, CEUS виявився ефективним, незважаючи на обмежене поле зору в артеріальній фазі. Грунтуючись на цих висновках, автори припустили, що включення CEUS в подальше спостереження за пацієнтами може знизити кількість обстежень кКТ і кМРТ, тим самим зменшуючи витрати і ризики.
Дифузні захворювання печінки
CEUS з SonoVue використовувався для оцінки тяжкості захворювання печінки в деяких дослідженнях, в яких за допомогою спеціального програмного забезпечення оцінювалося час появи контрасту в печінкових венах. Обгрунтування полягає в тому, що капіляризація синусоїд, поряд з наявністю артеріовенозних і порто-венозних шунтів, призводить до зменшення часу наповнення печінкової вени (HVAT) у пацієнтів з цирозом печінки. У дослідженні 160 послідовних пацієнтів з циротичними (n = 78) і не циротичними захворюваннями печінки (n = 82) і 14 здоровими контролями було показано, що HVAT був нижче у пацієнтів з цирозом, ніж у пацієнтів без цирозу і в контролі: 15,0 ± 2,8, 21,5 ± 3,4 і 25,6 ± 4,7 секунди відповідно (P <0,05).
Значення відсікання 17 секунд виключало цироз печінки з чутливістю 91,1% і специфічністю 93,6%. В іншому дослідженні, виконаному для виявлення пацієнтів з портальною гіпертензією, HVAT був значно коротший серед пацієнтів з цирозом печінки, ніж у контрольній групі (30,5 ± 3,3 проти 13,3 ± 3,2 секунди, P <0,001), а HVAT <14 секунд ідентифікував пацієнтів з клінічно значущою портальною гіпертензією (площа під характеристичною кривою приймаючого оператора 0,95; чутливість 90,0%; специфічність 86,7%) [36].
Незважаючи на ці цікаві результати, слід підкреслити, що існує великий збіг між прециротичною і циротичною стадіями захворювання.
Висновок
CEUS з SonoVue – це безпечна і економічно ефективна процедура візуалізації для визначення характеристик ВУП. Він забезпечує динамічну оцінку ВУП в режимі реального часу без радіаційного впливу і може використовуватися навіть тоді, коли протипоказаний кКТ або кМРТ. У деяких клінічних сценаріях метод є економічно ефективним в порівнянні з кКТ і кМРТ, але при цьому має однакову точність. CEUS дозволяє миттєво охарактеризувати більшість ВУП випадково виявлених під час УЗД, що дозволяє уникнути більш дорогих досліджень, які не вільні від потенційних ризиків.
Обмеження у використанні CEUS включають в себе відсутність великого поля зору і необхідність забезпечення наявності відповідного акустичного вікна. Більш того, результати залежать від досвіду оператора.
У нашому каталозі Ви можете ознайомиться з УЗ-апаратами, які підходять для проведення CEUS. Якщо виникнуть питання, наші менеджери із задоволенням на них дадуть відповідь!
Часті питання та відповіді (FAQ)
Що таке SonoVue і як він використовується при контрастному ультразвуковому дослідженні печінки?
- SonoVue – це контрастний засіб для ультразвукового дослідження (УЗД), що складається з мікропухирців, заповнених газом гексафториду сірки. Він використовується для покращення візуалізації кровотоку в печінці та характеристики вогнищевих уражень печінки (ВУП).
Які переваги використання SonoVue при дослідженні ВУП?
- SonoVue є безпечним і неінвазивним методом. Він дозволяє візуалізувати мікроциркуляцію в печінці, що допомагає диференціювати доброякісні та злоякісні ураження.
- На відміну від КТ та МРТ, SonoVue не має міжсудинної фази, що забезпечує динамічне дослідження мікроциркуляції.
- Його можна використовувати у пацієнтів з порушеною функцією нирок.
Як SonoVue допомагає диференціювати доброякісні та злоякісні ураження печінки?
- Доброякісні ураження, як правило, демонструють стійке посилення в портальній венозній та пізній фазах без ознак вимивання.
- Злоякісні ураження часто показують гіпопосилення в пізніх фазах, супроводжуване вимиванням контрастної речовини.
Наскільки точний метод CEUS з SonoVue при діагностиці ВУП?
- Мета-аналіз показав високу чутливість (93%) та специфічність (90%) CEUS для діагностики злоякісних уражень печінки.
- Дослідження показали, що CEUS має порівнянну точність з КТ та МРТ.
Чи є протипоказання до використання SonoVue?
- SonoVue, як правило, добре переноситься, але можуть бути побічні ефекти, такі як нудота, блювота або головний біль. Важливо проконсультуватися з лікарем про можливі ризики.
Чи використовується SonoVue в педіатрії?
- В Сполучених Штатах SonoVue (під назвою Lumason) схвалений для використання в педіатрії, але в Європі його застосування в цій віковій групі поки що не є стандартною практикою.
Яка роль SonoVue в моніторингу після аблятивного лікування пухлин печінки?
- CEUS з SonoVue ефективний для моніторингу після абляції, дозволяючи оцінити ефективність лікування та виявити залишкову життєздатну тканину.
- Він може допомогти зменшити кількість КТ та МРТ досліджень.