Резюме
Тяжкі менструальні кровотечі (ТМК) або аномальні маткові кровотечі (АМК) є поширеною причиною гінекологічних скарг у жінок в перименопаузі. Більшість жінок з ТМК/АМК у перименопаузальному віці, коли медикаментозна терапія виявляється неефективною, обирають гістеректомію, яка, на жаль, має значні проблеми, пов’язані з безпекою та довготривалою якістю життя, а також є тягарем для системи охорони здоров’я і коштує дорого для пацієнток. Існують хірургічні методи мінімального доступу, такі як гістероскопічна таргетна терапія, які є консервативними і щадять матку, уникаючи великих хірургічних втручань та їх ускладнень і наслідків. Гістероскопічне лікування ТМК – це мінімально інвазивний і цілеспрямований підхід у діагностиці та лікуванні патологічних уражень, що викликають симптоми, а не радикальний, як гістеректомія, яка має більше шансів виникнення небажаних явищ як під час, так і після операції. З точки зору якості життя, пов’язаної зі здоров’ям, жінки, які страждають на ТМК і які пройшли гістероскопічне консервативне лікування, мали кращі показники порівняно з пацієнтками, яким була виконана гістеректомія.
Метою цього огляду є аналіз доказів, отриманих для порівняння двох хірургічних методів – гістероскопічної таргетної терапії та гістеректомії – з точки зору їх ефективності, безпечності та впливу на якість життя жінок у перименопаузі з ТМК/АМК.
Вступ та передумови
Одними з найважливіших симптомів, з якими жінки звертаються до гінеколога, є аномальні маткові кровотечі (АМК) або тяжкі менструальні кровотечі (ТМК). Поширеність АМК/ТМК становить 11-13% у всіх вікових групах жінок, збільшуючись до 25-30% у віці 36-40 років [1].
В оновлених даних Міжнародної федерації гінекології та акушерства (FIGO), опублікованих у вересні 2021 року, зазначається, що показники поширеності ТМК можуть широко варіювати залежно від демографічних показників, визначення, яке використовується для ТМК, та інших факторів. За оцінками, майже 20% жінок страждають від АМК/ТМК під час дітонародження та в перименопаузальному віці [2].
Повідомляється, що в Індії частота виявлення ТМК/АМК в гінекологічних консультаціях сягає від 17 до 30% [1]. Аномальні маткові кровотечі є поширеною причиною страждань жінок перименопаузального віку, а також значно погіршують якість життя (ЯЖ).
Окрім впливу на загальну якість життя з точки зору фізичного, психічного та сексуального здоров’я, ТМК підвищує ризик хірургічних втручань, таких як гістеректомія. На жаль, гістеректомія все ще залишається найпоширенішою гінекологічною операцією, і в більшості випадків її проводять при доброякісних гінекологічних захворюваннях, а не як процедуру, що рятує життя. Майже 40-50% жінок, які перенесли гістеректомію з приводу ТМК/АМК, мають матку нормального розміру без значної патології органів малого тазу. У 40-60% жінок основною патологією, яку можна цілеспрямовано видалити, є поліп ендометрія або невелика субмукозна міома матки.
Завдяки досягненням і досвіду малоінвазивних і маткозберігаючих процедур, що виконуються за допомогою гістероскопії в гінекологічній практиці, радикальних процедур, таких як гістеректомія, і пов’язаних з ними ускладнень, можна уникнути в більшості випадків ТМК/АМК. Малоінвазивні гістероскопічні хірургічні процедури (наприклад, гістероскопічна поліпектомія, трансцервікальна резекція ендометрія (ТЦРЕ), гістероскопічна міомектомія) спрямовані на цілеспрямовану терапію і є консервативними в лікуванні. Окрім ТЦРЕ, гістероскопічна поліпектомія та міомектомія є цілеспрямованими операціями, які можуть повністю полегшити менструальні симптоми, пов’язані з ними.
Терапія першої лінії при АМК/ТМК здебільшого обирається як медикаментозний метод лікування, але у деяких пацієнток вона виявляється неефективною. Тому і лікарі, і пацієнтки обирають гістеректомію як надійний або остаточний метод лікування порушень менструальної кровотечі. Хоча цей метод ефективний, він дорогий і пов’язаний з ризиком анестезії та хірургічного втручання.
Протягом останніх трьох десятиліть підхід до доброякісних захворювань рухається в бік консервативних методів, особливо з появою малоінвазивної гістероскопії. Вона також слугує для цілеспрямованої терапії та збереження анатомії тазу матки, тим самим покращуючи якість життя цих жінок. Гістероскопічні процедури є менш інвазивними, пропонують цілеспрямовану терапію і зберігають матку та нормальну анатомію і функцію тазу.
Існує потреба у зміні мислення жінок і багатьох лікарів-гінекологів щодо можливостей лікування. Жінки повинні бути більш поінформовані про наявність щадних для матки методів лікування, які можуть полегшити їхні первинні симптоми і мають як короткострокові, так і довгострокові переваги збереження матки для якості життя. Покращення доказової бази та характеристика порівняння консервативного цілеспрямованого підходу шляхом гістероскопічного лікування ТМК/АМК з гістеректомією допоможуть у прийнятті обґрунтованих рішень та консультуванні цих жінок.
Метою даної оглядової статті є оцінка та порівняння маткозберігаючого (збереження матки та уникнення гістеректомії) консервативного методу гістероскопічної терапії з традиційною гістеректомією з точки зору ефективності, безпеки та зміни якості життя в якості лікувального хірургічного методу для жінок, які страждають на АМК/ТМК.
Мета
Ми маємо на меті проаналізувати дослідження та порівняти ефективність у полегшенні менструальних скарг, безпеку та вплив на післяопераційну якість життя двох методів – маткозберігаючої гістероскопічної хірургічної терапії та гістеректомії для лікування ТМК/АМК у пременопаузальній віковій групі.
Методи пошуку для ідентифікації досліджень
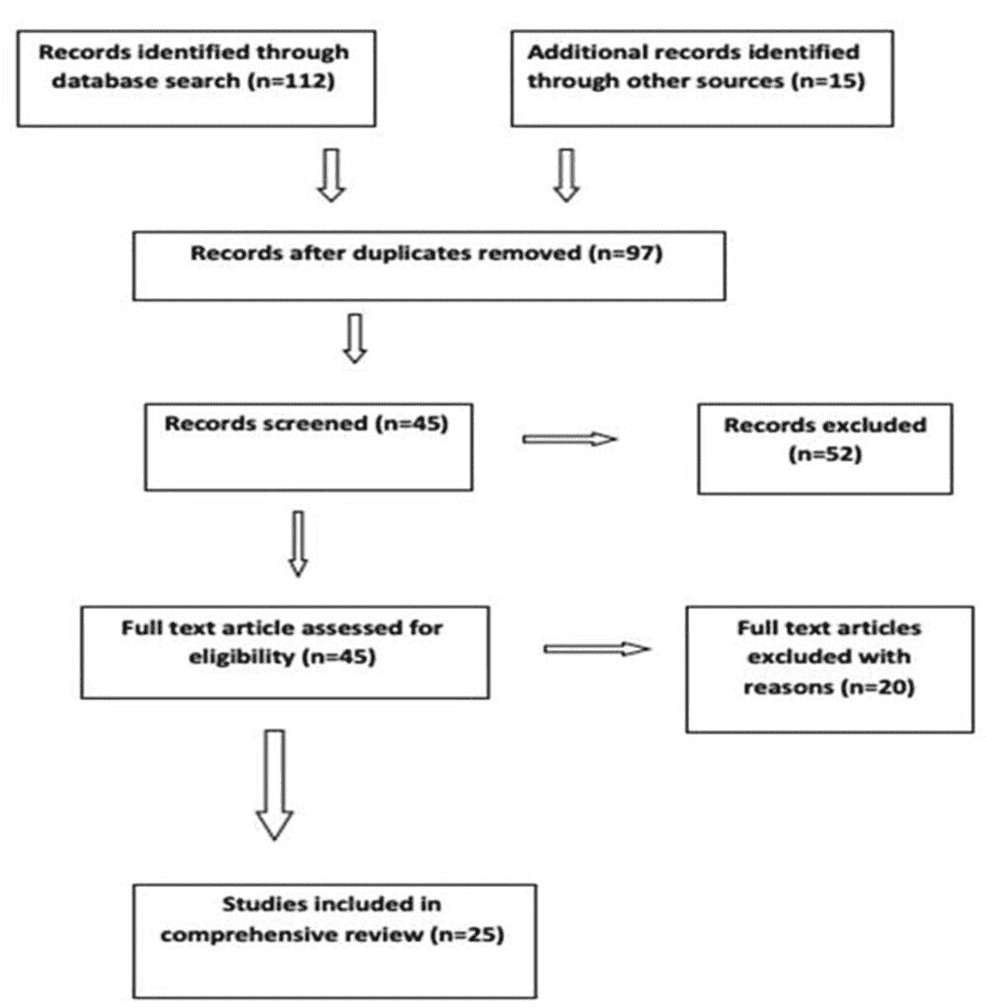
Ми провели пошук в електронних базах даних і бібліографіях знайдених статей оригінальних статей і оглядових статей, а також аналіз посилань на них. Також були проаналізовані відповідні публікації в матеріалах конференцій та журналах. Для пошуку в окремих базах даних використовували медичні предметні рубрики (МеПР). Терміни МеПР, включаючи всі підзаголовки і ключові слова, які ми використовували: гістероскопія, поліпи ендометрія, аномальні маткові кровотечі, поліпи ендометрія, гістероскопічна поліпектомія, субмукозна міома, гістероскопічна міомектомія, гістеректомія, резекція ендометрія і якість життя, пов’язана зі здоров’ям. На зображенні 1 показано стратегію пошуку, застосовану в цьому огляді.
Зображення 1: Стратегія пошуку, застосована в огляді.
Огляд
Майже 10%-30% жінок страждають від ТМК/АМК у перименопаузальному віці [3]. Goldstein і Lumsden у своєму дослідженні повідомили, що 20% гінекологічних консультацій у жінок у пременопаузі припадає на ТМК/АМК, тоді як цей показник зростає до 25% у тих, хто піддається хірургічним втручанням у перименопаузальному віці [4]. Whitaker і Critchley повідомили, що третина всіх амбулаторних гінекологічних візитів у репродуктивному віці і майже 69% у жінок перименопаузального віку пов’язані з сильними або аномальними матковими кровотечами [5]. В Ontario Health Technology Assessment Series було опубліковано, що в Онтаріо, за оцінками, від 15% до 20% жінок старше 30 років мають ТМК [6].
У дослідженні Acharya та співавт. (2019) 42% (148 з 354) жінок з ТМК/АМК були молодше 40 років, що свідчить про те, що значна кількість жінок з АМК/ТМК є молодшими і схильні до ризику проведення гістеректомії у віці до 40 років. Жінки приймають рішення про проведення гістеректомії у молодому віці (до 32 років) і піддаються ризику її проведення, а також проводять решту життя з ризиком виникнення наслідків ранньої менопаузи. У групі гістеректомії найнижчий вік, який спостерігався, був 31 рік [1].
Діагностика
Дослідження Goyal та співавт., в якому порівнювали трансвагінальну сонографію (ТВС) і гістероскопію в оцінці ТМК/АМК, показало, що у 57% пацієнток ендометрій і порожнина матки були в нормі при ТВС, в той час як в решті випадків були виявлені поліпи міоми і товстий ехо-комплекс ендометрія [7].
У дослідженні Bingol та співавт. повідомляється, що поліпозні ураження призвели до встановлення діагнозу, тоді як гіперплазія була другою найпоширенішою причиною серед досліджуваної популяції, що складалася з 137 жінок з аномальними матковими кровотечами [8].
У своєму дослідженні Selvanathan та співавт. проаналізували гістопатологічну діагностику АМК/ТМК. Двадцять три відсотки жінок мали нормальні результати УЗД органів малого тазу, 39,33% – потовщений ендометрій, 16,29% – гіперплазію + поліп, 22,36% – гіперплазію і 8,99% – фіброміому, тоді як у групі гістеректомії ці показники становили 31,25%, 36,36%, 11,93%, 15,34% і 5,11% відповідно. У більшості пацієнток була підозра на поліп або гіперплазію [1].
Вони також детально розглянули взаємозв’язок між ультразвуковим дослідженням органів малого тазу (УЗД) та результатами гістероскопії в групі гістероскопії. З 42 випадків, які за результатами УЗД були визнані нормальними, 28 мали нормальні результати гістероскопії, тоді як 14 мали поліпи ендометрію. З 70 випадків потовщення ендометрію за даними УЗД у 55 був виявлений поліп, у шести – гіперплазія + поліп, а у дев’яти – нормальні результати. З 31 випадку гіперплазії з поліпом у чотирьох була лише гіперплазія, у 18 – гіперплазія з поліпом і у двох – лише поліп. З 22 випадків гіперплазії у восьми були нормальні результати, у дев’яти – поліпи і в чотирьох – гіперплазія. Усі 13 випадків, які вказували на фіброміому, були фіброміомою при гістероскопії. Це свідчить про те, що прямий погляд всередину матки дає змогу поставити остаточний діагноз, а лікування можна обговорити і призначити цілеспрямоване. У цьому дослідженні не було жодного випадку атрофічного ендометрію, оскільки більшість наших пацієнток були молодшими (середній вік близько 40 років) у віковій групі [1].
Abid та співавт. провели дослідження для аналізу клінічного спектру та гістопатологічної діагностики АМК/ТМК. Найпоширенішим діагнозом був нормальний менструальний цикл (34%), далі йшли ановуляторний (27%), доброякісний поліп (14%), ендометрит (12%), атрофічний ендометрій (6%), гіперплазія ендометрію (5%) і карцинома ендометрію (2%). Вони дійшли висновку, що більшість ТМК мають органічну доброякісну патологію, і їх можна лікувати консервативними методами [9].
Ефективність двох хірургічних методів
Для оцінки менструальної крововтрати використовується графічна таблиця оцінки крові (PBAC). Оцінка за шкалою PBAC у 100 балів і більше вважається сильною кровотечею [10]. Нижче наведено огляд ефективності гістероскопічної хірургічної терапії, що застосовується для лікування ТМК/АМК, з точки зору покращення показників крововтрати та менструального циклу.
Покращення показників за шкалою PBAC
У дослідженні Selvanathan та співавт. середній передопераційний бал (PBAC) у групі гістероскопії становив 251,073 (СВ 75,41), тоді як у групі гістеректомії – 252,108 (СВ 74,98). У жінок, яким було проведено гістероскопію, спостерігалася значна зміна показника PBAC та покращення показників крововтрати. Через шість місяців після операції він становив 70,06 (СВ 38,06) із середньою зміною показника PBAC 181,6 при р-значенні 0,000, що є достовірним (ДІ 149,53-172,25). Через рік спостереження середній бал за шкалою PBAC ще більше знизився до 65,04469 (23,07) з р-значенням 0,000, що є значущим і свідчить про те, що через рік показник залишився майже незмінним і не погіршився. Результати свідчать про те, що протягом одного року кількість та характер менструальних кровотеч поступово покращилися. Ці моменти слід враховувати і пояснювати жінкам для кращого сприйняття методів лікування [1].
Кокранівський систематичний огляд Fergusson та співавт. щодо резекції та абляції ендометрія порівняно з гістеректомією при сильних менструальних кровотечах дійшов висновку, що консервативна резекція та абляція ендометрія не поступається гістеректомії в досягненні полегшення через один, два та чотири роки [11].
Вплив на менструальний цикл
Abbott та співавт. у своєму дослідженні проаналізували ефективність абляції ендометрію в лікуванні аномальних маткових кровотеч. Вони повідомили, що консервативна методика не поступається в контролі кількості та характеру кровотечі у жінок з АМК та задоволеності пацієнток. У їхньому дослідженні частота аменореї, гіпоменореї, еуменореї та менорагії після абляції через 12 місяців становила 16/37 (43%), 11/18 (61%) проти 10/37 (27%) та 5/18 (27%) [12].
У Кокранівському систематичному огляді Lethaby та співавт. щодо методів резекції та абляції ендометрія при лікуванні ДМК повідомляється про наступні показники аменореї при двох методах резекції ендометрія. Частота аменореї була порівнянною в обох групах в кінці одного року [13].
Matteson та співавт. у своєму систематичному огляді вивчили сім досліджень і повідомили про їх вплив на результати менструальних кровотеч. Кількість жінок, які досягли аменореї, коливалася в межах 13-64%. Хоча показник аменореї становив 100%, був один випадок, коли після гістеректомії у пацієнтки також спостерігалася персистуюча кровотеча з піхвового склепіння [14].
Stepniewska та співавт. вивчали і порівнювали довгострокові ефекти іншого маткозберігаючого методу лікування аденоміозу – радіочастотної термічної абляції (РТА) у 60 пацієнток. Вісім пацієнток перенесли гістеректомію. Вони дійшли висновку, що РЧА дозволяє уникнути гістеректомії в більшості випадків аденоміозу [15].
Piecak і Milart вивчали результати гістероскопічної міомектомії. Вони припустили, що більшість субмукозних міом можна видалити гістероскопічно як одномоментну операцію при правильному відборі пацієнтів, при цьому від 70 до 99% жінок після операції не мають жодних симптомів. Рівень успіху обернено пропорційний віку жінки [16].
Agdi і Tulandi вивчали ендоскопічне лікування міоми матки. Вони дійшли висновку, що гістероскопічна міомектомія є ефективним методом лікування підслизової міоми [17]. Фіброміома може рецидивувати навіть після гістероскопічної міомектомії, особливо в репродуктивному віці, як показали дослідження Selvanathan та ін. [1]. У їхньому дослідженні пацієнтки з рецидивом і персистуючою менорагією були молодше 40 років.
Camanni та співавт. у своєму дослідженні зазначають, що субмукозна міома діаметром 6 см і менше лікується ефективніше, ніж міоми більшого розміру. При більших розмірах може знадобитися два сеанси [18]. Градація міом за шкалою LASMAR дозволяє оцінити фіброміому з точки зору необхідності одного або двох хірургічних втручань і спрогнозувати безпеку операції [19]. Donnez та співавт. повідомили, що невдачі гістероскопічного лікування корелюють з неправильним відбором хворих, неадекватною резекцією та супутнім аденоміозом [20]. Van Dongen та співавт. рекомендували повну резекцію фіброміоми для полегшення симптомів [21]. У дослідженні Selvanathan та співавт. дві пацієнтки з персистуючою менорагією були молодше 40 років. При ультразвуковому дослідженні у них була виявлена нормальна порожнина матки з потовщеним ендометрієм. Це потовщення ендометрію могло бути наслідком притаманного фіброміомі гіперестрогенного статусу. Abdollahi Fard та співавт. вивчали гістероскопію для лікування ТМК/АМК. Гістероскопія була успішною у 73,5% жінок з кровотечею [22].
У дослідженні Selvanathan та співавт. дисменорея розглядалася як асоційований симптом АМК/ТМК у 28 з 178 (15,73%) випадків у групі гістероскопії та 34 з 176 (19,31%) у групі гістеректомії. Усі жінки, крім двох, з 28 (92,2%) у групі гістероскопії були позбавлені дисменореї.
Небажані явища та безпечність
Нижче наведено огляд літератури щодо порівняння безпеки та небажаних явищ при застосуванні гістероскопії та гістеректомії як методів лікування АМК.
У Кокранівському систематичному огляді Fergusson та співавт. порівнювали гістероскопічне лікування та гістеректомію як методи лікування ТМК/АМК. Гістероскопічне лікування було кращим з точки зору ефективності та безпеки порівняно з гістеректомією [11].
У якісному рандомізованому дослідженні абляції ендометрія порівняно з гістеректомією у жінок з ТМК/АМК Solnik і Munro повідомили про значну різницю в ранніх післяопераційних ускладненнях між гістероскопічними операціями і гістеректомією: 4/110 випадків при гістероскопічних операціях і 20/118 випадків при гістеректомії з ВР 0,21 [ДІ 0,08, 0,61] [23]. Аналогічна картина спостерігається в дослідженні Zupi та співавт. щодо ранніх ускладнень TCRE 3/89 і 4/92 для гістеректомії зі значно меншим ВР 0,78 [0,18, 3,37] для гістероскопічної процедури, як повідомляють Zupi та співавт. для ранніх ускладнень цих двох процедур [24].
У дослідженні, проведеному Selvanathan та співавт., значна кількість жінок, які перенесли гістеректомію, мали пізні та відстрочені небажані явища наприкінці одного року порівняно з гістероскопією, що свідчить про те, що гістероскопічний метод хірургічного втручання є безпечнішим, навіть коли жінки спостерігаються протягом одного року. Вони також стверджують, що у жінок, які перенесли гістеректомію, частіше виникали тазові болі, симптоми сечового міхура, сексуальний дискомфорт і менопаузальні симптоми, і вони тривали довше порівняно з гістероскопічною терапією [1].
Якість життя (ЯЖ)
Matteson та співавт. проаналізували шість досліджень, які оцінювали ЯЖ, і дійшли висновку, що обидва методи мали покращення. Вони також припустили, що існує потреба у вивченні довгострокового впливу на ЯЖ для порівняння двох хірургічних методів [14]. Аналогічні висновки були зроблені в огляді Zupi та співавт. та ін. [24].
У дослідженні Acharya та співавт. в обох групах – гістероскопічної терапії та гістеректомії – середні показники в усіх сферах поступово зростали протягом одного тижня, шести місяців і одного року спостереження, але в групі гістероскопії показники були значно кращими і покращувалися швидше і раніше порівняно з групою гістеректомії на всіх етапах післяопераційного спостереження, а пацієнтки рано повернулися до роботи [1].
Abbott та співавт. вивчали якість життя як первинний результат лікування абляції ендометрія і дійшли висновку, що якість життя жінок, які страждають на ДМК, покращується після гістероскопічної абляції, і це є успішним методом лікування таких жінок [25]. У таблиці 1, наведеній нижче, узагальнено аналіз 25 статей.
| No | Ім’я автора та номери посилань | Кількість учасників | Тип дослідження/втручання | Висновок |
| 1 | Acharya та співавт. [1] | 354 | Спостережне дослідження – дві групи. Група I – гістероскопічна хірургічна процедура – поліпектомія, резекція ендометрія, міомектомія. Група II – гістеректомія – абдомінальна гістеректомія, вагінальна гістеректомія, лапароскопічна гістеректомія. | Як короткострокова, так і довгострокова ЯЖ були кращими в групі гістероскопії, ніж у групі гістеректомії. |
| 2 | Munro та співавт. [2] | – | Міжнародний комітет з розладів менструального циклу (FIGO) досягнув консенсусу щодо перегляду основних термінологій АМК та варіантів лікування. | Уточнено термінологію, пов’язану з класифікацією типів АМК, діагностикою та методами лікування. |
| 3 | Vitale та співавт. [3] | 111 досліджень | Оглядова стаття | Індивідуалізований підхід покращує якість життя за допомогою належних варіантів лікування, обговорених з пацієнтом. |
| 4 | Goldstein and Lumsden [4] | 37 досліджень | Оглядова стаття | Оперативна гістероскопія ефективна для запобігання та відтермінування гістеректомії. |
| 5 | Whitaker and Critchley [5] | 56 досліджень | Оглядова стаття | Індивідуалізований та консервативний підхід до лікування АМК має кращі показники ЯЖ для цих жінок. |
| 6 | Medical Advisory Secretariat [6] | 43 досліджень | Систематичний огляд | Майже 15-20% жінок перименопаузального віку страждають від АМК. |
| 7 | Goyal та співавт. [7] | 100 пацієнтів | Інтервенційне дослідження | ТВС є першим неінвазивним дослідженням, рекомендованим для діагностики причини АМК. |
| 8 | Bingol та співавт. [8] | 346 пацієнтів | Інтервенційне дослідження | Соносальпінгографія з інфузією фізіологічного розчину перевершує ВС для діагностики АМК. |
| 9 | Abid та співавт. [9] | 241 пацієнт | Перехресне дослідження | Поліп ендометрія є найпоширенішою причиною АМК, тому слід обирати консервативний підхід. |
| 10 | Pai та співавт. [10] | – | Оглядова стаття | В огляді описано діагностичний алгоритм та зосереджено увагу на консервативних методах лікування АМК. |
| 11 | Fergusson та співавт. [11] | 11 RCT | Кокранівський огляд | Резекція та абляція ендометрія є альтернативою гістеректомії в якості хірургічного лікування сильних менструальних кровотеч. |
| 12 | Abbott та співавт. [12] | 37 пацієнтів | Інтервенційне дослідження | Рекомендується провести подальші дослідження емболізації маткових артерій, перш ніж вважати її ефективною та безпечною для лікування АМК. |
| 13 | Lethaby та співавт. [13] | 18 досліджень | Кокранівський систематичний огляд | Методи абляції ендометрію ефективні в лікуванні АМК. |
| 14 | Matteson та співавт. [14] | 7 досліджень | Оглядова стаття | Гістероскопічна поліпектомія повинна супроводжуватися резекцією ендометрія для полегшення симптомів АМК. |
| 15 | Stepniewska та співавт. [15] | 60 пацієнтів | Інтервенційне дослідження | Радіочастотна термічна абляція як консервативний підхід дозволяє уникнути гістеректомії при аденоміозі. |
| 16 | Piecak and Milart [16] | 8 досліджень | Оглядова стаття | Гістероскопічне видалення біполярною енергією ефективне для видалення субмукозної міоми. |
| 17 | Agdi and Tulandi [17] | 51 досліджень | Оглядова стаття | Велика кількість міом можна лікувати ендоскопічно і, таким чином, консервативно. |
| 18 | Camanni та співавт. [18] | 33 пацієнти | Інтервенційне дослідження | Гістероскопічна міомектомія ефективна при розмірах міоми 6 см і менше. |
| 19 | Lasmar та співавт. [19] | 191 пацієнт | Багатоцентрове проспективне дослідження | Класифікація STEPW дозволяє краще прогнозувати успішність видалення міоми. |
| 20 | Donnez та співавт. [20] | – | Оглядова стаття | Гісетроскопічна резекція міоми є ефективним консервативним методом лікування підслизових міом. |
| 21 | van Dongen та співавт. [21] | 60 пацієнтів | Рандомізоване контрольоване дослідження | Гістероскопічна морцеляція пропонує хорошу заміну звичайному методу резекції. |
| 22 | Abdollahi Fard та співавт. [22] | 277 пацієнтів | Описовий перехресний | Гістероскопія є безпечним, точним та ефективним методом лікування АМК |
| 23 | Solnik and Munro [23] | – | Оглядова стаття | Перед тим, як робити вибір на користь гістеректомії у жінок з АМК у перименопаузальному віці, слід шукати альтернативні методи лікування. |
| 24 | Zupi та співавт. [24] | 181 пацієнт | Інтервенційне дослідження | За і проти гістеректомії при АМК є те, що вона є остаточним методом лікування і пов’язана з короткостроковим і довгостроковим впливом на ЯЖ, що є плюсами і мінусами цього методу. |
| 25 | Abbott та співавт. [25] | 131 пацієнт | Інтервенційне дослідження | Якість життя жінок покращується при консервативному гістероскопічному підході до лікування АМК. |
Таблиця 1: Аналіз досліджень.
АМК: Аномальна маткова кровотеча; ТВС: Трансвагінальна сонографія; ЯЖ: Якість життя.
Висновки
Сильні менструальні кровотечі є поширеною причиною звернень до гінеколога, частота яких становить 24% від загальної кількості звернень до гінеколога. Гістероскопічна таргетна терапія ефективна для контролю менструальних кровотеч при АМК/ТМК. Вона також ефективна для полегшення обтяжливих менструальних симптомів, які є основною скаргою при АМК/ТМК. Гістероскопічні терапевтичні процедури встановлюють еуменорею або гіпоменорею та аменорею у більшості пацієнток при короткостроковому та довгостроковому спостереженні, що є бажаним ефектом з точки зору збереження матки та уникнення гістеректомії. У тих небагатьох пацієнток, які мають стійкі менструальні симптоми, є хороші шанси відповісти на медикаментозну терапію, оскільки первинна причина усувається за допомогою гістероскопії. Таким чином, гістероскопічні терапевтичні процедури є порівнянними за ефективністю в усуненні первинних скарг на порушення менструального циклу у жінок, які страждають на АМК/ТМК, і мають потенційну перевагу в уникненні великих і радикальних хірургічних процедур, таких як гістеректомія.
Гістероскопічні терапевтичні процедури є безпечнішими, оскільки знижують відносний ризик інтраопераційних, ранніх, пізніх та відстрочених післяопераційних ускладнень як хірургічний метод лікування АМК/ТМК порівняно з гістеректомією. Гістероскопічні операції також мають перевагу у вигляді меншого післяопераційного болю, коротшого часу операції та перебування в стаціонарі, що дає можливість раннього післяопераційного відновлення та уникнення втрат робочого часу порівняно з гістеректомією. Жінки, які перенесли гістеректомію, мають значно більший ризик тазового болю, дисфункції сечового міхура, сексуальної дисфункції та менопаузальних симптомів, які тривають довше порівняно з гістероскопічною терапією. Пацієнтки, які страждають на АМК/ТМК, мають низьку якість життя (ЯЖ), пов’язану зі здоров’ям. Як гістероскопічна терапія, так і гістеректомія як методи лікування ТМК покращують усі сфери якості життя. Покращення ЯЖ у всіх сферах є швидким і більш раннім при гістероскопічній терапії, ніж у групі гістеректомії.
Посилання на джерела
1.Selvanathan S, Acharya N, Singhal S: Quality of life after hysterectomy and uterus-sparing hysteroscopic management of abnormal uterine bleeding or heavy menstrual bleeding. J Midlife Health. 2019, 10:63-69. 10.4103/jmh.JMH_15_19
2.Munro MG, Critchley HO, Fraser IS: The two FIGO systems for normal and abnormal uterine bleeding symptoms and classification of causes of abnormal uterine bleeding in the reproductive years: 2018 revisions. Int J Gynaecol Obstet. 2018, 143:393-408. 10.1002/ijgo.12666
3.Vitale SG, Watrowski R, Barra F, et al.: Abnormal uterine bleeding in perimenopausal women: the role of hysteroscopy and its impact on quality of life and sexuality. Diagnostics (Basel). 2022, 12:1176. 10.3390/diagnostics12051176
4.Goldstein SR, Lumsden MA: Abnormal uterine bleeding in perimenopause. Climacteric. 2017, 20:414-420. 10.1080/13697137.2017.1358921
5.Whitaker L, Critchley HO: Abnormal uterine bleeding. Best Pract Res Clin Obstet Gynaecol. 2016, 34:54-65. 10.1016/j.bpobgyn.2015.11.012
6.Medical Advisory Secretariat: Thermal balloon endometrial ablation for dysfunctional uterine bleeding: an evidence-based analysis. Ont Health Technol Assess Ser. 2004, 4:1-89.
7.Goyal BK, Gaur I, Sharma S, Saha A, Das NK: Transvaginal sonography versus hysteroscopy in evaluation of abnormal uterine bleeding. Med J Armed Forces India. 2015, 71:120-125. 10.1016/j.mjafi.2014.12.001
8.Bingol B, Gunenc Z, Gedikbasi A, Guner H, Tasdemir S, Tiras B: Comparison of diagnostic accuracy of saline infusion sonohysterography, transvaginal sonography and hysteroscopy. J Obstet Gynaecol. 2011, 31:54-58. 10.3109/01443615.2010.532246
9.Abid M, Hashmi AA, Malik B, Haroon S, Faridi N, Edhi MM, Khan M: Clinical pattern and spectrum of endometrial pathologies in patients with abnormal uterine bleeding in Pakistan: need to adopt a more conservative approach to treatment. BMC Womens Health. 2014, 14:132. 10.1186/s12905-014-0132-7
10.Pai M, Chan A, Barr R: How I manage heavy menstrual bleeding. Br J Haematol. 2013, 162:721-729. 10.1111/bjh.12447
11.Fergusson RJ, Lethaby A, Shepperd S, Farquhar C: Endometrial resection and ablation versus hysterectomy for heavy menstrual bleeding. Cochrane Database Syst Rev. 2013, CD000329. 10.1002/14651858.CD000329.pub2
12.Abbott J, Hawe J, Hunter D: A double-blind randomized trial comparing the Cavaterm and the NovaSure endometrial ablation systems for the treatment of dysfunctional uterine bleeding. Fertil Steril. 2003, 80:203-208. 10.1016/s0015-0282(03)00549-1
13.Lethaby A, Hickey M, Garry R: Endometrial destruction techniques for heavy menstrual bleeding. Cochrane Database Syst Rev. 2005, CD001501. 10.1002/14651858.CD001501.pub2
14.Matteson KA, Boardman LA, Munro MG, Clark MA: Abnormal uterine bleeding: a review of patient-based outcome measures. Fertil Steril. 2009, 92:205-216. 10.1016/j.fertnstert.2008.04.023
15.Stepniewska AK, Baggio S, Clarizia R, et al.: Heat can treat: long-term follow-up results after uterine-sparing treatment of adenomyosis with radiofrequency thermal ablation in 60 hysterectomy candidate patients. Surg Endosc. 2022, 36:5803-5811. 10.1007/s00464-021-08984-z
16.Piecak K, Milart P: Hysteroscopic myomectomy. Prz Menopauzalny. 2017, 16:126-128. 10.5114/pm.2017.72757
17.Agdi M, Tulandi T: Endoscopic management of uterine fibroids. Best Pract Res Clin Obstet Gynaecol. 2008, 22:707-716. 10.1016/j.bpobgyn.2008.01.011
18.Camanni M, Bonino L, Delpiano EM, Ferrero B, Migliaretti G, Deltetto F: Hysteroscopic management of large symptomatic submucous uterine myomas. J Minim Invasive Gynecol. 2010, 17:59-65. 10.1016/j.jmig.2009.10.013
19.Lasmar RB, Lasmar BP, Celeste RK, da Rosa DB, de Batista Depes D, Lopes RG: A new system to classify submucous myomas: a Brazilian multicenter study. J Minim Invasive Gynecol. 2012, 19:575-580. 10.1016/j.jmig.2012.03.026
20.Donnez J, Polet R, Smets M, Bassil S, Nisolle M: Hysteroscopic myomectomy. Curr Opin Obstet Gynecol. 1995, 7:311-316.
21.van Dongen H, Janssen CA, Smeets MJ, Emanuel MH, Jansen FW: The clinical relevance of hysteroscopic polypectomy in premenopausal women with abnormal uterine bleeding. BJOG. 2009, 116:1387-1390. 10.1111/j.1471-0528.2009.02145.x
22.Abdollahi Fard S, Mostafa Gharabaghi P, Montazeri F, Mashrabi O: Hysteroscopy as a minimally invasive surgery, a good substitute for invasive gynecological procedures. Iran J Reprod Med. 2012, 10:377-382.
23.Solnik MJ, Munro MG: Indications and alternatives to hysterectomy. Clin Obstet Gynecol. 2014, 57:14-42. 10.1097/GRF.0000000000000010
24.Zupi E, Zullo F, Marconi D, Sbracia M, Pellicano M, Solima E, Sorrenti G: Hysteroscopic endometrial resection versus laparoscopic supracervical hysterectomy for menorrhagia: a prospective randomized trial. Am J Obstet Gynecol. 2003, 188:7-12. 10.1067/mob.2003.60
25.Abbott JA, Hawe J, Garry R: Quality of life should be considered the primary outcome for measuring success of endometrial ablation. J Am Assoc Gynecol Laparosc. 2003, 10:491-495. 10.1016/s1074-3804(05)60153-3