Точность тестирования на вирус папилломы человека высокого онкогенного риска с помощью теста Xpert ВПЧ на вагинальных самостоятельно собранных образцах сравнивали с образцами, отобранными врачом, в рамках исследования VALHUDES. Мы набрали 523 женщины в пяти бельгийских клиниках кольпоскопии, из которых 483 (средний возраст – 40 лет; интерквартильный размах – от 31 до 49 лет) были включены в основной анализ (226 были собраны с помощью щеточки Evalyn и 257 – с помощью Qvintip). Образцы из шейки матки были собраны с помощью Cervex-Brush. Результаты кольпоскопии и гистологии рассматривались как референтный стандарт. Анализ Xpert ВПЧ имел подобную точность для цервикальной интраэпителиальной неоплазии ≥2 на образцах, собранных самостоятельно, по сравнению с образцами, собранными врачом [относительная чувствительность 0,96 (95% ДИ, 0,91-1,02); и относительная специфичность 0,96 (95% ДИ, 0,89-1,04)]. Относительная точность несколько отличалась в зависимости от устройства для вагинального сбора [отношение чувствительности 0,98 (95% ДИ, 0,90-1,06) и 0,94 (95% ДИ, 0,87-1,02) для Evalyn и Qvintip соответственно; отношение специфичности 1,06 (95% ДИ, 0,95-1,19) и 0,88 (95% ДИ, 0,80-0,98) для Evalyn и Qvintip соответственно]. Не было выявлено разницы в значениях ПЦ между вагинальными и цервикальными образцами. Итак, чувствительность теста Xpert ВПЧ на цервикальную интраэпителиальную неоплазию ≥2 на вагинальных самостоятельно собранных образцах была подобной чувствительности образцов из шейки матки. Клиническая специфичность была ниже, чем на образцах, собранных врачом, когда самостоятельно собранные образцы были взяты с помощью Qvintip.
Скрининг на нуклеиновые кислоты типов вируса папилломы человека высокого онкогенного риска (ВПЧ), возбудителей рака шейки матки, является более эффективным, чем цитология, и поэтому рекомендован в последних руководствах по вторичной профилактике этой неоплазии.1, 2, 3 Более того, анализы на ВПЧ можно проводить на самостоятельно собранных образцах.4
Тестирование на ВПЧ с помощью самостоятельного забора образцов привлекло внимание всего мира благодаря своему потенциалу в охвате женщин, которые не участвуют в регулярном скрининге или не посещают его.5,6 Поскольку женщины, которые не проходят скрининг, остаются в группе риска развития рака шейки матки, охват этой группы населения стал приоритетной задачей здравоохранения во многих странах мира.6 Рандомизированные исследования продемонстрировали, что предложение самостоятельного забора образцов является более эффективным, чем традиционные приглашения в клинику для забора образцов из шейки матки медицинским работником.4,5 Кроме того, недавние исследования показали, что тестирование на ВПЧ на адекватно подготовленных вагинальных самостоятельно собранных образцах с помощью валидированного ПЦР-теста на основе ВПЧ имеет такую же точность выявления предрака шейки матки, как и тестирование на ВПЧ на образцах из шейки матки.5
Отсутствие международных стандартизированных протоколов по самостоятельному забору образцов вдохновило на разработку системы валидации анализов и устройств для забора образцов для тестирования на ВПЧ из влагалища и мочи (VALHUDES).7 Такие стандартизированные протоколы и валидация существуют для образцов шейки матки уже более десяти лет.8,9 Около десятка тестов на ДНК ВПЧ соответствуют международным критериям валидации на образцах, взятых врачами, и список клинически валидированных тестов постоянно расширяется.10 Подобные исследования необходимы для решения существующих проблем в рабочем процессе тестирования ВПЧ на основе самостоятельно собранных образцов.11 Предыдущие отчеты VALHUDES продемонстрировали, что два теста [Анализ на ВПЧ высокого онкогенного риска в режиме реального времени (Abbott Molecular Diagnostics, Дес-Плейнс, Иллинойс); и анализ на ВПЧ BD Onclarity (BD Diagnostics, Sparks, доктор медицинских наук)] имеют такую же точность выявления предрака шейки матки в вагинальных самостоятельно собранных образцах и в моче, взятой при первом мочеиспускании, как и в образцах, взятых врачами.12, 13, 14, 15.
В текущем отчете VALHUDES мы оцениваем аналитические и клинические характеристики теста Xpert ВПЧ (Xpert ВПЧ; Cepheid, Саннивейл, Калифорния), анализа на основе картриджа, который применяется в местах оказания медицинской помощи для самостоятельного забора вагинальных образцов.16
Материалы и методы
Структура исследования
Протокол VALHUDES (NCT03064087; https://clinicaltrials.gov, последний доступ 20 мая 2023 года)7 последний доступ 20 мая 2023 года)7 был разработан для оценки относительной клинической точности анализов на ВПЧ на самостоятельно собранных образцах из влагалища и мочи по сравнению с анализами на ВПЧ на образцах, взятых в клинике, в соответствии со Стандартами отчетности об исследовании диагностической точности, как описано выше.17 В период с декабря 2017 года по январь 2020 года 523 женщины были включены в исследование из-за имеющейся ВПЧ-инфекции или патологии шейки матки. Средний возраст участниц составлял 40 лет (интерквартильный размах от 31 до 49 лет). Набор проводился в пяти бельгийских клиниках кольпоскопии (университетские больницы Антверпена, Брюсселя, Гента и Льежа, а также общая региональная больница Heilig Hart Tienen). Критериями исключения из исследования были: беременность, гистерэктомия, отказ от участия, непонимание и неподписание информированного согласия. Все участники исследования подписали информированное согласие.
По прибытии в клинику кольпоскопии медсестры проинструктировали участниц исследования относительно самостоятельного забора вагинального образца с помощью вагинального устройства Qvintip (Aprovix AB, Стокгольм, Швеция) или щеточки Evalyn (Rovers Medical Devices, Осс, Нидерланды). Образцы из шейки матки собирались гинекологом с помощью Cervex-Brush (Медицинские приборы Rovers) в соответствии с европейскими рекомендациями.18 Клиники кольпоскопии в Брюсселе, Льеже и Tienen инициировали исследование, предложив участницам устройство Qvintip, тогда как клиники в Антверпене и Генте предложили щеточку Evalyn. Устройства для самостоятельного отбора образцов были заменены, когда было достигнуто почти половины объема выборки.
Сухие головки вагинальных щеточек хранились в клиниках кольпоскопии при комнатной температуре, тогда как образцы из шейки матки были ресуспендированы в 20 мл среды PreservCyt (Hologic, Inc., Бедфорд, штат Массачусетс) после отбора гинекологом. Оба образца были отправлены в лабораторию Algemeen Medisch (Антверпен, Бельгия) для хранения и дальнейшей обработки в течение максимум 6 дней после сбора. По прибытии в лабораторию Algemeen Medisch, сухие вагинальные образцы были помещены в 20 мл среды PreservCyt. Все образцы хранили при 4°C максимум до 3 месяцев, после чего вортексировали в течение 15-20 секунд и распределяли на аликвоты объемом 1 мл, которые замораживали при -80°C (Biobank; BB190002).
Тестирование на ВПЧ
Тестирование на ВПЧ было проведено на 499 парных образцах путем переноса 1 мл аликвоты цервикального и вагинального образцов непосредственно в картридж Xpert. Картридж содержит реагенты для экстракции ДНК и праймеры с зондами для амплификации и выявления ВПЧ. Xpert ВПЧ основан на мультиплексной ПЦР в реальном времени, нацеленной на онкогены E6 и E7 14 генотипов ВПЧ. Амплификация проводится в пяти флуоресцентных каналах для выявления следующих групп: ВПЧ 16, ВПЧ 18/45, ВПЧ 31/33/35/52/58, ВПЧ 51/59 и ВПЧ 39/56/66/68. Интерпретация результатов выполняется автоматически с помощью программного обеспечения GeneXpert. Гидроксиметилбилансинтазу человека определяли как контроль валидности и адекватности образцов и амплификационной способности ДНК. Положительность ВПЧ определялась, если отсечение ПЦ составляло ≤40 для ВПЧ 16 и ВПЧ 18/45, и ≤38 для ВПЧ 31/35/33/52/58, ВПЧ 51/59 и ВПЧ 39/68/56/66. Образцы считались адекватными, если гидроксиметилбилансинтаза была ≤38 ПЦ.19 Те же самые границы были применены для вагинальных и цервикальных образцов.
Для оценки клинической точности авторы определили тестирование на ВПЧ на вагинальных самостоятельно собранных образцах как индексный тест, а на цервикальных образцах – как компаратор, тогда как для референтного стандарта использовали результаты кольпоскопии и гистологии. Если биопсию не проводили, а кольпоскопия была удовлетворительной и не выявила подозрительных находок, результат классифицировали как цервикальную интраэпителиальную неоплазию (ЦИН) <2.
Статистический анализ
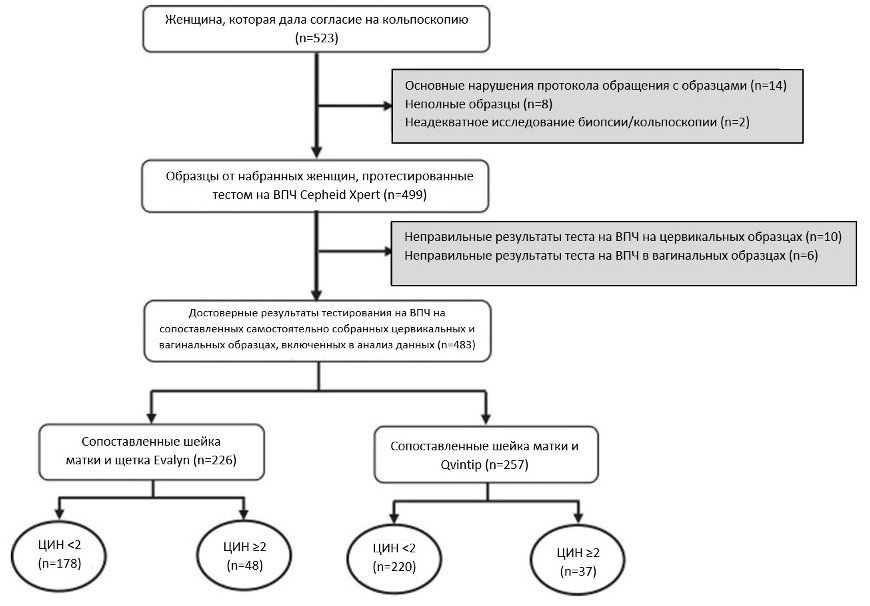
Всего в основной анализ было включено 483 женщины (средний возраст – 40 лет; интерквартильный размах – от 31 до 49 лет). Двадцать четыре женщины были исключены из исследования из-за серьезных нарушений протокола, как описано в других источниках.12,14 Шесть цервикальных и пять вагинальных образцов были повторно протестированы из-за системной ошибки, из которых один вагинальный образец остался недействительным после повторного тестирования. Десять цервикальных и пять вагинальных образцов были исключены из-за отсутствия β-глобина в соответствующих образцах (Рисунок 1). Один вагинальный образец был исключен из-за неудачного повторного теста. Абсолютную и относительную эффективность тестирования на ВПЧ оценивали для всей исследуемой популяции (N = 483) и для женщин в возрасте ≥30 лет (N = 386). Среди участниц 47% собирали вагинальный образец с помощью щеточки Evalyn (226/483) и 53% собирали вагинальный образец с помощью Qvintip (257/483). Характеристики исследуемой популяции были описаны ранее.12,15
Рисунок 1 Блок-схема образцов, включенных в исследование VALHUDES, протестированных с помощью теста Xpert ВПЧ. Серым цветом обозначены исключенные образцы. Причины исключения образцов перед тестированием на вирус папилломы человека (ВПЧ) были подробно описаны ранее.12 ЦИН – цервикальная интраэпителиальная неоплазия.
Авторы использовали тест МакНемара и парные 95% ДИ для сравнения различий между цервикальными и вагинальными образцами. Для оценки соответствия между образцами использовали коэффициент Каппа Коэна со следующей классификацией: 0,00-0,19 – плохая; 0,20-0,39 – удовлетворительная; 0,40-0,59 – умеренная; 0,60-0,79 – хорошая; и 0,80-1,00 – отличная согласованность. Согласованность и коэффициент Каппа Коэна оценивали для общей позитивности ВПЧ и групп генотипирования, как определено в анализе. Различия в средних значениях ПЦ между сопоставимыми цервикальными и вагинальными образцами, а также между результатами ЦИН ≥2 и ЦИН <2 оценивали с помощью t-критерия. Статистический анализ проводили с помощью программы Stata 16.1 (StataCorp LLC, Колледж-Стейшн, Техас).
Этическое одобрение
Исследование VALHUDES (NCT03064087) было одобрено центральным Комитетом по вопросам этики Университетской больницы Антверпена/Университета Антверпена (B300201733869) и локальными комитетами по вопросам этики всех других вовлеченных центров. Исследование проводилось в соответствии с Хельсинкской декларацией. Письменное информированное согласие было получено от всех участников исследования перед включением в него.
Результаты
Клиническая точность
Клиническая чувствительность Xpert ВПЧ для выявления ЦИН ≥2 в вагинальных самостоятельно собранных образцах с помощью щеточки Evalyn или Qvintip была подобной образцам из шейки матки (отношение 0,96; 95% ДИ, 0,91-1,02); однако чувствительность для выявления ЦИН 3 была на 9% ниже (отношение 0,91; 95% ДИ, 0,82-0,998). Специфичность для ЦИН <2 в вагинальных самостоятельных образцах не отличалась от цервикальных образцов (отношение 0,96; 95% ДИ, 0,89-1,04) (Таблица 1).
Таблица 1 Относительная чувствительность и специфичность теста Cepheid Xpert на ВПЧ на образцах, собранных врачом, по сравнению с самостоятельно собранными образцами
| Переменная | Относительная чувствительность (95% ДИ) ЦИН ≥2 | Относительная чувствительность (95% ДИ) ЦИН 3 | Относительная специфичность (95% ДИ) ЦИН <2 |
| Общее количество исследуемых (n = 483) | |||
| Вагинальная (E + Q) | 0.96 (0.91–1.02) | 0.91 (0.82–0.998) | 0.96 (0.89–1.04) |
| Evalyn Brush | 0.98 (0.90–1.06) | 0.91 (0.80–1.04) | 1.06 (0.95–1.19) |
| Qvintip | 0.94 (0.87–1.02) | 0.90 (0.78–1.04) | 0.88 (0.80–0.98) |
| Женщины в возрасте ≥30 лет (n = 386) | |||
| Вагинальная (E + Q) | 0.95 (0.87–1.03) | 0.88 (0.77–0.997) | 0.95 (0.88–1.03) |
| Evalyn | 0.97 (0.86–1.09) | 0.87 (0.71–1.06) | 1.06 (0.95–1.17) |
| Qvintip | 0.93 (0.83–1.03) | 0.88 (0.74–1.05) | 0.87 (0.77–0.98) |
ЦИН, цервикальная интраэпителиальная неоплазия; E + Q, образцы, собранные с помощью Evalyn Brush и Qvintip в сочетании.
При стратификации анализа по вагинальному устройству чувствительность для ЦИН ≥2 Xpert ВПЧ на образцах Evalyn Brush (соотношение 0,98; 95% ДИ, 0,90-1,06) и Qvintip (соотношение 0,94; 95% ДИ, 0,87-1,02) также была подобной чувствительности для образцов из шейки матки. Отношение относительной клинической чувствительности Xpert для ЦИН ≥2 на щеточке Evalyn к Qvintip составляло 1,04 (95% ДИ, 0,88-1,22; несравнимое сопоставление). Специфичность Xpert ВПЧ на образцах Evalyn Brush не отличалась от цервикальных образцов (соотношение 1,06; 95% ДИ, 0,95-1,19), тогда как на образцах Qvintip специфичность была значительно ниже (соотношение 0,88; 95% ДИ, 0,80-0,98). Соотношение специфичности щеточки Evalyn и Qvintip составило 1,12 (95% ДИ, 0,89-1,39; несравнимое сравнение).
При ограничении анализа женщинами в возрасте ≥30 лет точность была несколько ниже по сравнению с общей популяцией (Таблица 1).
Аналитическая эффективность
Xpert ВПЧ одновременно обнаружил ВПЧ в 56% (270/483) образцов, а 33% образцов были одновременно отрицательными на ВПЧ. Из этих образцов 5% (24/483) были положительными только на цервикальных образцах и 6% (28/483) были положительными только на вагинальных самостоятельно собранных образцах. Авторы наблюдали от умеренной до отличной общей и специфической для каждого типа теста согласованность между цервикальными и вагинальными образцами со значениями Каппа Коэна от 0,67 до 0,93 (Таблица 2).
Таблица 2 Общее и типоспецифическое сходство между цервикальным и вагинальным (Evalyn Brush + Qvintip) образцами
| Образец | Тип ВПЧ | +/+ | +/− | −/+ | −/− | Согласованность, % | Коэффициент Каппа Коэна (95% ДИ) |
| Общее количество исследуемых (n = 483) | врВПЧ | 270 | 24 | 28 | 161 | 89.2 | 0.773 (0.715–0.831) |
| ВПЧ 16 | 72 | 6 | 11 | 394 | 96.5 | 0.873 (0.814–0.932) | |
| ВПЧ 18/45 | 37 | 9 | 3 | 434 | 97.5 | 0.847 (0.762–0.932) | |
| ВПЧ 31/33/35/52/58 | 126 | 13 | 14 | 330 | 94.4 | 0.864 (0.814–0.914) | |
| ВПЧ 51/59 | 53 | 10 | 10 | 410 | 95.9 | 0.817 (0.740–0.895) | |
| ВПЧ 39/56/66/68 | 83 | 13 | 18 | 369 | 93.6 | 0.802 (0.736–0.869) | |
| ЦИН ≥2 (n = 85) | врВПЧ | 74 | 4 | 1 | 6 | 94.1 | 0.674 (0.409–0.939) |
| ВПЧ 16 | 39 | 2 | 0 | 44 | 97.7 | 0.953 (0.888–1.000) | |
| ВПЧ 18/45 | 7 | 1 | 1 | 76 | 97.7 | 0.862 (0.674–1.000) | |
| ВПЧ 31/33/35/52/58 | 33 | 2 | 1 | 49 | 96.5 | 0.927 (0.846–1.000) | |
| ВПЧ 51/59 | 12 | 1 | 1 | 71 | 97.7 | 0.909 (0.785–1.000) | |
| ВПЧ 39/56/66/68 | 17 | 2 | 5 | 61 | 91.8 | 0.775 (0.618–0.933) | |
| ЦИН <2 (n = 398) | врВПЧ | 196 | 20 | 27 | 155 | 88.2 | 0.761 (0.697–0.825) |
| ВПЧ 16 | 33 | 4 | 11 | 350 | 96.2 | 0.794 (0.693–0.895) | |
| ВПЧ 18/45 | 30 | 8 | 2 | 358 | 97.5 | 0.843 (0.749–0.938) | |
| ВПЧ 31/33/35/52/58 | 93 | 11 | 13 | 281 | 94.0 | 0.845 (0.785–0.905) | |
| ВПЧ 51/59 | 41 | 9 | 9 | 339 | 95.5 | 0.794 (0.702–0.886) | |
| ВПЧ 39/56/66/68 | 66 | 11 | 13 | 308 | 94.0 | 0.813 (0.755–0.870) |
Коэффициент согласованности Каппа Коэна между вагинальными и цервикальными образцами представлен следующим образом: от 0,00 до 0,20 – плохая; от 0,21 до 0,40 – удовлетворительная; от 0,41 до 0,60 – умеренная; от 0,61 до 0,80 – хорошая; от 0,81 до 1,00 – отличная.
+/+, положительный на вагинальных и цервикальных образцах; +/-, положительный только на цервикальных образцах; -/+, положительный только на вагинальных образцах; -/-, отрицательный на обоих типах образцов; ЦИН, цервикальная интраэпителиальная неоплазия; ВПЧ, вирус папилломы человека; врВПЧ, ВПЧ высокого онкогенного риска.
Средние значения ПЦ для амплификации ВПЧ и ДНК человека были ниже для общего количества ВПЧ и ВПЧ 16 у женщин с ЦИН ≥2 по сравнению с ЦИН <2 в образцах шейки матки. Не было выявлено разницы в средних значениях ПЦ в зависимости от статуса заболевания в вагинальных образцах, а также не наблюдалось разницы в средних значениях ПЦ между цервикальными и вагинальными образцами.
Обсуждение
В этом отчете VALHUDES мы продемонстрировали подобные аналитические и клинические показатели Xpert ВПЧ для ЦИН ≥2 при самостоятельно собранных вагинальных образцах по сравнению с образцами, отобранными врачом. В соответствии с нашими предыдущими выводами, мы наблюдали, что клинические результаты тестирования на ВПЧ отличаются в зависимости от устройства для забора вагинальных образцов. Xpert на щеточке Evalyn был аналогично чувствительным, но более специфичным, чем на Qvintip. В первых отчетах VALHUDES оценивали точность теста на ВПЧ высокого онкологического риска в режиме реального времени и BD Onclarity ВПЧ анализ. Оба теста показали подобную чувствительность для выявления ЦИН ≥2 в вагинальных самостоятельно собранных образцах по сравнению с цервикальными образцами, отобранными врачом, хотя тест на ВПЧ высокого онкологического риска в режиме реального времени требовал оптимизации отсечения числа циклов для достижения подобной чувствительности на вагинальных самостоятельно собранных образцах по сравнению с образцами, собранными врачом.12, 13, 14, 15.
Разница в точности между Evalyn и Qvintip может быть объяснена конструкцией устройства. Щеточка Evalyn имеет большую мягкую головку для сбора, похожую на щеточку, тогда как Qvintip имеет маленькую головку из твердого пластика с несколькими боковыми канавками для сбора клеток цервикально-вагинальных клеток. Поэтому щеточка Evalyn может собирать больше отшелушенных клеток шейки матки по сравнению с Qvintip, а следовательно, и точность воздействия будет выше.
Было опубликовано много статей об эффективности тестирования на ВПЧ на самостоятельно собранных образцах. В обновленный мета-анализ, проведенный Arbyn и др. 5 , было включено 56 исследований точности. Эта работа продемонстрировала такую же высокую точность тестов на ВПЧ для выявления предрака шейки матки на вагинальных самостоятельно собранных образцах, как и на образцах, собранных врачом, если используемый тест базировался на валидированном ПЦР-анализе, тогда как тесты на основе усиления сигнала были менее чувствительными при самостоятельном заборе образцов. Другой мета-анализ статистики согласования, который включал 26 исследований, объединивших более 10 000 участников, показал 89% согласования с коэффициентом 0,72 κ тестов на ВПЧ на основе ПЦР на вагинальных самостоятельно собранных образцах по сравнению с цервикальными образцами. Эти данные свидетельствуют о том, что если валидированные ПЦР-тесты на ВПЧ на цервикальных и вагинальных образцах продемонстрируют высокую согласованность и значение коэффициента Каппа Коэна с новыми устройствами/носителями, их можно будет распространить на альтернативные устройства и/или носители. 20 Такой подход может облегчить валидацию новых комбинаций тестов на ВПЧ и устройств или носителей для самостоятельного забора образцов и ускорить их внедрение в рамках скрининговых программ.
Xpert ВПЧ был валидирован для скрининга рака шейки матки на цервикальных образцах, хранящихся в PreservCyt в рамках VALGENT-2. 10,16 Анализ Xpert также был оценен на цервикальных образцах 535 женщин, живущих с ВИЧ, и 586 женщин, не живущих с ВИЧ, отобранных в контексте скрининга и кольпоскопии в клиниках в Южной Африке.21 Авторы модифицировали пороговые значения положительности ВПЧ, чтобы повысить специфичность теста в группе женщин, живущих с ВИЧ, поскольку распространенность ВПЧ и вирусная нагрузка у этих женщин выше, чем в общей популяции. Исследование показало, что для отдельных групп онкологического риска могут потребоваться скорректированные пороговые значения, чтобы найти оптимальный баланс между чувствительностью и специфичностью. Ранее мы использовали подобный апостериорный подход к оптимизации пороговых значений на собственных образцах; однако в текущем исследовании VALHUDES оптимизация пороговых значений не была необходимой, поскольку точность на самостоятельно собранных образцах по сравнению с клиническими образцами была подобной.12,14 Saidu и др. 22 аналогично оценивали тест Xpert на самостоятельно собранных образцах, включив более 1000 женщин из популяций скрининга и кольпоскопии в Южной Африке, как это рекомендовано для исследований диагностической точности. Xpert оказался одинаково чувствительным к самостоятельно собранным вагинальным образцам по сравнению с цервикальными образцами, взятыми врачом. Это совпадает с нашими результатами, но о более низкой специфичности сообщили Saidu и др. 22 в южноафриканском исследовании женщины самостоятельно собирали образцы с помощью стандартного тампона, который помещали в 4 мл раствора PreservCyt. В исследовании VALHUDES два использованные вагинальные устройства (Evalyn и Qvintip) ресуспендировали в 20 мл раствора PreservCyt. Авторы из Южной Африки сообщили, что меньший объем ресуспензии мог привести к более высокой концентрации вируса и, следовательно, к более низкой специфичности.
Питательные среды PreservCyt и SurePath одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов для скрининга рака шейки матки на основе цитологического исследования. PreservCyt и SurePath были разработаны для сохранения клеток, что позволяет проводить цитологическую интерпретацию, и содержат метанол и этанол соответственно, а потому являются относительно дорогими для транспортировки. По данным нашего исследования VALHUDES, тестирование на ВПЧ на вагинальных образцах с использованием PreservCyt показало такую же точность, как и результаты тестирования на ВПЧ на цервикальных образцах, собранных врачом, с использованием той же среды. Поскольку тесты на ВПЧ предназначены для выявления вирусной ДНК или РНК, спиртовые растворы не являются необходимыми для сохранения ДНК ВПЧ. Кроме того, высокая стоимость этих сред побуждает страны с ограниченными ресурсами искать более дешевые альтернативные решения. Поэтому для получения достаточных доказательств эффективности альтернативных носителей необходимы расширенные подходы к валидации. Хотя заинтересованность участников скрининга в использовании самостоятельно собранных образцов возросла, все еще нужны дополнительные исследования для получения необходимых знаний о влиянии различных преаналитических и аналитических параметров на клиническую точность.11,23
Xpert ВПЧ был протестирован на семи сериях разведений (от одного до семи имитированных 10-кратных разведений) искусственно подготовленной человеческой и вирусной ДНК из клеточных линий ВПЧ 16, ВПЧ 18 и ВПЧ 31, хранившихся в пяти различных транспортных средах.24 Раствор PreservCyt сравнивали с четырьмя безалкогольными растворами: фосфатно-буферным физиологическим раствором (Thermo Fisher Scientific, Уолтем, Массачусетс, США), Sigma Virocult (Medical Wire and Equipment, Великобритания), MSwab (Copan, Италия), и Xpert Transport Media (Cepheid). ДНК человека была обнаружена во всех средах и во всех концентрациях. Раствор MSwab был единственной средой, где ДНК ВПЧ была обнаружена в пятом 10-кратном разведении во всех трех клеточных линиях, и, следовательно, может быть альтернативой PreservCyt.24 Тем не менее, необходимы дальнейшие исследования для тестирования таких сред на реальных образцах, полученных от пациента, и образцах, собранных врачами. Сочетание альтернативных транспортных носителей с Xpert ВПЧ может быть более дешевым и эффективным подходом для стран с ограниченными ресурсами. Тестирование на ВПЧ с помощью Xpert проводится с использованием одного интегрированного картриджа, который содержит реагенты для экстракции ДНК, а также праймеры и зонды для амплификации и выявления ДНК ВПЧ.20,21 Для проведения тестирования на ВПЧ необходимы ограниченные ресурсы как с точки зрения лабораторных возможностей, так и с точки зрения человеческого потенциала; поэтому Xpert ВПЧ может представлять особый интерес для отдаленных стран с ограниченными ресурсами, учитывая его пригодность для проведения тестирования в местах оказания медицинской помощи.
Одним из ограничений исследования VALHUDES является то, что женщин набирали в клиниках, где проводят кольпоскопию, что привело к высокому показателю положительных результатов на ВПЧ и низкой абсолютной специфичности.12, 13, 14, 15 Эти данные согласуются с другими подобными исследованиями диагностической точности, проведенными в условиях кольпоскопии.5 Однако было продемонстрировано, что относительная точность тестирования на ВПЧ на основе самостоятельно собранных образцов по сравнению с образцами, собранными врачом, является сопоставимой в группах наблюдения и скрининга.5 Таким образом, относительная точность должна рассматриваться как устойчивый параметр для подобных исследований точности диагностирования. Сильные стороны и ограничения VALHUDES были подробно описаны ранее.12, 13, 14, 15
Заключение
Тестирование на врВПЧ с помощью Xpert ВПЧ на самостоятельно собранных вагинальных образцах оказалось таким же точным для выявления предрака, как и на образцах шейки матки, собранных врачом. На точность может влиять устройство для самостоятельного забора образцов.
Ссылки на источники
- Arbyn M, Ronco G, Anttila A, Meijer CJLM, Poljak M, Ogilvie G, Koliopoulos G, Naucler P, Sankaranarayanan R, Peto J: Evidence regarding human papillomavirus testing in secondary prevention of cervical cancer. Vaccine 2012, 30:F88eF99 Q21
- Arbyn M, Gultekin M, Morice P, Nieminen P, Cruickshank M, Poortmans P, Kelly D, Poljak M, Bergeron C, Ritchie D, Schmidt D, Kyrgiou M, Van den Bruel A, Bruni L, Basu P, Bray F, Weiderpass E: The European response to the WHO call to eliminate cervical cancer as a public health problem. Int J Cancer 2021, 148:277e284
- Bouvard V, Wentzensen N, Mackie A, Berkhof J, Brotherton J, GiorgiRossi P, Kupets R, Smith R, Arrossi S, Bendahhou K, Canfell K, Chirenje ZM, Chung MH, del Pino M, de Sanjosé S, Elfström M, Franco EL, Hamashima C, Hamers FF, Herrington CS, Murillo R, Sangrajrang S, Sankaranarayanan R, Saraiya M, Schiffman M, Zhao F, Arbyn M, Prendiville W, Indave Ruiz BI, Mosquera-Metcalfe I, Lauby-Secretan B: The IARC perspective on cervical cancer screening. N Engl J Med 2021, 385:1908e1918
- Arbyn M, Verdoodt F, Snijders PJ, Verhoef VM, Suonio E, Dillner L, Minozzi S, Bellisario C, Banzi R, Zhao FH, Hillemanns P, Anttila A: Accuracy of human papillomavirus testing on self-collected versus clinician-collected samples: a meta-analysis. Lancet Oncol 2014, 15: 172e183
- Arbyn M, Smith SB, Temin S, Sultana F, Castle P: Detecting cervical precancer and reaching underscreened women by using HPV testing on self samples: updated meta-analyses. BMJ 2018, 363:k4823
- Serrano B, Ibáñez R, Robles C, Peremiquel-Trillas P, de Sanjosé S, Bruni L: Worldwide use of HPV self-sampling for cervical cancer screening. Prev Med 2022, 154:106900
- Arbyn M, Peeters E, Benoy I, Vanden Broeck D, Bogers J, De Sutter P, Donders G, Tjalma W, Weyers S, Cuschieri K, Poljak M, Bonde J, Cocuzza C, Zhao FH, Van Keer S, Vorsters A: VALHUDES: a protocol for validation of human papillomavirus assays and collection devices for HPV testing on self-samples and urine samples. J Clin Virol 2018, 107:52e56
- Meijer CJLM, Berkhof J, Castle PE, Hesselink AT, Franco EL, Ronco G, Arbyn M, Bosch FX, Cuzick J, Dillner J, Heideman DAM, Snijders PJF: Guidelines for human papillomavirus DNA test requirements for primary cervical cancer screening in women 30 years and older. Int J Cancer 2009, 124:516e520
- Arbyn M, Depuydt C, Benoy I, Bogers J, Cuschieri K, Schmitt M, Pawlita M, Geraets D, Heard I, Gheit T, Tommasino M, Poljak M, Bonde J, Quint W: VALGENT: a protocol for clinical validation of human papillomavirus assays. J Clin Virol 2016, 76:S14eS21
- Arbyn M, Simon M, Peeters E, Xu L, Meijer C, Berkhof J, Cuschieri K, Bonde J, Ostrbenk Vanlencak A, Zhao FH, Rezhake R, Gultekin M, Dillner J, de Sanjosé S, Canfell K, Hillemanns P, Almonte M, Wentzensen N, Poljak M: 2020 List of human papillomavirus assays suitable for primary cervical cancer screening. Clin Microbiol Infect 2021, 27:1083e1095
- Arbyn M, Latsuzbaia A, Castle PE, Sahasrabuddhe VV, Broeck DV: HPV testing of self-samples: influence of collection and sample handling procedures on clinical accuracy to detect cervical precancer. Lancet Reg Health Eur 2022, 14:100332
- Van Keer S, Peeters E, Vanden Broeck D, De Sutter P, Donders G, Doyen J, Tjalma WAA, Weyers S, Vorsters A, Arbyn M: Clinical and analytical evaluation of the RealTime high risk HPV assay in Colli-Pee collected first-void urine using the VALHUDES protocol. Gynecol Oncol 2021, 162:575e583
- Van Keer S, Latsuzbaia A, Vanden Broeck D, De Sutter P, Donders G, Doyen J, Tjalma WAA, Weyers S, Arbyn M, Vorsters A: Analytical and clinical performance of extended HPV genotyping with BD Onclarity HPV Assay in home-collected first-void urine: a diagnostic test accuracy study. J Clin Virol 2022, 155:105271
- Latsuzbaia A, Vanden Broeck D, Van Keer S, Weyers S, Tjalma WAA, Doyen J, Donders G, De Sutter P, Vorsters A, Peeters E, Arbyn M: Clinical performance of the realtime high risk HPV assay on self-collected vaginal samples within the VALHUDES framework. Microbiol Spectr 2022, 10:e0163122
- Latsuzbaia A, Vanden Broeck D, Van Keer S, Weyers S, Donders G, Doyen J, Tjalma W, De Sutter P, Peeters E, Vorsters A, Arbyn M: Validation of BD Onclarity HPV assay on vaginal self-samples versus cervical samples using the VALHUDES protocol. Cancer Epidemiol Biomarkers Prev 2022, 31:2177e2184
- Cuschieri K, Geraets D, Cuzick J, Cadman L, Moore C, Vanden Broeck D, Padalko E, Quint W, Arbyn M: Performance of a cartridgebased assay for detection of clinically significant human papillomavirus (HPV) infection: lessons from VALGENT (Validation of HPV Genotyping Tests). J Clin Microbiol 2016, 54:2337e2342
- Cohen JF, Korevaar DA, Altman DG, Bruns DE, Gatsonis CA, Hooft L, Irwig L, Levine D, Reitsma JB, de Vet HC, Bossuyt PM: STARD 2015 guidelines for reporting diagnostic accuracy studies: explanation and elaboration. BMJ Open 2016, 6:e012799
- Arbyn M, Herbert A, Schenck U, Nieminen P, Jordan J, McGoogan E, Patnick J, Bergeron C, Baldauf JJ, Klinkhamer P, Bulten J, MartinHirsch P: European guidelines for quality assurance in cervical cancer screening: recommendations for collecting samples for conventional and liquid-based cytology. Cytopathology 2007, 18:133e139
- Castle PE, Smith KM, Davis TE, Schmeler KM, Ferris DG, Savage AH, Gray JE, Stoler MH, Wright TC Jr, Ferenczy A, Einstein MH: Reliability of the Xpert HPV assay to detect high-risk human papillomavirus DNA in a colposcopy referral population. Am J Clin Pathol 2015, 143:126e133
- Arbyn M, Castle PE, Schiffman M, Wentzensen N, HeckmanStoddard B, Sahasrabuddhe VV: Meta-analysis of agreement/concordance statistics in studies comparing self- vs cliniciancollected samples for HPV testing in cervical cancer screening. Int J Cancer 2022, 151:308e312
- Kuhn L, Saidu R, Boa R, Tergas A, Moodley J, Persing D, Campbell S, Tsai W-Y, Wright TC, Denny L: Clinical evaluation of modifications to a human papillomavirus assay to optimise its utility for cervical cancer screening in low-resource settings: a diagnostic accuracy study. Lancet Glob Health 2020, 8:e296ee304
- Saidu R, Kuhn L, Tergas A, Boa R, Moodley J, Svanholm-Barrie C, Persing D, Campbell S, Tsai WY, Wright TC, Denny L: Performance of Xpert HPV on self-collected vaginal samples for cervical cancer screening among women in South Africa. J Low Genit Tract Dis 2021, 25:15e21
- Arbyn M, Costa S, Latsuzbaia A, Kellen E, Girogi Rossi P, Cocuzza CE, Basu P, Castle PE: HPV-based cervical cancer screening on self-samples in the Netherlands: challenges to reach women and test performance questions. Cancer Epidemiol Biomarkers Prev 2023, 32: 159e163
- Badman SG, Vallely AJ, Pardo C, Mhango LP, Cornall AM, Kaldor JK, Whiley D: A comparison of ThinPrep against four nonvolatile transport media for HPV testing at or near the point of care. Pathology 2021, 53:264e266