Авторы: Ji Yoon Yoon, Nikhil A. Kumta, Michelle Kang Kim
Содержание:
- Вступление
- Нейроэндокринные опухоли двенадцатиперстной кишки
- Эндоскопическое УЗИ
- Эндоскопическая резекция
- Нейроэндокринные опухоли тощей и подвздошной кишки
- Видеокапсульная эндоскопия
- Баллонная энтероскопия
- Выводы
Вступление
Нейроэндокринные опухоли (НЭО) желудочно-кишечной системы представляют собой гетерогенную группу новообразований, поведение которых различается в зависимости от первичной локализации, гистологии и стадии.
Анализ популяционных регистров, таких как Программа наблюдения, эпидемиологии и конечных результатов (SEER), продемонстрировал рост заболеваемости НЭО, так что по состоянию на 2000 г. НЭО были наиболее распространенным злокачественным новообразованием тонкой кишки, обогнав аденокарциному.
НЭО тонкой кишки (НЭО-ТК) составляют примерно 30% НЭО желудочно-кишечного тракта. В дополнение к их растущей частоте, НЭО-ТК, вероятно, будут даже более распространенными, чем зафиксировано в реестре SEER, что может исключить более мелкие, более локализованные НЭО, которые часто считаются доброкачественными.
НЭО часто бессимптомны и диагностируются случайно при визуализации в поперечном сечении или эндоскопии по другим показаниям. Клиническая картина НЭО-ТК часто коварна и неспецифична, с такими симптомами, как дискомфорт в животе и диарея, которые проявляются за годы до постановки диагноза.
Типичный карциноидный синдром встречается редко даже при НЭО-ТК: у 26% пациентов наблюдается диарея, у 13% — гиперемия и у 2% — бронхоконстрикция. До четверти пациентов могут иметь кишечную непроходимость.
НЭО-ТК классифицируются по стадиям в соответствии с системой стадирования TNM Американского объединенного комитета по раку (AJCC) (таблица 1) и классифицируются в соответствии с системой оценок Европейского общества нейроэндокринных опухолей/Всемирной организации здравоохранения (таблица 2) для прогнозирования.
Таблица 1:
| Двенадцатиперстная кишка (исключая фатерову ампулу) | Тощая и подвздошная кишка | |
| Первичная опухоль (Т) | ||
| Тх | Первичная опухоль не может быть оценена | Первичная опухоль не может быть оценена |
| Т0 | Нет признаков первичной опухоли | Нет признаков первичной опухоли |
| Т1 | Вовлечена только слизистая или подслизистая оболочка на ≤1 см. | Вовлечена только собственная пластинка или подслизистая оболочка на ≤1 см. |
| Т2 | Распространяется на собственную мышечную оболочку или составляет >1 см | Распространяется на собственную мышечную оболочку или составляет >1 см |
| Т3 | Поражает поджелудочную железу или перипанкреатическую жировую ткань | Прорастает через собственную мускулатуру в подсерозную ткань, не проникая в вышележащую серозную оболочку. |
| Т4 | Прорастает в висцеральную брюшину (серозную оболочку) или другие органы | Прорастает в висцеральную брюшину (серозную оболочку) или другие органы или соседние структуры |
| Регионарный лимфатический узел (N) | ||
| Nx | Регионарные лимфатические узлы не могут быть оценены | Регионарные лимфатические узлы не могут быть оценены |
| N0 | Отсутствие поражения регионарных лимфатических узлов | Отсутствие поражения регионарных лимфатических узлов |
| N1 | Вовлечение регионарных лимфатических узлов | Метастазы в регионарные лимфатические узлы менее 12 узлов |
| N2 | Н/Д | Н/Д |
| Отдаленные метастазы (М) | ||
| M0 | Отсутствие отдаленных метастазов | Отсутствие отдаленных метастазов |
| M1 | Отдаленные метастазы | Отдаленные метастазы |
| M1a | Ограничены печенью | Ограничены печенью |
| M1b | По крайней мере, в одном внепеченочном месте | По крайней мере, в одном внепеченочном месте |
| M1c | Печеночные и внепеченочные метастазы | Печеночные и внепеченочные метастазы |
| Группы прогностических стадий AJCC | ||
| Стадия 1 | T1, N0, M0 | T1, N0, M0 |
| Стадия 2 | T2, N0, M0 | T2, N0, M0 |
| T3, N0, M0 | T3, N0, M0 | |
| Стадия 3 | T4, N0, M0 | Любая T, N1/N2, M0 |
| Любая T, N1, M0 | T4, N0, M0 | |
| Стадия 4 | Любая T, любой N, M1 | Любая T, любой N, M1 |
Таблица 2:
| Митотический индекс (митозы/HPF) | Индекс Ki-67 (%) | |
| GX | Оценка не может быть проведена | Оценка не может быть проведена |
| G1 | <2 | <3 |
| G2 | 2-20 | 3-20 |
| G3 | >20 | >20 |
Оценка НЭО часто включает комбинацию биохимических, визуализационных и эндоскопических методов. Биохимические маркеры могут включать гастрин (дуоденальные НЭО), 5-гидроксииндолуксусную кислоту (для тощекишечных/подвздошных НЭО) и хромогранин А, тогда как визуализация может включать компьютерную томографию (КТ), магнитно-резонансную томографию (МРТ) и сцинтиграфию с радиоактивной меткой, такую как 68Ga- дотация ПЭТ/КТ.
При эндоскопии НЭО-ТК обычно выглядят как круглые, иногда тонкие субэпителиальные поражения. Эндоскопические методы, такие как видеокапсульная эндоскопия и эндоскопическое ультразвуковое исследование (ЭУЗИ), могут быть полезны в диагностике НЭО, в то время как передовые эндоскопические методы, такие как эндоскопическая резекция слизистой оболочки (ЭРСО) и эндоскопическая подслизистая диссекция (ЭПСД), могут стать краеугольным камнем лечения НЭО-ТК. В этом обзоре мы стремились подчеркнуть роль эндоскопических методов в диагностике и лечении НЭО-ТК.
Нейроэндокринные опухоли двенадцатиперстной кишки
Дуоденальные НЭО часто обнаруживаются случайно при эндоскопии верхних отделов ЖКТ. Хотя они чаще всего являются нефункционирующими опухолями (то есть не связаны с клиническим синдромом), НЭО двенадцатиперстной кишки также могут быть связаны с синдромом Золлингера-Эллисона с его клинической триадой рефлюкса, язвенной болезни и диареи. Поскольку двенадцатиперстная кишка находится в пределах досягаемости обычной эндоскопии, ее расположение позволяет проводить гистологическую оценку, оценку стадии опухоли и даже лечебную эндоскопическую резекцию.
Эндоскопическое УЗИ
Размер и глубина инвазии являются важными факторами риска, связанными с лимфатическими узлами и отдаленными метастазами. Эндоскопическое ультразвуковое исследование (ЭУЗИ) предлагает метод точной оценки размера и глубины инвазии НЭО двенадцатиперстной кишки перед резекцией, что необходимо для определения метода резекции: эндоскопического или хирургического.
При поражениях размером менее 10 мм риск вовлечения лимфатических узлов или отдаленных метастазов и рецидивов низкий. Если инвазия собственной мышечной оболочки исключена при ЭУЗИ, эндоскопическая резекция подходит для опухолей такого размера.
Дуоденальная НЭО размером более 20 мм связана с более высоким риском рецидива и сниженной выживаемостью по конкретному заболеванию и является показанием к хирургической резекции для получения более широких краев.
Для НЭО между 10 и 20 мм данные менее четкие. При отсутствии инвазии мышечной оболочки на ЭУЗИ может быть рассмотрена первоначальная эндоскопическая резекция. Хирургическую резекцию следует рассматривать, если при патологоанатомическом исследовании обнаруживаются признаки высокого риска, такие как лимфоваскулярная инвазия, высокая степень, высокий митотический индекс или инвазия собственной мышечной оболочки.
Эндоскопическая резекция
Сообщалось о тенденции к эндоскопической резекции по сравнению с хирургической резекцией НЭО двенадцатиперстной кишки с преимуществом предотвращения хирургических осложнений. НЭО представляют собой подслизистые поражения; таким образом, простая полипэктомия не считается эффективной. Описаны различные методы резекции; однако единого мнения относительно оптимальной техники нет.
Были изучены эндоскопическая резекция слизистой оболочки (ЭРСО), эндоскопическая подслизистая диссекция (ЭПСД) и варианты этих методик – эндоскопическая резекция на всю толщину (ЭПР). Выбранный метод резекции должен иметь наибольшую вероятность резекции единым блоком и резекции R0 (гистологически чистые боковые и глубокие края).
Следует также учитывать частоту нежелательных явлений, поскольку двенадцатиперстная кишка имеет тонкие стенки и имеет более высокий риск перфорации, чем другие области желудочно-кишечного тракта (таблица 3). Данные об отдаленных исходах и рецидивах ограничены из-за коротких периодов наблюдения в доступных исследованиях.
Таблица 3:
| Техника | Выбор процедуры | Преимущества | Недостатки |
| ЭРСО | • Поражения <10 мм без инвазии мышечной оболочки
• Рассмотреть при поражениях размером 10–20 мм без инвазии в мышечную оболочку. |
• Простая техника, короткое время процедуры
• Низкий риск нежелательных явлений |
• Может быть трудно выполнить резекцию единым блоком и резекцию R0, особенно для глубокого края
• Коагуляционное повреждение образца может ограничивать гистологическую оценку краев |
| ЭПСД | • Поражения ≤20 мм без инвазии мышечной оболочки.
• Рассмотреть при поражениях > 20 мм без инвазии мышечной оболочки. |
• Более высокая частота резекции единым блоком и R0 по сравнению с ЭРСО | • Высокая частота осложнений в двенадцатиперстной кишке (перфорация, отсроченное кровотечение)
• Длительное время процедуры |
| ЭПР | • Поражения ≤20 мм без инвазии мышечной оболочки
• Рассмотреть при поражениях размером 10–20 мм без инвазии в мышечную оболочку. • Может рассматриваться как спасательная процедура для рецидивирующих/остаточных НЭО после других техник |
• Можно добиться резекции на всю толщину
• Высокая скорость резекции R0 |
• Высокая частота осложнений (перфорация, отсроченное кровотечение)
• Более длительное время процедуры, чем ЭРСО |
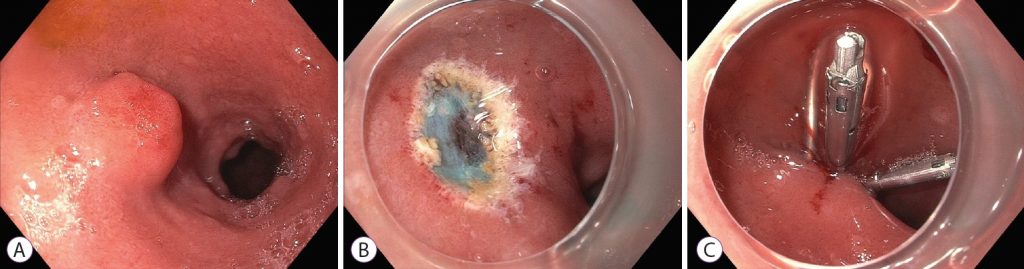
ЭРСО использует подслизистую инъекцию, чтобы поднять и отделить поражение от собственной мышечной оболочки. Это создает приподнятое поражение, которое можно резецировать с помощью прижигания в виде петли (рис. 1). Однако ЭРСО может привести к размозжению и коагуляции краев образца, что может ограничить патологическую оценку. Кроме того, может быть трудно добиться резекции единым блоком и четкого глубокого края даже при инъекционной подтяжке поражения.
ЭРСО с лигированием полос (band-ЭРСО или ЭРСО-ligation; ЭРСО-L) был предложен в качестве альтернативного метода, который позволяет избежать этих недостатков. При band-ЭРСО ткань отсасывается в колпачок, а под ним разворачивается бандаж, создавая псевдополип.
Рисунок 1: Эндоскопическая резекция слизистой оболочки двенадцатиперстной кишки при нейроэндокринной опухоли. (A) Нейроэндокринная опухоль луковицы двенадцатиперстной кишки. (B) После эндоскопической резекции слизистой оболочки. (C) Закрытие дефекта слизистой оболочки клипсами.
При НЭО двенадцатиперстной кишки с помощью ЭРСО достигается резекция единым блоком в 88–97% случаев, а резекция R0 — в 63–97% случаев. Точно так же band-ЭРСО обеспечивает резекцию единым блоком в 100% случаев, а резекцию R0 — в 61–92% случаев.
Зарегистрированные осложнения аналогичны для обоих методов, включая интрапроцедурное кровотечение, отсроченное кровотечение и перфорацию в 10-12%, 0-6% и 0-6% случаев соответственно.
ЭПСД продемонстрировала более высокую частоту резекций единым блоком и R0 по сравнению с ЭРСО, однако двенадцатиперстная кишка представляет собой технически сложное место с более высоким уровнем осложнений. ЭПСД включает в себя маркировку границы поражения перед выполнением кругового разреза слизистой оболочки с помощью электрохирургического ножа. Затем ножом проводят подслизистую диссекцию как можно ближе к собственной мышечной оболочке. Затем дефект можно закрыть с помощью зажимов. Среднее время процедуры составляет около 15 минут.
ЭПСД обеспечивает резекцию единым блоком в 80-100% случаев, а резекцию R0 в 88-100% случаев для двенадцатиперстной кишки. Хотя эти исследования ограничены небольшим числом, по-видимому, высока частота нежелательных явлений, при этом в некоторых исследованиях сообщается о перфорации в 23-25% случаев и отсроченном кровотечении в 7% случаев. Среднее время процедуры составляет около 90 минут.
Эндоскопическая полнослойная резекция с помощью клипс (ЭПР) также была предложена в качестве метода улучшения края образца при глубокой резекции. Сначала отмечают границу поражения с помощью аргоноплазменной коагуляции или электрохирургического ножа. Затем поражение всасывается в колпачок, иногда с использованием трехзубцового анкера для дальнейшего втягивания ткани в колпачок. На оттянутую ткань накладывается клипса за пределами эндоскопа, создавая псевдополип. Ткань над клипсой затем резецируется с помощью электрокаутерной петли.
Развертывание клипсы за пределами эндоскопа позволяет проводить глубокую резекцию с закрытием дефекта, что теоретически минимизирует риск перфорации. Использование этой методики в двенадцатиперстной кишке ограничено, но в исследованиях на сегодняшний день сообщалось о резекции R0 в 100% случаев. ЭПР также успешно используется в качестве спасательной процедуры для рецидивирующих или остаточных НЭО после других техник.
Сообщения о нежелательных явлениях были различными из-за ограниченного числа в каждом исследовании. В одном исследовании, которое включало 6 НЭО двенадцатиперстной кишки, перфорация, микроперфорация и кровоизлияние произошли в 1/6, 3/6 и 1/6 случаев соответственно. В двух других исследованиях, с таким же числом, побочных эффектов не было зарегистрировано. Сообщаемое время процедуры составляло приблизительно 50 минут.
Нейроэндокринные опухоли тощей и подвздошной кишки
НЭО средней части кишечника классически связаны с карциноидным синдромом и часто связаны со значительными симптомами, включая желудочно-кишечное кровотечение, боль в животе и диарею. НЭО подвздошной кишки встречаются гораздо чаще, чем НЭО тощей кишки, и часто связаны с мультифокальным заболеванием.
Иногда НЭО подвздошной кишки обнаруживаются случайно при интубации илеоцекального клапана во время скрининговой колоноскопии. Из-за менее доступного расположения тощекишечные и подвздошные НЭО могут представлять диагностическую проблему.
Видеокапсульная эндоскопия
Роль видеокапсульной эндоскопии (ВКЭ) в диагностике НЭО-ТК еще четко не установлена, и рекомендации по ее использованию зависят от местного опыта. ВКЭ может быть полезна для выявления мультифокальных НЭО, которые могут возникать у 30-50% пациентов и потенциально давать более плохой прогноз, чем при одиночных опухолях.
Хотя чувствительность визуализации и сцинтиграфии для выявления первичной опухоли тонкой кишки в последние годы повысилась, чувствительность визуализации при выявлении многоцентровых карциноидных опухолей не оценивалась. В этом контексте использование ВКЭ в предоперационной оценке может помочь в определении степени резекции.
Использование ВКЭ также может быть рассмотрено у пациентов с метастатическими НЭО неизвестного происхождения перед хирургическим исследованием. Метастатическое распостранение (обычно в печень) обнаруживается у 11% пациентов с хорошо дифференцированными НЭО, но первичная опухоль остается неизвестной. При хирургическом исследовании большинство метастатических НЭО обнаруживаются в тонкой кишке и не выявляются при визуализации в поперечном сечении или сцинтиграфии.
Идентификация первичной опухоли важна, так как некоторые данные свидетельствуют о том, что резекция первичной опухоли может улучшить прогноз даже при метастатическом заболевании.
В целом диагностическая ценность ВКЭ при выявлении опухолей тонкой кишки низкая (2–9%). У пациентов с НЭО с неизвестными первичными опухолями ВКЭ имела чувствительность 75% и специфичность 38% по сравнению с диагностической хирургией.
ВКЭ может быть ограниченА ложноположительными объемными образованиями, визуализируемыми из-за сокращений тонкой кишки и внешней компрессии. Когда видно истинное образование, эндоскопическая картина не является окончательной, а локализация неточной. Для выявления подозрительных выпячиваний, требующих дальнейшего исследования, была предложена система оценки эндоскопических данных, но она не была подтверждена в большой когорте. После идентификации с помощью ВКЭ требуется дополнительная инвазивная процедура, такая как баллонная энтероскопия, для подтверждения результатов и получения патологического подтверждения. Сцинтиграфия рецептора соматостатина с использованием 68Ga-DOTATATE улучшила обнаружение по сравнению с предыдущими агентами. Тем не менее, в его отсутствие ВКЭ все еще может иметь значение, учитывая ее низкий риск, особенно перед диагностической операцией.
Баллонная энтероскопия
С момента своего появления в 2004 году баллонная энтероскопия (БЭ) расширила сферу применения эндоскопических методов до ранее недоступной тонкой кишки по различным показаниям, включая оценку опухолей тонкой кишки. Диагностическая ценность БЭ при опухолях тонкой кишки по всем показаниям оценивается в 4–14%. У пациентов с подозрением на НЭО, но отрицательным исходным обследованием, диагностическая ценность составляет до 33%.
В одном исследовании БЭ имела чувствительность 88% для первичной НЭО-ТК по сравнению с 60% для КТ, 54% для МРТ и 56% для визуализации рецепторов соматостатина.
БЭ также можно рассматривать для выявления мультифокальных НЭО до операции. В одном ретроспективном исследовании пациентов, перенесших резекцию тонкой кишки, БЭ до операции выявила дополнительные поражения у 54% пациентов по сравнению с 18% после ВКЭ. В другом исследовании с аналогичным анамнезом энтероскопия тонкой кишки дала только 10% выход, по сравнению с ВКЭ с выходом 83%. Однако ВКЭ определила правильное количество опухолей только в 21% этих случаев.
Использование БЭ может быть ограничено справочными центрами. Учитывая эти ограничения, мультифокальные опухоли могут быть наиболее надежно обнаружены во время операции при исследовании всего кишечника, как подчеркивается в рекомендациях NANETS. Хотя было показано, что эндоскопические вмешательства, включая биопсию, клипирование и резекцию (включая резекцию карциномы), выполнимы через БЭ с минимальными осложнениями, эта практика не получила широкого распространения, и хирургическая резекция остается основой для НЭО тощей и подвздошной кишки.
Эндоскопическая резекция НЭО тощей и подвздошной кишки не рекомендуется, поскольку даже небольшие (менее сантиметра) поражения тонкой кишки могут быть связаны с инвазией и лимфатическим распространением, что требует более обширной хирургической резекции.
Выводы
Эндоскопия является краеугольным камнем диагностики и лечения НЭО-ТК. В двенадцатиперстной кишке ЭУЗИ является важным методом, который позволяет оценить размер опухоли и глубину инвазии, что необходимо для выбора подходящих кандидатов для эндоскопической резекции.
Для резекции НЭО в двенадцатиперстной кишке были изучены несколько эндоскопических методов, в том числе ЭРСО, band-ЭРСО, ЭРВТ, и ЭПР. С помощью EMR для НЭО может быть трудно добиться чистого результата; однако в настоящее время нет единого мнения об оптимальной технике. При тощекишечных и подвздошных НЭО эндоскопия предназначена в основном для диагностики, выявления мультифокальных опухолей перед хирургической резекцией или локализации первичного поражения в метастатических НЭО, где первоначальное обследование не позволяет выявить опухоль.