Резюме
Целью этого исследования было описать роль соногистерографии с инфузией физиологического раствора СИФ для оценки поражений матки. Инфузионная соногистеросальпингография обеспечивает трехмерные (3D) изображения с высоким разрешением, что, в свою очередь, дает хорошую ориентацию клиницистам и радиологам, в большинстве случаев, об основной патологии эндометрия и труб. Инфузионная соногистеросальпингография с физиологическим раствором является недостаточно используемым методом визуализации, который имеет некоторые преимущества над другими традиционными методами визуализации. Он может быть использован для диагностики гинекологических заболеваний. Соногистеросальпингография с инфузией физиологического раствора имеет преимущество над другими методами благодаря простоте использования, экономической эффективности и неинвазивности, при этом имеет сравнимую или даже лучшую точность, чем большинство методов визуализации, применяемых при гинекологических заболеваниях. Экономическая эффективность и отличная патологическая характеристика делают этот метод визуализации выгодным для индийских учреждений здравоохранения в целом и для сельских медицинских учреждений в частности, где пациенты не могут позволить себе дорогостоящие исследования. Этот обзор охватывает показания и противопоказания, технику визуализации, недостатки визуализации, использование СИФ при различных патологиях матки и, в конце, сравнение СИФ с другими методами визуализации. Инфузионная соногистеросальпингография с физиологическим раствором показана при большинстве распространенных гинекологических заболеваний в Индии, а сообщений о послепроцедурных осложнениях очень мало. Существует также несколько противопоказаний, о которых следует помнить, и которые упоминаются ниже. Во время процедуры следует соблюдать асептические меры. Сравнение между методами визуализации позволит определить наилучший метод для конкретного случая в соответствии с потребностями пациента.
Категории: Акушерство/гинекология, Радиология, Эпидемиология/общественное здоровье, Эпидемиология/общественное здоровье
Ключевые слова: сиф при врожденных аномалиях, сиф при синехиях матки, сиф при аденомиозе, сиф при карциноме эндометрия, сиф при субмукозной миоме, сиф при аденомиозе, соногистеросальпингография, соногистерография с инфузией физиологического раствора.
Введение и предпосылки
Ультрасонография, также известная как ультразвуковое исследование, является очень распространенным неинвазивным методом диагностики, который используется для визуализации структур, лежащих под кожей, и почти не имеет противопоказаний. Ультразвуковой аппарат состоит из датчика, подключенного к экрану компьютера. Датчик излучает волны, которые отражаются от подлежащих структур и принимаются датчиком. Информация от отраженных волн интерпретируется в компьютере и представляется в виде изображения на экране в режиме реального времени. Это очень широко используемый метод визуализации органов брюшной полости и таза и других структур, лежащих под кожей, в режиме реального времени [1]. Соногистерография с инфузией физиологического раствора (СИФ), которую также называют соногистеросальпингографией с инфузией физиологического раствора, – это метод радиологической визуализации, который используется для визуализации различных патологий эндоцервикса и эндометрия. Используя те же принципы, что и ультразвук, этот метод визуализирует полость эндометрия, которая предварительно заполняется физиологическим раствором. Наибольшую пользу СИФ приносит в выявлении и оценке поражений эндометрия и дифференциации их от патологий миометрия. Точность СИФ не уступает гистероскопии в оценке поражений эндометрия [2]. Инфузионная соногистерография с физиологическим раствором может одновременно оценивать проходимость маточных труб с точностью на уровне с гистеросальпингографией (ГСГ) [3,4].
Инфузионная соногистерография с физиологическим раствором выполняется путем введения стерильного физиологического раствора в полость матки с помощью катетера для растяжения полости эндометрия и одновременной визуализации органов малого таза с помощью трансабдоминальной или трансвагинальной сонографии. Во время выполнения процедуры принимаются асептические меры. Асептические меры включают использование стерильных перчаток и инструментов, а также очищение шейки матки ватным тампоном с антисептическим раствором. Для процедуры используется 10-20 мл теплого физиологического раствора, который вводится медленно. Техника визуализации предполагает растяжение полости матки, что позволяет рентгенологам или гинекологам визуализировать один слой полости матки. Это позволяет лучше охарактеризовать патологию [5]. Показана при большинстве гинекологических заболеваний, единственными противопоказаниями к проведению СИФ является наличие активной инфекции органов малого таза, беременность и наличие внутриматочной спирали [6]. Инфузионная соногистерография с физиологическим раствором является относительно неинвазивной процедурой, осложнений, о которых сообщается, очень мало, самым распространенным осложнением является постпроцедурная инфекция [7]. Недостатки СИФ немногочисленны, большинство из них можно устранить путем тщательного планирования и выполнения процедуры. Эти несколько недостатков легко перекрываются превосходными результатами визуализации, которые дает СИФ.
Инфузионная соногистерография с солевым раствором является менее распространенным методом визуализации, поэтому радиологи, клиницисты и студенты недостаточно хорошо знакомы с этой методикой, а также с полученными изображениями. Отсутствие опыта у большинства радиологов и недостаточная осведомленность клиницистов о высокой диагностической ценности СИФ является причиной того, что в Индии она выполняется преимущественно в больницах третичного уровня. Описаны наиболее распространенные гинекологические заболевания, а также традиционно используемые методы визуализации для их исследования. Результаты визуализации с помощью СИФ сравниваются с традиционным методом визуализации, который при большинстве патологий матки оказывается лучшим. Проведено детальное сравнение между СИФ и другими методами визуализации, а именно: трансвагинальной сонографией (ТВС), гистероскопией, гистеросальпингографией и магнитно-резонансной томографией (МРТ). МРТ является наиболее чувствительным методом визуализации, но не может использоваться как основной, поскольку он является очень дорогим и трудоемким, а также занимает много времени. Методы визуализации имеют свои преимущества и недостатки, сравнительное исследование позволит выявить наилучший метод визуализации для конкретной патологии матки.
Обзор
Показания и противопоказания
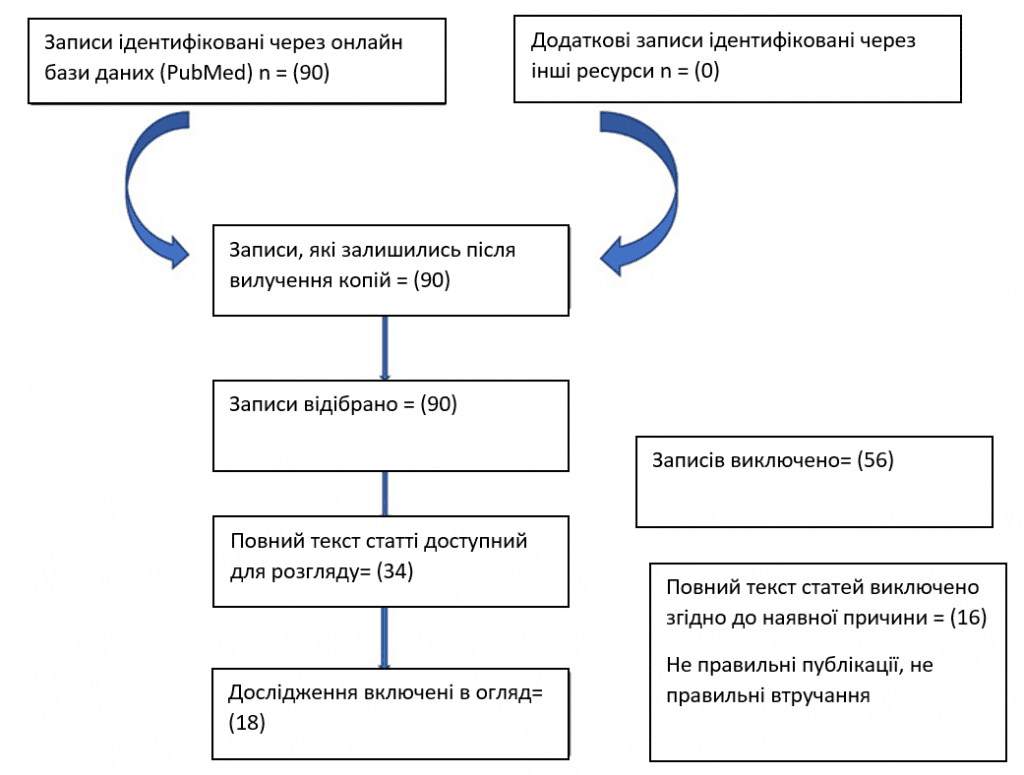
Аномальные маточные кровотечения (АМК) являются самым распространенным показанием к СИФ. АМК является очень распространенным гинекологическим заболеванием, которое требует полного обследования, особенно в возрастной группе перименопаузы и постменопаузы, поскольку оно прогрессирует до рака эндометрия, частота которого составляет 10-15%. Злокачественная опухоль эндометрия, вызывающая АМК, диагностируется с помощью гистероскопической биопсии эндометрия. Относительно неинвазивные методы, такие как ТВС, обычно выполняются как предварительные исследования. Однако при скрининге патологий эндометрия полезность ТВС ограничена [2]. Аномальные маточные кровотечения (АМК) являются Соногистерография с инфузией физиологического раствора обеспечивает лучшую дифференциацию очаговых и диффузных патологий, поскольку позволяет оценить один слой эндометрия за счет адекватного растяжения полости эндометрия во время ультразвукового исследования. Это позволяет проводить прицельный и точный забор образцов очаговых поражений с высокой диагностической эффективностью. Соногистерография с инфузией физиологического раствора является вторым по частоте показаний методом визуализации при бесплодии. Тридцать семь процентов случаев бесплодия связаны с женскими факторами, а еще 35% – с комбинированными женскими и мужскими факторами. Женские факторы бесплодия делятся на цервикальные, маточные, яичниковые, трубные и перитонеальные, что является самым распространенным показанием к СИФ. АМК является очень распространенным гинекологическим заболеванием, которое требует полного обследования, особенно в возрастной группе перименопаузы и постменопаузы, поскольку оно прогрессирует до рака эндометрия, частота которого составляет 10-15%. Злокачественная опухоль эндометрия, вызывающая АМК, диагностируется с помощью гистероскопической биопсии эндометрия. Относительно неинвазивные методы, такие как ТВС, обычно выполняются как предварительные исследования. Однако при скрининге патологий эндометрия полезность ТВС ограничена [8]. Для первичной оценки основным методом визуализации является ТВС. Проходимость труб и полости матки оценивают с помощью ГСГ. Инфузионная соногистерография с физиологическим раствором сочетает возможности ГСГ и ТВС и может одновременно визуализировать проходимость труб, полость матки и другие патологии (Рисунок 1).
Рисунок 1: Поисковая методика, которая использовалась чтобы отобрать наиболее релевантные статьи.
Повторные аборты, предоперационная оценка подслизистой или внутриполостной миомы матки, мониторинг после терапии тамоксифеном, подозрение на синехии матки и врожденные аномалии развития матки являются другими показаниями для проведения СИФ [9,10]. Противопоказаниями к проведению СИФ являются беременность, активная инфекция органов малого таза и наличие внутриматочных контрацептивов [6].
Техника визуализации
Лучшее время для проведения СИФ – между пятым и 10-м днями менструального цикла в ранней пролиферативной фазе, когда оболочка эндометрия является тонкой [9]. Планирование таким образом позволяет избежать ошибочного восприятия полипа или образования эндометрия за утолщенный эндометрий секреторной фазы, что является физиологическим [11]. Время визуализации также предотвращает вытеснение оплодотворенной яйцеклетки во время секреторной фазы промыванием физиологическим раствором. Из-за наличия остаточных сгустков крови в полости матки в течение первых четырех дней менструального цикла процедуру избегают, поскольку она может быть ошибочно принята за патологию. У женщин в постменопаузе, страдающих АМК, ее можно проводить в любое время цикла. Пациенткам, получающим заместительную гормональную терапию, ее назначают в конце прогестероновой фазы менструального цикла [5].
Однако, нельзя пропускать допроцедурную базовую ультразвуковую визуализацию. Скринингу таких патологий, как гидросальпинкс, может помочь УЗИ, поскольку во время СИФ его можно ошибочно принять за инъекционную жидкость. Скрининг активных воспалительных заболеваний органов малого таза, которые абсолютно противопоказаны для проведения СИФ, возможен с помощью предпроцедурной базовой визуализации. Определение размера и положения матки и шейки матки для лучшей оценки необходимого количества физиологического раствора и лучшего позиционирования катетера помогает перед процедурой [5]. Техника визуализации изображена на рисунке 2.
Рисунок 2: Техника визуализации при соногистерографии с инфузией физиологического раствора.
Недостатки СИФ при диагностике
Очевидной предпосылкой для проведения СИФ является адекватное растяжение полости матки; для этого используется безэхогенный физиологический раствор. Может возникнуть несколько проблем, связанных с пациенткой и техникой выполнения. Самой распространенной проблемой является невозможность доступа к шейке матки [5]. Этого можно избежать, правильно расположив пациентку и подобрав зеркало в соответствии с размером влагалища. Проблему переменной ориентации шейки матки можно решить, попросив пациентку лечь на спину после маневрирования зеркалом до известного положения наружного зева или используя тенакулум для тракции шейки матки [5,11]. Для продвижения катетера за пределы стенозированной шейки матки можно использовать цервикальные расширители или проводники. Для уменьшения боли на инструменты можно наносить нестероидные противовоспалительные препараты (НПВП) и местноанестезирующие смазывающие гели.
Затенение соответствующей патологии, подлежащей визуализации, может быть вызвано воздухом, содержащимся в полости матки. Визуализации могут мешать механические препятствия из-за наличия сгустков крови в полости эндометрия, особенно у пациенток с нерегулярным менструальным циклом, поскольку сложно запланировать процедуру на правильное время. Сгусток крови может быть ошибочно принят за полип эндометрия или другие очаговые поражения эндометрия. Сгустки крови можно отличить от полипов эндометрия с помощью допплерографии, которая показывает отсутствие кровотока. Адекватное раздувание баллона имеет важное значение для предотвращения смещения катетера [5].
Однако следует избегать чрезмерного растяжения, чтобы предотвратить затемнение патологии. Другим недостатком является то, что процедура предусматривает растяжение матки и может быть болезненной для некоторых пациенток. Процедура также может привести к занесению инфекции в полость матки, если не соблюдать соответствующие асептические меры.
Осложнения СИФ
Инфузионная соногистерография с физиологическим раствором, как процедура с минимальной инвазией, является сравнительно безопасной и хорошо переносится пациентками, а количество сообщений об осложнениях очень мало. Dessole и соавт. провели проспективное исследование, в котором описали осложнения примерно у 8,8% из 1153 пациенток, которым проводили СИФ [7]. Менее чем у 0,2% пациентов сообщалось о постпроцедурной инфекции [7].
Диагностическая эффективность СИФ при различных патологиях матки
Подслизистая фибромиома
Это доброкачественные опухоли матки из фиброзной ткани и гладких мышц, которые классифицируются на подслизистые, интрамуральные и серозные в зависимости от их локализации. Часто бессимптомные подслизистые миомы являются случайными находками при визуализации; однако симптоматические миомы являются самым распространенным показанием к гистерэктомии [12,13]. Боль в области таза, АМК, повторные потери беременности и бесплодие являются распространенными проявлениями симптоматической миомы [9,10].
Фибромиомы выглядят как гипоэхогенные, круглые и широкопрофильные образования при визуализации, тогда как полипы эндометрия выглядят как гиперэхогенные образования по сравнению с миометрием. На СИФ при миоме матки наблюдается потеря эндометриально-миоматозной границы, и она образует тупой угол с эндометрием. В противоположность этому, при полипах эндометрия интерфейс эндометрий-миометрий интактный и имеет острый угол с эндометрием [6].
Хотя одна питательная артерия встречается менее чем в половине случаев, она остается патогномоничным признаком полипов эндометрия [9,14,15], тогда как миома матки питается разветвленной сосудистой сетью [16]. Как правило, на УЗИ миома матки демонстрирует рефракционное заднее затенение [16].
Существуют как хирургические, так и гормональные методы лечения. Консервативное лечение обычно проводится в большинстве случаев, но подслизистые фибромиомы, сопровождающиеся АМК, могут быть удалены хирургическим путем. Соногистерография с инфузией физиологического раствора может быть использована для определения количества, локализации и объема проекции в полость фибромиомы [16]. У пациенток с множественными миомами на УЗИ органов малого таза можно увидеть искривленный или затемненный эндометрий.
Полип эндометрия
Это локализованная доброкачественная пролиферация желез эндометрия и стромальной ткани, которая прорастает в полость эндометрия. В зависимости от популяции и используемого метода диагностики, распространенность полипов эндометрия составляет от 16% до 34% [17]. Полип эндометрия является важной этиологической причиной АМК у женщин в пре- и постменопаузе. В некоторых случаях возможно сосуществование диффузной гиперплазии эндометрия и полипов [18]. Трансформация в злокачественную опухоль происходит редко; распространенность составляет менее 5% [19].
На УЗИ выглядит как гомогенно-эхогенное полипозное поражение, которое может подвергаться кровоизлияниям, некрозу и инфаркту [9,16]. При ТВС трудно дифференцировать полип эндометрия и диффузную гиперплазию эндометрия, поскольку оба выглядят как неспецифическое утолщение эхогенного эндометрия. При СИФ стенки эндометрия разделены безэхогенным физиологическим раствором, а поражение лучше очерчено, что помогает лучше охарактеризовать поражение эндометрия. В большинстве случаев эндометриальный полип имеет ножку с одним питательным сосудом [17]. Эхогенные образования с ровными контурами также можно дифференцировать от злокачественных. Полипы эндометрия необходимо удалять хирургическим путем, поскольку визуализация не может классифицировать их как доброкачественные или злокачественные [6].
Гиперплазия эндометрия
Это аномальная диффузная пролиферация стромы и желез эндометрия в отличие от очаговой пролиферации, которая наблюдается при полипах эндометрия. В зависимости от количества, наличия и степени атипии различают три типа – простую, сложную и атипичную гиперплазию.
На СИФ гиперплазия эндометрия выглядит как гомогенное утолщение эндометрия. Утолщение эндометрия может быть гетерогенным с кистозной дегенерацией. Очаговые поражения, такие как фибромиома, полипы или карцинома, могут имитироваться асимметричным утолщением эндометрия. Основными методами лечения гиперплазии эндометрия с атипией или без нее являются циклическая прогестероновая терапия или гистерэктомия соответственно [20].
Карцинома эндометрия
Эндометрий Женщины в постменопаузе чаще всего страдают от карциномы эндометрия и на них приходится 10% случаев постменопаузальных кровотечений [15]. Основными факторами риска развития карциномы эндометрия являются отсутствие эстрогенов, такие как синдром поликистозных яичников (СПКЯ), бесплодие, раннее менархе, поздняя менопауза, ожирение и метаболический синдром.
На УЗИ она выглядит как полипозное образование, очаговое утолщение эндометрия или гетерогенное диффузное утолщение эндометрия, а также нарушена граница между эндометрием и миометрием. Раннюю стадию рака эндометрия и гиперплазию эндометрия невозможно отличить только с помощью визуализации, поэтому для подтверждения диагноза необходимо гистологическое исследование. Гетерогенная эхотекстура, искаженная граница эндометрий-миометрий, жидкость в полости эндометрия и неровные края эндометрия указывают на злокачественную опухоль [9,15]. В противоположность этим результатам, гомогенная эхоструктура, четко очерченная граница между эндометрием и миометрием, кистозные изменения и ровные края эндометрия указывают на доброкачественную патологию. Основным методом хирургического лечения является тотальная абдоминальная гистерэктомия вместе с двусторонней сальпингоофоректомией. По показаниям могут также применяться химиотерапия и лучевая терапия [21].
Синехии матки
Синехии матки, также известные как маточные спайки, являются одной из важных причин повторных абортов и бесплодия. Во время обычного ТВС эти спайки трудно визуализировать, поскольку эндометрий часто выглядит нормальным [22,23]. Соногистерография с инфузией физиологического раствора обеспечивает лучшую визуализацию эхогенных полос, разделяя стенки матки. Кинетография в реальном времени обеспечивает лучшую визуализацию маточных спаек, которые выглядят как нерегулярные эхогенные полосы, присутствующие вдоль искривленной полости эндометрия. На поздних стадиях синехий матки адекватное растяжение полости матки становится сложным. Плохое растяжение полости эндометрия свидетельствует о синехии матки. Синехии или спайки эндометрия могут ограничивать растяжение полости эндометрия вследствие предыдущих процедур или введения маточных инструментов, или же инфекции могут привести к скреплению слизистой оболочки эндометрия между собой. Основным методом лечения является гистероскопический управляемый адгезиолиз. Реадгезию можно предотвратить путем введения внутриматочной спирали [22,23].
Аденомиоз
Это доброкачественная патология эндометрия с наличием эктопической стромы и эндометриальных желез в миометрии с гипертрофией гладких мышц [24]. Она может быть бессимптомной или проявляться тазовой болью, АМК или дисменореей [25]. На сонографии он выглядит как асимметричное утолщение стенки миометрия с шарообразным увеличением матки, неоднородной эхоструктурой миометрия, расширенным спаечным комплексом, кистами миометрия, эхогенными линейными полосами и заполнением трещин миометрия жидкостью в полости эндометрия [25,26]. Первым методом визуализации, который часто используется, является ТВС, но диагноз может быть неспецифическим. По сравнению с УЗИ, особенности МРТ являются более специфическими. Соногистерография с инфузией физиологического раствора также преодолевает недостатки ТВС и позволяет точно локализовать субэндометриальные кистозные изменения [25].
Кроме того, лучшая визуализация эндометрия обеспечивается растяжением полости матки физиологическим раствором, которое при других методах визуализации может быть затушевано лежащим в основе аденомиозом. Другие нехирургические методы лечения включают абляционную терапию эндометрия, гормональную терапию и эмболизацию маточных артерий [27].
Врожденные аномалии матки
Врожденные аномалии матки, такие как двурогая матка или перегородка матки, могут быть лучше охарактеризованы с помощью СИФ. Точная визуализация перегородки, ее толщины и типа возможна благодаря растяжению полости матки физиологическим раствором. Дифференцировать перегородку от двурогой матки также возможно с помощью СИФ. Послеоперационная оценка врожденных аномалий матки для определения адекватности лечения также может быть проведена с помощью СИФ.
Терапия тамоксифеном
Тамоксифен – это препарат с антиэстрогенными свойствами. Антиэстрогенное влияние тамоксифена на молочную железу используется для лечения рака молочной железы. Наблюдается повышенная частота заболеваний эндометрия, таких как кисты, полипы, гиперплазия и злокачественные опухоли эндометрия. При визуализации гиперплазия эндометрия, сопровождающаяся кистозными изменениями, является наиболее распространенной находкой [10]. Для мониторинга патологий эндометрия, развивающихся вторично на фоне терапии тамоксифеном, СИФ является полезным методом диагностики. Он имеет более высокую специфичность, чем ТВС, в оценке патологии эндометрия у женщин в постменопаузе с раком молочной железы на терапии тамоксифеном, не имеющих симптомов заболевания [28].
Сравнение СИФ с другими методами визуализации
СИФ против ТВС
В оценке состояния матки и придатков матки ТВС является основным методом. Однако он ограничен в выявлении небольших поражений внутриматочной полости и дифференциации диффузных и очаговых поражений эндометрия. Различные фазы менструального цикла затрудняют точную диагностику искривлений эндометрия, вызванных маточными образованиями. Нормальную выстилку эндометрия иногда можно ошибочно принять за гиперплазию эндометрия при ТВС из-за того, что слои находятся в непосредственной близости друг от друга. В отличие от ТВС, СИФ можно использовать для визуализации как очаговых, так и диффузных поражений эндометрия, поскольку он позволяет оценить один слой эндометрия [2].
СИФ против ГСГ
Бесплодие оценивается с помощью тестов на трубные факторы и проходимость маточных труб. На сегодняшний день скрининговым методом исследования проходимости труб является ГСГ [29]. СИФ является эффективным и безопасным заменителем оценки проходимости труб. Преимуществами СИФ над ГСГ являются экономичность, простота использования, отсутствие ионизирующего излучения и возможность одновременной визуализации всей полости матки. К недостаткам
СИФ является невозможность визуализации всей длины маточной трубы и уверенного определения проходимости одной или обеих маточных труб [3,4]. Различные исследования Christianson и соавт., Socolov и соавт. и Campbell и соавт. показали, что СИФ не уступает ГСГ в выявлении поражений матки, единственным недостатком является меньшая чувствительность в определении проходимости труб [4,30–32].
СИФ против гистероскопии
Гистероскопия является референтным стандартом в оценке поражений полости матки. Однако ее недостатки заключаются в том, что она является инвазивной и дорогостоящей, а также может привести к осложнениям, таким как кровотечение и перфорация, из-за своей инвазивной природы [33]. Роль гистероскопии в оценке поражений аднексиса и миометрия ограничена.
Исследования Scwarzler и соавт. и Epstein и соавт. показали сравнимую специфичность и чувствительность гистероскопии и СИФ в оценке внутриматочных поражений и очаговых поражений эндометрия. Хотя гистероскопия имела преимущество в дифференциации доброкачественных и злокачественных поражений эндометрия, ни один из этих методов не был надежным [34,35].
Таким образом, СИФ как неинвазивный и экономически эффективный метод визуализации с чувствительностью, сравнимой с чувствительностью диагностической гистероскопии, может быть использован как заменитель первичного скрининга при обследовании женщин с АМК. Преимуществом гистероскопии является возможность проведения биопсии одновременно с визуализацией для гистопатологической диагностики, что невозможно при СИФ.
СИФ против МРТ органов малого таза
Использование МРТ для оценки состояния женского таза растет благодаря лучшей визуализации мягких тканей, более высокому контрастному разрешению и возможностям мультипланарной визуализации. МРТ является лучшим методом визуализации миомы, МРТ имеет большее поле зрения и также используется для предоперационного картирования аденомиоза [36].
После проведения эмболизации маточных артерий МРТ предоставляет возможность выявить изменения интенсивности сигнала и объема фибромиомы [37]. МРТ также лучше подходит для стадирования и оценки рака эндометрия, поскольку позволяет определить предоперационное стадирование и оценить степень инвазии миометрия [38]. Способность МРТ демонстрировать расширенную зону соединения делает МРТ органов малого таза гораздо более точным методом оценки аденомиоза [39]. В оценке врожденных аномалий Мюллерова протока МРТ является референтным стандартом [40,41].
Преимуществами СИФ является одновременная оценка проходимости труб и оценка трубных факторов бесплодия. У пациентов, которые не могут пройти МРТ из-за противопоказаний, таких как почечная недостаточность, металлические имплантаты и клаустрофобия, может быть выполнена СИФ. Сравнение СИФ с другими методами визуализации, применяемыми в гинекологии, приведено в таблице 1.
ТАБЛИЦА 1: Итог сравнения СИФ с другими методами визуализации.
| СИФ против ТВС | |
| СИФ | ТВС |
| Лучшая дифференциация между диффузными и очаговыми поражениями эндометрия. Возможна однослойная оценка матки. |
Уступает в отношении точности. |
| СИФ против ГСГ | |
| СИФ | ГСГ |
| Безопасно, эффективно, экономически выгодно и без радиационного облучения. | Лучшая и более полная визуализация маточных труб. |
| СИФ против гистероскопии | |
| СИФ | Гистероскопия |
| СИФ Безопасная, неинвазивная, недорогая и с меньшим количеством осложнений. Хотя оба метода являются надежными, гистероскопия несколько лучше для скрининга, поскольку позволяет дифференцировать доброкачественные и злокачественные образования. | |
| СИФ против МРТ органов малого таза | |
| СИФ | МРТ органов малого таза |
| Недорогая, ее можно использовать у пациентов с металлическими имплантатами. | Лучшая визуализация в нескольких плоскостях, более высокое разрешение и большее поле зрения. |
СИФ: соногистеросальпингография с инфузией физиологического раствора
Заключение
СИФ обеспечивает лучшую визуализацию патологий эндометрия по сравнению с некоторыми рутинными методами визуализации в гинекологии и помогает дифференцировать их от субэндометриальных факторов, обеспечивая тем самым лучшие результаты диагностики. Дополнительным преимуществом является одновременная оценка проходимости маточных труб с сопоставимой точностью. Однако, при исследовании случаев бесплодия ГСГ является скрининговым методом выбора. Его способность визуализировать всю длину маточной трубы дает ему преимущество над СИФ. В случаях, связанных с бесплодием и аномальными маточными кровотечениями, СИФ играет важную роль в диагностике. Недостатки СИФ
Процедура СИФ является несколько болезненной и может привести к занесению инфекции, если не соблюдать адекватные асептические меры. СИФ может эффективно использоваться как дополнительный метод скрининга перед визуализацией органов малого таза. Прежде всего, его экономическая эффективность и сопоставимая точность дают ему преимущество над другими методами визуализации, где поражения не являются четко визуализированными. В таких странах, как Индия, где много сельского населения страдает от множества гинекологических заболеваний, СИФ, будучи дешевым, но эффективным, может использоваться для скрининга, а также для диагностики некоторых заболеваний.
Ссылки на источники
- Ihnatsenka B, Boezaart AP: Ultrasound: basic understanding and learning the language . Int J Shoulder Surg. 2010, 4:55-62. 10.4103/0973-6042.76960
- Aslam M, Ijaz L, Tariq S, Shafqat K, Meher-Un-Nisa, Ashraf R, Kazmi T: Comparison of transvaginal sonography and saline contrast sonohysterography in women with abnormal uterine bleeding: correlation with hysteroscopy and histopathology. Int J Health Sci (Qassim). 2007, 1:17-24.
- Sankpal RS, Confino E, Matzel A, Cohen LS: Investigation of the uterine cavity and fallopian tubes using three-dimensional saline sonohysterosalpingography. Int J Gynaecol Obstet. 2001, 73:125-9. 10.1016/s0020-7292(01)00363-0
- Christianson MS, Legro RS, Jin S, et al.: Comparison of sonohysterography to hysterosalpingogram for tubal patency assessment in a multicenter fertility treatment trial among women with polycystic ovary syndrome. 2023 Kumar et al. Cureus 15(2): e35424. DOI 10.7759/cureus.35424 7 of 9 J Assist Reprod Genet. 2018, 35:2173-80. 10.1007/s10815-018-1306-2
- Allison SJ, Horrow MM, Kim HY, Lev-Toaff AS: Saline-infused sonohysterography: tips for achieving greater success. Radiographics. 2011, 31:1991-2004. 10.1148/rg.317115074
- Frost AV, Routon SG, Angtuaco TL: Saline infusion sonohysterography: key findings and how to perform the examination. Contemp Diag Radiol. 2016, 39:1-5. 10.1097/01.CDR.0000482101.07628.03
- Dessole S, Farina M, Rubattu G, Cosmi E, Ambrosini G, Nardelli GB: Side effects and complications of sonohysterosalpingography. Fertil Steril. 2003, 80:620-4. 10.1016/s0015 0282(03)00791-x
- Recent advances in medically assisted conception . (1990). https://apps.who.int/iris/bitstream/handle/10665/38679/WHO_TRS_820_eng.pdf?sequence=1&isAllowed=y.
- Berridge DL, Winter TC: Saline infusion sonohysterography: technique, indications, and imaging findings . J Ultrasound Med. 2004, 23:97-115. 10.7863/jum.2004.23.1.97
- Yang T, Pandya A, Marcal L, Bude RO, Platt JF, Bedi DG, Elsayes KM: Sonohysterography: principles, technique and role in diagnosis of endometrial pathology. World J Radiol. 2013, 5:81-7. 10.4329/wjr.v5.i3.81
- Lindheim SR, Sprague C, Winter TC 3rd: Hysterosalpingography and sonohysterography: lessons in technique. AJR Am J Roentgenol. 2006, 186:24-9. 10.2214/ajr.05.0836
- Parker WH: Etiology, symptomatology, and diagnosis of uterine myomas . Fertil Steril. 2007, 87:725-36. 10.1016/j.fertnstert.2007.01.093
- Wallach EE, Vlahos NF: Uterine myomas: an overview of development, clinical features, and management . Obstet Gynecol. 2004, 104:393-406. 10.1097/01.AOG.0000136079.62513.39
- Bhaduri M, Tomlinson G, Glanc P: Likelihood ratio of sonohysterographic findings for discriminating endometrial polyps from submucosal fibroids. J Ultrasound Med. 2014, 33:149-54. 10.7863/ultra.33.1.149
- Bree RL, Bowerman RA, Bohm-Velez M, Benson CB, Doubilet PM, DeDreu S, Punch MR: US evaluation of the uterus in patients with postmenopausal bleeding: a positive effect on diagnostic decision making. Radiology. 2000, 216:260-4. 10.1148/radiology.216.1.r00jl37260
- Lane BF, Wong-You-Cheong JJ: Imaging of endometrial pathology. Top Magn Reson Imaging. 2010, 21:237-10.1097/RMR.0b013e31823d8045
- Rahimi S, Marani C, Renzi C, Natale ME, Giovannini P, Zeloni R: Endometrial polyps and the risk of atypical hyperplasia on biopsies of unremarkable endometrium: a study on 694 patients with benign endometrial polyps. Int J Gynecol Pathol. 2009, 28:522-8. 10.1097/PGP.0b013e3181a42228
- Grasel RP, Outwater EK, Siegelman ES, Capuzzi D, Parker L, Hussain SM: Endometrial polyps: MR imaging features and distinction from endometrial carcinoma. Clin Obstet Gynecol. 2000, 214:47-52. 10.1148/radiology.214.1.r00ja3647
- Tabrizi AD, Vahedi A, Esmaily HA: Malignant endometrial polyps: report of two cases and review of literature with emphasize on recent advances. J Res Med Sci. 2011, 16:574-9.
- Chandra V, Kim JJ, Benbrook DM, Dwivedi A, Rai R: Therapeutic options for management of endometrial hyperplasia. J Gynecol Oncol. 2016, 27: 10.3802/jgo.2016.27.e8
- Braun MM, Overbeek-Wager EA, Grumbo RJ: Diagnosis and management of endometrial cancer. Am Fam Physician. 2016, 93:468-74.
- Conforti A, Alviggi C, Mollo A, De Placido G, Magos A: The management of Asherman syndrome: a review of literature. Reprod Biol Endocrinol. 2013, 11: 10.1186/1477-7827-11-118
- AAGL practice report: practice guidelines for management of intrauterine synechiae . J Minim Invasive Gynecol. 2010, 17:1-7. 10.1016/j.jmig.2009.10.009
- Byun JY, Kim SE, Choi BG, Ko GY, Jung SE, Choi KH: Diffuse and focal adenomyosis: MR imaging findings. Radiographics. 1999, 19:161-70. 10.1148/radiographics.19.suppl_1.g99oc03s161
- Verma SK, Lev-Toaff AS, Baltarowich OH, Bergin D, Verma M, Mitchell DG: Adenomyosis: sonohysterography with MRI correlation. AJR Am J Roentgenol. 2009, 192:1112-6. 10.2214/AJR.08.1405
- Reinhold C, Tafazoli F, Mehio A, Wang L, Atri M, Siegelman ES, Rohoman L: Uterine adenomyosis: endovaginal US and MR imaging features with histopathologic correlation. Radiographics. 1999, 19:147-60. 10.1148/radiographics.19.suppl_1.g99oc13s147
- Siskin GP, Tublin ME, Stainken BF, Dowling K, Dolen EG: Uterine artery embolization for the treatment of adenomyosis: clinical response and evaluation with MR imaging. AJR Am J Roentgenol. 2001, 177:297-302. 10.2214/ajr.177.2.1770297
- Fong K, Kung R, Lytwyn A, et al.: Endometrial evaluation with transvaginal US and hysterosonography in asymptomatic postmenopausal women with breast cancer receiving tamoxifen. Radiology. 2001, 220:765-10.1148/radiol.2203010011
- Saunders RD, Shwayder JM, Nakajima ST: Current methods of tubal patency assessment. Fertil Steril. 2011, 95:2171-9. 10.1016/j.fertnstert.2011.02.054
- Socolov D, Lupaşcu IA, Danciu E, et al.: Sonohysterosalpingography versus hysterosalpingography in the evaluation of uterine and tubal infertility. [Article in Romanian]. Rev Med Chir Soc Med Nat Iasi. 2009, 113:803-8.
- Holz K, Becker R, Schürmann R: Ultrasound in the investigation of tubal patency. A meta-analysis of three comparative studies of Echovist-200 including 1007 women. Zentralbl Gynakol. 1997, 119:366-73.
- Campbell S, Bourne TH, Tan SL, Collins WP: Hysterosalpingo contrast sonography (HyCoSy) and its future role within the investigation of infertility in Europe. Ultrasound Obstet Gynecol. 1994, 4:245-53. 10.1046/j.1469-0705.1994.04030245.x
- Aas-Eng MK, Langebrekke A, Hudelist G: Complications in operative hysteroscopy – is prevention possible? Acta Obstet Gynecol Scand. 2017, 96:1399-403. 10.1111/aogs.13209
- Schwärzler P, Concin H, Bösch H, Berlinger A, Wohlgenannt K, Collins WP, Bourne TH: An evaluation of sonohysterography and diagnostic hysteroscopy for the assessment of intrauterine pathology. Ultrasound Obstet Gynecol. 1998, 11:337-42. 10.1046/j.1469-0705.1998.11050337.x
- Epstein E, Ramirez A, Skoog L, Valentin L: Transvaginal sonography, saline contrast sonohysterography and hysteroscopy for the investigation of women with postmenopausal bleeding and endometrium >5 mm. Ultrasound Obstet Gynecol. 2001, 18:157-62. 10.1046/j.1469-0705.2001.00472.x
- Dueholm M, Lundorf E, Hansen ES, Ledertoug S, Olesen F: Accuracy of magnetic resonance imaging and 2023 Kumar et al. Cureus 15(2): e35424. DOI 10.7759/cureus.35424 8 of 9 transvaginal ultrasonography in the diagnosis, mapping, and measurement of uterine myomas. Am J Obstet Gynecol. 2002, 186:409-15. 10.1067/mob.2002.121725
- Jha RC, Ascher SM, Imaoka I, Spies JB: Symptomatic fibroleiomyomata: MR imaging of the uterus before and after uterine arterial embolization. Radiology. 2000, 217:228-35. 10.1148/radiology.217.1.r00se49228
- Yamashita Y, Mizutani H, Torashima M, et al.: Assessment of myometrial invasion by endometrial carcinoma: transvaginal sonography vs contrast-enhanced MR imaging. AJR Am J Roentgenol. 1993, 161:595-9. 10.2214/ajr.161.3.8352114
- Ascher SM, Arnold LL, Patt RH, et al.: Adenomyosis: prospective comparison of MR imaging and transvaginal sonography. Radiology. 1994, 190:803-6. 10.1148/radiology.190.3.8115630
- Troiano RN: Magnetic resonance imaging of mullerian duct anomalies of the uterus . Top Magn Reson Imaging. 2003, 14:269-79. 10.1097/00002142-200308000-00002
- Pellerito JS, McCarthy SM, Doyle MB, Glickman MG, DeCherney AH: Diagnosis of uterine anomalies: relative accuracy of MR imaging, endovaginal sonography, and hysterosalpingography. Radiology. 1992, 183:795-800. 10.1148/radiology.183.3.1584936