АННОТАЦИЯ
ЦЕЛИ:
Несмотря на доказательства того, что с помощью цветного допплеровского картирования можно различить доброкачественные и злокачественные опухоли молочной железы, в клинический практике его применяют редко. Цель данного исследования заключается в том, чтобы выяснить могут ли определенные особенности васкуляризации новообразований в молочных железах, которые обнаружываються при дуплексной допплерографии или цветном допплеровском картировании (до и/или после введения контрастного вещества), предоставить дополнительную информацию к выводам анализа при проведении обычного УЗИ в В-режиме, и подтвердить классификацию BI-RADS (система анализа и протоколирования результатов ультразвуковых обследований молочной железы).
МЕТОДЫ:
С помощью обычного УЗИ в В-режиме, цветного доплеровского картирования и ультразвукового обследования с искусственным контрастированием было поочередно обследовано семьдесят плотных (solid) опухолей. Морфологический анализ и особенности васкуляризации новообразований были взаимосвязанными с результатами гистологического исследования.
РЕЗУЛЬТАТЫ:
После проведения чрескожной толстоигольной биопсии обнаружено, что 25/70 (17,5 %) опухолей были злокачественными, а 45 – доброкачественными. Гиперваскуляризированные образования с извилистыми и центральными сосудами, с индексом резистентности (ИР) ≥ 0,73 перед введением контрастного вещества и ИP ≥ 0,75 после него, имели явные симптомы злокачественности (p < 0,001).
ВЫВОД:
Сочетание данных, полученных при ультразвуковом обследовании с помощью усиленной или неусиленной дуплексной доплерографией или при цветном допплеровском картировании, может предоставить важную информацию для диагностики. Введение практики использования данных техник может происходить легко, в связи с тем, что в большинстве медицинских центров уже есть оборудование для проведения допплерографии.
ВВЕДЕНИЕ
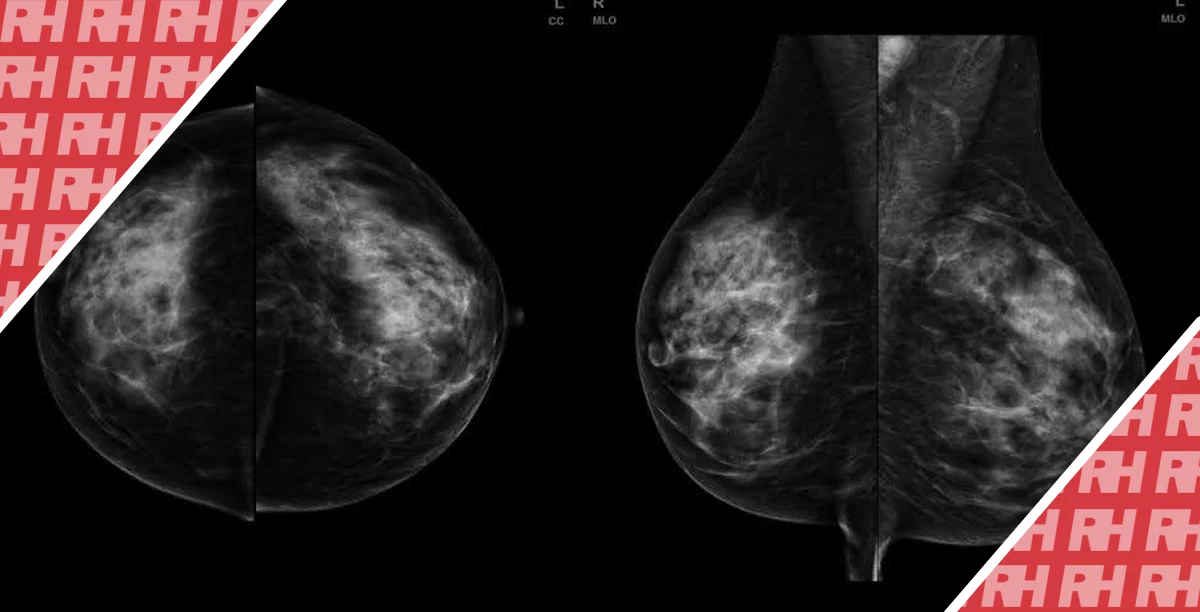
Несмотря на то, что ультразвуковая диагностика молочных желез обычно не является основным методом скрининга рака молочных желез, она является стандартной процедурой при осмотре плотных молочных желез у женщин с повышенным риском возникновения рака груди и используется для дифференциации между доброкачественными и злокачественными новообразованиями. В 2003 году Американское Общество радиологов (the American College of Radiology) опубликовало словарь системы анализа и протоколирования результатов ультразвукового обследования молочной железы (BI-RADS®) для УЗИ, в котором определен унифицированный язык и стандартизированная система классификации. Ключевые слова в основном связанные с морфологией опухолей. Также есть дескрипторы, связанные с васкулярностью опухолей, однако они упрощенные и дают мало информации (например, наличие или отсутствие, место нахождения в пределах новообразования, смежное с опухолью или в окружающих тканях).
Злокачественные новообразования часто продуцируют проангиогенные факторы, которые, в свою очередь, стимулируют рост новых сосудов. Новообразованные сосуды отличаются от старых тем, что имеют нестандартную, извилистую форму с переменным диаметром, и формируют ретикулярные сетчатые структуры с артериовенозными шунтами и дихотомическим разветвлением. Предварительные выводы указывают на то, что для демонстрации этих типичных характеристик неоваскуляризации, проявляющихся в непосредственной близости к злокачественным опухолям, может использоваться дуплексная допплерография (цветное допплеровское картирование с импульсным/спектральным анализом). УЗИ с искусственным контрастированием (УЗИИК) является важным инструментом для диагностики, в связи с тем, что может предоставлять дополнительную информацию о васкуляризации опухоли. Кроме того, УЗИИК не подвергает пациентов ионизирующему излучению (что характерно для маммографии), и не является нефротоксическим, как контрастные вещества магнитно-резонансной томографии (МРТ).
Контрастное УЗИ молочных желез является относительно новой методикой, последствия применения которой все еще оцениваются. Предыдущие исследования, включащие «первое поколение» контрастных препаратов и цветную допплерографию, дали обнадеживающие результаты. Дальнейшие исследования, которые проводились с помощью контрастных препаратов «второго поколения» (с более стабильными и выносливыми микропузырками) и импульсной инверсной гармоникой, позволили провести количественные и качественные анализы изображений с искусственным контрастом, что предоставляет дополнительную информацию о сосудистых морфологических рисунках и характерних особенностях их распространения. Несмотря на эти преимущества, до сих пор все еще не достигнут консенсус относительно использования контрастной ультразвуковой диагностики для осмотра новообразований в молочных железах.
Данное исследование впервые в Бразилии обратило внимание на клиническое использование усиленной и неусиленной дуплексной допплерографии для обследования опухолей в молочной железе. Цель данной работы заключалась в том, чтобы определить насколько хорошо серошкальный морфологический анализ (в В-режиме) и данные о васкулярности опухоли взаимосвязаны с гистопатологическими симптомами, что является золотым стандартом в диагностике опухолей молочной железы.
МАТЕРИАЛЫ И МЕТОДЫ
Пациенты
Данное исследование проводилось в отделении ультразвуковой диагностики, расположенном в Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo Сан-Пауло, Бразилия, в период между мартом 2007 года и январем 2008 года. Участниками стали пациентки Центра Обследование Молочных Желез, у которых было предварительно диагностировано наличие опухолей в груди (4 или 5 категория) и клинические или радиологические показания для проведения чрескожной биопсии молочных желез.
К первой группе образцов вошли 93 опухоли груди 73 пациенток. Пациенток с нетипичными результатам патологий или тех, которые не вернулись для проведения хирургического лечения (n = 9), было исключено, так как анализ лишь нескольких фрагментов не может характеризовать всю опухоль. Финальное обследование включало 70 плотных новообразований у 64 женщин, подлежащих проведению чрескожной биопсии в виде толстоигольной биопсии. Возраст этих пациенток достигал от 18 до 78 лет (средний показатель 49,12 года). Все пациенты предоставили информированные согласия на участие в исследовании, одобренные экспертным советом нашего учреждения (Комитет по этике Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo) от 23 ноября 2006 года (протокол 1021/ 06) .
План клинического исследования
Все осмотры проводились двумя радиологами, стаж каждого из которых в сфере ультразвуковой диагностики молочных желез превышает 10 лет (DS и MCC). Ультразвуковые обследования проводились с помощью аппарата TOSHIBA-APLIO XG (модель 2007 года, Токио, Япония), оборудованного линейным датчиком с частотой от 5 до 14 МГц. Статические и динамические изображения, полученные в ходе обследования, сохранены на электронных носителях.
Обследование перед искусственным контрастированием
Несмотря на то, что в Диагностическом Центре заболеваний молочной железы у Hospital das Clínicas новообразования предварительно классифицировали как BI-RADS 4 или 5, их повторно обследовали и провели еще одну классификацию, не учитывая ранее выявленные симптомы. Опухоли с типичными доброкачественными характеристиками отнесены к «возможно доброкачественным» (BI-RADS 3), даже если они подвергались пальпации (30 опухолей) новообразования с одним подозрительным симптомом злокачественности (или больше) классифицировали как BI-RADS 4 или 5.
После обследования в серошкальном режиме каждого пациента осмотрели с помощью цветного допплеровского картирования (ЦДК). Настройки ЦДК были отрегулированы для выявления кровотока с низкой скоростью или низким объемом. Окно цветного допплера расположено так, чтобы охватить опухоль и часть нормальной ткани молочной железы. Усиление цвета продолжалось пока не появился фоновый шум, а потом снизилось, пока шум не прекратился и появилась возможность обнаружить маленькие сосуды. Обследования проводились с минимальным давлением датчика, чтобы предотвратить спадание сосудов.
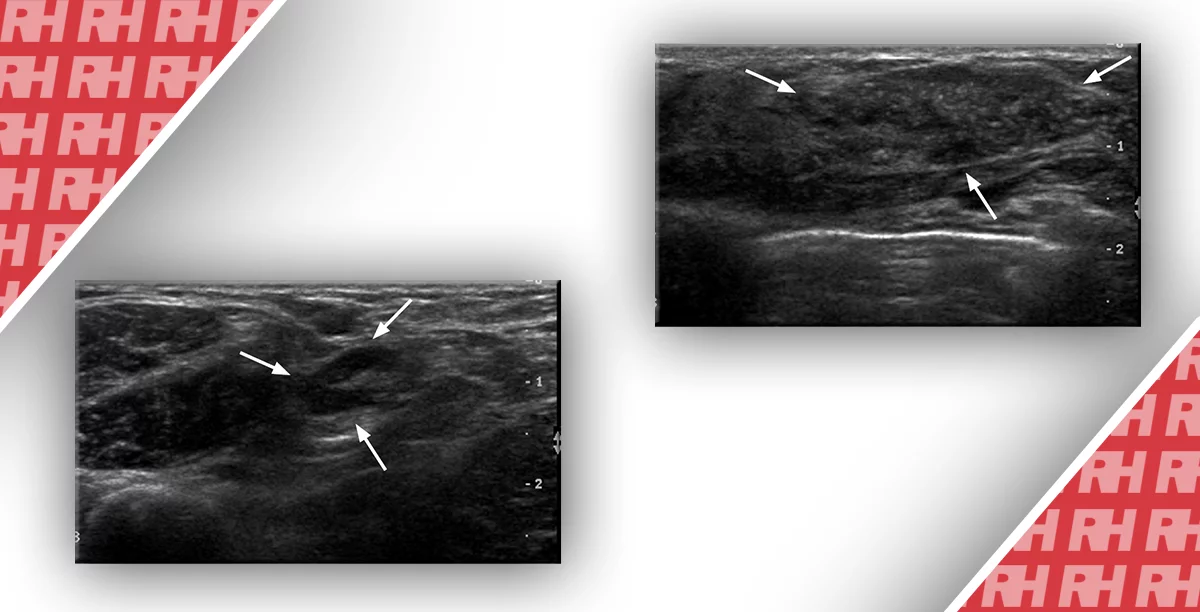
Опухоли подлежали качественной оценке по определенным Moon и другими критериям, которые кратко изложены в Таблице 1. Мы также отметили наличие проникающих сосудов, которые, как отмечают Raza и Baum, указывают на злокачественность. Опухоли отнесли к «возможно доброкачественным» (аваскулярные или гиповаскулярни новообразования с нормальными и периферийными сосудами, Рис. 1 и 2), «возможно злокачественным» (гиперваскулярные опухоли с сосудами неправильной формы и централизованным распределением, Рис. 3) или «подозрительным» (любой другой возможный вариант, Рис. 4).
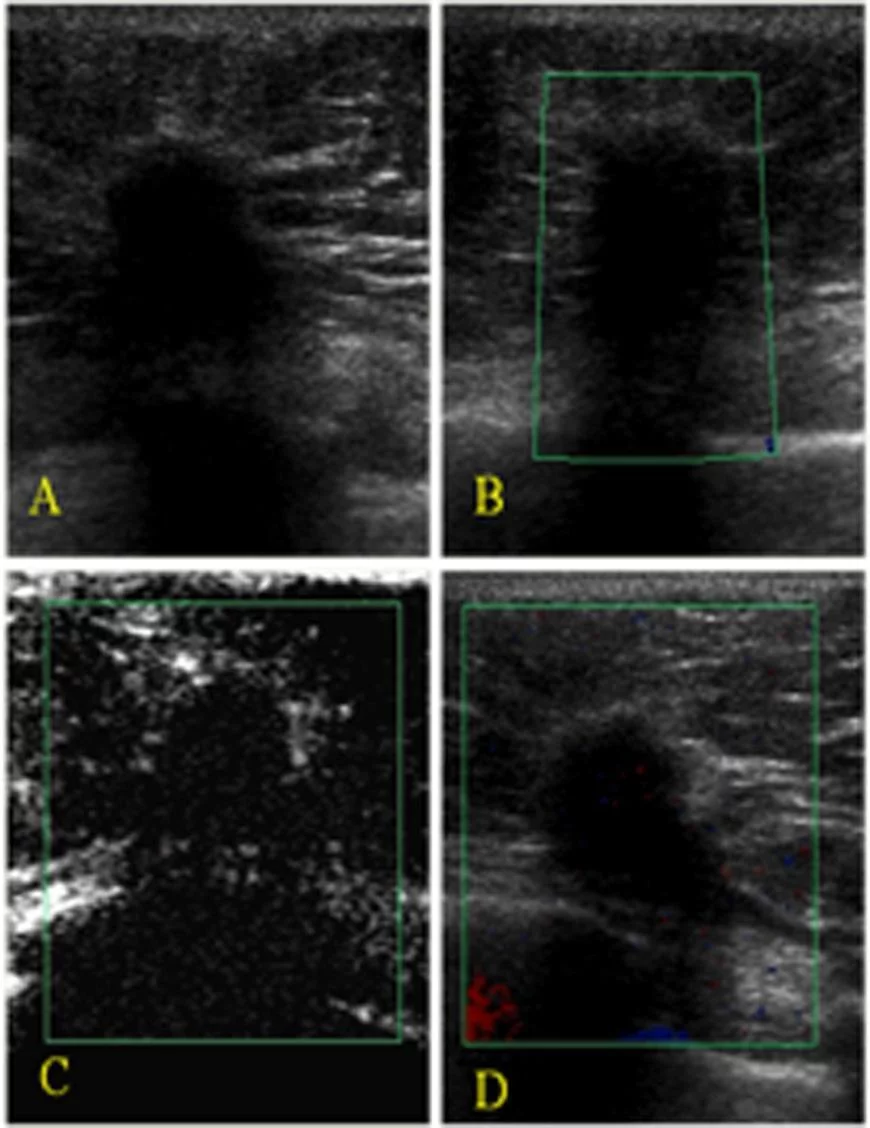
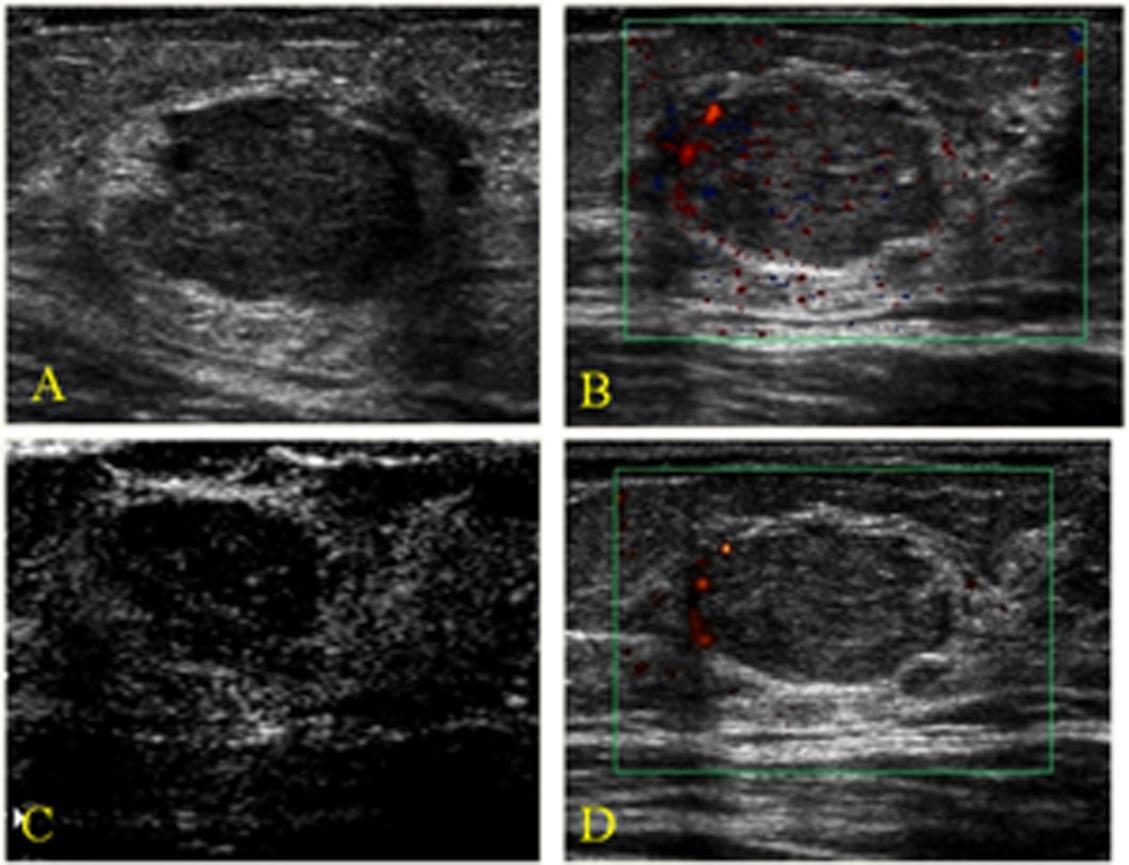
Рис. 1. Фиброаденома, обнаруженная в левой молочной железе 47-летней женщины. А) На серошкальном изображении наблюдаем дольковое новообразование нестандартной формы (BI- RADS 4). В) На цветном допплеровском картировании показано нормальную периферийную артерию. С) После введения контрастных препаратов мы заметили умеренное периферийное усиление. D) Усиленное цветное допплеровское картирование показывает ту же зону, которую при неусиленном доплеровском картировании изображено на Рисунке В. Не обнаружено никаких дополнительных артерий. Обследование с помощью энергетического допплера проводилось исключительно с целью получения более четких изображений для иллюстраций.
Рис. 2. Инвазивный рецидив проточной карциномы левой молочной железы у 63-летней женщины. А) На серошкальном изображении наблюдаем остроконечные новообразования неправильной формы с эхогенные ободком (halo), нарушением архитектуры, акустическим затенением и выпрямлением связки Купера (BI-RADS 5). В) Цветовое допплеровское картирование показывает аваскулярную опухоль. С) После введения контрастных веществ наблюдаем минимальное усиление. D) На усиленном допплеровском изображении видно аваскулярную опухоль.
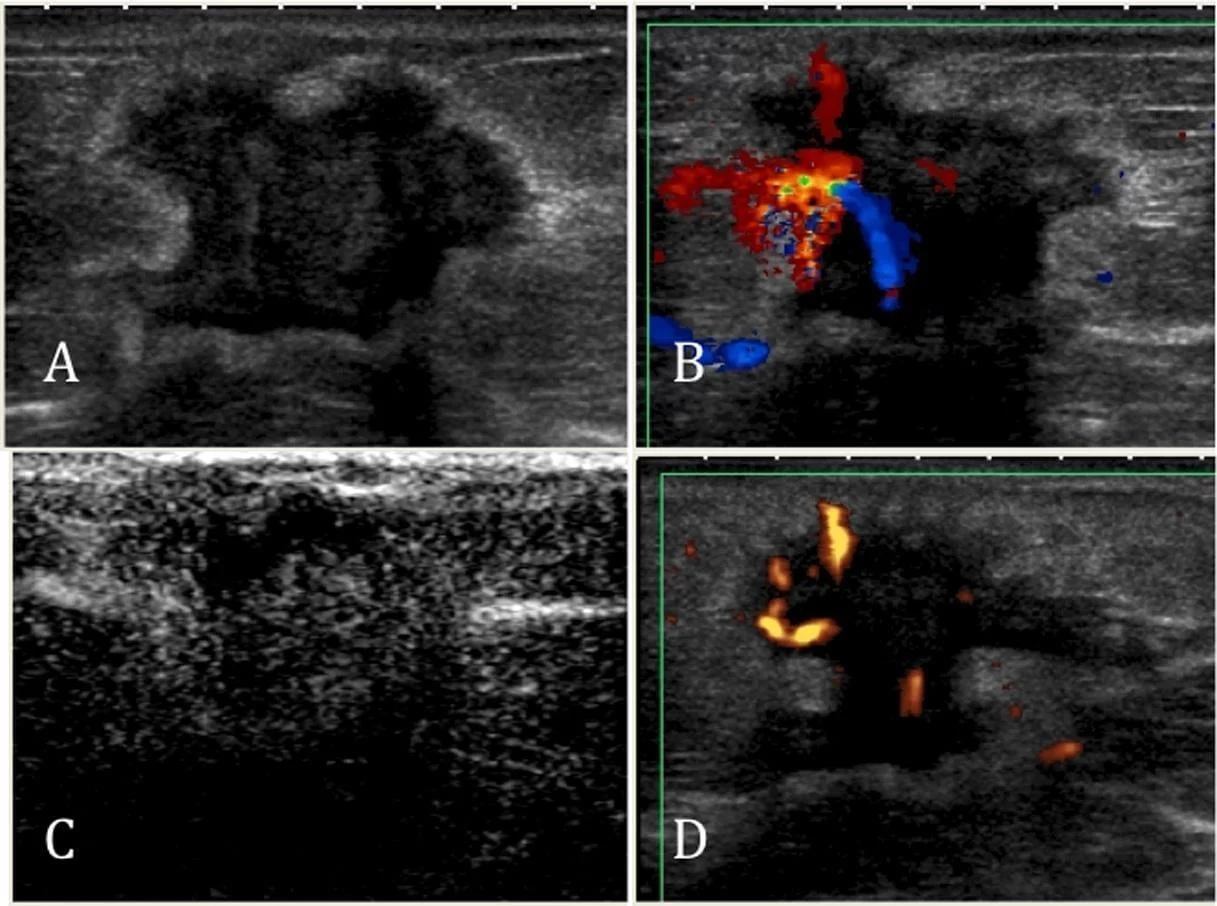
Рис. 3. Инвазивная протоковая карцинома в правой молочной железе 71-летней женщины. А) На серошкальном изображении показано дольковое новообразование нестандартной формы с эхогенным ободком (halo) и акустическим затенением (BI-RADS не 3). В) Цветное допплеровское картирование отображает гиперваскулярную опухоль с центральными артериями неправильной формы. С) После введения контрастных препаратов наблюдаем интенсивное усиление. D) Усиленное цветное допплеровское картирование выглядит аналогично неусиленному ЦДК. Обследование с помощью энергетического допплера проводилось исключительно с целью получения более четких изображений для иллюстраций.
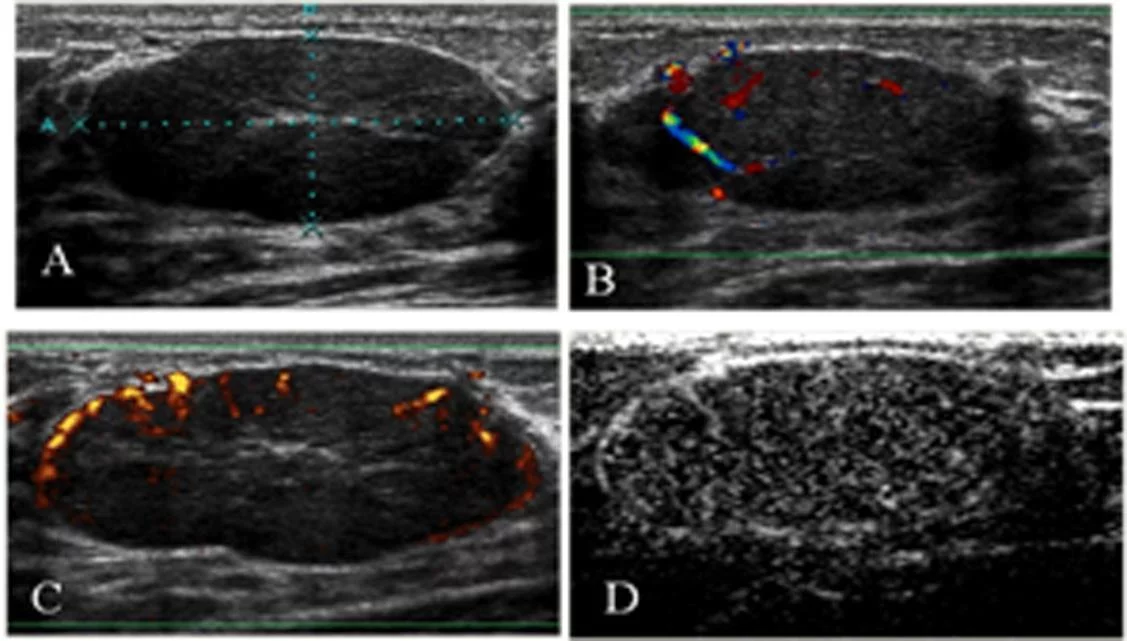
Рис. 4. Ювенильная фиброаденома в левой молочной железе 18-летней девушки. А) На изображении в В-режиме наблюдаем овальное отграниченое новообразование (BI-RADS 3). В) На изображении доплеровского картирования показано гиперваскулярное новообразование в центральных и обычных артериях. С) Усиленное цветное допплеровское картирование (ЦДК) выглядит аналогично неусиленному ЦДК. Обследование с помощью энергетического допплера проводилось исключительно с целью получения более четких изображений для иллюстраций. D) После введения контрастных веществ наблюдаем интенсивное усиление.
Таблица 1. Методы и дескрипторы, используемые для классификации новообразований.
| Метод | Класcификация | Дескрипторы | |||||
|
ОБСЛЕДОВАНИЕ ПЕРЕД ИСКУСТВЕННЫМ КОНТРАСТИРОВАНИЕМ |
|||||||
| В-режым УЗИ | BI-RADS | BI-RADS Дескрипторы | BI-RADS 3 | Не BI-RADS 3 | |||
| ЦДК | Качаственная | Количество артерий | Аваскулярные (не обнаружено ниодной) | Гиповаскулярные (1-2 артерии) | Гиперваскулярные (3 или больше артерий) | ||
| Распространене артерий | Стандартное | Нестандартное | |||||
| Морфология артерий | Периферийная | Центральная | Пенетрирующая артерия | ||||
| Количествення | Спектральный анализ | RI Индекс резистентности | |||||
|
ПОСТКОНТРАСТНЫЙ АНАЛИЗ |
|||||||
| PIH + Low MI | Кинетический анализ | Накопление | |||||
| Вывод | |||||||
| Уровень усиления | Отсутствует |
Минимальное
|
Умеренное | Интенсивное | |||
| E-CDUS | Качественный | Численность | Аваскулярные | Гиповаскулярные | Гиперваскулярные | ||
| Распространене артерий | Стандартные | Нестандартные | |||||
| Морфология | Периферийная | Центральная | Пенетрирующая артерия | ||||
| Количественнй | Спектральный анализ | RI Индекс резистентности | |||||
Нами также было проведено количественное исследование с использованием спектрального доплеровского картирования. Измерение индекса резистентности (ИР) проводилось для всех сосудов вокруг гиповаскулярного новообразования. В случае гиперваскулярних новообразований измерения проводились в трех или четырех различных сосудах, а также записаны показатели с наибольшего сосуда. Данный критерий использовался отдельно и не был принят во внимание при финальных расчетах.
Пост-контрастное обследование
Использовались два контрастных агента. Для 34 пациентов использовался коммерчески доступный препарат (Definity ®, Bristol-Myers Squibb, City, MA, USA), а для 30 пациентов использовался другой препарат, изготовленный в нашей больнице (облученный ультразвуком протеин, который испытал влияние перфторуглерода [PESDA]). Приготовление PESDA происходило по рецепту Porter и остальных. Ни у одного из пациентов не обнаружено побочных эффектов. После катетеризации периферической вены в локтевой сосуд было сначала введено болюс контрастное вещество (3 мл PESDA или 0,01 мл/кг Definity®), а затем 10 мл физиологического раствора. Перед введением контрастного вещества настройки на мониторе были изменены для контрастного обследования (гармоничное инверсное-импульсное сканирование и механический индекс ≤ 0,17). Как только болюс контрастного вещества был введен, активировался таймер.
Продолжительность накопления (ожидание достижения максимальной точки), продолжительность вывода (ожидание пока максимальная интенсивность внутри новообразования достигнет самой низкой отметки), и уровень усиления после введения контрастного вещества будет зафиксирован. Усиление разделили на 4 категории: отсутствует (без изменений в эхогенности новообразования), минимальное (незначительное или нечеткое усиления), умеренное (частичное усиление), или интенсивное (максимальное/мощное усиление). Данная классификация создана субъективно, на основе изменений в интенсивности внутри новообразования, которые наблюдались после введения контрастного вещества. Это связано с тем, что для данного вида обследования нет соответствующего количественного метода (Таблица 1).
После фазы выведения мы провели повторный анализ количества сосудов и их характеристик с помощью ЦДК после введения контрастного препарата, и классифицировали новообразования на основе упомянутых выше параметров. После введения контрастных препаратов мы также получили новые показатели ИР сосудов ( Таблица 1).
Гистопатология
После ультразвукового обследования все пациенты, включая тех, чьи новообразования отнесли к категории BI-RADS 3, вернулись в Центр диагностики заболеваний молочных желез для проведения чрескожной биопсии молочной железы с помощью 14-ти калиберного автоматического биопсийного пистолета и иглы BARD® (Bard Radiology, Covington, GA). С каждого узелка были извлечены минимум шесть фрагментов. Их залили парафином и провели гистологический анализ. Симптомы, обнаруженные на финальной стадии, добавили к другим симптомам, подлежащим статистическому анализу .
Статистический анализ
Статистический анализ проводился с помощью критерия хи-квадрат или независимого t-критерия (если первый не удалось применить). Кроме этих тестов разработан график зависимости чувствительности от частоты ложноположительных заключений (кривая-ROC), а также проведен анализ логистической регрессии данных.
РЕЗУЛЬТАТЫ
При-контрастное обследование
В общем, ультразвуковое обследование прошли 70 новообразований в молочных железах 64 пациенток, после которого проводилась пункционная биопсия для гистопатологического соотношения. Доброкачественные новообразования чаще диагностировали как фиброаденомы (28/45), стромальный фиброз (6 /45) или дуктальную гиперплазию без атипии (3/45). Почти 100% злокачественных новообразований диагностированы как инвазивная протоковая карцинома (23/25), за исключением одного анапластического новообразования и одной лимфомы. Симптомы, обнаруженные при последнем осмотре новообразования в В-режиме УЗИ, неусиленном ЦДК и усиленном ЦДК, отображены в Таблице 2.
Таблица 2. Последний осмотр новообразований в молочной железе с помощью В-режима УЗИ, неусиленного ЦДК и усиленного ЦДК.
|
Финальный диагноз |
В-режим УЗИ | Неусиленное ЦДК | Усиленное ЦДК | ||||||
| B3 | Не B3 | НД* | П** | НЗ*** | НД* | П** | НЗ*** | ||
| 30 | 15 | 26 | 14 | 5 | 21 | 18 | 6 | ||
| Доброкачественные | (100%) |
|
(89.6%) | (66.7%) | (25%) | (91.3%) | (81.8%) | (24%) | |
| 0 | 25 | 3 | 7 | 15 | 2 | 4 | 19 | ||
| Злокачественные | (0%) | (62.5%) | (10.3%) | (33.3%) | (75%) | (8.7%) | (18.2%) | (76%) | |
| В сумме | 30 | 40 | 29 | 21 | 20 | 23 | 22 | 25 | |
| Статистический анализ | |||||||||
| Чувствительность | 100% | 88% | 92% | ||||||
| Специфичность | 66.6% | 57.7% | 46.6% | ||||||
| 62.5% | 53.6% | 48% | |||||||
| 100% | 89.9% | 91% | |||||||
* ВС: наверное доброкачественный; ** П: подозрительный; *** НЗ: неверное злокачественный
Данные BI-RADS дескрипторы указывают на злокачественность (p < 0,001): вертикальное положение (80%), без четко отграниченных границ (64%), изменения в связке Купера (100 %), дуктальные изменения (78,9 %) и ретрактацию или неравенство кожного покрова (87%), а также наличие эхогенной зоны (94,4 %) или архитектурного искажения (100%).
В ходе проведенного нами ЦДК анализа было обнаружено, что для большинства злокачественных новообразований характерна центральная васкулярность (91,6 %) с гиперваскулярностью (68%), пенетрирующей артерией (66,6 %) и извилистыми сосудами (75%). Доброкачественные новообразования были в основном аваскулярными или гиповаскулярными (60%), и обычно имели нормальные сосуды (83,3 %). Из всех васкулярных доброкачественных новообразований только 16,6 % имели пенетрирующую артерию.
Согласно кривой-ROC, высокий показатель ИP для неусиленного спектрального доплеровского картирования (высокий уровень чувствительности и специфичности) равен 0,73, при данной величине было достигнуто 76 % чувствительности и 71 % специфичности. Этот высокий показатель ИР позволил добиться заметной разницы между доброкачественными и злокачественными новообразованиями (p < 0,001). У 25 проанализированных новообразованиях обнаружены средние показатели ИР 0,82 ± 0,16 (в диапазоне между 0,63-1,46 ), у 13 (80 %) злокачественных новообразований показатель ИР достигает ≥ 0,73 (p < 0,001). Средние показатели ИР 45 проанализированных доброкачественных новообразований составляли 0,48 ± 0,37 (в диапазоне между 0,46-1,29 ), и 14 (31,1 %) доброкачественных новообразований с показателем ИР ≥ 0,73 (p < 0,001).
Пост-контрастное обследование
После введения контрастного вещества для выявления уровня усиления и продолжительности фазы накопления и фазы высвобождения использовался кинетический анализ, цель которого заключалась в определении могут ли данные параметры предоставить полезную информацию для классификации новообразований на доброкачественные и злокачественные. Для большинства злокачественных новообразований характерно умеренное (14/25) или интенсивное (7/25) усиление. Никакого усиления не наблюдалось в одной карциноме или одной липоме, а в двух карциномах обнаружено минимальное усиление. Относительно доброкачественных новообразований, усиления не было обнаружено в 8 случаях, минимальное усиление обнаружено в 11 случаях, умеренное усиление – в 17 случаях и интенсивное усиление характерно в 9 случаях (включая фиброаденомы).
Средняя продолжительность фазы накопления для злокачественных новообразований составила 56,9 ± 32,3 сек. (в диапазоне между 19-180 сек.) и 56,6 ± 22,9 сек. (в диапазоне между 22-160 сек.) для доброкачественных новообразований. В ходе анализа кривой-ROC обнаружено, что продолжительность фазы накопления и высвобождения не позволяет эффективно различать доброкачественные и злокачественные новообразования.
Результаты нашего качественного усиленного ЦДК-анализа, проводившегося по аналогичным критериям с теми, которые используются для неусиленного ЦДК, представлены в Таблице 2. Большинство (24/25, 96,0%) злокачественных новообразований были гиперваскулярнимы. Из 24 гиперваскулярних злокачественных новообразований у 22 (22/45, 48 %) было центральное распространение, у 17 (70,8 %) была пенетрирующая аретрия, а у 20 (83,3 %) – извилистые сосуды. Примерно половина (22/45, 48%) доброкачественных новообразований были аваскулярными или гиповаскулярными. Среди 34 доброкачественных новообразований которые имели хотя бы один сосуд, периферийная васкулярнисть наблюдалась у 13 (38,2 %) новообразований, а центральная – у 21 новообразования (61,7 %). Большинство доброкачественных новообразований минимум с одним сосудом (28/34 ; 82,3 %) имели нормальную васкулярную морфологию.
Согласно кривой-ROC (наивысшая чувствительность и специфичность), в пост контрастном исследовании лучший показатель продолжительности фазы накопления ИР составил 0,75. С таким показателем ИР удалось достичь 72 % чувствительности и 67 % специфичности. Данный показатель позволяет хорошо различать доброкачественные и злокачественные новообразования (p < 0.001). При количественном пост-контрастном анализе обнаружено, что среднее значение ИР составляет 0,82 ± 0,16 (в диапазоне между 0,63-1,46 ), из которых у 19 злокачественных новообразований (76%) показатель ИР равен 0,75 (p = 0,001). Между тем средний показатель ИР в доброкачественных новообразованиях равен 0,48 ± 0,37 (в диапазоне между 0,46-1,29 ), величина ИР 17 из которых (37,8 %) составляла ≥ 0,75 (p = 0,001).
ОБСУЖДЕНИЕ
В данном исследовании классификация BI-RADS с использованием УЗИ в В-режиме показала высокую чувствительность к выявлению злокачественных новообразований, однако ей не хватало точности, с чем связано значительное количество ложноположительных результатов. Такие результаты подтверждают предыдущие исследования классификации BI-RADS. 15 ложноположительных результатов, полученных в нашем исследовании, касались в основном фиброаденом.
Несмотря на то, что в лексиконе BI-RADS есть дескрипторы, относящиеся к васкулярности новообразований, на наш взгляд, они не позволяют четко разграничивать доброкачественные и злокачественные новообразования; дескрипторы также не играют важной роли при описании, классификации или лечении опухолей в молочных железах. Однако злокачественные новообразования действительно проявляют характерные симптомы на дуплексных доплеровских изображениях, среди которых гиперваскулярность, пенетрация сосудов, неправильные сосуды, центральное распространение сосудов, ответвления и нарушенная морфология сосудов. Проведя исследование, мы обнаружили, что гиперваскулярность, свитые артерии, пенетрация сосудов и центральное распространение сосудов тесно связаны с злокачественностью. Результаты злокачественности и доброкачественности, которые мы получили, используя дуплексное допплеровское картирование, хорошо соотносятся с гистопатологическими диагнозами, доказывая, что выбранные нами критерии качественной оценки были эффективными и действенными.
Что касается количественного анализа, несколько исследований обнаружыли высокие показатели ИР в злокачественных новообразованиях по сравнению с доброкачественными (это связано с артериовенозным шунтированием и отсутствием гладких мышц, что привело к появлению высокоскоростного пульсирующего кровотока в опухоли). Однако, не существует порогового значения показателей ИР, которое бы позволило различать злокачественные и доброкачественные новообразования; предыдущие значения показателей ИР достигали от 0,7 до 1,0. В нашем исследовании оптимальные показатели чувствительности и специфичности удалось достичь с пороговым значением ИР 0,73 для неусиленного ЦДК, и 0,75 для усиленного ЦДК.
В ходе предыдущих исследований были обнаружены диагностические ошибки в неусиленном и усиленном ЦДК. Особенно гиперваскулярные доброкачественные, воспаленные новообразования, листовидные опухоли и фиброаденомы могут ошибочно принять за злокачественные образования, тогда как гиповаскулярные карциномы могут перепутать и ошибочно считать доброкачественными. Обнаруженные нами симптомы совпадали с результатами предыдущих исследований.
Полученные нами кинетические данные (продолжительность накопления, продолжительность вывода, интенсивность усиления после введения контрастного вещества) значительно не отличаются у доброкачественных и злокачественных новообразованиях, однако мы действительно наблюдали наличие интенсивного усиления в большинстве злокачественных опухолей. Неспособность кинетического анализа сформировать ассоциации может быть связана с тем, что анализ выполнялся субъективно из-за отсутствия объективных инструментов на время проведения исследования. Однако многие исследователи описали важность усиления микропузырьков для ультразвуковой диагностики новообразований в молочных железах, а благодаря контрастированию заметно улучшилась точность диагностирования.
Более актуальные исследования показали, что не только анализ кинетических кривых (как на МРТ), но и распределение контраста внутри новообразования, может указывать на злокачественность (гетерогенное или периферийное ободообразное гиперусиление с центростремительным наполнением) и неблагоприятный прогноз (наличие дефекта перфузии и пенетрирующих сосудов). Многообещающим направлением в исследовании является изучение эффективности неоадъювантной химиотерапии с помощью ЦДК; Wan и другие обнаружили, что изменения перфузии крови в опухоли происходят быстрее, чем изменение ее размера.
Несмотря на то, что с помощью данных, полученных при усиленном или неусиленном ЦДК, нельзя достоверно различить доброкачественные и злокачественные новообразования, с их помощью можно получить дополнительную информацию о стандартных симптомах, обнаруженных при ультразвуковом обследовании. Согласовано с предыдущими наработками других врачей, наше исследование показало, что гиперваскулярные новообразования с пенетрирующими и нестандартными сосудами и центральным разветвлением указывают на злокачественность новообразования. Поэтому мы убеждены, что эти дескрипторы могли бы усовершенствовать классификацию BI-RADS, в связи с чем их необходимо включить в лексикон BI-RADS.
Правда, наше исследование имеет значительное ограничение: это, в частности, отсутствие объективных методов для анализа динамичности. В связи с этим невозможно определить истинный потенциал усиленного УЗИ молочной железы. За исключением данного ограничения, наше исследование демонстрирует важность васкулярного анализа новообразований в молочных железах, что можно легко сделать с помощью неусиленного ЦДК.
Поэтому, данное исследование показывает, что характеристики васкуляризации, обнаруженные при спектральном или цветном допплеровском картировании, связанные с морфологическими дескрипторами в лексиконе BI-RADS, в связи с чем они предоставляют новую и важную информацию для определения природы новообразований в молочных железах. Учитывая то, что допплерографическая функция имеется почти в каждом современном ультразвуковом оборудовании, и то, что этот метод можно легко использовать без добавления значительных затрат к обычной ультразвуковой диагностики, мы рекомендуем использовать данные, полученные во время спектрального или цветного допплеровского картирования, при стандартных анализах новообразований в молочных железах.
УЗИ аппарат Toshiba Aplio XG – ультразвуковая диагностическая система для выполнения широкого спектра задач. Только лучшие предложения от компании RH.