Резюме
Цель
Валидация программного обеспечения для УЗИ, которое использует трансперинеальное ультразвуковое исследование для диагностики опущения матки (ОМ).
Методы
Многоцентровое, обсервационное, проспективное исследование с участием 155 пациенток, имевших показания к оперативному вмешательству по поводу дисфункциональной патологии тазового дна. Каждой пациентке в операционной под наркозом проводили обследование с помощью маточных щипцов с последующей хирургической коррекцией ОМ II-IV стадии в условиях анестезии. Для оценки разницы в размерах лобково-маточного дна использовали трансперинеальное ультразвуковое исследование. С помощью многофакторной логистической регрессионной бинарной модели (с измерением УЗИ в состоянии покоя, пробы Вальсальвы и возраста) с использованием неавтоматизированных методов прогнозирования ОМ. С целью оценки модели была построена таблица с координатами рабочей характеристики приемника (ROC), после чего была проведена оценка чувствительности и специфичности.
Результаты
Всего было включено 153 пациента (73 с диагнозом хирургического ОМ). Она была получена на основе AUC (0,89) вероятностей, предсказанных моделью (95% доверительный интервал, 0,84-0,95; P < 0,0005). На основе ROC-кривой для модели была получена чувствительность 91,8% и специфичность 72,7%, что является более высокими показателями, чем для клинического обследования при хирургическом ОМ (чувствительность: 80,8%; специфичность: 71,3%).
Заключения
Мы проверили программное обеспечение, которое использует трансперинеальное ультразвуковое исследование тазового дна и возраст пациента для установления более надежного диагноза хирургического ОМ, чем тот, который получен при клиническом обследовании.
Аббревиатуры
ИМТ
индекс массы тела
ДИ
доверительный интервал
МКО ПОМ-К
Количественная оценка пролапса органов малого таза Международного континентального общества
ПОМ
пролапс органов малого таза
СНС
стрессовое недержание мочи
ОМ
опущення матки
ИНС
императивное недержание мочи
Существуют индивидуальные особенности, которые могут способствовать появлению и прогрессированию пролапса органов малого таза (ПОМ).1, 2 Поддержание механизмов поддержки таза с помощью физической активности является сомнительным,3 поэтому хирургическое вмешательство иногда становится решением этой патологии. Однако гистерэктомия имеет ряд осложнений,4 включая риск рецидива опущения тазовых органов после операции.5 Существуют различные типы рецидивов пролапса органов малого таза,6, 7 и рекомендованы различные хирургические методики для избежания таких событий.8 Существуют многочисленные факторы риска, которые влияют на рецидив ПОМ,9, 10 причем основным механизмом является опускание апикальной опоры после вагинальной гистерэктомии,11, 12 в дополнение к ее связи с недержанием мочи.13, 14 Поэтому правильный диагноз перед операцией имеет решающее значение для правильного лечения пациенток.
Количественная оценка пролапса органов малого таза Международного континентального общества (МКО ПОМ-К)15 является классическим методом оценки опущения матки (ОМ) перед операцией. Однако было доказано, что визуализационные тесты, такие как магнитно-резонансная томография (МРТ), являются сопоставимыми с клиническими оценками для оценки пролапса матки.16 Однако оба метода диагностики имеют различные ограничения, поскольку клинические обследования охватывают только анатомическую поверхность, используя девственную плеву в качестве подвижной точки отсчета,15 а МРТ, которая является более экономически выгодным тестом, не всегда доступна для клиницистов для исследования ПОМ.
УЗИ тазового дна стало полезным инструментом в диагностике ПОМ, устанавливая значительное опущение каждого отдела по отношению к задне-нижнему краю лобкового симфиза во время пробы Вальсальвы.17, 18 Кроме того, дифференциальная диагностика в пределах каждого отдела была определена сонографически, для переднего 19–21, среднего 22, 23 и заднего 24 отделов. Ультразвуковая диагностика ОМ основывается на измерении положения дна матки между состоянием покоя и пробой Вальсальвы по отношению к лобку; ОМ определяется, когда этот показатель составляет ≥15 мм (чувствительность: 75% и специфичность: 95%).22 Однако, ОМ является многофакторным образованием, и этот аспект следует учитывать при постановке диагноза. По этой причине были предложены различные многофакторные регрессионные модели, в которых для постановки диагноза ОМ использовалось трансперинеальное ультразвуковое исследование.25 Модель, включающая измерение разницы между лобково-маточным дном в состоянии покоя и во время маневра Вальсальвы, а также возраст, продемонстрировала максимальную дискриминационную способность, при этом была более простой в применении в рутинной клинической практике, правильно диагностируя 96,7% пациентов с ОМ.25 Однако эта модель имеет ряд ограничений, поскольку популяции, которые изучались для ее разработки, включали пациенток с ОМ и пациенток с удлинением шейки матки без ОМ; кроме того, модель не имеет внешней валидации.25 Поэтому целью этого многоцентрового исследования была валидация программного обеспечения для ультразвукового исследования, которое использует трансперинеальное ультразвуковое исследование для диагностики ОМ.
Материалы и методы
Исследуемая группа
Это было многоцентровое, обсервационное и проспективное исследование. В нем участвовали четыре больницы (Университетская больница Вальме в Севилье [Испания], Университетский медицинский комплекс Гран-Канария [Испания], Университетский медицинский комплекс Леона [Испания] и Университетская больница Вирхен де ла Виктория в Малаге [Испания]).
В общем 155 пациентов были последовательно набраны в период с 1 сентября 2021 года по 30 сентября 2022 года.
Пациентки были отобраны во время специализированной консультации по вопросам тазового дна в каждом центре и должны были соответствовать следующим критериям включения:
- Показания к хирургическому вмешательству по поводу дисфункциональной патологии тазового дна, коррекции ПОМ или хирургического лечения недержания мочи с использованием безнатяжных лент; и
- Ознакомление и подписание информированного согласия на участие в исследовании.
Все пациентки, которые имели в анамнезе предыдущие корректирующие операции по поводу патологии тазового дна или предыдущую гистерэктомию, были исключены.
Метод исследования
Оценка во время консультации
Все пациенты, включенные в исследование, были обследованы во время консультаций, где проводилось стандартизированное анкетирование и клиническое обследование с использованием системы МКО ПОМ-К для оценки наличия и стадии ПМО.15 Клинический ОМ с критериями хирургических показаний определялся как ОМ II-IV стадии (симптоматический и влияющий на качество жизни), представленный во время консультации. В случаях недержания мочи определяли тип недержания (стрессовое недержание мочи [СНС] или императивное недержание мочи [ИСН]), а состояние СНС определяли с помощью простого стресс-теста. В случае сомнений для подтверждения типа недержания мочи проводили уродинамическое исследование.
Оценка в операционной
Каждой пациентке в операционной проводили анестезию, а перед операцией хирурги выполняли повторное обследование с помощью маточных щипцов для определения опущения матки по системе МКО ПОМ-К. Хирургическую коррекцию ОМ проводили, когда при обследовании с помощью маточных щипцов выявляли II-IV стадии ОМ (симптоматические и влияющие на качество жизни) по системе МКО ПОМ-К 15 (Рис. 1) (диагностика ОМ с помощью маточных щипцов с хирургическими критериями [золотой стандарт]).
Рисунок 1
Диагностика ОМ с помощью маточных щипцов.
Ультразвуковая оценка
Трансперинеальные УЗИ выполняли специалисты по УЗИ органов малого таза из каждой больницы; эксперты не были знакомы с результатами клинического обследования. Использовались ультразвуковые аппараты Canon i600 Aplio® (Canon Medical Systems Corp., Токио, Япония) с трехмерным абдоминальным датчиком PVT-675MV и ультразвуковая система Voluson E8 (GE Healthcare, Zipf, Австрия) с датчиком громкости 8-4-МГц. Изображения были получены у пациентов в положении дорсальной литотомии с пустым мочевым пузырем.26, 27 Для получения снимков использовали ранее описанную методику, проводя измерения 25 в состоянии покоя и во время пробы Вальсальвы (минимум 6 с28). Движение матки устанавливали путем расчета разницы между лобково-маточным дном (в состоянии покоя и по Вальсальве)25 (Рис. 2). Измерения проводили внутри задненижнего отдела лобка, согласно ранее установленной методике 25, 29 , измеряя лобково-маточное дно и разницу лобково-маточного дна в состоянии покоя и во время пробы Вальсальвы.
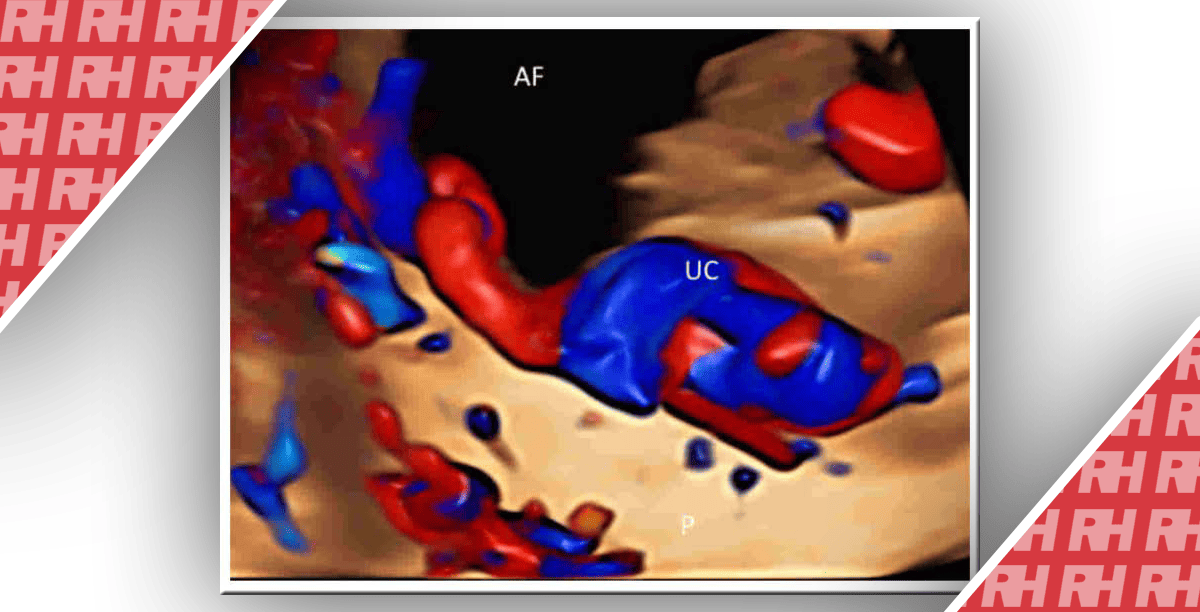
Рисунок 2
Ультразвуковое исследование опущения матки. Желтая линия ограничивает задне-нижний край лобка, а красная стрелка – расстояние между лобком и лоном в состоянии покоя (А) и по Вальсальве (B).
Статистическое исследование
Для числовых переменных использовали среднее значение и стандартное отклонение, а для качественных переменных – процент. Для сравнения числовых переменных использовали t-критерий Стьюдента или U-критерий Манна-Уитни, а для качественных переменных – χ2-критерий. Для определения индивидуальной прогностической способности использовали ROC и AUC. Статистически значимым для всех сравнений считался показатель P < .005.
С параметрами, которые использовались в описанном ранее программном обеспечении 25 , мы создали многомерную модель бинарной логистической регрессии, используя неавтоматизированные методы для прогнозирования ОМ, выполнив тест на адекватность (-2LL). Калибровка этой модели была проведена с помощью теста Хосмера-Лемешоу, и были проведены дальнейшие калибровки. Дискриминационная способность модели была определена с помощью статистики С-индекс Харрелла (получена как AUC).
В таблице с координатами ROC-кривой получена точка отсечения для анализа чувствительности и специфичности и оценки ее использования в диагностике ОМ; включены 95% доверительные интервалы (ДИ). Статистический анализ проводили с помощью статистического программного обеспечения IBM SPSS версии 28 (IBM, Армонк, Нью-Йорк).
Объем выборки
На основе формулы Педуцци, учитывая минимальное количество событий на переменную 10 (Harrell, 2005) и диагноз пролапса 20%, для этого исследования требовался 101 пациент. Из этих 101 пациента 20 имели ОМ, а 81 не имели ОМ. Таким образом, наше исследование соответствовало вышеупомянутым условиям.
Результаты
Всего было набрано 155 пациентов, 2 из которых были исключены, поскольку обследование не проводилось с помощью маточных щипцов. Из 153 пациентов, завершивших исследование, у 73 было выявлено хирургическую ОМ при обследовании с помощью маточных щипцов, по поводу которой была выполнена корректирующая операция, а у 80 не было выявлено хирургической ОМ при обследовании с помощью маточных щипцов (Табл. 1). Между 2 группами была статистически значимая разница по возрасту (62,3 против 53,9; P < 0,001), количеству вагинальных родов (2,4 против 2,0; P = 0,041), наличию стрессового недержания мочи (21,9% против 45,0%; P = 0,004), цистоцеле (89,0% против 71,3%; P = 0,008), диагностированный во время консультации ОМ (80,8% против 28,7%; P <0,001), ректоцеле (43,8% против 26,3%; P = 0,027) и энтероцеле (15,1% против 1,3%; P = 0,002).
Таблица 1. Общая и клиническая характеристика пациента включительно
| С правильным хирургическим вмешательством по поводу опущения матки (n = 73) | Без правильного хирургического вмешательством по поводу опущения матки (n = 80) | P | 95% ДИ | |
| Возраст | 62.3 ± 10.3 | 53.9 ± 10.1 | <.001 | 5.1; 11.7 |
| Вагинальные роды | 2.4 ± 1.5 | 2.0 ± 0.8 | .041 | 0.02; 0.8 |
| Аборты | 0.4 ± 0.7 | 0.5 ± 0.8 | .845 | −0.27; 0.22 |
| Кесарево сечение | 0.1 ± 0.5 | 0.1 ± 0.3 | .581 | −0.09; 0.17 |
| ИМТ | 27.1 ± 3.7 | 27.8 ± 4.5 | .337 | −2.2; 0.7 |
| Стрессовое недержание мочи | 16/73 (21.9%) | 36/80 (45.0%) | .004 | −37.5; −8.6 |
| Императивное недержание мочи | 27/73 (37.0%) | 35/80 (43.8%) | .414 | −21.7; 8.7 |
| Цистоцеле | 65/73 (89.0%) | 57/80 (71.3%) | .008 | 5.2; 30.4 |
| Стадия I | 4/65 (6.1%) | 3/57 (5.3%) | .027 | −8.9; 10.2 |
| Стадия II | 15/65 (23.1%) | 26/57 (45.6%) | −37.9; −5.7 | |
| Стадия III | 46/65 (70.8%) | 28/57 (49.1%) | 4.3; 37.4 | |
| Опущение матки | 59/73 (80.8%) | 23/80 (28.7%) | <.001 | 38.5; 65.6 |
| Стадия I | 4/59 (6.8%) | 7/23 (30.4%) | .020 | −44.5; −6.1 |
| Стадия II | 14/59 (23.7%) | 6/23 (26.1%) | −24.7; 15.9 | |
| Стадия III | 37/59 (62.7%) | 10/23 (43.5%) | −4.3; 40.3 | |
| Стадия IV | 4/59 (6.8%) | 0/23 (0%) | −8.1; 16.2 | |
| Ректоцеле | 32/73 (43.8%) | 21/80 (26.3%) | .027 | 2.5; 32.6 |
| Стадия I | 13/32 (40.6%) | 11/21 (52.4%) | .723 | −36.2; 14.6 |
| Стадия II | 15/32 (46.9%) | 8/21 (38.1%) | −17.6; 32.8 | |
| Стадия III | 4/32 (12.5%) | 2/21 (9.5%) | −17.8; 20.0 | |
| Энтероцеле | 11/73 (15.1%) | 1/80 (1.3%) | .002 | 5.1; 22.6 |
| Стадия I | 4/11 (36.4%) | 1/1 (100%) | .496 | −84.8; 20.6 |
| Стадия II | 6/11 (54.5%) | 0/1 (0%) | −29.1; 78.7 | |
| Стадия III | 1/11 (9.1%) | 0/1 (0%) | −70.6; 37.7 |
Размеры лобково-маточного дна у пациенток с диагнозом хирургического ОМ и без него при исследовании с помощью маточных щипцов приведены в Табл. 2. Пациентки с диагнозом хирургического ОМ при обследовании с помощью маточных щипцов имели большие показатели лобково-маточного дна в состоянии покоя (-70,7 против -78,1; P = 0,015) и во время пробы Вальсальвы (-48,5 против -71,0; P <0,001). Кроме того, разница в показателях лобково-маточного дна в состоянии покоя и во время пробы Вальсальвы также была больше у пациенток с диагнозом хирургического ОМ при обследовании с помощью маточных щипцов (22,2 против 7,1; P < 0,001).
Таблица 2. Измерения, полученные в средне-сагиттальной плоскости в состоянии покоя и при пробе Вальсальвы
| С правильным хирургическим вмешательством по поводу опущения матки (n = 73) | Без правильного хирургического вмешательством по поводу опущения матки (n = 80) | P | 95% ДИ | |
| Измерение лобково-маточного дна | ||||
| Состояние покоя | −70.7 ± 18.8 | −78.1 ± 18.0 | .015 | 1.5; 13.2 |
| Вальсальва | −48.5 ± 21.6 | −71.0 ± 19.7 | <.001 | 15.9; 29.1 |
| Измерение лобково-маточного дна. Разница между состоянием покоя и Вальсальвой | 22.2 ± 15.2 | 7.1 ± 6.8 | <.001 | 11.3; 19.0 |
Данные, полученные для пациенток, были применены к ранее опубликованной модели, которая включает разницу в расстоянии между лобком и дном матки в состоянии покоя и во время пробы Вальсальвы, а также возраст пациентки 25 (Рис. 3). C-индекс Харрелла был получен из AUC (0,89) вероятностей, предсказанных моделью (95% ДИ, 0,84-0,95; P < .0005) (Рис. 4). Калибровка модели была оценена путем расчета калибровочного наклона B, получив коэффициент детерминации 0,95 (95% ДИ, 0,86-1,00) (Рис. 5). На основе ROC-кривой для модели 30% было определено как наиболее подходящую точку отсечения для ультразвуковой диагностики хирургического ОМ с чувствительностью 91,8% и специфичностью 72,7%, что было выше, чем для клинического обследования хирургического ОМ (чувствительность 80,8% и специфичность 71,3%) (Таблица 3).
Рисунок 3
Пример использования бинарной модели, основанной на разнице между лобково-маточным расстоянием в состоянии покоя и при выполнении пробы Вальсальвы, а также на возрасте как предикторе развития ОМ. A, Пациентка в возрасте 45 лет с разницей между лобково-маточной расстоянием в состоянии покоя и при выполнении пробы Вальсальвы 12 мм имеет персонифицированный риск развития ОМ 21,4%. B, Пациентка в возрасте 50 лет с разницей между лобково-маточным дном в состоянии покоя и при проведении пробы Вальсальвы 17 мм имеет персонифицированный риск развития ОМ 74,5%..
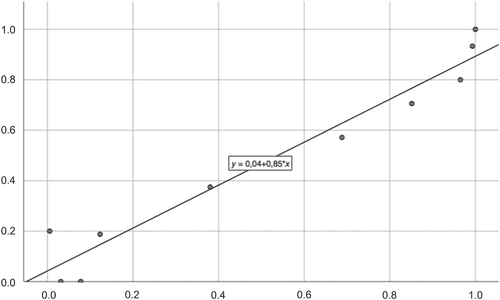
Рисунок 4
ROC-кривая для логистической регрессионной модели, полученная на основе связи между разницей между расстоянием между лобково-маточным дном в состоянии покоя и при выполнении пробы Вальсальвы и возрастом.
Рисунок 5
Калибровочный график оригинальной логистической регрессионной модели, полученной для связи между разницей между расстоянием между лобком и дном матки в состоянии покоя и при выполнении пробы Вальсальвы и возрастом.
Таблица 3. Сравнение диагностических возможностей ультразвукового и клинического обследования
| Чувствительность(%) | 95% ДИ | Специфичность | 95% ДИ | |
| Клиническое опущение матки с критериями к хирургическим показаниям | 80.8 | 69.9; 89.1 | 71.3 | 60.1; 80.8 |
| Ультразвуковое опущение матки с критериями к хирургическим показаниям | 91.8 | 82.9; 96.9 | 72.5% | 61.4; 81.9 |
Обсуждение
Основные выводы заключаются в том, что модель, которая учитывает разницу в расстоянии между лобком и дном матки в состоянии покоя и во время пробы Вальсальвы, а также возраст пациентки, имеет AUC 0,89 и калибровочный наклон 0,95. С помощью этой модели хирургическое ОМ можно определить более надежно, чем при клиническом обследовании, с большей чувствительностью (91,8% против 80,8) и специфичностью (72,7 против 71,3%). Ранее при ультразвуковом исследовании ОМ диагностировали, когда разница между лобково-маточным дном в состоянии покоя и при выполнении пробы Вальсальвы составляла ≥15 мм, с чувствительностью 75%, что ниже, чем в данном исследовании.22 Измерение ≥15 мм разницы расстояния между лобком и дном матки в состоянии покоя и во время пробы Вальсальвы показало в этом многоцентровом исследовании очень хорошую согласованность с клиническими обследованиями для выявления ОМ с использованием системы МКО ПОМ-К с каппа-индексом 0,826 (0,71; 0,94).30 Модель, проверенная в этом исследовании, имеет ряд преимуществ благодаря добавлению изолированной точки отсечения; модель позволяет включать различные ультразвуковые измерения, которые связаны с разным возрастом пациентов. Кроме того, это многоцентровое исследование подтверждает, что эта методика может быть легко применена во время консультаций различными экспертами и в разных центрах, с отличной надежностью между наблюдателями.23
Первые ультразвуковые описания значительных ПОМ среднего отдела базировались на измерении выпячивания шейки матки по отношению к задне-нижнему краю лобка во время пробы Вальсальвы.18 Впоследствии УЗИ было использовано для описания того, как проводить дифференциальную диагностику ПОМ среднего отдела путем измерения разницы в расстоянии между лобком и дном матки в состоянии покоя и во время пробы Вальсальвы.22 Наконец, с помощью этого же измерения можно было создать программное обеспечение для персонализации риска ОМ у пациенток с использованием ультразвуковых измерений и возраста.25 Измерение разницы расстояния между лобком и дном матки в состоянии покоя и во время пробы Вальсальвы позволяет опосредованно оценить уровень Деланси I (прямокишечно-маточно-кардинальный комплекс связи), устанавливая более достоверный диагноз ОМ, чем при клиническом обследовании, как показано в данном исследовании. Одним из объяснений этого результата является то, что система МКО ПОМ-К предоставляет информацию только об анатомической поверхности и использует подвижную точку мягких тканей как референтную (девственную плеву).15 Трансперинеальное УЗИ позволило определить различные патологии, которые могут влиять на дифференциальную диагностику среднего отдела ПОМ.25, 30, 31 Физиологическая основа этих исследований базируется на концепции, что ПОМ связана с поддержанием связок и закрытием щели подъемника.32 Поэтому у пациентов с ПОМ с недостаточной апикальной поддержкой кардинальные связи на 20% больше. Во время выполнения пробы Вальсальвы эти связи у пациентов с ПОМ вдвое длиннее, чем у пациентов с нормальной поддержкой.33 Выявление пациентов с апикальной поддержкой за пределами “нормального диапазона” полезно для избежания ненужного хирургического лечения.31 В этом исследовании мы валидировали ранее опубликованное программное обеспечение, которое диагностирует пациентов с хирургическим ОМ более надежным способом, чем клиническое обследование.25 Другие предыдущие исследования не описывали преимущество ультразвукового исследования над клинической оценкой при ПОМ менее 2 стадии, как определено с помощью ПОМ-К,34 или при симптоматических ПОМ.35 Но наблюдались различные корреляции, от хороших (r = 0,77)36 до плохих результатов.,37 между клиническими обследованиями при ПОМ среднего отдела и ультразвуковым исследованием.
Основное преимущество нашего исследования заключается в том, что проверка этой модели была проведена в многоцентровом исследовании с когортой пациентов, нуждающихся в хирургическом вмешательстве по поводу различных дисфункций тазового дна. Программное обеспечение является простым в применении (Рис. 3), объективным и имеет высокую надежность в выявлении вероятности страданий ОМ,25, 30 что делает его пригодным для использования в типичных клиниках.
Аспект этого исследования, который можно подвергнуть критике, – это метод оценки апикальной поддержки.25 Апикальная поддержка определяется по нижнему концу шейки матки; но мы считаем, что, изучая подвижность матки, мы косвенно оцениваем эту поддержку. Кроме того, условия, в которых проводились ультразвуковые исследования, были очень специфическими. Не исключено, что такое положение может ограничивать выход ПОМ, но не было описано никаких различий между положением дорсальной литотомии и положением стоя при нисходящем выведении ПОМ.38 Можно подумать, что существуют случаи, когда визуализация дна матки может быть затруднена (например, ревертированная матка или ПОМ в заднем отделе). Однако, использование низких частот и модификации усиления ультразвукового аппарата является достаточным для получения изображения дна матки, что позволяет получить отличную межнаблюдательную достоверность при измерении разницы в расстоянии от лобкового симфиза до дна матки в состоянии покоя и во время пробы Вальсальвы.23
Заключения
В заключение, мы проверили программное обеспечение, разработанное с использованием трансперинеального УЗИ тазового дна и возраст пациентки, которое позволяет установить более надежный диагноз, чем при клиническом обследовании для хирургического ОМ.
Ссылки на источники
- Orlicky DJ, Guess MK, Bales ES, et al. Using the novel pelvic organ prolapse histologic quantification system to identify phenotypes in uterosacral ligaments in women with pelvic organ prolapse. Am J Obstet Gynecol 2021; 224: 67.e1–67.e18. https://doi.org/10.1016/j.ajog.2020.10.040.
- Alperin M. Deeper dive into tissue-level events that incite and promote pelvic organ prolapse. Am J Obstet Gynecol 2021; 224: 1–2. https://doi.org/10.1016/j.ajog.2020.11.003.
- Nygaard IE, Wolpern A, Bardsley T, Egger MJ, Shaw JM. Early postpartum physical activity and pelvic floor support and symptoms 1 year postpartum. Am J Obstet Gynecol 2021; 224: 193.e1–193.e19. https://doi.org/10.1016/j.ajog.2020.08.033.
- Luchristt D, Brown O, Kenton K, Bretschneider CE. Trends in operative time and outcomes in minimally invasive hysterectomy from 2008 to 2018. Am J Obstet Gynecol 2021; 224: 202.e1–202.e12. https://doi.org/10.1016/j.ajog.2020.08.014.
- Gabriel I, Kalousdian A, Brito LG, Abdalian T, Vitonis ScM AF, Minassian VA. Pelvic organ prolapse after three modes of hysterectomy: long-term follow up. Am J Obstet Gynecol 2020; 224: 496.e1–496.e10. https://doi.org/10.1016/j.ajog.2020.11.008.
- Jelovsek JE, Gantz MG, Lukacz E, et al. Success and failure are dynamic, recurrent event states after surgical treatment for pelvic organ prolapse. Am J Obstet Gynecol 2021; 224: 362.e1–362.e11. https://doi.org/10.1016/j.ajog.2020.10.009.
- Jelovsek JE, Gantz MG, Lukacz ES, et al. Subgroups of failure after surgery for pelvic organ prolapse and associations with quality of life outcomes: a longitudinal cluster analysis. Am J Obstet Gynecol 2021; 225: 504.e1–504.e22. https://doi.org/10.1016/j.ajog.2021.06.068.
- Nager CW, Visco AG, Richter HE, et al. Effect of sacrospinous hysteropexy with graft vs vaginal hysterectomy with uterosacral ligament suspension on treatment failure in women with uterovaginal prolapse: 5-year results of a randomized clinical trial. Am J Obstet Gynecol 2021; 225: 153.e1–153.e31. https://doi.org/10.1016/j.ajog.2021.03.012.
- Schulten SF, Detollenaere RJ, IntHout J, Kluivers KB, Van Eijndhoven HW. Risk factors for pelvic organ prolapse recurrence after sacrospinous hysteropexy or vaginal hysterectomy with uterosacral ligament suspensión. Am J Obstet Gynecol 2022; 227: 252.e1–252.e9. https://doi.org/10.1016/j.ajog.2022.04.017.
- Schulten SFM, Claas-Quax MJ, Weemhoff M, et al. Risk factors for primary pelvic organ prolapse and prolapse recurrence: an updated systematic review and meta-analysis. Am J Obstet Gynecol 2022; 227: 192–208.
- Bowen ST, Moalli PA, Abramowitch SD, et al. Defining mechanisms of recurrence following apical prolapse repair based on imaging criteria. Am J Obstet Gynecol 2021; 225: 506.e1–506.e28. https://doi.org/10.1016/j.ajog.2021.05.041.
- Husby KR, Gradel KO, Klarskov N. Pelvic organ prolapse following hysterectomy on benign indication: a nationwide, nulliparous cohort study. Am J Obstet Gynecol 2022; 226: 386.e1–386.e9. https://doi.org/10.1016/j.ajog.2021.10.021.
- Mou T, Cadish LA, Gray EL, Bretschneider CE. Cost-effectiveness of prophylactic retropubic sling at the time of vaginal prolapse surgery. Am J Obstet Gynecol 2022; 227: 471.e1–471.e7. https://doi.org/10.1016/j.ajog.2022.05.044.
- Kowalski JT, Wiseman JB, Smith AR, et al. Natural history of lower urinary tract symptoms in treatment-seeking women with pelvic organ prolapse; the Symptoms of Lower Urinary Tract Dysfunction Research Network (LURN). Am J Obstet Gynecol 2022; 227: 875.e1–875.e12. https://doi.org/10.1016/j.ajog.2022.07.038.
- Bump RC, Mattiasson A, Bø K, et al. The standardization of terminology of female pelvic organ prolapse and pelvic floor dysfunction. Am J Obstet Gynecol 1996; 175: 10–17.
- Broekhuis SR, Fütterer JJ, Barentsz JO, Vierhout ME, Kluivers KB. A systematic review of clinical studies on dynamic magnetic resonance imaging of pelvic organ prolapse: the use of reference lines and anatomical landmarks. Int Urogynecol J Pelvic Floor Dysfunct 2009; 20: 721–729.
- Dietz HP, Lekskulchai O. Ultrasound assessment of prolapse: the relationship between prolapse severity and symptoms. Ultrasound Obstet Gynecol 2007; 29: 688–691.
- Shek KL, Dietz HP. What is abnormal uterine descent on translabial ultrasound? Int Urogynecol J 2015; 26: 1783–1787.
- Eisenberg VH, Chantarasorn V, Shek KL, Dietz HP. Does levator ani injury affect cystocele type? Ultrasound Obstet Gynecol 2010; 36: 618–623.
- Green TH Jr. Urinary stress incontinence: differential diagnosis, pathophysiology, and management. Am J Obstet Gynecol 1975; 122: 368–400.
- Chantarasorn V, Dietz HP. Diagnosis of cystocele type by clinical examination and pelvic floor ultrasound. Ultrasound Obstet Gynecol 2012; 39: 710–714.
- García-Mejido JA, Ramos-Vega Z, Armijo-Sánchez A, Fernández-Palacín A, García-Jimenez R, Sainz JA. Differential diagnosis of middle compartment pelvic organ prolapse with transperineal ultrasound. Int Urogynecol J 2021; 32: 2219–2225. https://doi.org/10.1007/s00192-020-04646-1.
- García-Mejido JA, Ramos Vega Z, Armijo Sánchez A, Fernández-Palacín A, Fernández CB, Sainz Bueno JA. Interobserver variability of ultrasound measurements for the differential diagnosis of uterine prolapse and cervical elongation without uterine prolapse. Int Urogynecol J 2021; 33: 2825–2831.
- Dietz HP, Steensma AB. Posterior compartment prolapse on two-dimensional and three-dimensional pelvic floor ultrasound: the distinction between true rectocele, perineal hypermotility and enterocele. Ultrasound Obstet Gynecol 2005; 26: 73–77.
- García-Mejido JA, Ramos-Vega Z, Fernández-Palacín A, et al. Predictive model for the diagnosis of uterine prolapse based on transperineal ultrasound. Tomography 2022; 8: 1716–1725.
- Dietz HP, Simpson JM. Levator trauma is associated with pelvic organ prolapse. BJOG 2008; 115: 979–984.
- Dietz HP, Shek KL. Tomographic ultrasound imaging of the pelvic floor: which levels matter most? Ultrasound Obstet Gynecol 2009; 33: 698–703.
- Orejuela F, Shek KL, Dietz HP. The time factor in the assessment of prolapse and levator ballooning. Int Urogynecol J 2012; 23: 175–178.
- Dietz H. Ultrasound imaging of the pelvic floor. Part 1: two-dimensional aspects. Ultrasound Obstet Gynecol 2004; 23: 80–92.
- García-Mejido JA, González-Diaz E, Ortega I, Borrero C, Fernández-Palacín A, Sainz-Bueno JA. 2D ultrasound diagnosis of middle compartment prolapse: a multicenter study. Quant Imaging Med Surg 2021; 12: 959.
- Swenson CW, Smith TM, Luo J, Kolenic GE, Ashton-Miller JA, DeLancey JO. Intraoperative cervix location and apical support stiffness in women with and without pelvic organ prolapse. Am J Obstet Gynecol 2017; 216: 155.e1–155.e8.
- Chen L, Ashton-Miller JA, DeLancey JO. A 3D finite element model of anterior vaginal wall support to evaluate mechanisms underlying cystocele formation. J Biomech 2009; 42: 1371–1377.
- Luo J, Betschart C, Chen L, Ashton-Miller JA, DeLancey JO. Using stress MRI to analyze the 3D changes in apical ligament geometry from rest to maximal Valsalva: a pilot study. Int Urogynecol J 2014; 25: 197–203.
- Lone FW, Thakar R, Sultan AH, Stankiewicz A. Accuracy of assessing Pelvic Organ Prolapse Quantification points using dynamic 2D transperineal ultrasound in women with pelvic organ prolapse. Int Urogynecol J 2012; 23: 1555–1560.
- Kluivers KB, Jan CM, Shek HC, Dietz HP. Pelvic organ prolapse symptoms in relation to POP-Q, ordinal stages and ultrasound prolapse assessment. Int Urogynecol J 2008; 19: 1299–1302.
- Dietz HP, Haylen BT, Broome J. Ultrasound in the quantification of female pelvic organ prolapse. Ultrasound Obstet Gynecol 2001; 18: 511–514.
- Broekhuis SR, Kluivers KB, Hendriks JCM, Futterer JJ, Barentsz JO, Vierhout ME. POP-Q, dynamic MR imaging and perineal ultrasonography: do they agree in quantification of female pelvic organ prolapse? Int Urogynecol J 2009; 20: 541–549.
- Rodríguez-Mias NL, Subramaniam N, Friedman T, Shek KL, Dietz HP. Prolapse assessment supine and standing: do we need different cutoffs for “significant prolapse”? Int Urogynecol J 2018; 29: 685–689.