Цель. Оценить эффективность измерений жесткости печени и селезенки с помощью акустической лучевой импульсной (ARFI– acoustic radiation force impulse) эластографии с целью неинвазивной оценки фиброза печени и варикозно расширенных вен пищевода у больных с хроническим вирусным гепатитом B.
Методы. Двести шестьдесят четыре участника включены в данное исследование. Из них: 60 были здоровыми добровольцами (классифицируется как стадия 0), 66 были пациенты с хроническим гепатитом B, которые были подвергнутых биопсии печени и 138 были пациенты с циррозом печени, как результат гепатита В. Были получены медианные значения жесткости печени и селезенки (метры в секунду) в результате 10 успешных измерений печени каждого участника. У пациентов с циррозом печени было проведено эндоскопическое исследование верхних отделов желудочно-кишечного тракта.
АВТОРЫ: Xiao-Ping Ye, MM, Hai-Tao Ran, MD, Juan Cheng, MM, Ye-Feng Zhu, MM, Da-Zhi Zhang, MD, Ping Zhang, MD, Yuan-Yi Zheng, MD
Цель. Оценить эффективность измерений жесткости печени и селезенки с помощью акустической лучевой импульсной (ARFI– acoustic radiation force impulse) эластографии с целью неинвазивной оценки фиброза печени и варикозно расширенных вен пищевода у больных с хроническим вирусным гепатитом B.
Методы. Двести шестьдесят четыре участника включены в данное исследование. Из них: 60 были здоровыми добровольцами (классифицируется как стадия 0), 66 были пациенты с хроническим гепатитом B, которые были подвергнутых биопсии печени и 138 были пациенты с циррозом печени, как результат гепатита В. Были получены медианные значения жесткости печени и селезенки (метры в секунду) в результате 10 успешных измерений печени каждого участника. У пациентов с циррозом печени было проведено эндоскопическое исследование верхних отделов желудочно-кишечного тракта.
Результаты. Были обнаружены значимые линейные корреляции между жесткостью печени (коэффициент Спирмена ρ = 0,87, р <0,001) и жесткостью селезенки (коэффициент Спирмена ρ = 0,76; р <0,001) и стадиями фиброза. Значения жесткости печени и селезенки увеличились с прогрессированием фиброза. Тем не менее, были обнаружены наложения значений жесткости печени при стадии 0 и 1, 1 и 2, и наложения значений жесткости селезенки наблюдались при стадии 0 и 1, 1 и 2, а также 2 и 3. Пороговые значения жесткости печени были 1,69 м/с для прогнозирования 3 стадии или выше (площадь под кривой рабочей характеристики приемника = 0,99 [AUROC – area under the receiver operating characteristic curve]) и 1,88 м/с для 4-й стадии (AUROC = 0,97). Пороговое значение жесткости селезенки было 2,72 м/с для 4-й стадии (AUROC = 0,96). Жесткость печени не коррелировала со степенью варикозного расширения вен пищевода, в то же время, была выявлена значительная линейная корреляция (коэффициент Спирмена ρ = 0,65; P <0,001) между жесткостью селезенки и степенью варикозного расширения. Оптимальное пороговое значение жесткости селезенки для прогнозирования варикозного расширения вен пищевода было 3,16 м/с (AUROC = 0,83).
Выводы. Значения жесткости печени и селезенки, измеренные с помощью ARFI эластографии, являются надежными предикторами фиброза печени. Жесткость селезенки, измеренная с помощью ARFI, может быть использована в качестве неинвазивного метода определения наличия и тяжести варикозного расширения вен пищевода. В то же время, доказательства, подтверждающие аналогичную роль для жесткости печени, отсутствуют.
Ключевые слова: акустическая лучевая импульсная эластография; ARFI, сдвиговая волна, shear wave, варикозное расширение вен пищевода; фиброз печени; жесткость печени; жесткость селезенки, купить УЗИ аппарат б/у.
Гепатит В, который вызывается вирусом гепатита В (HBV), представляет собой потенциально опасное для жизни инфекционное заболевание печени, которое является самым серьезным типом вирусного гепатита. Как сообщает Всемирная организация здравоохранения, около 2 млрд. человек были инфицированы вирусом гепатита В во всем мире, и более 350 миллионов человек страдают хроническим гепатитом В. В Китае, гепатит типа B, является наиболее распространенным вирусным гепатитом. Окончательной эволюционной стадией хронического гепатита В является цирроз печени. Портальная гипертензия является одной из основных причин варикозного расширения вен пищевода, которая, по данным литературы, развивается у 90% пациентов с циррозом печени. Ежегодная частота развития варикозного кровотечения составляет от 5% до 15%, а уровень смертности может достигать до 20%.
Лечение и прогноз хронического гепатита зависят от стадии фиброза. На сегодняшний день, биопсия печени – инвазивная техника, до сих пор считается эталоном диагностики. Тем не менее, её клиническое применение ограничено из-за своей инвазивной природы, потенциально серьезных осложнений, ошибочного результата гистологического образца и межисследовательской и внутриисследовательской диагностической вариабельности.
У больных с циррозом настоятельно рекомендуется скрининг варикозно расширенных вен пищевода, который считается чрезвычайно важной задачей, так как это тесно связано со схемой терапии неселективными Бета-адреноблокаторами или эндоскопической профилактикой предотвращения кровотечения из варикозных вен пищевода. В настоящее время методом скрининга является эндоскопия, которая проводится каждые 2-3 года у пациентов без варикозного расширения вен пищевода, каждые 1-2 года у пациентов с умеренным варикозом, и ежегодно у пациентов с декомпенсированным циррозом печени. Тем не менее, этот метод является инвазивным, дорогим и не легко принимается пациентами.
Для преодоления указанных выше ограничений, были предложены некоторые неинвазивные методы, которые могли бы служить в качестве маркеров для оценки степени фиброза печени и варикозного расширения вен пищевода. Среди методов были предложены: оценка сывороточных маркеров, транзиентная (Fibroscan) эластография, магнитно-резонансная эластография и акустическая лучевая импульсная (ARFI) эластография.
Акустическая лучевая импульсная визуализация является новой технологией, которая основана на обычной сонографии в B-режиме. Акустический толчковый импульс возбуждает ткани и генерирует сдвиговые волны, которые распространяются от ткани. Распространение сдвиговых волн могут быть измерены, и их скорость зависит от эластичности ткани. Поэтому ARFI обеспечивает числовыми измерениями жесткости ткани в виде скорости сдвига волны, которая выражается в метрах в секунду. Публикации в медицинской литературе показали, что значения жесткости печени хорошо коррелируют со стадией фиброза печени, которая определяется при инвазивной биопсии печени. Об измерениях жесткости селезенки с помощью ARFI эластографии у больных с хроническим заболеванием печени также было ранее доложено. Однако эти исследования сосредоточены в основном на пациентах инфицированных вирусом гепатита С (HCV).
Целью данного исследования было оценить точность измерений жесткости печени и селезенки с помощью ARFI эластографии для неинвазивной оценки фиброза печени у пациентов с хроническим гепатитом В, а также исследовать возможность использования значений жесткости печени и селезенки, в качестве прогностических критериев наличия и выраженности варикозного расширения вен пищевода.
МАТЕРИАЛЫ И МЕТОДЫ
Исследуемая популяция
Двести шестьдесят четыре участника (158 мужчин и 106 женщин, средний возраст ± SD (стандартное отклонение) – 39,3 ± 13,7 лет, диапазон – 19-74 лет) были зарегистрированы в нашем исследовании в период с июня по ноябрь 2011 года. Из этих участников, 60 были здоровыми пациентами – контрольная группа (не имели клинических признаков фиброза: стадия 0, средний возраст – 30,0 ± 9,0 лет; диапазон – 20-54 лет), 204 пациента имели хронический гепатит B. Информированное согласие было получено от всех участников, а местный Комитет по этике одобрил наше исследование.
Участники группы контроля были здоровыми добровольцами без какого-либо заболевания печени или пациентами из других отделений нашей больницы, которые имели нормальные результаты серологических анализов печени и нормальную сонографическию картину печени. Пациенты с увеличенной селезенкой по данным сонографии, с заболеваниями, поражающими печень, или регулярно употребляющие алкоголь, были исключены из исследования.
Среди 204 пациентов, 66 из них (средний возраст – 36,5 ± 10,9 года, диапазон – 19-63 лет) подверглись биопсии печени, в то же время 138 пациентам (средний возраст – 46,1 ± 10,9 лет, диапазон – 26-74 лет) уже был предварительно поставлен диагноз цирроз печени (4стадия) с помощью методов визуализации или биохимического анализа, или на основании их истории болезни. Пациенты были исключены из исследования, если они имели асцит, онкологические заболевания, болезни в терминальной стадии, аутоиммунные заболевания, были инфицированы другими вирусами печени или вирусом иммунодефицита человека, или в случае беременности.
Все пациенты прошли ARFI эластографию как печени, так и селезенки, а также на каждого участника были рассчитаны и выражены в метрах в секунду средние значения жесткости 10 успешных измерений. Пациенты с циррозом прошли эндоскопическое исследование для оценки варикозного расширения вен пищевода. Были отмечены серологические результаты исследований.
Измерения жесткости печени и селезенки
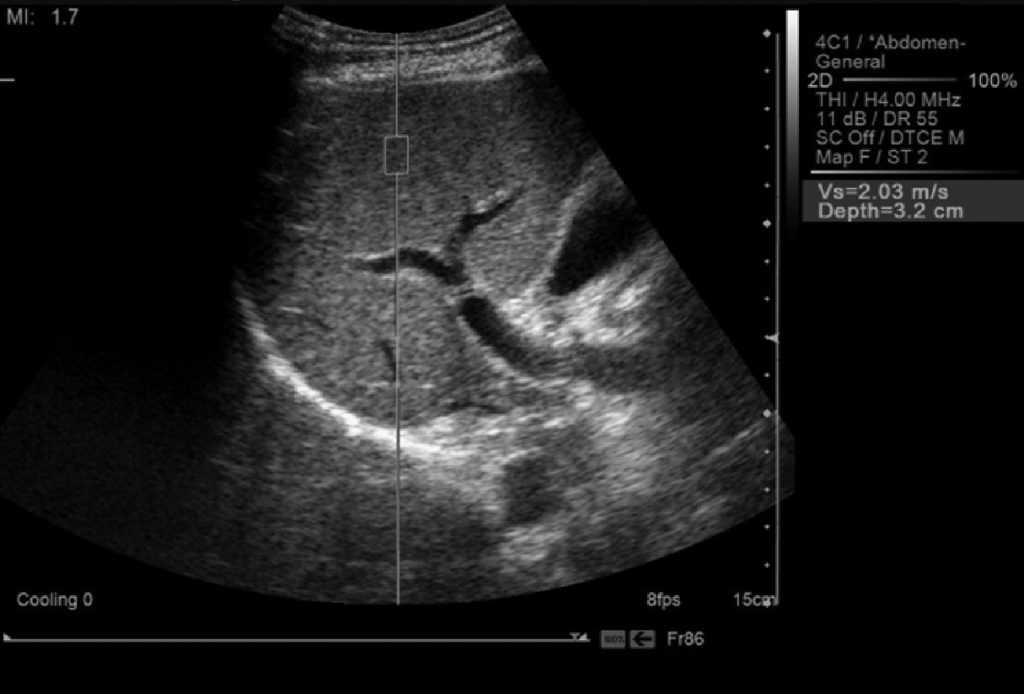
Измерения жесткости печени и селезенки были выполнены с помощью ультразвуковой системы Acuson S2000, которая оборудована программным обеспечением количественной оценки жесткости ткани – virtual touch tissue quantification (Siemens Medical Solutions, Mountain View, CA). Использовался конвексный датчик 4C1. Для проведения этого исследования можно также купить УЗИ для смартфона. Жесткость печени измеряли у пациентов, которые располагались в положении лежа на левом боку, правая рука находилась в максимальном приведении, в то время как жесткость селезенки измеряли у пациентов, которые лежали в положении лежа на правом боку и их левая рука находилась в максимальном приведении. Размер области интереса (ROI) был зафиксирован на уровне 10×5 мм. Область интереса была в паренхиме печени и селезенки в зоне, свободной от «видимых» сосудов. В частности, расположение области интереса в печени было в правой доле между седьмым и девятым межреберьем и между среднеключичной и среднеподмышечной линиями, от 2 до 3 см ниже капсулы печени; в свою очередь, в селезенке зона располагалась в средней ее части, от 1 до 2 см ниже селезеночной капсулы. Эти измерения были проведены через межреберье. Во время процедуры пациентов просили задержать дыхание на короткий промежуток в конце выдоха. Проводилось два или три измерения в течение каждого периода задержки дыхания, при этом было необходимо 4, 5 или более периодов для измерения в пределах одной области. Все измерения были выполнены одним опытным сонографистом (рисунки 1 и 2).
Рис. 1. Акустическая лучевая импульсная эластография – измерения жесткости в правой доли печени у 45-летнего мужчины с 4-й стадией фиброза. Область интереса была расположена на 2,1 см ниже капсулы печени и на 3,2 см ниже кожи. Скорость сдвига волны 2,03 м/с.
Рис. 2. Акустическая лучевая импульсная эластография – измерения жесткости в средней части селезенки 48-летнего мужчины с 4-й стадией фиброза. Область интереса располагалась на 1,7 см ниже селезеночной капсулы и на 3,2 см ниже кожи. Скорость сдвига волны была 4,07 м/с.
Интервал между этими измерениями и биопсией печени, которая выполнена 66 участникам исследования колебался от 1 до 3 дней (в среднем, 2,00 ± 0,84 дней). Акустическая лучевая импульсная визуализация выполнялась не сразу после биопсии, так как пациенты не были бы в состоянии терпеть боль, вызванную биопсией и сканирование сразу после процедуры, и потому им необходимы было время для отдыха в положении лежа на спине с монитором в течение первых 6 часов.
Правая доля была выбрана потому, что ARFI измерения правой доли, по данным литературы, потенциально превосходят таковые в левой доли для диагностики фиброза печени. Была выбрана точка от 2 до 3 см под капсулой печени, так как исследование 3 точек под капсулой печени (0-1, 1-2 и 2-3 см) обнаружило, что наиболее надежные значения эластичности печени получены при проведении ARFI измерений, которые проведены от 2 до 3 см под капсулой печени.
Гистологический анализ печени
Биопсия печени под сонографическим наведением проводилась у 66 больных с автоматически пистолетом для биопсии Magnum (C. R. Bard, Inc, Murray Hill, NJ) и иглы 16 калибра. Все образцы были длиной не менее 1,5 см и анализировались одним опытным патологоанатомом. Фиброз был поставлен по шкале от 0 до 4 следующим образом: стадия 0, нет фиброза; 1-я стадия, фиброзное портальное распространение и ограниченный перисинусоидальный или очаговый фиброз; 2-я стадия, перипортальный фиброз и несколько фиброзных септ, но интактная архитектура; 3-я стадия, многочисленные фиброзные септы с архитектурным искажением, но без очевидного цирроза; и 4-я стадия, цирроз печени.
Эндоскопическое исследование верхних отделов желудочно-кишечного тракта
Семьдесят три пациента с циррозом были готовы пройти эндоскопию, и они исследовались под внутривенным наркозом. Пищеводные вариксы были оценены с использованием GIF-XQ-2400 эндоскопа (Olympus Optical Co, Ltd, Токио, Япония). Вариксы оценивались следующим образом: 1-я степень, средняя, характеризуется как прямые вариксы без красных пятен; 2-я степень, умеренная, характеризуется как прямые вариксы с красными пятнами или возвышения извилистых вариксов без красных пятен; и 3-я степень, тяжелая, характеризуется как возвышения извилистых вариксов с красными пятнами или вариксы в форме спирали.
Биохимические маркеры сыворотки
Образцы венозной крови были взяты у всех участников после ночного голодания (8-12 часов) в тот же день, что и измерения ARFI. Образцы тестировались в той же лаборатории, при этом определяли уровни аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (AЛT).
Статистический анализ
Статистический анализ проводили с помощью программного обеспечения SPSS версия 19.0 (SSPS Inc, Chicago, IL); α = 0,05 считалось уровнем значимости. Количественные переменные жесткости печени были выражены как среднее ± стандартное отклонение (± SD). Диаграммы были использованы для иллюстрации распределения различных параметров. Levene тест был использован для исследования однородности дисперсии. Анализ дисперсии и т-тест наименьшей значимой разницы были использованы для сравнения различий в средних значениях жесткости печени у больных циррозом в зависимости от степени варикозного поражения. Тест Крускала-Уоллиса и тест Манна-Уитни U с поправкой Бонферрони (со скорректированным уровнем значимости а = 0,005) были использованы для сравнения различий в средних значениях жесткости печени в соответствии со стадией фиброза. Мы использовали независимый т-тест, чтобы сравнить значения жесткости печени между циррозом у пациентов с и без варикоза, а также у пациентов с циррозом с нормальным и повышенным уровнем АЛТ и АСТ. Количественные переменные жесткости селезенки анализировались таким же образом.
Диагностическую эффективность оценивали по чувствительности, специфичности и кривой рабочей характеристики приемника. Были выбраны оптимальные пороговые значения с целью максимизировать результирующую чувствительности и специфичности. Корреляция между различными параметрами была проанализирована с помощью коэффициентов корреляции Спирмена.
Результаты
Характеристики исследуемой популяции
Клинические и биохимические характеристики 264 участников приведены в таблице 1.
Таблица 1. Клинические и биохимические характеристики участников исследования
| Характеристика | Значение |
| Мужчин, n (%) | 158 (59.85) |
| Возраст, лет | 39,3 ± 13,7 |
| ИМТ, кг/м2 | 21,90 ± 2,87 |
| АСТ, Ед/л | 84,14 ± 99,08 |
| AЛT, U/L | 99,25 ± 120,13 |
Значения представляют собой среднее ± SD, где применимо. AЛT – аланинаминотрансфераза; АСТ – аспартатаминотрансфераза, а ИМТ – индекс массы тела
Из 66 пациентов, перенесших биопсию печени, 17 имели 1-ю стадию фиброзом; 23 имели 2-ю стадию; 23 имели 3-ю стадию и 3 имели 4-ю стадию. У 60 здоровых участников контроля были 0-я стадия. У 138 пациентов с циррозом были выставлена 4-я стадия.
Измерения жесткости печени для неинвазивной оценки фиброза печени
Жесткость печени измеряли у всех 264 участников исследования. Значительная линейная корреляция (коэффициент Спирмена ρ = 0,87; р <0,001) была обнаружена между жесткостью печени и стадией фиброза. В целом, наблюдалось значительное увеличение жесткости печени параллельно с прогрессированием фиброза печени. Тем не менее, различия между стадиями 0 и 1 (P = 0,018) и между стадиями 1 и 2 (P = 0,011) не были обнаружены. Статистические различия были обнаружены в следующих группах: стадия 0 против 2 (P <0,001), стадия 0 против 3 (P <0,001), стадия 0 против 4 (P <0,001), 1-й стадии по сравнению с 3 (P <0,001), 1-й стадии по сравнению с 4 (P <0,001), 2-я стадия против 3 (P <0,001), 2-я стадия по сравнению с 4 (P <0,001) и 3-я стадии против 4 (P <0,001). Значение жесткости печени для каждой стадии фиброза показано в таблице 2, а диаграмма показана на рисунке 3.
Таблица 2. Жесткость печени и селезенки в соответствии со стадиями фиброза.
| Стадии | Случаи, n | Жесткость печени, м/с | Жесткость селезенки, м/с |
| 0 | 60 | 1.13 ± 0.12 | 2.17 ± 0.22 |
| 1 | 17 | 1.27 ± 0.21 | 2.27 ± 0.21 |
| 2 | 23 | 1.50 ± 0.28 | 2.38 ± 0.31 |
| 3 | 23 | 1.85 ± 0.34 | 2.54 ± 0.46 |
| 4 | 141 | 2.50 ± 0.50 | 3.24 ± 0.44 |
Значения представляют собой среднее ± SD.
Рис 3. Изменение скорости сдвига волны в печени в зависимости от стадии фиброза (S). Средняя линия в каждой коробке представляет собой медиану. Верхняя и нижняя части представляют собой первый и третий квартили. Столбики ошибок показывают минимальные и максимальные значения (диапазон). Статистические различия были проанализированы с помощью теста Крускала-Уоллиса с поправкой Бонферрони. Скорость сдвига волны в печени возрастает по мере прогрессирования фиброза.
Анализ площади под кривой рабочей характеристики приемника (AUROC) показал, что ARFI измерения жесткости печени имели высокие прогностические значения для 3-й стадии или более высокой (AUROC = 0,99; Рис 4) и 4-й стадии (AUROC = 0,97; Рис 5).
Рис 4. Кривая рабочей характеристики приемника жесткости печени, измеренной с помощью акустической лучевой импульсной эластографии для прогнозирования фиброза 3-й стадии или более высокой (стадии 0-2 по сравнению со стадиями 3 и 4).
Рис 5. Кривая рабочей характеристики приемника жесткости печени, измеренной с помощью акустической лучевой импульсной эластографии для прогнозирования 4-й стадии фиброза (стадии 0-3 по сравнению с 4-й стадией).
Оптимальные пороговые значения были 1,69 м/с для 3-й стадии или более высокой (чувствительность – 93,9%; специфичность – 95,0%) и 1,88 м/с для 4-й стадии (чувствительность – 95,7%; специфичность – 91,8%).
Измерения жесткости селезёнки для неинвазивной оценки фиброза печени
Селезенка была оценена у всех 264 участников исследования. Значимая корреляция наблюдалась (коэффициент Спирмена ρ = 0,76; P <0,001) между жесткостью селезенки и стадиями фиброза. Статистически значимые различия между 4-й стадией и другими подгруппами были отмечены следующим образом: стадия 0 против 4 (P <0,001), стадия 1 против 4 (P <0,001), 2-я стадия по сравнению с 4 (Р <0,001), и 3-я стадия против 4 (P <0,001). В противоположность этому, различия не были найдены между любыми двумя подгруппами стадий от 0 до 3: 0 стадия по сравнению с 1 (P =0,374), стадия 0 против 2 (P =0,021), стадия 0 по сравнению с 3 (P = 0,006), 1-я стадия по сравнению со 2 (P =0,293), 1-я стадии против 3 (P =0,072) и 2-я стадия по сравнению с 3 (P =0,620). Величина жесткости селезенка для каждой стадии фиброза показано в таблице 2, и диаграмме на рисунке 6.
Рис 6. Изменение скорости сдвига волны селезенки в зависимости от стадии фиброза (S). Статистические различия были проанализированы с помощью теста Крускала-Уоллиса с поправкой Бонферрони. Скорость сдвига волны селезенки минимально изменяется от 0 до 3 стадии, но значительно выше при 4-й стадии, чем в любой другой подгруппе.
Анализ площади под кривой рабочей характеристики приемника показал, что жесткость селезенки была высоко эффективным показателем в прогнозировании наличия цирроза (стадия 4; AUROC = 0,96; Рис 7). Оптимальное пороговое значение 2,72 м/с (чувствительность – 88,4%; специфичность – 93,2%).
Рис 7. Кривая рабочей характеристики приемника жесткости селезенки, измеренной с помощью акустической лучевой импульсной эластографии для прогнозирования 4-й стадии фиброза (стадии 0-3 по сравнению с 4-й стадией).
Комбинированный анализ жесткости печени и селезенки для прогнозирования цирроза
Значения жесткости печени и селезенки были объединены для прогнозирования цирроза с использованием пороговых значений, которые были получены в данном исследовании: чувствительность и специфичность составили 99,3% и 92,7%, соответственно, когда один из методов дал положительный результаты, и 88,7% и 100%, когда оба метода дали положительные результаты.
Измерения жесткости печени и селезенки для прогнозирования варикозного расширения вен пищевода
Из 141 пациентов с циррозом, 73 согласились пройти эндоскопию. Наличие варикозного расширения вен пищевода было исключено у 25 пациентов, и они были отнесены к категории класса 0. Количество пациентов с варикозом приведены в таблице 3.
Таблица 3. Жесткость печени и селезенки в соответствии со степенью расширения вен пищевода.
| Вариксы | Случаи, n | Жесткость печени, м/с | Жесткость селезенки, м/с |
| Отсутствие | 25 (34.25) | 2.46 ± 0.42 | 2.94 ± 0.35 |
| Наличие (всего) | 48 (65.75) | 2.65 ± 0.49 | 3.44 ± 0.38 |
| 1 степень | 11 (15.07) | 2.65 ± 0.40 | 3.15 ± 0.35 |
| 2 степень | 16 (21.91) | 2.65 ± 0.53 | 3.38 ± 0.29 |
| 3 степень | 21 (28.77) | 2.65 ± 0.52 | 3.63 ± 0.37 |
Значения представляют собой среднее ± SD.
Не выявлено никакой корреляции между жесткостью печени и степенью варикозного расширения вен. Статистической разницы не наблюдалось между средними значениями жесткости печени у пациентов с и без варикоза (P = 0,107), или между 1 и 2 степенью (р = 0,985), также степенью 1 и 3 (р = 0,997), а также 2-й и 3-й степенью (p = 0,980). Средняя значение жесткости печени для каждой степени варикозного расширения вен пищевода показано в таблице 3. Тем не менее, значительная прямая линейная корреляция (коэффициент Спирмена ρ = 0,65; р <0,001) была обнаружена между жесткостью селезенки и степенью варикозного расширения вен. Статистические различия были обнаружены между группами с и без варикоза (Р <0,001), между 1 и 3 (P =0,001) степенями, а также между 2 и 3 степенями (P = 0,041). Однако, не было найдено никакой разницы между 1 и 2 степенями (Р = 0,093). Среднее значение жесткости селезенки для каждой степени варикозного расширения вен приведено в таблице 3. AUROC жесткости селезенки для прогнозирования наличия варикозного расширения вен пищевода (рисунок 8) и 3-й степени (рисунок 9) были 0,83 и 0,83, соответственно. Оптимальные пороговые значения были 3,16 м/с для прогнозирования наличия варикозно расширенных вен (чувствительность – 84,1%; специфичность – 81,0%) и 3,39 м/с для 3-й степени (чувствительность – 78,9%; специфичность – 78,3%).
Рис 8. Кривая рабочей характеристики приемника жесткости селезенки, измеренной с помощью акустической лучевой импульсной эластографии для прогнозирования наличия варикозного расширения вен пищевода.
Рис 9. Кривая рабочей характеристики приемника жесткости селезенки, измеренной с помощью акустической лучевой импульсной эластографии для прогнозирования наличия тяжелого (3 степени) варикозного расширенния вен пищевода.
Взаимосвязь между показателями жесткости печени и селезенки и биохимических маркеров сыворотки крови
Для оценки влияния уровней АЛТ и АСТ, мы разделили пациентов с циррозом на две группы: первая группа включала пациентов с нормальным уровнем АЛТ и АСТ, а вторая группа включала пациентов с повышенным уровнем АЛТ и АСТ. Средние значения жесткости печени и селезенки для каждой группы, приведены в таблице 4.
Таблица 4. Жесткость печени и селезенки при различных уровнях аланинаминотрансферазы и аспартатаминотрансферазы у пациентов с циррозом
| Параметр | Нормальный уровень AЛT и AСT | Повышенный уровень АСТ и АСТ | Р |
| Жесткость печени, м/с | 2,32 ± 0,45 | 2,61 ± 0,51 | 0,001 |
| Жесткость селезенки, м/с | 3,19 ± 0,47 | 3,27 ± 0,46 | 0,368 |
Значения представляют собой среднее ± SD. AЛT – аланинаминотрансфераза; а АСТ – аспартатаминотрансфераза.
Мы обнаружили значительную разницу между значениями жесткости печени в обеих группах. В таблице 4 показано, что у пациентов с повышенным уровнем АЛТ и АСТ имелись более высокие значения жесткости печени. И наоборот, различие не было статистически значимым между значениями жесткости для селезенки в этих группах.
ОБСУЖДЕНИЕ
Стадия фиброза печени может быть определена количественно с помощью ARFI эластографии. Недавние исследования показали, что измерение жесткости печени с использованием ARFI эластографии является новым, точным и надежным неинвазивным методом для оценки фиброза печени у пациентов с хроническим заболеванием печени. С прогрессированием фиброза печени, можно найти гемодинамические и патологические изменения в селезенке, особенно на поздних стадиях фиброза. В одном из исследований обнаружено, что размер селезенки увеличивался с прогрессированием фиброза печени, и был более выражен на поздних стадиях. Плотность селезенки, у пациентов с увеличенной селезенкой, изменяется из-за гиперплазии ткани, фиброза, портального и селезеночного застоя. Такие изменения в селезенке являются механическими свойствами, которые могут быть количественно оценены с помощью ARFI эластографии. Поэтому мы попытались показать, что значения жесткости печени и селезенки являются полезными прогностическими показателями для оценки фиброза печени при хроническом заболевании печени, а также оценить их эффективность в прогнозировании наличия варикозно расширенных вен пищевода у больных с циррозом. К тому же, насколько нам известно, об исследовании оценки фиброза печени и варикозного расширение вен пищевода, конкретно у HBV-инфицированных больных, не сообщалось ранее.
Полученные нами данные ясно показали, что жесткость печени хорошо коррелирует с фиброзом. Жесткость увеличивается со стадией фиброза. Тем не менее, были обнаружены наложение данных между стадиями 0 и 1 и стадиями 1 и 2. Подобно исследованию 112 пациентов с хроническим гепатитом C было обнаружено наложение данных между последовательными стадиями F1 и F2 и стадиями F2 и F3 (шкала METAVIR). Еще в одном исследовании 103 пациентов с хроническим гепатитом различной этиологии наблюдается наложение данных между стадиями F0 и F1 и стадиями F3 и F4 (шкала METAVIR). Эти данные свидетельствуют о том, что наложение данных между последовательными стадиями происходит независимо от этиологии. Для здоровых добровольцев (стадия 0), среднее значение жесткости печени в нашем исследовании было 1,13 ± 0,12 м/с, что сопоставимо с данными, опубликованными до сих пор: 1,13 ± 0,23 м/с у здоровых добровольцев и 1,16 ± 0,17 м/с стадия F0 у пациентов (шкала METAVIR) и 1,15 ± 0,21 м/с в другой группе здоровых добровольцев. Для пациентов с циррозом, среднее значение жесткости печени – 2,50 ± 0,50 м/с, что сопоставимо с 2,38 ± 0,74 м/с у 81 пациентов с HCV или HBV инфекцией и 2.552 ± 0,7782 м/с у больных с HCV инфекцией.
Мы обнаружили высокие результаты прогностических значений жесткости печени для 3-й стадии или более высокой, и 4-й стадии, которые были сходны с результатами в исследовании пациентов с хроническими гепатит С и исследованием пациентов с различной этиологией. Пороговое значение для 3-й стадии или более высокой было 1,69 м/с, которое было таким же, как и значение в исследовании Toshima и др., которое включало 79 пациентов с различной этиологией, а также было подобно значению в исследовании Lupsor и др., которое включало 112 пациентов с хроническим гепатитом С (1,61 м/с). Пороговое значение для 4-й стадии было 1,88 м/с, что несколько выше, чем значение в исследовании Toshima и др. (1,79 м/с) и ниже, чем значение в исследовании Lupsor и др. (2,0 м/с).
В данном исследовании сравнивали средние значения жесткости селезенки, измеренные при ARFI эластографии у пациентов от 0 до 4 стадиями фиброза. Выявлена корреляция между жесткостью селезенки и фиброзом (коэффициент Спирмена р = 0,76, р <0,001). Значения жесткости селезенки для стадий от 0 до 3 не различаются статистически, в то же время, при 4-й стадии среднее значение было значительно выше, чем при любой другой стадии. В нашем исследовании среднее значение жесткости селезенки у здоровых добровольцев (стадия 0) составило 2,17 ± 0,24 м/с, что несколько выше, чем полученное ранее значение – 2,04 ± 0,28 м/с у 15 здоровых добровольцев, и ниже, чем полученное ранее значение – 2,44 м/с у 35 здоровых добровольцев. Среднее значение жесткости селезенки у больных циррозом (стадия 4) составило 3,24 ± 0,44 м/с, что несколько выше, чем значение 3,10 ± 0,55 м/с в исследовании по Bota и др.
На сегодняшний день доступно только 2 источника, в котором проанализирована жесткость селезенки для прогнозирования цирроза. Один показал пороговое значение 2,55 м/с для прогнозирования цирроза с хорошей AUROC (0,91), и другой показал пороговое значение 2,73 м/с (AUROC = 0,82). Наши результаты показали высокую прогностическую ценность в определении цирроза (AUROC = 0,96), с пороговым значением (2,72 м/с), которая выше, чем в первом исследовании, и аналогична со вторым.
В этом исследовании комбинированный анализ жесткости печени и селезенки, измеренный с помощью ARFI для прогнозирования наличия цирроза печени, показал, что чувствительность и специфичность была выше, когда один из способов, описанных в сводном анализе, давал положительные результаты, чем в случае использования только одного метода, а специфичность была значительно выше в случае, когда оба метода давали положительные результаты.
У больных циррозом, тяжелым осложнением является портальная гипертензия, которая является фактором, способствующим формированию варикозно расширенных вен пищевода и служит прямой причиной варикозного кровотечения. В литературе сообщается, что жесткость печени, измеренная с использованием 1-мерной транзиторной эластографии (Fibroscan) показала статистически значимую связь с градиентом печеночного венозного давления. Некоторые исследования показали, что жесткость печени, измеренная с помощью 1-мерной транзиторной эластографии коррелировала с со степенью пищеводных вариксов, в то время как другие исследования показали, что жесткость печени коррелирует с наличием вариксов, но имеют слабую корреляцию с размеров вариксов или не имеют совсем. Акустическая лучевая импульсная эластографии является 2-мерной эластографической техникой. Насколько нам известно, не было еще сообщений об соотношении между жесткостью печени, измеренной с помощью ARFI и градиентом печеночного венозного давления или между жесткостью печени, измеренной с помощью ARFI и наличием варикозного расширения вен пищевода. Только одно исследование сообщает о корреляции между жесткостью селезенки, которое измерено с помощью ARFI, и варикозным расширением вен пищевода, в котором авторы не выявили существенных различий в средних значениях жесткости селезенке между пациентами с различными степенями варикоза и без него.
Наши данные по этому вопросу были неоднозначными. Мы обнаружили корреляцию между жесткостью селезенки и стадиями варикозного расширения вен пищевода и значительную разницу между пациентами с и без варикоза. Мы определили пороговую величину – 3,16 м/с для прогнозирования наличия варикозно расширенных вен пищевода (AUROC = 0,83). Мы также обнаружили существенную разницу между 2 и 3 степенью, но, к сожалению, мы не смогли выделить средние значения жесткости селезенки между 1 и 2 степенями. Эти результаты могут быть объяснены тремя возможными причинами. Во-первых, эндоскопическое исследование не была выполнено одними и теми же врачами, а в то же время оценка степени варикозного расширения вен субъективна. Во-вторых, не все пациенты согласились пройти эндоскопии и ARFI эластографию в тот же день; интервал между измерениями жесткости селезенки и эндоскопией колебался в диапазоне от 0 до 30 дней, в то время как самый длинный интервал в докладе Bota и др. доходил до 6 месяцев. В-третьих, распределение больных по степени варикозного расширения было неравномерным.
Наша статья ясно показывает, что не существует корреляция между жесткостью печени, которая измеряется с помощью ARFI и степенью варикозного расширения вен пищевода, а также не выявлено существенных различий среди степеней варикоза. Различные результаты между показателями жесткости печени и селезенки для оценки варикоза можно объяснить 2 возможными причинами. Во-первых, мы обнаружили, что у больных циррозом печени, с повышенным уровнем АЛТ и АСТ, были более высокие значения жесткости печени, чем у пациентов с нормальным уровнем АЛТ и АСТ. В то же время, разница не была значимой для значений жесткости селезенки между пациентами с нормальным уровнем АЛТ и АСТ, и пациентами, с повышенным уровнем АЛТ и АСТ. Некоторые издания сообщали о корреляции между значениями жесткости печени, которые измерены с помощью ARFI, и некровоспалением. Эти данные показывают, что повышенные уровни АЛТ и АСТ могут повлиять на печень, но не на значения жесткости селезенки, которые могут быть основным фактором, обусловливающим вышеупомянутые результаты. Во-вторых, неравномерное распределение пациентов согласно степени варикозного расширения вен пищевода, возможно, привело к различному количеству в каждой подгруппе.
В заключение, значения жесткости печени и селезенки, измеренные с помощью ARFI эластографии являются надежными предикторами фиброза печени, особенно для пациентов, которые подвергаются высокому риску или не готовы пройти биопсию печени. Жесткость селезенки может быть использована в качестве неинвазивного средства для прогнозирования наличия и степени варикозного расширения вен пищевода, а также может быть полезным инструментом для пациентов, которые отказываются пройти эндоскопию. Кроме того, были запланированы дальнейшие исследования по изучению жесткости печени и селезенки для оценки фиброза печени и варикозного расширения вен пищевода в большей группе населения. Для проведения исследований рекомендуем использовать аппарат от компании GE Voluson E8.














14.10.2019
Денис