АВТОРЫ: Simona Bota, Ioan Sporea, Roxana Sirli, Alina Popescu, Mirela Danila, Ana Jurchis, Oana Gradinaru-Tascau
Отделение гастроэнтерологии и гепатологии “Victor Babes” университета медицины и фармации, Тимишоара, Румыния
Ключевые слова: ARFI эластография, сдвиговая волна, жесткость печени, фиброз печени, надежные измерения, неудачные измерения, ненадежные измерения
Резюме
Введение: акустическая лучевая импульсная визуализация (ARFI) является неинвазивным методом эластографии сдвиговой волны для оценки фиброза печени.
Цель: оценить целесообразность применения ARFI эластографии в большой группе пациентов и выявить факторы, связанные с невозможностью получить надежные измерения жёсткости печени (liver stiffness – LS) с помощью этой техники.
Методы: в наше ретроспективное исследование были включены 1031 взрослых пациентов с, или без хронического заболевания печени. У каждого субъекта оценивали LS с помощью ARFI эластографии. Неудачными измерения ARFI считались в том случае, если не одного успешного измерения не было получено после того, как, по меньшей мере, проведено 10 попыток, и ненадежными в следующих ситуациях: менее 10 успешных измерений; среднее значение 10 успешных измерений имело вероятность успешных попыток (success rate – SR) <60%, и/или межквартильный интервальный диапазон (interquartile range interval – IQR) ≥ 30%.
Результаты: Неудачные измерения LS при помощи ARFI зарегистрированы у 4 пациентов (0,3%), ненадежными измерениями были у 66 пациентов (6,4%), соответственно, надежные измерения были получены у 961 пациентов (93,3%). При мономерном анализе следующие факторы риска были связаны с неудачными и ненадежными измерениями: возраст старше 58 лет (OR = 0,49; 95% ДИ 0.30-0.80, р = 0,005), мужской пол (OR = 0,58; 95% ДИ 0.34-0.94 , р = 0,04), ИМТ> 27,7 кг/м2 (OR = 0,23, 95% ДИ 0.13-0.41, р <0,0001). При многомерном анализе все факторы, упомянутые выше, были независимо связаны с риском неудачных и ненадежных измерений.
Выводы: надежные измерения LS с помощью ARFI эластографии были получены в 93,3% случаев. Пожилой возраст, более высокий индекс массы тела и мужской пол были связаны с риском неудачных попыток или ненадежных измерений, но их влияние ограничено в сравнении с транзиторной эластографией.
Введение
Акустическая лучевая импульсная визуализация (ARFI) является неинвазивным методом эластографии для оценки фиброза печени, эффективным для прогнозирования значительного и выраженного фиброза и показывает отличные результаты для прогнозирования цирроза печени. Этот метод эластографии эффективно применяется также в других органах, таких как: селезенка, щитовидная железа, молочная железа, почки и простата.
Принцип ARFI эластографии основан на компрессии исследуемой ткани, что вызывает в твердых тканях меньшую деформацию, чем в мягких тканях. Ультразвуковой датчик автоматически производит акустический “PUSH”(толчковый) импульс, что генерирует поперечные волны, которые распространяются в тканях. Их скорость, измеренная в м/с, отображается на экране. Кроме того, скорость сдвиговой волны может быть определена количественно, в точной анатомической области, сфокусировано в исследуемой зоне, с заданным размером (10 мм в длину и 5 мм в ширину), который предоставляется системой.
Опубликованные исследования показали высокий процент пациентов, у которых жесткость печени (liver stiffness – LS) может быть оценена с помощью ARFI эластографии, но не существует доступных данных относительно факторов, связанных с невозможностью получения надежных измерений LS с помощью этой эластографической техники.
Цель данного исследования состояла в том, чтобы оценить эффективность применения ARFI эластографии в большой группе пациентов и выявить факторы, связанные с невозможностью получать достоверные LS измерения с помощью этой техники.
Материалы и методы
2.1. Исследуемые пациенты
В наше ретроспективное исследование были включены 1031 взрослых пациентов с, или без хронического заболевания печени, которые обследовались в нашем отделении в период с октября 2009 по декабрь 2012 года. В наше исследование мы включили: здоровых добровольцев (были определены как субъекты без анамнеза патологии печени, с нормальной сонографической картиной брюшной полости, но дополнительные тесты, такие как анализ аминотрансфераз или вирусных маркеров не выполнялись); пациентов с хроническим гепатитом В и С оценивали с помощью ARFI эластографии и биопсии печени (liver biopsy – LB); пациенты с диагнозом цирроз печени, поставленным с помощью клинических, биологических, ультразвуковых, эндоскопических и/или лапароскопических критериев; пациенты с асцитом без цирроза, в том числе больные с выявленным перитонеальным карциноматозом с гистологическим подтверждением, с острым панкреатитом с асцитом, который позже исчезал, лимфатическим асцитом; и пациенты с очаговыми поражениями печени при отсутствии хронического заболевания печени.
Во время измерений ARFI, помимо эпидемиологических и демографических данных, у всех пациентов, включенных в наше исследование, за исключением здоровых добровольцев, определялись следующие сывороточные биологические параметры: аминотрансферазы, щелочная фосфатаза, гамма-глутамилтранспептидаза, общий билирубин, альбумин, холинэстераза, протромбиновое время.
Все участники исследования подписывали информированное согласие. Исследование было одобрено местным комитетом по этике и соответствовало Хельсинской декларации 1975 года.
2.2. ARFI эластография
ARFI исследование проводили всем больным натощак, с помощью ультразвуковой системы Siemens Acuson S2000 (Siemens AG, Эрланген, Германия), программное обеспечение версии 2.0, с ультразвуковым датчиком 4C1. Сканирование проводили между ребрами, в положении пациентов лежа на спине, в V или VIII сегментах правой доли печени, глубиной 1-2 см от капсулы, с минимальной компрессией при сканировании, которую оказывает оператор, при этом пациентов просили не дышать в момент измерения для того, чтобы свести к минимуму дыхательные движения. У каждого пациента мы стремились получить 10 результативных измерений в той же зоне правой доли печени. Затем рассчитывали медианное значение, результат которого измеряли в м/с (рис. 1).
Рис. 1. Измерения жесткости печени при помощи ARFI эластографии (действительное измерение).
Если измерение не являлось результативным, на экране отображалось “X.XX” (рис. 2).
Рис. 2. Нерезультативное измерение жесткости печени при помощи ARFI эластографии у пациента с ожирением.
Даже с учетом того, что производитель устройства не дает никаких указаний относительно качества измерений ARFI, опубликованные исследования показали, что для того, чтобы иметь наилучшую корреляцию измерений LS с помощью ARFI эластографии с гистологическими данными при фиброзе, должны использоваться параметры качества, аналогичные измерениям при транзиторной эластографии (Transient Elastography – TE). Параметры качества, которые использовали мы, были: межквартильный интервальный диапазон (interquartile range interval – IQR = разница между 75-м процентилем и 25-м процентилем, что по существу является диапазоном средних 50% данных) и показатель успешных попыток (success rate – SR = отношение результативных измерений к общему числу измерений).
Надежными измерения ARFI были определены как: среднее значение 10 результативных измерений LS с SR ≥ 60% и IQR <30%. Неудачными измерениями ARFI были определены нерезультативные измерения, полученные после того, как, по крайней мере, было проведено 10 попыток. Измерение считался ненадежным в следующих ситуациях: менее 10 успешных измерений; среднее значение 10 успешных измерений имело вероятность успешных попыток (success rate – SR) <60%, и/или межквартильный интервальный диапазон (interquartile range interval – IQR) ≥ 30%.
Эксперты, которые выполняли измерения ARFI, не имели клинических, серологических и гистологических данных пациентов.
2.3. Ультрасонография брюшной полости
Ультрасонография брюшной полости проводилась всем пациентам, которые были включены в исследование, с помощью ультразвуковой системы Siemens Acuson S2000 (Сименс, Эрланген, Германия) с ультразвуковой датчиком 4CI. Во всех случаях мы записывали структуру печени, наличие очаговых поражений печени, наличие асцита и передне-задний размер селезенки.
2.4. Биопсия печени
Биопсия печени была проведена под ультразвуковым наведением одновременно с ARFI измерениями у пациентов с хроническим гепатитом В и С, с использованием модифицированной иглы типа Менгини, 1,4 мм и 1,6 мм в диаметре.
Биопсия печени оценивались по шкале METAVIR, старшим патологоанатом, который не имел результатовв измерений ARFI и всех клинических, серологических и гистологических данных пациентов. Стадия фиброза выставлялась по шкале от 0 до 4: F0 – отсутствие фиброза; F1 – портальный фиброз без перегородок; F2 – портальный фиброз и несколько перегородок, проникающих в дольки; F3 – многочисленные перегородки, которые распространяются на соседние портальные тракты или терминальные печеночные венулы и F4 – цирроз.
2.5. Статистический анализ
Статистический анализ проводили с использованием программного обеспечения MedCalc версии 12.7.0 (MedCalc, Бельгия). Распределение численных переменных был сначала оценено с помощью теста Колмогорова-Смирнова. Для числовых величин с нормальным распределением, были представлены среднее значение и стандартное отклонение, а для значений с ненормальным распределением, были представлены срединные значения и интервалы диапазона. Различия между числовыми переменными были проанализированы с помощью параметрического (Т-тест) или непараметрических критериев (критерий Манна-Уитни) в соответствии с нормальным или ненормальным распределением. Качественные переменные были представлены в виде чисел и процентов. Хи-квадрат (Х2) тест (с поправкой Йейтса) использовали для сравнения пропорции, выраженной в процентах (“n” обозначает общее число пациентов, включенных в определенную подгруппу). Влияние демографических характеристик и биологических данных на получение неудачных и ненадежных измерений LS с помощью ARFI эластографии оценивали путем сравнения надежных измерений с неудавшимися и ненадежными измерениями, сперва с помощью моновариантного анализа. На втором этапе, независимые дискриминационные значения переменных, достигающие статистической значимости, оценивали с использованием моновариантного анализа с помощью пошагового логистического регрессионного анализа. Площади под кривой рабочей характеристики приемника (Areas under receiver operating characteristics – AUROC) были построены для различения пороговых значений, связанных с факторами риска неудачных и ненадежных измерений. Оптимальные пороговые значения были получены с помощью индекса Youden (чувствительность + специфичность – 1) из AUROC анализа кривых. Были рассчитаны 95% доверительные интервалы (confidence intervals – CI) для каждого прогностического теста, р-значение менее 0,05 считалось значимым для каждого статистического теста.
Результаты
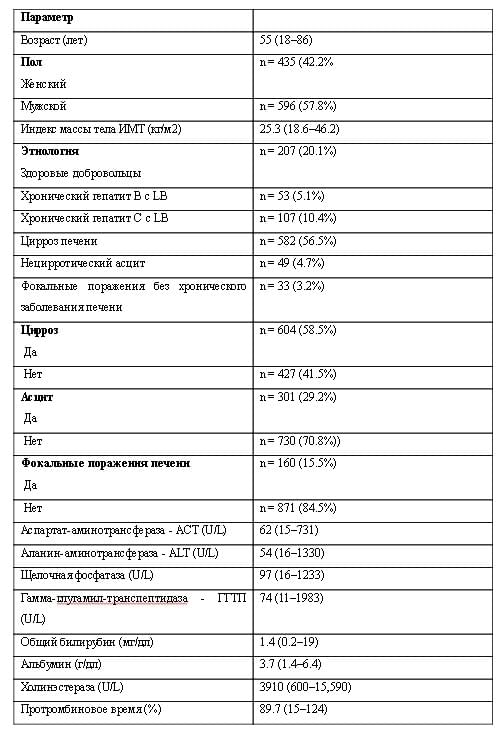
Основные характеристики 1031 пациентов, включенных в данное исследование, представлены в таблице 1.
Таблица 1
Основные характеристики пациентов. Численные величины с нормальным распределением представлены в виде среднего значения ± стандартное отклонение, переменные с ненормальным распределением представлены как медианные значения и интервалы диапазона.
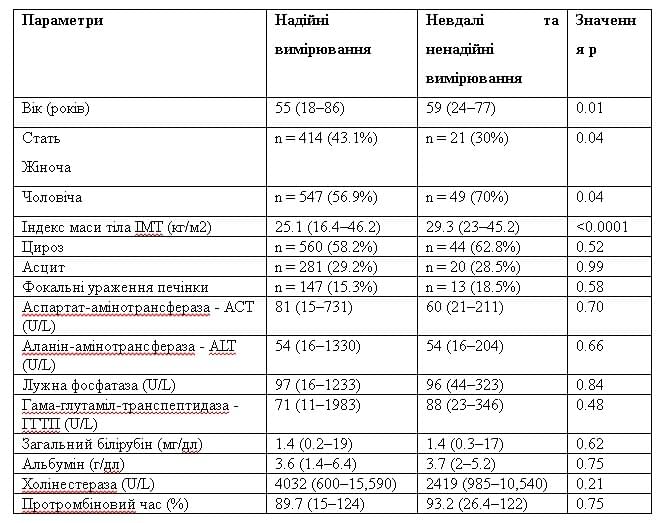
Из 1031 пациентов неудачные измерения LS при помощи ARFI зарегистрированы у 4 пациентов (0,3%), ненадежными измерениями были у 66 пациентов (6,4%), соответственно, надежные измерения были получены у 961 пациентов (93,3%). В моновариантном анализе, пожилой возраст, мужской пол и более высокий ИМТ были связаны с риском неудачных и ненадежных измерений (таблица 2).
Таблица 2
Мономерный анализ факторов, связанных с неудачными и ненадежными измерениями LS с помощью ARFI эластографии. Численные величины с нормальным распределением представлены в виде среднего значения ± стандартное отклонение, переменные с ненормальным распределением представлены как медианные значения и интервалы диапазона.
Все факторы, связанные с риском неудачных и ненадежных измерений LS по данным ARFI эластографии в моновариантного анализе, также были независимо связаны с невозможностью получить достоверные измерения и в многомерном анализе (Таблица 3).
Таблица 3
Многомерный анализ факторов, связанных с неудачными и ненадежными измерениями LS с помощью ARFI эластографии.
Кривые AUROC были построены для определения пороговых значений, связанных с факторами риска для неудачных и ненадежных измерений LS с помощью ARFI эластографии. Мы выявили следующие пороговые значения в качестве прогностических критериев неудачных и ненадежных измерений: возраст> 58 лет (AUROC = 0,590, р = 0,003) и ИМТ> 27,7 кг/м2 (AUROC = 0,653, р = 0,0001). Соотношения для неудачных и ненадежных измерений LS по данным ARFI эластографии и различных параметров представлены в таблице 4.
Таблица 4
Соотношения между неудачными и ненадежными измерениями LS с помощью ARFI эластографии и разными параметрами при мономерном анализе.
Частота достоверных измерений LS с помощью ARFI эластографии была значительно выше у пациентов с нормальной массой тела (ИМТ = 18.5-24.9 кг/м2), по сравнению с избыточной массой тела (ИМТ = 25-29,9 кг/м2) и ожирением (ИМТ ≥ 30 кг/м2): 97,3% против 93,4%, р = 0,01 и 97,3% против 82,4%, р <0,0001 соответственно. Кроме того, частота достоверных измерений ARFI была значительно выше у пациентов избыточной массой тела по сравнению с пациентами с ожирением: 93,4% против 82,4%, р = 0,0004.
Обсуждение
Оценка эффективности эластографических методов неинвазивной оценки фиброза печени является очень важным элементом, так как для использования в повседневной клинической практике метод должен позволять должным образом оценить большое количество пациентов.
Большие опубликованные исследования в области TE показали, что надежные измерения LS, с использованием стандартного М-датчика, получаются только в 70-85% случаев. Что касается ARFI эластографии, в связи с тем, что производитель не уточняет необходимые критерии качества для измерений ARFI, существует только несколько опубликованных исследований с использованием критериев качества, которые применяются для TE. Недавно опубликованные исследования показали важность параметров качества (особенно IQR) для корреляции LS измерений, произведенных с помощью ARFI, с гистологическими данными о фиброзе. Производитель признал важность этих технических параметров. В связи с этим было разработано новое программное обеспечение, которое автоматически отображает значение параметров критериев качества, аналогично TE.
До сих пор не проведено исследований, которые анализируют факторы, связанные с невозможностью получения надежных LS измерений с помощью ARFI эластографии. Наше исследование является первым, которое проводит детальный анализ факторов, связанных с неудачными и ненадежными измерениями ARFI в большой когорте пациентов.
Частота достоверных измерений LS, полученные в нашем исследовании, была достаточно высокой (93,3%) в соответствии с результатами других исследований, опубликованных в области ARFI эластографии, и значительно выше, чем в случае ТЕ (с использованием стандартного M-датчика).
Аналогично с TE, более старший возраст и высокий ИМТ, были связаны с невозможностью получения надежных результатов измерений ARFI. Но, в отличие от TE, при котором возраст> 50 лет и ИМТ> 30 кг/м2 были связаны с высоким показателем OR (3,5 и 10,5, соответственно) для неудачных и ненадежных измерений TE в исследовании Castera и др.; и (2,04 и 3,34 соответственно) для возраста > 52 лет и ИМТ> 30 кг/м2 в исследовании Sirli и др., в нашем исследовании OR было намного ниже: 0,49 при возрасте > 58 лет и 0,24 для ИМТ ≥ 30 кг/м2. Согласно нашим результатам, эти параметры имеют лишь ограниченное влияние в повседневной клинической практике. Таким образом, если у пациентов с ожирением надежные LS измерения с помощью TE (с использованием стандартного M-датчика) получаются только у 50% пациентов; в нашем исследовании надежные измерения ARFI были получены в 82,4% случаев. В данном исследовании частота надежных измерений LS с помощью ARFI эластографии у пациентов с ожирением была одинаковой или выше, чем представленные данные в исследованиях, которые использовали XL датчик, разработанный специально для пациентов с избыточной массой тела и ожирением для TE.
В исследованиях TE, женский пол был связан с неудачными и ненадежными LS измерениями, но наше исследование показало, что при ARFI эластографии именно мужской пол был связан с невозможностью получить достоверные измерения LS. Одним из объяснений может быть более старший возраст и высокий ИМТ в нашей группе мужчин, по сравнению с группой женщин: 56 (19-84) лет против 54 (18-86) лет, р = 0,0003 и 25,9 (19.2-45.2) кг/м2 по сравнению с 24,2 (18.6-46.2) кг/м2, р <0,0001, соответственно. Кроме того, OR было небольшим (0,58), это означает то, что этот фактор не имеет большого значения в повседневной клинической практике. В основном частота надежных измерений LS при помощи ARFI эластографии была выше 90% для обоих полов (95,1% у женщин и 91,7% у мужчин, соответственно).
Наше исследование показало, что наличие цирроза печени, асцита или очаговых поражений печени не оказывает влияния на частоту надежных измерений ARFI. Это является важным фактом в связи с тем, что ТЕ не может быть выполнена, если присутствует асцит вокруг печени. Другим преимуществом ARFI эластографии по сравнению с TE является то, что область интереса при ультразвуковом исследовании выбирается таким образом, что специалист может быть уверен в том, что измерение выполняется в зоне нормальной паренхимы печени при наличии очаговых поражений печени.
Как мы и предполагали, аминотрансферазы, щелочная фосфатаза, ГГТП, общий билирубин, холинэстераза, уровень сывороточного альбумина и протромбиновый индекс не оказывают влияния на частоту достоверных измерений LS с помощью ARFI эластографии. Но, согласно опубликованным исследованиям, высокий уровень аминотрансфераз и холестаз влияют на точность ARFI эластографии для неинвазивной оценки фиброза печени, и эти данные аналогичны опубликованным относительно TE.
Мы попытались проанализировать четыре случая с неудачными измерениями LS с помощью ARFI эластографии, но, так как это было ретроспективное исследование, были доступны не все данные. Все четыре пациента страдали ожирением (двое – с ИМТ от 30 до 35 кг/м2, один – с ИМТ между 35,1 и 40 кг/м2 и один – с ИМТ ≥ 40 кг/м2), трое пациентов с циррозом (два из них с асцитом) и один был здоровый доброволец. В заключении ультразвукового исследования было упоминание о наличии плохого акустического окна в трех случаях, а в одном случае (пациент с циррозом и с асцитом), пациент испытывал трудности с задержкой дыхания в момент оценки LS. Положение пациента для оценки LS посредством ARFI эластографии не изменялось ни в одном из этих четырех случаев.
Сильной стороной нашего исследования является большое количество пациентов, у которых оценивалась эффективность измерений LS с помощью ARFI эластографии. Однако наше исследование также имеет некоторые ограничения, такие как: ретроспективный дизайн и включение гетерогенной популяции: здоровые добровольцы, пациенты с хроническим гепатитом В и С, которые оценивались с помощью LB и ARFI эластографии; пациенты с циррозом, которые исследовались с помощью клинических, биологических, ультразвуковых, эндоскопических и/или лапароскопических критериев; пациенты с циррозом без асцита и пациенты с очаговыми поражениями печени при отсутствии хронического заболевания печени.
У больных с опухолями печени мы представили только данные, которые касаются только измерений ARFI в явно здоровой паренхиме, которая окружала очаговые образования печени, поскольку предметом настоящего исследования являлось оценка возможности ARFI эластографии для измерения LS. Следует уточнить, что оценка жесткости печени у больных с опухолями печени является очень важным этапом обследования. Так как если измерения LS предполагают выраженный фиброз или цирроз печени, то первым типом поражения, о котором мы должны думать, является гепатоцеллюлярная карцинома. В тоже время, если измерения LS предполагают отсутствие выраженного фиброза, в первую очередь мы должны думать о доброкачественном поражении печени, если опухоль является одиночной, или о печеночных метастазах, если имеется множественное поражение.
В заключение следует сказать, что надежные измерения LS с помощью ARFI эластографии в нашем исследовании были получены в 93,3% случаев. Пожилой возраст, более высокий индекс массы тела и мужской пол были связаны с риском неудачных попыток и ненадежных измерений, но их влияние ограничено по сравнению с методикой TE.








14.10.2019
Святослав