Ключові висновки дослідження
Нове рандомізоване клінічне дослідження HY-PER порівняло ефективність гістероскопії та вакуум-аспірації у лікуванні неповного спонтанного аборту. Результати показали, що гістероскопія не має переваг перед вакуум-аспірацією щодо настання наступної вагітності та безпеки процедури.
Методологія та результати
Дослідження включало 574 пацієнтки віком 18-44 роки, які планували завагітніти після неповного спонтанного аборту. Учасниці були рандомізовані на дві групи: гістероскопія (288 жінок) та вакуум-аспірація (286 жінок).Основні результати:
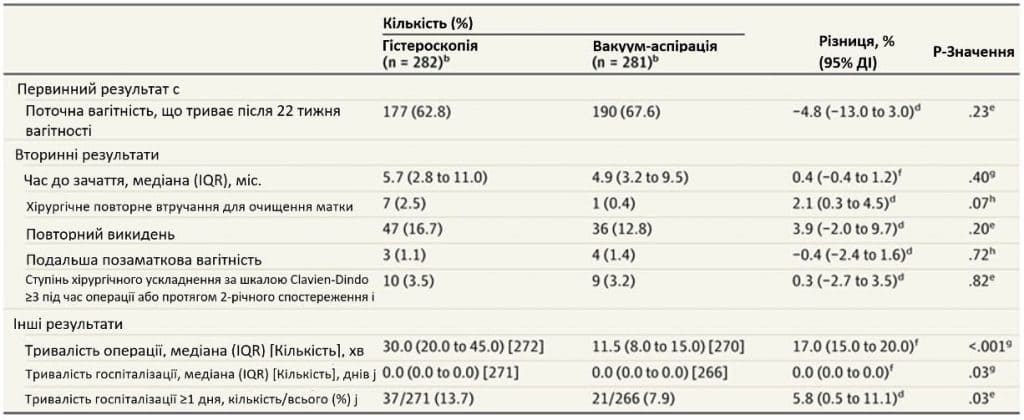
- Частота настання вагітності тривалістю не менше 22 тижнів протягом 2 років: 62,8% у групі гістероскопії проти 67,6% у групі вакуум-аспірації.
- Не виявлено статистично значущої різниці між групами щодо часу до настання вагітності.
- Тривалість операції та госпіталізації були довшими при гістероскопії.
- Частота ускладнень та повторних втручань не відрізнялася між групами.
Значення для клінічної практики
Це дослідження не підтверджує переваг використання гістероскопії як методу першої лінії для лікування неповного спонтанного аборту. Вакуум-аспірація залишається ефективним та безпечним методом, що не погіршує подальшу фертильність пацієнток.
Вступ
Викидень – це втрата вагітності на стадії, коли вона ще не є життєздатною. За оцінками, щороку відбувається 23 мільйони викиднів, що призводить до втрати 44 вагітностей щохвилини у всьому світі.
Популяційна поширеність жінок, у яких протягом життя стався принаймні 1 викидень, становить 10,8% (95% ДІ від 10,3% до 11,4%), а сукупний ризик невиношування вагітності становить приблизно 15% від усіх вагітностей.1 Після викидня 60% жінок, які бажають завагітніти в майбутньому, досягають цього впродовж 2 років.
Природний перебіг викидня – це спонтанний перебіг до повного вигнання продуктів зачаття. Якщо вигнання відбувається не повністю, продукти зачаття, що залишилися, можуть потребувати медикаментозного або хірургічного видалення.
Неповні спонтанні аборти лікуються за допомогою вичікувального, медикаментозного або хірургічного лікування.
Хірургічне втручання може бути проведене одразу або після безуспішного вичікувального або медикаментозного лікування. Нещодавній мережевий метааналіз показав, що за ефективністю хірургічні методи переважають вичікувальне та медикаментозне лікування.
Вакуум-аспірація є еталонним стандартом для хірургічного лікування. Процедура не проводиться з прямою візуалізацією і має відомі ризики рубцювання порожнини матки, що може поставити під загрозу післяопераційну фертильність, з оціночним 30% ризиком утворення внутрішньоматкових спайок.
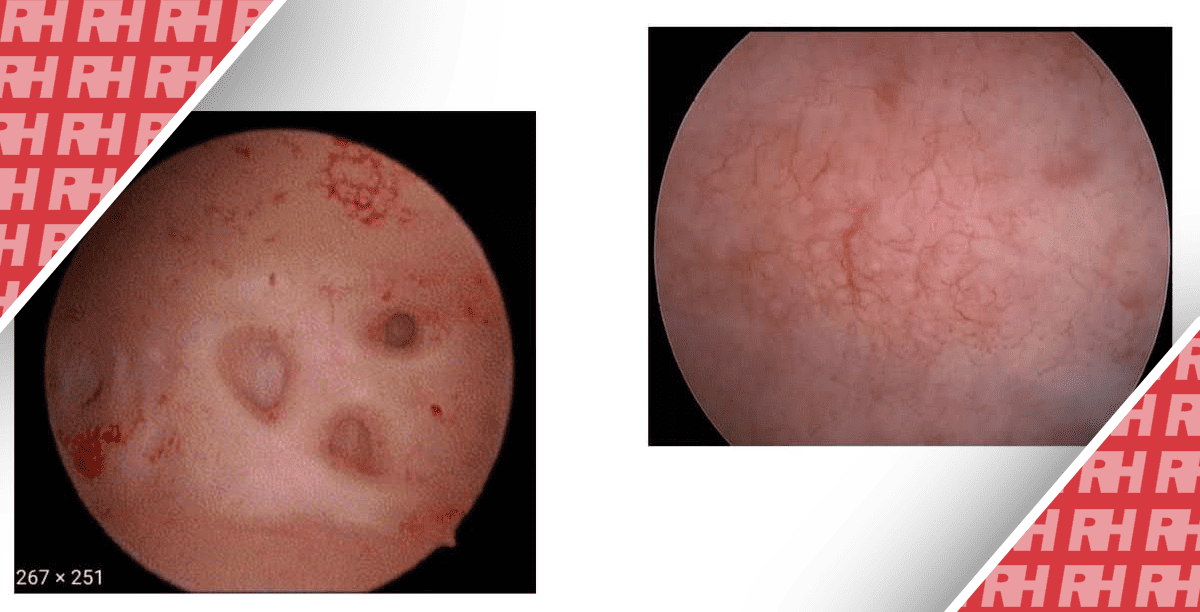
Гістероскопія, рутинна хірургічна процедура для лікування внутрішньоматкових патологій, виконується шляхом введення гістероскопа через цервікальний канал у порожнину ендометрію. Рідке розтягуюче середовище допомагає візуалізувати та лікувати патології в порожнині матки. Оскільки гістероскопія для видалення залишків зачаття виконується під прямим візуальним контролем, вона теоретично може зменшити ризики для порожнини матки, а отже, покращити майбутню фертильність.
Ретроспективні дослідження показують, що порівняно з вакуум-аспірацією, гістероскопія пов’язана з 13% ризиком післяопераційних внутрішньоматкових спайок і кращою подальшою фертильністю з більш коротким часом зачаття, причому до 70% прооперованих жінок знову завагітніли протягом 2 років після первинного втручання.
Тому ми припустили, що гістероскопія обмежить ускладнення операції та кількість повторних втручань через збереження продуктів зачаття або спайок, таким чином покращуючи післяопераційну фертильність серед жінок, які бажають завагітніти після неповного спонтанного аборту.
Однак, на даний момент немає остаточних доказів переваги гістероскопічної резекції щодо частоти наступних вагітностей.
Основною метою нашого дослідження було оцінити подальші показники фертильності після неповного спонтанного аборту серед жінок, які планують завагітніти, шляхом прагматичного порівняння тих, хто пройшов лікування за допомогою гістероскопії, і тих, хто пройшов вакуум-аспірацію.
Нашою вторинною метою було дослідити, чи пов’язана гістероскопія з меншою кількістю інтраопераційних і післяопераційних ускладнень, у тому числі хірургічного повторного втручання.
Методи
Комітет із захисту осіб, які беруть участь у медичних дослідженнях (CPP) Іль-де-Франс XI (№ 14040) та Національне агентство з безпеки лікарських засобів і виробів медичного призначення (ANSM) (№ 140516B-22) схвалили протокол дослідження 16 червня 2014 року. CPP Іль-де-Франс XI (№ 14040) також затвердив модифікований протокол, версію 2.1 від 6 травня 2015 року, 11 червня 2015 року. Детальний протокол дослідження був опублікований раніше.16 Дослідження проводилося відповідно до Керівництва зі звітності Консолідованих стандартів звітності про клінічні випробування (CONSORT).
Планування випробування та учасники
Дослідження HY-PER (Evaluation de l’efficacy de l’HYsteroscopie dans la Prise En charge de Rétentions trophoblastiques intra-utérines [Оцінка ефективності гістероскопії в лікуванні внутрішньоматкових трофобластичних затримок]) було однократним сліпим, рандомізованим, багатоцентровим прагматичним дослідженням, в якому порівнювали вакуум-аспірацію та гістероскопію у жінок з неповним спонтанним абортом.
Пацієнтів набирали з 15 центрів (загальних та університетських лікарень) по всій Франції.
Пацієнти, які відповідали критеріям відбору, мали такі характеристики.
- Особи віком від 18 до 44 років, застраховані у Французькому фонді соціального страхування, з неповним спонтанним абортом у першому триместрі (термін вагітності <14 тижнів, визначений за останньою менструацією та/або точною датою початку вагітності у випадках, коли вагітність була встановлена за допомогою раннього ультразвукового дослідження органів малого тазу) із збереженими продуктами зачаття, діагностованими за допомогою трансвагінального ультразвукового дослідження органів малого тазу, що демонструють неоднорідне внутрішньоматкове утворення або внутрішньоматковий міхур товщиною понад 15 мм, з ембріоном або без нього 2.
- Вагітність була бажаною і наступна вагітність була бажаною якнайшвидше після процедури
- Хірургічне лікування було обрано згідно з місцевими протоколами лікування відповідно до національних французьких рекомендацій.17
Критеріями виключення пацієнток були: відома вада розвитку матки, попереднє хірургічне лікування поточного викидня, необхідність екстреної хірургічної евакуації для лікування геморагічного викидня або наявність внутрішньоматкової спіралі. Пацієнтки з поточною вагітністю, підозрою на позаматкову вагітність, вагітністю невідомої локалізації, штучним абортом, вагітністю, отриманою за допомогою допоміжних репродуктивних технологій, або внутрішньоматковою затримкою матеріалу товщиною понад 50 мм, діагностованою за допомогою трансвагінального ультразвукового дослідження, також виключалися з дослідження.
Початкова оцінка включала повне гінекологічне обстеження з реєстрацією гемодинамічних показників (частота серцевих скорочень, артеріальний тиск, температура) для виявлення жінок, схильних до геморагічного шоку в разі сильної кровотечі. Гемодинамічна нестабільність ґрунтувалася на клінічній оцінці дослідника відповідно до рекомендацій (ЧСС >120/хв і систолічний артеріальний тиск нижче 90 мм рт.ст. оцінювалися двічі).18
Неповний спонтанний аборт діагностували за допомогою трансвагінального ультразвукового дослідження, яке проводив старший акушер-гінеколог, відповідно до раніше опублікованої стандартної методики УЗД органів малого тазу в умовах невідкладної гінекологічної допомоги.19 Зображення сонограми реєстрували. За відсутності ознак, що вказують на внутрішньоматковий плідний міхур, для підтвердження того, що вагітність була внутрішньоматковою, і для виключення будь-якої позаматкової вагітності, необхідно було провести ультразвукове сканування з видимою внутрішньоматковою вагітністю до постановки діагнозу неповного аборту.
Пацієнтки отримали письмову інформаційну довідку та усні пояснення щодо протоколу та його деталей. Після отримання відповідей на запитання учасниці підписали письмову інформовану згоду, яку передали старшому лікарю-гінекологу, що виступав у ролі місцевого дослідника в дослідженні.
Втручання
Усі процедури виконувалися в операційній сертифікованим акушером-гінекологом зі стажем хірургічної практики щонайменше 5 років. Хірурги-гінекологи, які брали участь у дослідженні, регулярно виконували гістероскопічну резекцію для різних процедур, таких як міомектомія та лікування внутрішньоматкових спайок.
Інтервенційна група: Гістероскопія
Шийку матки захоплювали гінекологічними щипцями Pozzi і розширювали, за необхідності використовуючи розширювач Hegar 9 розміру, щоб полегшити введення операційного гістероскопа (максимальний діаметр катетера 28F). Порожнину матки розширювали за допомогою ізотонічного розчину та високочастотного генератора, необхідного для системи біполярної резекції. Зовнішній вигляд порожнини матки фіксували з діагностичною метою перед втручанням. Збережені продукти зачаття видаляли хірургічним резектором зверху вниз, без застосування електричного струму, оскільки цей метод найкраще захищає ендометрій.7,8 Електричний струм використовували лише в крайньому випадку, якщо продукти зачаття не можна було видалити іншим способом. Якщо після операції виникала активна кровотеча, для зупинки внутрішньоматкової кровотечі можна було виконати планову коагуляцію за допомогою гістероскопа. Завершення процедури оцінювали за візуальною перевіркою того, що матка порожня. Об’єм використаного розтягувального середовища фіксувався.
Контрольна група: Вакуум-аспірація
Вакуум-аспірація проводилася за допомогою гнучкої або жорсткої вакуумної канюлі. Діаметр використовуваної канюлі, ступінь розширення шийки матки за допомогою дилататора Гегара, якщо необхідно, і використання інтраопераційного ультразвукового наведення залишалися на розсуд оператора і були стандартною практикою центру. Відсмоктування створювалося за допомогою електричного насоса.
Конверсія на процедуру, відмінну від призначеної групи, була визначена як необхідність вакуум-аспірації в групі гістероскопії або необхідність гістероскопії в групі вакуум-аспірації. Переведення могло бути здійснено через інтраопераційні несприятливі події або у випадку операційних труднощів (наприклад, неможливість видалення залишків плодового яйця).
Клінічна допомога надавалася відповідно до стандартних практик центру, включаючи антибіотикопрофілактику, мізопростол для розширення шийки матки, загальну або місцеву анестезію, а також профілактику для резус-негативних пацієнток. Видалені ретенційні продукти були відправлені на патологоанатомічне дослідження.
Результати
Первинним результатом було настання внутрішньоматкової вагітності з терміном понад 22 тижні гестації протягом 2 років після процедури. Поточні вагітності, що розпочалися протягом 2-річного спостереження, але з терміном гестації менше 22 тижнів до кінця спостереження, не відповідали визначенню первинного результату, навіть якщо ця вагітність закінчилася народженням живої дитини після 2-річного періоду спостереження.
Вторинними результатами були час до зачаття (час від операції до зачаття поточної вагітності понад 22 тижні), повторне хірургічне втручання для отримання порожньої матки після індексної процедури, а також будь-який наступний викидень або позаматкова вагітність протягом 2-річного періоду спостереження. Несприятливі події були інтраопераційними та післяопераційними ускладненнями і оцінювалися за модифікованою класифікацією Clavien-Dindo.20 Частота ускладнень 3-го ступеня (хірургічні ускладнення, що вимагають хірургічного, ендоскопічного або радіологічного втручання) або вище (4-й ступінь: ускладнення, що загрожує життю, яке вимагає лікування в умовах високої залежності, і 5-й ступінь: смерть) розглядалася як вторинний результат. Переведення в альтернативну групу не вважалося ускладненням. Іншими змінними, які збирали, були тривалість операції, успіх запланованої процедури, тривалість госпіталізації, кровотеча понад 500 мл, перфорація матки, подальші втручання для лікування синехії матки або трубного безпліддя.
Подальші дії
Пацієнти відвідали післяопераційну консультацію через 3-8 тижнів після втручання для перевірки відсутності ускладнень. Після цього вони отримували подальші оцінки по телефону через 6 місяців, 1 рік і 2 роки після хірургічного лікування. У випадках успішного завершення наступної вагітності спостереження закінчувалося під час пологів. Через 2 роки спостереження не продовжувалося, навіть у випадках, коли вагітність тривала. У разі відсутності телефонного зв’язку для подальшого спостереження надсилали електронне повідомлення, лист або і те, і інше. Під час кожного подальшого спостереження збирали інформацію про наступні вагітності, хірургічні втручання та гінекологічні висновки, такі як діагноз внутрішньоутробної патології. Медичні записи могли бути використані для доповнення інформації у випадках пологів у тій самій лікарні або при проведенні додаткових обстежень чи хірургічних процедур.
- Одинадцять учасниць були виключені після рандомізації і виключені з усіх подальших аналізів (6 з групи гістероскопії; 5 з групи вакуум-аспірації).
- Згідно з французьким законодавством, учасники, які відкликали свою згоду, не можуть бути включені в аналіз.
- Аналіз прихильності до лікування проводився відповідно до групи лікування, до якої пацієнти були розподілені при рандомізації, незалежно від процедури, яку вони отримували, та тривалості спостереження за ними. Пацієнти, позначені як виключені, не були включені в аналіз наміру лікуватися.
- Аналіз за протоколами включав усіх рандомізованих пацієнтів, за винятком тих, хто не отримав повну призначену операцію після рандомізації, а також пацієнтів, втрачених для подальшого спостереження.
- Для оцінки первинного результату використовували популяцію з наміром лікуватись та популяцію по кожному протоколу. Первинним результатом було настання внутрішньоматкової вагітності з терміном понад 22 тижні гестації протягом 2 років після рандомізації.
Обсяг вибірки
Орієнтовна кількість необхідних учасників ґрунтується на первинному результаті. Середній показник живонароджуваності через 2 роки після неповного спонтанного аборту, який лікували методом вакуум-аспірації, становить приблизно 60%.3 Непорівняльні дослідження показали, що гістероскопічна резекція покращує подальшу фертильність, причому у жінок, які пройшли лікування, живонароджуваність спостерігається у 70%-75% випадків.7,8,13
Щоб продемонструвати, що використання гістероскопії збільшує частоту вагітностей тривалістю не менше 22 тижнів протягом 2 років спостереження з 60% до 72%, з потужністю 80% і 2-рівневим α = 0,05, ми підрахували, що для цього дослідження потрібно 520 пацієнток (260 на групу), використовуючи наближення, отримане Casagrande і Pike.21 Припускаючи, що 10% пацієнток у кожній групі буде втрачено під час спостереження, ми планували включити 572 пацієнтки (по 286 на групу).
Рандомізація
Пацієнтки були рандомізовані для отримання хірургічного лікування методом вакуум-аспірації або гістероскопічної резекції (Зображення 1). Безпосередньо перед процедурою хірург проводив рандомізацію за допомогою веб-системи рандомізації в режимі реального часу з використанням електронної форми звіту про випадок. Спонсор надав послідовність розподілу 1:1 (переставлені блоки по 4 і комп’ютерний генератор випадкових чисел), яка була стратифікована за центром. Списки рандомізації не розголошувалися дослідницьким центрам, моніторам, статистику проекту або команді проекту.
Засліплення
Це було одноразове сліпе дослідження; пацієнтки не були поінформовані ні до, ні після процедури, яку вони проходили. Операційні були стандартно підготовлені до гістероскопії. Запечатаний хірургічний звіт, що детально описує всю процедуру і будь-які несподівані події, залишався в медичній картці пацієнтки на випадок необхідності під час подальшого спостереження. Пацієнтки отримували стандартизований хірургічний звіт, в якому не згадувався тип процедури. Під час телефонних опитувань учасників систематично запитували, чи знають вони про конкретну процедуру, яку вони перенесли. Особи, залучені до управління даними, також не знали про призначення лікування.22
Аналіз популяцій
Аналіз наміру лікуватися проводився відповідно до групи рандомізації, незалежно від отриманої процедури та тривалості спостереження. За учасниками, які не пройшли призначену процедуру, спостерігали протягом 2 років для реєстрації їх первинних і вторинних кінцевих точок і аналізували відповідно до їх групи рандомізації, за винятком 7 учасників, які відкликали свою згоду. З аналізу за протоколами були виключені учасники, які не отримали повної призначеної операції після рандомізації, а також учасники, які були втрачені для подальшого спостереження.
Статистичний аналіз
Відсоток учасниць, які досягли первинного результату, порівнювали між 2 групами за допомогою χ2-тесту. При аналізі первинного результату було враховано, що в учасниць з відсутнім або неповним спостереженням вагітність тривалістю понад 22 тижні не настала. Гетерогенність між центрами перевіряли графічно. Абсолютну різницю в первинній кінцевій точці та 95% ДІ оцінювали за допомогою узагальненої лінійної змішаної моделі (GLMM) з біноміальним розподілом та функцією тотожності зв’язку.
Вторинний аналіз первинної кінцевої точки проводився з використанням цензурованих даних. Час до події – це час до зачаття поточної вагітності, яка тривала понад 22 тижні, оцінений за методом Каплана-Майєра.23 Учасниці з неповним спостереженням були проаналізовані відповідно до їхнього останнього відомого статусу, а учасниці з успішною прогресуючою вагітністю не відповідали визначенню первинного результату, якщо за ними не спостерігали до 22 тижнів гестації протягом 2-річного періоду. Інші жінки були відсіяні на дату останнього спостереження. У цьому аналізі для порівняння частоти зачаття між двома групами рандомізації використовувався лог-ранговий тест. Регресійна модель пропорційних ризиків Кокса була використана для оцінки співвідношення ризиків (СР) з 95% ДІ. Проміжні аналізи не планувалися.
Вторинні кінцеві точки були проаналізовані та порівняні між 2 групами за допомогою χ2-тесту. Абсолютні відмінності ризику розраховували за допомогою GLMM. Всі застосовні статистичні тести були 2-сторонніми і визначали значущість як P = .05. Поправки для множинних порівнянь не застосовували, оскільки всі вторинні цілі вважалися дослідницькими. Всі точкові оцінки представлені з 95% ДІ.
Результати
У період з 6 листопада 2014 року по 3 травня 2017 року було рандомізовано 574 учасниці, 11 з яких були виключені після рандомізації і не були включені в аналіз намірів щодо лікування. З 563 включених учасниць 281 була призначена на вакуум-аспірацію, а 282 – на гістероскопію (Зображення 1). Всі учасниці групи вакуум-аспірації отримали призначену процедуру; 1 учасниця не бажала вагітності в майбутньому, а 25 учасниць були втрачені для подальшого спостереження. У групі гістероскопії 23 учасниці не отримали призначену процедуру, що було розцінено як відхилення від протоколу (4 помилково отримали вакуум-аспірацію, 18 – гістероскопію з подальшим переходом на вакуум-аспірацію, і 1 процедура не вдалася), а 22 учасниці були втрачені для подальшого спостереження. Після виключення цих учасниць в аналізі залишилося 492 учасниці (Зображення 1). У Таблиці 1 представлено базові характеристики включених учасників.
a Вказує на кількість пацієнтів, якщо категорія не повідомила інше числове значення.
b Симптоми не є взаємовиключними і тому можуть становити більше 100% (симптоматичні пацієнтки можуть мати як вагінальну кровотечу, так і тазовий біль).
c Ембріональна гестація вимагала попередньої внутрішньоматкової вагітності (ВМВ) на інтравагінальному ультразвуковому дослідженні, щоб встановити, що ВМВ колись існувала.
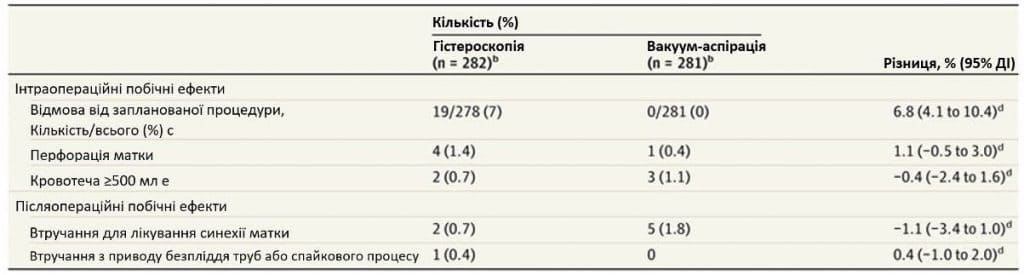
У Таблиці 2 представлені первинні та вторинні результати, результати вагітності, а в Таблиці 3 – інтраопераційні та післяопераційні побічні ефекти. Тривалість операції та госпіталізації були значно довшими при гістероскопії (Таблиця 2). Інтраопераційне ультразвукове спостереження застосовували у 151/279 (54,1%) пацієнток у групі гістероскопії та 229/274 (83,6%) пацієнток у групі вакуумування. Не було повідомлень про перевантаження рідиною, гіпонатріємію, трансфузії або післяопераційні кровотечі.
Серед 574 рандомізованих пацієнтів 11 пацієнтів були виключені після рандомізації: 4 через невідповідність критеріям участі (1 – через вік >45 років, 1 – через вагітність, спричинену екстракорпоральним заплідненням, 1 – через вигнання до процедури, 1 – через утримання після штучного аборту) і 7 – через відкликання згоди згідно з французьким законодавством.
- Вказується кількість пацієнтів, за винятком категорій, для яких вказано інше числове значення.
- Поточна вагітність тривалістю не менше 22 тижнів протягом 2-річного спостереження. Вагітність, що розпочалася під час 2-річного спостереження, але тривала менше 22 тижнів гестації до кінця спостереження, не відповідала визначенню первинного результату, навіть якщо вагітність, що розпочалася під час спостереження, закінчилася народженням живої дитини після 2-річного періоду спостереження.
- Абсолютні різниці ризиків та 95% ДІ були оцінені за допомогою узагальненої лінійної моделі.
- Розраховано за допомогою χ2-критерію.
- Розраховано за допомогою оцінки довірчого інтервалу Ходжа-Лемана для медіанних різниць.
- Розраховано за допомогою критерію Вілкоксона-Манна-Вітні.
- Розраховано за допомогою точного критерію Фішера.
- Класифікація Clavien-Dindo – це стандартизована система класифікації хірургічних ускладнень.17 Ступінь 1 визначається як будь-яке відхилення від нормального післяопераційного перебігу без необхідності фармакологічного лікування або хірургічних, ендоскопічних чи радіологічних втручань. 2 ступінь – це ускладнення, що потребують фармакологічного лікування препаратами, відмінними від тих, що дозволені при ускладненнях 1 ступеня. 3 ступінь – хірургічні ускладнення, що потребують хірургічного, ендоскопічного або радіологічного втручання (3а без загальної анестезії та 3b під загальною анестезією). 4 ступінь – це ускладнення, що загрожує життю і вимагає лікування в умовах високої залежності.
- Усі пацієнтки були госпіталізовані до гінекологічних відділень, у відділеннях невідкладної допомоги не було жодного випадку. Більшість пацієнток були госпіталізовані в денний стаціонар. Таким чином, кількість днів госпіталізації відповідає кількості ночей, проведених у стаціонарі для хірургічного лікування неповного спонтанного аборту.
- Серед 574 рандомізованих пацієнтів 11 пацієнтів були виключені після рандомізації: 4 через невідповідність критеріям участі (1 – через вік >45 років, 1 – через вагітність, спричинену екстракорпоральним заплідненням, 1 – через вигнання до процедури, 1 – через утримання після штучного аборту) і 7 – через відкликання згоди згідно з французьким законодавством.
- Вказується кількість пацієнтів, за винятком категорій, для яких вказано інше числове значення.
- Вказує на процедуру з переходом на іншу процедуру або невдачу.
- Абсолютна різниця ризиків та 95% ДІ були оцінені за допомогою узагальненої лінійної моделі.
- Крововилив кількісно визначали за допомогою аспірації та/або пакета для збору крові з підсідничної ділянки.
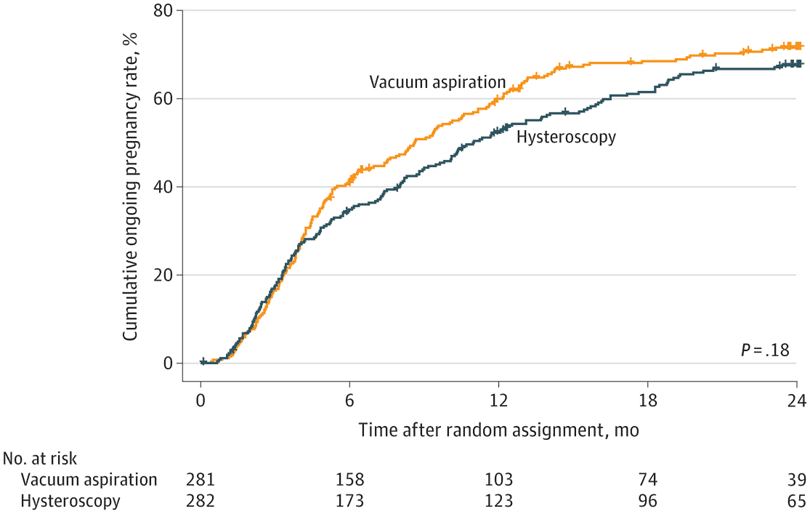
Протягом 2-річного спостереження у групі жінок, які мали намір лікуватися, 177 учасниць (62,8%) у групі гістероскопії та 190 учасниць (67,6%) у групі аспірації мали принаймні 1 вагітність, що тривала понад 22 тижні гестації (різниця -4,8% [95% ДІ, від -13% до 3,0%]). Не було ніякої гетерогенності між центрами. На Зображенні 2 показано графік Каплана-Майєра, який демонструє, що аналіз виживання не виявив різниці у часі до зачаття між 2 групами (відношення ризиків 0,87 [95% ДІ, від 0,71 до 1,07]; P = 0,18). Не спостерігалося різниці між групами щодо виникнення інших вторинних результатів: подальший викидень (47 [16,7%] у групі гістероскопії та 36 [12,8%] у групі вакуум-аспірації), подальша позаматкова вагітність (3 [1,1%] у групі гістероскопії та 4 [1. 4%] у групі вакуум-аспірації), хірургічні ускладнення за Clavien-Dindo, що перевищували або дорівнювали 3 ступеню (10 [3,5%] у групі гістероскопії та 9 [3,2%] у групі вакуум-аспірації), а також хірургічні повторні втручання для спорожнення матки (7 [2,5%] у групі гістероскопії та 1 [0,4%] у групі вакуум-аспірації) (Таблиця 2). Через рік після процедури 88/424 учасниці (20,8%) повідомили, що знають про своє лікування; 50 (57%) – правильно.
Сукупна триваюча внутрішньоматкова вагітність тривалістю понад 22 тижні гестації в групах гістероскопічної та вакуум-аспірації.
Медіана часу спостереження в групі гістероскопії становила 307 днів (IQR 102-727 днів), а в групі вакуум-аспірації – 232 дні (IQR 116-611 днів).
При аналізі за протоколами 165 пацієнток у групі гістероскопії (69,6%) і 190 пацієнток у групі аспірації (74,5%) мали принаймні 1 вагітність тривалістю 22 тижні або більше (різниця -4,9% [95% ДІ, від -12,8% до 3,0%]; P = 0,23). Аналіз виживання не виявив суттєвої різниці у часі до зачаття між 2 групами (відношення ризиків 0,85 [95% ДІ від 0,69 до 1,04]).
Обговорення
Результати нашого дослідження суперечать попереднім дослідженням, які накопичили низький або помірний рівень доказів переваги гістероскопічної резекції порівняно з традиційною вакуум-аспірацією.6–13 У жінок зі спонтанним неповним абортом, які бажають завагітніти якомога швидше, гістероскопічна резекція не покращує перспективи фертильності порівняно зі стандартною вакуум-аспірацією. Крім того, виконання гістероскопічної резекції не у всіх випадках було можливим і призводило до незадовільного рівня завершення процедури або повторного втручання для випорожнення матки від продуктів зачаття. Очікувалося, що частота ускладнень також буде на користь використання гістероскопії, оскільки ця хірургічна техніка дозволяє візуалізувати порожнину матки.13 Частота ускладнень була низькою в обох групах, і гістероскопічна резекція не надавала переваги з точки зору частоти серйозних ускладнень. Крім того, час перебування в операційній і тривалість госпіталізації були значно довшими в групі гістероскопії, і хоча результати не були статистично значущими, в групі гістероскопії було більше перфорацій матки і повторних операцій з випорожнення матки. Ці несприятливі результати, а також практичні питання медичних витрат і часового навантаження на пацієнток у поєднанні з нижчим відсотком успіху, чітко підтверджують неповноцінність гістероскопії порівняно з вакуум-аспірацією.
Переваги
Однією з сильних сторін нашого дослідження є успішне проведення хірургічного рандомізованого клінічного дослідження, яке включало понад 550 пацієнток з періодом спостереження 2 роки і втратою до моменту спостереження менше 10%. Всі процедури в цьому дослідженні виконувалися старшими гінекологічними хірургами, які регулярно виконують гістероскопічну резекцію при різних процедурах, а всі центри, що брали участь у дослідженні, були референтними центрами ендоскопічної хірургії зі значними обсягами гістероскопічної хірургії. Ще однією перевагою є надійний критерій, використаний для нашого первинного результату: поточна вагітність тривалістю понад 22 тижні, що відповідає визначенню пологів.17 Цей результат набагато ближчий до того, чого хочуть батьки (дитина вдома) в цю еру результатів, про які повідомляють пацієнти, ніж більшість сурогатних результатів, таких як зменшення спайок матки або зачаття внутрішньоматкової вагітності.24
Обмеження
Це дослідження має кілька обмежень. По-перше, використання одинарного сліпого методу можна вважати обмеженням нашого дослідження, хоча подвійний сліпий метод мав би прагматичні обмеження з огляду на втручання. По-друге, 11 пацієнтів довелося виключити після рандомізації, причому 4 з них – через неналежну рандомізацію пацієнтів, які не відповідали критеріям включення після оцінки центру моніторингу спонсором. Це може бути пов’язано з включенням пацієнтів у невідкладних станах, які потребували швидкого втручання. По-третє, кількість учасниць, які перейшли з гістероскопії на вакуум-аспірацію, могла обмежити інтерпретацію аналізу наміру лікуватися. Це становить 8% дисбаланс проти гістероскопії, а отже, обмеження постфактум можливості продемонструвати вплив гістероскопії на фертильність. Однак, з прагматичної точки зору, більшість змін у групах рандомізації були зумовлені неможливістю виконання запланованої гістероскопічної резекції. Крім того, після виключення цих осіб з аналізу за протоколами, результати дослідження не змінилися. По-четверте, це дослідження було обмежене хірургічним лікуванням осіб з неповним мимовільним абортом першого триместру вагітності. Необхідно з обережністю узагальнювати ці результати на пацієнток з персистуючими ретенційними продуктами зачаття після 14 тижнів гестації.
Висновки
Дослідження HY-PER надає докази того, що вакуум-аспірація повинна залишатися стандартом лікування пацієнток з неповним спонтанним абортом у першому триместрі вагітності. Це дослідження, як і інші нещодавні хірургічні дослідження, підкреслює нагальну потребу в оцінці часто використовуваних хірургічних методів, незважаючи на низький рівень доказовості.25 Хірургічне лікування шляхом гістероскопії неповних спонтанних абортів у пацієнток, які бажають завагітніти знову, не було пов’язане ні з більшою кількістю наступних пологів, ні з кращим профілем безпеки, ніж вакуум-аспірація. Більше того, оперативна гістероскопія не у всіх випадках була можливою.
Посилання на джерела
- Quenby S, Gallos ID, Dhillon-Smith RK, et al. Miscarriage matters: the epidemiological, physical, psychological, and economic costs of early pregnancy loss. Lancet. 2021;397(10285):1658-1667. doi:10.1016/S0140-6736(21)00682-6
- Smith LF, Ewings PD, Quinlan C. Incidence of pregnancy after expectant, medical, or surgical management of spontaneous first trimester miscarriage: long term follow-up of miscarriage treatment (MIST) randomised controlled trial. BMJ. 2009;339:b3827. doi:10.1136/bmj.b3827
- Ankum WM, Wieringa-De Waard M, Bindels PJ. Management of spontaneous miscarriage in the first trimester: an example of putting informed shared decision making into practice. BMJ. 2001;322(7298):1343-1346. doi:10.1136/bmj.322.7298.1343
- Webster K, Eadon H, Fishburn S, Kumar G; Guideline Committee. Ectopic pregnancy and miscarriage: diagnosis and initial management: summary of updated NICE guidance. BMJ. 2019;367:l6283. doi:10.1136/bmj.l6283
- Ghosh J, Papadopoulou A, Devall AJ, et al. Methods for managing miscarriage: a network meta-analysis. Cochrane Database Syst Rev. 2021;6(6):CD012602.PubMedGoogle Scholar
- Hooker AB, Aydin H, Brölmann HAM, Huirne JA. Long-term complications and reproductive outcome after the management of retained products of conception: a systematic review. Fertil Steril. 2016;105(1):156-64.e1-2. doi:10.1016/j.fertnstert.2015.09.021
- Faivre E, Deffieux X, Mrazguia C, et al. Hysteroscopic management of residual trophoblastic tissue and reproductive outcome: a pilot study. J Minim Invasive Gynecol. 2009;16(4):487-490. doi:10.1016/j.jmig.2009.04.011
- Golan A, Dishi M, Shalev A, Keidar R, Ginath S, Sagiv R. Operative hysteroscopy to remove retained products of conception: novel treatment of an old problem. J Minim Invasive Gynecol. 2011;18(1):100-103. doi:10.1016/j.jmig.2010.09.001
- Sonnier L, Torre A, Broux P, Fauconnier A, Huchon C. Evaluation of fertility after operative hysteroscopy to remove retained products of conception. Eur J Obstet Gynecol Reprod Biol. 2017;211:98-102. doi:10.1016/j.ejogrb.2017.02.003
- Cohen SB, Kalter-Ferber A, Weisz BS, et al. Hysteroscopy may be the method of choice for management of residual trophoblastic tissue. J Am Assoc Gynecol Laparosc. 2001;8(2):199-202. doi:10.1016/S1074-3804(05)60577-4
- Ben-Ami I, Melcer Y, Smorgick N, Schneider D, Pansky M, Halperin R. A comparison of reproductive outcomes following hysteroscopic management versus dilatation and curettage of retained products of conception. Int J Gynaecol Obstet. 2014;127(1):86-89. doi:10.1016/j.ijgo.2014.05.003
- Rein DT, Schmidt T, Hess AP, Volkmer A, Schöndorf T, Breidenbach M. Hysteroscopic management of residual trophoblastic tissue is superior to ultrasound-guided curettage. J Minim Invasive Gynecol. 2011;18(6):774-778. doi:10.1016/j.jmig.2011.08.003
- Vitale SG, Parry JP, Carugno J, et al. Surgical and reproductive outcomes after hysteroscopic removal of retained products of conception: a systematic review and meta-analysis. J Minim Invasive Gynecol. 2021;28(2):204-217. doi:10.1016/j.jmig.2020.10.028
- Smorgick N, Barel O, Fuchs N, Ben-Ami I, Pansky M, Vaknin Z. Hysteroscopic management of retained products of conception: meta-analysis and literature review. Eur J Obstet Gynecol Reprod Biol. 2014;173:19-22. doi:10.1016/j.ejogrb.2013.11.020
- Patsopoulos NA. A pragmatic view on pragmatic trials. Dialogues Clin Neurosci. 2011;13(2):217-224. doi:10.31887/DCNS.2011.13.2/npatsopoulos
- Huchon C, Koskas M, Agostini A, et al. Operative hysteroscopy versus vacuum aspiration for incomplete spontaneous abortion (HY-PER): study protocol for a randomized controlled trial. Trials. 2015;16:363. doi:10.1186/s13063-015-0900-1
- Huchon C, Deffieux X, Beucher G, et al; Collège National des Gynécologues Obstétriciens Français. Pregnancy loss: French clinical practice guidelines. Eur J Obstet Gynecol Reprod Biol. 2016;201:18-26. doi:10.1016/j.ejogrb.2016.02.015
- Fauconnier A, Provot J, Le Creff I, et al. A framework proposal for quality and safety measurement in gynecologic emergency care. Obstet Gynecol. 2020;136(5):912-921. doi:10.1097/AOG.0000000000004132
- Salomon LJ, Nassar M, Bernard JP, Ville Y, Fauconnier A; Société Française pour l’Amélioration des Pratiques Echographiques (SFAPE). A score-based method to improve the quality of emergency gynaecological ultrasound examination. Eur J Obstet Gynecol Reprod Biol. 2009;143(2):116-120. doi:10.1016/j.ejogrb.2008.12.003
- Clavien PA, Barkun J, de Oliveira ML, et al. The Clavien-Dindo classification of surgical complications: five-year experience. Ann Surg. 2009;250(2):187-196. doi:10.1097/SLA.0b013e3181b13ca2
- Casagrande JT, Pike MC. An improved approximate formula for calculating sample sizes for comparing two binomial distributions. Biometrics. 1978;34(3):483-486. doi:10.2307/2530613
- Schulz KF, Grimes DA. Blinding in randomised trials: hiding who got what. Lancet. 2002;359(9307):696-700. doi:10.1016/S0140-6736(02)07816-9
- Bland JM, Altman DG. Survival probabilities (the Kaplan-Meier method). BMJ. 1998;317(7172):1572. doi:10.1136/bmj.317.7172.1572
- Hooker AB, de Leeuw R, van de Ven PM, et al. Prevalence of intrauterine adhesions after the application of hyaluronic acid gel after dilatation and curettage in women with at least one previous curettage: short-term outcomes of a multicenter, prospective randomized controlled trial. Fertil Steril. 2017;107(5):1223-1231.e3. doi:10.1016/j.fertnstert.2017.02.113
- Ramirez PT, Frumovitz M, Pareja R, et al. Minimally invasive versus abdominal radical hysterectomy for cervical cancer. N Engl J Med. 2018;379(20):1895-1904. doi:10.1056/NEJMoa1806395