Авторы: Jérôme Baranger, Olivier Villemain, Matthias Wagner, Mariella Vargas-Gutierrez, Mike Seed, Olivier Baud, Birgit Ertl-Wagner, Julien Aguetg
Вступление
Церебральный кровоток у новорожденных может быть нарушен из-за различных клинических состояний. Недоношенность, перинатальная асфиксия и различные врожденные пороки сердца – частые, но не исчерпывающие примеры.
Нарушение церебральной перфузии может привести к нарушениям нейрокогнитивного развития и последующей инвалидности, которая может достигать зрелого возраста, что делает его серьезной проблемой для общественного здравоохранения. Развитие методов неонатальной визуализации перфузии может оказать большое влияние на перинатальную медицину, поскольку позволит своевременно и точно диагностировать церебральные ситуации повышенного риска.
В настоящее время существуют различные принципиально разные технологии для визуализации и количественной оценки перфузии мозга. Для магнитно-резонансной томографии (МРТ) они включают методы перфузии с контрастным усилением, включая Т1-взвешенные методы контрастирования с динамическим контрастом и динамической восприимчивостью, а также ASL-МРТ и IVIM. Ультразвуковые методы включают оценку прекраниальных артерий с помощью обычного ультразвука и, в последнее время, оценку полной перфузии головного мозга с помощью сверхбыстрой ультразвуковой визуализации (UUI). Дополнительные методы визуализации перфузии включают обычную однофотонную эмиссионную компьютерную томографию (SPECT), методы позитронно-эмиссионной томографии (PET), перфузионную компьютерную томографию и спектроскопию в ближнем инфракрасном диапазоне.
Методы с усиленным контрастированием требуют внутривенного (IV) доступа и введения экзогенного контрастного вещества. Для КТ используется контраст на основе йода, и связанные риски включают нефротоксичность, вызванную контрастом, в основном при нарушении функции почек и аллергические реакции различной степени тяжести. Для МРТ используется контраст на основе гадолиния, и помимо редких и часто легких аллергических реакций существует редкий риск нефрогенного системного фиброза. В недавних исследованиях описываются отложения гадолиния в головном мозге, значение которых еще не полностью изучено (Young et al., 2018). Таким образом, существует потребность в неинвазивных методах визуализации перфузии, которые не включают ионизирующее излучение, особенно в особо уязвимой популяции новорожденных. С недавним появлением UUI, обеспечивающего высокое пространственное и временное разрешение для допплеровской визуализации, стал возможен количественный анализ вплоть до микрососудистого уровня у постели пациента (Demene et al., 2019).
3. Методы визуализации для оценки церебрального кровообращения у новорожденных
3.1. Магнитно-резонансная томография (МРТ)
Существуют различные методы перфузии МРТ, основанные на различных импульсных последовательностях. В этих методах используются экзогенные или эндогенные контрастные вещества для оценки как регионарной, так и глобальной церебральной перфузии.
3.1.1. МРТ-перфузия с контрастированием динамической восприимчивости
Перфузия контрастом с динамической восприимчивостью основана на вызванной восприимчивостью к потере сигнала, наблюдаемой на обычных T2-взвешенных (T2w) или градиентных эхо-T2-взвешенных (T2 * w) изображениях во время первого прохода экзогенного внутривенно введенного парамагнитного контрастного вещества на основе гадолиния.
Гемодинамические изменения оцениваются как на глобальном, так и на региональном уровне и выражаются как среднее время прохождения, время до пика и объем церебральной крови (CBV), которые, в свою очередь, используются для расчета церебрального кровообращения. Можно получить цветные карты этих количественных измерений (рис. 1). Применение этого метода к новорожденным оказалось трудным на различных уровнях, и существует лишь несколько исследований на эту тему.
Рисунок 1: Перфузия на МРТ с динамическим контрастом восприимчивости. Панели A и B показывают карты перфузии с церебральным кровотоком слева и церебральным объемом крови справа от каждой панели на двух разных уровнях, чтобы проиллюстрировать выраженную гиперперфузию в затылочных долях (A), базальных ганглиях (B) и моторной коре (A и B). Отражает картину повреждения базальных ганглиев. Изображение адаптировано и использовано с разрешения Wintermark et al.
3.1.2. МРТ-перфузия с динамическим контрастированием
Перфузия с динамическим контрастированием основана на эффекте контрастного вещества на основе гадолиния, заключающегося в сокращении времени релаксации T1, что приводит к увеличению сигнала. Путем введения болюса контрастного вещества на основе гадолиния, картину усиления интересующей области можно изучить путем получения исходных изображений без контраста с последующей быстрой последовательностью повторных T1-взвешенных изображений (T1w).
Региональное накопление контрастного вещества на основе гадолиния в кровеносных сосудах, а также фракция контрастного вещества на основе гадолиния, которая диффундировала во внесосудистое внеклеточное пространство, приведет к увеличению сигнала из-за укорочения T1. Перфузионная МРТ с динамическим контрастированием оценивает свойства перфузии тканей на микрососудистом уровне.
Посредством фармакокинетического моделирования можно измерить параметры, отражающие проницаемость капилляров, регионарный объем крови и регионарный кровоток. Использование МРТ с динамическим контрастированием в первую очередь описано для визуализации опухолей и периферической сосудистой системы.
3.1.3. Фазово-контрастная МРТ
Фазово-контрастная МРТ позволяет получать количественные изображения движущихся жидкостей на основе принципа, что спины, движущиеся вдоль градиента магнитного поля, развивают фазовый сдвиг, пропорциональный их скорости. Путем анализа информации о фазе в поперечном сечении данного интересующего сосуда можно вычислить скорость для каждого вокселя и получить фазово-контрастное изображение (рис. 2). Затем программное обеспечение постобработки позволяет количественно оценить эту скорость и построить кривую потока, например для полного сердечного цикла (Lotz et al., 2002).
При применении этого принципа на уровне экстракраниальных, прецеребральных артерий, включая внутренние сонные артерии и позвоночные артерии, можно надежно измерить общий церебральный кровоток (Spilled et al., 2002).
Объем мозга измеряется путем сегментации изотропных трехмерных последовательностей с высоким пространственным разрешением (Prsa et al., 2014, Werner et al., 2010). Затем рассчитывают средний общий кровоток путем деления общего кровотока на объем мозга. Применительно к недоношенным и доношенным новорожденным было показано, что общий церебральный кровоток, измеренный с помощью МРТ с фазовым контрастом, в значительной степени коррелирует с постконцептуальным возрастом и массой тела, что подтверждает полезность такого неинвазивного метода для измерения общего церебрального кровотока у новорожденного (Benders et al., 2011). Однако этот метод дает только оценку среднего глобального церебрального кровотока и не дает информации о региональном церебральном кровотоке.
Рисунок 2: Фазово-контрастная МРТ. Сагиттальное двухмерное фазово-контрастное изображение (A) для иллюстрации расположения аксиального двухмерного фазово-контрастного изображения, показывающего интенсивность сигнала в плоскости потока внутри внутренних сонных артерий (B: 1 и 2) и базилярной артерии (B: 3). Изображение адаптировано и использовано с разрешения Benders et al.
3.1.4. Маркировка артериального спина (ASL) МРТ
В то время как методы контраста с динамической восприимчивостью и МРТ-перфузии с динамическим контрастированием требуют введения экзогенного контрастного агента, мечение артериального спина использует собственный эндогенный контрастный агент, молекулы воды в крови.
Перед процессом маркировки создается изображение для намагничивания фона в мозгу. Затем вода артериальной крови маркируется путем выборочного инвертирования намагниченности водных спинов артериальной крови, циркулирующих в головном мозге на уровне шеи, которые отображаются на уровне мозга после короткого времени прохождения (рис. 3). Вычитание двух изображений дает изображение, взвешенное по перфузии (Ferre et al., 2013). Количественная оценка кровотока (в единицах мл / 100 г ткани головного мозга / мин) с помощью ASL основана на математических моделях с использованием усредненных по времени интенсивностей сигналов в фоновой намагниченности и изображениях с метками спина артерий (Олсоп и др., 2015, Варела и др. ., 2015).
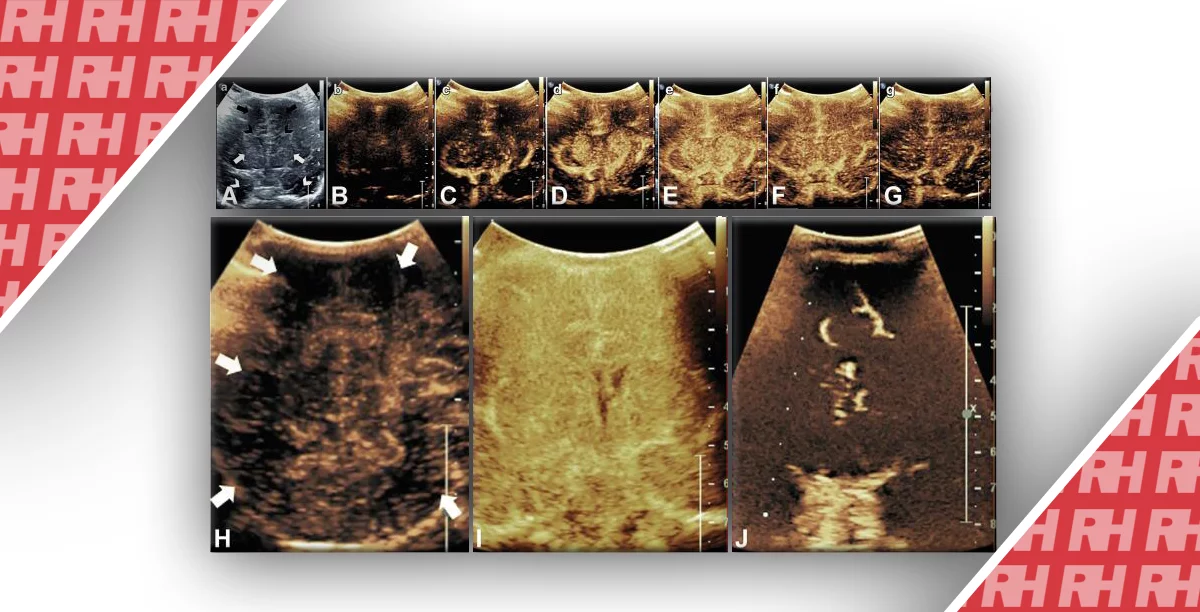
Рисунок 3: МРТ ASL. A: Намагничивание водяных спинов артериальной крови в прецеребральных артериях инвертируется путем применения радиочастотного импульса (слева, пунктирная рамка) с последующей короткой задержкой, в течение которой спины достигают мозгового кровообращения, где получается «помеченное» изображение. Предыдущее намагничивание фона фиксируется в том же поле зрения (левая пунктирная рамка). Вычитание двух изображений генерирует взвешенное по перфузии изображение (PWI). Количественная оценка церебрального кровотока (в единицах мл / 100 г ткани мозга / мин) с помощью ASL основана на математических моделях, использующих усредненные по времени интенсивности сигналов в фоновой намагниченности и изображениях с метками спинов в артериях. B: изображения перфузии ASL, представляющие церебральный кровоток у трех младенцев, родившихся в гестационном возрасте 25 недель (верхний ряд), гестационном возрасте 31 недели (средний ряд) и сканированном гестационном возрасте 40 недель (нижний ряд). Перфузия в центральной борозде увеличивается со сроком беременности (средний ряд) и более равномерно распространяется у доношенных новорожденных (нижний ряд). Изображение адаптировано и использовано с разрешения De Vis et al.
Вес мозга оценивается на основе сегментации полученных анатомических трехмерных последовательностей (Ferre et al., 2013). Можно изучать как региональную, так и глобальную церебральную перфузию. Существует несколько методов маркировки, из которых псевдонепрерывное маркирование оказалось более точным у новорожденных, обеспечивая превосходное качество изображения за счет повышения эффективности маркировки и отношения сигнал / шум (SNR) по сравнению с другими методами (Олсоп и др., 2015, Boudes et al., 2014, Wu et al., 2011).
Поскольку он позволяет избежать внутривенного введения экзогенного контрастного вещества и ионизирующего излучения, ASL является привлекательным методом визуализации перфузии головного мозга у новорожденных (Miranda et al., 2006). Когда артефакты движения при приеме пищи и сна мешают оценке, последовательность может быть повторена (Антонов и др., 2017, Виндрам и др., 2012). Несколько исследований продемонстрировали возможность применения ASL у новорожденных и младенцев. Референсные значения были установлены у здоровых людей в возрасте от 6 месяцев до 15 лет (Carsin-Vu et al., 2018).
3.1.5. Интравоксельное некогерентное движение (IVIM) МРТ
МРТ с диффузионным взвешиванием оценивает случайное движение отдельных молекул воды в ткани. Каждая молекула обладает тепловой энергией, которая вызывает движение, приводящее к столкновениям с другими молекулами и, как следствие, изменению их направления движения. В магнитном поле с примененными кодирующими импульсами градиента наблюдается ослабление сигнала, вторичное по отношению к диффузности, которая увеличивается со степенью кодирования градиента поля, обычно известной как значение b в диффузионно-взвешенной МРТ (Le Bihan, 2019).
Впервые описано Le Bihan et al. В сочетании с концепцией диффузии 1986 года (Le Bihan et al., 1986) коллективное движение молекул воды в сети случайно ориентированных капилляров равно кровотоку и называется «псевдодиффузией» (Le Bihan, 2019). Псевдодиффузия, выведенная из уравнения Стокса-Эйнштейна, выражается в виде коэффициента, зависящего от средней длины сегмента капилляра и средней скорости внутри него.
И диффузия, и псевдодиффузия вносят свой вклад в затухание сигнала, что приводит к биэкспоненциальной кривой затухания сигнала, учитывая в десять раз более быстрое затухание сигнала псевдодиффузии при низких значениях b. Это отклонение называется эффектом IVIM. Полученные данные о затухании сигнала затем обрабатываются с помощью математических алгоритмов, которые выходят за рамки данного обзора. Ле Бихан и Тернер показали, как параметры IVIM могут быть связаны с обычными параметрами перфузии на основе двух важных переменных: длины сегмента капилляра и общей длины капилляра (Le Bihan and Turner, 1992). Учитывая, что эти две длины постоянны для данной ткани, относительную перфузию или кровоток можно оценить по произведению D * fIVIM, где D – псевдодиффузия, а fIVIM – фракция текущей крови (рис. 4).
Рисунок 4: Интравоксельная перфузия на МРТ с некогерентным движением (IVIM). Параметры IVIM fIVIM (A), D * (B) и D *. FIVIM (C) отражают гиперперфузию в обеих лобных долях, преимущественно справа. Спад интенсивности сигнала как функция от b с соответствующим биэкспоненциальным соответствием представлен для интересующей области в пределах гиперперфузированной правой лобной доли (D) и в пределах левой теменной контрольной области (E). Изображение адаптировано и использовано с разрешения Federau et al.
На сегодняшний день микрососудистая перфузия изучается в основном при визуализации опухолей как на глобальном, так и на региональном уровне (Stieb et al., 2016).
МРТ перфузия на основе IVIM предоставляет информацию как о тканевой микроциркуляции, так и о кровотоке в рамках одной последовательности и не требует введения контрастного вещества, что делает эту концепцию привлекательной для визуализации церебрального кровотока новорожденных.
3.2. Ультразвуковое исследование
Ультрасонография головного мозга новорожденного использует естественные анатомические окна через передние и, по возможности, задние роднички, тонкую височную кость и сосцевидную часть височной кости. Благодаря своей широкой доступности, отсутствию воздействия ионизирующего излучения и отсутствию необходимости в седативных средствах, УЗИ позволяет проводить оценку состояния головного мозга новорожденных у постели больного. Однако для достижения приемлемой воспроизводимости требуется соответствие стандартизированному протоколу визуализации, знание оборудования и пользовательский опыт (Dudink et al., 2020). Существует несколько подходов к оценке церебральной перфузии.
3.2.1. Обычный допплер
Так называемый УЗ-допплер использует эффект Допплера, который определяется сдвигом частоты звуковой волны из-за отражателя, то есть клетки крови, движущейся к объекту или от объекта, то есть датчика. В частности, спектральная допплеровская (или импульсно-волновая допплеровская) ультрасонография использует анализ Фурье для усреднения этих частот за определенный период времени, преобразуя их в скорости и отображает спектр частот в виде волны.
Общий церебральный кровоток оценивался с использованием объема внутрисосудистого кровотока, рассчитанного с помощью скорректированных по углу усредненных по времени скоростей и площади поперечного сечения сосудов внутри экстракраниальных внутренних сонных и позвоночных артерий (Ehehalt et al., 2005).
Точность этого подхода зависит от точного измерения малых диаметров просвета (менее 2 мм для позвоночных артерий), выбора оптимального угла исследования и правильной оценки усредненной по времени скорости, поскольку даже небольшие ошибки приводят к значительным изменениям. Полученная информация о прецеребральном кровотоке информирует только в глобальном внутрицеребральном масштабе и не может демонстрировать региональные изменения.
Другие распространенные инструменты ультразвукового допплера включают цветной допплер и энергетический допплер. В то время как цветной допплер проявляет недостаточную чувствительность к медленному кровотоку, энергетический допплер пропорционален объему церебрального кровотока (Rubin et al., 1995) и более чувствителен к микрососудистому кровотоку. Его можно использовать для изучения регионарной церебральной перфузии у новорожденных в корковой или глубокой структуре, такой как базальные ганглии (Heck et al., 2012) (рис. 5). Вышеупомянутый пропорциональный закон между объемом церебрального кровотока и энергетическим допплером зависит от нескольких параметров, включая затухание сигнала, а также геометрию и высоту ультразвукового луча. Следовательно, в пределах данного пикселя говорят, что энергетический допплер представляет собой фракционный объем движущейся крови и представлен в относительных единицах (% или дБ). Следовательно, энергетический допплер больше подходит для относительных измерений между областями или временными точками, чем для количественных измерений церебрального кровотока.
Рисунок 5: Обычное ультразвуковое допплеровское исследование. Картирование потока с помощью энергетического допплера наложено на корональный вид в B-режиме базальных ганглиев и передних рогов боковых желудочков, включая средние мозговые артерии. Региональная васкуляризация измеряется во время постобработки путем подсчета количества и силы цветных пикселей в предварительно выбранной области. Изображение адаптировано и использовано с разрешения Heck et al.
3.2.2. Динамическое измерение тканевой перфузии
Динамическое измерение тканевой перфузии количественно определяет среднюю интенсивность перфузии (выраженную в см / с) в выбранной области интереса на основе видеозаписи цветного допплера, снятого на протяжении как минимум одного сердечного цикла (Scholbach, 2009, Scholbach, 2008) (рис. 6 ).
Этот метод недавно был применен для ретроспективного изучения перфузии базальных ганглиев у небольшой популяции младенцев, получавших терапевтическую гипотермию всего тела по поводу гипоксически-ишемической энцефалопатии (ГИЭ) (Faingold et al., 2016). Как и в случае с другими традиционными ультразвуковыми методами, динамическое измерение тканевой перфузии требует стандартизированного подхода к выбранным интересующим областям и позволяет только региональный анализ количественной оценки средней интенсивности перфузии. Сравнение с другими более широко используемыми количественными параметрами, такими как церебральная перфузия, является сложной задачей, поскольку динамическое измерение тканевой перфузии не учитывает объем ткани.
Рисунок 6: Динамическое измерение тканевой перфузии. Интересующая область выбирается в пределах базальных ганглиев на цветном допплеровском ультразвуковом режиме, полученном в течение как минимум одного сердечного цикла, для количественной оценки средней интенсивности перфузии (в см / с), показанной на кривой интенсивности внизу у однодневного пациента. Диагностирована гипоксически-ишемическая энцефалопатия. Изображение адаптировано и использовано с разрешения Faingold et al.